Опытным путём было доказано, что масса ядра оказывается меньше, чем масса протонов и нейтронов, из которых состоит ядро. Разница между этими массами называется дефектом массы ядра.
Дефект массы ядра (
Δm
) — это разница между суммарной массой свободных нуклонов, из которых состоит ядро, и массой ядра.
Почему же масса нуклонов, связанных ядерными силами в ядро, оказывается меньше массы этих же нуклонов в свободном состоянии? Оказывается, что масса и энергия взаимосвязаны.
Всякое тело массой m обладает энергией, которая называется энергией покоя (
E0
):
, где c — скорость света в вакууме.
Впервые соотношение между энергией и массой вывел Альберт Эйнштейн, поэтому это выражение и получило название «уравнение Эйнштейна».
Уменьшение энергии покоя нуклонов в ядре вызвано наличием ядерных сил, которые удерживают протоны и нейтроны в ядре. Работа, которую необходимо совершить для разрыва ядерных сил и разъединения нуклонов, равна энергии, которая связывает нуклоны вместе. Эта энергия называется энергией связи (
Eсв
) ядра.
Энергия связи и дефект массы ядра связаны между собой уравнением Эйнштейна:
Удельной энергией связи ядра называют энергию связи, приходящуюся на (1) нуклон:
Удельная энергия равна средней энергии, необходимой для отрыва (1) нуклона от ядра.
Вычисления показали, что наибольшей удельной энергией связи обладают элементы, находящиеся в центре Периодической системы химических элементов. С увеличением порядкового номера начинает уменьшаться удельная энергия связи. Именно поэтому ядра элементов с порядковым номером больше (83) являются радиоактивными. Благодаря небольшой удельной энергии связи они способны самопроизвольно распадаться.
Единицы измерения энергии
В ядерной физике принято измерять энергию в мегаэлектронвольтах ((1) МэВ):
(1) МэВ (=)
106
эВ
≈1,6⋅10−13
Дж.
Для вычисления энергии связи удобно пользоваться переводным коэффициентом для массы и энергии.
Дефекту массы в (1) а. е. м. соответствует энергия, равная
кг
⋅(3⋅108
м/с
)2≈1,49⋅10−10
Дж
=931,5
МэВ.
Обрати внимание!
Для выражения изменения энергии системы в мегаэлектронвольтах нужно
изменение массы системы в атомных единицах массы умножить на переводной коэффициент (931,5) МэВ/а. е. м.
(1) а. е. м. (=) (931,5) МэВ.
В уроке 2 «Изотопы элементов» из курса «Химия для чайников» рассмотрим что такое изотопы элементов и как правильно их обозначают; кроме того мы научимся определять массовое число, дефект массы и энергию связи ядра. Данный урок полностью опирается на основы химии, изложенные в первом уроке, в котором мы рассмотрели строение атома и атомного ядра, поэтому настоятельно вам рекомендую его изучить от корки до корки.
Что такое изотоп?
Хотя все атомы одного элемента имеют одинаковое число протонов, эти атомы могут отличаться числом имеющихся у них нейтронов. Такие различные атомы одного и того же элемента называются изотопами. Количество протонов, а также количество электронов у изотопа и исходного элемента совпадает. По этой причине в природе существует гораздо больше химических элементов, чем указано в таблице Менделеева, которая систематизирует элементы по числу протонов (порядковый номер).
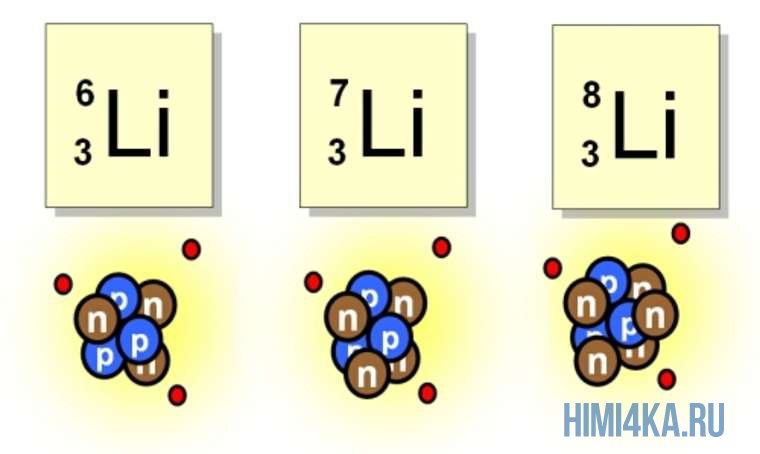
Например, все атомы Li имеют 3 протона, но в природе существуют изотопы, содержащие от 3 до 5 нейтронов. Для обозначения изотопа, слева от символа элемента подписывают нижним индексом его порядковый номер, а верхним — массовое число. Массовое число — это суммарное число нуклонов (протонов и нейтронов) в атомном ядре, численно близкое к атомной массе элемента. Нижний индекс, обозначающий порядковый номер элемента, указывать не обязательно, так как все атомы лития имеют в своем ядре по 3 протона. Также, обсуждая эти изотопы, можно пользоваться записью «литий-6» и «литий-8».
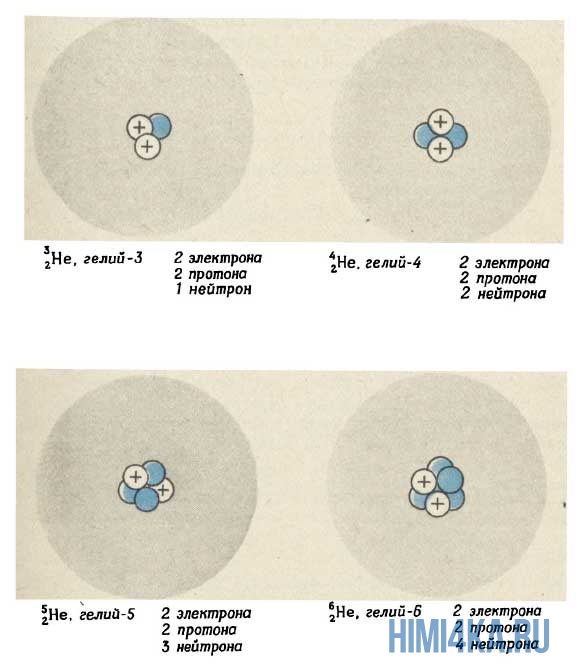
На рисунке выше изображен состав четырех изотопов гелия (Не). Все атомы гелия содержат два протона (и, следовательно, два электрона), но число нейтронов у них может быть разным. В природе большинство атомов гелия имеет два нейтрона (гелий-4) и реже одного раза на миллион встречаются атомы гелия с одним нейтроном (гелий-3). Другие изотопы гелия — гелий-5 , гелий-6 и гелий-8 (не показанный на рисунке) — неустойчивы и обнаруживаются лишь на очень непродолжительное время в ядерных реакциях (подробнее об этом будем говорить еще не скоро). Размеры ядер на рисунке очень сильно увеличены. Если бы они были такими, как это показано на рисунке, диаметр атома должен был достигать примерно 0,5 км.
Пример 1. Сколько протонов, нейтронов и электронов содержится в атоме урана-238? Запишите символ этого изотопа.
Решение: Порядковый номер урана (см. таблицу Менделеева) равен 92, а массовое число изотопа равно 238 (по условию). Следовательно, он содержит 92 протона, 92 электрона и 238 — 92 = 146 нейтронов. Его символ 238U.
Дефект массы и энергия связи ядра
Затронув тему изотопов, нельзя пройти мимо феномена дефект массы ядра. Когда из отдельных нуклонов образуется атомное ядро, часть их массы превращается в энергию. Другими словами, вот взяли вы щепотку протонов и нейтронов, хорошенько их смяли вместе, и получили ядро, но его масса будет меньше массы исходных компонентов. Это и есть дефект масс. Формула для расчета дефекта массы ядра:
- ∆m=(Zmp+Nmn)-Mя
где Mя – масса ядра, Z – число протонов в ядре, N – число нейтронов в ядре, mp – масса протона, mn – масса нейтрона.
Если к атому подвести энергию (которая эквивалентна дефекту масс), то можно разделить его ядро обратно на нуклоны. Эта энергия носит название энергия связи ядра. Формула для расчета энергии связи ядра:
- ∆Eсв=∆mc2
где с — скорость света, ∆m — дефект массы ядра
Проверьте себя, как вы усвоили понятия дефект массы и энергия связи ядра, самостоятельно решив задачу пользуясь формулами выше.
Пример 2. Если образовать атом углерода-12 из субатомных частиц, какое значение будет иметь дефект масс?
Показать
Ответ: 0,0990 а.е.м.
[свернуть]
Теперь нам известно, что каждый изотоп элемента характеризуется порядковым номером (суммарным числом протонов), массовым числом (суммарным числом протонов и нейтронов) и атомной массой (массой атома, выраженной в атомных единицах массы). Поскольку дефект массы при образовании атома очень мал, массовое число обычно совпадает с атомной массой изотопа, округленной до ближайшего целого числа. (Например, атомная масса хлора-37 равна 36,966, что после округления дает 37.) Если в природе встречается несколько изотопов одного элемента, то экспериментально наблюдаемая атомная масса (естественная атомная масса) равна средневзвешенному значению атомных масс отдельных изотопов. Это средневзвешенное значение определяется соответственно относительному содержанию изотопов в природе. Хлор существует в природе в виде смеси из 75,53% хлора-35 (атомная масса 34,97 а.е.м.) и 24,47% хлора-37 (36,97 а.е.м.), поэтому средневзвешенное значение масс этих изотопов равно
- (0,7553·34,97 а.е.м.) + (0,2447·36,97 а.е.м.) = 35,46 а.е.м.
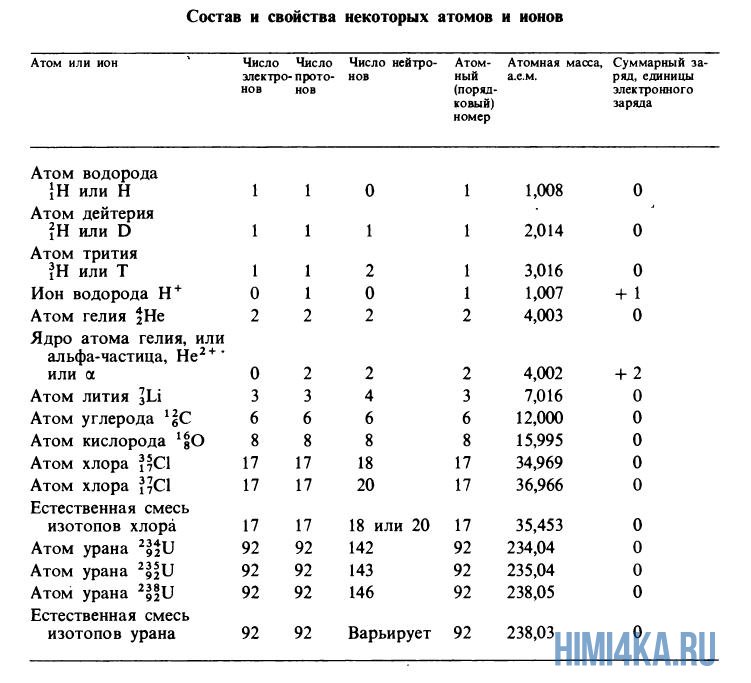
Атомные массы, указанные в таблице Менделеева представляют собой во всех случаях средневзвешенные значения атомных масс изотопов, встречающихся в природе, и именно этими значениями мы будем пользоваться в дальнейшем, за исключением тех случаев, когда будет обсуждаться какой-нибудь конкретный изотоп. Все изотопы одного элемента в химическом отношении ведут себя практически одинаково. На рисунке ниже изображены состав и свойства некоторые атомов, ионов и изотопов элементов.
Пример 3. Магний (Mg) в основном состоит из трех естественных изотопов: 78,70% всех атомов магния имеют атомную массу 23,985 а.е.м., 10,13% — 24,986 а.е.м. и 11,17% — 25,983 а.е.м. Сколько протонов и нейтронов содержится в каждом из этих трех изотопов? Чему равно средневзвешенное значение их атомных масс?
Решение: Все изотопы магния содержат по 12 протонов. Изотоп с атомной массой 23,985 а.е.м. имеет массовое число 24 (суммарное число протонов и нейтронов), следовательно, он имеет 24 — 12 = 12 нейтронов. Символ этого изотопа 24Mg. Аналогично находим, что изотоп с атомным весом 24,986 а.е.м. имеет массовое число 25, содержит 13 нейтронов и имеет символ 25Mg. Третий изотоп (25,983 а.е.м.) имеет массовое число 26, содержит 14 нейтронов и имеет символ 26Mg. Средняя атомная масса магния находится следующим образом:
- (0,7870·23,985 а.е.м.) + (0,1013·24,986 а.е.м.) + (0,1117·25,983 а.е.м.) = 24,31 а.е.м.
Надеюсь урок 2 «Изотопы элементов» помог вам понять что из себя представляют изотопы. Если у вас возникли вопросы, пишите их в комментарии.
Видеоурок: Физика атомного ядра. Дефект массы
Лекция: Дефект массы ядра
Существует огромное количество таблиц, в которых можно определить точное значение массы того или иного изотопа. Но Вы можете спросить, зачем они нужны, ведь можно просто взять и сложить массы всех частиц ядра и получить конечное его значение. До некоторого времени так и делали, пока не стало известно, что сумма масс всех нуклонов не совпадает с массой ядра. Масса ядра всегда меньше, чем сумма масс всех нуклонов. Разность этих масс называется дефектом масс.
Дефект масс находится по формуле:
Обратите внимание, в данной формуле М — это масса ядра. Однако, в таблице Менделеева и других таблицах указана масса всего атома. Поэтому из известного значения следует вычесть массу всех имеющихся электроном.
Например, давайте рассмотрим ядро Гелия и найдем для него дефект масс. Для начала найдем значение массы атома гелия и вычтем из нее массы двух имеющихся электронов:
Далее найдем массу всех нуклонов гелия:
В результате получим величину дефекта масс:
Урок решение задач по теме:
«Энергия связи. Дефект масс». 9 класс
Цель урока: научить решать задачи на расчет дефекта масс,
энергии связи атомных ядер.
Демонстрации. Таблица «Периодическая система химических
элементов Д. И. Менделеева».
Ход урока.
I.
Организационный
момент — 1 мин.
II.
Проверка знаний -5
мин( фронтальный опрос) Вопросы.
1.
Что называется энергией
связи ядра?
Ответ: Минимальная энергия, необходимая для расщепления ядра
на отдельные нуклоны, называется энергией связи ядра.
2. Запишите формулу для определения дефекта массы ядра
любого атома. Ответ:
, где
— масса ядра атома, Z –
число протонов, N – число нейтронов, — масса протона,
— масса нейтрона. Масса
ядра всегда меньше суммы масс нуклонов, из которых оно состоит.
Разность между суммы масс нуклонов и массы ядра называется дефектом
масс.
называет дефектом масс.
2.
Запишите формулу для
расчета энергии связи ядра атома.
Ответ:, где с =
— скорость света в вакууме.
III.
Решение задач. 35
мин
Учитель.
В ядерной физике
массу принято выражать в атомных единицах массы (а.е.м.).
А.е.м.
равна 1/12 массы нуклида углерода 12С, что в единицах СИ составляет
1,660565 • 10 — 27 кг.
Масса покоя электрона
равна 5,4858 ∙ 10 – 4 а.е.м. = 9,1∙10 -31кг
Масса покоя протона равна 1,00728 а.е.м. =1,6726∙10-27
кг
Масса покоя нейтрона равна 1,00866 а.е.м. =1,6749∙10-27
кг
Масса покоя водорода равна 1,00783 а.е.м.
Масса покоя дейтерия равна 2,01410 а.е.м.
Масса покоя гелия равна 4,00260 а.е.м.
с2 = 931,5
МэВ/ а.е.м., где с — скорость света.
Масса
электрона мы пренебрегаем при решении задач.
те тр
Образец решения
задачи.
Задачи. Вычислите
энергию связи Е0 ядра гелия
.
Решение. Масса
атома гелия: 4,00260 а.е.м. Z=2, N =2
Масса отдельных
(невзаимодействующих между собой) нуклонов:
2∙ тр = 2
∙1,00728 а.е.м.= 2,01456 а.е.м.
2∙тп
= 2 ∙1,00866 а.е.м. = 2,01732 а.е.м.
4,03188 а.е.м.
4,03188 а.е.м. — 4,00260 а.е.м. = 0,02928
а.е.м.
= 0,02928 а.е.м. • 931,5 МэВ/ а.е.м. =
27,27432 МэВ
Ответ: энергия связи ядра гелия
≈27,3 МэВ.
≈ 27,3 МэВ или
Дж =43,68
Дж.
Решите задачи.
Задача 1. Вычислите энергию связи E0 ядра гелия
|
Решение:
Ответ:
|
1.Дано:
Мя ( = 3,01602 а.е.м.
Z = 2; N =1
2∙ тр = 2 ∙1,00728 а.е.м.=
2,01456 а.е.м.
1∙тп = 1∙ 1,00866 а.е.м. =1,00866 а.е.м.
E0 =?
Задача 2. Вычислите энергию связи E0 ядра трития
.
Решение:
=(1,00728+2,01732)
а.е.м.–
= 0,00855 а.е.м. ∙
931,5 МэВ/ а.е.м. =7,964325 МэВ
Ответ:
≈
7,96 МэВ
Дано:
Мя(
Z = 1; N =2
1∙ тр = 1 ∙1,00728 а.е.м.=
1,00728 а.е.м.
2∙тп = 2∙ 1,00866 а.е.м. =2,01732 а.е.м.
E0 =?
Задача 3. Вычислите энергию связи ядра лития .,
Дано:
Мя ( =7,01601 а.е.м.
Решение:
=(3,02184+4,03464)
а.е.м.–
= 0,04047 а.е.м. ∙
931,5 МэВ/ а.е.м. =37,697805 МэВ
Ответ:
≈
37,70 МэВ
Z = 3; N =4
3∙ тр = 3 ∙1,00728 а.е.м.=
3,02184 а.е.м.
4∙тп = 4∙ 1,00866 а.е.м. =4,03464 а.е.м.
E0 =?
Задача 4
Рассчитайте дефект
массы и энергию связи ядра атома кислорода .
Решение:
=(8,05824+8,06928)
а.е.м.– =
= 0,13261∙1,66кг ≈2,2
кг
=0,13261 а.е.м. ∙ 931,5
МэВ/ а.е.м. ≈123,53 МэВ =123,53∙1,6Дж= 197,64
Дж
Ответ:
≈
197,64Дж ≈1,98
Дж
Дано:
Мя ( =15,99491 а.е.м.
Z = 8; N =8
8∙ тр = 8 ∙1,00728 а.е.м.=
8,05824 а.е.м.
8∙тп = 8∙ 1,00866 а.е.м. = 8,06928 а.е.м.
E0 =?
Задача5. Определите энергию связи ядра лития
Решение:
=(3,02184+3,02598)
а.е.м.–
= 0,03272 а.е.м. ∙
931,5 МэВ/ а.е.м. =30,47868 МэВ
Ответ:
≈ 30,48 МэВ
Дано:
Мя ( =6,0151 а.е.м.
Z = 3; N =3
3∙ тр = 3 ∙1,00728 а.е.м.=
3,02184 а.е.м.
3∙тп
= 3∙ 1,00866 а.е.м. =3,02598
а.е.м.
E0 =?
Планируемые результаты обучения
Метапредметные
·
Овладеть регулятивными
УУД на примерах решения задач на расчет дефекта масс и энергию связи атомных
ядер;
·
уметь выражать свои мысли
и высказывать их при решении задач.
Частные предметные:
·
объяснять физический смысл
понятий «энергия связи», «дефект масс».
Общие предметные:
·
применять знания о строении
ядра атома, дефекте масс и энергии связи при решении расчетных задач;
·
анализировать полученные
числовые результаты;
Личностные:
·
сформировать
познавательный интерес к изучению ядерной физики, расширить свой
политехнический кругозор.
Домашнее задание. § 57. Вопросы после § 57 (устно). Итоги урока,
выставление оценок — 4 мин.
Задача 1. Определите дефект масс ядра атома бора в
атомных единицах массы и килограммах. Мя ( =10,01294 а.е.м
Задача2. Вычислите энергию связи ядра лития
Мя
( =26,98153 а.е.м
Литература.
1.Учебник физика 9 класс
А.В. Перышкина, Е.М. Гутник .
2.Л.А. Крик Физика 9 класс Контрольные и
самостоятельные работы.
3.Е.М. Гутник, О.А. Черникова
Методическое пособие к учебнику А.В.
Перышкина, Е.М. Гутник
« физика 9 класс»
4.О.И. Громцева
Контрольные и самостоятельные работы по физике.
К учебнику А.В. Перышкина, Е.М. Гутник
« физика 9 класс»
Дефект массы и энергия связи ядра
Масса ядра mя
меньше чем масса составляющих его
частиц в свободном состоянии. Уменьшение
массы ядра обусловлено тем, что при его
образовании выделяется энергия. Мерой
разности масс ядра и входящих в него
частиц служит так называемый дефект
массы ядра Δm.
Это разность между суммарной массой
протонов mр
и нейтронов
mn
и массой ядра mя
Δm
= Zmp
+ (A – Z)mn
– mя
,
Для вычисления
дефекта массы ядра удобнее пользоваться
формулой, в которой масса протона тр
заменяется массой первого изотопа
водорода
,
а масса ядратя
заменяется массой соответствующего
атома та.
,
Вычисления приводят
к одинаковым результатам.
Работу, которую
нужно совершить при разложении ядра на
составные части – протоны и нейтроны,
называют энергией связи ядра Есв
Есв
= Δm
с2,
Есв
= [Z·mp+
(A-Z)mn
– mя]·c2.
Согласно
закону сохранения энергии при образовании
ядра должна выделяться энергия, равная
энергии связи ядра. Удельной энергией
связи называют отношение
В выражении для
Есв
массы частиц и ядра берут в атомных
единицах массы.
1 а.е.м. = 1,667·10-27
кг. Одной
а.е.м. соответствует энергия, равная 931
МэВ (мегаэлектронвольт).
У ядер с массами
от 40 до 120 Еуд
8,6 МэВ/нуклон. Максимум энергии связи
наблюдается у ядер с четными числами
протонов и нейронов:;
;
,
минимумы у ядер с нечетными числами
протонов и нейронов:;
.
Ядра, как и атомы,
характеризуются дискретными значениями
энергии. Ядро в основном состоянии имеет
энергию Е, равную энергии связи Е = Есв.
Если Е > Есв
, то ядро находится в возбужденном
состоянии. Если Е = 0, то это значит, что
ядро расщеплено на составляющие его
нуклоны.
Ядерные силы
Хотя в чрезвычайно
малом объёме ядра сконцентрированы
одноимённые заряды (протоны), между
которыми действуют кулоновские силы
отталкивания, ядра атомов являются
чрезвычайно устойчивыми образованиями.
Силы, удерживающие нуклоны в ядре ни
электрического, ни гравитационного
происхождения. Эти силы получили название
ядерных. Взаимодействие между нуклонами
в ядре являет пример сильных взаимодействий.
Ядерные силы
обладают рядом свойств, некоторые из
которых следующие:
-
Ядерные
силы являются силами притяжения. -
Ядерные силы –
короткодействующие, радиус действия
ядерных сил ≃
10-15
м, т.е. порядка размера ядра. -
Ядерные силы
обладают свойством зарядовой
независимости. Это означает, что ядерные
силы, действующие между протоном и
нейтроном, нейтроном и нейтроном,
протоном и протоном одинаковы. На
справедливость этого свойства указывает
величина энергии связи зеркальных
ядер.
Ядра
и
являются зеркальными, т.к.ZH
= NHe,
а NH
=ZHe.
Энергия связи их ядер 8,49 МэВ и 7,72 МэВ.
Энергия связи у ядра гелия ниже, т.к.
взаимное отталкивание протонов в нем
уменьшает энергию связи
-
Ядерные силы не
являются центральными, как, например,
кулоновские и гравитационные.
Нецентральность ядерных сил зависит
от ориентации спинов нуклонов –
параллельными или антипараллельными
они являются. Эксперименты по рассеянию
нейтронов на молекулах орто- и параводорода
подтверждают это. В молекулах ортоводорода
спины обоих протонов в ядре параллельны,
а в молекулах пара Н2
– антипараллельны и поток нейтронов
на них рассеивается по разному. -
Ядерные силы
обладают свойством насыщения. Каждый
нуклон взаимодействует не со всеми
нуклонами ядра, а только с ограниченным
числом ближайших к нему нуклонов.
Удельная энергия связи нуклонов в ядре
при увеличении числа нуклонов остается
примерно постоянной. Примером полного
насыщения является α-частица.
Соседние файлы в папке Физика
- #
- #
- #
- #
- #
- #
- #