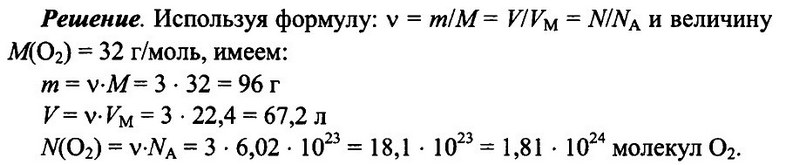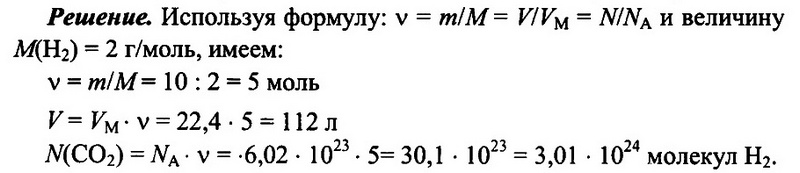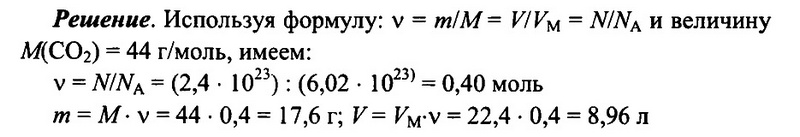Молярный объём
Vm
— это отношение объёма данной порции вещества к его количеству.
Численно молярный объём равен объёму (1) моль вещества.
Обрати внимание!
Молярный объём любого газа при нормальных условиях (давлении (101,3) кПа и температуре (0) °С) равен (22,4) дм³/моль.
Вычисление объёма газа по его количеству
Преобразуем формулу молярного объёма — выразим из неё
V
:
— объём газа равен произведению его количества на молярный объём.
Пример:
вычисли объём (н. у.) метана количеством (1,5) моль.
дм³.
Вычисление количества газа по его объёму
Выразим из формулы молярного объёма
n
:
— количество газа можно вычислить, если его объём разделить на молярный объём.
Пример:
вычисли количество водорода, соответствующее при н. у. его объёму (11,2) дм³.
моль.
Молярная масса
Вы знаете, что одинаковое химическое количество любых веществ содержит одно и то же число структурных единиц. Но у каждого вещества его структурная единица имеет собственную массу. Поэтому и массы одинаковых химических количеств различных веществ тоже будут различны.
Молярная масса — это масса порции вещества химическим количеством 1 моль.
Молярная масса вещества Х обозначается символом M(Х). Она равна отношению массы данной порции вещества m(Х) (в г или кг) к его химическому количеству n(Х) (в моль):
В Международной системе единиц молярная масса выражается в кг/моль. В химии чаще используется дольная единица — г/моль.
Определим молярную массу углерода. Масса углерода химическим количеством 1 моль равна 0,012 кг, или 12 г. Отсюда:
Молярная масса любого вещества, если она выражена в г/моль, численно равна его относительной молекулярной (формульной) массе.
Например:
На рисунке 47 показаны образцы веществ (H2O, CaCO3, Zn), химическое количество которых одно и то же — 1 моль. Как видите, массы разных веществ химическим количеством 1 моль различны.
Молярная масса является важной характеристикой каждого отдельного вещества. Она отражает зависимость между массой и химическим количеством вещества. Зная одну из этих величин, можно определить вторую — массу по химическому количеству:
и, наоборот, химическое количество по массе:
а также число структурных единиц:
Взаимосвязь между этими тремя характеристиками вещества в любом его агрегатном состоянии можно выразить простой схемой:
Формула и алгоритм нахождения объёма
Сегодня мы научимся одному немаловажному умению в химии – находить объём различных растворов и прочих веществ. Это знание необходимо потому, что оно поможет нам в решении многих задач как в тетради, так и в жизни. Нужно лишь знать устоявшуюся формулу.
Важно понимать, что формула нахождения объёма может быть разной в зависимости от того вещества, объём которого нам предстоит найти, а точнее, от агрегатного состояния этого вещества. Для нахождения объёма газа и жидкости используются разные, непохожие друг на друга формулы.
Чёткая и правильная формула для расчёта объёма жидкости выглядит следующим образом: С=n/V.
В этом случае:
- C – молярная масса раствора (моль на литр).
- n – количество вещества (моль).
- V – объём вещества-жидкости (литры).
Из этого следует что V=n/c.
Cуществует и вторая формула для нахождения объёма жидкости при другой задаче и других данных: V=m/p.
Здесь, соответственно:
- V – объём и измеряется он в миллилитрах.
- m – масса, измеряется в граммах.
- p – плотность, измеряется в граммах, делённых на миллилитры.
В случае если, кроме объёма, требуется также найти массу, это можно сделать, зная формулу и количество нужного вещества. При помощи формулы вещества находим его молярную массу путём сложения атомной массы всех элементов, которые входят в его состав.
Для примера возьмём M (AuSo2) и при расчётах у нас должно выйти 197+32+16 * 2 = 261 г/моль. После проведённых расчётов находим массу по формуле m=n*M, где, следовательно:
- m – масса.
- n – количество вещества, которое измеряется в молях (моль).
- M – молярная масса вещества: граммы, делённые на моль.
Количество вещества, как правило, даётся в задаче. Если же нет, то, скорее всего, допущена опечатка или ошибка в условии, и вам стоит обратиться за помощью и объяснениями к учителю, а не пытаться самим вывести несуществующую величину. Основные формулы и алгоритмы решения приведены в данной статье.
Также существует формула для нахождения объёма газа, и выглядит она так – V=n*Vm:
- V – объём газа (литры).
- n – количество вещества (моль).
- Vm – молярный объём газа (литры/моль).
Но есть своего рода исключение. Оно состоит в том, что при нормальных условиях, то есть при определённом давлении и температуре, объём газа является постоянной величиной, равной 22,3 л/моль.
Есть и третий вариант. Если в самом задании будет присутствовать уравнение реакции, тогда ход решения должен проходить иначе. Из уравнения, которое у вас имеется, можно найти количество каждого вещества, оно будет равняться коэффициенту. К примеру, Ch4 + 2O2 = CO2 + H2O. Из этого уравнения следует, что 1 моль метана и 2 моль кислорода при взаимодействии дают 1 моль углерода и 1 моль воды. Даже если учесть тот факт, что в условии имеется количество вещества лишь одного-единственного компонента, не составит труда найти количество всех остальных веществ. Если количество метана составит 0,3 моль, значит, n(Сh4) будет равняться 0,6 моль, n(CO2) = 0,3 моль, n(H2O) = 0.3 моль.
б) Газовые законы объем газа
Кроме вышеуказанной формулы для решения расчетных химических задач, нередко приходится использовать газовые законы, известные из курса физики.
— Закон Бойля-Мариотта
При постоянной температуре объем данного количества газа обратно пропорционален давлению, под которым он находится:
pV = const
— Закон Гей-Люссака
При постоянном давлении изменение объема газа прямо пропорционально температуре:
V/T = const
— Объединенный газовый закон Бойля-Мариотта и Гей-Люссака
pV/T = const
Помимо этого, если известна масса или количество газа, его объем можно вычислить, используя уравнение Менделеева-Клапейрона:
pV = nRT;
pV = n/M ×RT,
где n–число молей вещества, m–масса (г), Ь – молярная масса газа (г/моль), R – универсальная газовая постоянная равная 8,31 Дж/(моль×К).
Молярный объем кристаллов
Объем Vя элементарной ячейки кристалла вычисляют с помощью характеристик кристаллической структуры, которые определяют на основании результатов рентгеноструктурного анализа.
Зависимость между объемом ячейки и молярным объемом:
Vm=VяNA/Z
где Z — определяет, сколько формульных единиц в элементарной ячейке.
Молярный объем
В отличие от твердых и жидких веществ все газообразные вещества химическим количеством 1 моль занимают одинаковый объем (при одинаковых условиях). Эта величина называется молярным объемом и обозначается Vm.
Подобно молярной массе, молярный объем газа равен отношению объема данного газообразного вещества V(Х) к его химическому количеству n(Х):
Так как объем газа зависит от температуры и давления, то при проведении различных расчетов берутся обычно объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимаются температура 0 °С и давление 101,325 кПа.
Установлено, что при нормальных условиях отношение объема любой порции газа к химическому количеству газа есть величина постоянная и равная 22,4 дм3/моль. Другими словами, молярный объем любого газа при нормальных условиях:
Молярный объем — это объем, равный 22,4 дм3, который занимает 1 моль любого газа при нормальных условиях.
Пример 1. Вычислите химическое количество SiO2, масса которого равна 240 г.
Спойлер
[свернуть]
Пример 2. Определите массу серной кислоты H2SO4, химическое количество которой 2,5 моль.
Спойлер
[свернуть]
Пример 3. Сколько молекул CO2 и сколько атомов кислорода содержится в углекислом газе массой 110 г?
Спойлер
[свернуть]
Пример 4. Какой объем занимает кислород химическим количеством 5 моль при нормальных условиях?
Спойлер
[свернуть]
Краткие выводы урока:
- Масса вещества химическим количеством 1 моль называется его молярной массой. Она равна отношению массы данной порции вещества к его химическому количеству.
- Объем газообразных веществ химическим количеством 1 моль при нормальных условиях одинаков и равен 22,4 дм3.
- Величина, равная 22,4 дм3/моль, называется молярным объемом газов.
Надеюсь урок 9 «» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Данный урок был заключительным в главе «».
Теги
Как находить объем вещества в химии — V и его массу
Химия – одна из самых важных и разнообразных наук в нашей жизни. Это необязательно школьный предмет, ведь она окружает нас повсюду. В ней всё довольно запутано и порой даже противоречиво. Множество реакций протекает вокруг нас прямо сейчас, к примеру, приготовление пищи или же наложение компресса на рану. По сути, вся наша жизнь – это химическая реакция, поэтому химия очень важна.
Содержание:
- Введение
- Формула и алгоритм нахождения объёма
- Формула и алгоритм нахождения НЮ
- Видео
Введение
Знать, что такое объём в химии — недостаточно. Важно понимать как и что происходит, как протекает химическая реакция. Это нужно не просто для того, чтобы сдать очередную контрольную в школе или институте, а для того чтобы быть элементарно грамотным и знать: как, что и где применять, как приготовить раствор, какие вещества смешивать нельзя, а какие можно, какие из них опасны и какие безопасны. Всё это определённо приносит нам пользу, и, более того, делает нас умнее.
Формула и алгоритм нахождения объёма
Сегодня мы научимся одному немаловажному умению в химии – находить объём различных растворов и прочих веществ. Это знание необходимо потому, что оно поможет нам в решении многих задач как в тетради, так и в жизни. Нужно лишь знать устоявшуюся формулу.
Важно понимать, что формула нахождения объёма может быть разной в зависимости от того вещества, объём которого нам предстоит найти, а точнее, от агрегатного состояния этого вещества. Для нахождения объёма газа и жидкости используются разные, непохожие друг на друга формулы.
Чёткая и правильная формула для расчёта объёма жидкости выглядит следующим образом: С=n/V.
В этом случае:
- C – молярная масса раствора (моль на литр).
- n – количество вещества (моль).
- V – объём вещества-жидкости (литры).
Из этого следует что V=n/c.
Cуществует и
вторая формула для нахождения объёма жидкости при другой задаче и других данных: V=m/p.
Здесь, соответственно:
- V – объём и измеряется он в миллилитрах.
- m – масса, измеряется в граммах.
- p – плотность, измеряется в граммах, делённых на миллилитры.
В случае если, кроме объёма, требуется также найти массу, это можно сделать, зная формулу и количество нужного вещества. При помощи формулы вещества находим его молярную массу путём сложения атомной массы всех элементов, которые входят в его состав.
Для примера возьмём M (AuSo2) и при расчётах у нас должно выйти 197+32+16 * 2 = 261 г/моль. После проведённых расчётов находим массу по формуле m=n*M, где, следовательно:
- m – масса.
- n – количество вещества, которое измеряется в молях (моль).
- M – молярная масса вещества: граммы, делённые на моль.
Количество вещества, как правило, даётся в задаче.
Если же нет, то, скорее всего, допущена опечатка или ошибка в условии, и вам стоит обратиться за помощью и объяснениями к учителю, а не пытаться самим вывести несуществующую величину. Основные формулы и алгоритмы решения приведены в данной статье.
Также существует формула для нахождения объёма газа, и выглядит она так – V=n*Vm:
- V – объём газа (литры).
- n – количество вещества (моль).
- Vm – молярный объём газа (литры/моль).
Но есть своего рода исключение. Оно состоит в том, что при нормальных условиях, то есть при определённом давлении и температуре, объём газа является постоянной величиной, равной 22,3 л/моль.
Есть и третий вариант. Если в самом задании будет присутствовать уравнение реакции, тогда ход решения должен проходить иначе. Из уравнения, которое у вас имеется, можно найти количество каждого вещества, оно будет равняться коэффициенту. К примеру, Ch5 + 2O2 = CO2 + h3O. Из этого уравнения следует, что 1 моль метана и 2 моль кислорода при взаимодействии дают 1 моль углерода и 1 моль воды.
Даже если учесть тот факт, что в условии имеется количество вещества лишь одного-единственного компонента, не составит труда найти количество всех остальных веществ. Если количество метана составит 0,3 моль, значит, n(Сh5) будет равняться 0,6 моль, n(CO2) = 0,3 моль, n(h3O) = 0.3 моль.
Формула и алгоритм нахождения НЮ
Кроме того, нужно научиться находить так называемое НЮ в химии, ведь эти термины близко связаны и часто стоят рядом в какой-либо задачке.
НЮ в этом случае – количество вещества.
И как же нам его найти, спросите вы?
НЮ также находится довольно просто. Необходимо лишь применить логику и формулы, и все получится.
Для нахождения НЮ нам лишь нужно массу разделить на молярную массу. В виде формулы это будет выглядеть так: v=m/M.
Соответственно:
- m – масса.
- M – молярная масса.
Теперь вы знаете как в химии находится объём и масса вещества.
Видео
Из этого видео вы узнаете, как решать задачи по химии в несколько действий.
,
Онлайн калькулятор: Молярный объем газа
УчебаХимия
Этот онлайн калькулятор рассчитывает молярный объем идеального газа для разных условий (не-стандартных температуре и давлении)
Данный онлайн калькулятор рассчитывает молярный объем идеального газа в зависимости от условий (разных значений температуры и давления). Формулы и перечисление некоторых часто используемых значений для описания физических условий можно найти под калькулятором.
Молярный объем газа
Давление
Единицы измеренияатмПабармм.рт.ст.
Температура
Единицы измеренияградусы Цельсияградусы Кельвина
Точность вычисления
Знаков после запятой: 3
Молярный объем, литры
Калькулятор использует уравнение молярного объема идеального газа:
Уравнение идеального газа является достаточно близкой аппроксимацией для многих реальных газов. Для заданных температуры и давления, молярный объем для всех идеальных газов один и тот же, и известен с точностью совпадающей с точностью универсальной газовой постоянной: R = 0.082 057 338(47) Л атм K−1 моль−1, то есть относительная стандартная неопределенность молярного объема равна 5.7×10−7, в соответствии с рекомендацией CODATA от 20141
Так как молярный объем одинаков для всех газов, он может быть вычислен независимо от газа по температуре и давлению (физическим условиям).
по версии НИСТ (стандартной температуре 273.15 K и стандартному давлению 101.325 kPa), молярный объем идеального газа равен 22.413962×10-3 м3 моль-1 со стандартной неопределенностью 0.000013 x 10-3 м3 моль-12
Собственно, слова стандартные условия или нормальные условия (что не одно и тоже) для давления и температуры — это отсылка к «справочным», известным значениям температуры и давления, применяющимся для вычисления значений других физических величин, зависящих от давления и температуры.
Для удобства значения молярного объема для некоторых общеупотребимых физических условий приведены в таблице ниже.
| Физические условия | Температура | Давление | Молярный объем, литры |
|---|---|---|---|
| Стандартные условия (НИСТ) | 0C (273.15K) | 101.325кПа (1атм) | 22.414 |
| Стандартные условия (ИЮПАК) | 0C (273. 15K) 15K) |
100.000кПа (1бар) | 22.711 |
| Нормальные условия (некоторые ГОСТы, НИСТ) | 20C (293.15K) | 101.325кПа (1атм) | 24.055 |
Разные отрасли и организации, могут использовать свои значения температуры и давления для расчетов. Используя калькулятор, мы можете ввести нужные вам значения температуры и давления и получить молярный объем газа.
Обратите внимание, что для больших значений (сотни атмосфер и тысячи градусов) поведение реальных газов отличается от поведения идеальных газов (собственно, поэтому они и не «идеальные») и использовать уравнение, приведенное выше, нельзя.
-
Молярный объем (википедия) ↩
-
Молярный объем идеального газа (справочник НИСТ) ↩
Ссылка скопирована в буфер обмена
Похожие калькуляторы
- • Перевод литров газа в граммы и наоборот
- • Перевод молей в литры и литров в моли
- • Уравнение Клапейрона-Менделеева.
Связь между числом молей газа, его температурой, объемом и давлением.
- • Концентрация газа из ppm в мг/м³ и обратно
- • Молярная масса соединений
- • Раздел: Химия ( 15 калькуляторов )
#Газы #химия Газы давление идеальный газ литры молярный объем объем температура Химия
PLANETCALC, Молярный объем газа
Timur2020-11-03 14:19:38
Молярный объем Химия — 2022
Молярный объем – это объем, занимаемый одним молем любого газа при определенном давлении и температуре. Обозначается V м . Молярный объем вещества зависит от температуры и давления. Единицей молярного объема является литр на моль или миллилитр на моль.
Согласно закону Авогадро, равные объемы всех газов содержат равное количество молекул при постоянной температуре и давлении.
Стандартный молярный объем
Стандартный молярный объем газа – это объем, занимаемый 1 молем любого газа при температуре 273 К и давлении 1 атм (СТД). Он равен 22,4 литра 22 400 мл. Он одинаков для всех газов.
Запомнить
S.T.P. = Стандартная температура и давление
Стандартная температура = 0 o C или 273 K
Стандартное давление = 1 атм или 760 мм ртутного столба
Расчет молярного объема
Пример кислорода
Масса 1 л кислорода при STP = 1,429 г
Масса 1 моля кислорода = 32 г
Объем: масса
1 л: 1,429 г
x : 32 г
x = 9000/ 1,429
x= 22,4 литра
В следующей таблице показано соотношение между граммовой молекулярной массой (GMW), числом молей, молярным объемом и числом частиц для газов при нормальных условиях.
Зависимость между различными параметрами газов по СТП
| Gas | Molecular Formula | GMW (in g) |
No.Of Moles | Molar Volume dm 3 or l |
No.of moles in 1 mole |
| Hydrogen | H 2 | 2 | 1 | 22.4 | 6.023x 10 23 |
| Oxygen | O 2 | 32 | 1 | 22.4 | 6.023x 10 23 |
| Nitrogen | N 2 | 28 | 1 | 22.4 | 6.023x 10 23 |
| Chlorine | Cl 2 | 71 | 1 | 22.4 | 6.023x 10 23 |
| Carbon dioxide | CO 2 | 44 | 1 | 22. 4 4 |
6.023x 10 23 |
| Nitrogen dioxide | NO 2 | 46 | 1 | 22.4 | 6.023x 10 23 |
| Ammonia | NH 3 | 17 | 1 | 22.4 | 6.023x 10 23 |
| Methane | CH 4 | 16 | 1 | 22.4 | 6.023x 10 23 |
| Sulphur dioxide | SO 2 | 64 | 1 | 22,4 | 6,023X 10 23 |
Проблемы на основе молярного объема
Пример:
.cord Copplaulate Of -Office Oppired. (N=14, H=1)
Раствор
Молекулярная масса аммиака в граммах (NH 3 ) = (1 x 14) + (3 + 1) = 14 + 3 = 17 г
Масса 1 моля аммиака = 17 г
Молярный объем = 22,4 литра
Объем 3,4 г аммиака при нормальных условиях = ?
Масса: том
17 г: 22,4 л
3,4 г: x
x = (3,4 x 22,4)/17
x = 4,48 литры
Торг.
Пример:
56 мл диоксида углерода имеет массу 0,11 г при нормальных условиях. Какова молярная масса углекислого газа?
Раствор:
Масса 56 мл диоксида углерода при нормальных условиях = 0,11 г
Масса 22400 мл диоксида углерода = ?
Масса: том
0,11 г: 56 мл
x g: 22400 мл
x = (0,11 x 22400)/56
x = 44 г
Масса 22400 мл углерода в STP = 44 G
Молярный Масса углекислого газа = 44 г/моль.
Пример:
Один грамм чистого диоксида серы имеет объем 350 мл при стандартной температуре. Какова относительная молекулярная масса диоксида серы?
Раствор:
Объем газообразного диоксида серы = 350 мл при стандартных условиях
Масса газообразного диоксида серы = 1 г
Масса одного моля диоксида серы = x г/моль
Объем 1 моля диоксида серы = 22400 мл при стандартных условиях
Масса: объем
1 : 350 мл x 1)/350 = 64
Масса 1 моля SO 2 = 64 г/моль
Относительная молекулярная масса диоксида серы = 64.
Относительная молекулярная масса
Относительная молекулярная масса представляет собой отношение масс одной молекулы вещества на массу 1/12
атома углерода или 1 а.е.м.
Плотность пара
Плотность пара представляет собой отношение массы объема газа к массе равного объема водорода, измеренное при тех же условиях температуры и давления.
плотность пара =
масса n молекул газа / масса n молекул водорода . (и таким образом: молярная масса = ~2 × плотность пара) Например, плотность пара смеси NO 2 и N 2 O 4 равно 38,3 . Плотность пара – безразмерная величина.
Закон Авогадро
Согласно закону Авогадро, в равных объемах всех газов содержится одинаковое количество молекул.
Таким образом, пусть количество молекул в одном объеме = n,
или,
Относительная молекулярная масса = 2 x Плотность пара
Зарегистрируйтесь на форуме и выполните задание :
Найдите вопросы в конце каждого урока.
Объявление: Получите БЕСПЛАТНУЮ Библию :
Обрести истинный покой. Нажмите здесь, чтобы узнать, как получить БЕСПЛАТНУЮ Библию.
По вопросам размещения рекламы/партнерства пишите [email protected]
Загрузите наше бесплатное мобильное приложение для Android :
Сохраняйте свои данные при использовании нашего бесплатного приложения. Нажмите на картинку, чтобы скачать. Нет подписки.
Мы заинтересованы в продвижении БЕСПЛАТНОГО обучения. Расскажите своим друзьям о Stoplearn.com. Нажмите кнопку «Поделиться» ниже!
Видео с вопросами: Расчет молярного объема газа при стандартной температуре и давлении (STP)
Стенограмма видео
Что такое молярный объем газа
при стандартной температуре и давлении до двух значащих цифр?
Это значение обычно указывается как
исходная величина. В этой задаче мы просто
получение этого значения, чтобы мы знали, откуда оно берется.
газ при стандартной температуре и давлении запоминается, вы можете использовать это эталонное значение
без выполнения математики, показанной здесь. Но для этой задачи мы будем нести
вне расчетов. Напомним, что молярный объем
количество литров, поглощаемое молем газа. Стандартная температура и давление
относится к температуре ноль градусов по Цельсию и давлению в один бар. Так как мы хотим, чтобы наша температура была
в кельвинах вместо градусов по Цельсию, мы просто добавляем 273 к нашему значению в градусах по Цельсию, чтобы найти
эта температура в кельвинах.
Формула молярного объема: 𝑉
m равно 𝑉, деленному на 𝑛, где 𝑉 m равно молярному объему, 𝑉 равно объему,
а 𝑛 равно количеству в молях. Однако мы не знаем объема
или количество в молях, поэтому мы не можем провести расчет напрямую. Тем не менее, мы знаем давление,
температура и значение газовой постоянной.
можно поставить 𝑉 на 𝑛 в терминах чисел, которые мы уже знаем, чтобы найти значение для 𝑉
над 𝑛. Если мы воспользуемся алгеброй и разделим оба
сторон уравнения на 𝑃 умножить на 𝑛, мы получим уравнение 𝑉 над 𝑛 равным
𝑅𝑇 над 𝑃. Мы сгруппировали все переменные
что мы не знаем значения в левой части уравнения и всех
переменные, значение которых мы знаем в правой части уравнения.
Мы знаем, что молярный объем
равно 𝑉 над 𝑛. Мы не знаем непосредственно значения
𝑉 больше 𝑛, но мы знаем, что оно равно 𝑅𝑇 больше 𝑃, значение, которое мы можем
рассчитать. Мы хотим использовать значение 𝑅, которое
соответствует единицам измерения, которые мы используем, а именно литрам и барам. Итак, мы хотим использовать значение 𝑅 равно
0,8315 литровых бар на моль-кельвин. Если мы подключим наши известные значения обратно
в уравнение, мы получаем 0,8315 литров бар на моль-кельвин умножить на 273 кельвина разделить
на один бар.
Решение задач на количество вещества,
массу и объем
Ключевые слова: решение задач на количество вещества, решение задач по химии на массу и объем, какое количества вещества содержится, какое число молекул содержится, определите объем (н.у.), определите массу, какова масса порции, определите молярную массу, назовите вещество, найдите молярную массу, определите абсолютную массу молекулы, сколько атомов содержится, определите относительную плотность.
ФОРМУЛЫ ДЛЯ РЕШЕНИЯ ЗАДАЧ
Количество вещества характеризует число структурных единиц (атомов, молекул, ионов), которое содержится в определенном образце данного вещества. Единицей измерения количества вещества является моль. Количество вещества (ν) связано с числом структурных единиц (N) в образце вещества, его массой (m) и объемом (V) — для газообразных веществ при н. у. — следующими уравнениями:

Vm = 22,4 л/моль (мл/ммоль, м3/кмоль) при н.у.,
Na = 6,02 • 1023 (постоянная Авогадро),
а молярная масса (М) численно равна относительной молекулярной массе вещества:
Наличие подобной взаимосвязи позволяет, зная одну из величин (количество вещества, массу, объем, число структурных величин) определить все другие величины.
РЕШЕНИЯ ПРОСТЫХ ЗАДАЧ
Задача № 1.
Какое количество вещества содержится в 33 г оксида углерода (IV)?
Ответ: ν(СО2) = 0,75 моль.
Задача № 2.
Какое число молекул содержится в 2,5 моль кислорода?
Ответ: N(O2) = 1,505 • 1024.
Задача № 3.
Определите объем (н. у.), который займут 0,25 моль водорода.
Задача № 4.
Какую массу будет иметь порция оксида серы (IV), объем которой 13,44 л (н. у.)?
Задача № 5.
Имеется 3 моль кислорода О2 при н.у. Определите массу кислорода, его объем, а также число имеющихся молекул кислорода.
Ответ: m = 96 г; V = 67.2 л; N(O2) = 1,81 • 1024.
Задача № 6.
Имеется 10 г водорода Н2. Определите количество водорода, его объем при н.у., а также число имеющихся молекул водорода.
Ответ: 5 моль; 112 л; 3,01 • 1024.
Задача № 7.
Имеется 56 л хлора Сl2 при н.у. Определите количество вещества хлора, его массу и число имеющихся молекул хлора.
Ответ: 2,5 моль; 177,5 г; 1,5 • 1024.
Задача № 8.
Имеется 2,4 • 1023 молекул оксида углерода (IV) СO2. Определите количество вещества углекислого газа, его массу, а также объем (н.у.) углекислого газа.
Ответ: 0,4 моль; 17,6 г; 8,96 л.
Задача № 9.
Какова масса порции оксида азота (IV), содержащей 4,816 • 1023 молекул? Каков ее объем (н. у.)?
Задача № 10.
Масса порции простого вещества, содержащей 1,806 • 1024 молекул, равна 6 г. Определите молярную массу данного вещества и назовите его.
Внимание! В данном конспекте рассматриваются задачи обычной сложности. Чтобы перейти к конспекту решения сложных задач на количественные характеристики и задачи с кратким ответом нажмите на кнопку ниже…
Сложные задачи на количество …
Решение задач на количество вещества, массу и объем. Выберите дальнейшие действия:
- Перейти дальше: Решение задач с долей вещества в смеси, в соединении
- Вернуться к списку конспектов по Химии.
- Проверить знания по Химии.
Молярный объем газа

4.3
Средняя оценка: 4.3
Всего получено оценок: 503.
4.3
Средняя оценка: 4.3
Всего получено оценок: 503.
Для того, чтобы узнать состав любых газообразных веществ необходимо уметь оперировать такими понятиями, как молярный объем, молярная масса и плотность вещества. В данной статье рассмотрим, что такое молярный объем, и как его вычислить?
Количество вещества
Количественные расчеты проводят с целью, чтобы в реальности осуществить тот или иной процесс или узнать состав и строение определенного вещества. Эти расчеты неудобно производить с абсолютными значениями массы атомов или молекул из-за того, что они очень малы. Относительные атомные массы также в большинстве случаев невозможно использовать, так как они не связаны с общепринятыми мерами массы или объема вещества. Поэтому введено понятие количество вещества, которое обозначается греческой буквой v (ню) или n. Количество вещества пропорционально числу содержащихся в веществе структурных единиц (молекул, атомных частиц).
Единицей количества вещества является моль.
моль – это такое количество вещества, которое содержит столько же структурных единиц, сколько атомов содержится в 12 г изотопа углерода.
Масса 1 атома равна 12 а. е. м., поэтому число атомов в 12 г изотопа углерода равно:
Na= 12г/12*1,66057*10в степени-24г=6,0221*10 в степени 23
Физическая величина Na называется постоянной Авогадро. Один моль любого вещества содержит 6,02*10 в степени 23 частиц.
Молярный объем газа
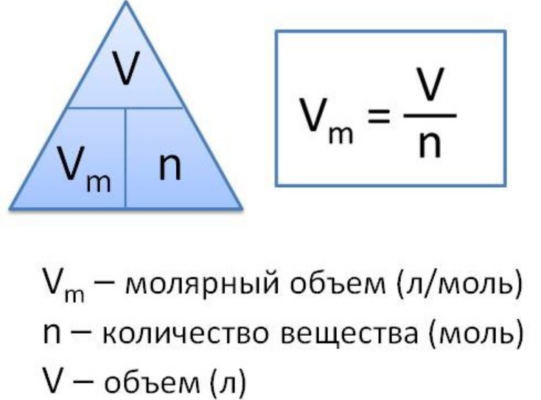
Молярный объем газа – это отношение объема вещества к количеству этого вещества. Эту величину вычисляют при делении молярной массы вещества на его плотность по следующей формуле:
Vm=M/p,
где Vm – молярный объем, М – молярная масса, а p – плотность вещества.
В международной системе Си измерение молярного объема газообразных веществ осуществляется в кубических метрах на моль (м3 /моль)
Молярный объем газообразных веществ отличается от веществ, находящихся в жидком и твердом состоянии тем, что газообразный элемент количеством 1 моль всегда занимает одинаковый объем (если соблюдены одинаковые параметры).
Объем газа зависит от температуры и давления, поэтому при расчетах следует брать объем газа при нормальных условиях. Нормальными условиями считается температура 0 градусов и давление 101,325 кПа. Молярный объем 1 моля газа при нормальных условиях всегда одинаков и равен 22,41 дм3 /моль. Этот объем называется молярным объемом идеального газа. То есть, в 1 моле любого газа (кислород, водород, воздух) объем равен 22,41 дм3 /м.
Таблица «молярный объем газов»
В следующей таблице представлен объем некоторых газов:
| Газ | Молярный объем, л |
| H2 | 22,432 |
| O2 | 22,391 |
| Cl2 | 22,022 |
| CO2 | 22,263 |
| NH3 | 22,065 |
| SO2 | 21,888 |
| Идеальный | 22,41383 |
Что мы узнали?
Молярный объем газа, изучаемый по химии (8 класс) наряду с молярной массой и плотностью являются необходимыми величинами для определения состава того или иного химического вещества. Особенностью молярного газа является то, что в одном моле газа всегда содержится одинаковый объем. Этот объем называется молярным объемом газа.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Аэлита Коробка
5/5
-
Александр Котков
5/5
-
Настя Бабич
5/5
-
Александр Котков
5/5
Оценка доклада
4.3
Средняя оценка: 4.3
Всего получено оценок: 503.
А какая ваша оценка?















 Связь между числом молей газа, его температурой, объемом и давлением.
Связь между числом молей газа, его температурой, объемом и давлением.