При диагностике подагры или мочекислого диатеза показатель кислотности мочи играет ключевую роль. Определение pH мочи является стандартным скрининговым тестом, выполняемым при профосмотре или при поступлении в стационарное отделение больницы.
Этот тест входит в общий анализ мочи, который, помимо уровня кислотности урины, учитывает количество, цвет, плотность, наличие клеточных элементов, белков и кристаллов солей.
Что такое кислотность мочи
В процессе метаболизма в организме человека происходит множество химических реакций, необходимых для роста, развития и поддержания жизни.
Для прохождения всех этих реакций в кровеносной системе и внутриклеточном пространстве должно поддерживаться определенное кислотно-основное состояние.
Делается это за счет различных биохимических буферных систем и выделения продуктов обмена в окружающую среду. К органам, отвечающим за утилизацию побочных элементов, относятся печень, легкие, кожа и почки.
Почки являются важнейшим органом выделения, т. к. в моче, производимой ими, находятся азотсодержащие соединения. Эти вещества, накапливаясь в организме, способны оказывать пагубное влияние на мозг, сердце и другие жизненно важные органы.
Помимо этого, моча – это прекрасный индикатор, указывающий на множество изменений, происходящих в организме.
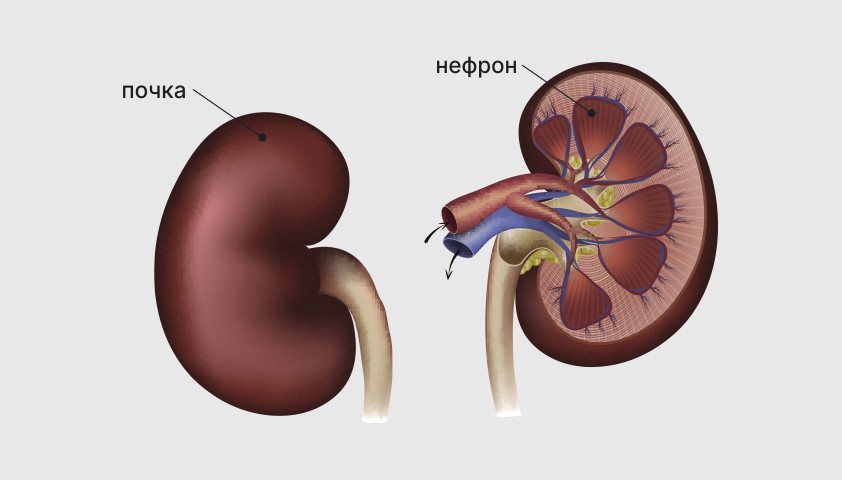
В почках есть функциональная единица, называемая нефроном, в которой и образуется моча посредством ультрафильтрации крови. Что же такое кислотность?
Если воспринимать урину в качестве неорганического раствора, то в ней будет присутствовать огромное количество солей, кислот, щелочей и свободных ионов, попавших туда при фильтрации в почечных нефронах. pH мочи зависит от количества несвязанных атомов водорода.
При повышении свободных H+ кислотные свойства урины будут более выражены. Это означает, что чем выше показатель ионов водорода в моче, то тем больше будет кислотность.
Нормы рН

Нормальная кислотность – это довольно обширный термин, который не дает полное представление о состоянии организма на данный момент ввиду влияния многочисленных факторов.
Существуют общепринятые показатели, выход за пределы которых, характеризуется как наличие патологии. Для мочи норма pH будет находиться в пределах от 5,0 до 7,0. Кратковременные колебания показателя кислотности от 4,5 до 8,0 могут считаться нормой, если они несут кратковременный характер, и нет тревожных симптомов вроде полиурии, олигурии или боли при мочеиспускании.
Также показатели pH колеблются в зависимости от времени суток, степени физической активности, индивидуальных особенностей организма или диеты. Например, в утреннее время pH — 6-6,5, а вечером кислотность поднимается до 7. Кроме того, имеет большое значение соотношение выделяемой жидкости к выпитой.
Оптимальные цифры кислотности у мужчин могут быть выше, чем у женщин, за счет большего процента мышечной массы, а также стереотипа питания, подразумевающего употребление большего количества мясных продуктов. Как бы там ни было, оптимальным общепринятым значением кислотности для взрослых является диапазон от 6,3 до 6,5.
У женщин на период вскармливания грудью этот показатель может подниматься до 7,8. В результате высокого уровня обмена веществ для новорожденных детей цифры кислотности будут совершенно другие. У среднестатистического ребенка уровень pH мочи составляет от 5,4 до 5,9 единиц, а для преждевременно рожденных — 4,8-5,4.
Причины изменения кислотности мочи
Большинство продуктов обмена веществ выводится из организма через почки, поэтому нужно понимать, что кислотность обусловлена влиянием многих факторов.
По большому счету, кислотность – это динамическая величина, которая отличается у разных людей и даже меняется у одного человека в зависимости от употребляемой пищи, принимаемых лекарственных веществ, образа жизни или времени суток. Изменение pH мочевого осадка может происходить в сторону закисления или в сторону защелачивания.
Закисление
Закисление урины – это состояние, при котором pH становится менее 5,0. Это может происходить вследствие смены диеты, при усиленных физических нагрузках или при патологии мочевыделительной системы.
Существует огромная масса заболеваний, способствующих изменению кислотности мочи. В основном pH снижается до 5 при сахарном диабете. Кислая реакция мочи возникает при следующих состояниях:
- метаболический ацидоз;
- для сахарного диабета характерно значительное изменение состава урины не только в плане снижения кислотности, но и в виде повышения количества глюкозы;
- лихорадка;
- подагра – распространенное ревматологическое заболевание, характерным признаком которого является кислая среда мочи. Заболевание обусловлено нарушением пуринового обмена, вследствие чего в организме начинает накапливаться большое количество мочевой кислоты;
- лейкоз;
- питание продуктами с низким содержанием углеводов;
- увеличение кислотности мочи может быть вызвано препаратами, повышающими диурез. Это значит, что подобные лекарственные средства разрешается пить только короткими курсами;
- инфекционные заболевания мочевыделительной системы, вызванные кишечной палочкой или микобактерией;
- хроническая почечная недостаточность;
- употребление продуктов с высоким содержанием белков. Помимо мяса, к кислотоповышающим продуктам относятся белый хлеб, рыба и сыр;
- сепсис;
- лечение аскорбиновой кислотой в дозировке более 2 г в день значительно увеличивает pH урины, а также повышает риск развития мочекаменной болезни;
- патологии пищеварительной системы.

Также небольшое снижение уровня pH мочевого осадка встречается у новорожденных детей. Кислая моча у новорожденного полностью физиологична и не должна вызывать беспокойства у родителей. По мере взросления ребенка кислотность мочи будет выравниваться.
Защелачивание
Защелачиванием мочи называется состояние, при котором уровень pH становится более 7. Щелочь в моче может обнаруживаться при регулярном употреблении молочнокислых или растительных продуктов, а также при бактериальных и обменных заболеваниях. Причинами таких отклонений могут быть следующие факторы:
- хроническая бактериальная инфекция мочевыводящих путей. Микробы способны ферментировать азотсодержащие соединения до аммиака, что приводит к повышению pH;
- гиперкалиемия;
- недостаточность гормонов надпочечников;
- почечно-канальцевый ацидоз;
- метаболический и респираторный алкалоз;
- выделение мочи с кровью (гематурия);
- повышенный уровень фосфатсодержащих соединений в моче;
- употребление большого количества минеральной воды;
- диета, содержащая большое количество растительной пищи, черного хлеба, молока;
- воспаление стенок мочевыводящих путей (цистит, уретрит);
- послеоперационный период.

Также временное защелачивание мочи может быть вызвано внутривенным введением раствора буферной соды. Его вводят в экстренных случаях, сопровождаемых значительным закислением крови (сепсис, печеночная недостаточность, кетоацидотическая кома).
Клинически повышение уровня pH проявляется общей слабостью, диффузной головной болью, тошнотой и рвотой.
Способы определения рН мочи

Необходимо брать только свежую мочу, потому что при длительном хранении изменяются ее физико-химические свойства, что дает искаженные результаты диагностического теста. Определение pH в анализе мочи осуществляется несколькими способами.
Анализ в лабораторных условиях позволяет не только учитывать физико-химические свойства, но и определить наличие клеточных элементов (эритроциты, лейкоциты), белков, кристаллов, цилиндров, сахара и много другого.
Расшифровка анализа проводится врачом-лаборантом, и на основании результатов могут рекомендоваться дополнительные методы исследования, позволяющие при необходимости уточнить диагноз. Лабораторные исследования являются наиболее точными, поэтому при подозрении на наличие заболевания лучше всего прибегать к ним.
На данный момент в любой аптеке можно приобрести полоски для определения кислотности. Это особые индикаторные тесты, которые учитывают несколько показателей. Такие полоски значительно упрощают анализ и позволяют проводить тест в домашних условиях.
Нужно понимать, что однократный тест не может быть достоверным по нескольким причинам. Во-первых, на результат влияют употребляемые продукты.
Например, если у человека в норме pH 6,0, то длительная белковая диета снижает этот показатель, поэтому перед тестом рекомендуется отказаться от употребления большого количества мяса. Во-вторых, тесты могут быть неточны, поэтому при получении результата лучше провести анализ повторно.
Результаты теста должны интерпретироваться только врачом. Ни в коем случае нельзя самостоятельно назначать лечение, иначе это может усугубить состояние и привести к непоправимым последствиям. В то же время некоторым больным, с разрешения доктора, иногда рекомендуется периодическое измерение кислотности мочи в домашних условиях.
Регулярный анализ мочи с целью определения уровня pH рекомендован лицам, страдающим от мочекаменной болезни. Делается это для оценки эффективности лечебной диеты и определения риска дальнейшего прогресса формирования конкрементов.
В заключение

Показатели pH могут иметь широкий диапазон, на который влияет огромное количество факторов, поэтому для получения более точных результатов все лабораторные исследования должны проводиться повторно.
Как образуется моча
Моча образуется в процессе фильтрации крови почками. Проходя через почки, кровь очищается от ненужных веществ. Основной её объём отправляется обратно в кровоток, а небольшое количество жидкости выводится из организма в виде мочи.
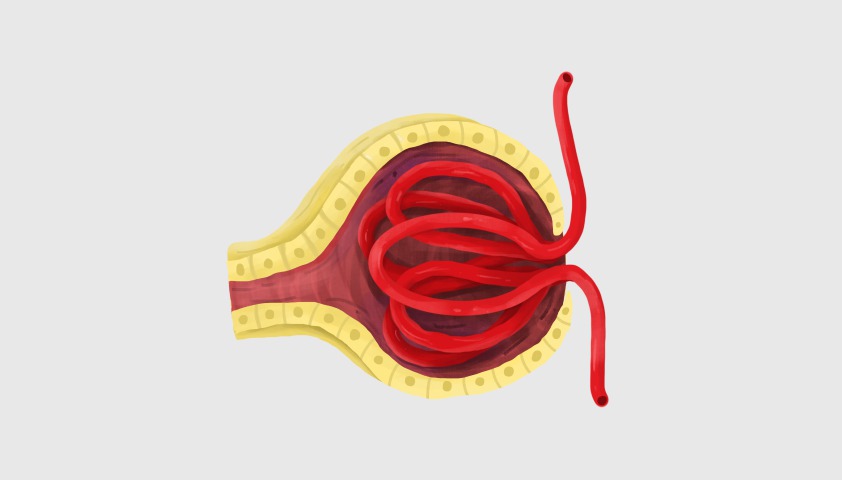
Каждая почка состоит из нескольких сегментов — нефронов. В нефроне есть клубочки и канальцы
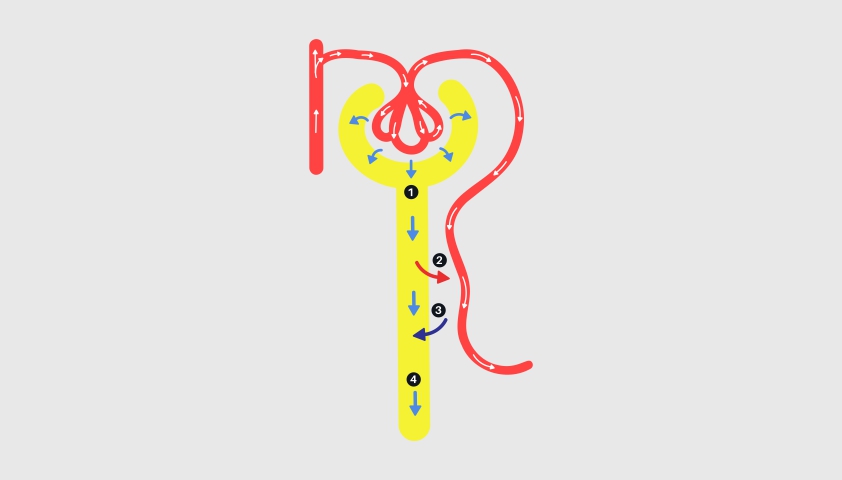
В клубочках почки происходит фильтрация крови. Образующаяся жидкость называется первичной мочой
В канальцах почки первичная моча фильтруется повторно, и часть жидкости снова отправляется в кровоток (этот процесс называется реабсорбция)
Моча на 95% состоит из воды и на 5% из примесей: электролитов, продуктов распада компонентов клеток.
Если человек заболевает, состав мочи меняется. Например, при воспалительных заболеваниях почек моча может стать мутной или поменять цвет. А при сахарном диабете — значительно увеличивается объём выделяемой жидкости.
Основные характеристики мочи
Изменения мочи могут говорить о самых разных патологиях: заболеваниях почек, инфекционных процессах, эндокринных нарушениях.
Какие-то нарушения можно заметить самостоятельно. Например, что позывов в туалет и отделяемой мочи стало меньше или что жидкость изменила оттенок или запах. Другие можно выявить только в ходе лабораторных исследований.
9.1. 
1 день

9.2. 
1 день

10.1. 
Колич. 1 день

120.1. 
1 день

1.48.31. 
5 дней

Есть ряд характеристик мочи, которые используются для оценки мочевыделительной, эндокринной и других систем. Изменения могут быть качественными и количественными. Среди качественных — такие показатели, как цвет, прозрачность, пенистость. Среди количественных — объём жидкости, выделяемый в течение суток.
Количество
Количество выделяемой мочи, или диурез, определяется в ходе суточного анализа: пациент в течение 24 часов собирает мочу в ёмкость, а затем оценивает её приблизительный объём. Нормальным считается количество мочи от 800 мл до 2 л. Если диурез менее 500 мл, ставят диагноз «олигурия». Если более 2 л — «полиурия».
Возможные причины изменения объёма мочи
Олигурия — снижение количества отделяемой мочи — может говорить об обезвоживании (например, при повышении температуры тела или рвоте), сильных кровопотерях (при травме, после операции, во время менструаций).
Полиурия может указывать на развитие сахарного или несахарного диабета, избыточную выработку гормона околощитовидными железами или корой надпочечников. Также полиурия может указывать на заболевания мочевыделительной системы.
Цвет
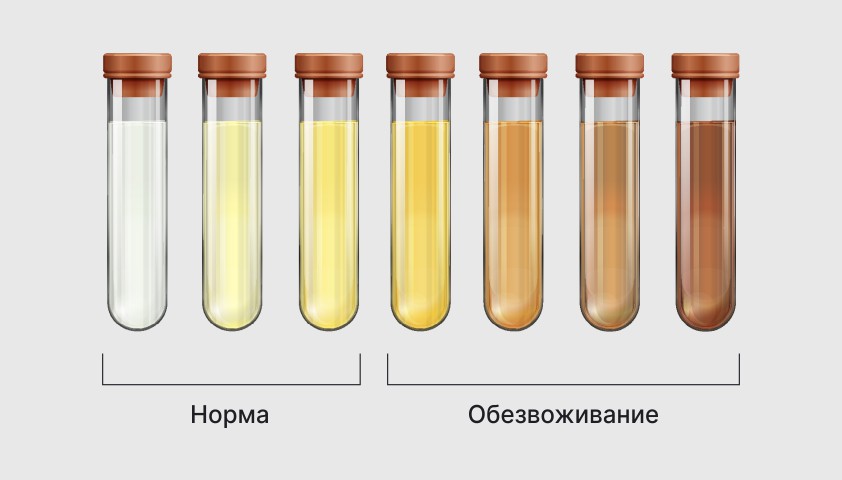
Цвет мочи определяет жёлчный пигмент, который вырабатывается в печени при распаде гемоглобина. В норме моча должна быть прозрачной или светло-жёлтой.
Возможные причины изменения цвета мочи
Перемена цвета мочи не всегда говорит о патологии. Оттенок может меняться из-за натуральных или синтетических красителей, присутствующих в пище, или изменения обьёма потребляемой жидкости.
По цвету мочи можно определить общее состояние организма и выявить некоторые патологии, в том числе обезвоживание
Также на цвет мочи могут влиять принимаемые лекарства: в зависимости от препарата, она может становиться ярко-жёлтой, оранжевой, красноватой или тёмно-коричневой.
Однако если цвет мочи изменился без явной причины, это повод пройти обследование. Оттенок может меняться на фоне заболеваний почек
(пиелонефрит, мочекаменная болезнь, инфаркт почки) и печени (гепатит, цирроз, желчнокаменная болезнь) или при нарушении обмена веществ.
Прозрачность
Свежая моча в норме должна быть полностью прозрачной. Постепенно в ней может выпадать осадок из солей и слизи.
Возможные причины изменения прозрачности
Если моча мутная или со взвесью, это может говорить о том, что в ней присутствуют соли, бактерии, слизь. Такой состав указывает на воспалительные заболевания органов мочевыделительной системы, мочекаменную болезнь или нарушение обмена веществ.
Также моча может помутнеть, если человек ест много рыбы и морепродуктов.
Удельный вес (плотность)
Удельный вес говорит о том, насколько моча плотная, то есть концентрированная. Показатель достаточно нестабилен: меняется в течение суток (утром моча имеет наибольшую плотность), зависит от количества выпиваемой жидкости и даже от температуры воздуха на улице. Однако значительные отклонения от нормы могут указывать на развитие патологических процессов.
Возможные причины изменения удельного веса
Значительное отклонение плотности мочи от нормы может развиваться при нарушении обмена веществ, заболеваниях почек или мочевого пузыря, гормональном дисбалансе, воспалительных заболеваниях. Также плотность может повышаться при обезвоживании: поносе, рвоте, интенсивных тренировках.
Это один из показателей, которые человек может заметить даже без лабораторного исследования: чем насыщенней цвет мочи, тем выше её удельный вес. Повышение плотности мочи без очевидной причины (например, недавнего отравления) — повод обратиться к врачу.
Запах и пенистость
В норме свежая моча практически не имеет запаха и не пенится.
Возможные причины появления запаха или пенистости
Если у мочи появился резкий или специфический запах, это может говорить об обезвоживании, заболеваниях органов мочевыделительной системы (пиелонефрит, цистит), мочеполовых инфекциях или серьёзных метаболических нарушениях.
Пенистость, как правило, вызывает белок. Он может попадать в мочу при патологиях почек.
Если моча пенится, следует обратиться к врачу и сдать анализы
Кислотность (рН)
Реакция мочи — более кислая или щелочная — отражает кислотно-щелочной баланс во всём организме. По этому показателю можно выявить ряд нарушений и определить способность организма противостоять инфекциям.
Возможные причины изменения кислотности
Изменение pH может говорить о заболеваниях почек и мочевого пузыря, например нарушении работы щитовидной железы, сахарном диабете, подагре. Кислотность может меняться при острых патологических процессах: повышении температуры, рвоте.
Также на реакцию влияют особенности диеты: если человек ест много мяса и белковой пищи, среда становится кислой, если в рационе преобладают овощи и крупы — щелочной. При голодании кислотность повышается.
PH мочи можно определить самостоятельно при помощи тест-полосок
Что следует делать при изменениях мочи
Отклонения от нормы не всегда говорят о патологических нарушениях. В первую очередь при сборе велика вероятность погрешности — например, слизь может появиться, если плохо подмыться или собрать не среднюю, а первую порцию мочи. Среди других факторов, которые могут повлиять на результат: неверное хранение материала (в тёплом месте, более 12 часов), использование нестерильного контейнера, обследование во время менструации.
Если анализ не в норме, врач, скорее всего, попросит сдать мочу повторно.
К каким врачам обращаться, если выявлены нарушения
При любых отклонениях в свойствах или анализе мочи нужно обратиться к терапевту. Он проведёт первичную диагностику и при необходимости направит к профильным специалистам: нефрологу, эндокринологу, гинекологу, гастроэнтерологу.
Лечение
Изменение мочи может быть физиологичным или указывать на заболевания, которые нужно лечить. Решение о необходимости терапии принимает врач. Как правило, одного анализа мочи для постановки диагноза недостаточно. Скорее всего, потребуется ряд дополнительных исследований, чтобы уточнить диагноз: анализ крови, УЗИ почек, печени, органов малого таза.
Источники
- Мочекаменная болезнь : клинические рекомендации / Минздрав РФ. 2021.
- Инфекция мочевыводящих путей у детей : клинические рекомендации / Минздрав РФ. 2021.
Содержание
- Что такое pH урины?
- Факторы, влияющие на кислотность
- Когда необходим анализ уровня pH мочи у женщин и мужчин?
- Подготовка и проведение исследования
- Как измерить кислотность в домашних условиях?
- Результаты анализа
- Причины повышения кислотности и симптомы
- Проявления и причины снижения pH
- Лечение отклонений
- Диета при патологии
- Основной вывод
Важный показатель здоровья человека — pH мочи. Урина образуется в канальцах почки, как результат фильтрации плазмы крови. Составляющими веществами является вода, которая на 97% наполняет урину и 3% состава — вещества, формирующиеся в результате распада белковых микроэлементов. Представлен в виде солей и элементов азотистого происхождения.
Что такое pH урины?
Кислотность мочи — лабораторный показатель, характеризующий реакцию жидкости. Ее измеритель — десятитысячный показатель логарифма концентрации pH — power hydrogen (дословный перевод — сила гидрогена). Щелочная реакция и уровень кислоты урины варьируется в зависимости от активности обменных процессов организма. Показатели рН мочи связаны с количеством свободных ионов водорода, которые выделяются при распаде кислот и кислых солей. Осадок урины появляется после процессов фильтрации и реабсорбции, происходящих в парном органе.
Уровень pH не может быть ниже 0,86.
Факторы, влияющие на кислотность
Реакция мочи варьируется вследствие воздействия нескольких внутренних и внешних факторов. Источниками, воздействующими на pH мочи, являются:
- продукты питания;
- возрастные особенности;
- наличие/отсутствие воспалительных процессов;
- тяжелая физическая работа;
- сниженные защитные свойства организма;
- плохие экологические условия;
- частые стрессы;
- нарушения работы ЖКТ;
- прием медикаментов.
Повышенная кислотность наблюдается в случае сбоя в работе организма. Нормальный уровень гидрогена в урине — показатель хорошего здоровья и залог успешной самообработки мочевого пузыря. Также, если показатель в норме, то это способствует угнетению функционирования болезнетворных бактерий и микроорганизмов, и тем самым предотвращается развитие недугов.
Когда необходим анализ уровня pH мочи у женщин и мужчин?
Анализ для исследования pH мочи назначают в качестве комплексного, обязательного исследования состояния здоровья человека. У женщин и у мужчин, работающих на предприятиях, оно входит в программу обязательных. Иногда исследуют рН крови и слюны, но понятный результат открывается, если исследовать урину. Анализ мочи назначают при подозрении на наличие воспалительных процессов и сбои метаболизма. Показатель того, насколько концентрированная моча у взрослого или у ребенка может помочь предотвратить развитие недуга до внешнего проявления.
Подготовка и проведение исследования
Кислотность мочи определяют в лабораторных условиях. Пациент требуется правильно подготовиться, для того чтобы общий анализ показал достоверные результаты. За день до забора материала нельзя есть морковку и свеклу, потому как эти овощи обладают возможностью менять физические свойства урины. Также запрещено употреблять мочегонные и слабительные лекарства.
Чтобы результат был достоверным, у детей необходимо помыть половые органы, а у взрослых — проследить, чтобы в материал для исследования не попали волосы. После того как моча для анализа попадает в лабораторию, специалист применяет специальные индикаторы, которые способные менять цвет, в зависимости от реакции. Чаще всего используют лакмусовую бумагу. Также для исследования урины применяют прибор — ионометр. Эта методика отличается особенной точностью, максимальный сдвиг — на 0,01 единицу.
Из-за возможности вещества менять свои особенности, некоторым больным рекомендуют проводить исследование ежедневно на протяжении 7 дней, в разное время.
Как измерить кислотность в домашних условиях?
Высокая кислотность мочи может быть выявлена дома. Для этого необходим ионометр или лакмусовая бумага. В домашних условиях лучше применять аппаратную методику, потому как лакмус может не показать достоверный результат. Важно также понимать, что вне лабораторных условий определить серьезные отклонения невозможно, и анализ покажет только поверхностные нарушения.
Результаты анализа
Данные измерения показывают, есть ли в организме человека недуг, и насколько ярко он выражен. Нормальная реакция у каждого человека может отличаться, так как на этот показатель влияет возраст, способ жизни, присущие организму особенности. Конечно, по мере взросления и развития, граничный показатель смещается, из-за гормональных изменений. Так, нейтральный уровень может измениться в период полового созревания, беременности или при приеме гормональных препаратов.
Норма у ребенка
Реакция мочи у маленьких пациентов связана с возрастом. У здорового новорожденного уровень pH низкий — 5,5—6. У недоношенного малыша определение кислотности варьируется в границах 4,8—5,4. Через несколько дней показатель меняется. У ребенка более щелочная моча, индикатор колеблется в пределах 6,8—7,9. При грудном вскармливании уровень кислотности у малыша выше, тогда как искусственные методы питания могут снизить показатель реакции до 5,4—6,9. Окончательная нейтральная норма для ребенка устанавливается после перехода на обычное питание.
Оптимальные показатели у взрослых
Кислотность урины у женщины и мужчины одинаковая. Показатели могут меняться в течение дня, потому как в утреннее время происходит активное выделение токсических веществ и моча слабокислая. Нейтральное значение реакции у взрослого составляет 6,5—7 единиц. В вечернее время активизируется щелочная среда, и показатель может снизиться. Если показатель щелочи держится на уровне 6,5, необходимо добавить в своей рацион другую пищу, для повышения содержания кислоты.
Норма при беременности
Во время вынашивания ребенка реакция не должна выходить за рамки 4,5—8 единиц. Если результат ниже нормы, то это свидетельство недостаточного количества витаминов или жидкости. Часто такое отклонение встречается в период токсикоза. Если pH урины превышает максимальный граничный показатель, это означает, что следует исключить развитие патологических изменений функционирования парного органа или дисфункцию паращитовидных желез. Беременная должна повторно пройти исследование или сдать дополнительные анализы.
Причины повышения кислотности и симптомы
Уровень кислоты может быть повышен под воздействием многих внутренних и внешних факторов. Воздействие на организм любого раздражителя может привести к тому, что щелочь будет существенно снижена. Если вовремя не ликвидировать это отклонение, есть риск развития ацидоза — закисления организма. Это тяжелое состояние, требующее серьезного лечения. Провоцирующие факторы и проявления, рассмотрены в таблице:
| Причины | Симптомы |
| Постоянное питание жирными продуктами | Появление лишнего веса |
| Воспалительные процессы мочеполовой системы | Болезненные ощущения внизу живота |
| Нарушение работы ЖКТ | Запоры |
| Алкоголизм | Ослабленность |
| Сильная физическая нагрузка | Нарушение иммунных свойств |
Проявления и причины снижения pH
Кислая моча может резко стать щелочной, под воздействием некоторых факторов. К ним относятся:
- недостаток витаминов, попадающих в организм через пищу;
- лечение мочегонными;
- неполное выведение натрия;
- рахит;
- употребление сырых продуктов;
- почечная недостаточность;
- чрезмерное употребление соды или продуктов, содержащих ее содержащих;
- избыток калия.
Симптомы того, что кислая среда становится щелочной проявляются в зависимости от причин. Человек, страдающий от такого отклонения, часто чувствует усталость, быстро устает. Иногда наблюдается тошнота и рвота, нарушение стула и болезненные ощущения внизу живота. При такой реакции необходимо пересмотреть рацион и сдать материал для дополнительного исследования.
Лечение отклонений
Если измерительный прибор или другая методика показали повышение или снижение уровня pH, это значит что нужно начинать терапию патологии. Делать это можно в домашних условиях: необходимо сменить продукты питания, отказаться от вредных привычек и наладить режим дня. Если отклонение серьезное, проводится очищение крови в условиях медицинского учреждения. Пациенту могут назначить внутривенные инъекции бикарбоната калия, или содержащих его медикаментов.
Диета при патологии
Понизить уровень кислоты можно при помощи правильного рациона. Существуют продукты, которые могу поднять уровень щелочи и тем самым наладить кислотное содержание урины. Диета основывается на приеме 50% сырой пищи: свежих овощей и фруктов. Необходимо отказаться от крепкого кофе и алкогольных напитков. При такой патологии диета должна включать:
- бобовые;
- растительные масла;
- все виды зелени;
- орехи;
- гречневую крупу;
- просо.
Основной вывод
Уровень pH урины — важный показатель состояния здоровья человека. Важно регулярно измерять этот показатель, чтобы предотвратить развитие тяжелых патологий и серьезных заболеваний. Поддерживать этот индикатор на нормальном уровне можно без медикаментозного вмешательства за счет правильно составленного рациона и соблюдения здорового образа жизни.
Введение
Мочекаменная болезнь (МКБ) является широко распространённой урологической патологией, занимающей второе место в структуре всех урологических заболеваний после неспецифических воспалительных заболеваний почек и мочевыводящих путей. Её встречаемость составляет не менее 3,0% среди трудоспособного населения в возрасте от 20 до 40 лет, а к 70-летнему возрасту она обнаруживается у каждого восьмого [1]. Распространённость МКБ в разных странах колеблется от 3,5 до 9,6%, при этом в экономически развитых странах отмечается её неуклонный рост. В странах Западной Европы её распространённость достигает 5,0–14,0%, в Великобритании и США — 7,0–15,0% [2]. В России наблюдаются те же тенденции. В период с 2005 по 2019 год заболеваемость МКБ увеличилась на 16,2%, а встречаемость достигла 35,4%. Анализ полученных эпидемиологических данных показал прямую корреляцию между увеличением случаев МКБ и ростом количества случаев диабета, ожирения, а также увеличением потребления мясных продуктов. Подтверждением влияния этих факторов на прирост заболеваемости является отсутствие увеличения заболеваемости среди детей на протяжении всего анализируемого периода [3].
Отличительной чертой МКБ является высокая частота её рецидивирования. Согласно номограмме риска рецидивного камнеобразования ROKS (Recurrence оf Kidney Stone), в основе которой лежит анализ историй болезни более 4-х тысяч пациентов, частота рецидивирования МКБ достигает 11%, 20%, 31% и 39% в течение 2-х, 5-ти, 10-ти и 15-ти лет, соответственно [4]. По другим данным, при отсутствии адекватной профилактики риск возникновения рецидива и повторного оперативного лечения достигает 25–50% в течение ближайших 5-ти лет и 60–75% в течение 10-ти лет после удаления камня [5]. Это определяет высокую актуальность проведения адекватной метафилактики, профилактики рецидива камнеобразования после удаления конкремента хирургическим путём или его самостоятельного отхождения, эффективность которой может достигать 80% [6] и основывается она прежде всего на понимании механизмов камнеобразования, диагностики и оперативном устранении литогенных нарушений.
Согласно современным представлениям, уролитиаз является полиэтилогичным заболеванием, а формирование конкремента является результатом нарушения баланса многих литогенных факторов и ингибиторов камнеобразования. К основным литогенным субстанциям относятся ионы кальция, мочевая кислота, оксалаты, фосфаты, цистин и др. Основными ингибиторами камнеобразования считаются цитрат, ионы магния, неорганический пирофосфат, нефрокальцин, белок Tamm – Horsfall и др.
В значительной степени литогенный потенциал мочи определяется её кислотно-основным состоянием, где концентрацию свободных ионов водорода в среде отражает водородный показатель (pH), который равен отрицательному десятичному логарифму этой концентрации: pH =-lg[H+]. Он в значительной степени влияет на степень диссоциации основных веществ, участвующих в литогенезе. В норме pH мочи находится в диапазоне от 4,5 до 8,0, преимущественно около 6,0.
В настоящий момент pH мочи признан независимым фактором, влияющим на образование всех видов мочевых конкрементов (рис. 1) [7][8]. Однако зачастую при проведении метафилактики мочекаменной болезни данному показателю не уделяется должного внимания.
Цель исследования: обобщить имеющиеся данные о формировании рН мочи, его влиянии на камнеобразование, а также клинических аспектах его модификации при проведении метафилактики различных форм мочекаменной болезни.
Рисунок 1. Зависимость растворимости в моче литогенных веществ от pH (с изменениями по N. Laube [9])
Figure 1. pH dependence of lithogenic substances solubility in urine (changes according to N. Laube [9]): 1 — calcium oxalate; 2 — phosphates; 3 — ammonium urate; 4 — uric acid; 5 — cystine
Алгоритм литературного поиска
Выполнен поиск и анализ зарубежной и отечественной литературы с использованием баз данных SCOPUS/ScienceDirect, PubMed/MEDLINE, eLIBRARY, Google Scholar с 1990 по 2021 год, по ключевым словам: «kidney stones», «urolithiasis», «pH urine». Для выявления дополнительных потенциально релевантных исследований проведён анализ ссылок во включённых источниках.
Результаты
Роль почек в поддержании кислотно-основного равновесия организма. Кислотно-основное состояние (КОС) является одним из важнейших компонентов гомеостаза. Например, диапазон допустимых показателей рН крови крайне узок: совместимые с жизнью значения рН крови находятся в пределах от 6,80 до 7,80. Норме соответствует ещё более узкий диапазон рН: 7,35–7,45 — для артериальной крови и 7,32–7,42 — для венозной. В процессе клеточного метаболизма в организме в сутки образуется 15 моль углекислого газа и минеральных кислот (сульфаты, фосфаты и др.) в количестве приблизительно 1 мЭкв/кг массы тела (60–70 мЭкв). Поскольку концентрация свободных ионов водорода в плазме крови составляет около 40*10-6 мЭкв/л, очевидно, что ежедневное накопление даже такого небольшого количества, как 60–70 мЭкв ионов водорода, было бы для организма смертельным. Физиологический оптимум концентрации протонов (Н+) в организме поддерживается за счёт сбалансированной активности функционально единой системы, включающей в себя буферные, биохимические и физиологические процессы.
Основная роль почек в поддержании кислотно-основного равновесия крови состоит в выведении ионов водорода и в восстановлении бикарбонатного буфера крови. Регуляция почками КОС базируется на процессах фильтрации, секреции, реабсорбции различных веществ и процессе глюконеогенеза [10].
Физиологические процессы, определяющие pH мочи. В отличие от pH крови, pH мочи не является физиологической константой, и его значения могут варьироваться в широких пределах (от 4,5 до 8,0). Колебания pH мочи в норме могут быть обусловлены циркадианным ритмом, физической нагрузкой, приёмом лекарственных препаратов, приёмами пищи и другим [11].
Одним из ключевых соединений, участвующих в регуляции КОС и оказывающих влияние на pH мочи, является бикарбонат (HCO3—). В нормальных условиях при отсутствии алкалоза бикарбонат практически полностью реабсорбируется из мочи, и выведение его минимальных количеств влияния на pH мочи не оказывает. Он начинает определяться в моче в случае, если его концентрация в плазме крови превышает 28 ммоль/л. Являясь низкомолекулярным соединением, бикарбонат легко фильтруется в почечных клубочках. За сутки гломерулярной фильтрации подвергается 4,0–4,5 моль бикарбоната, однако 95% его количества реабсорбируется в канальцах, и только 5% экскретируется с мочой. Реабсорбция бикарбоната происходит в проксимальных канальцах (до 80% его содержания), в толстом восходящем отделе петли Генле и дистальном извитом канальце (16%) и в собирательных трубках (4%).
Реабсорбция бикарбоната в проксимальных канальцах показана на рисунке 2. Бикарбонат, поступивший в просвет канальца в результате клубочковой фильтрации, взаимодействует с протонами, секретирующимися сюда канальцевыми клетками с помощью Na+/H+-обменника (NHE3). В результате образуется угольная кислота, которая под влиянием люминальной карбоангидразы IV типа распадается на воду и углекислый газ, диффузией поступающий внутрь клеток. В цитоплазме клеток углекислый газ взаимодействует с водой при участии карбоангидразы II типа, и формирующаяся угольная кислота диссоциирует на бикарбонат и протон (НСО3— и Н+). С помощью Na+/H+-обменника протоны вновь секретируются в просвет канальца, где описанный ранее цикл повторяется, а бикарбонат через Na+-зависимые бикарбонатные котранспортеры (семейство NBC) на базолатеральной мембране поступает в интерстиций и по околоканальцевым капиллярам возвращается в системный кровоток.
В обычных условиях в дистальных канальцах большая часть бикарбоната уже реабсорбирована. Механизм реабсорбции бикарбоната в дистальных отделах нефрона и собирательных трубочках в целом схож с таковым в проксимальных канальцах, но есть и ряд отличий. Во-первых, выход бикарбоната через базолатеральную мембрану клеток осуществляется через Cl—/HCO3—-обменник (семейство анионных обменников AE). Во-вторых, отличается механизм секреции протонов: они преимущественно переносятся с помощью первично активного транспорта вакуолярной H+-ATФазой (V-АТФаза) и в меньшей степени с помощью К+/H+-обменника.
Рисунок 2. Реабсорбция профильтровавшегося бикарбоната клетками проксимального канальца (А), аммониогенез и продукции нового бикарбоната (B). Пояснение: Верхняя клетка (А) — процесс реабсорбции профильтровавшегося бикарбоната. Нижняя клетка (Б) — процессы аммониогенеза и продукции нового бикарбоната. NHE3 — Na+/H+-обменник, NBCe1 — Na+/бикарбонатный котранспортер, KA II и KA IV — карбоангидраза II типа (цитоплазматическая) и IV типа (люминальная), ЦТК — цикл трикарбоновый кислот, ПГ — почечная глутаминаза, волнистая стрелка — простая диффузия
Figure 2. Reabsorption of filtered bicarbonate by proximal tubule cells (A), ammoniogenesis and production of new bicarbonate (B). The upper cell (A) — the process of reabsorption of filtered bicarbonate. The lower cell (B) — the processes of ammoniogenesis and the production of new bicarbonate. NHE3 — Na+/H+-exchanger, NBCe1 — Na/bicarbonate cotransporter, СA II and СA IV — carbonic anhydrase of type II (cytoplasmic) and type IV (luminal), TCA — tricarboxylic acid cycle), RG — renal glutaminase, wavy arrow — simple diffusion
Важную роль в образовании максимально кислой мочи играет секреция протонов вставочными клетками А-типа (рис. 3). В проксимальных канальцах концентрация протонов может повышаться только в 3–4 раза (рН снижается до 6,7), а в собирательных трубочках содержание протонов способно возрастать в 900 раз (при этом рН мочи достигает минимально возможного уровня — 4,5). Несмотря на это, в количественном отношении лишь небольшая часть ионов водорода выделяется с конечной мочой в свободном виде. Выделение основного количества ионов водорода происходит за счёт связывания протонов с буферными системами в просвете канальцев. Наиболее важными буферными соединениями являются фосфаты и ионы аммония, меньше вклад цитратной и уратной буферных систем.
Рисунок 3. Секреция протонов и продукция нового бикарбоната А-клетками собирательных трубок, транспорт фосфатов и фосфатный буфер мочи. Пояснение: V-АТФаза — вакуолярная Н+-АТФаза, АЕ1 — бикарбонат-хлоридный обменник
Figure 3. Proton secretion and production of new bicarbonate by A-cells of collecting tubes, transport of phosphates and urine phosphate buffer. V-ATPase — vacuolar H+-ATPase, AE1 — chloride-bicarbonate exchanger
С клинической точки зрения, важно понимать, какие факторы определяют количество секретируемых канальцами протонов. Определяющую роль играет рН внеклеточных жидкостей, но секреция Н+ также существенно меняется при снижении объёма циркулирующей крови и колебаниях концентрации калия в крови.
Основной в количественном отношении буферной системой в почечных канальцах является следующая система — аммиак (NH3) – аммоний (NH4+). Источником ионов аммония служит глутамин, образующийся при метаболизме аминокислот в печени и доставляющийся с током крови к почкам. Аммониогенез происходит главным образом в эпителии проксимальных канальцев (рис. 2), а также толстого восходящего отдела петли Генле и дистальных извитых канальцев нефрона.
В результате гидролиза глутамина под действием ферментов почечной глутаминазы и глутаматдегидрогеназы образуется две молекулы аммиака (NH3) и альфа-кетоглутарат. Аммиак свободно проходит через билипидный слой мембраны клеток в просвет канальцев, где соединяется с водородом с образованием ионов аммония (NH4+). Часть аммиака превращается в NH4+ внутриклеточно и выводится в просвет канальца через Na+/H+-обменник. В просвете канальца ионы аммония могут соединяться с анионами (сульфатами, хлоридами, фосфатами) с образованием аммонийных солей, выделяющихся с мочой. По мере дальнейшего метаболизма альфа-кетоглутарата в канальцевых клетках в ходе цикла Кребса или глюконеогенеза образуется две молекулы бикарбоната, которые поступают во внеклеточную жидкость, возмещая бикарбонат, который потребовался для изначальной нейтрализации неорганических кислот. Ионы бикарбоната, образованные в ходе данного процесса, представляют собой вновь синтезированные соединения. Таким образом, почки ежедневно образуют примерно 50–100 ммоль «нового» бикарбоната и способны пополнять запасы бикарбонатов во внеклеточной жидкости.
Второй буферной системой является фосфатная буферная система (рис. 3). Значительная часть секретирующихся протонов в просвете канальцев соединяется с гидрофосфат-ионом (HPO32-) с образованием дигидрофосфат-иона (H2PO3—). При снижении рН канальцевой жидкости до 5,8 практически весь HPO32- переходит в H2PO3—. Главным образом, этот процесс происходит в дистальных отделах нефрона и собирательных трубочках [9]. Количество протонов, выводимых в связанном виде, составляет 10–40 мЭкв в сутки.
Снижение pH мочи и влияние на литогенез. Негативное влияние длительного снижения pH мочи < 5,8 (обозначаемого в англоязычной литературе термином «acid arrest») на течение мочекаменной болезни обусловлено повышенной склонностью к кристаллизации мочевой кислоты, повышением интенсивности формирования кристаллов оксалата кальция и снижением экскреции цитрата, ингибирующего камнеобразование [12]. Применительно к патогенезу мочекаменной болезни представляет интерес хронический ацидоз. Ацидотическое состояние признается хроническим при длительности его существования более 5–7 дней [13].
Наиболее распространённой причиной длительной стойкой ацидификации мочи является метаболический синдром, составляющими которого являются инсулинорезистентность, абдоминальное ожирение, гипергликемия, дислипидемия и артериальная гипертензия [14]. Снижение pH при инсулинорезистентности объясняется такими процессами, как снижением экскреции ионов аммония и увеличением экскреции протонов и органических кислот [15].
В клетках проксимального почечного канальца в условиях резистентности к инсулину повышается активность Na+/H+ переносчика, что приводит к снижению рН в его просвете. Повышается активность cубстрата инсулинового рецептора 2 типа IRS-2, что усиливает реабсорбцию бикарбоната из просвета канальца, ещё больше снижая рН мочи (рис. 4).
В клетках дистального почечного канальца в условиях инсулинорезистентности также наблюдается перегрузка свободными жирными кислотами, увеличивающая внутриклеточное содержание H+. Это повышает активность карбоангидразы и увеличивает секрецию Н+ в просвет, тем самым результируя в низкий рН мочи (рис. 5).
Рисунок 4. Клетка проксимального почечного канальца в условиях резистентности к инсулину. Пояснение: NHE3 — Na+/H+-обменник, NBCe1 — Na/бикарбонатный котранспортер, KA II и KA IV — карбоангидраза II типа (цитоплазматическая) и IV типа (люминальная), ЦТК — цикл трикарбоновый кислот, ПГ — почечная глутаминаза, волнистая стрелка — простая диффузия, СЖК — свободные жирные кислоты, URAT1 и GLUT9 — переносчики уратов
Figure 4. Proximal renal tubule cell in conditions of insulin resistance. NHE3 — Na/H-exchanger, NBCe1 — Na/bicarbonate cotransporter, CA II and CA IV — carbonic anhydrase of type II (cytoplasmic) and type IV (luminal), TCA cycle — tricarboxylic acid cycle, RG — renal glutaminase, wavy arrow — simple diffusion, FFA — free fatty acids, URAT1 and GLUT9 — urate transporters
Рисунок 5. Клетка дистального почечного канальца в условиях резистентности к инсулину. Пояснение: V-АТФаза — вакуолярная Н+-АТФаза, АЕ1 — бикарбонат-хлоридный обменник, НКА — Н+/К+-АТФаза
Figure 5. Distal renal tubule cell in conditions of insulin resistance. V-ATPase — vacuolar H+-ATPase, AE1 — chloride-bicarbonate exchanger
Кроме этого, при наличии инсулинорезистентности повышается экскреция мочевой кислоты (вероятно, при глюкозурии ингибируется реабсорбция мочевой кислоты при участии транспортера GLUT9). Таким образом, резистентность к инсулину повышает риск возникновения как мочекислых, так и кальций-оксалатных конкрементов [16]. Метаболический синдром в целом и его отдельные компоненты признаны независимыми факторами камнеобразования [17].
Снижение pH мочи также наблюдается при метаболическом ацидозе — расстройстве кислотно-основного состояния, при котором наблюдаются снижение pH крови, снижение бикарбонатов в крови при нормальном или повышенном содержании кислот. С целью компенсации в условиях ацидоза в почках повышается активность ренальной глутаминазы, что усиливает гидролиз глутамина в эпителии почечных канальцев с образованием аммиака. Образующийся аммиак связывает протоны с образованием аммонийных солей, которые экскретируются с мочой.
Метаболический ацидоз также наблюдается у пациентов с инсулинозависимым сахарным диабетом, с первичной надпочечниковой недостаточностью, гипоренинемическим гипоальдостеронизмом [18].
Причиной стойкой ацидификации мочи может быть потеря бикарбоната с каловыми массами вследствие хронической диареи, которой страдают пациенты с неспецифическим язвенным колитом, болезнью Crohn, илеостомой, перенесшие резекцию тонкой кишки либо при длительном приёме слабительных [19]. Встречаемость мочекислых камней у таких пациентов достигает 30%, что на 8–10% превышает распространённость мочекислого нефролитиаза в европейской популяции [20]. Также у данной группы пациентов высока вероятность развития гиперкальциурии, гипероксалурии, гипоцитратурии и снижение суточного диуреза, что значительно повышает литогенный потенциал мочи [18]. Причиной снижения pH мочи также может быть пищевое поведение, при котором в рационе присутствует большое количества белка и жиров животного происхождения при минимальном потреблении продуктов растительного происхождения [21].
Отдельно стоит отметить, что хронический ацидоз у пациентов с хронической болезнью почек, возникающий вследствие снижения активности канальцевого аммониогенеза, снижения канальцевой секреции протонов и нарушения клубочковой элиминации остатков органических кислот не сопровождается снижением pH мочи.
Повышение pH мочи и влияние на литогенез. Выраженное повышение pH мочи наблюдается у пациентов с уреазопродуцирующей инфекцией мочевых путей, при почечном канальцевом ацидозе, метаболическом алкалозе, и в меньшей степени — у приверженцев вегетарианской и веганской диет [22]. Персистирующая уреазопродуцирующая инфекция мочевых путей является наиболее частой причиной стойкого повышения pH мочи. Бактериальная уреаза гидролизует мочевину до углекислого газа и аммиака, который подвергается дальнейшему метаболизму с образованием катиона аммония и гидроксида, что приводит к существенному сдвигу pH мочи в щелочную сторону. Ионы аммония соединяются с магнием, фосфатом и водой с образованием магний-аммоний-фосфатных конкрементов (струвита), карбонат анионы соединяются с кальцием и фосфатами с образованием апатитовых конкрементов (гидроксиапатит и карбонатапатит) (рис. 6). Кристаллизация карбонатапатита происходит при рН мочи выше 6,8, струвита — при рН выше 7,2 [23]. Следует также отметить наличие прямого токсичного действия образующейся высокой концентрации аммиака на уроэпителиальные клетки, приводящего к разрушению гликозаминогликанового слоя клеток и облегчению адгезии к ним бактерий [24].
Рисунок 6. Формирование конкрементов из струвитов, карбонатапатита и урата аммония при уреазопродуцирующей инфекции
Figure 6. Formation of struvites, carbonatapatite and ammonium urate stones in urease-producing infection
К облигатным уреазопродуцирующим бактериям относятся Proteus spp., Providencia rettgeri, Morganella morganii, Corynebacterium urealyticum, Ureaplasma urealyticum.
Proteus spp. вырабатывает уреазу с чрезвычайно высокой активностью и является причиной камнеобразования у более половины пациентов с инфекционным уролитиазом [25]. К факультативным уреазопродуцирующим бактериям относятся Enterobacter gergoviae, Klebsiella spp., Providencia stuartii, Serratia marcescens, Staphylococcus spp., Escherichia coli. Считается, что только 1,4% штаммов E. coli обладает уреазопродуцирующей способностью [26].
Риск образования кальций-фосфатных и кальций-оксалатных конкрементов существенно выше у пациентов с почечным канальцевым ацидозом (ПКА), отличительной чертой которого является стойкое повышение pH мочи. Это заболевание характеризуется нарушением ацидификации мочи при отсутствии выраженного снижения функции клубочкового аппарата, что приводит к метаболическому ацидозу и стойкой щелочной реакции мочи. ПКА может быть наследственным или приобретённым вследствие рецидивирующего пиелонефрита, обструктивной уропатии, острого канальцевого некроза, саркоидоза, идиопатической гиперкальциурии, первичного гиперпаратиреоза и других заболеваний.
Наибольшее клиническое значение имеет ПКА 1 типа (дистальный), при котором нарушена секреция протонов в дистальных почечных канальцах. Клиническим признаком ПКА являются стойкие показатели pH мочи выше 5,8 при условии, что исключена инфекция мочевыводящих путей.
Для верификации диагноза дистального ПКА в основном проводится нагрузочный кислотный тест с пероральным приёмом аммония хлорида (рис. 7). Суть теста заключается в изучении резерва кислотовыделительной способности почек в условиях ацидоза, обусловленного приёмом аммония хлорида. Тест считается положительным, если однократный приём аммония хлорида в дозе 0,1 г/кг массы тела или трёхдневный приём в дозе 0,05 г/кг не снизил pH мочи ниже 5,4. Однако проведение данного теста ограничено тем, что в Российской Федерации аммония хлорид не зарегистрирован в качестве лекарственного препарата.
Рисунок 7. Алгоритм диагностики почечного канальцевого ацидоза 1 типа
Figure 7. Diagnostic algorithm of renal tubular acidosis type 1
Альтернативой может быть более доступный в клинической практике фуросемид-флудрокортизоновый тест (FF test). Вечером накануне тестирования пациенту назначается 1 мг флудрокортизона внутрь (желательно на фоне ограничения приема соли менее 1 г/сут в течение 3 дней), а следующим утром парентерально вводится фуросемид в дозе 1 мг/кг с целью создания относительного дефицита натрия. Фуросемид блокирует Na+/K+/2Cl—-котранспортер в толстом восходящем отделе петли Henle, что увеличивает доставку натрия в собирательные трубочки. Усиленная реабсорбция натрия главными клетками собирательных трубок приводит к возникновению негативного трансэпителиального потенциала, что у здоровых людей должно увеличивать экскрецию ионов калия и водорода с мочой, тем самым снижая рН мочи [27].
Другим механизмом повышения рН мочи могут быть компенсаторные процессы при метаболическом алкалозе, который характеризуется повышением уровня pH крови и увеличением концентрации бикарбоната крови. Причиной алкалоза может быть использование щелочных растворов (например, гидрокарбоната натрия), органических соединений (лактата, цитрата и ацетата) [28].
При длительном респираторном ацидозе компенсаторно увеличивается образование бикарбоната почками. При проведении искусственной вентиляции лёгких в режиме гипервентиляции резко снижается парциальное давление углекислого газа в крови, развивается преходящая гипербикарбонатемия и повышается pH крови (состояние, обозначаемое как постгиперкапнический метаболический алкалоз).
Повышение pH мочи также наблюдается при сильной рвоте вследствие потери протонов и снижения секреции бикарбоната в желудочно-кишечном тракте, однако данные состояния являются преходящими и не влияют на камнеобразование.
Влияние pH мочи на экскрецию цитрата. Уровень pH мочи оказывает прямое влияние на экскрецию цитрата — одного из важнейших ингибиторов камнеобразования. Гипоцитратурия или выделение менее 2,5 ммоль цитрата в сутки являются распространённым литогенным нарушением у пациентов с мочекаменной болезнью [29]. Цитрат образует соединение с кальцием, уменьшая его свободное количество в моче, а также уменьшает преципитацию кристаллов оксалата и фосфата кальция и их агломерацию [30]. Стоит отметить, что практически весь поступающий с пищей цитрат всасывается в желудочно-кишечном тракте, при этом его абсорбция не различается у лиц с камнеобразованием и у здоровых людей [31].
В плазме крови концентрация общего цитрата (преимущественно в виде кальциевых, натриевых и магниевых солей лимонной кислоты) составляет от 0,05 до 0,3 ммоль/л. Большая часть поступившего из желудочно-кишечного тракта цитрата метаболизируется в печени до углекислого газа и воды (в итоге до бикарбоната). Синтез эндогенного цитрата происходит в митохондриях при участии фермента цитрат-синтазы из оксалоацетата и ацетил-кофермента А. Синтез цитрата является одним из этапов цикла трикарбоновых кислот (цикл Krebs) — центральной части пути катаболизма большей части органических молекул. Эндогенный цитрат и небольшая часть абсорбированного в желудочно-кишечном тракте цитрата, не подвергшаяся катаболизму в печени, поступают в кровоток и затем подвергаются клубочковой фильтрации. Цитрат свободно фильтруется в клубочках, после чего большая часть профильтровавшегося цитрата (от 65 до 90%) реабсорбируется с последующим метаболизмом до углекислого газа и воды [32]. С мочой выделяется лишь около 5–10% профильтровавшегося цитрата. Таким образом, концентрация цитрата в моче определяется интенсивностью процессов его реабсорбции, а не фильтрации. Наиболее важным фактором, влияющим на активность процессов реабсорбции цитрата, является pH мочи [33]. Реабсорбция цитрата происходит в проксимальных канальцах нефрона и осуществляется Na-зависимым переносчиком дикарбоксилата (NaDC-1) (рис. 8). Он транспортирует молекулу двухвалентного цитрата, в то время как в просвете проксимальных канальцев цитрат находится преимущественно в трёхвалентной форме.
Рисунок 8. Реабсорбция цитрата в проксимальных канальцах. Пояснение: NaDC-1 — натрий-дикарбоксилатный котранспортер
Figure 8. Citrate reabsorption in proximal tubules. NaDC-1 — a sodium dicarboxylate cotransporter
Повышение содержания протонов в канальцевой жидкости приводит к переходу цитрата в двухвалентную форму. Даже небольшое снижение pH (с 7,4 до 7,2) в почечных канальцах значительно увеличивает реабсорбцию цитрата с помощью NaDC-1 [34]. Внутриклеточное снижение рН повышает количество NaDC-1 в апикальной мембране, подавляет синтез и стимулирует катаболизм цитрата в эпителии проксимальных почечных канальцев. Фермент АТФ-цитратлиаза активирует окисление цитрата до оксалоацетата и ацетил-кофермента А в цитоплазме, а аконитаза катализирует изомеризацию цитрата до изоцитрата в митохондриях. Низкий уровень внутриклеточного цитрата способствует его реабсорбции в клетку из просвета проксимальных канальцев.
Таким образом, при заболеваниях, ассоциированных со снижением рН мочи или снижением pH внутри клеток, снижается и экскреция цитрата с развитием гипоцитратурии. К таким заболеваниям относят метаболический ацидоз, тубулярный ацидоз, метаболический синдром, хроническую диарею (вследствие потери бикарбонатов) [35].
К гипоцитратурии могут приводить гипокалиемия и внутриклеточный ацидоз на фоне применения тиазидных диуретиков (потому рекомендован приём цитратных смесей на фоне терапии тиазидами), а также скудное поступление цитрата с пищей при полном отказе от употребления фруктов или при потреблении большого количества животного белка.
Влияние pH мочи на активность антибактериальных препаратов. Значение pH среды влияет на активность большинства антибактериальных препаратов. Фторхинолоны, аминогликозиды, макролиды, ко-тримоксазол и фосфомицин максимально активны при щелочном рН, тогда как тетрациклины, нитрофурантоин и многие бета-лактамные антибиотики проявляют максимальную активность в более кислых условиях. Активность сульфаметоксазола, оксациллина, амоксициллина, ванкомицина, имипенема и клиндамицина не зависит от pH среды. Целесообразно учитывать данные особенности антибактериальных препаратов при выборе протокола терапии для повышения эффективности их использования [36].
Измерение pH мочи в клинической практике. Для понимания исходного статуса и целесообразности проведения модификации pH мочи в качестве инструмента метафилактики необходимо ориентироваться на данные исходной суточной pH-метрии. Европейская ассоциация урологов рекомендует измерять уровень pH в свежевыделенной моче 4 раза в день с помощью индикаторных тест-полосок или цифровых pH-метров. Максимальную точность измерения обеспечивают цифровые pH-метры, которые считаются «золотым стандартом» измерения pH мочи [37]. Они позволяют измерять pH с интервалом, равным 0,1, однако имеют ряд недостатков, таких как высокая стоимость и необходимость их периодической калибровки.
Более простым методом определения pH является использование индикаторных тест-полосок. В России доступные в розничной сети индикаторные полоски позволяют измерять pH в пределах от 5,0 до 9,0. Однако у некоторых производителей отсутствуют промежуточные значения в диапазоне между 5,0 и 6,0 и имеется большой шаг измерений в диапазоне от 6,0 до 9,0, равный 0,5, что снижает точность определения и ценность полученных результатов. Более точные результаты измерений могут обеспечивать индикаторные полоски, входящие в комплект упаковки лекарственных препаратов цитратных смесей. Они позволяют определять, в зависимости от производителя, pH в пределах от 5,4 до 7,4 с шагом 0,4 или от 5,6 до 8,0 с шагом 0,3.
Модификация pH мочи с помощью диеты. Пищевой рацион оказывает прямое влияние на pH мочи. Употребление богатой животным белком пищи приводит к ацидификации мочи, а переход на диету со сниженным потреблением животного белка или вегетарианскую сопровождается повышением pH мочи [38].
Степень влияния каждого продукта на pH мочи выражается индексом PRAL (potential renal acid load) — потенциальной кислотной нагрузки на почки. Концепция PRAL была представлена в 1995 году сотрудниками отдела питания и здоровья Научно-исследовательского института детского питания в Дортмунде Thomas Remer и Friedrich Manz [39]. Она была разработана для практического применения в профилактике рецидивов мочекаменной болезни с помощью диеты или в других областях диетологии. Продукты с положительным PRAL индексом закисляют мочу. PRAL индекс основных продуктов представлен в таблице 1. Для удобства подсчёта можно использовать онлайн-калькуляторы или мобильные приложения, например, «Daily PRAL Calculator» или «PRAL dos alimentos».
Наибольший индекс PRAL имеют продукты с высоким содержанием белка животного происхождения (мясо, рыба, морепродукты, твёрдые сыры). Продукты с отрицательным PRAL индексом (овощи и фрукты), наоборот, повышают pH мочи. Показано, что потребление продуктов с высоким PRAL индексом ассоциировано с увеличением риска образования мочекислого и кальций-оксалатного уротилиаза. Такая диета сопряжена с повышением экскреции кальция и гипоцитратурией, являющимися основными литогенными нарушениями при формировании кальций-оксалатных конкрементов [40]. Увеличение потребления фруктов и овощей при гипоцитратурии повышает pH мочи и увеличивает суточную экскрецию цитрата, калия и магния, снижая перенасыщение мочи солями мочевой кислоты и оксалата кальция [21]. При вегетарианской диете в сравнении со всеядной диетой ниже риск образования конкрементов из мочевой кислоты [41].
Таблица 1. PRAL индекс популярных продуктов, по T. Remer et al. [39]
Table 1. PRAL index of popular products, according to T. Remer et al. [39]
|
Вид продукта |
PRAL |
Вид продукта |
PRAL |
|
Напитки: |
Бобовые: |
||
|
Разливное пиво |
−0,2 |
Фасоль |
−3,1 |
|
Бутылочное пиво |
−0,1 |
Чечевица |
3,5 |
|
Coca-Cola |
0,4 |
Горох |
1,2 |
|
Кофе |
−1,4 |
Мясо и мясопродукты: |
|
|
Красное вино |
−2,4 |
Говядина |
7,8 |
|
Чай |
−0,3 |
Курица |
8,7 |
|
Белое вино |
−1,2 |
Сосиски |
6,7 |
|
Жиры и масла: |
Свинина |
7,9 |
|
|
Сливочное масло |
0,6 |
Индейка |
9,9 |
|
Маргарин |
−0,5 |
Молочные продукты и яйца: |
|
|
Оливковое масло |
0 |
Сыр Гауда |
18,6 |
|
Подсолнечное масло |
0 |
Творог |
8,7 |
|
Рыба: |
Сливки |
1,2 |
|
|
Треска |
7,1 |
Яйца куриные |
8,2 |
|
Пикша |
6,8 |
Творожный сыр |
4,3 |
|
Сельдь |
7 |
Твердый сыр |
19,2 |
|
Форель |
10,8 |
Мороженое |
0,6 |
|
Фрукты, орехи и соки: |
Молоко |
0,7 |
|
|
Яблочный сок несладкий |
−2,2 |
Пармезан |
34,2 |
|
Абрикосы |
−4,8 |
Плавленый сыр |
28,7 |
|
Бананы |
−5,5 |
Йогурт |
1,2 |
|
Черная смородина |
−6,5 |
Сахар и сладости: |
|
|
Вишня |
3,6 |
Мед |
−0,3 |
|
Виноградный сок |
−1,0 |
Сахар |
−0,1 |
|
Фундук |
−2,8 |
Овощи: |
|
|
Киви |
−4,1 |
Спаржа |
−0,4 |
|
Лимонный сок |
−2,5 |
Брокколи |
−1,2 |
|
Апельсины |
−2,7 |
Морковь |
−4,9 |
|
Персики |
−2,4 |
Цветная капуста |
−4,0 |
|
Ананас |
−2,7 |
Сельдерей |
−5,2 |
|
Изюм |
−21,0 |
Огурец |
−0,8 |
|
Клубника |
−2,2 |
Баклажан |
−3,4 |
|
Грецкие орехи |
6,8 |
Листья салата |
−2,5 |
|
Арбуз |
−1,9 |
Грибы |
−1,4 |
|
Зерновые продукты: |
Лук |
−1,5 |
|
|
Хлеб из ржаной муки |
4,0 |
Картофель |
−4,0 |
|
Хлеб из пшеничной муки |
3,8 |
Редис красный |
−3,7 |
|
Рис белый |
1,7 |
Томатный сок |
−2,8 |
|
Пшеничная мука |
6,9 |
Помидоры |
−3,1 |
Медикаментозные методы повышения pH мочи. Повышение pH мочи сопряжено с увеличением растворимости мочевой кислоты и цистина, увеличением экскреции мочевого цитрата, поэтому оно считается важным инструментом в лечении данных вариантов уролитиаза. Для повышения pH мочи используются препараты, содержащие лимонную кислоту и её соли (натрия, калия и магния цитраты) и соли угольной кислоты (натрия и калия бикарбонаты). Часто их называют «цитратными смесями» или «щелочными цитратами».
Цитрат инактивирует фосфатзависимую глутаминазу почечных канальцев, что снижает активность аммониогенеза и приводит к повышению pH мочи. Цитратные смеси содержат большое количество лимонной кислоты или её солей, которые обладают практически 100% биодоступностью. Однако только 1,5–2% поступившего из желудочно-кишечного тракта цитрата выводится с мочой, так как большая его часть метаболизируется в печени. Увеличение мочевого цитрата при терапии цитратными смесями в первую очередь происходит благодаря уменьшению его реабсорбции в дистальных почечных канальцах при повышении pH.
Повышение рН более 6,8 позволяет проводить литолиз мочекислых конкрементов, так как константа диссоциации мочевой кислоты в моче составляет 5,5. Мочевая кислота переходит в растворимую форму вследствие замещения водорода гидроксильных групп пуринового ядра мочевой кислоты щелочными металлами, поступающими из солей лимонной кислоты. Необходимая для достижения указанных значений pH доза цитратной смеси может достигать 6–18 г в сутки, следствием чего является высокая натриевая нагрузка, достигающая 3–4 г в сутки. Это способствует гиперкальциуриии и как следствие возможному образованию кальций оксалатных камней, а также к повышению артериального давления [42].
Повышение рН мочи рекомендуется пациентам с постоянно низким рН мочи и гипоцитратурией при проведении профилактики кальций-оксалатного уролитиаза [43]. Цитрат образует комплексы с кальцием, что уменьшает количество свободного кальция в моче. Также он связывается с поверхностью кристаллов оксалата кальция и фосфата кальция, замедляя их дальнейший рост и агломерацию [30]. В лабораторных условиях было показано, что даже незначительное повышение концентрации цитрата в моче также замедляет рост кристаллов фосфата [44].
С учётом риска развития гиперкальциурии вследствие высокой натриевой нагрузки следует отдавать предпочтение цитратным смесям с низким содержания натрия. Эффективность коррекции гипоцитратурии с помощью монотерапии лимонной кислотой несколько снижается за счёт создаваемой ею кислотной нагрузки, поэтому предпочтение отдаётся цитратам калия и магния. Целесообразность долгосрочного применения калия цитрата при проведении метафилактики МКБ показана во многих, в том числе рандоминизированных, исследованиях [45]. Однако такой терапии придерживается только около 13% пациентов [46]. Низкая приверженность терапии обусловлена многими причинами, в том числе побочными эффектами в виде болей в животе, диареи и высокой стоимости лечения. Для повышения рН мочи может применяться цитрат магния, однако его приём в эффективных терапевтических дозировках так же сопряжён с высокой частотой развития диареи.
Применение цитратных смесей может приводить к обострению гиперацидного гастрита и язвенной болезни желудка, что ограничивает их применение у ряда пациентов. Целесообразно одновременное проведение гастропротективной терапии ингибиторами протонной помпы и препаратами, увеличивающими уровень простагландина Е2 в слизистой оболочке желудка. В качестве альтернативы цитратным смесям можно рассматривать натрия бикарбонат (пищевую соду), который является доступным и недорогим средством. Негативной стороной монотерапии бикарбонатом натрия является существенное повышение экскреции натрия [42].
Выраженное повышение pH мочи наблюдается при применении ингибиторов фермента карбоангидразы, которыми являются диуретики ацетазоламид (препарат диакарб) и метазоламид (не зарегистрирован в Российской Федерации). Ингибиторы карбоангидраз приводят к уменьшению образования и диссоциации угольной кислоты в проксимальных канальцах, вследствие чего уменьшается поступление в кровь бикарбоната, необходимого для пополнения щелочных резервов крови, и дефициту протонов водорода в эпителиальных клетках канальца (рис. 9).
Рисунок 9. Механизм действия ингибиторов карбоангидразы в проксимальном канальце и в собирательных трубках
Figure 9. Acting mechanism of carbonic anhydrase inhibitors in the proximal tubule and collecting tubes
Дефицит протонов приводит к снижению активности Na+/H+-транспортера, вследствие чего в просвете канальцев возникает избыток катионов натрия и дефицит протонов водорода. Натрий выводится с изоосмотическим количеством воды, что приводит к увеличению диуреза. Дефицит протонов в просвете канальцев приводит к уменьшению его связывания с находящимся в избытке в почечном фильтрате бикарбонатом с образованием угольной кислоты. Поэтому дефицит протонов в итоге приводит к избытку бикарбоната, который начинает выводиться с мочой, в итоге, повышая её рН. Недостаточное восполнение бикарбонатного буфера крови может привести к развитию гиперхлоремического ацидоза.
Ингибиторы карбоангидразы применяются при лечении хронической сердечной недостаточности, отёчном синдроме, повышении внутричерепного давления, глаукоме, эпилепсии. Высокие дозы эффективно повышают pH мочи. Было показано, что ацетозоламид в дозе 500 мг при применении через каждые 6 часов увеличил средний показатель рН мочи с 5,9 до 7,2 [47]. Плохая переносимость пациентами ацетазоламида ограничивает его применение в качестве подщелачивающего мочу средства у пациентов с мочекаменной болезнью. Так, вследствие развития побочных эффектов половина пациентов с мочекислыми и цистиновыми конкрементами не смогла продолжить терапию препаратом в дозе 500 мг в сутки с целью усиления подщелачивающего эффекта терапии [48]. Теоретически терапия высокими дозами ингибиторов карбоангидразы может быть полезна при назначении высоких доз препаратов, кристаллизующихся в кислой моче, например, метотрексата, так низкая его растворимость в кислой моче может привести к кристаллизации препарата в почечных канальцах с развитием острой почечной недостаточности. Однако ввиду риска развития внутриклеточного ацидоза не рекомендуется проводить терапию высокими дозами препарата более 48 часов [49].
Медикаментозные методы снижения pH мочи. Длительная ацидификация мочи рассматривается в качестве одного из инструментов метафилактики инфекционного нефролитиаза, поскольку образование таких камней происходит при pH мочи выше 6,8. Считается, что снижение pH ниже этих значений препятствует формированию инфекционных конкрементов [50]. Также известно, что кислая среда оказывает ингибирующее действие на бактериальную флору, однако рассчитывать на значимый эффект нельзя, поскольку он возникает при недостижимых in vivo значениях рН мочи менее 4,5 [51]. На практике даже снижение pH менее 6,8 у пациентов с персистирующей уреазопродуцирующей флорой в моче при инфекционном нефролитиазе представляет собой сложную задачу.
В качестве препаратов для ацидификации мочи рассматриваются L-метионин, аскорбиновая кислота, аммония хлорид [52]. L-метионин представляет собой незаменимую аминокислоту, участвующую в обмене серосодержащих аминокислот, адреналина, креатинина, цианкобаламина, аскорбиновой и фолиевой кислот, гормонов, ферментов. Он обладает высокой биодоступностью и в небольшом количестве выделяется с мочой. Приём здоровыми добровольцами 1500 мг L-метионина в день приводил к снижению pH мочи и насыщения её брушитом и струвитом [53]. 10-летнее наблюдение за 19 пациентами со струвитными камнями показало, что длительное применение L-метионина в дозе 1500–3000 мг в сутки позволило снизить частоту рецидивирования камнеобразования. Исследование мочи каждые три месяца у этих пациентов демонстрировало снижение её pH и увеличение суточной экскреции ингибиторов камнеобразования цитрата, магния, калия [51]. Однако целесообразность рутинного применения L-метионина для профилактики инфекционного нефролитиаза вызывает сомнения ввиду отсутствия значимых исследований по оценке эффективности препарата и его слабого влияния на pH мочи при приёме в рекомендуемой дозировке (до 1500 мг в сутки) [54].
В качестве альтернативы L-метионину рассматривается аммония хлорид. Описаны результаты длительного перорального приёма раствора аммония хлорида в дозе до 3 г в сутки 11 пациентами с инфекционным нефролитиазом в течение 32 месяцев, на протяжении которых отмечалось значимое снижение pH мочи [53]. Однако широкое применение аммония хлорида ограничено риском развития такого серьёзного осложнения, как метаболический ацидоз. В России в качестве лекарственного препарата аммония хлорид не зарегистрирован.
В качестве ещё одного средства для ацидификации мочи рассматривалась аскорбиновая кислота. Однако исследования показали отсутствие значимого влияния её перорального приёма и парентерального введения на кислотность мочи [55, 56].
Обсуждение
В настоящий момент не вызывает сомнений, что pH мочи оказывает значительное влияние на процессы камнеобразования. Необходимость проведения оценки pH мочи у больных уролитиазом и при необходимости его коррекция отражена в клинических рекомендациях по ведению пациентов с МКБ [43][58].
Хорошо изучена роль длительной ацидофикации мочи. Снижение рН мочи ниже 5,5 (ниже константы диссоциации мочевой кислоты в моче) является главной причиной образования мочекислых конкрементов. Такое стойкое снижение pH мочи наблюдается у пациентов с избыточным весом вследствие развития гиперинсулинемии и инсулинорезистентности вследствие висцерального ожирения, нарушения экскреции аммония и подкисления мочи в проксимальных канальцах.
Также причиной длительного снижения pH может быть рацион питания. Современная диета западного типа отличается дефицитом фруктов и овощей и чрезмерным потреблением продуктов животного происхождения. Это приводит к накоплению неметаболизируемых анионов — диетическому метаболическому ацидозу. В ответ реализуются ренальные компенсаторные механизмы, направленные на восстановление кислотно-щелочного баланса: удаление неметаболизируемых анионов, сохранение цитрата, усиление почечного аммиагенеза, и выделение ионов аммония. Эти адаптивные процессы снижают рН мочи и способствуют литогенным изменениям в составе мочи, включающим гипоцитратурию, гиперкальциурию, потерю азота и фосфатов. Поэтому снижение pH мочи ниже 5,8 считается одним фактором образования кальций-оксалатных конкрементов, несмотря на то что камни из оксалата кальция могут образовываться при любых значениях рН мочи.
Повышение pH достигается путём изменения пищевого рациона (снижения потребления животного белка и увеличением потребления фруктов и овощей) и применением цитратных смесей, реже — бикарбоната натрия. Следует отметить, что длительная терапия цитратными смесями ограничена риском развития гастродуоденопатии и натриевой нагрузки. Для патогенетической коррекции нарушений кислотности мочи у пациентов с избыточным весом, сахарным диабетом 2 типа необходимо проводить лечение данных заболеваний.
Целевой диапазон pH мочи при проведении профилактики мочекислого уролитиаза определён в пределах 6,0–6,5, при проведении литолиза таких конкрементов — в пределах 6,8–7,2. Повышение pH выше этих цифр при проведении литолиза нецелесообразно, так как сопряжено с повышением риска образования кальций-фосфатных конкрементов.
Пациентам с кальций-оксалатным нефролитиазом, имеющим постоянно низкий уровень pH (ниже 5,8), целесообразно повышение pH мочи до величин профилактического диапазона 6,0–6,5. Более высоких значений pH в пределах 7,0–8,0 необходимо достигать пациентам с цистиновым нефролитиазом, поскольку растворимость цистина существенно увеличивается при pH выше 7,5.
В условиях высоких значений pH происходит формирования кальций-фосфатных и инфекционных конкрементов. Таким пациентам целесообразно снижение pH мочи ниже литогенного показателя 6,5. Однако возможности медикаментозной ацидификации мочи существенно ограничены ввиду низкой эффективностью доступного в клинической практике препарата (метионина).
Выводы
- Показатель pH мочи является одним из маркеров, свидетельствующих о наличии патологических изменений как в организме в целом, так и в мочевыделительной системе в частности. Это один из ключевых параметров, определяющих литогенные свойства мочи, и оказывающий значительное влияние на формирование всех типов конкрементов.
- Определение рН мочи является важным этапом обследования пациентов с уролитиазом и должно проводиться 3–4 раза в день с помощью индикаторных тест-полосок или электронных pH-метров.
- Поддержание pH мочи в её нелитогенном диапазоне с учётом состава конкремента должно применяться в качестве инструмента профилактики рецидива.
- В клинической практике доступны немедикаментозные (модификация пищевого рациона) и демонстрирующие более высокую эффективность медикаментозные методы (назначение щелочных цитратов), которые успешно применяются для повышения pH мочи при проведении метафилактики мочекислых, кальций-оксалатных и цистиновых конкрементов.
- Вместе с этим следует признать, что в настоящий момент в арсенале уролога отсутствуют средства, позволяющие безопасно проводить длительную и эффективную ацидификацию pH мочи.
1. Wein AJ, Kavoussi LR, Partin AW, Peters AC. Campbell-Walsh Urology: 4-Volume Set. 11th Edition. Philadelphia: Elsevier; 2015. ISBN-10: 1455775673.
2. Sorokin I, Mamoulakis C, Miyazawa K, Rodgers A, Talati J, Lotan Y. Epidemiology of stone disease across the world. World J Urol. 2017;35(9):1301-20. https://doi.org/10.1007/s00345-017-2008-6
3. Gadzhiev N, Prosyannikov M, Malkhasyan V, Akopyan G, Somani B, Sivkov A, Apolikhin O, Kaprin A. Urolithiasis prevalence in the Russian Federation: analysis of trends over a 15-year period. World J Urol. 202;39(10):3939-44. https://doi.org/10.1007/s00345-021-03729-y
4. Rule AD, Lieske JC, Li X, Melton LJ 3rd, Krambeck AE, Bergstralh EJ. The ROKS nomogram for predicting a second symptomatic stone episode. J Am Soc Nephrol. 2014;25(12):2878-86. https://doi.org/10.1681/ASN.2013091011
5. Turney BW, Reynard JM, Noble JG, Keoghane SR. Trends in urological stone disease. BJU Int. 2012;109(7):1082-7. https://doi.org/10.1111/j.1464-410X.2011.10495.x
6. Ferraro PM, Curhan GC, D’Addessi A, Gambaro G. Risk of recurrence of idiopathic calcium kidney stones: analysis of data from the literature. J Nephrol. 2017;30(2):227-33. https://doi.org/10.1007/s40620-016-0283-8
7. Wagner CA, Mohebbi N. Urinary pH and stone formation. J Nephrol. 2010;23 Suppl 16:S165-9. PMID: 21170875
8. Cicerello E. Uric acid nephrolithiasis: An update. Urologia. 2018;85(3):93-8. https://doi.org/10.1177/0391560318766823
9. Laube N, Berg W. Praxisorientiertes Kompendium. Uro-News. 2013;17(11):47-49. https://doi.org/10.1007/s00092-013-0411-x
10. Rennke HG, Denker BM. Renal Pathophysiology: The Essentials. 5th edition. Philadelphia: Wolters Kluwer; 2020. ISBN-10: 1975109597.
11. Murayama T, Taguchi H. The role of the diurnal variation of urinary pH in determining stone compositions. J Urol. 1993;150(5 Pt 1):1437-9. https://doi.org/10.1016/s0022-5347(17)35801-9
12. Simpson DP. Citrate excretion: a window on renal metabolism. Am J Physiol. 1983;244(3):F223-34. https://doi.org/10.1152/ajprenal.1983.244.3.F223
13. Kraut JA, Madias NE. Metabolic acidosis: pathophysiology, diagnosis and management. Nat Rev Nephrol. 2010;6(5):274-85. https://doi.org/10.1038/nrneph.2010.33
14. Strohmaier WL, Wrobel BM, Schubert G. Overweight, insulin resistance and blood pressure (parameters of the metabolic syndrome) in uric acid urolithiasis. Urol Res. 2012;40(2):171-5. https://doi.org/10.1007/s00240-011-0403-9
15. Maalouf NM, Cameron MA, Moe OW, Adams-Huet B, Sakhaee K. Low urine pH: a novel feature of the metabolic syndrome. Clin J Am Soc Nephrol. 2007;2(5):883-8. https://doi.org/10.2215/CJN.00670207
16. Spatola L, Ferraro PM, Gambaro G, Badalamenti S, Dauriz M. Metabolic syndrome and uric acid nephrolithiasis: insulin resistance in focus. Metabolism. 2018;83:225-33. https://doi.org/10.1016/j.metabol.2018.02.008
17. Гаджиев Н.К., Малхасян В.А., Мазуренко Д.А., Гусейнов М.А., Тагиров Н.С. Мочекаменная болезнь и метаболический синдром. Патофизиология камнеобразования. Экспериментальная и клиническая урология. 2018;(1):66-75. https://doi.org/10.29188/2222-8543-2018-9-1-66-75
18. Patschan D, Patschan S, Ritter O. Chronic Metabolic Acidosis in Chronic Kidney Disease. Kidney Blood Press Res. 2020;45(6):812-22. https://doi.org/10.1159/000510829
19. Bambach CP, Robertson WG, Peacock M, Hill GL. Effect of intestinal surgery on the risk of urinary stone formation. Gut. 1981;22(4):257-63. https://doi.org/10.1136/gut.22.4.257
20. Knudsen L, Marcussen H, Fleckenstein P, Pedersen EB, Jarnum S. Urolithiasis in chronic inflammatory bowel disease. Scand J Gastroenterol. 1978;13(4):433-6. https://doi.org/10.3109/00365527809181917
21. Lin PH, Ginty F, Appel LJ, Aickin M, Bohannon A, Garnero P, Barclay D, Svetkey LP. The DASH diet and sodium reduction improve markers of bone turnover and calcium metabolism in adults. J Nutr. 2003;133(10):3130-6. https://doi.org/10.1093/jn/133.10.3130
22. Meschi T, Maggiore U, Fiaccadori E, Schianchi T, Bosi S, Adorni G, Ridolo E, Guerra A, Allegri F, Novarini A, Borghi L. The effect of fruits and vegetables on urinary stone risk factors. Kidney Int. 2004;66(6):2402-10. https://doi.org/10.1111/j.1523-1755.2004.66029.x
23. Schwartz BF, Stoller ML. Nonsurgical management of infection-related renal calculi. Urol Clin North Am. 1999;26(4):765-78, viii. https://doi.org/10.1016/s0094-0143(05)70217-2
24. Parsons CL, Stauffer C, Mulholland SG, Griffith DP. Effect of ammonium on bacterial adherence to bladder transitional epithelium. J Urol. 1984;132(2):365-6. https://doi.org/10.1016/s0022-5347(17)49628-5
25. Jones BD, Mobley HL. Genetic and biochemical diversity of ureases of Proteus, Providencia, and Morganella species isolated from urinary tract infection. Infect Immun. 1987;55(9):2198-203. https://doi.org/10.1128/iai.55.9.2198-2203.1987
26. Flannigan R, Choy WH, Chew B, Lange D. Renal struvite stones—pathogenesis, microbiology, and management strategies. Nat Rev Urol. 2014;11(6):333-41. https://doi.org/10.1038/nrurol.2014.99
27. Dhayat NA, Gradwell MW, Pathare G, Anderegg M, Schneider L, Luethi D, Mattmann C, Moe OW, Vogt B, Fuster DG. Furosemide/Fludrocortisone Test and Clinical Parameters to Diagnose Incomplete Distal Renal Tubular Acidosis in Kidney Stone Formers. Clin J Am Soc Nephrol. 2017;12(9):1507-1517. https://doi.org/10.2215/CJN.01320217
28. Антонов В.Г., Карпищенко А.И. Кислотно-основное состояние. В кн.: Медицинская лабораторная диагностика: программы и алгоритмы. Под ред.: А.И. Карпищенко. 3-е изд. перераб. и доп. М.: ГЭОТАР-Медиа; 2014. ISBN: 978-5-9704-2958-7.
29. Welshman SG, McGeown MG. Urinary citrate excretion in stone-formers and normal controls. Br J Urol. 1976;48(1):7-11. https://doi.org/10.1111/j.1464-410x.1976.tb02731.x
30. Zuckerman JM, Assimos DG. Hypocitraturia: pathophysiology and medical management. Rev Urol. 2009;11(3):134-44. PMCID: PMC2777061
31. Fegan J, Khan R, Poindexter J, Pak CY. Gastrointestinal citrate absorption in nephrolithiasis. J Urol. 1992;147(5):1212-4. https://doi.org/10.1016/s0022-5347(17)37520-1
32. Unwin RJ, Capasso G, Shirley DG. An overview of divalent cation and citrate handling by the kidney. Nephron Physiol. 2004;98(2):p15-20. https://doi.org/10.1159/000080259
33. Zacchia M, Preisig P. Low urinary citrate: an overview. J Nephrol. 2010;23 Suppl 16:S49-56. PMID: 21170889
34. Hamm LL, Alpern RJ. Regulation of acid–base balance, citrate, and urine pH. In: Coe FL, Favus MJ, Pak CYC, Parks JH, Preminger GM, editors. Kidney Stones: Medical and Surgical Management. Lippincott-Raven; Philadelphia: 1996. ISBN-13: 978-0781702638.
35. Domrongkitchaiporn S, Stitchantrakul W, Kochakarn W. Causes of hypocitraturia in recurrent calcium stone formers: focusing on urinary potassium excretion. Am J Kidney Dis. 2006;48(4):546-54. https://doi.org/10.1053/j.ajkd.2006.06.008
36. Yang L, Wang K, Li H, Denstedt JD, Cadieux PA. The influence of urinary pH on antibiotic efficacy against bacterial uropathogens. Urology. 2014;84(3):731.e1-7. https://doi.org/10.1016/j.urology.2014.04.048
37. Ilyas R, Chow K, Young JG. What is the best method to evaluate urine pH? A trial of three urinary pH measurement methods in a stone clinic. J Endourol. 2015;29(1):70-4. https://doi.org/10.1089/end.2014.0317
38. Welch AA, Mulligan A, Bingham SA, Khaw KT. Urine pH is an indicator of dietary acid-base load, fruit and vegetables and meat intakes: results from the European Prospective Investigation into Cancer and Nutrition (EPIC)-Norfolk population study. Br J Nutr. 2008;99(6):1335-43. https://doi.org/10.1017/S0007114507862350
39. Remer T, Manz F. Potential renal acid load of foods and its influence on urine pH. J Am Diet Assoc. 1995;95(7):791-7. https://doi.org/10.1016/S0002-8223(95)00219-7
40. Trinchieri A, Maletta A, Lizzano R, Marchesotti F. Potential renal acid load and the risk of renal stone formation in a case-control study. Eur J Clin Nutr. 2013;67(10):1077-80. https://doi.org/10.1038/ejcn.2013.155
41. Siener R, Hesse A. The effect of a vegetarian and different omnivorous diets on urinary risk factors for uric acid stone formation. Eur J Nutr. 2003;42(6):332-7. https://doi.org/10.1007/s00394-003-0428-0
42. Pinheiro VB, Baxmann AC, Tiselius HG, Heilberg IP. The effect of sodium bicarbonate upon urinary citrate excretion in calcium stone formers. Urology. 2013;82(1):33-7. https://doi.org/10.1016/j.urology.2013.03.002
43. Pearle MS, Goldfarb DS, Assimos DG, Curhan G, Denu-Ciocca CJ, Matlaga BR, Monga M, Penniston KL, Preminger GM, Turk TM, White JR; American Urological Assocation. Medical management of kidney stones: AUA guideline. J Urol. 2014;192(2):316-24. https://doi.org/10.1016/j.juro.2014.05.006
44. Rimer JD, Sakhaee K, Maalouf NM. Citrate therapy for calcium phosphate stones. Curr Opin Nephrol Hypertens. 2019;28(2):130-139. https://doi.org/10.1097/MNH.0000000000000474
45. Barcelo P, Wuhl O, Servitge E, Rousaud A, Pak CY. Randomized double-blind study of potassium citrate in idiopathic hypocitraturic calcium nephrolithiasis. J Urol. 1993;150(6):1761-4. https://doi.org/10.1016/s0022-5347(17)35888-3
46. Dauw CA, Yi Y, Bierlein MJ, Yan P, Alruwaily AF, Ghani KR, Wolf JS Jr, Hollenbeck BK, Hollingsworth JM. Factors Associated With Preventive Pharmacological Therapy Adherence Among Patients With Kidney Stones. Urology. 2016;93:45-9. https://doi.org/10.1016/j.urology.2016.03.030
47. Shamash J, Earl H, Souhami R. Acetazolamide for alkalinisation of urine in patients receiving high-dose methotrexate. Cancer Chemother Pharmacol. 1991;28(2):150-1. https://doi.org/10.1007/BF00689708
48. Sterrett SP, Penniston KL, Wolf JS Jr, Nakada SY. Acetazolamide is an effective adjunct for urinary alkalization in patients with uric acid and cystine stone formation recalcitrant to potassium citrate. Urology. 2008;72(2):278-81. https://doi.org/10.1016/j.urology.2008.04.003
49. Van Berkel MA, Elefritz JL. Evaluating off-label uses of acetazolamide. Am J Health Syst Pharm. 2018;75(8):524-531. https://doi.org/10.2146/ajhp170279
50. Jarrar K, Boedeker RH, Weidner W. Struvite stones: long term follow up under metaphylaxis. Ann Urol (Paris). 1996;30(3):112-7. PMID: 8766146
51. Bibby JM, Hukins DW. Acidification of urine is not a feasible method for preventing encrustation of indwelling urinary catheters. Scand J Urol Nephrol. 1993;27(1):63-5. https://doi.org/10.3109/00365599309180415
52. Wall I, Tiselius HG. Long-term acidification of urine in patients treated for infected renal stones. Urol Int. 1990;45(6):336-41. https://doi.org/10.1159/000281732
53. Siener R, Struwe F, Hesse A. Effect of L-Methionine on the Risk of Phosphate Stone Formation. Urology. 2016;98:39-43. https://doi.org/10.1016/j.urology.2016.08.007
54. Karki N, Leslie SW. Struvite And Triple Phosphate Renal Calculi. 2022 May 27. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022. Bookshelf ID: NBK568783
55. Barton CH, Sterling ML, Thomas R, Vaziri ND, Byrne C, Ryan G. Ineffectiveness of intravenous ascorbic acid as an acidifying agent in man. Arch Intern Med. 1981;141(2):211-2. PMID: 7458517
56. Hetey SK, Kleinberg ML, Parker WD, Johnson EW. Effect of ascorbic acid on urine pH in patients with injured spinal cords. Am J Hosp Pharm. 1980 Feb;37(2):235-7. PMID: 7361797
57. Skolarikos A, Neisius A, Petřík A, Somani B, Thomas K, Gambaro G. Urolithiasis. In: EAU Guidelines. Edn. presented at the EAU Annual Congress Amsterdam, 2022. ISBN 978-94-92671-16-5. URL: https://uroweb.org/guideline/urolithiasis/
Анализ мочи — один из наиболее часто запрашиваемых врачами лабораторных анализов. Проводить анализ просто, дешево и быстро. Можно получить результаты общего анализа мочи через несколько часов, чтобы в тот же день узнать, все ли в порядке. В противном случае нужно как можно скорее обратиться к врачу.
Если, например, подозревается инфекция мочевыделительной системы, общий анализ мочи может четко ответить на вопрос, действительно ли произошло инфицирование. Общий анализ мочи позволяет быстро и эффективно диагностировать и начать лечение (обычно после более длительного периода инокуляции).
pH мочи – тест
Анализ мочи измеряет несколько основных параметров, указывающих на здоровье организма. Параметры включают цвет исследуемой мочи, ее удельный вес, pH мочи, наличие глюкозы, а также белок, билирубин и кетоновые тела. Кроме того, общий осмотр — это также оценка осадка и наличия в нем бактерий, плоского эпителия, эритроцитов и лейкоцитов.
О самом анализе мочи и интерпретации каждого из отдельных параметров можно написать несколько страниц. Однако в этой небольшой статье будут рассмотрены только один критерий, а именно pH мочи. Каким должен быть индикатор pH мочи, когда он может измениться, в какой момент следует беспокоиться и что вообще показывает этот индикатор.
Как и в случае с любым другим тестом, у анализа мочи есть свои стандарты. Описанный в этой статье тест определяет pH мочи.
pH мочи колеблется от 0 до 7; нейтральный — значение принимает pH мочи 7 или щелочной. Тогда значения начинаются с pH мочи 7 и заканчиваются на pH мочи 14.
В случае pH мочи он также бывает кислым, нейтральным. В этом исследовании значения, которые не должны беспокоить, несколько ограничены. Они не имеют того же диапазона, что и весь диапазон pH, и колеблются только в пределах диапазона pH мочи 4,5 — pH 8 мочи. Диапазоны реакции основаны на шкале кислотности-щелочности (pH).
Но зачем вообще проверять pH мочи и что на основании этого можно сделать?
Анализы мочи и, в частности, pH мочи могут предоставить много информации, в том числе:
- потенциальные нарушения обмена веществ;
- гормональные нарушения (особенно у женщин);
- инфекции;
- дефицит или избыток калия чаще всего связаны с текущим питанием, но иногда и с серьезными заболеваниями;
Нормальный pH мочи
Какой правильный pH мочи? Казалось бы, поскольку pH мочи 7 указывает на нейтральный pH мочи, именно pH мочи 7 является наиболее желательным и считается идеальным результатом теста. Фактически, pH 6,5 считается наиболее оптимальным pH мочи. У здоровых людей без выявленных нарушений обмена веществ, соблюдающих сбалансированное питание, моча должна быть слабокислой. Значение ниже нейтрального уровня связано с безопасностью. Кислая среда способствует росту низкому проценту микроорганизмов. И бактерии, и грибки плохо себя чувствуют в такой среде, поэтому, если моча слегка кислая, человек может чувствовать безопасность.
Слегка низкий или слегка повышенный pH мочи
Однако иногда при проверке pH мочи при общем осмотре выясняется, что pH повышен. Как правило, небольшие изменения, такие как pH мочи 7 или pH 6, являются стандартными и в большинстве случаев не указывают на какую-либо угрозу здоровью. Такие небольшие изменения могут быть результатом недостаточного или чрезмерного увлажнения тела. Еще одно объяснение — ежедневный рацион.
Люди, которые едят больше продуктов животного происхождения, обычно имеют кислый pH мочи. Вегетарианцы будут иметь щелочной pH мочи. Ни в том, ни в другом случае это не особо опасный показатель. Но следует помнить, что лучше всего, если диета будет разнообразной и не вызывает отклонений ни в одном из параметров нашего тела.
Низкий pH мочи
Что делать, если низкий pH мочи? Что ж, проблема может начаться, если нормы pH мочи значительно отклонятся от установленных норм.
С более кислой мочой, pH которой колеблется в районе 4,5-5, можно сделать вывод, что эти значения неверны и требуют консультации врача.
Очень низкий pH мочи может указывать на заболевание почек, включая почечную недостаточность. Кроме того, легко распознать неправильно регулируемый диабет, потому что он вызывает кислотность мочи.
Заболевания легких также могут быть еще одной причиной повышенной кислотности мочи. Эмфизема также характеризуется низким уровнем pH мочи человека.
Щелочная моча
Проблема также может возникнуть, если моча имеет pH выше 7. Результат мочи 8, конечно, все еще является значением в пределах нормального диапазона, и, как уже упоминалось ранее, это значение также не должно означать ничего серьезного. Влияние вегетарианской диеты также может привести к этому значению в общем исследовании. Однако обычно значительная щелочность мочи, то есть pH между pH 7 и 8, позволяет предположить или просто подтвердить (с дополнительными параметрами, например, анализом осадка мочи) об инфекции мочевыделительной системы.
Щелочной pH, помимо инфекций мочевыводящих путей, заболеваний почек или диеты, богатой калием (гиперкалиемия), также является показанием для тестов на работу паращитовидных желез и, опять же, дыхательной системы. Хотя повышенная кислотность мочи может быть вызвана эмфиземой, чрезмерное повышение pH, то есть повышение щелочности мочи, иногда является симптомом астмы.
Один параметр и множество различных интерпретаций помогают в диагностике и лечении заболеваний, связанных не только с выделительной системой. Анализ мочи — это не только анализ, проводимый при подозрении на заболевания или инфекции мочевыделительной системы. Он дает общее представление о состоянии здоровья, и простое изменение pH может помочь определить, в чем проблема.