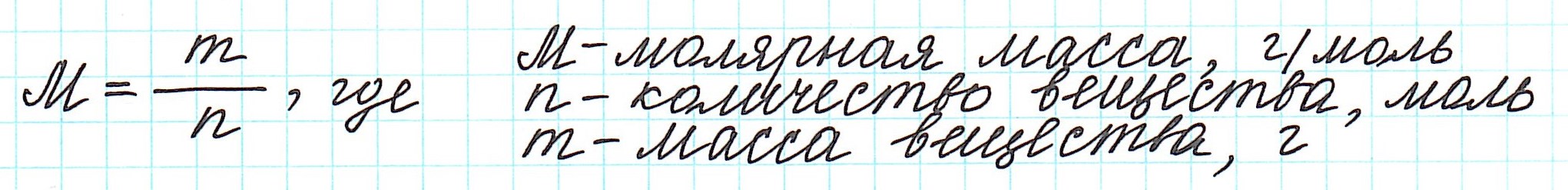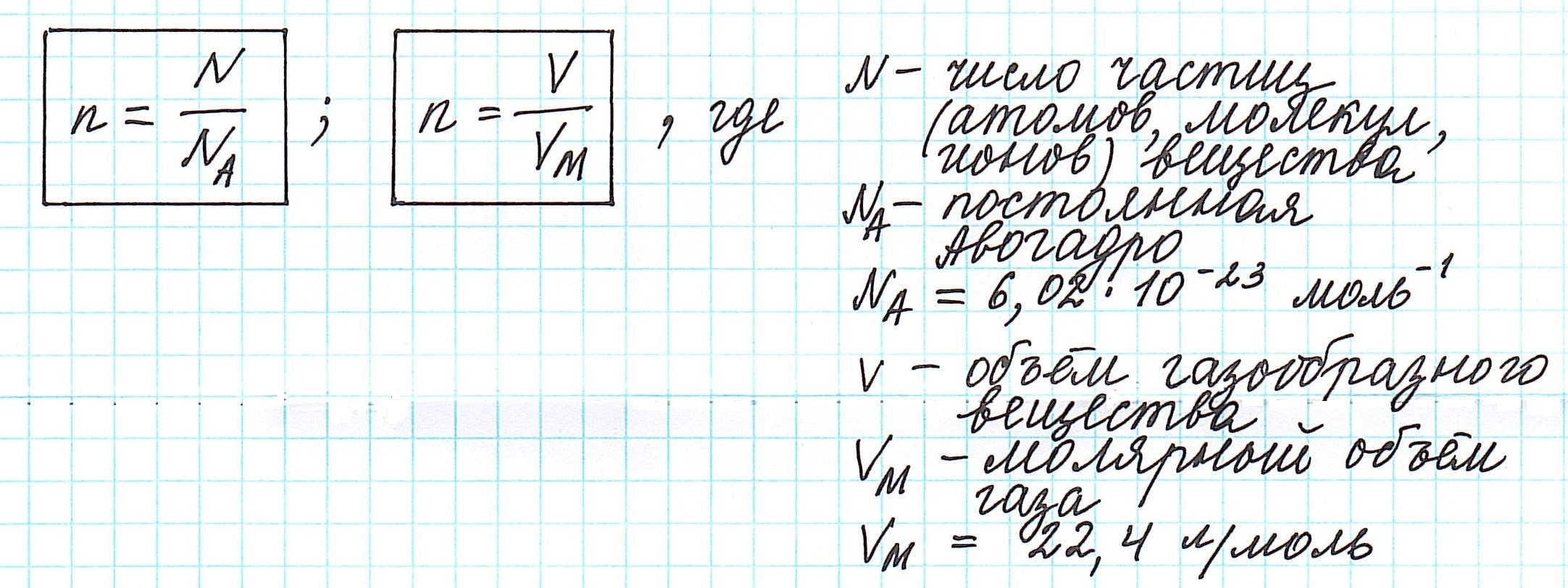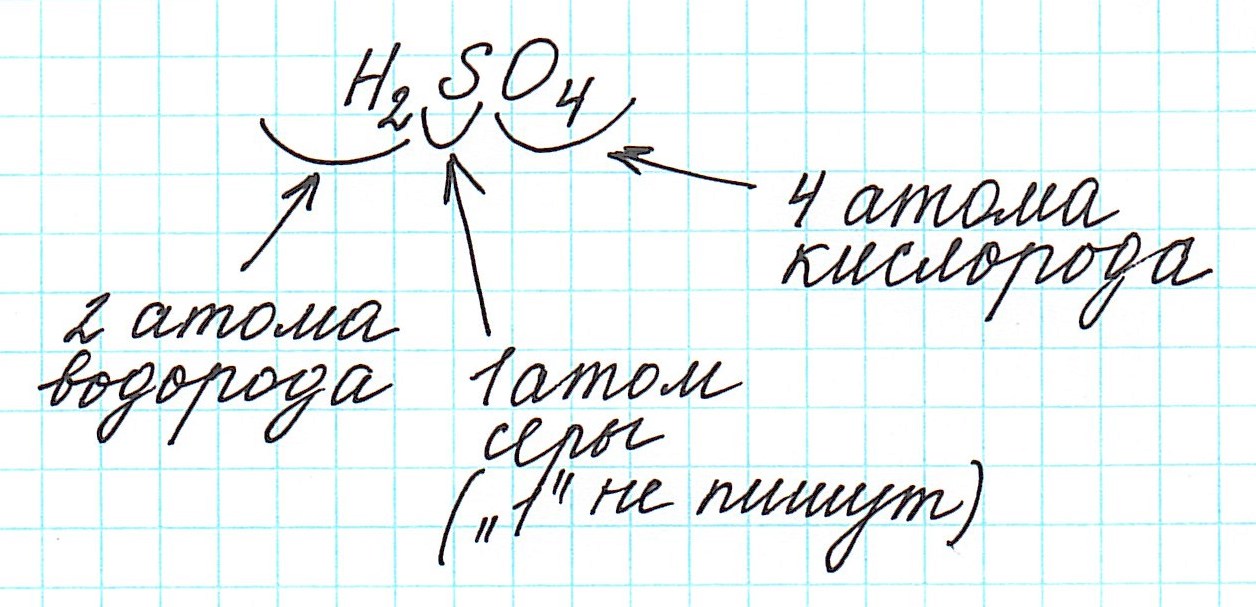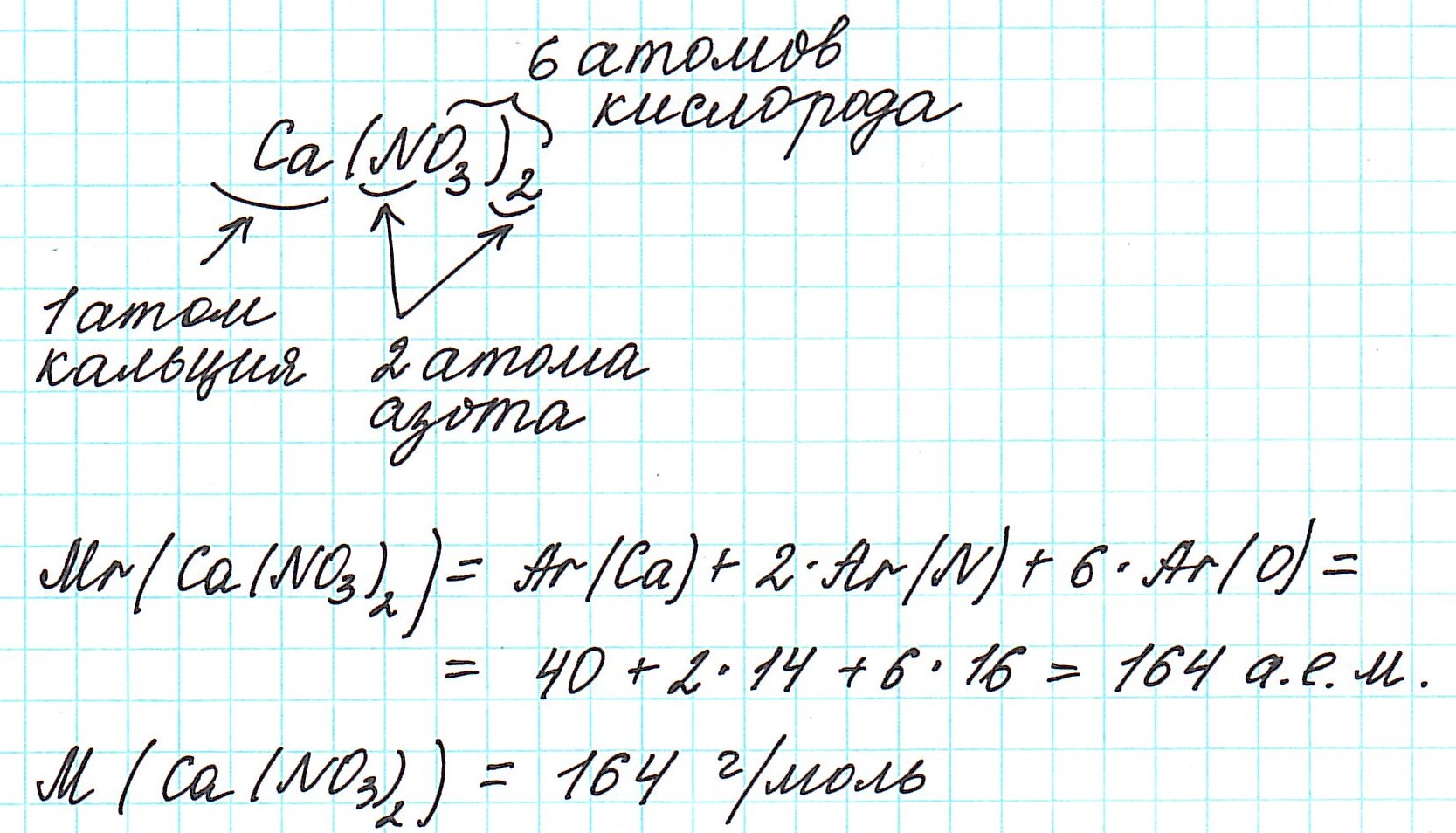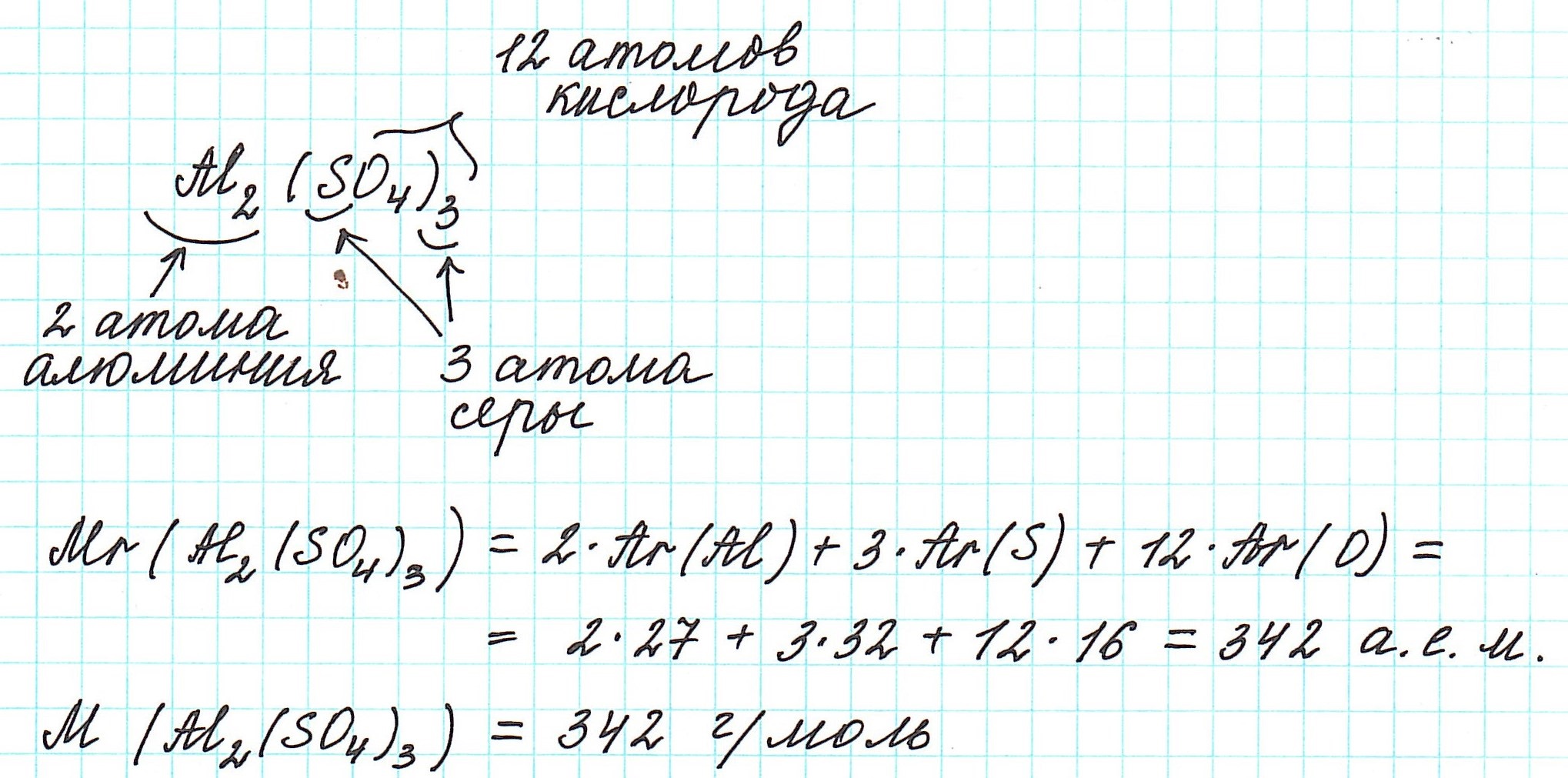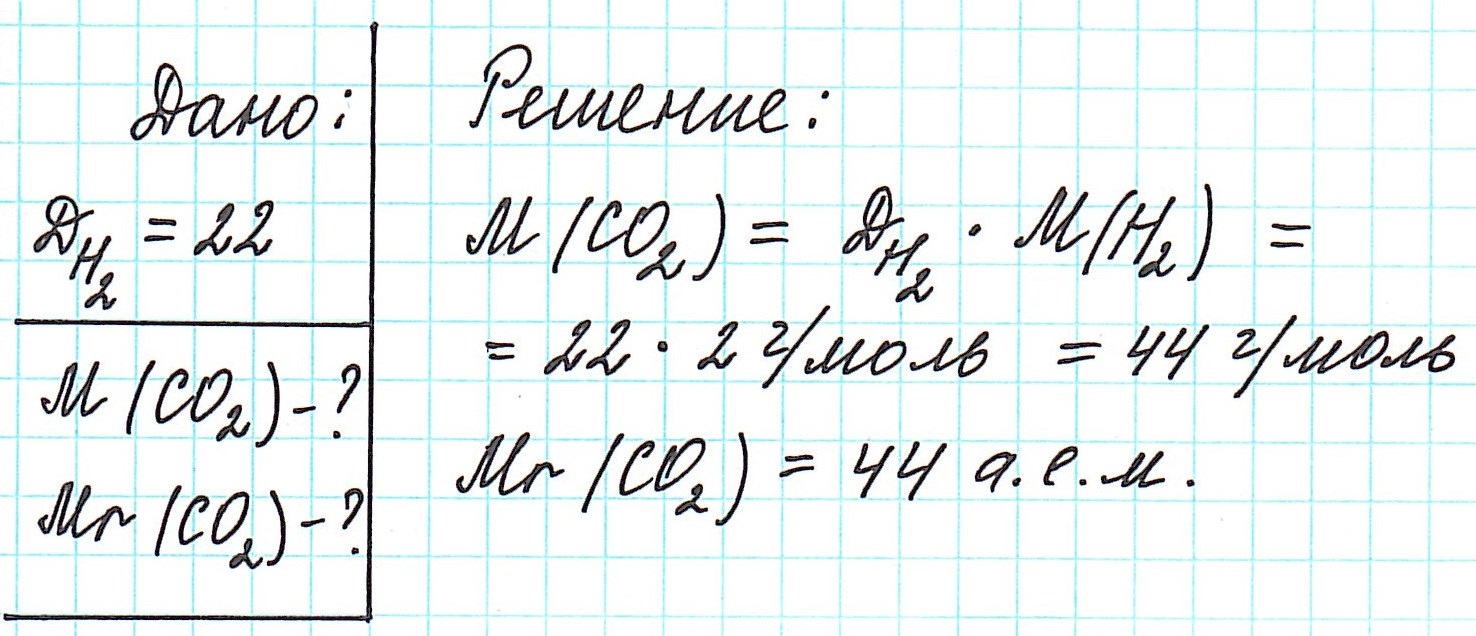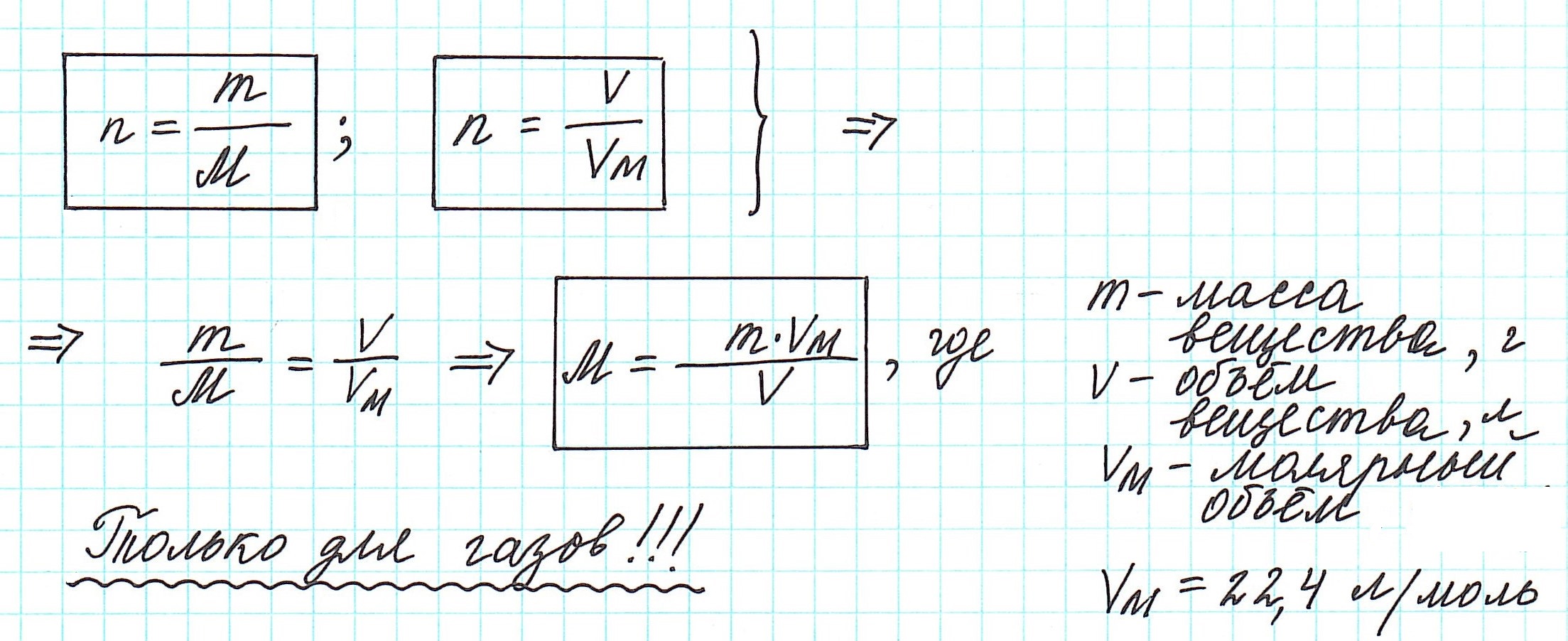Абсолютное значение — масса
Cтраница 1
Абсолютные значения масс т, т и ji находятся по точкам пересечения с осями Е / с или Р гипербол, проведенных через точки, изображающие соответствующие частицы.
[1]
Погрешность определения абсолютных значений масс электрона и атомных частиц ( в килограммах или граммах) выше, чем погрешность определения относительных масс ( в атомных единицах массы), так как ограничена погрешностью определения числа Авогадро.
[2]
В химии традиционно применяют не абсолютные значения масс, а относительные. За единицу относительных атомных масс с 1961 г. принята атомная единица массы ( сокращенно а.
[3]
Зная число Авогадро, можно найти абсолютное значение массы любого атома и оценить размеры атомов. Массу атома m находят делением массы моля элемента ( мольная масса) А на число Авогадро: m A / N &.
[4]
Зная число Авогадро, можно найти абсолютное значение массы любого атома и оценить размеры атомов. Массу атома m находят делением массы моля элемента ( мольная масса) А на число Авогадро: m AjN.
[5]
Погрешность показаний характеризует предельную погрешность при определении абсолютного значения массы груза, равного предельной нагрузке весов методом прямого взвешивания и включает погрешности гирь соответствующих классов.
[7]
Все вышеуказанное относилось к случаю применения гирь для определения абсолютного значения массы. Однако аэростатические силы могут сказываться и при относительных взвешиваниях, когда определяется относительное изменение массы навески.
[8]
Масс-спектрометриче-ские методы позволяют определять не только относительные, но и абсолютные значения масс атомов и молекул, хотя и со значительно меньшей точностью.
[10]
Материало — и металлоемкость измеряют, как правило, в абсолютных значениях массы ( т или кг) или с отнесением массы к единице продукции.
[11]
Случайные погрешности имеют превалирующее значение при относительных измерениях, когда устанавливается не абсолютное значение массы, а ее изменение в относительном ( например, процентном) выражении. Такие измерения типичны для некоторых видов химико-аналитических работ. При определении абсолютного значения массы сказываются неисключенные остатки систематических погрешностей и, в частности, погрешности гирь. В этой связи необходимо подчеркнуть, что погрешности определения абсолютного значения массы не могут быть меньше чем неучтенные погрешности гирь, которые используются для взвешивания или при градуировке весов.
[12]
Аналогичной формулой определяется и относительная атомная масса, надо лишь под тмол в (1.2) понимать абсолютное значение массы атома.
[13]
Для прецизионных измерений масс обычно применяется так называемый метод дублетов, в котором непосредственное измерение абсолютных значений масс заменяется измерением разности между двумя почти равными массами.
[14]
Атомы и молекулы вещества характеризуются определенной массой. Абсолютные значения массы атома и молекулы чрезвычайно малы и неудобны для расчетов. Поэтому для измерения масс атомов и молекул принята специальная единица — атомная единица массы.
[15]
Страницы:
1
2
Как вычислить молярную массу вещества? В каких единицах она измеряется?
А еще есть относительная молекулярная масса. Почему она относительная и численно равна молярной массе? Может быть это одно и то же?
Вот сколько вопросов возникает сразу в отношении такого простого на первый взгляд понятия, как молярная масса.
Разберемся по порядку и научимся ее определять.
Содержание:
1.Относительная атомная масса
2.Почему атомная масса дробная?
3.Относительная молекулярная масса
4.Количество вещества и молярная масса
5.Как вычислить молярную массу вещества
Относительная атомная масса
Огромнейший вклад в развитие и обоснование понятия относительная атомная масса внесли в разное время французский ученый Гей-Люссак, итальянский ученый А.Авогадро и шведский ученый Й.Я. Берцелиус.
Не углубляясь в историю вопроса, вспомним, что любой химический элемент представляет собой определенную разновидность атомов. Сегодня мы знаем, что атомы химических элементов имеют свои особые характеристики.
И самая главная из них, определяющая практически все остальные, это заряд ядра. А так как заряд ядра обусловлен присутствием в нем протонов, а заряд одного протона равен +1, то и количество протонов, соответственно, также является важнейшей характеристикой атомов химических элементов.
Основную массу атома составляет ядро, которое кроме протонов содержит еще и нейтроны. Масса последних сопоставима с массой первых. Оболочку атома составляют электроны.
По числу частиц в атоме, а точнее, по их суммарной массе, атомы химических элементов можно условно разделить на тяжелые и легкие. Например, легким элементом является водород, так как его атомы имеют самую маленькую массу. А свинец — это уже тяжелый элемент. Масса его атома в 302 раза тяжелее массы атома водорода.
Но тем не менее, как бы мы не делили все атомы на тяжелые или легкие, абсолютная масса (mA) каждого из них ничтожно мала, как мала и масса составляющих их частиц. Например,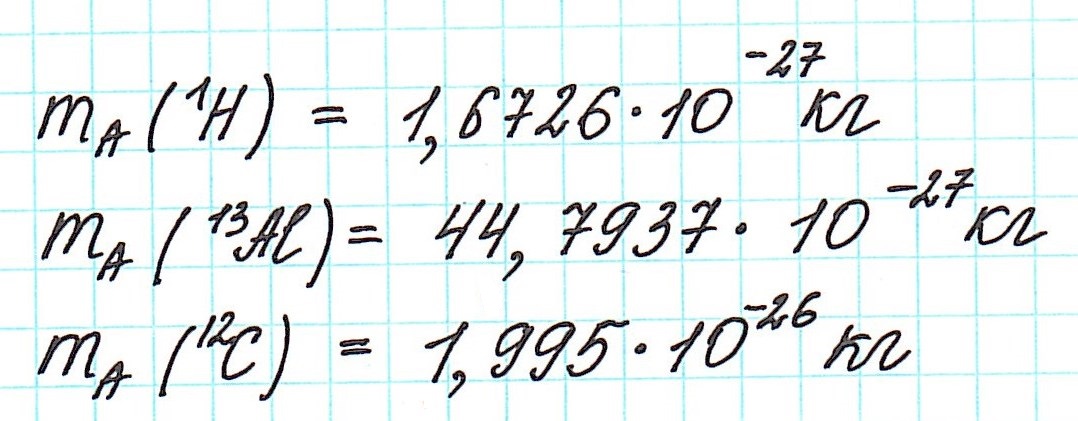
Величина, с которой сравнивают массу атома
Первоначально еще Дальтон сравнивал массы атомов с массой атома водорода, как самого легкого. Позднее появилась так называемая кислородная единица, равная 1/16 части массы атома кислорода. К ней перешли потому, что большинство атомов химических элементов образуют соединения с кислородом.
Однако, с развитием атомной физики и эта единица стала крайне неудобной. Все потому, что кислород в природе имеет несколько изотопов (а именно 3 устойчивых, всего же их 16). А изотопы, как известно, отличаются своей атомной массой. Из-за большого разнообразия изотопов и их различной устойчивости кислородная единица утратила свою актуальность.
В настоящее время (с 1961 года) общепринятой является углеродная единица, так называемая атомная единица массы (сокращенно а.е.м.). Она равна 1/12 части массы атома углерода (изотопа 12С).
Почему именно углерод? Да потому, что:
— у углерода всего 2 изотопа: 12С и 13С; причем первого 98,9%;
— количество органических веществ (их основу составляет, как известно, именно углерод) в сотни раз больше, чем неорганических;
— при переходе от кислородной единицы к углеродной уже посчитанные относительные атомные массы всех элементов изменились не существенно, что оказалось очень удобным.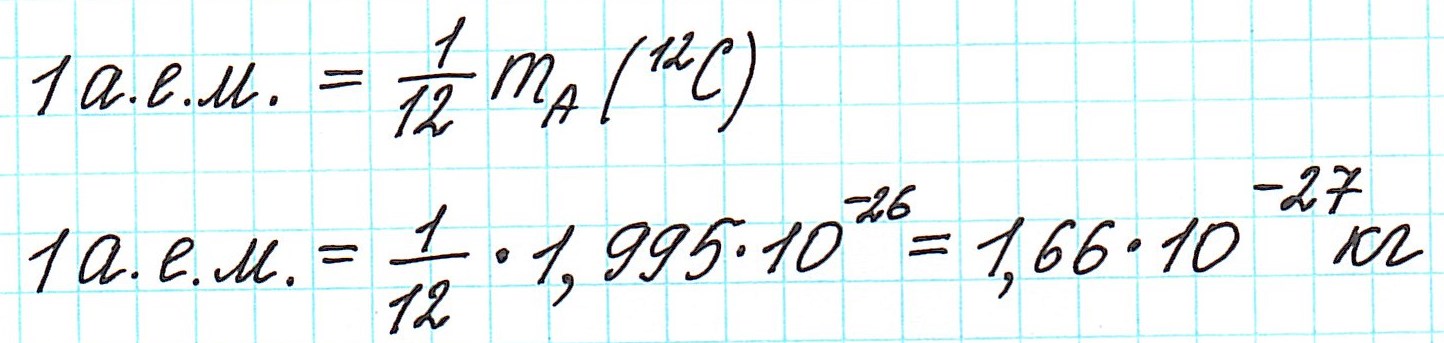
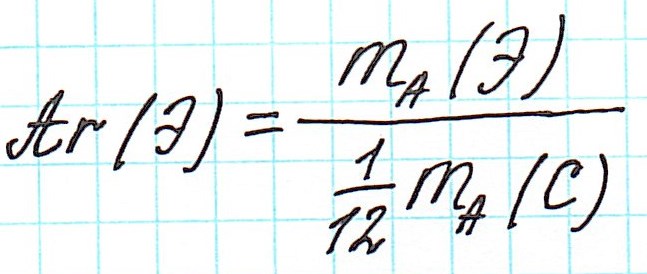
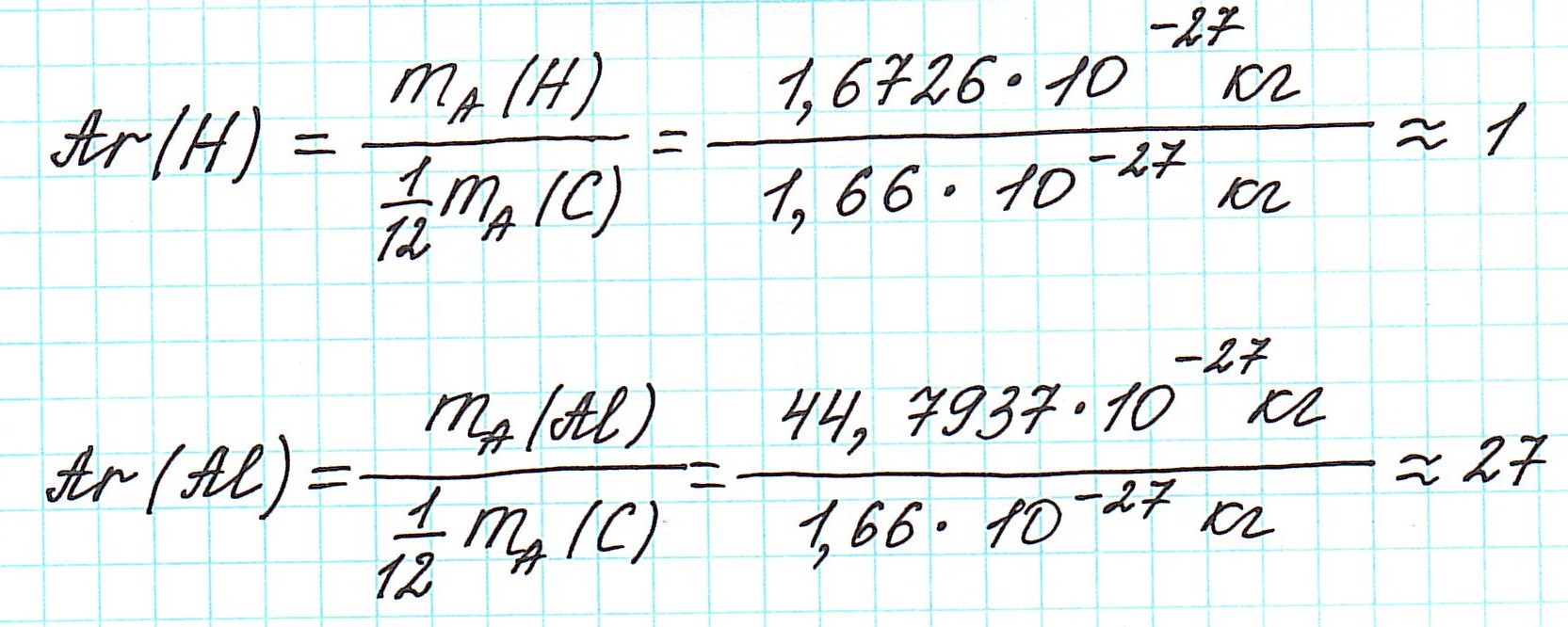
Почему атомная масса дробная?
Вернемся к строению атома.
Масса атома складывается из массы всех составляющих его частиц.
Массы протона и нейтрона приняты равными 1. А вот массой электрона обычно пренебрегают (по крайней мере в химии), так как даже относительная она безнадежно мала (0,0005485799090659(16) а.е.м.). То есть можно сказать, что масса атома определяется массой его ядра.
В составе ядра целое количество частиц. Например, в атоме одного из изотопов кислорода 8 протонов и 8 нейтронов. Значит, его Ar должна быть равна 16. Так почему же Ar представлена в периодической системе химических элементов в виде десятичной дроби? Для кислорода это Ar(О)=15,9994.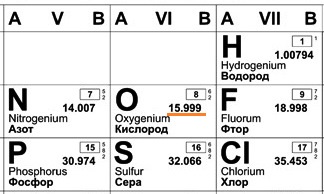
Например, химический элемент кислород в природе состоит на 99,76% из изотопа 16О, на 0,04% из изотопа 17О и на 0,20% из изотопа 18О. Таким образом, Ar для кислорода является средним значением, учитывающим относительное содержание его изотопов.
Относительная молекулярная масса
А как же найти относительную молекулярную массу?
Здесь не все так просто. Понятие «относительная молекулярная масса» не всегда применяется корректно. Правильнее было бы говорить о «формульной массе».
Дело в том, что молекулы характерны для веществ с ковалентными связями: вода H2O, серная кислота H2SO4, глюкоза C6H12O6 и т.д. И к ним в полной мере можно применить термин «относительная молекулярная масса».
Так как молекулы состоят из атомов, то относительная молекулярная масса (Mr) будет складываться из их относительных атомных масс. Например: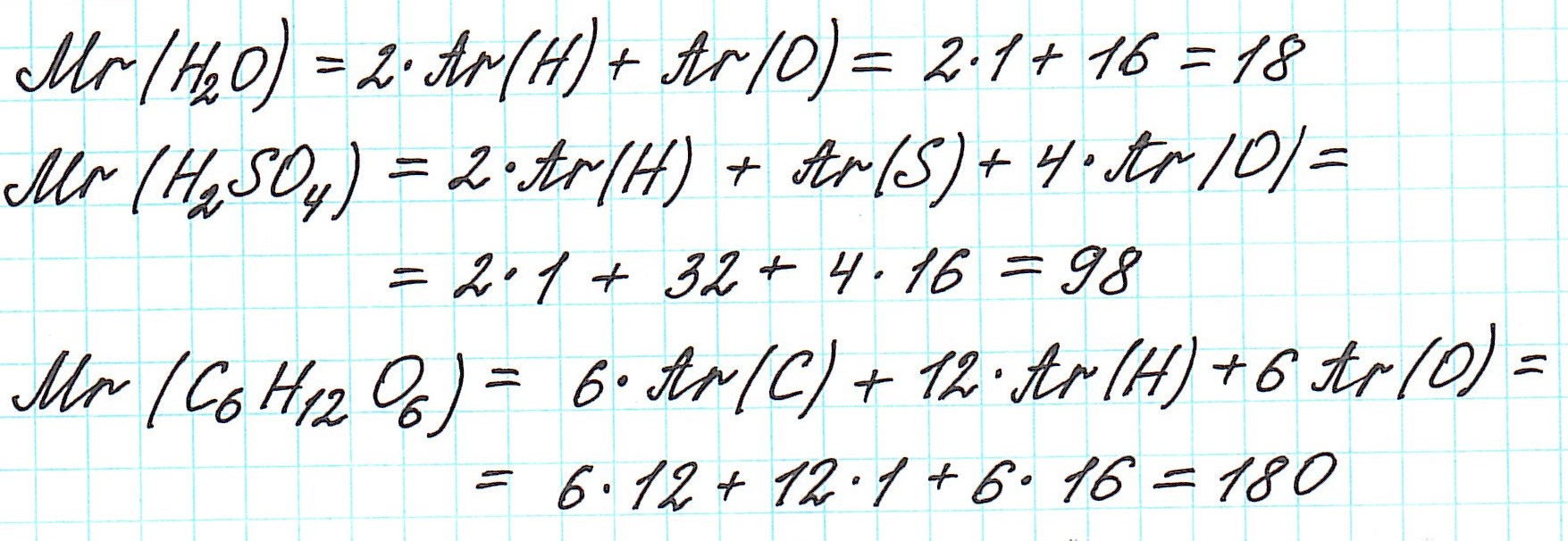
Например, формула NaCl показывает, что в кристалле хлорида натрия на один ион натрия Na+ приходится один ион хлора Cl—. На самом деле формула хлорида натрия должна выглядеть так: Na∞Cl∞. Поэтому запомним, что к ионным соединениям термины «молекула» и «молекулярная масса» не применимы.
В связи с этим для подобных веществ вычисляется формульная масса. А вычисляется она все по тому же принципу, что и молекулярная масса. Обозначается так же — Mr. Например, для хлорида натрия:
Точно так же, как относительную атомную массу (Ar), относительную молекулярную массу (Mr) будем сопоставлять с 1/12 частью атома изотопа углерода 12С.
В последующем говорим о Mr.
Количество вещества и молярная масса
В практических расчетах все-таки требуется вычислять массы, взятые в граммах, килограммах ато и в тоннах (если речь идет о каком-то производстве, например).
Как же поступают тогда?
Введена новая и тоже относительная величина – моль.
Точно было посчитано, что определенное количество атомов изотопа углерода 12С, а именно 6,02·1023, имеют массу ровно 12 г. Обратите внимание, что относительная молекулярная масса для этого же изотопа равна 12, но не грамм!
Количество вещества, которое содержит столько же частиц (атомов, ионов, молекул – в зависимости от строения), что и 12 г изотопа углерода 12С, назвали молем.
Один моль вещества (любого!) всегда содержит 6,02·1023 его частиц (постоянная Авогадро).
Ну, а так как атомы элементов отличаются по своей массе, то и 1 моль вещества тоже будет отличаться по массе.
Массу одного моля вещества называют молярной массой (М) и вычисляют в г/моль.
Таким образом, молярная масса и количество вещества связаны соотношением:
Можно также определить и такие отношения, связанные с количеством вещества:
Почему же относительная молекулярная и молярная массы равны?
Итак, относительная молекулярная и молярная массы, как следует из их определений – это не одно и то же.
Докажем, каким образом обе массы численно могут быть равны:
Как вычислить молярную массу вещества
Мы уже знаем, что относительная молекулярная масса складывается из относительных атомных масс.
При нахождении относительной молекулярной массы (Mr), а значит и молярной (М), выполняем следующие действия:
1) правильно записываем формулу вещества;
2) анализируем качественный состав (атомы каких элементов составляют вещество) и количественный состав (в каких количествах находятся эти атомы – смотрим по индексам, которые стоят справа внизу от знака химического элемента);
3) в периодической системе химических элементов находим элементы, атомы которых составляют вещество, и округляем относительную атомную массу, стоящую рядом со знаком элемента, до целого числа (! у хлора – до 35,5);
4) складываем относительные атомные массы всех элементов с учетом количества атомов.
Рассмотрим еще примеры:
Как вычислить молярную массу вещества, находящегося в газообразном состоянии
Определить молекулярную (а значит и молярную) массу газообразного вещества можно, используя закон Авогадро. Он гласит, что в равных объемах газов, взятых при одинаковой температуре, а также одинаковом давлении, содержится равное число молекул.
Это означает, что в данных условиях отношение масс газов друг к другу является отношением их молярных масс:


Запомните, что средняя молярная масса воздуха равна 29 г/моль.
Вычислить молярную массу вещества (а, значит, и относительную молекулярную), находящегося в газообразном состоянии, можно, используя молярный объем газа (VM):
Итак, подведем итог:
- Относительная молекулярная масса (Mr) показывает отношение массы молекулы к 1/12 части массы атома изотопа углерода 12С.
- Молярная масса (М) – масса одного моля вещества, равная отношению массы вещества к его количеству и выраженная в г/моль.
- Относительная молекулярная и молярная массы численно равны.
- Вычислить молярную массу вещества (и относительную молекулярную также) можно, используя значения относительных атомных масс, записанных в периодической системе.
Без вычисления молярной массы не обходится решение практически ни одной задачи. Если вы поняли, что такое молярная и относительная молекулярная массы и как их вычислять, но еще не умеете решать задачи с их применением, то самое время научиться.
Разбор простых типовых задач по химии в книге, которую вы можете совершенно БЕСПЛАТНО скачать здесь.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
Одной
из важнейших характеристик атомов
является его масса.
Абсолютной
называется масса атома, выраженная в
килограммах (граммах).
Абсолютная
масса атома (maтома)
величина чрезвычайно малая. Так, атом
легкого изотопа водорода (протия) имеет
массу 1,66 · 10–27
кг.
m(Н)
= 1,66 ·
10–27
кг, m(Н)
= 1,66 · 10–24
г,
атом
одного из изотопов кислорода имеет
массу 2,67 · 10–26
кг,
m(О) =
2,67 · 10–26
кг, m(О)
= 2,67 · 10–23
г,
атом
изотопа углерода 12С
имеет массу 1,99 · 10–26
кг,
m(С) =
1,99 · 10–26
кг, m(С)
= 1,99 · 10–23
г.
В
практических расчётах пользоваться
такими величинами крайне неудобно.
Поэтому обычно пользуются значениями
не абсолютных масс атомов, а значениями
относительных атомных
масс.
Относительная
атомная масса обозначается Ar,
индекс r – начальная буква
английского слова relative,
что значит относительный.
В
качестве единицы для измерения масс
атомов и молекул принята атомная
единица массы (а.е.м.).
Атомная
единица массы (а.е.м.) представляет собой
1/12 часть массы атома изотопа углерода
12С,
т.е.
а.е.м. =
=
· 1,99 · 10–26
кг =
· 1,99 · 10–23
г.
Относительная
атомная масса показывает, во сколько
раз масса атома данного элемента больше
1/12 части массы атома изотопа углерода
12С,
т. е. атомной единицы массы.
Относительная
атомная масса является безразмерной
величиной, но допускается обозначение
ее величины в атомных единицах массы
(а.е.м.). Например:
Таким
образом, значение относительной атомной
массы элемента водорода равно 1,001 или,
округленно,
Аr(Н)
≈ 1 а.е.м, а кислорода – Аr(O)
= 15,999 ≈ 16 а.е.м.
Значения
величин относительных атомных масс
элементов приведены в периодической
системе Д.И. Менделеева. Эти величины
представляют собой усредненное значение
массы атома какого-либо элемента с
учетом существующих в природе изотопов
этого элемента и их количества. Для
обычных расчетов следует пользоваться
округленными значениями относительных
атомных масс элементов (см.
табл. 4 приложения).
Аналогично
понятиям абсолютная масса атома и
относительная атомная масса можно
сформулировать понятия абсолютная
масса молекулы и относительная
молекулярная масса.
Абсолютная
масса молекулы (m)мол.
– масса
молекулы химического вещества, выраженная
в килограммах (граммах).
Относительная
молекулярная масса (Мr)
(или просто молекулярная масса) – масса
молекулы, выраженная в атомных единицах
массы.
Зная
химическую формулу соединения, можно
легко определить значение его молекулярной
массы, которая определяется как сумма
значений атомных масс всех элементов,
входящих в состав молекулы вещества.
Например,
относительная молекулярная масса серной
кислоты Мr(Н2SO4)
будет складываться из двух значений
относительных атомных масс элемента
водорода, одной относительной атомной
массы элемента серы и четырех относительных
атомных масс элемента кислорода:
Мr(Н2SO4)
= 2Аr (Н) + Аr
(S) + 4Аr(O)
= 2·1 + 32 + 4·16 = 98.
Таким
образом, значение молекулярной массы
серной кислоты равно 98 или 98 а.е.м.
Молекулярная
масса (относительная молекулярная
масса) показывает, во сколько раз масса
молекулы данного вещества больше 1/12
части массы атома углерода 12С.
В
приведенном выше примере значение
молекулярной массы серной кислоты равно
98 а.е.м., то есть молекула серной кислоты
имеет массу в 98 раз большую, чем 1/12 часть
массы атома углерода 12
С.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Как найти массу вещества
Окружающее нас пространство наполнено разными физическими телами, которые состоят из разных веществ с различной массой. Школьные курсы химии и физики, ознакомляющие с понятием и методом нахождения массы вещества, прослушали и благополучно забыли все, кто учился в школе. Но между тем теоретические знания, приобретенные когда-то, могут понадобиться в самый неожиданный момент.
1
Вычисление массы вещества с помощью удельной плотности вещества. Пример – имеется бочка на 200 литров. Нужно заполнить бочку любой жидкостью, скажем, светлым пивом. Как найти массу наполненной бочки? Используя формулу плотности вещества p=m/V, где p – удельная плотность вещества, m – масса, V – занимаемый объем, найти массу полной бочки очень просто:
- Меры объемов – кубические сантиметры, метры. То есть бочка на 200 литров имеет объем 2 м³.
- Мера удельной плотности находится с помощью таблиц и является постоянной величиной для каждого вещества. Измеряется плотность в кг/м³, г/см³, т/м³. Плотность пива светлого и других алкогольных напитков можно посмотреть на сайте. Она составляет 1025,0 кг/м³.
- Из формулы плотности p=m/V => m=p*V: m = 1025,0 кг/м³* 2 м³=2050 кг.
Бочка объемом 200 литров, полностью наполненная светлым пивом, будет иметь массу 2050 кг.
2
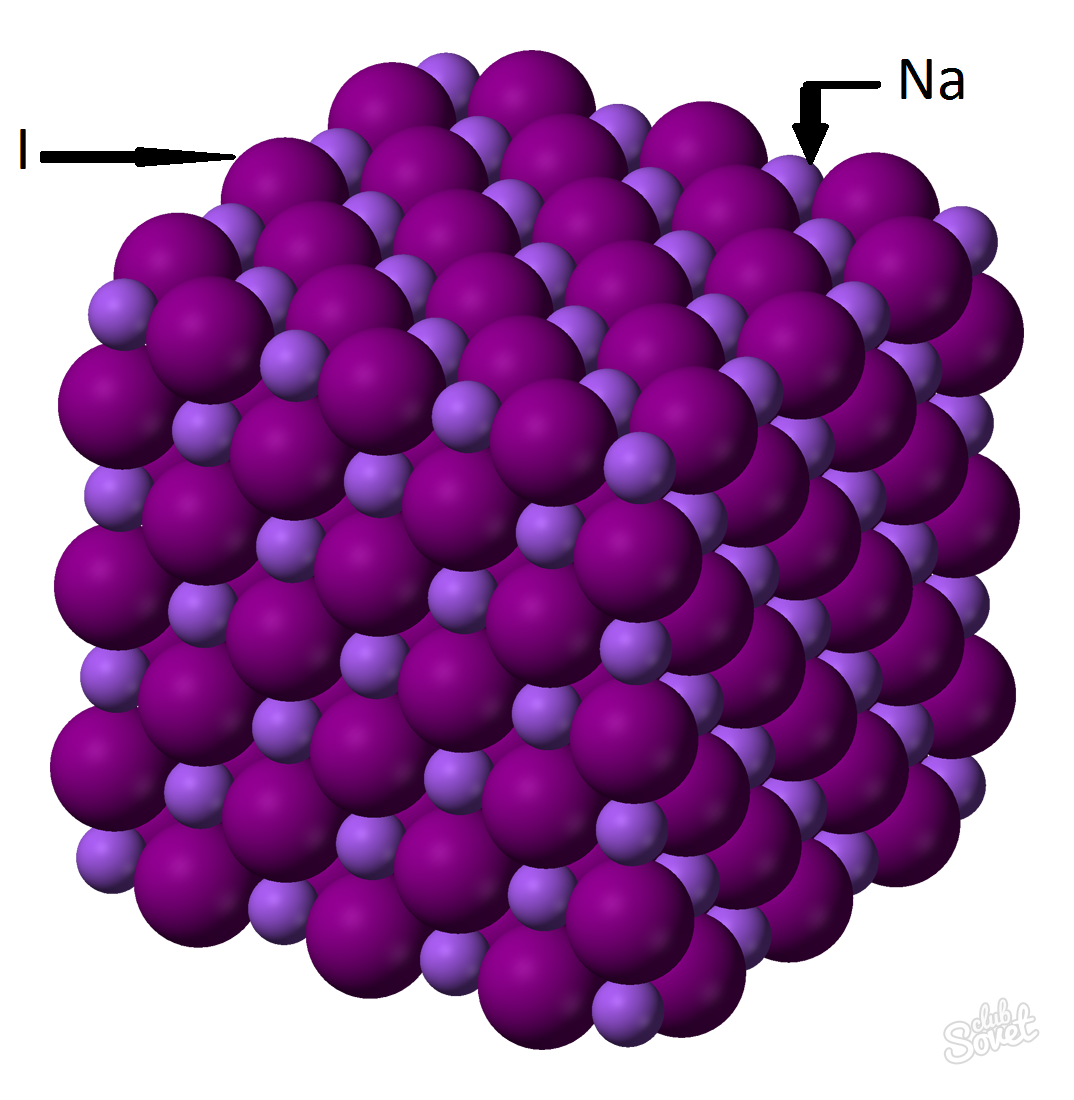
Нахождение массы вещества с помощью молярной массы. M (x)=m (x)/v (x) – это отношение массы вещества к его количеству, где M (x) – это молярная масса X, m (x) – масса X, v (x) – количество вещества X. Если в условии задачи прописывается только 1 известный параметр – молярная масса заданного вещества, то нахождение массы этого вещества не составит труда. Например, необходимо найти массу йодида натрия NaI количеством вещества 0,6 моль.
- Молярная масса исчисляется в единой системе измерений СИ и измеряется в кг/моль, г/моль. Молярная масса йодида натрия – это сумма молярных масс каждого элемента: M (NaI)=M (Na)+M (I). Значение молярной массы каждого элемента можно вычислить по таблице, а можно с помощью онлайн-калькулятора на сайте: M (NaI)=M (Na)+M (I)=23+127=150 (г/моль).
- Из общей формулы M (NaI)=m (NaI)/v (NaI) => m (NaI)=v (NaI)*M (NaI)= 0,6 моль*150 г/моль=90 грамм.
Масса йодида натрия (NaI) с массовой долей вещества 0,6 моль составляет 90 грамм.
3
Нахождение массы вещества по его массовой доле в растворе. Формула массовой доли вещества ω=[m (вещества)/m (раствора)]*100%, где ω – массовая доля вещества, а m (вещества) и m (раствора) – массы, измеряемые в граммах, килограммах. Общая доля раствора всегда принимается за 100%, иначе будут погрешности в вычислении. Несложно из формулы массовой доли вещества вывести формулу массы вещества: m (вещества)=[ω*m (раствора)] /100%. Однако есть некоторые особенности изменения состава раствора, которые нужно учитывать при решении задач на эту тему:
- Разбавление раствора водой. Масса вещества растворенного X не изменяется m (X)=m’(X). Масса раствора увеличивается на массу добавленной воды m’ (р)=m (р)+m (H2O).
- Выпаривание воды из раствора. Масса растворенного вещества X не изменяется m (X)=m’ (X). Масса раствора уменьшается на массу выпаренной воды m’ (р)=m (р)-m (H2O).
- Сливание двух растворов. Массы растворов, а также массы растворенного вещества X при смешивании складываются: m’’ (X)=m (X)+m’ (X). m’’ (р)=m (р)+m’ (р).
- Выпадение кристаллов. Массы растворенного вещества X и раствора уменьшаются на массу выпавших кристаллов: m’ (X)=m (X)-m (осадка), m’ (р)=m (р)-m (осадка).
4
Алгоритм нахождения массы продукта реакции (вещества), если известен выход продукта реакции. Выход продукта находится по формуле η=[m (x практическая)/m (x теоретическая)]*100%, где m (x практическая) – масса продукта х, которая получена в результате практического процесса реакции, m (x теоретическая) – рассчитанная масса вещества х. Отсюда m (x практическая)=[η*m (x теоретическая)]/100% и m (x теоретическая)=[m (x практическая)*100%]/η. Теоретическая масса получаемого продукта всегда больше практической, в связи с погрешностью реакции, и составляет 100%. Если в задаче не дается масса продукта, полученного в практической реакции, значит, она принимается за абсолютную и равна 100%.
Варианты нахождение массы вещества – небесполезный курс школьного обучения, а вполне применяемые на практике способы. Каждый сможет без труда найти массу необходимого вещества, применяя вышеперечисленные формулы и пользуясь предлагаемыми таблицами. Для облегчения задания прописывайте все реакции, их коэффициенты.