Физические свойства алюминия
Алюминий — мягкий, легкий, серебристо-белый металл с высокой тепло- и электропроводностью. Температура плавления 660°C.
По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния среди всех атомов и 1-е место — среди металлов.
К достоинствам алюминия и его сплавов следует отнести его малую плотность (2,7 г/см3), сравнительно высокие прочностные характеристики, хорошую тепло- и электропроводность, технологичность, высокую коррозионную стойкость. Совокупность этих свойств позволяет отнести алюминий к числу важнейших технических материалов.
Алюминий и его сплавы делятся по способу получения на деформируемые, подвергаемые обработке давлением и литейные, используемые в виде фасонного литья; по применению термической обработки — на термически не упрочняемые и термически упрочняемые, а также по системам легирования.
Получение
Впервые алюминий был получен Гансом Эрстедом в 1825 году. Современный метод получения разработали независимо друг от друга американец Чарльз Холл и француз Поль Эру. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием графитовых электродов. Такой метод получения требует больших затрат электроэнергии, и поэтому оказался востребован только в XX веке.
Применение
Алюминий широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — легкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной пленкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки.
Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий).
Электропроводность алюминия сравнима с медью, при этом алюминий дешевле. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Правда, у алюминия как электротехнического материала есть неприятное свойство — из-за прочной оксидной пленки его тяжело паять.
Благодаря комплексу свойств широко распространен в тепловом оборудовании.
Внедрение алюминиевых сплавов в строительстве уменьшает металлоемкость, повышает долговечность и надежность конструкций при эксплуатации их в экстремальных условиях (низкая температура, землетрясение и т.п.).
Алюминий находит широкое применение в различных видах транспорта. На современном этапе развития авиации алюминиевые сплавы являются основными конструкционными материалами в самолетостроении. Алюминий и сплавы на его основе находят все более широкое применение в судостроении. Из алюминиевых сплавов изготовляют корпусы судов, палубные надстройки, коммуникацию и различного рода судовое оборудование.
Идут исследования по разработке пенистого алюминия как особо прочного и легкого материала.
Драгоценный алюминий
В настоящее время алюминий является одним из самых популярных и нашедших широкое применение металлов. С самого момента открытия в середине XIX века его считали одним из ценнейших благодаря удивительным качествам: белый как серебро, легкий по весу и не подверженный воздействию окружающей среды. Стоимость его была выше цен на золото. Не удивительно, что в первую очередь алюминий нашел свое применение в создании ювелирных изделий и дорогих декоративных элементов.
В 1855 г. на Универсальной выставке в Париже алюминий был самой главной достопримечательностью. Изделия из алюминия располагались в витрине, соседствующей с бриллиантами французской короны. Постепенно зародилась определенная мода на алюминий. Его считали благородным малоизученным металлом, используемым исключительно для создания произведений искусства.
Наиболее часто алюминий использовали ювелиры. При помощи особой обработки поверхности ювелиры добивались наиболее светлого цвета металла, из-за чего его часто приравнивали к серебру. Но в сравнении с серебром, алюминий обладал более мягким блеском, чем обуславливалась еще большая любовь к нему ювелиров.
Так как химические и физические свойства алюминия сначала были слабо изучены, ювелиры сами изобретали новые техники его обработки. Алюминий технически легко обрабатывать, этот мягкий металл позволяет создавать отпечатки любых узоров, наносить рисунки и создавать желаемой формы изделия. Алюминий покрывался золотом, полировался и доводился до матовых оттенков.
Но со временем алюминий стал падать цене. Если в 1854-1856 годах стоимость одного килограмма алюминия составляла 3 тысячи старых франков, то в середине 1860-х годов за килограмм этого металла давали уже около ста старых франков. Впоследствии из-за низкой стоимости алюминий вышел из моды.
В настоящее время самые первые алюминиевые изделия представляют большую редкость. Большинство из них не пережило обесценивания металла и было заменено серебром, золотом и другими драгоценными металлами и сплавами. В последнее время вновь наблюдается повышенный интерес к алюминию у специалистов. Этот металл стал темой отдельной выставки , организованной в 2000 году Музеем Карнеги в Питсбурге. Во Франции расположен Институт истории алюминия, который в частности занимается исследованием первых ювелирных изделий из этого металла.
В Советском союзе из алюминия делали общепитовские приборы, чайники и т.д. И не только. Первый советский спутник был выполнен из алюминиевого сплава. Другой потребитель алюминия — электротехническая промышленность: из него делаются провода высоковольтных линий передач, обмотки моторов и трансформаторов, кабели, цоколи ламп, конденсаторы и многие другие изделия. Кроме того, порошок алюминия применяют во взрывчатых веществах и твердом топливе для ракет, используя его свойство быстро воспламеняться: если бы алюминий не покрывался тончайшей оксидной пленкой, то мог бы вспыхивать на воздухе.
Последнее изобретение — пеноалюминий, т.н. «металлический поролон», которому предсказывают большое будущее.
Кусок чистого алюминия
Алюминий — очень редкий минерал семейства меди-купалита подкласса металлов и интерметаллидов класса самородных элементов. Преимущественно в виде микроскопических выделений сплошного мелкозернистого строения. Может образовывать пластинчатые или чешуйчатые кристаллы до 1 мм., отмечены нитевидные кристаллы длиной до 0,5 мм. при толщине нитей несколько мкм. Лёгкий парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке.
- Структура
- Свойства
- Запасы и добыча
- Происхождение
- Применение
- Классификация
- Физические свойства
- Оптические свойства
- Кристаллографические свойства
СТРУКТУРА
Кубическая гранецентрированная структура. 4 оранжевых атома
Кристаллическая решетка алюминия — гранецентрированный куб, которая устойчива при температуре от 4°К до точки плавления. В алюминии нет аллотропических превращений, т.е. его строение постоянно. Элементарная ячейка состоит из четырех атомов размером 4,049596×10-10 м; при 25 °С атомный диаметр (кратчайшее расстояние между атомами в решетке) составляет 2,86×10-10 м, а атомный объем 9,999×10-6 м3/г-атом.
Примеси в алюминии незначительно влияют на величину параметра решетки. Алюминий обладает большой химической активностью, энергия образования его соединений с кислородом, серой и углеродом весьма велика. В ряду напряжений он находится среди наиболее электроотрицательных элементов, и его нормальный электродный потенциал равен -1,67 В. В обычных условиях, взаимодействуя с кислородом воздуха, алюминий покрыт тонкой (2-10-5 см), но прочной пленкой оксида алюминия А1203, которая защищает от дальнейшего окисления, что обусловливает его высокую коррозионную стойкость. Однако при наличии в алюминии или окружающей среде Hg, Na, Mg, Ca, Si, Си и некоторых других элементов прочность оксидной пленки и ее защитные свойства резко снижаются.
СВОЙСТВА
Самородный алюминий. Поле зрения 5 x 4 мм. Азербайджан, Гобустанский район, Каспийское море, Хере-Зиря или остров Булла
Алюминий — мягкий, легкий, серебристо-белый металл с высокой тепло- и электропроводностью, парамагнетик. Температура плавления 660°C. К достоинствам алюминия и его сплавов следует отнести его малую плотность (2,7 г/см3), сравнительно высокие прочностные характеристики, хорошую тепло- и электропроводность, технологичность, высокую коррозионную стойкость. Совокупность этих свойств позволяет отнести алюминий к числу важнейших технических материалов. Он легко вытягивается в проволоку и прокатывается в тонкие листы. Алюминий химически активен (на воздухе покрывается защитной оксидной пленкой – оксидом алюминия.) надежно предохраняет металл от дальнейшего окисления. Но если порошок алюминия или алюминиевую фольгу сильно нагреть, то металл сгорает ослепительным пламенем, превращаясь в оксид алюминия. Алюминий растворяется даже в разбавленных соляной и серной кислотах, особенно при нагревании. А вот в сильно разбавленной и концентрированной холодной азотной кислоте алюминий не растворяется. При действии на алюминий водных растворов щелочей слой оксида растворяется, причем образуются алюминаты – соли, содержащие алюминий в составе аниона.
ЗАПАСЫ И ДОБЫЧА
Кусочки алюминия
По распространённости в земной коре Земли занимает 1-е место среди металлов и 3-е место среди элементов, уступая только кислороду и кремнию. Массовая концентрация алюминия в земной коре, по данным различных исследователей, оценивается от 7,45 до 8,14%.
Современный метод получения, процесс Холла—Эру был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых анодных электродов. Такой метод получения требует очень больших затрат электроэнергии, и поэтому получил промышленное применение только в XX веке.
ПРОИСХОЖДЕНИЕ
Аллюминий, агрегированный с коркой байерита на поверхности. Узбекистан, Навойская область, Учкудук
Вследствие высокой химической активности он не встречается в чистом виде, а лишь в составе различных соединений. Так, например, известно множество руд, минералов, горных пород, в состав которых входит алюминий. Однако добывается он только из бокситов, содержание которых в природе не слишком велико. Самые распространенные вещества, содержащие рассматриваемый металл: полевые шпаты; бокситы; граниты; кремнезем; алюмосиликаты; базальты и прочие. В небольшом количестве алюминий обязательно входит в состав клеток живых организмов. Некоторые виды плаунов и морских обитателей способны накапливать этот элемент внутри своего организма в течение жизни.
ПРИМЕНЕНИЕ
Украшение из алюминия
Широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость. Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 4 раза дешевле за килограмм, но, за счёт в 3,3 раза меньшей плотности, для получения равного сопротивления его нужно приблизительно в 2 раза меньше по весу. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при напылении проводников на поверхности кристаллов микросхем.
Когда алюминий был очень дорог, из него делали разнообразные ювелирные изделия. Так, Наполеон III заказал алюминиевые пуговицы, а Менделееву в 1889 г. были подарены весы с чашами из золота и алюминия. Мода на ювелирные изделия из алюминия сразу прошла, когда появились новые технологии его получения, во много раз снизившие себестоимость. Сейчас алюминий иногда используют в производстве бижутерии.
Алюминий (англ. Aluminium) – Al
| Молекулярный вес | 26.98 г/моль |
| Происхождение названия | от латинского alumen |
| IMA статус | утверждён в 1978 |
КЛАССИФИКАЦИЯ
Hey’s CIM Ref1.21
| Strunz (8-ое издание) | 1/A.03-05 |
| Nickel-Strunz (10-ое издание) | 1.AA.05 |
| Dana (7-ое издание) | 1.1.22.1 |
| Dana (8-ое издание) | 1.1.1.5 |
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | серовато-белый, белый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 2-3 |
| Прочность | ковкий |
| Плотность (измеренная) | 2.7 г/см3 |
| Радиоактивность (GRapi) | 0 |
ОПТИЧЕСКИЕ СВОЙСТВА
Плеохроизмне плеохроирует
| Тип | изотропный |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
| Магнетизм | парамагнетик |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | (4/m 3 2/m) – изометричная гексаоктаэдральная |
| Пространственная группа | F m3m, P m3m |
| Сингония | кубическая |
| Параметры ячейки | a = 4.04Å |
Интересные статьи:

Ирина Морозли
Молярная концентрация вещества рассчитывается по формуле Cм=n/V(р-ра) , где V — объём раствора (в литрах) ,
а «n» — количество вещества (моль) .
В свою очередь, количество вещества легко рассчитать по формуле: n=m/M, где М — молярная масса сульфата алюминия Al2(SO4)3
Алюминий (Al, лат. aluminium) — элемент 13-й группы периодической таблицы химических элементов (по устаревшей классификации — элемент главной подгруппы III группы), третьего периода, с атомным номером 13. Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости химический элемент в земной коре (после кислорода и кремния).
Простое вещество алюминий — лёгкий парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия.
|
|
|
| Название, символ, номер | Алюминий / Aluminium (Al), 13 |
|---|---|
| Группа, период, блок | 13, 3, |
| Атомная масса (молярная масса) |
26,9815386(8) а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s2 3p1 |
| Электроны по оболочкам | 2, 8, 3 |
| Радиус атома | 143 пм |
| Ковалентный радиус | 121 ± 4 пм |
| Радиус Ван-дер-Ваальса | 184 пм |
| Радиус иона | 51 (+3e) пм |
| Электроотрицательность | 1,61 (шкала Полинга) |
| Электродный потенциал | −1,66 В |
| Степени окисления | 0; +3 |
| Энергия ионизации |
1‑я: 577,5 (5,984) кДж/моль (эВ) 2‑я: 1816,7 (18,828) кДж/моль (эВ) |
| Термодинамическая фаза | Твёрдое вещество |
| Плотность (при н. у.) | 2,6989 г/см³ |
| Температура плавления | 660 °C, 933,5 K |
| Температура кипения | 2518,82 °C, 2792 K |
| Уд. теплота плавления | 10,75 кДж/моль |
| Уд. теплота испарения | 284,1 кДж/моль |
| Молярная теплоёмкость | 24,35 24,2 Дж/(K·моль) |
| Молярный объём | 10,0 см³/моль |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 4,050 Å |
| Температура Дебая | 394 K |
| Теплопроводность | (300 K) 237 Вт/(м·К) |
| Скорость звука | 5200 м/с |
| Номер CAS | 7429-90-5 |
Кодовый символ, указывающий, что алюминий может быть вторично переработан
Содержание
- 1 История
- 2 Нахождение в природе
- 2.1 Распространённость
- 2.2 Природные соединения алюминия
- 2.3 Изотопы алюминия
- 3 Получение
- 4 Физические свойства
- 5 Химические свойства
- 6 Производство и рынок
- 7 Применение
- 7.1 В качестве восстановителя
- 7.2 Сплавы на основе алюминия
- 7.3 Алюминий как добавка в другие сплавы
- 7.4 Ювелирные изделия
- 7.5 Столовые приборы
- 7.6 Стекловарение
- 7.7 Пищевая промышленность
- 7.8 Военная промышленность
- 7.9 Алюминий и его соединения в ракетной технике
- 7.10 Алюмоэнергетика
- 8 Алюминий в мировой культуре
- 9 Токсичность

История
Впервые алюминий был получен датским физиком Гансом Эрстедом в 1825 году действием амальгамы калия на хлорид алюминия с последующей отгонкой ртути.
Название элемента образовано от лат. alumen — квасцы.
До развития промышленного электролитического способа получения алюминия этот металл был дороже золота. В 1889 году британцы, желая почтить богатым подарком великого русского химика Д. И. Менделеева, подарили ему аналитические весы у которых чашки были изготовлены из золота и алюминия.
Нахождение в природе
Распространённость
По распространённости в земной коре занимает 1-е место среди металлов и 3-е место среди элементов, уступая только кислороду и кремнию. Массовая концентрация алюминия в земной коре, по данным различных исследователей, оценивается от 7,45 до 8,14 %.
Природные соединения алюминия
В природе алюминий, в связи с высокой химической активностью, встречается почти исключительно в виде соединений. Некоторые из природных минералов алюминия:
- Бокситы — Al2O3 · H2O (с примесями SiO2, Fe2O3, CaCO3)
- Нефелины — KNa3[AlSiO4]4
- Алуниты — (Na,K)2SO4·Al2(SO4)3·4Al(OH)3
- Глинозёмы (смеси каолинов с песком SiO2, известняком CaCO3, магнезитом MgCO3)
- Корунд (сапфир, рубин, наждак) — Al2O3
- Полевые шпаты — (K,Na)2O·Al2O3·6SiO2, Ca[Al2Si2O8]
- Каолинит — Al2O3·2SiO2 · 2H2O
- Берилл (изумруд, аквамарин) — 3ВеО · Al2О3 · 6SiO2
- Хризоберилл (александрит) — BeAl2O4.
Тем не менее, в некоторых специфических восстановительных условиях (жерла вулканов) найдены ничтожные количества самородного металлического алюминия.
В природных водах алюминий содержится в виде малотоксичных химических соединений, например, фторида алюминия. Вид катиона или аниона зависит, в первую очередь, от кислотности водной среды. Концентрации алюминия в водоёмах России колеблются от 0,001 до 10 мг/л. В морской воде его концентрация 0,01 мг/л.
Изотопы алюминия
Основная статья: Изотопы алюминия
Природный алюминий состоит практически полностью из единственного стабильного изотопа 27Al с ничтожными следами 26Al, наиболее долгоживущего радиоактивного изотопа с периодом полураспада 720 тыс. лет, образующегося в атмосфере при расщеплении ядер аргона 40Arпротонами космических лучей с высокими энергиями.
Получение
Алюминий образует прочную химическую связь с кислородом. По сравнению с другими металлами, восстановление алюминия до металла из природных оксидов и алюмосиликатов более сложно в связи с его высокой реакционной способностью и с высокой температурой плавления всех его руд, например таких, как бокситы, корунды.
Обычное восстановление до металла обжигом оксида с углеродом (как например, в металлургических процессах восстановления железа) — невозможно, так как сродство к кислороду у алюминия выше, чем у углерода.
Возможно получение алюминия посредством неполного восстановления алюминия с образованием промежуточного продукта — карбида алюминия Al4C3, который далее подвергается разложению при 1900—2000 °С с образованием металлического алюминия. Этот способ производства алюминия изучается, предполагается, что он более выгоден, чем классический электролитический способ производства алюминия процесс Холла — Эру, так как требует меньших энергозатрат и приводит к образованию меньшего количества CO2.
Современный метод получения, процесс Холла — Эру, был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых анодных электродов. Такой метод получения требует очень больших затрат электроэнергии и поэтому получил промышленное применение только в XX веке.
Электролиз в расплаве криолита:
-
- 2Al2O3 →Na3AlF6 4Al + 3O2
Для производства 1000 кг чернового алюминия требуется 1920 кг глинозёма, 65 кг криолита, 35 кг фторида алюминия, 600 кг анодных графитовых электродов и около 17 МВт·ч электроэнергии (~61 ГДж).
Лабораторный способ получения алюминия предложил Фридрих Вёлер в 1827 году восстановлением металлическим калием безводного хлорида алюминия (реакция протекает при нагревании без доступа воздуха):
-
- AlCl3 + 3K → 3KCl + Al
Физические свойства
Микроструктура алюминия на протравленной поверхности слитка, чистотой 99,9998 %, размер видимого сектора около 55×37 мм
- Металл серебристо-белого цвета, лёгкий
- плотность — 2712 кг/м³
- температура плавления у технического алюминия — 658 °C, у алюминия высокой чистоты — 660 °C
- удельная теплота плавления — 390 кДж/кг
- температура кипения — 2518,8 °C
- удельная теплота испарения — 10,53 МДж/кг
- удельная теплоёмкость — 897 Дж/кг·K
- временное сопротивление литого алюминия — 10—12 кг/мм², деформируемого — 18—25 кг/мм², сплавов — 38—42 кг/мм²
- Твёрдость по Бринеллю — 24—32 кгс/мм²
- высокая пластичность: у технического — 35 %, у чистого — 50 %, прокатывается в тонкий лист и даже фольгу
- Модуль Юнга — 70 ГПа
- Коэффициент Пуассона — 0,34
- Алюминий обладает высокой электропроводностью (37·106 См/м — 65 % от электропроводности меди) и теплопроводностью (203,5 Вт/(м·К)), обладает высокой светоотражательной способностью.
- Слабый парамагнетик.
- Температурный коэффициент линейного расширения 24,58⋅10−6 К−1 (20—200 °C).
- Удельное сопротивление 0,0262—0,0295 Ом·мм²/м
- Температурный коэффициент электрического сопротивления 4,3⋅10−3 K−1. Алюминий переходит в сверхпроводящее состояние при температуре 1,2 кельвина.
Алюминий образует сплавы почти со всеми металлами. Наиболее известны сплавы с медью и магнием (дюралюминий) и кремнием (силумин).
Химические свойства
При нормальных условиях алюминий покрыт тонкой и прочной оксидной плёнкой и потому не реагирует с классическими окислителями: с O2, HNO3 (без нагревания), H2SO4(конц), но легко реагирует с HCl и H2SO4(разб). Благодаря этому алюминий практически не подвержен коррозии и потому широко востребован современной промышленностью. Однако при разрушении оксидной плёнки (например, при контакте с растворами солей аммония NH4+, горячими щелочами или в результате амальгамирования), алюминий выступает как активный металл-восстановитель. Не допустить образования оксидной плёнки можно, добавляя к алюминию такие металлы, как галлий, индий или олово. При этом поверхность алюминия смачивают легкоплавкие эвтектики на основе этих металлов.
Легко реагирует с простыми веществами:
- с кислородом, образуя оксид алюминия:
-
- 4Al + 3O2 → 2Al2O3
- с галогенами при комнатной температуре (кроме фтора), образуя хлорид, бромид или иодид алюминия:
-
- 2Al + 3Hal2 → 2AlHal3(Hal = Cl , Br , I )
- с другими неметаллами реагирует при нагревании:
-
- со фтором, образуя фторид алюминия:
-
- 2Al + 3F2 → 2AlF3
-
- с серой, образуя сульфид алюминия:
-
- 2Al + 3S → Al2S3
-
- с азотом, образуя нитрид алюминия:
-
- 2Al + N2 → 2AlN
-
- с углеродом, образуя карбид алюминия:
-
- 4Al + 3C → Al4C3
Сульфид и карбид алюминия полностью гидролизуются:
-
- Al2S3 + 6H2O → 2Al(OH)3 + 3H2S
-
- Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
Со сложными веществами:
- с водой (после удаления защитной оксидной плёнки, например, амальгамированием или растворами горячей щёлочи):
-
- 2Al + 6H2O → 2Al(OH)3 + 3H2
- со щелочами (с образованием тетрагидроксоалюминатов и других алюминатов):
-
- 2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
-
- 2Al + 6NaOH → 2Na3AlO3 + 3H2
- Легко растворяется в соляной и разбавленной серной кислотах:
-
- 2Al + 6HCl → 2AlCl3 + 3H2
-
- 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
- При нагревании растворяется в кислотах — окислителях, образующих растворимые соли алюминия:
-
- 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O
-
- Al + 6HNO3 → Al(NO3)3 + 3NO2 + 3H2O
- восстанавливает металлы из их оксидов (алюминотермия):
-
- 8Al + 3Fe3O4 → 4Al2O3 + 9Fe
-
- 2Al + Cr2O3 → Al2O3 + 2Cr
Производство и рынок
Основная статья: Алюминиевая промышленность
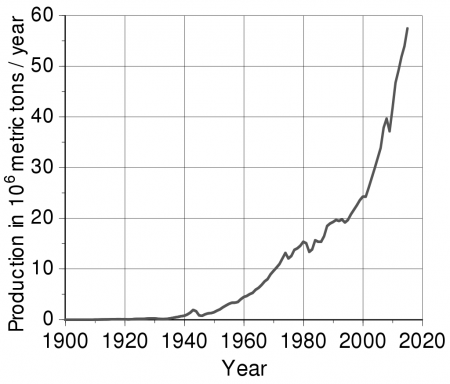
Производство алюминия в миллионах тонн
Достоверных сведений о получении алюминия до XIX века нет. Встречающееся иногда со ссылкой на «Естественную историю» Плиния утверждение, что алюминий был известен при императоре Тиберии, основано на неверном толковании источника.
В 1825 году датский физик Ганс Христиан Эрстед получил несколько миллиграммов металлического алюминия, а в 1827 году Фридрих Вёлер смог выделить крупинки алюминия, которые, однако, на воздухе немедленно покрывались тончайшей плёнкой оксида алюминия.
До конца XIX века алюминий в промышленных масштабах не производился.
Только в 1854 году Анри Сент-Клер Девиль (его исследования финансировал Наполеон III, рассчитывая, что алюминий пригодится его армии) изобрёл первый способ промышленного производства алюминия, основанный на вытеснении алюминия металлическим натрием из двойного хлорида натрия и алюминия NaCl·AlCl3. В 1855 году был получен первый слиток металла массой 6—8 кг. За 36 лет применения, с 1855 по 1890 год, способом Сент-Клер Девиля было получено 200 тонн металлического алюминия. В 1856 году он же получил алюминий электролизом расплава хлорида натрия-алюминия.
В 1885 году был построен завод по производству алюминия в немецком городе Гмелингеме, работающий по технологии, предложенной Николаем Бекетовым. Технология Бекетова мало чем отличалась от способа Девиля, но была проще и заключалась во взаимодействии между криолитом (Na3AlF6) и магнием. За пять лет на этом заводе было получено около 58 т алюминия — более четверти всего мирового производства металла химическим путём в период с 1854 по 1890 год.
Метод, изобретённый почти одновременно Чарльзом Холлом в США и Полем Эру во Франции (1886 год) и основанный на получении алюминия электролизом глинозёма, растворённого в расплавленном криолите, положил начало современному способу производства алюминия. С тех пор, в связи с улучшением электротехники, производство алюминия совершенствовалось. Заметный вклад в развитие производства глинозёма внесли русские учёные К. И. Байер, Д. А. Пеняков, А. Н. Кузнецов, Е. И. Жуковский, А. А. Яковкин и др.
Первый алюминиевый завод в России был построен в 1932 году в городе Волхов. Металлургическая промышленность СССР в 1939 году производила 47,7 тыс. тонн алюминия, ещё 2,2 тыс. тонн импортировалось.
Вторая мировая война значительно стимулировала производство алюминия. Так, в 1939 году общемировое его производство, без учёта СССР, составляло 620 тыс. т, но уже к 1943 году выросло до 1,9 млн т.
К 1956 году в мире производилось 3,4 млн т первичного алюминия, в 1965 году — 5,4 млн т, в 1980 году — 16,1 млн т, в 1990 году — 18 млн т.
В 2007 году в мире было произведено 38 млн т первичного алюминия, а в 2008 — 39,7 млн т. Лидерами производства являлись:
- КНР (в 2007 году произвёл 12,60 млн т, а в 2008 — 13,50 млн т)
- Россия (3,96/4,20)
- Канада (3,09/3,10)
- США (2,55/2,64)
- Австралия (1,96/1,96)
- Бразилия (1,66/1,66)
- Индия (1,22/1,30)
- Норвегия (1,30/1,10)
- ОАЭ (0,89/0,92)
- Бахрейн (0,87/0,87)
- ЮАР (0,90/0,85)
- Исландия (0,40/0,79)
- Германия (0,55/0,59)
- Венесуэла (0,61/0,55)
- Мозамбик (0,56/0,55)
- Таджикистан (0,42/0,42)
В 2016 году было произведено 59 млн тонн алюминия
См. также: Список стран по выплавке алюминия
На мировом рынке запас составляет 2,224 млн т., а среднесуточное производство — 128,6 тыс. т. (2013.7).
В России монополистом по производству алюминия является компания «Российский алюминий», на которую приходится около 13 % мирового рынка алюминия и 16 % глинозёма.
Мировые запасы бокситов практически безграничны, то есть несоизмеримы с динамикой спроса. Существующие мощности могут производить до 44,3 млн т первичного алюминия в год. Следует также учитывать, что в будущем некоторые из применений алюминия могут быть переориентированы на использование, например, композитных материалов.
Цены на алюминий (на торгах международных сырьевых бирж) с 2007 по 2015 годы составляли в среднем 1253—3291 долларов США за тонну.
Применение
Широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной плёнкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки. Первые же три свойства сделали алюминий основным сырьём в авиационной и авиакосмической промышленности (в последнее время медленно вытесняется композитными материалами, в первую очередь, углеволокном).
Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому для упрочнения его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий).
Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 4 раза дешевле за килограмм, но, за счёт в 3,3 раза меньшей плотности, для получения равного сопротивления его нужно приблизительно в 2 раза меньше по весу. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при напылении проводников на поверхности кристаллов микросхем. Меньшую электропроводность алюминия (3,7·107 См/м) по сравнению с медью (5,84·107 См/м), для сохранения одинакового электрического сопротивления, компенсируют увеличением площади сечения алюминиевых проводников. Недостатком алюминия как электротехнического материала является образование на его поверхности прочной диэлектрической оксидной плёнки, затрудняющей пайку и за счёт ухудшения контактного сопротивления вызывающей повышенное нагревание в местах электрических соединений, что, в свою очередь, отрицательно сказывается на надёжности электрического контакта и состоянии изоляции. Поэтому, в частности, 7-я редакция Правил устройства электроустановок, принятая в 2002 году, запрещает использовать алюминиевые проводники сечением менее 16 мм².
- Благодаря комплексу свойств широко распространён в тепловом оборудовании.
- Алюминий и его сплавы не приобретают хрупкость при сверхнизких температурах. Благодаря этому он широко используется в криогенной технике. Однако известен случай приобретения хрупкости криогенными трубами из алюминиевого сплава из-за их гибки на медных кернах при разработке РН Энергия.
- Высокий коэффициент отражения в сочетании с дешевизной и лёгкостью вакуумного напыления делает алюминий оптимальным материалом для изготовления зеркал.
- В производстве строительных материалов как газообразующий агент.
- Алитированием придают коррозионную и окалиностойкость стальным и другим сплавам, например, клапанам поршневых ДВС, лопаткам турбин, нефтяным платформам, теплообменной аппаратуре, а также заменяют цинкование.
- Сульфид алюминия используется для производства сероводорода.
- Идут исследования по разработке пенистого алюминия как особо прочного и лёгкого материала.
В качестве восстановителя
- Как компонент термита, смесей для алюмотермии.
- В пиротехнике.
- Алюминий применяют для восстановления редких металлов из их оксидов или галогенидов.
- Ограничено применяется как протектор при анодной защите.
Сплавы на основе алюминия
Основная статья: Алюминиевый сплав
В качестве конструкционного материала обычно используют не чистый алюминий, а разные сплавы на его основе. Обозначение серий сплавов в данной статье приведена для США (стандарт H35.1 ANSI) и согласно ГОСТ России. В России основные стандарты — это ГОСТ 1583 «Сплавы алюминиевые литейные. Технические условия» и ГОСТ 4784 «Алюминий и сплавы алюминиевые деформируемые. Марки». Существует также UNS маркировка и международный стандарт алюминиевых сплавов и их маркировки ISO R209 b.
- Алюминиево-магниевые Al-Mg (ANSI: серия 5ххх у деформируемых сплавов и 5xx.x у сплавов для изделий фасонного литья; ГОСТ: АМг). Сплавы системы Al-Mg характеризуются сочетанием удовлетворительной прочности, хорошей пластичности, очень хорошей свариваемости и коррозионной стойкости. Кроме того, эти сплавы отличаются высокой вибростойкостью.
В сплавах этой системы, содержащих до 6 % Mg, образуется эвтектическая система соединения Al3Mg2 c твёрдым раствором на основе алюминия. Наиболее широкое распространение в промышленности получили сплавы с содержанием магния от 1 до 5 %.
Рост содержания Mg в сплаве существенно увеличивает его прочность. Каждый процент магния повышает предел прочности сплава на 30 МПа, а предел текучести — на 20 МПа. При этом относительное удлинение уменьшается незначительно и находится в пределах 30—35 %.
Сплавы с содержанием магния до 3 % (по массе) структурно стабильны при комнатной и повышенной температуре даже в значительно нагартованном состоянии. С ростом концентрации магния в нагартованном состоянии структура сплава становится нестабильной. Кроме того, увеличение содержания магния свыше 6 % приводит к ухудшению коррозионной стойкости сплава.
Для улучшения прочностных характеристик сплавы системы Al-Mg легируют хромом, марганцем, титаном, кремнием или ванадием. Попадания в сплавы этой системы меди и железа стараются избегать, поскольку они снижают их коррозионную стойкость и свариваемость.
- Алюминиево-марганцевые Al-Mn (ANSI: серия 3ххх; ГОСТ: АМц). Сплавы этой системы обладают хорошей прочностью, пластичностью и технологичностью, высокой коррозионной стойкостью и хорошей свариваемостью.
Основными примесями в сплавах системы Al-Mn являются железо и кремний. Оба этих элемента уменьшают растворимость марганца в алюминии. Для получения мелкозернистой структуры сплавы этой системы легируют титаном.
Присутствие достаточного количества марганца обеспечивает стабильность структуры нагартованного металла при комнатной и повышенной температурах.
- Алюминиево-медные Al-Cu (Al-Cu-Mg) (ANSI: серия 2ххх, 2xx.x; ГОСТ: АМ). Механические свойства сплавов этой системы в термоупрочненном состоянии достигают, а иногда и превышают, механические свойства низкоуглеродистых сталей. Эти сплавы высокотехнологичны. Однако у них есть и существенный недостаток — низкое сопротивление коррозии, что приводит к необходимости использовать защитные покрытия.
В качестве легирующих добавок могут применяться марганец, кремний, железо и магний. Причем наиболее сильное влияние на свойства сплава оказывает последний: легирование магнием заметно повышает пределы прочности и текучести. Добавка кремния в сплав повышает его способность к искусственному старению. Легирование железом и никелем повышает жаропрочность сплавов второй серии.
Нагартовка этих сплавов после закалки ускоряет искусственное старение, а также повышает прочность и сопротивление коррозии под напряжением.
- Сплавы системы Al-Zn-Mg (Al-Zn-Mg-Cu) (ANSI: серия 7ххх, 7xx.x). Сплавы этой системы ценятся за очень высокую прочность и хорошую технологичность. Представитель системы — сплав 7075 является самым прочным из всех алюминиевых сплавов. Эффект столь высокого упрочнения достигается благодаря высокой растворимости цинка (70 %) и магния (17,4 %) при повышенных температурах, резко уменьшающейся при охлаждении.
Однако существенным недостатком этих сплавов является крайне низкая коррозионная стойкость под напряжением. Повысить сопротивление коррозии сплавов под напряжением можно легированием медью.
Нельзя не отметить открытой в 1960-е годы закономерности: присутствие лития в сплавах замедляет естественное и ускоряет искусственное старение. Помимо этого, присутствие лития уменьшает удельный вес сплава и существенно повышает его модуль упругости. В результате этого открытия были разработаны новые системы сплавов Al-Mg-Li, Al-Cu-Li и Al-Mg-Cu-Li.
- Алюминиево-кремниевые сплавы (силумины) лучше всего подходят для литья. Из них часто отливают корпуса разных механизмов.
- Комплексные сплавы на основе алюминия: авиаль.
Алюминий как добавка в другие сплавы
Алюминий является важным компонентом многих сплавов. Например, в алюминиевых бронзах основные компоненты — медь и алюминий. В магниевых сплавах в качестве добавки чаще всего используется алюминий. Для изготовления спиралей в электронагревательных приборах используют (наряду с другими сплавами) фехраль (Fe, Cr, Al). Добавка алюминия в так называемые «автоматные стали» облегчает их обработку, давая чёткое обламывание готовой детали с прутка в конце процесса.
Ювелирные изделия
Когда алюминий был очень дорог, из него делали разнообразные ювелирные изделия. Так, Наполеон III заказал алюминиевые пуговицы, а Менделееву в 1889 году были подарены весы с чашами из золота и алюминия. Мода на ювелирные изделия из алюминия сразу прошла, когда появились новые технологии его получения, во много раз снизившие себестоимость. Сейчас алюминий иногда используют в производстве бижутерии.
В Японии алюминий используется в производстве традиционных украшений, заменяя серебро.
Столовые приборы

По приказу Наполеона III были изготовлены алюминиевые столовые приборы, которые подавались на торжественных обедах ему и самым почётным гостям. Другие гости при этом пользовались приборами из золота и серебра.
Затем столовые приборы из алюминия получили широкое распространение, со временем использование алюминиевой кухонной утвари существенно снизилось, но и в настоящее время их всё ещё можно увидеть лишь в некоторых заведениях общественного питания — несмотря на заявления некоторых специалистов о вредности алюминия для здоровья человека. Кроме того, такие приборы со временем теряют привлекательный вид из-за царапин и форму из-за мягкости алюминия.
Из алюминия делают посуду для армии: ложки, котелки, фляжки.
Стекловарение
В стекловарении используются фторид, фосфат и оксид алюминия.
Пищевая промышленность
Алюминий зарегистрирован в качестве пищевой добавки Е173.
Алюмогель — студенистый осадок, образующийся при быстром осаждении гидроксида алюминия из солевых растворов, не имеющий кристаллического строения и содержащий большое количество воды используется в качестве основы для антацидных, обезболивающих и обволакивающих средств (алгелдрат; в смеси с гидроксидом магния — альмагель, маалокс, гастрацид и др.) при заболеваниях желудочно-кишечного тракта.
Военная промышленность
Дешевизна и вес металла обусловили широкое применение в производстве ручного стрелкового оружия, в частности автоматов и пистолетов.
Алюминий и его соединения в ракетной технике
Алюминий и его соединения используются в качестве высокоэффективного ракетного горючего в двухкомпонентных ракетных топливах и в качестве горючего компонента в твёрдых ракетных топливах. Следующие соединения алюминия представляют наибольший практический интерес как ракетное горючее:
- Порошковый алюминий как горючее в твёрдых ракетных топливах. Применяется также в виде порошка и суспензий в углеводородах.
- Гидрид алюминия.
- Боранат алюминия.
- Триметилалюминий.
- Триэтилалюминий.
- Трипропилалюминий.
Триэтилалюминий (обычно в смеси с триэтилбором) используется также для химического зажигания (как пусковое горючее) в ракетных двигателях, так как он самовоспламеняется в газообразном кислороде. Ракетные топлива на основе гидрида алюминия, в зависимости от окислителя, имеют следующие характеристики:
| Окислитель | Удельная тяга (Р1, с) |
Температура сгорания, °С |
Плотность топлива, г/см³ |
Прирост скорости, ΔVид, 25, м/с |
Весовое содержание горючего, % |
|---|---|---|---|---|---|
| Фтор | 348,4 | 5009 | 1,504 | 5328 | 25 |
| Тетрафторгидразин | 327,4 | 4758 | 1,193 | 4434 | 19 |
| ClF3 | 287,7 | 4402 | 1,764 | 4762 | 20 |
| ClF5 | 303,7 | 4604 | 1,691 | 4922 | 20 |
| Перхлорилфторид | 293,7 | 3788 | 1,589 | 4617 | 47 |
| Фторид кислорода | 326,5 | 4067 | 1,511 | 5004 | 38,5 |
| Кислород | 310,8 | 4028 | 1,312 | 4428 | 56 |
| Пероксид водорода | 318,4 | 3561 | 1,466 | 4806 | 52 |
| N2O4 | 300,5 | 3906 | 1,467 | 4537 | 47 |
| Азотная кислота | 301,3 | 3720 | 1,496 | 4595 | 49 |
Алюмоэнергетика
Алюмоэнергетика использует алюминий как универсальный вторичный энергоноситель. Его применения в этом качестве:
- Окисление алюминия в воде для производства водорода и тепловой энергии.
- Окисление алюминия кислородом воздуха для производства электроэнергии в воздушно-алюминиевых электрохимических генераторах.
Алюминий в мировой культуре
- В романе Н. Г. Чернышевского «Что делать?» (1862—1863) один из главных героев описывает в письме свой сон — видение будущего, в котором люди живут, отдыхают и работают в многоэтажных зданиях из стекла и алюминия; из алюминия выполнены полы, потолки и мебель (во времена Н. Г. Чернышевского алюминий ещё только начинали открывать).
- Алюминиевые огурцы — это образ и название песни Виктора Цоя 1987 года.
Токсичность
Несмотря на широкую распространённость в природе, ни одно живое существо не использует алюминий в метаболизме — это «мёртвый» металл. Отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. Наиболее ядовиты хлориды, нитраты, ацетаты, сульфаты и др. Для человека токсическое действие при попадании внутрь оказывают следующие дозы соединений алюминия (мг/кг массы тела):
- ацетат алюминия — 0,2—0,4;
- гидроксид алюминия — 3,7—7,3;
- алюминиевые квасцы — 2,9.
В первую очередь действует на нервную систему (накапливается в нервной ткани, приводя к тяжёлым расстройствам функции ЦНС). Однако свойство нейротоксичности алюминия стали изучать с середины 1960-х годов, так как накоплению металла в организме человека препятствует механизм его выведения. В обычных условиях с мочой может выделяться до 15 мг элемента в сутки. Соответственно, наибольший негативный эффект наблюдается у людей с нарушенной выделительной функцией почек.
Норматив содержания алюминия в воде хозяйственно-питьевого использования в России составляет 0,2 мг/л. При этом данная ПДК может быть увеличена до 0,5 мг/л главным государственным санитарным врачом по соответствующей территории для конкретной системы водоснабжения.
По некоторым биологическим исследованиям, поступление алюминия в организм человека было сочтено фактором в развитии болезни Альцгеймера, но эти исследования были позже раскритикованы, и вывод о связи одного с другим опровергался.
Соединения алюминия также, возможно, стимулируют рак молочной железы при применении антиперспирантов на основе хлорида алюминия. Но научных данных, подтверждающих это меньше, чем противоположных.
В ряде источников, авторство которых не указывается, содержатся утверждения о том, что алюминий якобы способен замещать кальций в костной ткани. Это противоречит научным данным, поскольку в электрохимическом ряду активности металлов алюминий стоит правее кальция — то есть, является менее химически активным металлом.
Вопросы, рассмотренные в материале:
- Как был открыт алюминий и каковы его основные свойства
- Основные физические свойства алюминия
- Основные химические свойства алюминия
- Как применяют основные свойства алюминия
- Как используют основные свойства алюминия в строительстве
Основные свойства алюминия делают этот материал по-настоящему универсальным и ценным. Его используют во всех видах промышленного производства, в сельском хозяйстве, в быту, в коммерции. Обладает огромным количеством преимуществ по отношению к стали и другим видам металла.
Самые популярные сферы применения алюминия – изготовление металлоконструкций и металлообработка. О том, какие свойства металла и где конкретно они нашли свое применение, читайте далее.
Как был открыт алюминий и каковы его основные свойства
Алюминий представляет собой парамагнитный металл, достаточно легкий, имеющий серебристый цвет. Он хорошо поддается механической обработке и литью, просто формуется. В земной коре этот элемент третий по распространенности, впереди только кислород и кремний. Наши недра содержат целых 8 % данного металла, что значительно больше золота, количество которого составляет не более пяти миллионных долей процента.

Алюминий активно используется в большинстве сфер производства. Его сплавы применяются для изготовления бытовой техники, транспорта, в машиностроении и электротехнике. Капитальное строительство также не может обойтись без него.
Он чрезвычайно распространен в земной коре, являясь первым из металлов и третьим химическим элементом (первое место у кислорода, второе – у кремния). Доля алюминия в наших недрах – 8,8 %. Металл является частью большого количества горных пород и минералов, основной из которых – алюмосиликат.
В виде соединений алюминий находится в базальтах, полевых шпатах, гранитах, глине и пр. Однако в основном его получают из бокситов, которые достаточно редко встречаются в виде месторождений. В России такие залежи есть только на Урале и в Сибири. В промышленных масштабах алюминий можно также добывать из нефелинов и алунитов.
Ткани животных и растений содержат алюминий в виде микроэлемента. Некоторые организмы, например, моллюски и плауны, являются его концентраторами, накапливая в своих органах.
Человечеству с давних времен знакомо соединение алюминия под названием алюмокалиевые квасцы. Применялось оно в процессе выделки кожи, в качестве средства, которое, набухая, связывает различные компоненты смеси. Во второй половине XVIII в. ученые открыли оксид алюминия. А вот вещество в чистом виде получили значительно позже.
Впервые это удалось Ч. К. Эрстеду, который выделил алюминий из хлорида. Проводя опыт, он обрабатывал соли калия амальгамой, в результате чего выделился порошок серого цвета, признанный всеми чистым алюминием.
В дальнейшем, исследуя металл, ученые определили его химические свойства, проявляющиеся в высокой способности к восстановлению и активности. Именно поэтому с алюминием долгое время не работали.
Но уже в 1854 г. французский ученый Девиль, применив электролиз расплава, сумел получить металл в слитках. Данный метод используется и сейчас. В промышленных масштабах алюминий стали производить в начале XX в., когда предприятия смогли получить доступ к большому количеству электроэнергии.

Сегодня алюминий является одним из самых используемых в производстве бытовой техники и строительстве металлом.
Основные физические свойства алюминия
Основные характеристики алюминия – высокая электро- и теплопроводность, пластичность, устойчивость к холоду и коррозии. Его можно обрабатывать посредством прокатки, ковки, штамповки, волочения. Алюминий прекрасно поддается сварке.

Примеси, присутствующие в металле в различных количествах, значительно ухудшают механические, технологические и физико-химические свойства чистого алюминия. Основными из них являются титан, кремний, железо, медь и цинк.
По степени очистки алюминий разделяют на технический металл и высокой чистоты. На практике различия данных типов – в стойкости к коррозии в различной среде. Стоимость напрямую зависит от чистоты алюминия. Технический металл подходит для производства проката, различных сплавов, кабельно-проводниковых изделий. Чистый используют для специальных целей.
Алюминий обладает высокой электропроводностью, уступая только золоту, серебру, меди. Однако сочетание данного показателя с малой плотностью позволяет использовать его при производстве кабельно-проводниковых изделий наравне с медью. Электропроводность металла может увеличиваться при длительном отжиге или ухудшаться при нагартовке.
Увеличивая чистоту алюминия, производители повышают его теплопроводность. Снизить данное свойство способны примеси меди, марганца и магния. Более высокую теплопроводность имеют исключительно медь и серебро. Именно благодаря данному свойству данный металл используют для производства радиаторов охлаждения и теплообменников.

Удельная теплоемкость алюминия, как и температура его плавления, достаточно высока. Данные показатели значительно превышают аналогичные значения большей части металлов. С повышением чистоты металла увеличивается и его способность отражать от поверхности световые лучи. Алюминий хорошо поддается полировке и прекрасно анодируется.
Металл близок по свойствам к кислороду, его поверхность на воздухе быстро затягивается пленкой из оксида алюминия – тонкой и прочной. Обладая антикоррозионными свойствами, она защищает металл от образования ржавчины и предупреждает дальнейшее окисление. Алюминий не взаимодействует с азотной кислотой (концентрированной и разбавленной) и органическими кислотами, он стоек к воздействию пресной, соленой воды.
Эти особенности алюминия придают ему устойчивость к коррозии, что и используется людьми. Именно поэтому его особенно широко применяют в строительстве. Интерес к нему увеличивается еще и по причине его легкости в сочетании с прочностью и мягкостью. Такие характеристики есть далеко не у всякого вещества.
Помимо вышеуказанных, алюминий имеет еще несколько интересных физических свойств:
- Ковкость и пластичность – алюминий стал материалом изготовления прочной и легкой тонкой фольги, а также проволоки.
- Плавление происходит при температуре +660 °С.
- Температура кипения +2 450 °С.
- Плотность – 2,7 г/см³.
- Наличие объемной гранецентрированной металлической кристаллической решетки.
- Тип связи – металлический.
Области использования алюминия определяются его химическими и физическими свойствами. Характеристики металла, рассмотренные выше, применяются в бытовых целях. Основные свойства алюминия, как прочного, особо легкого, антикоррозийного материала, используются в судо- и авиастроении. Именно поэтому важно их знать.
Основные химические свойства алюминия
С химической точки зрения алюминий является чрезвычайно сильным восстановителем, имеющим способность в чистом виде быть высоко активным веществом. Основное условие – убрать оксидную пленку.

Алюминий способен вступать в реакции с:
- щелочными соединениями;
- кислотами;
- серой;
- галогенами.
Алюминий не взаимодействует в обычных условиях с водой. Йод – единственный из галогенов, с которым у металла происходит реакция без нагревания. Для взаимодействия с прочими требуется увеличение температуры.
Рассмотрим несколько примеров, показывающих химические свойства данного металла. Это уравнения, иллюстрирующие взаимодействие с:
- щелочами: 2Al + 6H2O + 2NaOH = Na[Al(OH)4] + 3Н2;
- кислотами: AL + HCL = AlCL3 + H2;
- серой: 2AL + 3S = AL2S3;
- галогенами: AL + Hal = ALHal3.
Основным свойством алюминия считается его способность восстанавливать иные вещества из их соединений.
Реакции его взаимодействия с оксидами иных металлов хорошо показывают все восстановительные свойства вещества. Алюминий прекрасно выделяет металлы из различных соединений. Примером может служить: Cr2O3 + AL = AL2O3 + Cr.
Металлургическая промышленность активно использует эту способность алюминия. Методика получения веществ, которая основывается на данной реакции, называется алюминотермия. Химическая индустрия использует алюминий чаще всего для получения иных металлов.
Как применяют основные свойства алюминия
Алюминий в чистом виде имеет слабые механические свойства. Именно поэтому наиболее часто применяют его сплавы.

Таких сплавов достаточно много, вот основные из них:
- алюминий с марганцем;
- дюралюминий;
- алюминий с магнием;
- алюминий с медью;
- авиаль;
- силумины.
В основе этих сплавов лежит алюминий, отличаются они исключительно добавками. Последние же делают материал прочным, легким в обработке, более стойким к износу, коррозии.
Есть несколько основных областей применения алюминия (чистого или в виде сплава). Из металла изготавливают:
- фольгу и проволоку для бытового использования;
- посуду;
- морские и речные суда;
- самолеты;
- реакторы;
- космические аппараты;
- архитектурные и строительные элементы и конструкции.
Алюминий является одним из самых важных металлов наравне с железом и его сплавами. Эти два элемента таблицы Менделеева наиболее широко применяются человеком в своей деятельности.
Как используют основные свойства алюминия в строительстве
Строительство – одна из основных отраслей-потребителей алюминия. 25 % всего вырабатываемого металла используется именно в ней. Современный облик мегаполисов был бы невозможен без использования алюминия. Он дает возможность создавать функциональные и красивые здания, стремящиеся ввысь. Небоскребы офисных центров имеют фасады из стекла, закрепленные на прочных, легких рамах из алюминия.

Современные торговые, развлекательные и выставочные центры в основе своей имеют каркас из алюминия. Конструкции из данного металла используются для возведения бассейнов, стадионов и других спортивных строений. Алюминий – один из самых востребованных у архитекторов, строителей, дизайнеров металлов. Почему? Давайте разберемся.
Алюминий – прочный и легкий металл, не поддающийся коррозии, имеющий долгий срок службы и совершенно нетоксичный. Он легко поддается обработке, сварке, паянию, его просто сверлить, распиливать, связывать и соединять шурупами. Этот металл способен принять любую форму посредством экструзии. Алюминий поможет воплотить самый смелый замысел архитектора. Из него изготавливаются конструкции, которые невозможно сделать из иных материалов: пластика, дерева или стали.
За прошлый век алюминий прошел путь от металла, редко используемого в строительстве из-за дороговизны и недостаточных объемов производства, до наиболее часто применяемого. 1920-е годы стали переломными. Благодаря электролизной технологии значительно снизилась стоимость его производства – в 5 раз. Алюминий стали применять в производстве стеновых панелей и водостоков, декоративных элементов, а не только для сводов и отделки крыш.
Empire State Building – первый небоскреб, при возведении которого широко применялся алюминий. Он был построен в 1931 году и оставался самым высоким в мире до 1970 г.

Алюминий активно использовался в конструкциях этого здания. В интерьере его также применяли достаточно широко. Фреска, расположенная на стенах и полке лобби, являющаяся визитной карточкой сооружения, сделана из алюминия и золота в 23 карата.
80 лет – таков минимальный срок эксплуатации конструкций из алюминия. Применение этого металла не ограничено климатическими условиями, его свойства остаются прежними при температурах от -80 °С и до +300 °C. Пожары редко могут разрушить алюминиевые сооружения. Низкие же температуры, наоборот, увеличивают его прочность.

Примером может служить алюминиевый сайдинг. Отражающее покрытие в виде фольги и теплоизоляция создают вместе с ним прекрасную защиту от холода, которая в 4 раза более эффективна, чем облицовка кирпичом толщиной 10 см или камнем толщиной 20 см. Именно поэтому алюминий все чаще можно встретить при строительстве объектов в условиях холодного климата: в РФ – на Северном Урале, в Якутии и Сибири.

Но еще более важным качеством алюминия является его легкость. При одинаковой жесткости пластина из алюминия в два раза легче стальной. И все благодаря низкому удельному весу. Если посчитать, то выйдет, что вес алюминиевой конструкции при равной несущей способности в два, а иногда и в три раза ниже массы стальной и в семь раз ниже железобетонной.
В настоящее время алюминий используют для строительства небоскребов и иных высоких строений. Металл делает здание значительно легче, что удешевляет постройку за счет меньшей глубины фундамента. Ведь чем больший вес имеют сооружения, тем фундамент должен быть глубже. Разводные мосты, выполненные из алюминия, также имеют небольшой вес, что облегчает работу механизмов, противовесы для таких конструкций должны быть минимальными. Данный металл вообще дает возможность архитекторам не ограничивать фантазию. Да и работать с таким легким материалом значительно проще, быстрее и удобнее.