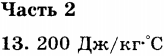Количество теплоты
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: количество теплоты, удельная теплоёмкость вещества, уравнение теплового баланса.
Как мы знаем, одним из способов изменения внутренней энергии является теплопередача (теплообмен). Предположим, что тело участвует в теплообмене с другими телами, и при этом не совершается механическая работа — ни самим телом, ни другими телами над этим телом.
Если в процессе теплообмена внутренняя энергия тела изменилась на величину , то говорят, что тело получило соответствующее количество теплоты:
.
Если при этом величина отрицательна, т.е. тело отдавало энергию, то говорят также, что тело отдавало тепло. Например, вместо формально верной, но несколько нелепой фразы «тело получило —5 Дж тепла» мы скажем: «тело отдало 5 Дж тепла».
Удельная теплоёмкость вещества
Предположим, что в процессе теплообмена агрегатное состояние вещества тела не изменяется (не происходит плавление, кристаллизация, парообразование или конденсация). Начальную температуру тела обозначим , конечную температуру —
.
Опыт показывает, что количество теплоты, полученное телом, прямо пропорционально массе тела и разности конечной и начальной температур:
Коэффициент пропорциональности c называется удельной теплоёмкостью вещества тела. Удельная теплоёмкость не зависит от формы и размеров тела. Удельные теплоёмкости различных веществ можно найти в таблицах.
Введя обозначение , получим также:
Чтобы понять физический смысл удельной теплоёмкости, выразим её из последней формулы:
Мы видим, что удельная теплоёмкость численно равна количеству теплоты, которое необходимо для нагревания 1кг данного вещества на (или, что то же самое, на
). Измеряется удельная теплоёмкость в Дж/(кг·
C) или в Дж/(кг·K).
Чем больше удельная теплоёмкость вещества, тем большее количество теплоты требуется для нагревания тела данной массы на заданное количество градусов.
В задачах часто фигурируют вода и лёд. Их удельные теплоёмкости желательно помнить.
Вода: Дж/(кг·
C).
Лёд: Дж/(кг·
C).
Произведение удельной теплоёмкости вещества на массу тела называется теплоёмкостью тела и обозначается :
Соответственно, для количества теплоты имеем:
Уравнение теплового баланса
Рассмотрим два тела (обозначим их 1 и 2), которые образуют замкнутую систему. Это означает, что данные тела могут обмениваться энергией только друг с другом, но не с другими телами. Считаем также, что механическая работа не совершается — внутренняя энергия тел меняется только в процессе теплообмена.
Имеется фундаментальный закон природы, подтверждаемый всевозможными экспериментами — закон сохранения энергии. Он гласит, что полная энергия замкнутой системы тел не меняется со временем.
В данном случае закон сохранения энергии утверждает, что внутренняя энергия нашей системы будет оставаться одной и той же: . Если изменение внутренней энергии первого тела равно
, а изменение внутренней энергии второго тела равно
, то суммарное изменение внутренней энергии будет равно нулю:
Но — количество теплоты, полученное первым телом в процессе теплообмена; аналогично
— количество теплоты, полученное вторым телом в процессе теплообмена. Стало быть,
(1)
Попросту говоря, сколько джоулей тепла отдало одно тело, ровно столько же джоулей получило второе тело. Так как система замкнута, ни один джоуль наружу не вышел. Соотношение (1) называется уравнением теплового баланса. В общем случае, когда тел образуют замкнутую систему и обмениваются энергией только с помощью теплопередачи, из закона сохранения энергии с помощью тех же рассуждений получаем общее уравнение теплового баланса:
(2)
В качестве простого примера применения уравнения теплового баланса рассмотрим следующую задачу.
Смешали г воды при температуре
и
г воды при температуре
. Найти установившуюся температуру смеси.
Обозначим искомую установившуюся температуру через . Запишем уравнение теплового баланса (1):
где — удельная теплоёмкость воды. Раскрываем скобки и находим:
Благодарим за то, что пользуйтесь нашими материалами.
Информация на странице «Количество теплоты» подготовлена нашими авторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать необходимые и поступить в высшее учебное заведение или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из разделов нашего сайта.
Публикация обновлена:
08.05.2023
Количество теплоты. Удельная теплоёмкость
1. Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количеством теплоты.
Количеством теплоты называется изменение внутренней энергии тела в процессе теплопередачи без совершения работы.
Количество теплоты обозначают буквой ( Q ). Так как количество теплоты является мерой изменения внутренней энергии, то его единицей является джоуль (1 Дж).
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
2. Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество теплоты требуется ему для нагревания. То же самое и с охлаждением: тело большей массы при охлаждении отдаёт большее количество теплоты. Эти тела сделаны из одного и того же вещества и нагреваются они или охлаждаются на одно и то же число градусов.
[ Qsim m ]
3. Если теперь нагревать 100 г воды от 30 до 60 °С, т.е. на 30 °С, а затем до 100 °С, т.е. на 70 °С, то в первом случае на нагревание уйдёт меньше времени, чем во втором, и, соответственно, на нагревание воды на 30 °С, будет затрачено меньшее количество теплоты, чем на нагревание воды на 70 °С. Таким образом, количество теплоты прямо пропорционально разности конечной ( (t_2,^circ C) ) и начальной ( (t_1,^circ C) ) температур: ( Qsim(t_2-t_1) ).
4. Если теперь в один сосуд налить 100 г воды, а в другой такой же сосуд налить немного воды и положить в неё такое металлическое тело, чтобы его масса и масса воды составляли 100 г, и нагревать сосуды на одинаковых плитках, то можно заметить, что в сосуде, в котором находится только вода, температура будет ниже, чем в том, в котором находятся вода и металлическое тело. Следовательно, чтобы температура содержимого в обоих сосудах была одинаковой нужно воде передать большее количество теплоты, чем воде и металлическому телу. Таким образом, количество теплоты, необходимое для нагревания тела зависит от рода вещества, из которого это тело сделано.
5. Зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К), называется удельной теплоёмкостью вещества.
Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой ( c ). Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Удельная теплоёмкость свинца 140 Дж/кг °С. Это значит, что для нагревания 1 кг свинца на 1 °С необходимо затратить количество теплоты 140 Дж. Такое же количество теплоты выделится при остывании 1 кг воды на 1 °С.
Поскольку количество теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты ( Q ), необходимое для нагревания тела массой ( m ) от температуры ( (t_1,^circ C) ) до температуры ( (t_2,^circ C) ), равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
[ Q=cm(t_2{}^circ-t_1{}^circ) ]
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
6. Пример решения задачи. В стакан, содержащий 200 г воды при температуре 80 °С, налили 100 г воды при температуре 20 °С. После чего в сосуде установилась температура 60 °С. Какое количество теплоты получила холодная вода и отдала горячая вода?
При решении задачи необходимо выполнять следующую последовательность действий:
- записать кратко условие задачи;
- перевести значения величин в СИ;
- проанализировать задачу, установить, какие тела участвуют в теплообмене, какие тела отдают энергию, а какие получают;
- решить задачу в общем виде;
- выполнить вычисления;
- проанализировать полученный ответ.
1. Условие задачи.
Дано:
( m_1 ) = 200 г
( m_2 ) = 100 г
( t_1 ) = 80 °С
( t_2 ) = 20 °С
( t ) = 60 °С
______________
( Q_1 ) — ? ( Q_2 ) — ?
( c_1 ) = 4200 Дж/кг · °С
2. СИ: ( m_1 ) = 0,2 кг; ( m_2 ) = 0,1 кг.
3. Анализ задачи. В задаче описан процесс теплообмена между горячей и холодной водой. Горячая вода отдаёт количество теплоты ( Q_1 ) и охлаждается от температуры ( t_1 ) до температуры ( t ). Холодная вода получает количество теплоты ( Q_2 ) и нагревается от температуры ( t_2 ) до температуры ( t ).
4. Решение задачи в общем виде. Количество теплоты, отданное горячей водой, вычисляется по формуле: ( Q_1=c_1m_1(t_1-t) ).
Количество теплоты, полученное холодной водой, вычисляется по формуле: ( Q_2=c_2m_2(t-t_2) ).
5. Вычисления.
( Q_1 ) = 4200 Дж/кг · °С · 0,2 кг · 20 °С = 16800 Дж
( Q_2 ) = 4200 Дж/кг · °С · 0,1 кг · 40 °С = 16800 Дж
6. В ответе получено, что количество теплоты, отданное горячей водой, равно количеству теплоты, полученному холодной водой. При этом рассматривалась идеализированная ситуация и не учитывалось, что некоторое количество теплоты пошло на нагревание стакана, в котором находилась вода, и окружающего воздуха. В действительности же количество теплоты, отданное горячей водой, больше, чем количество теплоты, полученное холодной водой.
Содержание
- ПРИМЕРЫ ЗАДАНИЙ
- Часть 1
- Часть 2
- Ответы
ПРИМЕРЫ ЗАДАНИЙ
Часть 1
1. Удельная теплоёмкость серебра 250 Дж/(кг · °С). Что это означает?
1) при остывании 1 кг серебра на 250 °С выделяется количество теплоты 1 Дж
2) при остывании 250 кг серебра на 1 °С выделяется количество теплоты 1 Дж
3) при остывании 250 кг серебра на 1 °С поглощается количество теплоты 1 Дж
4) при остывании 1 кг серебра на 1 °С выделяется количество теплоты 250 Дж
2. Удельная теплоёмкость цинка 400 Дж/(кг · °С). Это означает, что
1) при нагревании 1 кг цинка на 400 °С его внутренняя энергия увеличивается на 1 Дж
2) при нагревании 400 кг цинка на 1 °С его внутренняя энергия увеличивается на 1 Дж
3) для нагревания 400 кг цинка на 1 °С его необходимо затратить 1 Дж энергии
4) при нагревании 1 кг цинка на 1 °С его внутренняя энергия увеличивается на 400 Дж
3. При передаче твёрдому телу массой ( m ) количества теплоты ( Q ) температура тела повысилась на ( Delta t^circ ). Какое из приведённых ниже выражений определяет удельную теплоёмкость вещества этого тела?
1) ( frac{mDelta t^circ}{Q} )
2) ( frac{Q}{mDelta t^circ} )
3) ( frac{Q}{Delta t^circ} )
4) ( QmDelta t^circ )
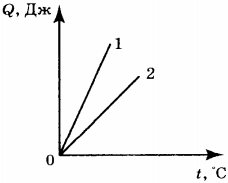
4. На рисунке приведён график зависимости количества теплоты, необходимого для нагревания двух тел (1 и 2) одинаковой массы, от температуры. Сравните значения удельной теплоёмкости (( c_1 ) и ( c_2 )) веществ, из которых сделаны эти тела.
1) ( c_1=c_2 )
2) ( c_1>c_2 )
3) ( c_1<c_2 )
4) ответ зависит от значения массы тел
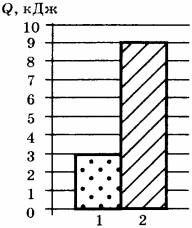
5. На диаграмме представлены значения количества теплоты, переданного двум телам равной массы при изменении их температуры на одно и то же число градусов. Какое соотношение для удельных теплоёмкостей веществ, из которых изготовлены тела, является верным?
1) ( c_1=c_2 )
2) ( c_1=3c_2 )
3) ( c_2=3c_1 )
4) ( c_2=2c_1 )
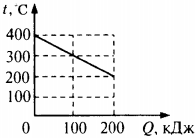
6. На рисунке представлен график зависимости температуры твёрдого тела от отданного им количества теплоты. Масса тела 4 кг. Чему равна удельная теплоёмкость вещества этого тела?
1) 500 Дж/(кг · °С)
2) 250 Дж/(кг · °С)
3) 125 Дж/(кг · °С)
4) 100 Дж/(кг · °С)
7. При нагревании кристаллического вещества массой 100 г измеряли температуру вещества и количество теплоты, сообщённое веществу. Данные измерений представили в виде таблицы. Считая, что потерями энергии можно пренебречь, определите удельную теплоёмкость вещества в твёрдом состоянии.
1) 192 Дж/(кг · °С)
2) 240 Дж/(кг · °С)
3) 576 Дж/(кг · °С)
4) 480 Дж/(кг · °С)
8. Чтобы нагреть 192 г молибдена на 1 К, нужно передать ему количество теплоты 48 Дж. Чему равна удельная теплоёмкость этого вещества?
1) 250 Дж/(кг · К)
2) 24 Дж/(кг · К)
3) 4·10-3 Дж/(кг · К)
4) 0,92 Дж/(кг · К)
9. Какое количество теплоты необходимо для нагревания 100 г свинца от 27 до 47 °С?
1) 390 Дж
2) 26 кДж
3) 260 Дж
4) 390 кДж
10. На нагревание кирпича от 20 до 85 °С затрачено такое же количество теплоты, как для нагревания воды такой же массы на 13 °С. Удельная теплоёмкость кирпича равна
1) 840 Дж/(кг · К)
2) 21000 Дж/(кг · К)
3) 2100 Дж/(кг · К)
4) 1680 Дж/(кг · К)
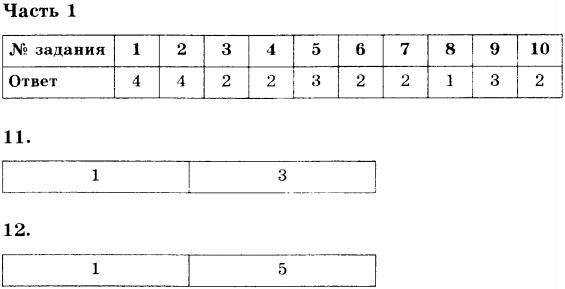
11. Из перечня приведённых ниже высказываний выберите два правильных и запишите их номера в таблицу.
1) Количество теплоты, которое тело получает при повышении его температуры на некоторое число градусов, равно количеству теплоты, которое это тело отдаёт при понижении его температуры на такое же число градусов.
2) При охлаждении вещества его внутренняя энергия увеличивается.
3) Количество теплоты, которое вещество получает при нагревании, идёт главным образом на увеличение кинетической энергии его молекул.
4) Количество теплоты, которое вещество получает при нагревании, идёт главным образом на увеличение потенциальной энергии взаимодействия его молекул
5) Внутреннюю энергию тела можно изменить, только сообщив ему некоторое количество теплоты
12. В таблице представлены результаты измерений массы ( m ), изменения температуры ( Delta t ) и количества теплоты ( Q ), выделяющегося при охлаждении цилиндров, изготовленных из меди или алюминия.
Какие утверждения соответствуют результатам проведённого эксперимента? Из предложенного перечня выберите два правильных. Укажите их номера. На основании проведенных измерений можно утверждать, что количество теплоты, выделяющееся при охлаждении,
1) зависит от вещества, из которого изготовлен цилиндр.
2) не зависит от вещества, из которого изготовлен цилиндр.
3) увеличивается при увеличении массы цилиндра.
4) увеличивается при увеличении разности температур.
5) удельная теплоёмкость алюминия в 4 раза больше, чем удельная теплоёмкость олова.
Часть 2
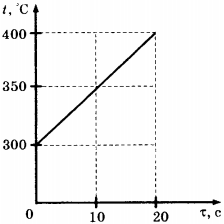
C1.Твёрдое тело массой 2 кг помещают в печь мощностью 2 кВт и начинают нагревать. На рисунке изображена зависимость температуры ( t ) этого тела от времени нагревания ( tau ). Чему равна удельная теплоёмкость вещества?
1) 400 Дж/(кг · °С)
2) 200 Дж/(кг · °С)
3) 40 Дж/(кг · °С)
4) 20 Дж/(кг · °С)
Ответы
Количество теплоты. Удельная теплоёмкость
3.1 (62.81%) 64 votes
Количество теплоты, удельная теплоемкость
От чего зависит количество теплоты
Внутренняя энергия тела изменяется при совершении работы или теплопередаче. При явлении теплопередачи внутренняя энергия передается теплопроводностью, конвекцией или излучением.
Каждое тело при нагревании или охлаждении (при теплопередаче) получает или теряет какое-то количество энергии. Исходя из этого, принято это количество энергии назвать количеством теплоты.
Итак, количество теплоты — это та энергия, которую отдает или получает тело в процессе теплопередачи.
Какое количество теплоты необходимо для нагревания воды? На простом примере можно понять, что для нагревания разного количества воды потребуется разное количество теплоты. Допустим, возьмем две пробирки с 1 литром воды и с 2-мя литрами воды. В каком случае потребуется большее количество теплоты? Во втором, там, где в пробирке 2 литра воды. Вторая пробирка будет нагреваться дольше, если мы подогреваем их одинаковым источником огня.
Таким образом, количество теплоты зависит от массы тела. Чем больше масса, тем большее количество теплоты требуется для нагрева и, соответственно, на охлаждение тела требуется большее время.
От чего еще зависит количество теплоты? Естественно, от разности температур тел. Но это еще не все. Ведь если мы попытаемся нагреть воду или молоко, то нам потребуется разное количество времени. Т.е получается, что количество теплоты зависит от вещества, из которого состоит тело.
В итоге получается, что количество теплоты, которое нужно для нагревания или количество теплоты, которое выделяется при остывании тела, зависит от его массы, от изменения температуры и от вида вещества, из которого состоит тело.
В чем измеряется количество теплоты
За единицу количества теплоты принято считать 1 Джоуль. До появления единицы измерения энергии ученые считали количество теплоты калориями. Сокращенно эту единицу измерения принято писать — “Дж”
Калория — это количество теплоты, которое необходимо для того, чтобы нагреть 1 грамм воды на 1 градус Цельсия. Сокращенно единицу измерения калории принято писать — “кал”.
1 кал = 4,19 Дж.
Обратите внимание, что в этих единицах энергии принято отмечать пищевую ценность продуктов питания кДж и ккал.
1 ккал = 1000 кал.
1 кДж = 1000 Дж
1 ккал = 4190 Дж = 4,19 кДж
Что такое удельная теплоемкость
Каждое вещество в природе имеет свои свойства, и для нагрева каждого отдельного вещества требуется разное количество энергии, т.е. количества теплоты.
Удельная теплоемкость вещества — это величина, равная количеству теплоты, которое нужно передать телу с массой 1 килограмм, чтобы нагреть его на температуру 1 0C
Удельная теплоемкость обозначается буквой c и имеет величину измерения Дж/кг*
Например, удельная теплоемкость воды равна 4200 Дж/кг*0C. То есть это то количество теплоты, которое нужно передать 1 кг воды, чтобы нагреть ее на 1 0C
Следует помнить, что удельная теплоемкость веществ в разных агрегатных состояниях различна. То есть для нагревания льда на 1 0C потребуется другое количество теплоты.
Как рассчитать количество теплоты для нагревания тела
Например, необходимо рассчитать количество теплоты, которое нужно потратить для того, чтобы нагреть 3 кг воды с температуры 15 0С до температуры 85 0С. Нам известна удельная теплоемкость воды, то есть количество энергии, которое нужно для того, чтобы нагреть 1 кг воды на 1 градус. То есть для того, чтобы узнать количество теплоты в нашем случае, нужно умножить удельную теплоемкость воды на 3 и на то количество градусов, на которое нужно увеличить температуры воды. Итак, это 4200*3*(85-15) = 882 000.
В скобках мы рассчитываем точное количество градусов, отнимая от конечного необходимого результата начальное
Итак, для того, чтобы нагреть 3 кг воды с 15 до 85 0С, нам потребуется 882 000 Дж количества теплоты.
Количество теплоты обозначается буквой Q, формула для его расчета выглядит следующим образом:
Q=c*m*(t2-t1).
Разбор и решение задач
Задача 1. Какое количество теплоты потребуется для нагрева 0,5 кг воды с 20 до 50 0С
Дано:
m = 0,5 кг.,
с = 4200 Дж/кг*0С,
t1 = 20 0С,
t2 = 50 0С.
Величину удельной теплоемкость мы определили из таблицы.
Решение:
количество теплоты определяется по формуле Q=c*m*(t2-t1).
Подставляем значения:
Q=4200*0,5*(50-20) = 63 000 Дж = 63 кДж.
Ответ: Q=63 кДж.
Задача 2. Какое количество теплоты потребуется для нагревания алюминиевого бруска массой 0,5 кг на 85 0С?
Дано:
m = 0,5 кг.,
с = 920 Дж/кг*0С,
t1 = 0 0С,
t2 = 85 0С.
Решение:
количество теплоты определяется по формуле Q=c*m*(t2-t1).
Подставляем значения:
Q=920*0,5*(85-0) = 39 100 Дж = 39,1 кДж.
Ответ: Q= 39,1 кДж.
ОГЭ 2021 по физике ›
1. Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количеством теплоты.
Количеством теплоты называется изменение внутренней энергии тела в процессе теплопередачи без совершения работы.
Количество теплоты обозначают буквой ( Q ). Так как количество теплоты является мерой изменения внутренней энергии, то его единицей является джоуль (1 Дж).
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
2. Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество теплоты требуется ему для нагревания. То же самое и с охлаждением: тело большей массы при охлаждении отдаёт большее количество теплоты. Эти тела сделаны из одного и того же вещества и нагреваются они или охлаждаются на одно и то же число градусов.
[ Qsim m ]
3. Если теперь нагревать 100 г воды от 30 до 60 °С, т.е. на 30 °С, а затем до 100 °С, т.е. на 70 °С, то в первом случае на нагревание уйдёт меньше времени, чем во втором, и, соответственно, на нагревание воды на 30 °С, будет затрачено меньшее количество теплоты, чем на нагревание воды на 70 °С. Таким образом, количество теплоты прямо пропорционально разности конечной ( (t_2,^circ C) ) и начальной ( (t_1,^circ C) ) температур: ( Qsim(t_2-t_1) ).
4. Если теперь в один сосуд налить 100 г воды, а в другой такой же сосуд налить немного воды и положить в неё такое металлическое тело, чтобы его масса и масса воды составляли 100 г, и нагревать сосуды на одинаковых плитках, то можно заметить, что в сосуде, в котором находится только вода, температура будет ниже, чем в том, в котором находятся вода и металлическое тело. Следовательно, чтобы температура содержимого в обоих сосудах была одинаковой нужно воде передать большее количество теплоты, чем воде и металлическому телу. Таким образом, количество теплоты, необходимое для нагревания тела зависит от рода вещества, из которого это тело сделано.
5. Зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К), называется удельной теплоёмкостью вещества.
Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой ( c ). Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Удельная теплоёмкость свинца 140 Дж/кг °С. Это значит, что для нагревания 1 кг свинца на 1 °С необходимо затратить количество теплоты 140 Дж. Такое же количество теплоты выделится при остывании 1 кг воды на 1 °С.
Поскольку количество теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты ( Q ), необходимое для нагревания тела массой ( m ) от температуры ( (t_1,^circ C) ) до температуры ( (t_2,^circ C) ), равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
[ Q=cm(t_2{}^circ-t_1{}^circ) ]
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
6. Пример решения задачи. В стакан, содержащий 200 г воды при температуре 80 °С, налили 100 г воды при температуре 20 °С. После чего в сосуде установилась температура 60 °С. Какое количество теплоты получила холодная вода и отдала горячая вода?
При решении задачи необходимо выполнять следующую последовательность действий:
- записать кратко условие задачи;
- перевести значения величин в СИ;
- проанализировать задачу, установить, какие тела участвуют в теплообмене, какие тела отдают энергию, а какие получают;
- решить задачу в общем виде;
- выполнить вычисления;
- проанализировать полученный ответ.
1. Условие задачи.
Дано: ( m_1 ) = 200 г ( m_2 ) = 100 г ( t_1 ) = 80 °С ( t_2 ) = 20 °С ( t ) = 60 °С ______________
( Q_1 ) — ? ( Q_2 ) — ? ( c_1 ) = 4200 Дж/кг · °С
2. СИ: ( m_1 ) = 0,2 кг; ( m_2 ) = 0,1 кг.
3. Анализ задачи. В задаче описан процесс теплообмена между горячей и холодной водой. Горячая вода отдаёт количество теплоты ( Q_1 ) и охлаждается от температуры ( t_1 ) до температуры ( t ). Холодная вода получает количество теплоты ( Q_2 ) и нагревается от температуры ( t_2 ) до температуры ( t ).
4. Решение задачи в общем виде. Количество теплоты, отданное горячей водой, вычисляется по формуле: ( Q_1=c_1m_1(t_1-t) ).
Количество теплоты, полученное холодной водой, вычисляется по формуле: ( Q_2=c_2m_2(t-t_2) ).
5. Вычисления. ( Q_1 ) = 4200 Дж/кг · °С · 0,2 кг · 20 °С = 16800 Дж ( Q_2 ) = 4200 Дж/кг · °С · 0,1 кг · 40 °С = 16800 Дж
6. В ответе получено, что количество теплоты, отданное горячей водой, равно количеству теплоты, полученному холодной водой. При этом рассматривалась идеализированная ситуация и не учитывалось, что некоторое количество теплоты пошло на нагревание стакана, в котором находилась вода, и окружающего воздуха. В действительности же количество теплоты, отданное горячей водой, больше, чем количество теплоты, полученное холодной водой.
Понятие количества теплоты.
Мы знаем, что внутреннюю энергию тела можно изменить двумя способами. Путем совершения работы и путём теплообмена. При осуществлении 2 способа изменение внутренней энергии равно количеству переданной теплоты. Количество теплоты может быть, как положительным, так и отрицательным.
Если внутренняя энергия тела увеличивается в процессе теплообмена, то количество теплоты больше нуля. Если внутренняя энергия тела уменьшается в процессе теплообмена, то количество теплоты меньше нуля. То есть тело отдает количество теплоты. Отсюда можно сделать вывод:
Количеством теплоты называют ту часть внутренней энергии, которую тело теряет или получает при теплопередаче.
Как рассчитать количество теплоты для нагревания тела
Например, необходимо рассчитать количество теплоты, которое нужно потратить для того, чтобы нагреть 3 кг воды с температуры 15 0С до температуры 85 0С. Нам известна удельная теплоемкость воды, то есть количество энергии, которое нужно для того, чтобы нагреть 1 кг воды на 1 градус. То есть для того, чтобы узнать количество теплоты в нашем случае, нужно умножить удельную теплоемкость воды на 3 и на то количество градусов, на которое нужно увеличить температуры воды. Итак, это 4200*3*(85-15) = 882 000.
В скобках мы рассчитываем точное количество градусов, отнимая от конечного необходимого результата начальное
Итак, для того, чтобы нагреть 3 кг воды с 15 до 85 0С, нам потребуется 882 000 Дж количества теплоты.
Количество теплоты обозначается буквой Q, формула для его расчета выглядит следующим образом:
Q=c*m*(t2-t1).
Отчего зависит Q
Опыт № 1: Возьмём два одинаковых сосуда. Нальем в один из них воду массой 400 г, а в другой растительное масло массой 400 г. Начнём их нагревать с помощью одинаковых горелок. Наблюдая за показаниями термометров. Мы видим, что масло нагревается быстрее. Значит количество теплоты зависит от температуры. Опыт 2: Возьмём 1 кг воды и 1 кг подсолнечного масла. Нагреем оба сосуда на 1 градус. На нагревание воды было потрачено 4.200 Дж. А для нагревания масла потрачено 1700 Дж. Отсюда можно сделать вывод: Количество теплоты зависит от рода вещества.
Физическая величина, показывающая, какое количество теплоты требуется для нагревания 1 кг вещества на 1 градус называется удельной теплоемкостью вещества.
Обозначается буквой С. Измеряется в Дж, поделить на кг, умножить на градус по Цельсию.
Опыт 3: Возьмём в одном сосуде 400 г воды, а в другом сосуде 200 г воды. Нагреем оба сосуда на одинаковое количество градусов. Для нагревания 1 сосуда потребовалось потратить большее количество теплоты. Вывод: количество теплоты зависит от массы.
Удельная теплоемкость вещества
Это физическая величина, выражающая количество тепла, необходимое веществу на единицу массы для повышения температуры на одну единицу.
Таким образом, удельная теплоёмкость является свойством вещества, поскольку его значение является репрезентативным для каждого вещества, каждое из которых, в свою очередь, имеет различные значения в зависимости от того, в каком состоянии оно находится (жидкое, твердое или газообразное).
Удельная теплоёмкость обозначается маленькой буквой c и измеряется в Дж/кг∗°С, представляет собой коэффициент повышения температуры в одной единице всей системы или всей массы вещества.
Кроме того, удельная теплоёмкость меняется в зависимости от физического состояния вещества, особенно в случае твердых частиц и газов, поскольку его молекулярная структура влияет на теплопередачу в системе частиц. То же самое относится и к условиям атмосферного давления: чем выше давление, тем ниже удельное тепло.
Основной состав удельной теплоты вещества должен быть с = С/m, т. е. удельная теплота равна соотношению калорийности и массы.
Однако когда это применяется к данному изменению температуры, говорят о средней удельной теплоемкости, которая рассчитывается на основе следующей формулы:
где:
Q — передача тепловой энергии между системой и средой (Дж);
m — масса системы (кг);
Δt или (t2 — t1) — повышение температуры, которой она подвергается (°C).
Формула для нахождения количества теплоты Q:
Q = c∗m(t2
— t1)
Чем выше удельная теплоёмкость вещества, тем больше тепловой энергии потребуется, чтобы его температура повысилась. Например, для нагрева воды (своды = 4200 Дж/кг∗°С) потребуется больше тепловой энергии, чем для нагрева свинца (ссвинца = 140 Дж/кг∗°С).
Уравнение теплового баланса:
Q отданное + Q полученное = 0.
Ниже представлена таблица значений удельной теплоёмкости некоторых веществ:
Q требуется
При нагревании
Формула: Q = cm (t2 -t1)
При плавлении вещества
Плавлением называют переход вещества из твердого состояния в жидкое состояние.
Формула: Q = m * λ
.
Физический смысл удельной теплоты плавления: лямбда показывает, какое количество теплоты необходимо для того, чтобы расплавить 1 кг вещества при температуре плавления.
Единица измерения: Дж/кг.
В чем измеряется количество теплоты
За единицу количества теплоты принято считать 1 Джоуль. До появления единицы измерения энергии ученые считали количество теплоты калориями. Сокращенно эту единицу измерения принято писать — “Дж”
Калория — это количество теплоты, которое необходимо для того, чтобы нагреть 1 грамм воды на 1 градус Цельсия. Сокращенно единицу измерения калории принято писать — “кал”.
1 кал = 4,19 Дж.
Обратите внимание, что в этих единицах энергии принято отмечать пищевую ценность продуктов питания кДж и ккал.
1 ккал = 1000 кал.
1 кДж = 1000 Дж
1 ккал = 4190 Дж = 4,19 кДж
Количество теплоты выделяется
- При горении топлива.
- При охлаждении вещества.
- При кристаллизации жидкости.
- При конденсации пара.
Для нагревания тел часто используют энергию, выделяющуюся при сгорании топлива.
Различают виды топлива: уголь, нефть, бензин, керосин, торф, спирт, природный газ и так далее.
Энергия, выделяющееся при полном сгорании топлива, называют теплотой сгорания топлива.
Формула: Q = m * q
где q называется удельной теплотой сгорания топлива.
Физический смысл: q показывает какое количество теплоты выделится при горении 1 кг топлива.
Единицы: Дж / кг.
При охлаждении веществ: (Так же как и при нагревании вещества).
Формула Q = cm (t2 — t1)
При кристаллизации веществ: (Так же как и при плавлении вещества).
Формула Q = m * λ
Как связаны и чем отличаются количество теплоты и удельная теплоемкость
Будем рассматривать такие процессы, как нагревание и охлаждение.
- нагревание — тело получает тепловую энергию (количество теплоты).
- охлаждение – тело отдает тепловую энергию в окружающее пространство.
Благодаря процессам нагревания и охлаждения мы можем обогреваться зимой с помощью русской печи. Сначала печь получит количество теплоты (тепловую энергию) от сгорающего топлива — дров. А затем, будет остывать и отдавать это количество теплоты всем телам, находящимся в помещении.
Отличия удельной теплоемкости от количества теплоты
Запомнить, что такое количество теплоты, и чем оно отличается от удельной теплоемкости, можно так (рис. ):
- Количество теплоты – это энергия нагревания (охлаждения) нескольких килограммов на несколько градусов.
- Удельная теплоемкость – это энергия нагревания 1-го килограмма на 1 градус.
Связь количества теплоты и удельной теплоемкости — формула
Если известны:
- удельная теплоемкость вещества;
- количество килограммов вещества;
- количество градусов, на которое нужно нагреть вещество,
то легко посчитать общую тепловую энергию – т. е. количество теплоты.
Для этого используем формулу:
[large boxed{ Q = c cdot m cdot (t_{text{конеч}} — t_{text{нач}}) }]
(large Q left( text{Дж} right) ) – количество теплоты, т. е. общая тепловая энергия;
(large c left( frac{text{Дж}}{text{кг} cdot text{град}} right) ) – удельная теплоемкость;
(large m left( text{кг} right) ) – масса вещества;
(large t_{text{конеч}} left( text{град} right) ) – температура после нагревания;
(large t_{text{нач}} left( text{град} right) ) – температура до нагревания;
Гордюнин С.А. Закон сохранения энергии в электростатике // Квант
Закон сохранения энергии определяет в самом общем виде энергетический баланс при всевозможных изменениях в любой системе. Запишем его следующим образом:
(1)
где Aвнеш — работа, совершенная над рассматриваемой системой внешними силами, ΔW — изменение энергии системы, Q — количество теплоты, выделяемое в системе. Договоримся, что если Aвнеш > 0, то над системой совершают положительную работу, а если Aвнеш < 0, положительную работу совершает система; если ΔW > 0, то энергия системы увеличивается, а если ΔW < 0, энергия уменьшается; наконец, если Q > 0, то в системе выделяется тепло, а если Q < 0, тепло системой поглощается.
В этой статье мы рассмотрим, как закон сохранения энергии «работает» в электростатике. В общем случае электростатическая система содержит взаимодействующие между собой заряды, находящиеся в электрическом поле.
Рассмотрим каждое слагаемое в уравнении (1) по отдельности.
Начнем с энергии. Энергия взаимодействия зарядов выражается через характеристики электрического поля этой системы зарядов. Так, например, энергия заряженного конденсатора емкостью C задается известным выражением
(2)
где q — заряд обкладок, U — напряжение между ними. Напомним, что конденсатор — это система двух проводников (обкладок, пластин), обладающая следующим свойством: если с одной обкладки на другую перенести заряд q (т. е. одну обкладку зарядить зарядом +q, а другую –q), то все силовые линии созданного таким образом поля будут начинаться на одной (положительно заряженной) обкладке и заканчиваться на другой. Поле конденсатора существует только внутри него.
Энергию заряженного конденсатора можно представить также как энергию поля, локализованного в пространстве между пластинами с плотностью энергии где E — напряженность поля. В сущности, именно этот факт дает основание говорить о поле как об объекте, реально существующем, — у этого объекта есть плотность энергии. Но надо помнить, что это просто эквивалентный способ определения энергии взаимодействия зарядов (которую теперь мы называем энергией электрического поля). Таким образом, мы можем считать энергию конденсатора как по формулам (2), так и по формуле
(3)
где V — объем конденсатора. Последней формулой легко пользоваться, конечно, только в случае однородного поля, но представление энергии в такой форме очень наглядно, а потому удобно.
Конечно, кроме энергии взаимодействия зарядов (энергии электрического поля) в энергию системы может входить и кинетическая энергия заряженных тел, и их потенциальная энергия в поле тяжести, и энергия пружин, прикрепленных к телам, и т. п.
Теперь о работе внешних сил. Помимо обычной механической работы Aмех (например, по раздвиганию пластин конденсатора), для электрической системы можно говорить о работе внешнего электрического поля. Например, о работе батареи, заряжающей или перезаряжающей конденсатор. Задача батареи — создать фиксированную, присущую данному источнику разность потенциалов между теми телами, к которым она присоединена. Делает она это единственно возможным способом — забирает заряд от одного тела и передает его другому. Источник никогда не создает заряды, а только перемещает их. Общий заряд системы при этом сохраняется — это один из краеугольных законов природы.
В источниках разных конструкций электрическое поле, необходимое для перемещения зарядов, создают различные «механизмы». В батареях и аккумуляторах — это электрохимические реакции, в динамомашинах — электромагнитная индукция. Существенно, что для выбранной системы зарядов (заряженных тел) это поле — внешнее, стороннее. Когда через источник с ЭДС от отрицательного полюса к положительному протекает заряд Δq, сторонние силы совершают работу
(4)
При этом если Δq > 0, то Aбат > 0 — батарея разряжается; если же Δq < 0, то Aбат < 0 — батарея заряжается и в ней накапливается химическая (или магнитная) энергия.
Наконец, о выделении тепла. Заметим только, что это джоулево тепло, т.е. тепло, связанное с протеканием тока через сопротивление.
Теперь обсудим несколько конкретных задач.
Задача 1. Два одинаковых плоских конденсатора емкостью C каждый присоединены к двум одинаковым батареям с ЭДС . В какой-то момент один конденсатор отключают от батареи, а другой оставляют присоединенным. Затем медленно разводят пластины обоих конденсаторов, уменьшая емкость каждого в n раз. Какая механическая работа совершается в каждом случае?
Если процесс изменения заряда на конденсаторе осуществляется все время медленно, тепло выделяться не будет. Действительно, если через резистор сопротивлением R протек заряд Δq за время t, то на резисторе за это время выделится количество теплоты
При достаточно больших t количество теплоты Q может оказаться сколь угодно малым.
В первом случае фиксирован заряд на пластинах (батарея отключена), равный Механическая работа определяется изменением энергии конденсатора:
Во втором случае фиксирована разность потенциалов на конденсаторе и работает батарея, поэтому
Через батарею протекает заряд
Этот заряд меньше нуля, значит, батарея заряжается и ее работа
Энергия поля в конденсаторе уменьшается:
Таким образом,
Зарядка батареи происходит за счет работы по раздвиганию пластин и за счет энергии конденсатора.
Заметим, что слова про раздвигание пластин существенной роли не играют. Такой же результат будет при любых других изменениях, приводящих к уменьшению емкости в n раз.
Задача 2. В схеме, изображенной на рисунке, найдите количество теплоты, выделившееся в каждом резисторе после замыкания ключа. Конденсатор емкостью C1 заряжен до напряжения U1, а конденсатор емкостью C2 — до напряжения U2. Сопротивления резисторов R1 и R2.
Рис. 1
Закон сохранения энергии (1) для данной системы имеет вид
т. е.
Начальная энергия конденсаторов равна
Для определения энергии в конечном состоянии воспользуемся тем, что суммарный заряд конденсаторов не может измениться. Он равен (для случаев, когда конденсаторы были соединены одноименно или разноименно заряженными пластинами соответственно). После замыкания ключа этим зарядом оказывается заряжен конденсатор емкостью C1 + C2 (конденсаторы емкостями C1 и C2 соединены параллельно). Таким образом,
и
Как и должно быть, в обоих случаях выделяется тепло — есть джоулевы потери. Замечательно, что выделившееся количество теплоты не зависит от сопротивления цепи — при малых сопротивлениях текут большие токи и наоборот.
Теперь найдем, как количество теплоты Q распределяется между резисторами. Через сопротивления R1 и R2 в каждый момент процесса перезарядки текут одинаковые токи, значит, в каждый момент мощности, выделяемые на сопротивлениях, равны
и
Следовательно,
Кроме того, . Поэтому окончательно
Задача 3. В схеме на рисунке 2 конденсатор емкостью C заряжен до напряжения U. Какое количество химической энергии запасется в аккумуляторе с ЭДС после замыкания ключа? Какое количество теплоты выделится в резисторе?
Рис. 2
Первоначальный заряд на конденсаторе . После окончания перезарядки заряд на конденсаторе станет равным . Протекший через батарею заряд в случае, когда к минусу батареи подключена отрицательно заряженная обкладка конденсатора, будет равен
В противном случае и при этом аккумулятор будет разряжаться (Δq > 0). А в первом случае при аккумулятор заряжается (Δq < 0), и количество химической энергии, запасенной в аккумуляторе после замыкания ключа, равно работе батареи:
Теперь запишем закон сохранения энергии (1) –
– и найдем выделившееся количество теплоты:
Задача 4. Плоский конденсатор находится во внешнем однородном поле с напряженностью , перпендикулярной пластинам. На пластинах площадью S распределены заряды +q и –q. Расстояние между пластинами d. Какую минимальную работу надо совершить, чтобы поменять пластины местами? Расположить параллельно полю? Вынуть из поля?
Работа будет минимальной, когда процесс проводится очень медленно — при этом не выделяется тепло. Тогда, согласно закону сохранения энергии,
Чтобы найти ΔW, воспользуемся формулой (3). Поле между пластинами представляет собой суперпозицию поля данного плоского конденсатора –
– и внешнего поля .
При перемене пластин местами поле меняется на –, а поле снаружи не меняется, т. е. изменение энергии системы связано с изменением ее плотности между пластинами конденсатора:
Если направления векторов и были одинаковы, то плотность энергии между пластинами уменьшилась после перемены пластин местами, а если направления были противоположны, то плотность энергии увеличилась. Таким образом, в первом случае — конденсатор хочет сам развернуться и его надо удерживать (A < 0), а во втором случае
Когда пластины конденсатора расположены параллельно полю и перпендикулярны друг другу. Энергия поля внутри конденсатора в этом случае равна . Тогда
Когда конденсатор вынули из поля, в том месте, где он был, поле стало , а в нем самом теперь поле , т.е. ΔW и Amin оказываются такими же, как и в предыдущем случае.
Задача 5. Конденсатор емкостью С без диэлектрика заряжен зарядом q. Какое количество теплоты выделится в конденсаторе, если его заполнить веществом с диэлектрической проницаемостью ε? То же, но конденсатор присоединен к батарее с ЭДС .
При заливании диэлектрика емкость конденсатора увеличилась в ε раз.
В первом случае фиксирован заряд на пластинах, внешних сил нет, и закон сохранения энергии (1) имеет вид
Отсюда
Тепло выделяется за счет уменьшения энергии взаимодействия зарядов.
Во втором случае есть работа батареи и фиксировано напряжение на конденсаторе:
Тогда из уравнения (1) следует
Задача 6. Две соединенные проводником пластины площадью S каждая находятся на расстоянии d друг от друга (это расстояние мало по сравнению с размерами пластин) во внешнем однородном поле с напряженностью , перпендикулярной пластинам (рис. 3). Какую работу надо совершить, чтобы сблизить их до расстояния d/2?
Рис. 3
Пластины эквипотенциальны, и между ними поля нет. Результатом работы по сближению является создание поля с напряженностью Е в объеме . Тогда, в соответствии с уравнениями (1) и (3),
Упражнения
1. Два одинаковых плоских конденсатора емкостью С каждый соединены параллельно и заряжены до напряжения U. Пластины одного из конденсаторов медленно разводят на большое расстояние. Какая при этом совершается работа?
2. Два конденсатора, каждый емкостью С, заряжены до напряжения U и соединены через резистор (рис. 4). Пластины одного из конденсаторов быстро раздвигают, так что расстояние между ними увеличивается вдвое, а заряд на пластинах за время их перемещения не изменяется. Какое количество теплоты выделится в резисторе?
Рис. 4
3. Плоский воздушный конденсатор присоединен к батарее с ЭДС . Площадь пластин S, расстояние между ними d. В конденсаторе находится металлическая плита толщиной d1, параллельная пластинам (рис. 5). Какую минимальную работу нужно затратить, чтобы удалить плиту из конденсатора?
Рис. 5
4. Большая тонкая проводящая пластина площадью S и толщиной d помещена в однородное электрическое поле с напряженностью , перпендикулярной поверхности пластины. Какое количество теплоты выделится в пластине, если поле мгновенно выключить? Какую минимальную работу надо совершить, чтобы удалить пластину из поля?
5. Одна из пластин плоского конденсатора подвешена на пружине (рис. 6). Площадь каждой пластины S, расстояние между ними в начальный момент d. Конденсатор на короткое время подключили к батарее, и он зарядился до напряжения U. Какой должна быть минимальная жесткость пружины, чтобы не произошло касание пластин? Смещением пластин за время зарядки пренебречь.
Рис. 6
Ответы.
1. (весь заряд оказывается на конденсаторе, пластины которого не раздвигали).
2. (в первый момент после разведения пластин замкнутыми друг на друга оказываются конденсатор емкостью С с напряжением U и конденсатор емкостью С/2 с напряжением 2U).
3. (минимальная работа по удалению плиты равна разности изменения энергии конденсатора и работы батареи).
4. (сразу после выключения внешнего поля в пластине есть поле поляризационных зарядов, напряженность которого равна Е удаление пластины из поля эквивалентно созданию поля с напряженностью Е в объеме пластины).
5. (результат получается из закона сохранения энергии и из условия равновесия пластины ).
На
прошлых уроках мы говорили о том, что изменить состояние термодинамической
системы можно двумя способами. Первый характеризуется передачей энергии в
процессе механического взаимодействия тел. Такую форму передачи энергии в
термодинамике (как и в механике) называют работой.
Второй
способ передачи энергии осуществляется при непосредственном обмене энергией
между хаотически движущимися частицами взаимодействующих тел. Если, например,
привести в соприкосновение два тела с разными температурами, то частицы более
нагретого тела будут передавать часть своей энергии частицам более холодного
тела. В результате внутренняя энергия первого тела уменьшается, а второго —
увеличивается.
Процесс
передачи энергии от одного тела к другому без совершения работы называют
теплопередачей.
Ещё
в восьмом классе мы говорили о том, что существуют три вида теплопередачи: это
теплопроводность, конвекция и излучение.
Давайте
вспомним, что теплопроводностью называется процесс теплообмена между телами
(или частями тела) при их непосредственном контакте. При теплопроводности
не происходит переноса вещества.
Конвекция
представляет собой теплопередачу нагретыми потоками жидкости или газа от одних
участков занимаемого ими объёма в другие (то есть конвекция сопровождается
переносом вещества). Она может протекать только в жидкостях и
газах, так как в твёрдом теле вещество не может перемещаться по объёму.
А
теплообмен при излучении осуществляется на расстоянии посредством
электромагнитных волн. Главной особенностью излучения
является то, что оно возможно не только в среде, но и в вакууме.
Количественной
мерой энергии, переходящей от одного тела к другому в процессе теплопередачи,
является количество теплоты.
Напомним,
что обозначается количество теплоты большой латинской буквой Q.
А единицей её измерения в СИ является джоуль (Дж). Но иногда для измерения
количества теплоты используют и внесистемную единицу — калорию.
Одна
калория — это количество теплоты, которое необходимо затратить, чтобы нагреть
один грамм воды на один градус Цельсия^ 1 кал = 4,19 Дж.
Основное
отличие работы от количества теплоты состоит в том, что работа характеризует
процесс изменения внутренней энергии системы, сопровождающийся превращением
энергии из одного вида в другой. Количество теплоты же характеризует процесс
передачи внутренней энергии от одних тел к другим (от более нагретых к менее
нагретым), не сопровождающийся превращениями энергии.
А
теперь давайте с вами вспомним от чего зависит количество теплоты. Для этого
давайте проведём несколько простых экспериментов. Возьмём два одинаковых сосуда
в которых находится разное количество воды, но при одинаковой температуре.
При
помощи электроплитки будем подводить тепло к сосудам. Спустя несколько минут
после включения плитки мы с вами заметим, что вода в сосуде с меньшим
количеством воды нагрелась на большее число градусов, хотя оба сосуда получили
одно и тоже количество теплоты. Следовательно, чем больше масса тела, тем
большее количество теплоты требуется к нему подвести для нагревания на одно и
тоже число градусов.
Продолжим
опыты. Опять берём два одинаковых сосуда, но с равным количеством воды при
одинаковой температуре. Будем нагревать воду в первом сосуде на 20 оС,
а во втором — на 60 оС. Включим секундомер одновременно с плиткой и
немного подождём.
На
нагревание воды на 20 оС тратится почти в три раза меньше времени,
чем на нагревание такой же массы воды, но на 60 оС. Значит, количество
теплоты пропорционально изменению температуры тела.
Теперь
пусть у нас в одном из сосудов находится вода, а во втором — такое же
количество бензина. Через несколько минут после включения нагревателей,
проверим температуры обеих жидкостей.
Не
трудно заметить, что, получив за одинаковый промежуток времени от нагревателя
равное с водой количество теплоты, бензин нагрелся сильнее. Значит, количество
теплоты, которое необходимо затратить для увеличения температуры тела, зависит
и от рода вещества, из которого это тело сделано:
При
остывании тела его конечная температура оказывается меньше начальной, и,
поэтому, количество теплоты, отдаваемой телом, отрицательно.
В
полученной нами в формуле коэффициент с — это удельная теплоёмкость
вещества. Она численно равна количеству теплоты, которую получает или отдаёт
вещество массой один килограмм при изменении его температуры на один кельвин
(или один градус Цельсия, так изменение температуры в этих шкалах совпадают).
Из
определения следует, что единицей удельной теплоёмкости в СИ является:
Значения
удельной теплоёмкости веществ определяют экспериментально.
Самую
большую удельную теплоёмкость, из представленных в таблице веществ, имеет вода.
Для нагревания одного её килограмма всего на один кельвин необходимо затратить
4200 Дж теплоты.
Обратите
внимание ещё и на то, что в этой таблице нет удельных теплоёмкостей газов. Дело
в том, что их удельная теплоёмкость зависит от того, при каком процессе
осуществляется теплопередача. Например, для нагревания газа при постоянном
давлении ему нужно передать большее количество теплоты, чем для его нагревания
при постоянном объёме, так как в первом случае газ будет расширяться и
совершать работу, а во втором — только нагреваться. Но об удельной теплоёмкости
газов мы с вами поговорим в одном из следующих уроков.
Следует
помнить, что формула, которую мы получили для определения количества теплоты,
справедлива только в том случае, если процесс теплопередачи НЕ сопровождается
изменением агрегатного состояния вещества. Давайте посмотрим, что же будет
происходить при фазовых переходах. Для этого проведём такой опыт. Возьмём два
сосуда в которые поместим разное количество льда, находящегося при температуре
плавления, и будем их нагревать. Не трудно заметить, что несмотря на постоянное
подведение теплоты, температура льда остаётся постоянной. И она не будет
изменяться до тех пор, пока весь лёд не перейдёт в жидкое состояние. Только
после этого температура образовавшейся изо льда воды начинает повышаться. При
этом, обратите внимание, что количество теплоты, которое необходимо
затратить на плавление кристаллического вещества, предварительно нагретого до
температуры плавления, прямо пропорционально массе этого вещества:
При
обратном процессе, то есть в процессе кристаллизации, такое же количество
теплоты вещество будет отдавать:
Коэффициент
пропорциональности λ, входящий в формулу, называется удельной
теплотой плавления. Она численно равна количеству теплоты, необходимому для
превращения кристаллического вещества массой один килограмм, взятого при
температуре плавления, в жидкость той же температуры:
Из
определения следует, что единицей измерения удельной теплоты плавления в СИ
является джоуль, делённый на килограмм:
Продолжим
наши опыты. Пусть у нас есть сосуд с водой, к которому постоянно подводится
теплота. Пока нагреваемая жидкость не кипит, часть сообщаемой ей энергии
расходуется на компенсацию потери энергии при испарении, а часть — на
увеличение внутренней энергии, о чём свидетельствует увеличение её температуры.
Однако,
когда жидкость закипит, её температура перестаёт меняться, хотя теплота
продолжает подводится. Очевидно, что теперь вся подводимая теплота расходуется
на переход жидкости в газообразное состояние. И так происходит до тех пор, пока
вся жидкость не превратится в пар.
Таким
образом, чтобы превратить в пар жидкость при температуре кипения, необходимо
передать ей определённое количество теплоты, которое прямо пропорционально
массе жидкости:
При
конденсации пара происходит выделение такого же количества теплоты:
Коэффициент
пропорциональности «Эр» (r),
входящий в формулу, называется удельной теплотой парообразования. Он
численно равен количеству теплоты, которое необходимо передать жидкости массой
один килограмм, находящейся при температуре кипения, для превращения её при
постоянной температуре в пар:
Из
определения следует, что единицей измерения удельной теплоты плавления в СИ
является джоуль на килограмм:
В
заключение отметим, что при теплообмене двух или нескольких тел абсолютное
значение количества теплоты, которое отдало более нагретое тело, равно
количеству теплоты, которое было получено более холодным телом.
Учитывая,
что отданное количество теплоты считается отрицательным, а полученное —
положительным, получается, что при теплообмене между телами, образующими
теплоизолированную систему, суммарное количество теплоты, полученное ими,
равняется нулю:
Записанное
нами равенство называется уравнением теплового баланса и выражает, по
сути, закон сохранения энергии.