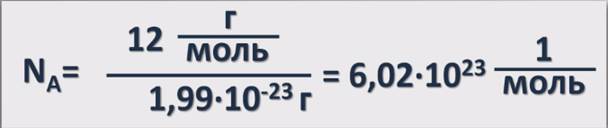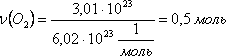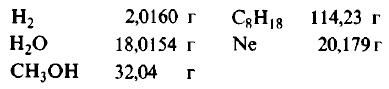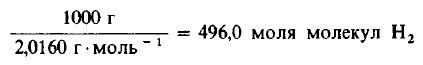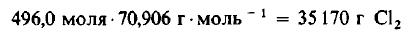В этой статье мы коснемся нескольких краеугольных понятий в химии, без которых совершенно невозможно
решение задач. Старайтесь понять смысл физических величин, чтобы усвоить эту тему.
Я постараюсь приводить как можно больше примеров по ходу этой статьи, в ходе изучения вы увидите множество примеров
по данной теме.

Относительная атомная масса — Ar
Представляет собой массу атома, выраженную в атомных единицах массы. Относительные атомные массы указаны в периодической
таблице Д.И. Менделеева. Так, один атом водорода имеет атомную массу = 1, кислород = 16, кальций = 40.
Относительная молекулярная масса — Mr
Относительная молекулярная масса складывается из суммы относительных атомных масс всех атомов, входящих в состав вещества.
В качестве примера найдем относительные молекулярные массы кислорода, воды, перманганата калия и медного купороса:
Mr (O2) = (2 × Ar(O)) = 2 × 16 = 32
Mr (H2O) = (2 × Ar(H)) + Ar(O) = (2 × 1) + 16 = 18
Mr (KMnO4) = Ar(K) + Ar(Mn) + (4 × Ar(O)) = 39 + 55 + (4 * 16) = 158
Mr (CuSO4*5H2O) = Ar(Cu) + Ar(S) + (4 × Ar(O)) + (5 × ((Ar(H) × 2) +
Ar(O))) = 64 + 32 + (4 × 16) + (5 × ((1 × 2) + 16)) = 160 + 5 * 18 = 250
Моль и число Авогадро
Моль — единица количества вещества (в системе единиц СИ), определяемая как количество вещества, содержащее столько же структурных единиц
этого вещества (молекул, атомов, ионов) сколько содержится в 12 г изотопа 12C, т.е. 6 × 1023.
Число Авогадро (постоянная Авогадро, NA) — число частиц (молекул, атомов, ионов) содержащихся в одном моле любого вещества.

Больше всего мне хотелось бы, чтобы вы поняли физический смысл изученных понятий. Моль — международная единица количества вещества, которая
показывает, сколько атомов, молекул или ионов содержится в определенной массе или конкретном объеме вещества. Один моль любого вещества
содержит 6.02 × 1023 атомов/молекул/ионов — вот самое важное, что сейчас нужно понять.
Иногда в задачах бывает дано число Авогадро, и от вас требуется найти, какое вам дали количество вещества (моль). Количество вещества в химии
обозначается N, ν (по греч. читается «ню»).
Рассчитаем по формуле: ν = N/NA количество вещества 3.01 × 1023 молекул воды и 12.04 × 1023 атомов углерода.
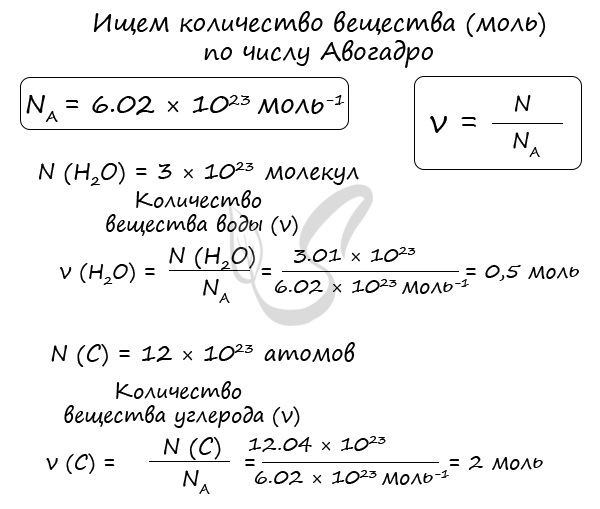
Мы нашли количества вещества (моль) воды и углерода. Сейчас это может показаться очень абстрактным, но, иногда не зная, как найти
количество вещества, используя число Авогадро, решение задачи по химии становится невозможным.
Молярная масса — M
Молярная масса — масса одного моля вещества, выражается в «г/моль» (грамм/моль). Численно совпадает с изученной нами ранее
относительной молекулярной массой.
Рассчитаем молярные массы CaCO3, HCl и N2
M (CaCO3) = Ar(Ca) + Ar(C) + (3 × Ar(O)) = 40 + 12 + (3 × 16) = 100 г/моль
M (HCl) = Ar(H) + Ar(Cl) = 1 + 35.5 = 36.5 г/моль
M (N2) = Ar(N) × 2 = 14 × 2 = 28 г/моль
Полученные знания не должны быть отрывочны, из них следует создать цельную систему. Обратите внимание: только что мы рассчитали
молярные массы — массы одного моля вещества. Вспомните про число Авогадро.
Получается, что, несмотря на одинаковое число молекул в 1 моле (1 моль любого вещества содержит 6.02 × 1023 молекул),
молекулярные массы отличаются. Так, 6.02 × 1023 молекул N2 весят 28 грамм, а такое же количество молекул
HCl — 36.5 грамм.
Это связано с тем, что, хоть количество молекул одинаково — 6.02 × 1023, в их состав входят разные атомы, поэтому и
массы получаются разные.

Часто в задачах бывает дана масса, а от вас требуется рассчитать количество вещества, чтобы перейти к другому веществу в реакции.
Сейчас мы определим количество вещества (моль) 70 грамм N2, 50 грамм CaCO3, 109.5 грамм HCl. Их молярные
массы были найдены нам уже чуть раньше, что ускорит ход решения.

ν (CaCO3) = m(CaCO3) : M(CaCO3) = 50 г. : 100 г/моль = 0.5 моль
ν (HCl) = m(HCl) : M(HCl) = 109.5 г. : 36.5 г/моль = 3 моль
Иногда в задачах может быть дано число молекул, а вам требуется рассчитать массу, которую они занимают. Здесь нужно использовать
количество вещества (моль) как посредника, который поможет решить поставленную задачу.
Предположим нам дали 15.05 × 1023 молекул азота, 3.01 × 1023 молекул CaCO3 и 18.06 × 1023 молекул
HCl. Требуется найти массу, которую составляет указанное число молекул. Мы несколько изменим известную формулу, которая поможет нам связать
моль и число Авогадро.

Теперь вы всесторонне посвящены в тему. Надеюсь, что вы поняли, как связаны молярная масса, число Авогадро и количество вещества.
Практика — лучший учитель. Найдите самостоятельно подобные значения для оставшихся CaCO3 и HCl.
Молярный объем
Молярный объем — объем, занимаемый одним молем вещества. Примерно одинаков для всех газов при стандартной температуре
и давлении составляет 22.4 л/моль. Он обозначается как — VM.
Подключим к нашей системе еще одно понятие. Предлагаю найти количество вещества, количество молекул и массу газа объемом
33.6 литра. Поскольку показательно молярного объема при н.у. — константа (22.4 л/моль), то совершенно неважно, какой газ мы
возьмем: хлор, азот или сероводород.
Запомните, что 1 моль любого газа занимает объем 22.4 литра. Итак, приступим к решению задачи. Поскольку какой-то газ
все же надо выбрать, выберем хлор — Cl2.


Моль (количество вещества) — самое гибкое из всех понятий в химии. Количество вещества позволяет вам перейти и к
числу Авогадро, и к массе, и к объему. Если вы усвоили это, то главная задача данной статьи — выполнена 

Относительная плотность и газы — D
Относительной плотностью газа называют отношение молярных масс (плотностей) двух газов. Она показывает, во сколько раз одно вещество
легче/тяжелее другого. D = M (1 вещества) / M (2 вещества).
В задачах бывает дано неизвестное вещество, однако известна его плотность по водороду, азоту, кислороду или
воздуху. Для того чтобы найти молярную массу вещества, следует умножить значение плотности на молярную массу
газа, по которому дана плотность.
Запомните, что молярная масса воздуха = 29 г/моль. Лучше объяснить, что такое плотность и с чем ее едят на примере.
Нам нужно найти молярную массу неизвестного вещества, плотность которого по воздуху 2.5

Предлагаю самостоятельно решить следующую задачку (ниже вы найдете решение): «Плотность неизвестного вещества по
кислороду 3.5, найдите молярную массу неизвестного вещества»

Относительная плотность и водный раствор — ρ
Пишу об этом из-за исключительной важности в решении
сложных задач, высокого уровня, где особенно часто упоминается плотность. Обозначается греческой буквой ρ.
Плотность является отражением зависимости массы от вещества, равна отношению массы вещества к единице его объема. Единицы
измерения плотности: г/мл, г/см3, кг/м3 и т.д.
Для примера решим задачку. Объем серной кислоты составляет 200 мл, плотность 1.34 г/мл. Найдите массу раствора. Чтобы не
запутаться в единицах измерения поступайте с ними как с самыми обычными числами: сокращайте при делении и умножении — так
вы точно не запутаетесь.

Иногда перед вами может стоять обратная задача, когда известна масса раствора, плотность и вы должны найти объем. Опять-таки,
если вы будете следовать моему правилу и относится к обозначенным условным единицам «как к числам», то не запутаетесь.
В ходе ваших действий «грамм» и «грамм» должны сократиться, а значит, в таком случае мы будем делить массу на плотность. В противном случае
вы бы получили граммы в квадрате 
К примеру, даны масса раствора HCl — 150 грамм и плотность 1.76 г/мл. Нужно найти объем раствора.

Массовая доля — ω
Массовой долей называют отношение массы растворенного вещества к массе раствора. Важно заметить, что в понятие раствора входит
как растворитель, так и само растворенное вещество.
Массовая доля вычисляется по формуле ω (вещества) = m (вещества) / m (раствора). Полученное число будет показывать массовую долю
в долях от единицы, если хотите получить в процентах — его нужно умножить на 100%. Продемонстрирую это на примере.

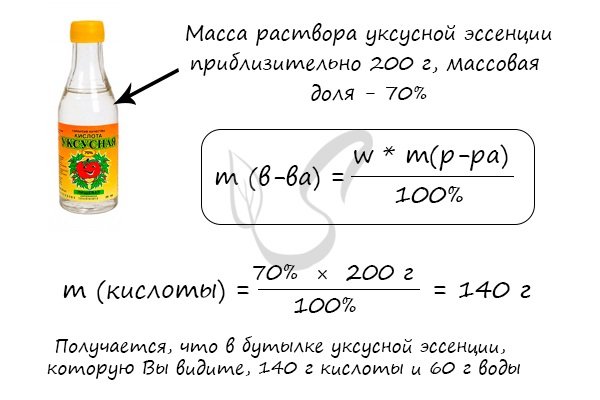
Решим несколько иную задачу и найдем массу чистой уксусной кислоты в широко известной уксусной эссенции.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Содержание:
- § 1 Количество вещества
- § 2 Моль
- § 3 Молярная масса
§ 1 Количество вещества
В химической практике, имея дело с веществами, а не с отдельными атомами или молекулами, химики редко используют массы, измеряемые в атомных единицах. Масса порции реагирующих веществ или продуктов реакции чаще измеряется в граммах или в более крупных единицах.
Чтобы перейти от молекул к порциям веществ, воспользуемся единицей измерения, которая называется моль.
Химик и физик из Франции Жозеф Луи Гей-Люссак в 1808 году изучал интересную химическую реакцию, в которой в результате взаимодействия двух газов – хлороводорода и аммиака – получалось кристаллическое вещество – хлорид аммония.
HCl + NH3 →NH4Cl
Оказалось, что для реакции требуются одинаковые объемы хлороводорода и аммиака. Если одного из этих газов вначале будет больше, то по окончании реакции этот избыток оставался неиспользованным.
Гей-Люссак привел свои наблюдения в статье, но никаких выводов из них не сделал. Важные заключения через три года привел итальянский химик Амедео Авогадро. В 1811 году, в результате экспериментов и расчетов, Авогадро пришел к мысли, что равные объемы газов, находящихся при одинаковых условиях, содержат одно и то же число молекул.
Гипотеза Авогадро долго считалась спорной, поскольку не подтверждалась расчетами, основанными на ошибочном мнении о немолекулярном строении простых газообразных веществ. Однако в 1865 году австрийский физик и химик Иоганн Лошмидт предпринял попытку рассчитать число молекул газа в заданном объеме.
Когда гипотеза Авогадро была признана, ученые получили возможность правильно определять состав молекул химических соединений, рассчитывать атомные и молекулярные массы. Эти знания позволяли легко рассчитывать массовые соотношения веществ в химических реакциях. Пользоваться этими соотношения очень удобно: измеряя массу веществ в граммах, ученые как бы оперировали молекулами.
§ 2 Моль
Количество вещества, численно равное относительной молекулярной массе, но выраженное в граммах, назвали грамм-молекулой или молем.
Слово «моль» придумал в начале XX века немецкий физико-химик, лауреат Нобелевской премии Вильгельм Оствальд. Слово происходит от слова «молекула».
Моль – это количество вещества, содержащее столько структурных единиц (атомов, молекул), сколько содержится атомов в 0,012 кг углерода.
Согласно Международной системе единиц СИ моль является единицей измерения особой физической величины – количества вещества. Под количеством вещества (обозначается греческой буквой ν) понимают число структурных единиц этого вещества (атомов, молекул и др.).
Самое важное заключается в том, что 1 моль любого вещества содержит одно и то же число молекул. Это число называется постоянной или числом Авогадро. Она обозначается символом NA. Постоянная Авогадро рассчитана давно и представляет собой очень большое число.
Если массу 1 моля углерода 12 г/моль разделить на массу 1 атома углерода 1,9910-23 г, то получится число, равное 6,02·1023. Поскольку это число обозначает количество частиц в 1 моле, единицы его пишут как 1/моль, моль-1 или обратный моль.
Чтобы как-то представить это число, скажем лишь, что оно больше, чем число стаканов воды, которое содержится в Мировом океане, а 6,02·1023 зёрен пшеницы имели бы массу порядка 2·1016 тонн.
Для сбора такого урожая потребовалось бы более 2 миллионов лет. Из примеров ясно: применение числа Авогадро для отсчета макротел бессмысленно. Главное его назначение – определение количества частиц (атомов и молекул) микромира и связь единиц микро и макромира.
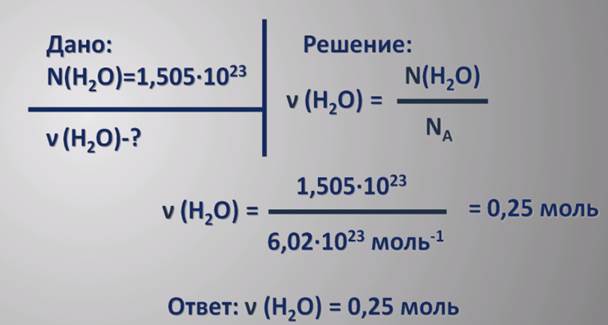
Зная количество вещества, можно судить о числе частиц в определенной его порции и брать вещества для реакций в необходимых количествах. Таким образом, химики могут определять число атомов и молекул путём взвешивания порций веществ. Приведём примеры таких расчётов. Чтобы вычислить количество вещества, зная число частиц, используем формулу 2 где ν – количество вещества в молях, N – число частиц вещества, NА – постоянная Авогадро.
Задача.Какое количество вещества содержит 1,505·1023 молекул воды?
В химии редко используется такая величина как число частиц. Гораздо легче использовать величины, которые легко измерить. Такой величиной является масса вещества. Как же связаны между собой масса и количество вещества? Зная число молекул вещества в одном моле и массу одной молекулы, можно подсчитать массу одного моля вещества. Например, известно, что масса молекулы воды равна
2,992·10-23г. Умножив ее на постоянную Авогадро, 6,02·1023 обратных молей, мы получим
18 г/моль – массу одного моля воды или молярную массу воды.
§ 3 Молярная масса
Молярной массой называется масса вещества, взятого в количестве 1 моль. Измеряется она в г/моль и обозначается латинской буквой М. Чтобы найти молярную массу вещества, нет необходимости проделывать столь сложные расчеты. Достаточно помнить, что молярная масса численно равна относительной молекулярной массе и имеет размерность г/моль.
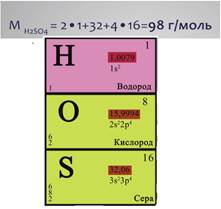
Например, относительная молекулярная масса серной кислоты Н2SО4 равна 2·1+32+4·16=98, следовательно, молярная масса серной кислоты Н2SО4 равна 98 г/моль.
Молярную массу используют для перевода количества вещества в массу и наоборот. Для расчетов используют формулу: количество вещества ν равно отношению массы вещества m к молярной массе этого вещества М.
Решим задачу. Вычислить количество вещества азотной кислоты массой 75,6 г.
Если требуется найти массу, зная количество вещества, формулу преобразуют: масса вещества m равна произведению количества вещества ν на молярную массу этого вещества М.
Список использованной литературы:
- Н.Е. Кузнецова. Химия. 8 класс. Учебник для общеобразовательных учреждений. – М. Вентана-Граф, 2012.
Использованные изображения:
Для
определения числа атомов (молекул) в
определенном количестве вещества
необходимо воспользоваться следующей
формулой: N = ν · NA,
где
N — число частиц (атомов или молекул).
Например,
определим количество атомов алюминия,
содержащиеся в 2 моль вещества алюминия:
N (Al) = ν (Al) · NA.
N
(Al) = 2 моль · 6,02 · 1023
= 12,04 · 1023
(атомов).
Кроме того, можно определить
количество вещества по известным числом
атомов (молекул):
.
Например,
определим количество вещества
молекулярного кислорода, которая
содержит 3,01 · 1023
молекул кислорода:.
.
.
Количество вещества определяется числом
структурных единиц (атомов, молекул,
ионов или других частиц) этого вещества.
Количество вещества обозначается
буквой.
9.
Уравнение Менделеева- Клайперона.
PV=(m/M)RT,
где R-
универсальная газовая постоянная,
равная 8,31 Дж/(К*моль)
10.
Эквивалент. Закон эквивалентов.
Эквивалент-
часть вещества, реагирующая без остатка
с одним эквивалентом водорода или вообще
с одним эквивалентом любого другого
вещества.
Закон
эквивалентов: «Вещества
взаимодействуют друг с другом в
эквивалентных количествах» , или «массы
реагирующих веществ пропорциональны
их эквивалентам либо эквивалентным
массам (объемам): m1/m2=
Э1/Э2».
11.
Значения эквивалентов водорода и
кислорода.
Эm(Н2)=1
г/экв
Эm(О2)=
8 г/экв
12.
Молярная масса эквивалента, молярный
объем эквивалента.
Молярная
масса эквивалента элемента в соединении
не является величиной постоянной,
зависит от валентности элемента в данном
соединении и выражается уравнением:

где
М – молярная масса элемента, г/моль; Z –
валентность элемента в данном соединении;
1/z – фактор эквивалентности
Эквивалентный
объем или объем моля эквивалента Vэ(X)
– это объем, который занимает один моль
эквивалентов газообразного вещества
при нормальных условиях (н.у.).
13.
Эквивалент кислоты, основания, соли.
Кислоты:
определяется отношением Mr
основания к числу атомов водорода в
формуле кислоты, способных заместиться
на металл (основность кислоты). Например
эквивалент серной кислоты Н2SO4=
98/2= 49 (1/2*М)
Основания:
определяется отношением Mr
основания к числу гидроксильтных групп
ОН в формуле основания, способных
заместиться на кислотный остаток
(кислотность основания). Например,
эквивалент едкого натра равен ЭNaOH=
40/1= 40, т.е. у этого вещества значения
эквивалента и молекулярной массы
совпадают. (1/3*М)
Соли:
определяется как частное от деления Mr
соли на суммарный заряд катионов. Так,
эквивалент сульфата аллюминия ЭAl2SO4=
342/6= 57. (М/ сумм. Заряд)
Оксида:
равен сумме эквивалентов кислорода и
элемента, образующего данный оксид.
Например, эквивалент оксида аллюминия
равен: Al2O3=
ЭAl+
ЭО. Поскольку алюминий трехвалентен,
то ЭAl=
ArAl/B=
27/3=9, следовательно, ЭAl2O3=
9+8=17. Тоже получим, разделив Mr
оксида на суммарный заряд катионов
металла: 102/6=17.
14.
Закон Авогадро. Следствия из закона
Авогадро.
Закон:
«В равных объемах любых газов при
одинаковых условиях содержится одинаковое
число молекул» .
Следствия:
—
одинаковое число молекул различных
газов при одинаковых условиях ( давлении
и температуре) занимает одинаковый
объем.
—
один моль любого газа при определенных
условиях занимает постоянный объем.
15.
Строение атома: модель Томпсона.
В
атоме Томсона положительное электричество
«размазано» по сфере, в которую вкраплены,
как изюм в пудинг, электроны. В простейшем
атоме водорода электрон находится в
центре положительно заряженной сферы.
При смещении из центра на электрон
действует квазиупругая сила
электростатического притяжения, под
действием которой электрон совершает
колебания. Частота этих колебаний
определяется радиусом сферы, зарядом
и массой электрона, и если радиус сферы
имеет порядок радиуса атома, частота
этих колебаний совпадает с частотой
колебания спектральной линии атома. В
многоэлектронных атомах электроны
располагаются по устойчивым конфигурациям,
рассчитанным Томсоном. Томсон считал
каждую такую конфигурацию определяющей
химические свойства атомов. Он предпринял
попытку теоретически объяснить
периодическую систему элементов Д. И.
Менделеева. Эту попытку Бор позднее
назвал «знаменитой» и указал, что со
времени этой попытки «идея о разделении
электронов в атоме на группы сделалась
исходным пунктом и более новых воззрений».
Отметив, что теория Томсона оказалась
несовместимой с опытными фактами, Бор
тем не менее считал, что эта теория
«содержит много оригинальных мыслей и
оказала большое влияние на развитие
атомной теории».
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·1023 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·1023 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·1023).
Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·1023 атомов. Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·1023 молекул. Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
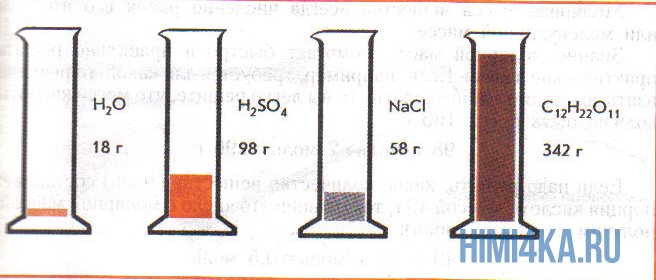
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·1023; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·1023 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·1023 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·1023 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·1023 × 0,25 = 1,505·1023 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·1023 молекул/моль, что равно 2,99·1026 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.