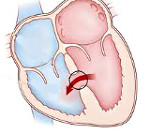
Дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки – врожденная внутрисердечная аномалия, характеризующаяся наличием сообщения между правым и левым желудочками. Дефект межжелудочковой перегородки проявляется одышкой, отставанием в физическом развитии, быстрой утомляемостью, учащенным сердцебиением, наличием «сердечного горба». Инструментальная диагностика дефекта межжелудочковой перегородки включает проведение ЭКГ, ЭхоКГ, рентгенографии органов грудной клетки, вентрикулографии, аортографии, катетеризации камер сердца, МРТ. При дефектах межжелудочковой перегородки проводят радикальные (закрытие дефекта) и паллиативные (сужение легочной артерии) вмешательства.
Общие сведения
Дефект межжелудочковой перегородки (ДМЖП) – отверстие в перегородке, разделяющей полости левого и правого желудочка, наличие которого приводит к патологическому шунтированию крови. В кардиологии дефект межжелудочковой перегородки – наиболее часто встречающийся врожденный порок сердца (9–25% от всех ВПС). Частота критических состояний при дефекте межжелудочковой перегородки составляет около 21%. С одинаковой частотой порок обнаруживается у новорожденных мальчиков и девочек.
Дефект межжелудочковой перегородки может быть единственной внутрисердечной аномалией (изолированный ДМЖП) или входить в структуру сложных пороков (тетрады Фалло, общего артериального ствола, транспозиции магистральных сосудов, атрезии трехстворчатого клапана и др.). В ряде случаев межжелудочковая перегородка может отсутствовать полностью — такое состояние характеризуется как единственный желудочек сердца.
Дефект межжелудочковой перегородки
Причины ДМЖП
Чаще всего дефект межжелудочковой перегородки является следствием нарушения эмбрионального развития и формируется у плода при нарушениях закладки органов. Поэтому дефекту межжелудочковой перегородки часто сопутствуют другие сердечные пороки: открытый артериальный проток (20%), дефект межпредсердной перегородки (20%), коарктация аорты (12%), стеноз устья аорты (5%), аортальная недостаточность (2,5—4,5%), недостаточность митрального клапана (2%), реже — аномальный дренаж легочных вен, стеноз легочной артерии и др.
В 25-50% случаев дефект межжелудочковой перегородки сочетается с пороками развития внесердечной локализации — болезнью Дауна, аномалиями развития почек, расщелиной твердого неба и заячьей губой.
Непосредственными факторами, вызывающими нарушение эмбриогенеза, выступают вредные воздействия на плод в I триместре гестации: заболевания беременной (вирусные инфекции, эндокринные нарушения), алкогольная и лекарственная интоксикации, ионизирующая радиация, патологическое течение беременности (выраженные токсикозы, угроза самопроизвольного прерывания беременности и пр.). Имеются данные о наследственной этиологии дефекта межжелудочковой перегородки. Приобретенные дефекты межжелудочковой перегородки могут являться осложнением инфаркта миокарда.
Особенности гемодинамики
Межжелудочковая перегородка образует внутренние стенки обоих желудочков и составляет примерно 1/3 площади каждого из них. Межжелудочковая перегородка представлена мембранозным и мышечным компонентами. В свою очередь, мышечный отдел состоит из 3-х частей — приточной, трабекулярной и отточной (инфундибулярной).
Межжелудочковая перегородка, наряду с другими стенками желудочков, принимает участие в сокращении и расслаблении сердца. У плода она полностью формируется к 4-5-ой неделе эмбрионального развития. Если этого по каким-либо причинам не происходит, в межжелудочковой перегородке остается дефект. Нарушения гемодинамики при дефекте межжелудочковой перегородки обусловлены сообщением левого желудочка с высоким давлением и правого желудочка с низким давлением (в норме в период систолы давление в левом желудочке в 4 — 5 раз выше, чем в правом).
После рождения и установления кровотока в большом и малом кругах кровообращения из-за дефекта межжелудочковой перегородки возникает лево-правый сброс крови, объем которого зависит от размеров отверстия. При небольшом объеме шунтируемой крови давление в правом желудочке и легочных артериях остается нормальным либо незначительно повышается. Однако при большом поступлении крови через дефект в малый круг кровообращения и ее возврате в левые отделы сердца, развивается объемная и систолическая перегрузка желудочков.
Значительное повышение давления в малом круге кровообращения при больших дефектах межжелудочковой перегородки способствует возникновению легочной гипертензии. Повышение легочно-сосудистого сопротивления взывает развитие сброса крови из правого желудочка в левый (обратного или перекрестного шунтирования), что приводит к артериальной гипоксемии (синдром Эйзенменгера).
Многолетняя практика кардиохиругов показывает, что наилучших результатов закрытия дефекта межжелудочковой перегородки можно добиться при сбросе крови слева направо. Поэтому при планировании операции тщательно учитываются гемодинамические параметры (давление, сопротивление и объем сброса).
Классификация
Размер дефекта межжелудочковой перегородки оценивается, исходя из его абсолютной величины и сопоставления с диаметром аортального отверстия: маленький дефект составляет 1-3 мм (болезнь Толочинова–Роже), средний – равен примерно 1/2 диаметра аортального отверстия, большой – равен или превышает его диаметр.
С учетом анатомического расположения дефекта выделяют:
- перимембранозные дефекты межжелудочковой перегородки — 75% (приточные, трабекулярные, инфундибулярные) расположены в верхней части перегородки под аортальным клапаном, могут закрываться самопроизвольно;
- мышечные дефекты межжелудочковой перегородки – 10% (приточные, трабекулярные) — расположены в мышечном отделе перегородки, на значительном удалении от клапанной и проводящей систем;
- надгребневые дефекты межжелудочковой перегородки — 5% — расположены выше наджелудочкового гребня (мышечного пучка, отделяющего полость правого желудочка от его выносящего тракта), самопроизвольно не закрываются.
Симптомы ДМЖП
Клинические проявления больших и малых изолированных дефектов межжелудочковой перегородки различны. Малые дефекты межжелудочковой перегородки (болезнь Толочинова—Роже) имеют диаметр менее 1 см и встречаются в 25-40% от числа всех ДМЖП. Проявляются нерезко выраженной утомляемостью и одышкой при нагрузке. Физическое развитие детей, как правило, не нарушено. Иногда у них определяется слабо выраженное куполообразное выпячивание грудной клетки в области сердца — «сердечный горб». Характерным клиническим признаком малых дефектов межжелудочковой перегородки служит аускультативно выявляемое наличие грубого систолического шума над областью сердца, который фиксируется уже на первой неделе жизни.
Большие дефекты межжелудочковой перегородки, имеющие размеры более 1/2 диаметра устья аорты или более 1 см, проявляются симптоматически уже в первые 3 месяца жизни новорожденных, приводя в 25-30% случаев к развитию критического состояния. При больших дефектах межжелудочковой перегородки отмечается гипотрофия, одышка при физической нагрузке или в покое, повышенная утомляемость. Характерны затруднения при кормлении: прерывистое сосание, частые отрывы от груди, одышка и бледность, потливость, пероральный цианоз. В анамнезе у большинства детей с дефектом межжелудочковой перегородки — частые респираторные инфекции, затяжные и рецидивирующие бронхиты и пневмонии.
В возрасте 3-4-лет, по мере нарастания сердечной недостаточности, у таких детей появляются жалобы на сердцебиение и боли в области сердца, склонность к носовым кровотечениям и обморокам. Транзиторный цианоз сменяется постоянным пероральным и акроцианозом; беспокоит постоянная одышка в покое, ортопноэ, кашель (синдром Эйзенменгера). На наличие хронической гипоксии указывают деформация фаланг пальцев и ногтей («барабанные палочки», «часовые стекла»).
При обследовании выявляется «сердечный горб», развитый в меньшей или большей степени; тахикардия, расширение границ сердечной тупости, грубый интенсивный пансистолический шум; гепатомегалия и спленомегалия. В нижних отделах легких выслушиваются застойные хрипы.
Диагностика
К методам инструментальной диагностики дефекта межжелудочковой перегородки относятся ЭКГ, ФКГ, рентгенография грудной клетки, ЭхоКС, катетеризация камер сердца, ангиокардиография, вентрикулография.
Электрокардиограмма при дефекте межжелудочковой перегородки отражает перегрузку желудочков, наличие и степень выраженности легочной гипертензии. У взрослых больных могут регистрироваться аритмии (экстрасистолия, мерцание предсердий), нарушения проводимости (блокада правой ножки пучка Гиса, синдром WPW). Фонокардиография фиксирует высокочастотный систолический шум с максимумом в III-IV межреберье слева от грудины.
Эхокардиография позволяет выявить дефект межжелудочковой перегородки или заподозрить его по характерным нарушениям гемодинамики. Рентгенография органов грудной клетки при больших дефектах межжелудочковой перегородки обнаруживает усиление легочного рисунка, усиленную пульсацию корней легких, увеличение размеров сердца. Зондирование правых полостей сердца выявляет повышение давления в легочной артерии и правом желудочке, возможность проведения катетера в аорту, повышенную оксигенацию венозной крови в правом желудочке. Аортография проводится для исключения сопутствующих ВПС.
Дифференциальная диагностика дефекта межжелудочковой перегородки проводится с открытым атриовентрикулярным каналом, общим артериальным стволом, дефектом аортолегочной перегородки, изолированным стенозом легочной артерии, стенозом аорты, врожденной митральной недостаточностью, тромбоэмболией.
Лечение дефекта межжелудочковой перегородки
Асимптомное течение дефекта межелудочковой перегородки при его небольших размерах позволяет воздержаться от хирургического вмешательства и осуществлять динамическое наблюдение за ребенком. В ряде случаев возможно спонтанное закрытие дефекта межжелудочковой перегородки к 1-4 годам жизни или в более позднем возрасте. В остальных случаях показано хирургическое закрытие дефекта межжелудочковой перегородки, как правило, после достижения ребенком 3-х лет.
При развитии сердечной недостаточности и легочной гипертензии проводится консервативное лечение с помощью сердечных гликозидов, мочегонных препаратов, ингибиторов ангиотензинпревращающего фермента, кардиотрофиков, антиоксидантов.
Кардиохирургическое лечение дефекта межжелудочковой перегородки может быть радикальным и паллиативным. К радикальным операциям относятся ушивание малых дефектов межжелудочковой перегородки П-образными швами; пластика больших дефектов синтетической (тефлон, дакрон и др.) заплатой или биологической (консервированный ксеноперикард, аутоперикард) тканью; рентгенэндоваскулярная окклюзия дефекта межжелудочковой перегородки.
У грудных детей с выраженной гипотрофией, большим лево-правым шунтированием крови и множественными дефектами предпочтение отдается паллиативной операции, направленной на создание искусственного стеноза легочной артерии с помощью манжетки. Данный этап позволяет подготовить ребенка к радикальной операции по устранению дефекта межжелудочковой перегородки в более старшем возрасте.
Течение беременности при ДМЖП
Женщины с небольшим дефектом межжелудочковой перегородки, как правило, в состоянии нормально выносить и родить ребенка. Однако, при больших размерах дефекта, аритмии, сердечной недостаточности или легочной гипертензии риск осложнений во время беременности значительно повышается. Наличие синдрома Эйзенменгера является показанием для искусственного прерывания беременности. У женщин с дефектом межжелудочковой перегородки имеется повышенная вероятность рождения ребенка с аналогичным или другим врожденным пороком сердца.
Перед планированием беременности пациентке с пороком сердца (оперированным или нет) необходимо проконсультироваться с акушером-гинекологом, кардиологом, генетиком. Ведение беременности у категории женщин с дефектом межжелудочковой перегородки требует повышенного внимания.
Прогноз
Естественное течение дефекта межжелудочковой перегородки в целом не позволяет надеяться на благоприятный прогноз. Продолжительность жизни при данном пороке зависит от величины дефекта и составляет в среднем около 25 лет. При больших и средних дефектах 50-80% детей умирают в возрасте до 6 мес. или 1 года от сердечной недостаточности, застойной пневмонии, бактериального эндокардита, нарушений ритма сердца, тромбоэмболических осложнений.
В редких случаях ДМЖП не оказывает существенного влияния на продолжительность и качество жизни. Спонтанное закрытие дефекта межжелудочковой перегородки наблюдается в 25-40% случаев, преимущественно при его малом размере. Однако даже в этом случае больные должны находиться под наблюдением кардиолога в связи с возможными осложнениями со стороны проводящей системы сердца и высоким риском возникновения инфекционного эндокардита.
Дефект межжелудочковой перегородки — лечение в Москве
Дата публикации 17 января 2023Обновлено 28 февраля 2023
Определение болезни. Причины заболевания
Дефект межпредсердной перегородки (Atrial septal defect) — это врождённый порок сердца, при котором в межпредсердной перегородке образуется отверстие. Через него кровь поступает из левого предсердия в правое, из-за чего сосуды лёгких получают больше крови, чем нужно.
Дефект межпредсердной перегородки (ДМПП) составляет примерно 7 % от всех врождённых пороков сердца и является одним из самых частых пороков у детей старше 3 лет [1].
ДМПП часто протекает бессимптомно, поэтому может долго оставаться незамеченным. У некоторых пациентов этот дефект может приводить к одышке и быстрой утомляемости при физической нагрузке. Также родители детей с ДМПП указывают на частые респираторные заболевания, умеренную задержку физического развития и повышенную потливость у ребёнка. С возрастом могут появиться жалобы на перебои в работе сердца (аритмии).
ДМПП могут различаться размерами, формой и расположением. Дефекты могут располагаться в разных отделах межпредсердной перегородки, а по размеру бывают как совсем маленькими, так и очень большими, вплоть до полного отсутствия перегородки, т. е. объединения двух предсердий в одно. Также у пациента может быть несколько ДМПП или этот дефект может сопровождать другие врождённые пороки сердца.
Причины дефекта межпредсердной перегородки
ДМПП формируется во время эмбрионального развития, поэтому в группу риска попадают генетически предрасположенные новорождённые, т. е. если у кого-то из близких кровных родственников был порок сердца. Также на формирование дефекта может повлиять:
- экология;
- инфекционные заболевания, сильный токсикоз, угроза выкидыша, сахарный диабет у матери во время беременности (в том числе гестационный СД);
- употребление наркотиков или алкоголя родителями ребёнка [1][2][10].
Открытое овальное окно и ДМПП: в чём разница
Иногда возникает путаница в определениях открытого овального окна и дефекта межпредсердной перегородки. Открытое овальное окно — это норма при внутриутробном развитии. По размеру оно не превышает 5–6 мм, размер ДМПП больше. Ребёнок рождается с этим отверстием, в норме оно должно закрыться в первый год жизни, но может остаться открытым до 5–6 лет, а у 20 % пациентов сохраняется на всю жизнь — в таком случае может потребоваться лечение [13].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы дефекта межпредсердной перегородки
ДМПП может долго протекать бессимптомно, а его проявления могут быть разнообразными, поэтому дефект часто не распознают сразу, а выявляют уже при выраженных симптомах либо в подростковом или взрослом возрасте. В первые месяцы жизни ДМПП может проявляться только утомляемостью и посинением носогубного треугольника при плаче младенца.
При небольшом дефекте (10–15 мм) симптомы проявляются ближе к 20–30 годам. До этого никаких жалоб или нарушения физического развития может не быть. У взрослого пациента может проявиться одышка, нарушение сердечного ритма (аритмия), посинение носогубного треугольника и других участков кожи [1][5][8].
При ДМПП повышен объём крови в малом круге кровообращения, из-за чего могут чаще возникать, дольше и тяжелее проходить респираторные заболевания: бронхит и пневмония, которые сопровождаются влажными хрипами, кашлем и одышкой. У детей школьного возраста ДМПП может проявляться склонностью к обморокам и головокружению, одышкой, быстрой утомляемостью при физических упражнениях и даже небольших нагрузках. На эти симптомы обычно указывают родители ребёнка.
При средних и больших дефектах симптомы могут ярко проявиться уже к полугоду и концу первого года жизни. На ДМПП будет указывать отставание в физическом развитии, бледность кожи, недостаточный набор веса, одышка и учащённое сердцебиение (тахикардия). Проявления сердечной недостаточности при ДМПП незначительны и могут ограничиваться умеренной слабостью, потливостью и бледностью кожи. В некоторых случаях со временем развивается лёгочная гипертензия, при которой повышено давление в лёгочной артерии. При больших дефектах (равных примерно половине от всей длины межпредсердной перегородки) увеличивается печень и появляются отёки ног.
Патогенез дефекта межпредсердной перегородки
Чтобы понять, как работает кровеносная система, рассмотрим циркуляцию крови в здоровом сердце.
Сердце разделено перегородками на четыре камеры: две правые — правое предсердие и правый желудочек, и две левые — левое предсердие и левый желудочек. Предсердия и желудочки соединены клапанами, которые регулируют ток крови из предсердия в желудочек.
Правое предсердие и желудочек собирают венозную кровь, которая поступает из всех органов и тканей. Она тёмно-бордового цвета, содержит мало кислорода и много углекислоты. Правый желудочек выталкивает эту кровь в лёгочную артерию, и вся венозная кровь поступает в артерии и капилляры лёгких, где методом диффузии насыщается кислородом и очищается от углекислоты. Кровь обогащается кислородом, становится более красной и поступает в левое предсердие по четырём лёгочным венам. На этом заканчивается малый круг кровообращения и начинается большой.
Из левого предсердия кровь поступает в левый желудочек, а оттуда после мощного сокращения расходится по аорте и её ответвлениям в органы и ткани. Когда кровь отдаст весь кислород органам, тканям и капиллярам, она снова станет венозной. Венозные капилляры соединяются в более толстые вены, которые в итоге образуют верхнюю и нижнюю полые вены. Верхняя полая вена переносит кровь от головы, рук и стенок туловища, а нижняя — от ног, органов брюшной полости и таза. Верхняя и нижняя полые вены приносят кровь в правое предсердие. На этом заканчивается большой круг кровообращения.
При ДМПП происходит избыточный сброс крови из левого предсердия в правое — через отверстие в перегородке кровь, насыщенная кислородом, находит дополнительный выход в правое предсердие. Малый круг кровообращения при этом перенасыщается кровью, что дополнительно нагружает правое предсердие и заставляет усиленно работать правый желудочек. При длительном переполнении кровью малого круга повышается давление в лёгочной артерии, из-за чего в пожилом возрасте может развиться обструктивная болезнь лёгочных сосудов, что может проявляться постоянной синюшностью кожи, даже в покое.
Классификация и стадии развития дефекта межпредсердной перегородки
Дефекты межпредсердной перегородки подразделяются:
- на открытое овальное окно;
- первичный и вторичный дефект межпредсердной перегородки;
- дефект венозного синуса: верхний и нижний;
- дефект коронарного синуса (обескрышенный коронарный синус).
Открытое овальное окно — это норма при внутриутробном развитии. Лёгкие у плода ещё не раскрыты и не работают, поэтому кровь проходит в овальное окно и замыкает малый круг кровообращения. В норме оно закрывается в первые 2–3 недели после рождения, но это может произойти и позже — в возрасте до 5–6 лет.
Если открытое овальное окно выявлено на УЗИ после этого возраста и сопровождается симптомами, то может потребоваться хирургическое вмешательство.
Первичный дефект возникает из-за недоразвития первичной перегородки у эмбриона (межпредсердная перегородка развивается в два этапа: сначала нарастает первый листок — первичная перегородка, потом параллельно ей растёт вторичная перегородка). Типичное расположение первичного дефекта — на уровне фиброзного кольца атриовентрикулярных клапанов. Фиброзные кольца митрального и трикуспидального клапанов становятся нижней стенкой дефекта. Дефект иногда сочетается с другими пороками, такими как расщепление митрального или трикуспидального клапанов и атриовентрикулярным каналом. В таких случаях признаки сердечной недостаточности проявятся раньше и пациентам потребуется консервативная терапия либо ранняя коррекция порока.
Вторичный дефект чаще всего встречается среди врождённых пороков сердца. Он возникает из-за нарушений развития вторичной перегородки у эмбриона. Такой дефект легче всего переносится пациентом.
Дефект венозного синуса расположен на задней стороне перегородки возле верхней или нижней полой вены. Он часто связан с аномальным возвратом крови из правой верхней или нижней лёгочной вены в правое предсердие или полую вену. Кровообращение при таком дефекте примерно такое же, как при больших ДМПП. При лечении, помимо устранения дефекта, ещё выполняется коррекция аномального дренажа лёгочных вен — врождённого порока, при котором одна или несколько лёгочных вен впадают в правое предсердие, либо в полые вены, либо в их основные ветви.
Дефект коронарного синуса (обескрышенный коронарный синус) — это дефект стенки коронарного синуса, при котором происходит сброс крови из левого предсердия в коронарный синус, а затем в правое предсердие. Такой дефект часто протекает бессимптомно. Составляет 10 % от всех вариантов ДМПП [2]. При наличии значимого сброса крови через дефект устраняется только хирургическим путём.
При выявлении любого типа ДМПП проводится дополнительное обследование и может потребоваться хирургическое лечение [2][9][10].
Осложнения дефекта межпредсердной перегородки
При длительно существующем ДМПП может возникнуть аритмия, при которой спонтанно на некоторое время учащается сердцебиение, затем ритм также внезапно снова становится нормальным. Также может возникнуть трепетание предсердий, что сопровождается частым регулярным ритмом, из-за чего ухудшается общее самочувствие, повышается утомляемость, появляется одышка и непереносимость физической нагрузки. Кроме того, может развиться фибрилляция предсердий, при которой сердце сокращается то быстрее, то медленнее, что также доставляет беспокойство пациенту. В основном все эти симптомы появляются после 20–40 лет [2][10].
В дальнейшем из-за постоянного повышения давления и сопротивления в лёгочной артерии кровь протекает как в соседнее предсердие, так и обратно, что сопровождается синдромом Эйзенменгера. При этом осложнении возникает нехватка кислорода, могут быть обмороки, повышенная утомляемость, головокружение, одышка, боль в груди, синюшность кожи и слизистых (эти признаки могут быть как в покое, так и при физической нагрузке). При развитии этого осложнения необходимо как можно скорее лечь в стационар на обследование, так как состояние опасно для жизни.
Диагностика дефекта межпредсердной перегородки
При диагностике ДМПП проводится сбор анамнеза (истории болезни), аускультация (выслушивание сердца), электрокардиография (ЭКГ) и эхокардиография (ЭхоКГ).
Сбор анамнеза
При обследовании ребёнка врач уточняет у родителей, были ли врождённые пороки сердца у ближайших родственников и как протекала беременность у матери. Также он спрашивает об одышке, сбоях ритма сердца, утомляемости и частых заболеваниях у ребёнка. Медленный набор веса тоже является симптомом ДМПП.
Аускультация сердца
Первый и самый простой метод — это выслушивание сердца. Врач может услышать шумы и сбой ритма и назначить инструментальное обследование, чтобы подтвердить диагноз.
Инструментальная диагностика
- Электрокардиография (ЭКГ) — показывает отклонения в частоте и регулярности сокращений сердца, позволяет диагностировать аритмию и перегрузку правого предсердия и желудочка.
- Эхокардиография (ЭхоКГ) — ультразвуковой метод, позволяющий выявить точное расположение дефекта и изменение камер сердца, чтобы определиться с тактикой лечения. С помощью цветной допплерографии определяют сброс крови и вычисляют систолическое давление в правом желудочке. Эхокардиография также помогает выявить дополнительные пороки, определить вид ДМПП, направление сброса крови и соотношение лёгочного и системного кровотока (Qp/Qs). Разновидностью эхокардиографии является чреспищеводная ЭхоКГ. Она проводится у взрослых пациентов, чтобы уточнить информацию о расположении и краях дефекта, что в дальнейшем помогает подобрать подходящий метод лечения.
- Рентгенография органов грудной клетки показывает деформацию ствола лёгочной артерии, гипертрофию сердца и усиление лёгочного рисунка.
Если перечисленных методов недостаточно для получения полной информации о дефекте и выбору метода лечения, проводится зондирование камер сердца — исследование его камер и ближайших больших сосудов с помощью катетера.
На основе проведённых исследований кардиолог, кардиохирург и врачи других специальностей (если это необходимо) подбирают метод лечения дефекта, в том числе оперативный [1][2][10].
Дифференциальная диагностика
Симптомы ДМПП похожи на многие дефекты с перенасыщением малого круга кровью (гиперволемией), поэтому только по клинической картине этот порок нельзя отличить от других заболеваний. Определить тип порока врач может после проведения ЭхоКГ.
Лечение дефекта межпредсердной перегородки
При небольших ДМПП обычно нет симптомов и не требуется терапия. Пациенты наблюдаются у кардиолога по месту жительства и проходят ЭхоКГ не реже одного раза в год [1].
При большом дефекте, приводящем к изменению кровотока, возможно только хирургическое лечение. При значимых дефектах показанием к коррекции является гиперволемия малого круга кровообращения и риск развития лёгочной гипертензии.
Выбор метода зависит от вида и свойств дефекта, а также от наличия сопутствующих врождённых пороков сердца. При симптомах сердечной недостаточности сперва может быть назначено консервативное лечение.
Суть любого метода лечения состоит в закрытии дефекта. После сбора анамнеза и обследования врач может назначить лечение одним из перечисленных методов:
- Классический метод — открытая операция с доступом к сердцу через грудину. Проводится с подключением аппарата искусственного кровообращения, сердце при этом кровью не снабжается. Дефект ушивается, если это возможно, если нет — накладывается заплата, чаще из бычьего перикарда [1][2][8]. После операции пациент восстанавливается примерно 7–10 дней.
- Миниинвазивная операция через боковую торакотомию по средней подмышечной линии — это щадящая открытая операция с небольшим доступом (4–6 см) на правой стороне грудной клетки. Отличается от классического метода быстрым восстановлением (5–7 дней) и менее заметным рубцом [3].
- Робот-ассистированное торакоскопическое вмешательство — операция, которая проводится хирургическим комплексом Da Vinci с помощью нескольких проколов грудной клетки. Этот метод позволяет пациенту восстановиться быстрее, чем при классической операции (примерно через 4–5 дней) [4]. Однако комплекс Da Vinci есть не во всех центрах и, учитывая высокую стоимость такого лечения, предпочтение обычно отдаётся транскатетерному способу закрытия дефекта.
- Эндоваскулярное вмешательство — проводится через прокол в бедренной вене с помощью системы специальных внутрисосудистых устройств (катетеров). Через эту систему в дефект устанавливают окклюдер — специальное устройство в виде «зонтика» или «шпульки», которое в сложенном состоянии проводится до дефекта и раскрывается по типу зонтика, закрывая отверстие. Эндоваскулярное вмешательство выполняется под рентгенологическим контролем и не требует общего наркоза [10]. Примерно 70–80 % изолированных вторичных ДМПП могут быть закрыты этим способом. Восстановление после операции проходит достаточно быстро: через 1–3 дня пациент может быть выписан из стационара.
Показания и противопоказания к операциям
Открытая операция противопоказана при малом диаметре дефекта, тяжёлой стадии лёгочной гипертензии, смене направления сброса через дефект, дополнительных нарушениях в малом и большом кругах кровообращения.
Для эндоваскулярного вмешательства противопоказанием является ДМПП с частичным дренажем лёгочных вен, дефекты большого размера (более 4–5 см) или без нижнего края. Если ДМПП сочетается с другими патологиями, требуется классическая открытая операция.
В каждом конкретном случае происходит коллегиальная оценка и определяется оптимальный способ коррекции, с учётом всех особенностей пациента. Подробнее о показаниях и противопоказаниях лечащий врач расскажет во время консультации и обследования.
Реабилитация и диспансерное наблюдение после хирургического лечения
Если после операции сохранилась остаточная лёгочная гипертензия и/или есть признаки недостаточности кровообращения, пациенту рекомендуется в течение трёх месяцев пройти восстановительное лечение в кардиологическом санатории или реабилитационном центре.
После операции кардиолога нужно посетить через месяц, полгода и год. Диспансерное наблюдение включает ЭКГ, ЭхоКГ и при необходимости тесты с дозированной физической нагрузкой и пульсоксиметрию. Дальнейшее наблюдение при наличии показаний проводится с интервалом 12 месяцев и больше [1].
После установки окклюдера рекомендуется пройти ЭхоКГ, чтобы определить положение устройства и исключить осложнения. ЭхоКГ в таком случае выполняется через 24 часа после операции, затем через месяц, полгода и год с последующими регулярными обследованиями, назначенными лечащим врачом.
После транскатетерного закрытия ДМПП рекомендуется в течение шести месяцев применять ингибиторы агрегации тромбоцитов.
Прогноз. Профилактика
Примерно 15–30 % вторичных ДМПП размером до 6 мм спонтанно закрываются в раннем детстве [1]. Если к 5–6-летнему возрасту этого не происходит, рекомендуется проконсультироваться с кардиохирургом, чтобы определить сроки и подобрать метод оперативного лечения. Лучше всего дети восстанавливаются при операции, перенесённой в возрасте от 2 до 6 лет. Продолжительность жизни пациентов после коррекции ДМПП такая же, как и у остальных людей.
Вторичный ДМПП протекает благоприятно до 20–30 лет, но без лечения средняя продолжительность жизни составляет 36–40 лет.
Пациентам с ДМПП (оперированным или нет) нужно всю жизнь периодически посещать кардиолога.
Малые дефекты, которые, тем не менее, не закрылись в детстве, во взрослом и пожилом возрасте могут проявляться симптомами. Поэтому обследование сердца нужно проводить на первом году жизни ребёнка вне зависимости от предрасположенности к ДМПП [1][2][4][7].
Искривление носовой перегородки — очень распространенная проблема. Она встречается (по разным данным) примерно у 60-90% населения. К чему может привести легкомысленное отношение к этому дефекту? Можно ли вылечиться без операции? И какие страхи излишни?
Мы задали 15 распространенных вопросов врачу-оториноларингологу медицинского центра «Нордин».
Сергей Ешенко
врач-оториноларинголог первой квалификационной категории
медицинского центра «Нордин»
1. По каким причинам происходит искривление перегородки?
— Выделяют три основных причины:
1. Физиологическая причина — самая частая.
Перегородка носа состоит из переднего (хрящевого) и заднего (костного) отделов. Во время периода полового созревания рост хрящевой и костной тканей в носу прекращается, при этом передний и задний отдел должны правильно упереться друг в друга. Но ключевое здесь именно слово «правильно». К сожалению, так бывает крайне редко.
2. Посттравматическая — более редкая причина.
Это деформация из-за внешнего воздействия, то есть из-за полученной травмы.
3. Компенсаторная. Когда перегородка искривляется из-за наличия в носу инородного тела, полипов и вследствие определенных заболеваний.
2. Искривленную перегородку можно определить визуально?
— Это зависит от того, в каком отделе носа проблема. Если говорить об искривлении в переднем отделе — да, дефект будет виден невооруженным взглядом как минимум из-за того, что деформируется и кончик носа. Опытный врач это легко заметит.
В случае искривления в заднем отделе визуальной оценки мало. Нос может быть идеально ровным, хотя дефект присутствует. Просто он спрятан от глаз.
3. Проблема может передаваться по наследству?
— Безусловно. Ведь форма носа сама по себе часто передается последующим поколениям. Поэтому, если у родителей, дедушек и бабушек есть проблемы с дыханием, вполне возможно, что они появятся и у младшеньких. Но прямой зависимости нет. Это лотерея.
4. Искривление перегородки чаще встречается у мужчин или у женщин?
— У мужчин. Во-первых, из-за того, что травмы носа, по статистике, у них все же бывают чаще. Во-вторых, крупная форма носа у представителей сильного пола более распространена, а с этим связаны и проблемы с перегородкой.
5. Какие симптомы говорят о том, что у человека искривлена перегородка?
— Наиболее частые признаки — это:
- затруднение носового дыхания с одной или с обеих сторон;
- выделения из носа;
- носовые кровотечения (при значительном искривлении);
- образование корки на слизистой носа (особенно в отопительный сезон и в сухом климате);
- головные боли;
- храп.
6. Если решить проблему с искривленной перегородкой, храп исчезнет?
— Вообще храп — это часть здорового сна. Далеко не всегда стоит его бояться. Даже абсолютно здоровые люди после тяжелого дня могут первые 5-10 минут сна храпеть. Но в фазе глубокого сна все проходит. Тот же сценарий может проиграться и за 5-10 минут до пробуждения.
А вот когда храп длится в течение всего сна или сопровождается остановками дыхания — вот это нехороший «звоночек», на который обязательно стоит обратить внимание.
Конечно, скорее всего, если выровнять перегородку, исчезнет и храп. Но только в том случае, если причина крылась именно в искривлении перегородки. Ведь причин у храпа много. Например, если носовые раковины во время сна отекают и перекрывают доступ воздуха к носоглотке (место, где нос сообщается с горлом). И так далее.
7. Можно ли жить с искривленной перегородкой и не ощущать никакого дискомфорта?
— Да, конечно. Иногда для людей эта проблема становится неожиданностью. Например, во время медицинского обследования.
Отсутствие дискомфорта может наблюдаться даже при выраженной деформации. И если человек чувствует себя хорошо, то и операция ему не требуется.
8. Можно ли эту проблему вылечить без операции?
— Необходимо детальное обследование. Помимо осмотра ЛОРа, пациенту нужно сделать компьютерную томографию либо 3D-исследование околоносовых пазух.
В некоторых случаях врач действительно сперва назначает консервативное лечение и специальные препараты, физиопроцедуры, изменение режима дня и так далее.
Операция необходима в тех случаях, когда, например, кроме искривления перегородки, наблюдаются изменения в пазухах носа, вторичный синусит, признаки изменений слизистой оболочки носа и при других сопутствующих проблемах. Тем не менее, решение остается за пациентом, так как операция не входит в число неотложных.
9. А если не лечиться, какими могут быть последствия?
— В таком случае возможно развитие вторичных заболеваний полости носа. Прежде всего — это хронический синусит и хронический гнойный синусит, а также образование кист и полипов. Причем если пациент отказывается вовремя делать операцию даже при настоятельном совете врача, то запоздалое оперативное вмешательство впоследствии, скорее всего, не поможет ему убрать симптомы хронического синусита. В общем, самое главное — не допустить хроники.
10. Операция по исправлению носовой перегородки — это сложная операция?
— Да, операция, которая называется септопластика, действительно относится к категории сложных. Она представляет собой удаление части хрящевой и/или костной перегородки носа под слизистой оболочкой.
Многие пациенты опасаются именно того, что им будут что-то ломать. На самом деле задача врачей — очень нежно и аккуратно с помощью специальных инструментов поднять слизистую оболочку носа (не повредив ее) и далее, проведя манипуляции над костным, хрящевым отделами, аккуратно ее назад уложить.
Вместе с септопластикой обычно выполняется операция на нижних носовых раковинах (подслизистая вазотомия). Эти действия взаимосвязаны и, как правило, необходимы.
Одновременно могут происходить и другие вмешательства, все зависит от конкретного человека и его индивидуальных проблем.
— Сегодня стало возможным выполнение эндоскопической септопластики, когда операция выполняется под контролем эндоскопа (специального аппарата с камерой). Такой подход позволяет сделать разрез в конкретном месте проблемы, намного уменьшая травматизацию и не затрагивая всю слизистую носа, как в классической операции. Однако подобная операция выполняется строго по показаниям. Провести ее возможно лишь в 30% случаев.
11. Есть ли противопоказания к операции?
— Да, это, например, заболевания крови, заболевания, связанные с нарушением свертываемости крови, гипертония, сахарный диабет. Также мы редко выполняем данные операции пациентам старше 60 лет, ведь при операции возможно сильное кровотечение. Но все эти противопоказания относительные. Каждый случай необходимо разбирать индивидуально.
12. Можно ли операцию делать детям?
— Довольно сложный вопрос. Рост и изменения носовой перегородки продолжаются (по разным данным) до 15-20 лет. Несвоевременное вмешательство может повлечь за собой последствия в виде вторичной деформации перегородки из-за того, что организм продолжает свое физиологическое развитие. Все же лучше делать операцию после 18 лет.
Тем не менее, если есть серьезные проблемы, допустим, нос не дышит вообще либо выявлены вторичные нарушения околоносовых структур, то, конечно, операция показана в любом возрасте. Но стоит помнить, что пациенту необходимо продолжать наблюдаться у ЛОРа. Важно отслеживать дальнейшее состояние перегородки и носа в принципе.
13. Какие есть варианты анестезии?
— Операция может быть выполнена как под местной анестезией, так и под общим наркозом.
Я считаю, что местная анестезия предпочтительнее, так как пациент находится в сознании. Операция похожа на процесс лечения зубов. Человек не чувствует боли, может лишь слышать определенные звуки. Все происходит быстро — около 20-30 минут. И прийти в себя после такой анестезии значительно легче, чем после общего наркоза.
Минусы общего наркоза также в том, что некоторое время человек не сможет дышать сам. Его необходимо подключать к специальному аппарату, который будет дышать за него. Многие пациенты этого боятся, да и сложность операции, конечно, возрастает.
14. Как проходит реабилитация?
— Пациенту рекомендуется минимум сутки находиться в условиях стационара под наблюдением врачей.
Период реабилитации длится примерно 7-10 дней. Первые сутки-двое нос будет закрыт тампонами. Стоит быть готовым к тому, что это время придется дышать ртом. Человека могут беспокоить периодические головные боли, незначительная температура (37,2-37,5 градуса). Возможны также общая слабость и болевой синдром, но последний купируется обезболивающими средствами.
— Кстати, некоторое время после операции ни в коем случае нельзя совершать полеты на самолете из-за резких перепадов давления. Противопоказано также посещение бассейнов, бань и саун. Уточните у врача, в течение какого срока лично вам нужно беречь себя и находиться в покое.
В любом случае, бояться операции не стоит. Организм после нее восстанавливается довольно быстро. Если ваша работа не подразумевает физической активности, вы можете выходить с больничного уже через несколько дней.
15. Эффект от операции сохраняется навсегда?
— Если операция выполнена качественно и нет хронических сопутствующих заболеваний, то, как правило, эффект сохраняется на всю жизнь.
Как я уже говорил, проблемы могут возникнуть, если операция выполнена в подростковом возрасте или если имели место послеоперационные осложнения. Но чаще всего при соблюдении пациентом всех рекомендаций врача и ответственном отношении к собственному здоровью никаких негативных последствий не появляется.
Фото: Александр Задорин

Что такое легочная гипертензия и значение эхокардиографии?
- Эхокардиография показывает, что у пациентов с легочной гипертензией (ЛГ) и легочным сердцем отмечается высокая заболеваемость и смертность.
- На легочное сердце приходится 20% госпитализаций по поводу сердечной недостаточности и 40 000 смертей в год в России.
- Симптомы и физические данные, связанные с легочной гипертензией и легочным сердцем, недостаточно специфичны.
- История болезни и физикальное обследование ограничены в определении этиологии, тяжести и прогноза ЛГ и легочного сердца.
ОПРЕДЕЛЕНИЕ: Легочное сердце – это дилатация правого желудочка, гипертрофия или диастолическая или систолическая дисфункция из-за ЛГ в отсутствии болезни левого сердца.
ОБЩИЕ ЭТИОЛОГИЧЕСКИЕ ФАКТОРЫ ЛЕГОЧНОЙ ГИПЕРТОНИИ
- Облитерирующая: хроническая обструктивная болезнь легких, характеризующаяся разрушением легочных капиллярных пластов.
- Сосудосуживающее: обструктивное апноэ во сне и гиповентиляция от ожирения.
- Обструктивная: острая или хроническая легочная эмболия, на которую приходится более 300 000 случаев легочной гипертонии в России каждый год; также включает первичную легочную (ПЛГ) с частотой двух случаев на миллион и соотношением женщин и мужчин 1,7: 1,0.
- Гиперкинетический: шунтирование слева направо от дефекта межпредсердной или желудочковой перегородки, открытого артериального протока или аномального легочного венозного оттока, приводящего к объему правого желудочка, а затем к перегрузке правого желудочкового давления.
ЭХОКАРДИОГРАФИЯ (ПОКАЗАНИЯ ПРИ ЛГ)
Показания класса I для проведения эхокардиографии
- Трансторакальная эхокардиография (TTЭ) может установить диагноз, степень тяжести и прогноз у пациентов с ЛГ с легочным сердцем или без него.
- TTЭ может дифференцировать острое от хронического легочного сердца и правое заболевание сердца, вторичное по отношению к заболеванию левого сердца.
- Эхокардиография может определить степень дилатации правого желудочка, гипертрофию и его дисфункцию.
- Чреспищеводная эхокардиография (ЧПЭхоКГ) может выявлять крупные проксимальные тромбоэмболии легочной артерии у пациентов с гемодинамически нарушенной функцией правого желудочка.
- ЧПЭхоКГ превосходит ТТЭ в обнаружении и характеристике тромбов в правом предсердии и правом желудочке, что может иметь дополнительное диагностическое значение при внутрисердечных шунтах.
- Внутрисосудистое ультразвуковое исследование обеспечивает гистологическую и функциональную оценку легочной сосудистой системы и помогает дифференцировать первичную легочную гипертензию от хронической тромбоэмболии легочной артерии.
Показания класса I для эхокардиографии при легочной гипертонии и легочном сердце
- Подозревается легочная гипертензия.
- Для различия сердечной и некардиальной этиологии одышки у пациентов, у которых клинические и лабораторные признаки неоднозначны.
- Оценка и наблюдение давления в легочной артерии у пациентов с легочной гипертензией для оценки ответа на лечение.
- Заболевание легких с клиническим подозрением на поражение сердца (подозрение на легочное сердце).
- Отеки с клиническими признаками повышенного центрального венозного давления, когда подозревается потенциальная этиология болезней сердца или когда центральное венозное давление не может быть достоверно оценено, и клиническое подозрение на патологию сердца является высоким.
- Одышка с клиническими признаками порока сердца.
- Пациент с необъяснимой гипотонией, особенно в отделении интенсивной терапии.
- Диагностика и оценка тяжести гемодинамики правосторонней клапанной регургитации.
- Оценка размера, функции и / или гемодинамики правого желудочка у пациента с правосторонней клапанной регургитацией.
- Тромбоэмболия легочной артерии и подозреваемые тромботические сгустки в правом предсердии или желудочке или ветвях основной легочной артерии.
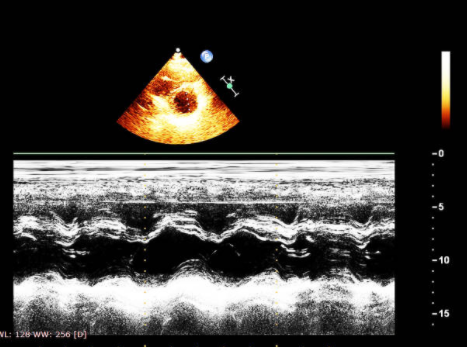
М-режим и двумерная эхокардиография: морфология правого сердца. Лучшие подходы для изучения правых отделов
- Парастернальная позиция ЭхоКГ по длинной и короткой осям, а также апикальные и подреберные четырехкамерные изображения.
- ЧПЭхоКГ из трансгастральной позиции с видом на длинную ось и короткую ось правого желудочка (ПЖ) и средне-пищеводный четырехкамерный вид.
Ключевые диагностические особенности специфических отклонений на эхокардиографии
Правожелудочковая дилатация
- Диастолический диаметр правого желудочка> 3,5 см с парастернальной и подреберной проекций> 4 см и с апикальной четырехкамерной проекции указывает на расширение правого желудочка.
- При легкой дилатации правого желудочка его площадь остается меньше, чем область левого желудочка.
- Соотношение конечного диастолического отдела правого желудочка и левого желудочка <0,6 является нормальным, 0,6-1,0 указывает на легкую дилатацию, а> 1,0 указывает на выраженную дилатацию правого желудочка.
- Верхушка правого желудочка обычно расположена ниже верхушки левого желудочка на одну треть расстояния от основания до вершины. Любое изменение этого признака предполагает расширение правого желудочка.
Гипертрофия правого желудочка на эхокардиографии
- Нормальная свободная стенка ПЖ имеет размеры от 0,2 до 0,5 см в конце диастолы. Гипертрофия правого желудочка (ГПЖ) присутствует, если утолщение свободной стенки правого желудочка превышает 0,5 см.
- ГПЖ является предиктором высокого систолического давления в правом желудочке.
Правожелудочковая систолическая дисфункция
- С помощью контрастных методов установлено, что нормальная фракция выброса правого желудочка составляет ≥40%.
- Систолическая функция правого желудочка на эхокардиографии обычно оценивается визуально.
- Систолическое отклонение кольца трехстворчатого клапана вниз зависит от систолической функции правого желудочка.
- Функция правого желудочка в норме, если отклонение фиброзного кольца к верхушке> 2 см.
- Кольцевая систолическая экскурсия правого желудочка <2 см, <1 см и <0,5 см указывает на легкую, среднюю и тяжелую дисфункцию правого желудочка, соответственно.
Систолическое давление в правом желудочке и объемная перегрузка на эхокардиографии
Высокое систолическое давление в правом желудочке приводит к удлинению фазы выброса, и в результате давление в правом желудочке превышает давление в левом желудочке во время поздней систолы и ранней диастолы. Таким образом, перегрузка правого желудочка приводит к уплощенной или изогнутой перегородке в направлении левого желудочка (ЛЖ) во время поздней систолы и ранней диастолы («D-образный ЛЖ»), которая восстанавливает свою обычную форму во время средней и поздней диастолы. Эта картина движения перегородки наблюдается у пациентов с легочной гипертензией (давление> 45 мм рт. ст.), но может отсутствовать у пациентов с повышенным конечным диастолическим давлением в левом желудочке. При перегрузке объемом правого желудочка смещение перегородки к ЛЖ наблюдается в середине диастолы, так как диастолическое давление превышает таковое в левом желудочке на этой фазе. Во время систолы перепад давления меняется на противоположный, и перегородка восстанавливает свой нормальный контур. Эта картина движения перегородки менее заметна, если сосуществуют перегрузка давлением и объемом. Парадоксальное движение перегородки редко встречается при легкой перегрузке объема и наблюдается у ≤50% пациентов с умеренной перегрузкой объемом. Хроническая перегрузка давлением приводит к дилатации и дисфункции правого желудочка, что ведет к умеренной или тяжелой трикуспидальной регургитации (ТР) и, следовательно, к парадоксальным перегородочным движениям от давления и перегрузки объемом.
Хроническая ЛГ приводит к расширению оттока правого желудочка и легочной артерии (ЛА) (> 3 см). При хронической ЛГ средней тяжести М-режим клапана легочной артерии показывает срединно-систолическое закрытие и потерю нормальной волны А в 30–60% случаев. При стенозе легочного клапана волна А увеличивается, а срединно-систолическое закрытие клапана отсутствует. При остром легочном сердце из-за эмболии в легочные сосуды правый желудочек и толщина его свободной стенки обычно нормальны, но наблюдается общее снижение сократимости. В этом случае могут быть видны правожелудочковые или правые предсердные тромбы.
Тромбы в правых отделах сердца на эхокардиографии
При венозной тромбоэмболии в правом предсердии, ПЖ или ЛА может наблюдаться транзитный тромб. Эти тромбы представляют собой подвижные, нерегулярные и свободно плавающие линейные образования (часто выпадающие через трикуспидальный клапан). Тромб может быть фиксирован к сети Киари или визуализирован через открытое овальное отверстие, ведущее к парадоксальной эмболии. Повреждение эндокарда, связанное с размещением правых катетеров и кардиостимуляторов или автоматических имплантируемых электродов сердечного дефибриллятора, может привести к образованию тромба in situ. На эхокардиографии эти тромбы неподвижны, имеют четкие края и широкое основание и прикреплены к стенке предсердия или катетеру, или к обоим структурам.
Дилатация правого предсердия и легочная гипертония на эхокардиографии
- Увеличение правого предсердия и ЛГ возникают при хроническом давлении в правом желудочке или перегрузке объемом.
- Размер правого предсердия или площадь ≥ левого предсердия указывает на увеличение правого предсердия.
- Право предсердное давление оценивается по диаметру и степени инспираторного коллапса нижней полой вены (НПВ). Правое предсердное давление составляет <5 мм рт. ст., если диаметр НПВ мал (<1,0 см) и она спадается при вдохе; От 5 до 10 мм рт. ст., если НПВ составляет от 1,0 до 1,5 см спадается > 50% при вдохе; От 10 до 15 мм рт.ст., если НПВ ≥1,5 см и коллабирует <50% при вдохе; От 15 до 20 мм рт. ст., Если НПВ> 1,5 см и коллапс <50%; и> 20 мм рт. ст., если печеночные вены расширены и НПВ не спадается при вдохе.
- Неспособность НПВ спадаться на вдохе указывает на давление в правом предсердии> 20 мм рт.
- При тяжелой легочной гипертензии в правом предсердии наблюдается перегиб межпредсердной перегородки в направлении левого предсердия.
- Дилатация печеночных вен и, редко, коронарного синуса, указывает на тяжелую легочную гипертензию в правом предсердии.
Ловушки и ошибки при проведении эхокардиографии
- Ложноположительная дилатация правого желудочка возникает, когда датчик не расположен над верхушкой левого желудочка.
- Ложноотрицательная дилатация правого желудочка может возникнуть при одновременном увеличении ЛЖ.
- Оценка сократимости ПЖ с помощью двумерной визуализации менее надежна, чем в М-режиме, из-за более низкой частоты кадров и, как следствие, снижения разрешения для оценки эндокарда.
- Из-за трудностей в определении внешнего края тонкого эндокарда со свободной стенкой правого желудочка степень оценки ФВ правого желудочки не была установлена.
- Чувствительность эхокардиографии к гипертрофии ПЖ также низка, потому что правожелудочковый ответ на перегрузку давлением иногда создает его дилатацию вместо гипертрофии.
- Точная фракция выброса правого желудочка редко определяется на эхокардиографии, а нормальные значения не стандартизированы.
- Из-за трудностей с измерением объема правого желудочка количественная оценка фракции выброса правого желудочка будет неточной.
- Оценка право предсердного давления по динамике НПВ не точна при вентиляции с положительным давлением на ИВЛ и у юных спортсменов.
Сегодня многие проблемы малыша можно выявить уже внутриутробно, что позволяет заранее определить тактику лечения после родов. Одними из нередко выявляемых являются пороки сердца. Это различные аномалии в строении клапанов, перегородок или крупных сосудов детского сердца. Основной опасностью их является нарушение нормального тока крови по малому или большому кругам кровообращения, изменение давления внутри камер с перегрузкой одних отделов и обеднением других. Это приводит к формированию определенных симптомов, отклонений в физическом развитии и освоении навыков. Во многих случаях для спасения ребёнка и полноценной его жизни требуется кардиохирургическая операция.
Дефект межжелудочковой перегородки: в чем суть порока сердца?
Достаточно редким определяется порок сердца, затрагивающий перегородку между желудочками сердца. В норме эта плотная перегородка полностью разделяет и изолирует желудочки сердца друг от друга. При наличии пороков сердца, которые могут иметь как врожденное, так и приобретенное (что бывает у детей намного реже) происхождение, эта перегородка имеет отверстие, в силу чего часть крови из одного желудочка перетекает в другой, что нарушает кровообращение организма.
Подобный порок сердца приводит к смешиванию крови, идущей в большой круг (из левого желудочка), и тех порций, что должны отправляться в малый круг (из правого желудочка). Степень насыщения кислородом и углекислотой у них различна, что и определяет клинические проявления аномалии.
Виды поражения сердца: изолированный или комбинированный порок
Наиболее часто дефекты в строении межжелудочковой перегородки образуются в раннем внутриутробном периоде, когда идет закладка камер и клапанов детского сердца. Приобретенный вариант данного порока у детей бывает исключительно редко. Возможно два варианта поражения сердца ребёнка — изолированный порок, при котором поражена только перегородка между желудочками. Кроме того, сердце может иметь сразу несколько пороков — это тетрада или пентада Фалло, сочетание поражения перегородки с другими отделами.
Частота возникновения этого варианта поражения сердца достаточно высока, он оставляет до ¼ от всех возможных сердечных пороков у детей. Встречается с частотой до 1:1000 новорожденных. Сегодня с развитием технологий в медицине и кардиохирургической помощи новорожденным, исправление порока в раннем возрасте приводит к тому, что ребёнок в дальнейшем ничем не отличается от сверстников, живет полной жизнью.
В чем причины развития: роль инфекций, лекарств
Развитие пороков сердца происходит в ранний период, зачастую, когда женщина даже еще не знает о своей беременности. Влияние различных негативных факторов — инфекций, вредных привычек, различных патологий, требующих приема серьезных лекарств, — может стать одним из факторов развития пороков. Особенно это опасно в период от 3-4 недели до 7-8-ой.
Зачастую влияние на развитие плода является комплексным, одновременно влияют сразу несколько провоцирующих факторов, ведущими среди них являются:
- Генетическая предрасположенность. Это наследование малышом мутировавших генов, которые определяют неверную закладку структур сердца внутриутробно.
- Вирусная, микробная инфекция, которая перенесена в ранние сроки. Особенно опасны такие инфекции, как грипп или корь, краснуха, герпес или токсоплазмоз.
- Вредные привычки — курение и прием алкоголя, особенно имеющие системный характер.
- Медикаменты, если ими лечится острая инфекция (антибиотики, противовирусные препараты) или средства, принимаемые для лечения хронических соматических, эндокринных или неврологических патологий (препараты от эпилепсии, транквилизаторы, препараты против депрессии).
- Сахарный диабет с плохо контролируемой гликемией, эндокринные болезни.
- Длительная работа родителей на вредных предприятиях, если они подвергаются облучениям, воздействию химических веществ.
Варианты дефекта: особенности смешивания крови
Степень тяжести порока определяется размерами имеющегося в перегородке дефекта. Если отверстие небольшое (от 2 до 10 мм), кровь смешивается незначительно, прогнозы для жизни и здоровья могут быть вполне благоприятными. Если же это дефект более 10-12 мм, кровь смешивается в больших объёмах, существенно страдает кровообращение и без оперативной коррекции прогнозы очень неблагоприятные.
Кроме того, выделяются три типа порока, которые различаются по тяжести и прогнозу, исходя из локализации самого отверстия.
- Мембранозный дефект расположен в верхнем сегменте перегородки между желудочками, сразу под клапаном аорты. Обычно отверстие небольшое, сброс крови незначительный, нередко закрывается в процессе роста.
- Мышечный дефект, локализованный в толще мышц, он лежит относительно далеко от клапанного аппарата и проводящих путей. Если размер дефекта небольшой и сброс крови незначительный, может самостоятельно закрываться.
- Надгребневый дефект располагается в области отводящих сосудов сердца, не имеет тенденции к самостоятельному закрытию.
Особенности давления на фоне порока
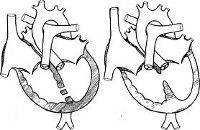
Проблема порока сердца в том, что наличие отверстий приводит к резкому изменению давления внутри камер, из-за чего страдает кровоснабжение тела. Так, давление в правом желудочке у здорового малыша ниже, чем в левом. Это и понятно — из левого желудочка кровь течет в большой круг, питает большую часть тела и должна вытекать под определенным давлением в аорту. А из правого — в легочный круг, чтобы насытить кровь кислородом.
Если есть отверстие перегородки, кровь во время сокращения уходит из зоны более высокого давления в зону более низкого. То есть, происходит сброс части крови в правый желудочек, из-за чего он перегружается. Внутри него повышается давление для того, чтобы прокачать такой высокий объём крови — стенка желудочка утолщается (гипертрофируется), но когда ресурсы исчерпываются, начинает растягиваться. Избыточный объём крови, которая поступает из правого перегруженного желудочка в легочный круг, перегружает сосуды и приводит к застою крови. А в левых отделах крови при этом может даже не хватать для полноценного обеспечения всего организма.
Кардиология. Национальное руководства / под ред. Е. В. Шляхто – 2015
Хирургическая коррекция травматического дефекта межжелудочковой перегородки и недостаточности трехстворчатого клапана / И.Таричко Ю.В., Иванов В.А. // Хирургия. Журнал им. Н.И. Пирогова – 1985 – Т. 61 №6