Опытным путём было доказано, что масса ядра оказывается меньше, чем масса протонов и нейтронов, из которых состоит ядро. Разница между этими массами называется дефектом массы ядра.
Дефект массы ядра (
Δm
) — это разница между суммарной массой свободных нуклонов, из которых состоит ядро, и массой ядра.
Почему же масса нуклонов, связанных ядерными силами в ядро, оказывается меньше массы этих же нуклонов в свободном состоянии? Оказывается, что масса и энергия взаимосвязаны.
Всякое тело массой m обладает энергией, которая называется энергией покоя (
E0
):
, где c — скорость света в вакууме.
Впервые соотношение между энергией и массой вывел Альберт Эйнштейн, поэтому это выражение и получило название «уравнение Эйнштейна».
Уменьшение энергии покоя нуклонов в ядре вызвано наличием ядерных сил, которые удерживают протоны и нейтроны в ядре. Работа, которую необходимо совершить для разрыва ядерных сил и разъединения нуклонов, равна энергии, которая связывает нуклоны вместе. Эта энергия называется энергией связи (
Eсв
) ядра.
Энергия связи и дефект массы ядра связаны между собой уравнением Эйнштейна:
Удельной энергией связи ядра называют энергию связи, приходящуюся на (1) нуклон:
Удельная энергия равна средней энергии, необходимой для отрыва (1) нуклона от ядра.
Вычисления показали, что наибольшей удельной энергией связи обладают элементы, находящиеся в центре Периодической системы химических элементов. С увеличением порядкового номера начинает уменьшаться удельная энергия связи. Именно поэтому ядра элементов с порядковым номером больше (83) являются радиоактивными. Благодаря небольшой удельной энергии связи они способны самопроизвольно распадаться.
Единицы измерения энергии
В ядерной физике принято измерять энергию в мегаэлектронвольтах ((1) МэВ):
(1) МэВ (=)
106
эВ
≈1,6⋅10−13
Дж.
Для вычисления энергии связи удобно пользоваться переводным коэффициентом для массы и энергии.
Дефекту массы в (1) а. е. м. соответствует энергия, равная
кг
⋅(3⋅108
м/с
)2≈1,49⋅10−10
Дж
=931,5
МэВ.
Обрати внимание!
Для выражения изменения энергии системы в мегаэлектронвольтах нужно
изменение массы системы в атомных единицах массы умножить на переводной коэффициент (931,5) МэВ/а. е. м.
(1) а. е. м. (=) (931,5) МэВ.
Энергия связи ядра.
-
Ядерные силы.
-
Атомная единица массы.
-
Дефект массы и энергия связи.
-
Удельная энергия связи.
-
Насыщение ядерных сил.
Автор — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев.
Темы кодификатора ЕГЭ: энергия связи нуклонов в ядре, ядерные силы.
Атомное ядро, согласно нуклонной модели, состоит из нуклонов — протонов и нейтронов. Но какие силы удерживают нуклоны внутри ядра?
За счёт чего, например, держатся вместе два протона и два нейтрона внутри ядра атома гелия? Ведь протоны, отталкиваясь друг от друга электрическими силами, должны были бы разлететься в разные стороны! Может быть, это гравитационное притяжение нуклонов друг к другу не даёт ядру распасться?
Давайте проверим. Пусть два протона находятся на некотором расстоянии друг от друга. Найдём отношение силы
их электрического отталкивания к силе
их гравитационного притяжения:
Заряд протона Кл, масса протона
кг, поэтому имеем:
Какое чудовищное превосходство электрической силы! Гравитационное притяжение протонов не то что не обеспечивает устойчивость ядра — оно вообще не заметно на фоне их взаимного электрического отталкивания.
Следовательно, существуют иные силы притяжения, которые скрепляют нуклоны внутри ядра и превосходят по величине силу электрического отталкивания протонов. Это — так называемые ядерные силы.
к оглавлению ▴
Ядерные силы.
До сих пор мы знали два типа взаимодействий в природе — гравитационные и электромагнитные. Ядерные силы служат проявлением нового, третьего по счёту типа взаимодействий — сильного взаимодействия. Мы не будем вдаваться в механизм возникновения ядерных сил, а лишь перечислим их наиболее важные свойства.
1. Ядерные силы действуют между любыми двумя нуклонами: протоном и протоном, протоном и нейтроном, нейтроном и нейтроном.
2. Ядерные силы притяжения протонов внутри ядра примерно в 100 раз превосходят силу электрического отталкивания протонов. Более мощных сил, чем ядерные, в природе не наблюдается.
3. Ядерные силы притяжения являются короткодействующими: радиус их действия составляет около м. Это и есть размер ядра — именно на таком расстоянии друг от друга нуклоны удерживаются ядерными силами. При увеличении расстояния ядерные силы очень быстро убывают; если расстояние между нуклонами станет равным
м, ядерные силы почти полностью исчезнут.
На расстояниях, меньших м, ядерные силы становятся силами отталкивания.
Сильное взаимодействие относится к числу фундаментальных — его нельзя объяснить на основе каких-то других типов взаимодействий. Способность к сильным взаимодействиям оказалась свойственной не только протонам и нейтронам, но и некоторым другим элементарным частицам; все такие частицы получили название адронов. Электроны и фотоны к адронам не относятся — они в сильных взаимодействиях не участвуют.
к оглавлению ▴
Атомная единица массы.
Массы атомов и элементарных частиц чрезвычайно малы, и измерять их в килограммах неудобно. Поэтому в атомной и ядерной физике часто применяется куда более мелкая единица — так
называемая атомная единица массы (сокращённо а. е. м.).
По определению, атомная единица массы есть 1/12 массы атома углерода . Вот её значение с точностью до пяти знаков после запятой в стандартной записи:
а. е. м.
кг
г.
(Такая точность нам впоследствии понадобится для вычисления одной очень важной величины, постоянно применяющейся в расчётах энергии ядер и ядерных реакций.)
Оказывается, что 1 а. е. м., выраженная в граммах, численно равна величине, обратной к постоянной Авогадро моль
:
моль.
Почему так получается? Вспомним, что число Авогадро есть число атомов в 12г углерода. Кроме того, масса атома углерода равна 12 а. е. м. Отсюда имеем:
г
а. е. м.,
поэтому а. е. м.=
г, что и требовалось.
Как вы помните, любое тело массы m обладает энергией покоя E, которая выражается формулой Эйнштейна:
. (1)
Выясним, какая энергия заключена в одной атомной единице массы. Нам надо будет провести вычисления с достаточно высокой точностью, поэтому берём скорость света с пятью знаками после запятой:
м/с.
Итак, для массы а. е. м. имеем соответствующую энергию покоя
:
Дж. (2)
В случае малых частиц пользоваться джоулями неудобно — по той же причине, что и килограммами. Существует гораздо более мелкая единица измерения энергии — электронвольт (сокращённо эВ).
По определению, 1 эВ есть энергия, приобретаемая электроном при прохождении ускоряющей разности потенциалов 1 вольт:
эВ
Кл
В
Дж. (3)
(вы помните, что в задачах достаточно использовать величину элементарного заряда в виде Кл, но здесь нам нужны более точные вычисления).
И вот теперь, наконец, мы готовы вычислить обещанную выше очень важную величину — энергетический эквивалент атомной единицы массы, выраженный в МэВ. Из (2) и (3) получаем:
эВ
. (4)
Итак, запоминаем: энергия покоя одной а. е. м. равна 931,5 МэВ. Этот факт вам неоднократно встретится при решении задач.
В дальнейшем нам понадобятся массы и энергии покоя протона, нейтрона и электрона. Приведём их с точностью, достаточной для решения задач.
а. е. м.,
МэВ;
а. е. м.,
МэВ;
а. е. м.,
МэВ.
к оглавлению ▴
Дефект массы и энергия связи.
Мы привыкли, что масса тела равна сумме масс частей, из которых оно состоит. В ядерной физике от этой простой мысли приходится отвыкать.
Давайте начнём с примера и возьмём хорошо знакомую нам -частицу ядро
. В таблице (например, в задачнике Рымкевича) имеется значение массы нейтрального атома гелия: она равна 4,00260 а. е. м. Для нахождения массы M ядра гелия нужно из массы нейтрального атома вычесть массу двух электронов, находящихся в атоме:
а. е. м.
В то же время, суммарная масса двух протонов и двух нейтронов, из которых состоит ядро гелия, равна:
а. е. м.
Мы видим, что сумма масс нуклонов, составляющих ядро, превышает массу ядра на
а. е. м.
Величина называется дефектом массы. В силу формулы Эйнштейна (1) дефекту массы отвечает изменение энергии:
МэВ:
Величина обозначается также
и называется энергией связи ядра
. Таким образом, энергия связи
-частицы составляет приблизительно 28 МэВ.
Каков же физический смысл энергии связи (и, стало быть, дефекта масс)?
Чтобы расщепить ядро на составляющие его протоны и нейтроны, нужно совершить работу против действия ядерных сил. Эта работа не меньше определённой величины ; минимальная работа
по разрушению ядра совершается в случае, когда высвободившиеся протоны и нейтроны покоятся.
Ну а если над системой совершается работа, то энергия системы возрастает на величину совершённой работы. Поэтому суммарная энергия покоя нуклонов, составляющих ядро и взятых по отдельности, оказывается больше энергии покоя ядра на величину .
Следовательно, и суммарная масса нуклонов, из которых состоит ядро, будет больше массы самого ядра. Вот почему возникает дефект массы.
В нашем примере с -частицей суммарная энергия покоя двух протонов и двух нейтронов больше энергии покоя ядра гелия на 28 МэВ. Это значит, что для расщепления ядра
на составляющие его нуклоны нужно совершить работу, равную как минимум 28 МэВ. Эту величину мы и назвали энергией связи ядра.
Итак, энергия связи ядра — это минимальная работа, которую необходимо совершить для расщепления ядра на составляющие его нуклоны.
Энергия связи ядра есть разность энергий покоя нуклонов ядра, взятых по отдельности, и энергии покоя самого ядра. Если ядро массы состоит из
протонов и
нейтронов, то для энергии связи
имеем:
.
Величина , как мы уже знаем, называется дефектом массы.
к оглавлению ▴
Удельная энергия связи.
Важной характеристикой прочности ядра является его удельная энергия связи, равная отношению энергии связи к числу нуклонов:
.
Удельная энергия связи есть энергия связи, приходящаяся на один нуклон, и имеет смысл средней работы, которую необходимо совершить для удаления нуклона из ядра.
На рис. 1 представлена зависимость удельной энергии связи естественных (то есть встречающихся в природе 1) изотопов химических элементов от массового числа A.
Рис. 1. Удельная энергия связи естественных изотопов
Элементы с массовыми числами 210–231, 233, 236, 237 в естественных условиях не встречаются. Этим объясняются пробелы в конце графика.
У лёгких элементов удельная энергия связи возрастает с ростом , достигая максимального значения 8,8 МэВ/нуклон в окрестности железа
(то есть в диапазоне изменения
примерно от 50 до 65). Затем она плавно убывает до величины 7,6 МэВ/нуклон у урана
.
Такой характер зависимости удельной энергии связи от числа нуклонов объясняется совместным действием двух разнонаправленных факторов.
Первый фактор — поверхностные эффекты. Если нуклонов в ядре мало, то значительная их часть находится на поверхности ядра. Эти поверхностные нуклоны окружены меньшим числом соседей, чем внутренние нуклоны, и, соответственно, взаимодействуют с меньшим числом соседних нуклонов. При увеличении доля внутренних нуклонов растёт, а доля поверхностных нуклонов — падает; поэтому работа, которую нужно совершить для удаления одного нуклона из ядра, в среднем должна увеличиваться с ростом
.
Однако с возрастанием числа нуклонов начинает проявляться второй фактор — кулоновское отталкивание протонов. Ведь чем больше протонов в ядре, тем большие электрические силы отталкивания стремятся разорвать ядро; иными словами, тем сильнее каждый протон отталкивается от остальных протонов. Поэтому работа, необходимая для удаления нуклона из ядра, в среднем должна уменьшаться с ростом .
Пока нуклонов мало, первый фактор доминирует над вторым, и потому удельная энергия связи возрастает.
В окрестности железа действия обоих факторов сравниваются друг с другом, в результате чего удельная энергия связи выходит на максимум. Это область наиболее устойчивых, прочных ядер.
Затем второй фактор начинает перевешивать, и под действием всё возрастающих сил кулоновского отталкивания, распирающих ядро, удельная энергия связи убывает.
к оглавлению ▴
Насыщение ядерных сил.
Тот факт, что второй фактор доминирует у тяжёлых ядер, говорит об одной интересной особенности ядерных сил: они обладают свойством насыщения. Это означает, что каждый нуклон в большом ядре связан ядерными силами не со всеми остальными нуклонами, а лишь с небольшим числом своих соседей, и число это не зависит от размеров ядра.
Действительно, если бы такого насыщения не было, удельная энергия связи продолжала бы возрастать с увеличением — ведь тогда каждый нуклон скреплялся бы ядерными силами со всё большим числом нуклонов ядра, так что первый фактор неизменно доминировал бы над вторым. У кулоновских сил отталкивания не было бы никаких шансов переломить ситуацию в свою пользу!
Спасибо за то, что пользуйтесь нашими статьями.
Информация на странице «Энергия связи ядра.» подготовлена нашими авторами специально, чтобы помочь вам в освоении предмета и подготовке к экзаменам.
Чтобы успешно сдать необходимые и поступить в ВУЗ или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из разделов нашего сайта.
Публикация обновлена:
08.05.2023
В ядре существуют силы особой природы — ядерные силы, которые
действуют между нуклонами на расстояниях, сравнимыми с размерами самих ядер, и
препятствуют взаимному электростатическому отталкиванию между протонами в ядре.
Таким образом, чтобы расщепить
ядро на отдельные нуклоны, не взаимодействующие между собой, необходимо
совершить работу по преодолению ядерных сил. Другими словами, сообщить ядру
определённую энергию.
Так вот, минимальная
энергия, необходимая для расщепления ядра на отдельные нуклоны, называется
энергией связи.
Очевидно, что чем больше эта
величина, тем стабильнее ядро.
— А каким образом можно
определить величину энергии связи?
Самый простой способ
определения этой энергии основан на одном замечательном законе природы,
устанавливающим соотношение между массой тел и их энергией. Закон этот был открытым
знаменитым учёным Альбертом Эйнштейном в 1905 году:
То есть, согласно этому закону,
изменение массы тела влечёт за собой изменение энергии этого тела.
Из записанного соотношения
видно, что ничтожному изменению массы тела соответствует значительное изменение
энергии. Для примера подсчитаем, какое количество энергии выделится при
уменьшении массы какого-нибудь тела на один грамм?
— А какое отношение имеет
рассмотренный нами закон к подсчёту энергии связи атомных ядер?
Всё очень просто. Дело в том,
что при образовании ядер из протонов и нейтронов освобождается энергия
электромагнитного излучения, то есть излучаются фотоны, а энергия ядерной
системы уменьшается. Следовательно, это явление должно вести за собой уменьшение
массы, так как фотоны уносят с собой некоторую её часть. Значит масса
получившегося ядра должна быть меньше суммы масс, входящих в него нуклонов. Эту
разность масс называют дефектом массы ядра.
Иными словами, дефект масс
— это разность между суммарной массой всех нуклонов ядра в свободном состоянии
и массой ядра.
В соответствии с соотношением
Эйнштейна между массой и энергией, дефект массы и характеризует энергию
связи атомного ядра.
Обращаем ваше внимание на то,
что при использовании данной формулы, массу входящих в неё частиц следует
выражать в килограммах. Тогда значение полученной энергии связи будет выражено
в джоулях.
Для примера, давайте
рассчитаем энергию связи ядра изотопа лития-семь, если известна масса его ядра.
Как видим, энергии микромира
крайне малы и работать с такими числами представляется крайне неудобным.
Гораздо проще рассчитывать энергию связи в электронвольтах и мегаэлектронвольтах
(эВ и МэВ).
Один электронвольт равен
энергии, необходимой для переноса элементарного заряда в электростатическом
поле между точками с разницей потенциалов в один вольт.
Иначе говоря, величина одного
электронвольта равна значению элементарного заряда в джоулях:
Но энергии связи таковы, что
для их вычисления удобно использовать миллионы электронвольт, то есть
мегаэлектронвольты (МэВ).
В этом случае формула для
определения энергии связи примет вид:
Теперь обратим внимание на тот
факт, что в таблице Менделеева и в таблицах масс изотопов приводятся, как
правило, не массы ядер, а массы нейтральных атомов. Поэтому формулу для дефекта
масс целесообразно преобразовать так, чтобы в неё входила не масса ядра, а
масса соответствующего атома.
Ещё одной важной
характеристикой в ядерной физике является удельная энергия связи. Так
называют энергию связи, приходящуюся на один нуклон.
Чем она больше, тем стабильнее
оказывается ядро изотопа. Как правило, лёгкие ядра обладают достаточно малой
удельной энергией связи (за исключением гелия два-четыре).
К середине таблицы Менделеева
энергия связи достигает своего максимального значения, а к концу — вновь
начинает убывать. Поэтому наиболее устойчивы ядра со средними значениями
массовых чисел. Лёгкие ядра имеют тенденцию к слиянию (реакция синтеза), а
тяжёлые — к распаду (реакция деления). Энергию, выделяющуюся или поглощающуюся
в процессе таких ядерных реакций, можно определить, если известны массы
взаимодействующих и образующихся в результате этого взаимодействия ядер и
частиц. Эту энергию называют энергетическим выходом ядерной реакции.
Следует обратить внимание и на
то, что синтез лёгких ядер сопровождается примерно в 6 раз большим выделением
энергии на один нуклон по сравнению с делением тяжёлых ядер. Но подобные
реакции могут протекать только при очень высоких температурах. Поэтому их
называют термоядерными. Но о них мы с вами поговорим в ближайшее время.
7
Лекция 18. Элементы
физики атомного ядра
[1] гл. 32
План лекции
-
Атомное ядро.
Дефект массы, энергия связи ядра. -
Радиоактивное
излучение и его виды. Закон радиоактивного
распада. -
Законы сохранения
при радиоактивных распадах и ядерных
реакциях.
Состав атомного
ядра
Ядерная физика
— наука о строении, свойствах и превращениях
атомных ядер. В 1911 году Э. Резерфорд
установил в опытах по рассеянию -частиц
при их прохождении через вещество, что
нейтральный атом состоит из компактного
положительно заряженного ядра и
отрицательного электронного облака.
В. Гейзенберг и Д.Д. Иваненко (независимо)
высказали гипотезу о том, что ядро
состоит из протонов и нейтронов.
Атомное ядро
— центральная массивная часть атома,
состоящая из протонов и нейтронов,
которые получили общее название нуклонов.
В ядре сосредоточена почти вся масса
атома (более 99,95%). Размеры ядер порядка
10-13
— 10-12
см и зависят от числа нуклонов в ядре.
Плотность ядерного вещества как для
легких, так и для тяжелых ядер почти
одинакова и составляет около 1017
кг/м3,
т.е. 1 см3
ядерного вещества весил бы 100 млн. т.
Ядра имеют положительный электрический
заряд, равный абсолютной величине
суммарного заряда электронов в атоме.
Протон
(символ p) —
элементарная частица, ядро атома
водорода. Протон обладает положительным
зарядом, равным по величине заряду
электрона. Масса протона mp
= 1,6726 10-27
кг = 1836 me
, где me
— масса электрона.
В ядерной физике
принято выражать массы в атомных единицах
массы:
1 а.е.м. = 1,65976 10-27
кг.
Следовательно,
масса протона, выраженная в а.е.м., равна
mp
= 1,0075957 а.е.м.
Число протонов в
ядре называется зарядовым
числом
Z. Оно равно
атомному номеру данного элемента и,
следовательно, определяет место элемента
в периодической системе элементов
Менделеева.
Нейтрон
(символ n) —
элементарная частица, не обладающая
электрическим зарядом, масса которой
незначительно больше массы протона.
Масса нейтрона mn
= 1,675 10-27
кг = 1,008982 а.е.м. Число нейтронов в ядре
обозначается N.
Суммарное число
протонов и нейтронов в ядре (число
нуклонов) называется массовым
числом и
обозначается буквой А,
А = Z + N.
Для обозначения
ядер применяется символ
,
где Х — химический символ элемента.
Изотопы
— разновидности атомов одного и того же
химического элемента, атомные ядра
которых имеют одинаковое число протонов
(Z) и разное число нейтронов (N). Изотопами
называют также ядра таких атомов. Изотопы
занимают одно и то же место в периодической
системе элементов. В качестве примера
приведем изотопы водорода:
.
Понятие о ядерных
силах.
Ядра атомов —
чрезвычайно прочные образования,
несмотря на то, что одноименно заряженные
протоны, находясь на очень малых
расстояниях в атомном ядре, должны с
огромной силой отталкиваться друг от
друга. Следовательно, внутри ядра
действуют чрезвычайно большие силы
притяжения между нуклонами, во много
раз превышающие электрические силы
отталкивания между протонами. Ядерные
силы представляют собой особый вид сил,
это самые сильные из всех известных
взаимодействий в природе.
Исследования
показали, что ядерные силы обладают
следующими свойствами:
-
ядерные силы
притяжения действуют между любыми
нуклонами, независимо от их зарядового
состояния; -
ядерные силы
притяжения являются короткодействующими:
они действуют между любыми двумя
нуклонами на расстоянии между центрами
частиц около 2·10-15
м и резко спадают при увеличении
расстояния (при расстояниях более
3·10-15
м они уже практически равны нулю); -
для ядерных сил
характерна насыщенность, т.е. каждый
нуклон может взаимодействовать только
с ближайшими к нему нуклонами ядра; -
ядерные силы не
являются центральными, т.е. они не
действуют вдоль линии, соединяющей
центры взаимодействующих нуклонов.
В настоящее время
природа ядерных сил изучена не до конца.
Установлено, что они являются так
называемыми обменными силами. Обменные
силы носят квантовый характер и не имеют
аналога в классической физике. Нуклоны
связываются между собой третьей частицей,
которой они постоянно обмениваются. В
1935 г. японский физик Х. Юкава показал,
что нуклоны обмениваются частицами,
масса которых примерно в 250 раз больше
массы электрона. Предсказанные частицы
были обнаружены в 1947 г. английским ученым
С. Пауэллом при изучении космических
лучей и впоследствии названы -мезонами
или пионами.
Взаимные превращения
нейтрона и протона подтверждаются
различными экспериментами.
Дефект масс
атомных ядер. Энергия связи атомного
ядра.
Нуклоны в атомном
ядре связаны между собой ядерными
силами, поэтому, чтобы разделить ядро
на составляющие его отдельные протоны
и нейтроны, необходимо затратить большую
энергию.
Минимальная
энергия, необходимая для разделения
ядра на составляющие его нуклоны,
называется энергией
связи ядра.
Такая же по величине энергия освобождается,
если свободные нейтроны и протоны
соединяются и образуют ядро.
Точные
масс-спектроскопические измерения масс
ядер показали, что масса покоя атомного
ядра меньше суммы масс покоя свободных
нейтронов и протонов, из которых
образовалось ядро. Разность между суммой
масс покоя свободных нуклонов, из которых
образовано ядро, и массой ядра называется
дефектом
массы:
Этой разности масс
m
соответствует энергия связи ядра Есв,
определяемая соотношением Эйнштейна:
или, подставив
выражение для m,
получим:
Энергию связи
обычно выражают в мегаэлектронвольтах
(МэВ). Определим энергию связи,
соответствующую одной атомной единице
массы (,
скорость света в вакууме
):
.
Переведем полученную
величину в электронвольты:
В связи с этим на
практике удобнее пользоваться следующим
выражением для энергии связи:
,
где множитель m
выражен в атомных единицах массы.
Важной характеристикой
ядра служит удельная энергия связи
ядра, т.е. энергия связи, приходящаяся
на нуклон:
.
Чем больше
,
тем сильнее связаны между собой нуклоны.
Рис.1
Зависимость
величины
от массового числа ядра показана на
рисунке 1. Как видно из графика, сильнее
всего связаны нуклоны в ядрах с массовыми
числами порядка 50-60 (Cr-Zn).
Энергия связи для этих ядер достигает
Соседние файлы в папке лекции
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
В уроке 2 «Изотопы элементов» из курса «Химия для чайников» рассмотрим что такое изотопы элементов и как правильно их обозначают; кроме того мы научимся определять массовое число, дефект массы и энергию связи ядра. Данный урок полностью опирается на основы химии, изложенные в первом уроке, в котором мы рассмотрели строение атома и атомного ядра, поэтому настоятельно вам рекомендую его изучить от корки до корки.
Что такое изотоп?
Хотя все атомы одного элемента имеют одинаковое число протонов, эти атомы могут отличаться числом имеющихся у них нейтронов. Такие различные атомы одного и того же элемента называются изотопами. Количество протонов, а также количество электронов у изотопа и исходного элемента совпадает. По этой причине в природе существует гораздо больше химических элементов, чем указано в таблице Менделеева, которая систематизирует элементы по числу протонов (порядковый номер).
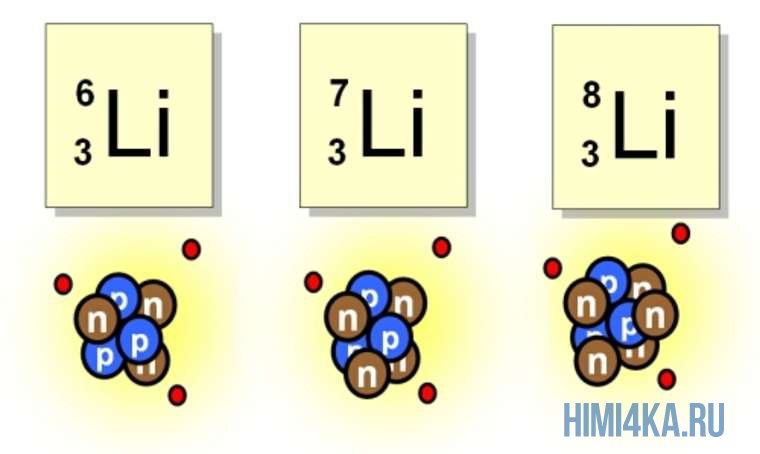
Например, все атомы Li имеют 3 протона, но в природе существуют изотопы, содержащие от 3 до 5 нейтронов. Для обозначения изотопа, слева от символа элемента подписывают нижним индексом его порядковый номер, а верхним — массовое число. Массовое число — это суммарное число нуклонов (протонов и нейтронов) в атомном ядре, численно близкое к атомной массе элемента. Нижний индекс, обозначающий порядковый номер элемента, указывать не обязательно, так как все атомы лития имеют в своем ядре по 3 протона. Также, обсуждая эти изотопы, можно пользоваться записью «литий-6» и «литий-8».
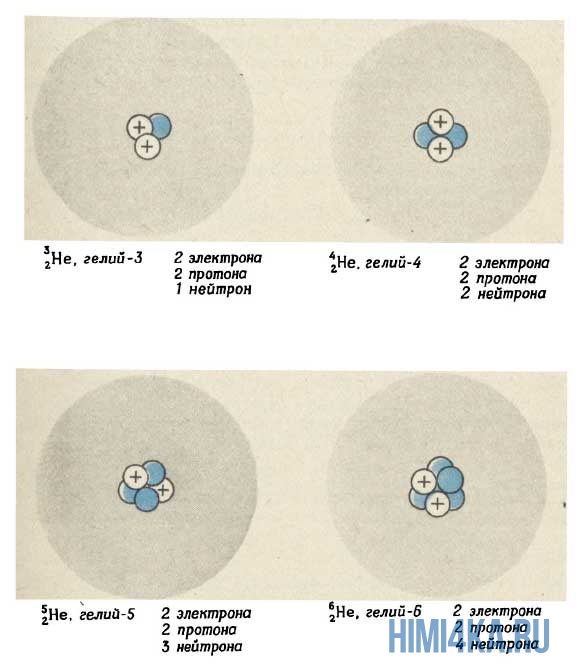
На рисунке выше изображен состав четырех изотопов гелия (Не). Все атомы гелия содержат два протона (и, следовательно, два электрона), но число нейтронов у них может быть разным. В природе большинство атомов гелия имеет два нейтрона (гелий-4) и реже одного раза на миллион встречаются атомы гелия с одним нейтроном (гелий-3). Другие изотопы гелия — гелий-5 , гелий-6 и гелий-8 (не показанный на рисунке) — неустойчивы и обнаруживаются лишь на очень непродолжительное время в ядерных реакциях (подробнее об этом будем говорить еще не скоро). Размеры ядер на рисунке очень сильно увеличены. Если бы они были такими, как это показано на рисунке, диаметр атома должен был достигать примерно 0,5 км.
Пример 1. Сколько протонов, нейтронов и электронов содержится в атоме урана-238? Запишите символ этого изотопа.
Решение: Порядковый номер урана (см. таблицу Менделеева) равен 92, а массовое число изотопа равно 238 (по условию). Следовательно, он содержит 92 протона, 92 электрона и 238 — 92 = 146 нейтронов. Его символ 238U.
Дефект массы и энергия связи ядра
Затронув тему изотопов, нельзя пройти мимо феномена дефект массы ядра. Когда из отдельных нуклонов образуется атомное ядро, часть их массы превращается в энергию. Другими словами, вот взяли вы щепотку протонов и нейтронов, хорошенько их смяли вместе, и получили ядро, но его масса будет меньше массы исходных компонентов. Это и есть дефект масс. Формула для расчета дефекта массы ядра:
- ∆m=(Zmp+Nmn)-Mя
где Mя – масса ядра, Z – число протонов в ядре, N – число нейтронов в ядре, mp – масса протона, mn – масса нейтрона.
Если к атому подвести энергию (которая эквивалентна дефекту масс), то можно разделить его ядро обратно на нуклоны. Эта энергия носит название энергия связи ядра. Формула для расчета энергии связи ядра:
- ∆Eсв=∆mc2
где с — скорость света, ∆m — дефект массы ядра
Проверьте себя, как вы усвоили понятия дефект массы и энергия связи ядра, самостоятельно решив задачу пользуясь формулами выше.
Пример 2. Если образовать атом углерода-12 из субатомных частиц, какое значение будет иметь дефект масс?
Показать
Ответ: 0,0990 а.е.м.
[свернуть]
Теперь нам известно, что каждый изотоп элемента характеризуется порядковым номером (суммарным числом протонов), массовым числом (суммарным числом протонов и нейтронов) и атомной массой (массой атома, выраженной в атомных единицах массы). Поскольку дефект массы при образовании атома очень мал, массовое число обычно совпадает с атомной массой изотопа, округленной до ближайшего целого числа. (Например, атомная масса хлора-37 равна 36,966, что после округления дает 37.) Если в природе встречается несколько изотопов одного элемента, то экспериментально наблюдаемая атомная масса (естественная атомная масса) равна средневзвешенному значению атомных масс отдельных изотопов. Это средневзвешенное значение определяется соответственно относительному содержанию изотопов в природе. Хлор существует в природе в виде смеси из 75,53% хлора-35 (атомная масса 34,97 а.е.м.) и 24,47% хлора-37 (36,97 а.е.м.), поэтому средневзвешенное значение масс этих изотопов равно
- (0,7553·34,97 а.е.м.) + (0,2447·36,97 а.е.м.) = 35,46 а.е.м.
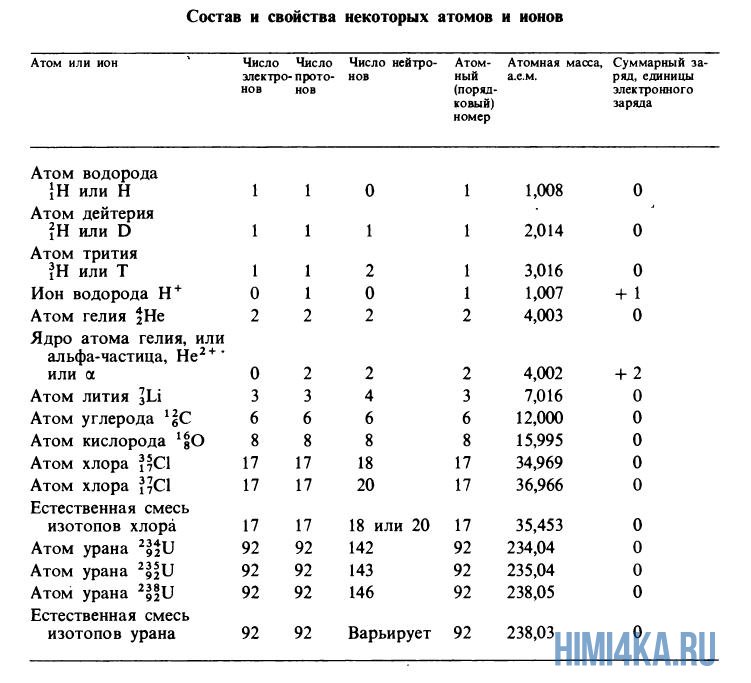
Атомные массы, указанные в таблице Менделеева представляют собой во всех случаях средневзвешенные значения атомных масс изотопов, встречающихся в природе, и именно этими значениями мы будем пользоваться в дальнейшем, за исключением тех случаев, когда будет обсуждаться какой-нибудь конкретный изотоп. Все изотопы одного элемента в химическом отношении ведут себя практически одинаково. На рисунке ниже изображены состав и свойства некоторые атомов, ионов и изотопов элементов.
Пример 3. Магний (Mg) в основном состоит из трех естественных изотопов: 78,70% всех атомов магния имеют атомную массу 23,985 а.е.м., 10,13% — 24,986 а.е.м. и 11,17% — 25,983 а.е.м. Сколько протонов и нейтронов содержится в каждом из этих трех изотопов? Чему равно средневзвешенное значение их атомных масс?
Решение: Все изотопы магния содержат по 12 протонов. Изотоп с атомной массой 23,985 а.е.м. имеет массовое число 24 (суммарное число протонов и нейтронов), следовательно, он имеет 24 — 12 = 12 нейтронов. Символ этого изотопа 24Mg. Аналогично находим, что изотоп с атомным весом 24,986 а.е.м. имеет массовое число 25, содержит 13 нейтронов и имеет символ 25Mg. Третий изотоп (25,983 а.е.м.) имеет массовое число 26, содержит 14 нейтронов и имеет символ 26Mg. Средняя атомная масса магния находится следующим образом:
- (0,7870·23,985 а.е.м.) + (0,1013·24,986 а.е.м.) + (0,1117·25,983 а.е.м.) = 24,31 а.е.м.
Надеюсь урок 2 «Изотопы элементов» помог вам понять что из себя представляют изотопы. Если у вас возникли вопросы, пишите их в комментарии.