поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,666 -
гуманитарные
33,654 -
юридические
17,917 -
школьный раздел
611,992 -
разное
16,906
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
В уроке 2 «Изотопы элементов» из курса «Химия для чайников» рассмотрим что такое изотопы элементов и как правильно их обозначают; кроме того мы научимся определять массовое число, дефект массы и энергию связи ядра. Данный урок полностью опирается на основы химии, изложенные в первом уроке, в котором мы рассмотрели строение атома и атомного ядра, поэтому настоятельно вам рекомендую его изучить от корки до корки.
Что такое изотоп?
Хотя все атомы одного элемента имеют одинаковое число протонов, эти атомы могут отличаться числом имеющихся у них нейтронов. Такие различные атомы одного и того же элемента называются изотопами. Количество протонов, а также количество электронов у изотопа и исходного элемента совпадает. По этой причине в природе существует гораздо больше химических элементов, чем указано в таблице Менделеева, которая систематизирует элементы по числу протонов (порядковый номер).
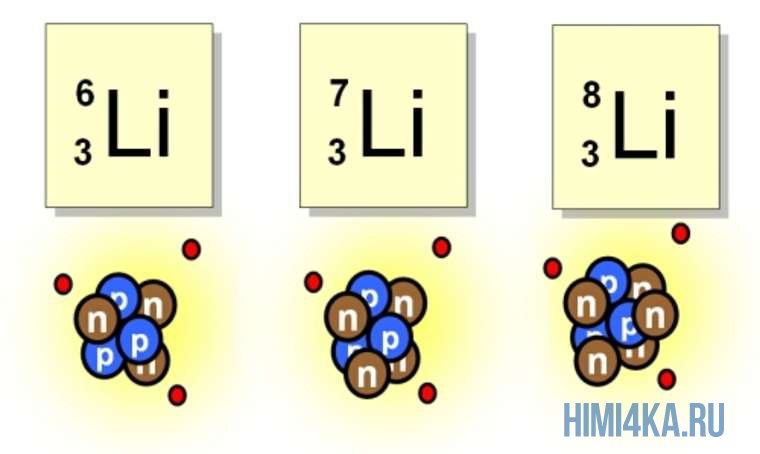
Например, все атомы Li имеют 3 протона, но в природе существуют изотопы, содержащие от 3 до 5 нейтронов. Для обозначения изотопа, слева от символа элемента подписывают нижним индексом его порядковый номер, а верхним — массовое число. Массовое число — это суммарное число нуклонов (протонов и нейтронов) в атомном ядре, численно близкое к атомной массе элемента. Нижний индекс, обозначающий порядковый номер элемента, указывать не обязательно, так как все атомы лития имеют в своем ядре по 3 протона. Также, обсуждая эти изотопы, можно пользоваться записью «литий-6» и «литий-8».
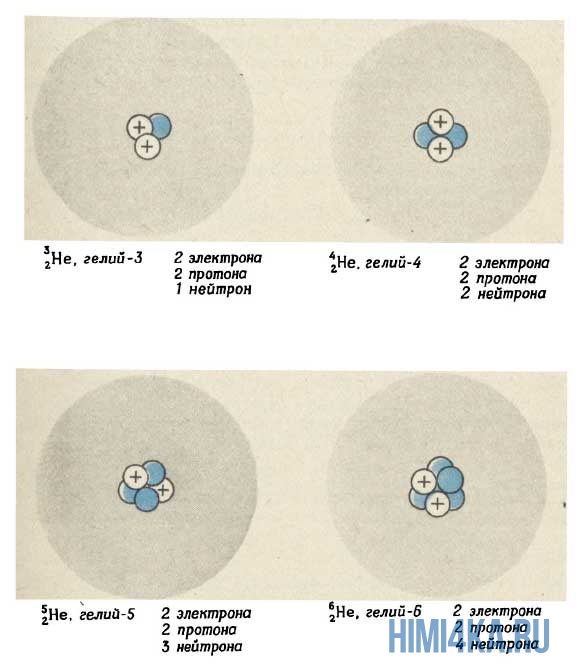
На рисунке выше изображен состав четырех изотопов гелия (Не). Все атомы гелия содержат два протона (и, следовательно, два электрона), но число нейтронов у них может быть разным. В природе большинство атомов гелия имеет два нейтрона (гелий-4) и реже одного раза на миллион встречаются атомы гелия с одним нейтроном (гелий-3). Другие изотопы гелия — гелий-5 , гелий-6 и гелий-8 (не показанный на рисунке) — неустойчивы и обнаруживаются лишь на очень непродолжительное время в ядерных реакциях (подробнее об этом будем говорить еще не скоро). Размеры ядер на рисунке очень сильно увеличены. Если бы они были такими, как это показано на рисунке, диаметр атома должен был достигать примерно 0,5 км.
Пример 1. Сколько протонов, нейтронов и электронов содержится в атоме урана-238? Запишите символ этого изотопа.
Решение: Порядковый номер урана (см. таблицу Менделеева) равен 92, а массовое число изотопа равно 238 (по условию). Следовательно, он содержит 92 протона, 92 электрона и 238 — 92 = 146 нейтронов. Его символ 238U.
Дефект массы и энергия связи ядра
Затронув тему изотопов, нельзя пройти мимо феномена дефект массы ядра. Когда из отдельных нуклонов образуется атомное ядро, часть их массы превращается в энергию. Другими словами, вот взяли вы щепотку протонов и нейтронов, хорошенько их смяли вместе, и получили ядро, но его масса будет меньше массы исходных компонентов. Это и есть дефект масс. Формула для расчета дефекта массы ядра:
- ∆m=(Zmp+Nmn)-Mя
где Mя – масса ядра, Z – число протонов в ядре, N – число нейтронов в ядре, mp – масса протона, mn – масса нейтрона.
Если к атому подвести энергию (которая эквивалентна дефекту масс), то можно разделить его ядро обратно на нуклоны. Эта энергия носит название энергия связи ядра. Формула для расчета энергии связи ядра:
- ∆Eсв=∆mc2
где с — скорость света, ∆m — дефект массы ядра
Проверьте себя, как вы усвоили понятия дефект массы и энергия связи ядра, самостоятельно решив задачу пользуясь формулами выше.
Пример 2. Если образовать атом углерода-12 из субатомных частиц, какое значение будет иметь дефект масс?
Показать
Ответ: 0,0990 а.е.м.
[свернуть]
Теперь нам известно, что каждый изотоп элемента характеризуется порядковым номером (суммарным числом протонов), массовым числом (суммарным числом протонов и нейтронов) и атомной массой (массой атома, выраженной в атомных единицах массы). Поскольку дефект массы при образовании атома очень мал, массовое число обычно совпадает с атомной массой изотопа, округленной до ближайшего целого числа. (Например, атомная масса хлора-37 равна 36,966, что после округления дает 37.) Если в природе встречается несколько изотопов одного элемента, то экспериментально наблюдаемая атомная масса (естественная атомная масса) равна средневзвешенному значению атомных масс отдельных изотопов. Это средневзвешенное значение определяется соответственно относительному содержанию изотопов в природе. Хлор существует в природе в виде смеси из 75,53% хлора-35 (атомная масса 34,97 а.е.м.) и 24,47% хлора-37 (36,97 а.е.м.), поэтому средневзвешенное значение масс этих изотопов равно
- (0,7553·34,97 а.е.м.) + (0,2447·36,97 а.е.м.) = 35,46 а.е.м.
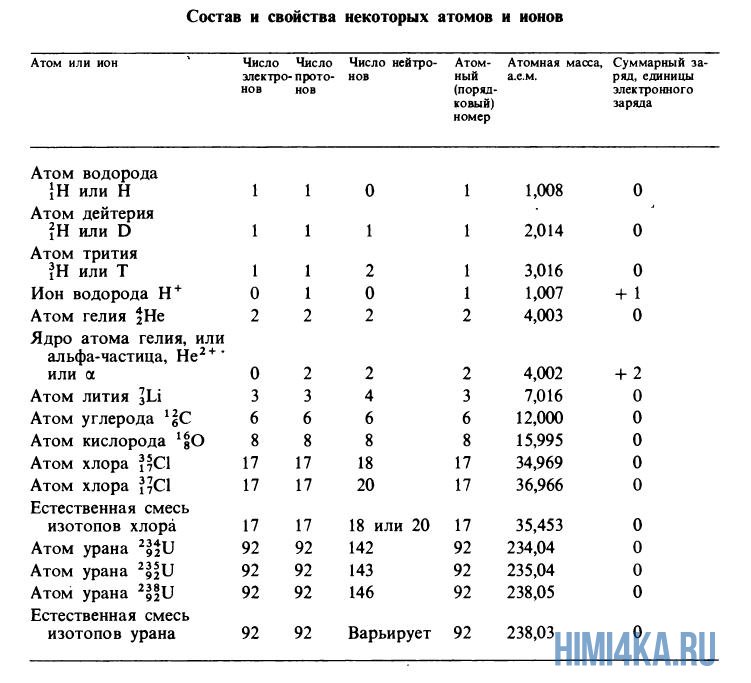
Атомные массы, указанные в таблице Менделеева представляют собой во всех случаях средневзвешенные значения атомных масс изотопов, встречающихся в природе, и именно этими значениями мы будем пользоваться в дальнейшем, за исключением тех случаев, когда будет обсуждаться какой-нибудь конкретный изотоп. Все изотопы одного элемента в химическом отношении ведут себя практически одинаково. На рисунке ниже изображены состав и свойства некоторые атомов, ионов и изотопов элементов.
Пример 3. Магний (Mg) в основном состоит из трех естественных изотопов: 78,70% всех атомов магния имеют атомную массу 23,985 а.е.м., 10,13% — 24,986 а.е.м. и 11,17% — 25,983 а.е.м. Сколько протонов и нейтронов содержится в каждом из этих трех изотопов? Чему равно средневзвешенное значение их атомных масс?
Решение: Все изотопы магния содержат по 12 протонов. Изотоп с атомной массой 23,985 а.е.м. имеет массовое число 24 (суммарное число протонов и нейтронов), следовательно, он имеет 24 — 12 = 12 нейтронов. Символ этого изотопа 24Mg. Аналогично находим, что изотоп с атомным весом 24,986 а.е.м. имеет массовое число 25, содержит 13 нейтронов и имеет символ 25Mg. Третий изотоп (25,983 а.е.м.) имеет массовое число 26, содержит 14 нейтронов и имеет символ 26Mg. Средняя атомная масса магния находится следующим образом:
- (0,7870·23,985 а.е.м.) + (0,1013·24,986 а.е.м.) + (0,1117·25,983 а.е.м.) = 24,31 а.е.м.
Надеюсь урок 2 «Изотопы элементов» помог вам понять что из себя представляют изотопы. Если у вас возникли вопросы, пишите их в комментарии.
Легкая задача по химии
Определите дефект масс ядра изотопа дейтерия 2 1 Н (тяжёлого водорода). Масса протона приблизительно равна 1,0073 а.е.м., нейтрона 1,0087 а.е.м., ядра дейтерия 2,0141 а.е.м., 1 а.е.м. = 1,66 • 10^~27 кг
Все этапы решения и правильный ответ можно увидеть здесь:
Из условия задачи следует, что нам неизвестен дефект масс ядра изотопа дейтерия 2 1 H, что есть тяжелый водород. Далее в условии приведены массы протона и нейтронов и ядер дейтерия. Здесь нужно использовать первую формулу, указанную выше в решении. Далее следует подставить все известные значения и посчитать. В итоге получается, что дефект масс ядра изотопа дейтерия 2 1 H будет равен 3,15 на 10 в минус 30 кг. Это значение и есть дельта масс, что и является правильным ответом на вопрос.
larisaorlova65
8 лет назад
Светило науки — 4523 ответа — 53388 раз оказано помощи
∆m -дефект
массы ядра: ∆m = Zmp + ( А- Z) mn — Мя
Из символической записи изотопа
лития 7 3 Li ,
видим, что А = 7 и Z =3, т.е в ядре изотопа лития
7 нуклонов, из них 3 протона и 4 нейтрона (N =А – Z)
Подставив значения А и
Z в формулу, получим:
Δm= Zmp + ( А- Z) mn — Мя ,
Δm =3∙1,6724∙10⁻²⁷ + 4∙ 1,6748 ∙10⁻²⁷ — 11,6475 ∙10⁻²⁷ =0,0689 *10⁻²⁷ кг
1а.е.м.=1,66056*10⁻²⁷кг
Δm=0,0415 а.е.м.
(91 оценка)
топное содержание, естественно, должно составлять 100%. Например, кремний обнаруживается в природных соединениях с таким естественным изотопным содержанием: 92.28% 28Si, 4.67% 29Si, 3.05% 30Si.
Относительная атомная масса Аr химического элемента (именно она приведена наряду с символом элемента и его порядковым номером в каждой клетке периодической системы Д. И. Менделеева) представляет собой среднее значение относительных изотопных масс с учетом изотопного содержания. Относительная атомная масса фактически показывает, во сколько раз масса данного атома больше, чем масса 1/12 изотопа углерода. Как любая относительная величина, Ar является величиной безразмерной.
За единицу измерения атомной массы (атомная единица массы – а.е.м.) в настоящее время принята 1/12 часть массы нуклида 12C. Этому нуклиду приписывают массу 12.0000 а.е.м. Истинное значение атомной единицы массы составляет 1.661·10-27 кг.
Массы трех фундаментальных частиц, выраженные в а.е.м., имеют следующие значения:
масса протона – 1.007277 а.е.м., масса нейтрона – 1.008665 а.е.м., масса электрона – 0.000548 а.е.м.
Можно считать, что массы протона и нейтрона приблизительно равны единице. Поэтому масса ядра с массовым числом А приблизительно равна А а.е.м.
Если рассчитать массу какого-либо изотопа (изотопную массу), суммируя массы соответствующего числа протонов, нейтронов и электронов, результат не даст точного соответствия с экспериментом. Расхождение между вычис-
39
ленным и экспериментально найденным значениями изотопных масс называют
дефектом массы.
Так, например, изотопная масса одного из изотопов хлора 35Cl, полученная сложением масс семнадцати протонов, восемнадцати нейтронов и семнадцати электронов равна:
17·1.007277 + 18·1.008665 + 17·0.000548 = 35.289005 а.е.м.
Однако точные экспериментальные определения этой величины дают результат 34.96885 а.е.м. Дефект массы составляет 0.32016 а.е.м.
Объяснения явлению дефекта массы можно дать с помощью представлений, сформулированных Альбертом Эйнштейном в теории относительности. Дефект массы соответствует той энергии, которая необходима для преодоления сил отталкивания между протонами.
Иными словами, дефект массы есть мера энергии связи ядерных частиц. Если бы удалось разделить ядро на составляющие его нуклоны, то масса системы возросла бы на величину дефекта массы. Энергия связи показывает разность между энергией нуклонов в ядре и их энергией в свободном состоянии, т.е. энергия связи – это энергия, которую нужно затратить для разделения ядра на составляющие его нуклоны.
Энергию связи можно вычислить по формуле А. Эйнштейна:
E = mc2,
где: m – масса в кг, с – скорость света – 2.9979·108 м/с, E – энергия в Дж. Например, энергия связи для одного моль (4 г) нуклида 4He (молярный
дефект массы составляет 3.0378·10-5 кг) равна:
∆Е = (3.0378·10-5 кг/моль)·(2.9979·108 м/с)2 = 2.730·1012 Дж/моль Такая энергия превышает энергию обычной ковалентной связи более, чем
в 10 миллионов раз. Для получения подобной энергией за счет химической реакции нужно было бы использовать десятки тонн вещества.
40
Поскольку энергия связи крайне велика, принято выражать ее в мегаэлектронвольтах (1 МэВ = 9.6·1010 Дж/моль) на один нуклон. Так, энергия связи на один нуклон в ядре 4He составляет примерно 7 МэВ, в ядре 35Cl – 8.5 МэВ.
1.9.5. Ядерные силы
Ядро атома – особый объект для изучения. Даже при поверхностном его рассмотрении возникает множество недоумений. Почему протоны, входящие в состав ядра не отталкиваются согласно элементарным законам электростатики? Простейший расчет с помощью закона Кулона показывает, что на ядерных расстояниях два протона должны отталкиваться с силой около 6000 Н, а они притягиваются друг к другу с силой, в 40 раз превосходящей эту величину. Причем эта сила одинаково действует как между двумя протонами, так и между двумя нейтронами, а также между протоном и нейтроном, т.е. совершенно не зависит от заряда частиц.
Очевидно, ядерные силы представляют собой совершенно иной класс сил, сводить их к электростатическим взаимодействиям нельзя. Энергия, сопровождающая ядерные реакции, в миллионы раз превышает энергию, характеризующую химические превращения.
Применение принципов квантовой механики к описанию движения электронов дает в настоящее время весьма удовлетворительные результаты. Можно ли использовать эту теорию для моделирования процессов, происходящих в ядре атома? Важнейшей особенностью ядерных сил является чрезвычайно малый радиус их действия. Действительно, движение электрона происходит в области пространства, оцениваемой величинами порядка 10-8 см, а все внутриядерные явления происходят на расстояниях порядка 10-12 см и меньше. Эти величины чуть больше собственных размеров нуклонов. Соотношение масштабов, характеризующих движение электрона с одной стороны и внутриядерных явлений с другой по порядку величин можно сопоставить с тем же соотношением
41
для макромира, подчиняющегося законам классической механики, и микромира, живущего по законам квантовой механики.
При столь малых размерах ядра в нем сосредоточена практически вся масса атома. Зная приблизительный объем ядра и массу атома, можно оценить плотность ядерного вещества: она превосходит среднюю плотность обычной материи в 2·1017 раз и составляет величину порядка 1013 — 1014 г/см3. Попытка реально осознать подобные величины приводит к такой иллюстрации: при подобной плотности вещества в объеме спичечной головки (примерно 5 мм3) должна содержаться масса, равная массе 1 миллиона тонн воды. Если бы такая спичечная головка упала на поверхность Земли, она пробила бы все горные породы и проникла бы в центр планеты.
1.9.6. Ядерные превращения
Превращения атомных ядер, обусловленные их взаимодействиями с элементарными частицами или друг с другом, называются ядерными реакциями.
Самопроизвольный распад ядер – естественная радиоактивность – сопровождается излучением трех видов.
Альфа-излучение представляет собой поток ядер атомов гелия с зарядом +2 и массовым числом 4 (4He). Положительный заряд этих частиц объясняет факт отклонения альфа-лучей в электрическом поле в сторону отрицательно заряженной пластины, а сравнительно большой размер атомов гелия обосновывает значительно меньшую по сравнению с двумя другими видами излучений проникающую способность.
Очевидно, при испускании такой частицы ядро теряет два протона и два нейтрона. Потеря двух протонов уменьшает атомный номер на две единицы, следовательно, результатом является образование нового химического элемента.
42
Например, нуклид радия-226 при потере альфа-частицы превращается в нуклид радона-222, что может быть представлено в виде уравнения ядерной реакции:
88Ra → 86Rn + 2He.
При составлении подобных уравнений следует соблюдать равенство сумм атомных номеров и сумм массовых чисел в левой и правой части (должно быть обеспечено сохранение заряда и массы).
В ряде случаев используется и сокращенная форма записи уравнения ядерной реакции: слева записывают исходный нуклид, справа – конечный, в скобках между ними указывают сначала частицу, вызывающую данное превращение, а затем испускаемую в его результате. При этом для таких частиц применяют буквенные обозначения: α (альфа-частица), p (протон), n (нейтрон), d (ядро дейтерия – дейтрон) и т.п. Например, для рассмотренного выше альфараспада:
226 222
Ra (-, α) Rn.
Знак «-» говорит об отсутствии бомбардирующей частицы (распад ядра происходит самопроизвольно).
Бета-излучение в свою очередь подразделяется на β—(его обычно назы-
вают просто β-излучением) и β+-излучение. β—-излучение представляет собой поток электронов, движущихся со скоростью, близкой к скорости света. Эти электроны возникают в результате распада нейтрона:
0n → 1p + -1e.
Поскольку в ядре возникает дополнительный протон, атомный номер увеличивается на единицу, происходит образование нового химического элемента, например:
43
90Th → 91Pa + -1e.
Нуклиды тория-234 и протактиния-234 обладают одинаковыми массовыми числами. Такие нуклиды называются изобарами.
Возникновение β+-излучения обусловлено превращением протона в нейтрон, сопровождаемое испусканием позитрона – элементарной частицы, являющейся аналогом электрона, но обладающей положительным зарядом:
1p → 0n + +1e.
При этом атомный номер уменьшается на единицу за счет потери одного протона, а массовое число остается прежним: потеря массы одного протона компенсируется массой возникающего нейтрона. Примером ядерной реакции этого типа может служить превращение нуклида калия в нуклид аргона:
19K → 18Ar + +1e.
Гамма-излучение является жестким электромагнитным излучением с меньшими длинами волн, чем рентгеновское. Оно не отклоняется в электрическом и магнитном полях и обладает высокой проникающей способностью.
Испускание γ-лучей сопровождает α— и β-распад, а также процесс электронного захвата ядром. В последнем случае ядро захватывает электрон с низкого энергетического уровня (K- или L-электрон), и один из протонов превращается в нейтрон:
Массовое число нуклида не изменяется, а атомный номер уменьшается на единицу, например:
44
49 0 49
23V + -1e → 22Ti.
Неустойчивые, самопроизвольно распадающиеся нуклиды называют ра-
дионуклидами или радиоактивными изотопами. Их распад продолжается до тех пор, пока не образуются устойчивые изотопы. Устойчивые изотопы уже не подвержены радиоактивному распаду, поэтому они сохраняются в природе. Примерами могут служить16O и 12C.
Периодом полураспада неустойчивого изотопа называют время, в течение которого его радиоактивность уменьшается вдвое по сравнению с исходной. Периоды полураспада могут составлять от миллионных долей секунды до миллионов лет (табл. 1.2).
Таблица 1.2
Периоды полураспада некоторых изотопов
|
Изотоп |
Период полураспада |
|||
|
212 |
Po |
3·10-7 c |
||
|
214 |
Bi |
19.7 мин |
||
|
224 |
Ra |
3.64 суток |
||
|
210 |
Pb |
19.7 года |
||
|
14 |
C |
5.7·103 |
лет |
|
|
238 |
U |
4.5·109 |
лет |
|
|
232 |
Th |
1.39·1010 лет |
||
45
Многие реакции радиоактивного распада являются составными частями более сложных последовательных ядерных реакций – так называемых рядов радиоактивных превращений или радиоактивных рядов.
Каждое превращение в таком ряду приводит к образованию неустойчивого изотопа, который в свою очередь претерпевает радиоактивный распад. Исходный нуклид называют материнским изотопом, а образующийся – дочерним изотопом. На следующей стадии дочерний изотоп становится материнским, превращаясь в следующий дочерний и т.д. Эта цепь последовательных превращений продолжается до тех пор, пока результатом ядерной реакции не станет устойчивый изотоп.
Так, радиоактивный ряд урана начинается от изотопа 238U и в результате четырнадцати последовательных реакций ядерного распада заканчивается на устойчивом изотопе 206Pb. При этом суммарная потеря массы составляет 32 единицы.
Как устойчивые, так и неустойчивые нуклиды можно получать с помощью ядерных реакций, бомбардируя ядра частицами с высокой энергией. Пер-
вое искусственное ядерное превращение осуществил Э. Резерфорд: в 1915 го-
ду, пропуская альфа-лучи через азот, он получил устойчивый изотоп кислорода 17O. В 1935 году Ирен и Фредерик Жолио-Кюри доказали, что в результате бомбардировки алюминия альфа-частицами образуется радиоактивный изотоп фосфора, излучающий позитроны. За открытие искусственной радиоактивности ученые были удостоены Нобелевской премии.
При проведении ядерных реакций ядерную мишень бомбардируют протонами, нейтронами, электронами, что приводит к изменению ядерного состава и образованию нового химического элемента. Бомбардирующие частицы должны обладать высокой кинетической энергией для преодоления электростатических сил отталкивания со стороны мишени. Поэтому частицы разгоняют до высоких скоростей в специальных установках, называемых ускорителями (два их основных типа: линейный ускоритель и циклотрон).
46
|
Таблица 1.3 |
||||||||
|
Ядерные реакции |
||||||||
|
Примеры |
||||||||
|
№ |
Тип |
|||||||
|
Полное уравнение |
Сокращенная форма |
|||||||
|
1 |
(α,p) |
14 |
4 |
17 |
1 |
|||
|
7N + 2He |
→ 8O |
+ 1H |
14N (α,p)17O |
|||||
|
2 |
(α,n) |
27 |
4 |
30 |
1 |
|||
|
13Al + 2He → 15P + 0n |
27Al (α,n)30P |
|||||||
|
3 |
(p,n) |
23 |
1 |
23 |
1 |
|||
|
11Na + 1H → 12Mg + 0n |
23Na (p,n)23Mg |
|||||||
|
4 |
(p, α) |
9 |
1 |
6 |
4 |
|||
|
4Be + 1H → 3Li + 2He |
9Be (p, α)6Li |
|||||||
|
5 |
γ |
14 |
1 |
15 |
||||
|
(p, ) |
||||||||
|
7N + 1H → 8O + γ |
14N (p,γ)15O |
|||||||
|
6 |
(d,p) |
31 |
2 |
32 |
1 |
|||
|
15P + 1H → 15P + 1H |
31P (d,p)32P |
|||||||
|
7 |
(d,n) |
27 |
2 |
28 |
1 |
|||
|
13Al + 1H → 14Si + 0n |
27Al (d,n)28Si |
|||||||
|
8 |
(n,p) |
14 |
1 |
14 |
1 |
|||
|
7N + 0n → 6C + 1H |
14N (n,p)14C |
|||||||
|
9 |
γ |
59 |
1 |
60 |
||||
|
(n, ) |
||||||||
|
27Co + 0n →27Co + γ |
59Co (n,γ) 60Co |
|||||||
|
10 |
(n, α) |
27 |
1 |
24 |
4 |
|||
|
13Al + 0n → 11Na + 2He |
27Al (n,α)24Na |
|||||||
Искусственные ядерные превращения можно классифицировать по типу бомбардирующих и испускаемых в результате реакции частиц (табл. 1.3.).
47
С помощью ядерных реакций были синтезированы новые химические элементы с порядковыми номерами 99 и более. С этой целью ядерная мишень бомбардируется тяжелыми частицами, например, 7N или 12C. Так, элемент эйнштейний был получен в результате бомбардировки урана-238 ядрами азота-14:
92U + 7N →99Es + 4 0n,
а элемент с порядковым номером 102 (нобелий) – путем бомбардировки кюрия246 ядрами углерода-12:
|
246 |
12 |
254 |
1 |
|
96Cm + 6C |
→ 102No + |
4 0n. |
М А Т Е Р И А Л Ы Д Л Я П О В Т О Р Е Н И Я
Размеры атома: ≈ 10-8 см Размеры ядра: ≈ 10-12 – 10-13 см
Плотность ядерного вещества: ≈ 1014 г/см3
Субатомные частицы
|
частица |
масса |
заряд, |
автор |
||
|
услов. |
открытия (дата) |
||||
|
г |
а.е.м. |
||||
|
ед. |
|||||
|
ЭЛЕКТРОН |
9.110 10-28 |
0 |
-1 |
Томпсон (1897) |
|
|
ПРОТОН |
1.673 10-24 |
1 |
+1 |
Резерфорд (1914) |
|
|
НЕЙТРОН |
1.675 10-24 |
1 |
0 |
Чедвик (1932) |
|
48
Квантовые числа
|
№ |
Название |
Обозначение |
Принимаемые |
Что характеризует |
|
|
значения |
|||||
|
1 |
Главное |
n |
1, 2, 3, … |
энергетический |
|
|
уровень |
|||||
|
2 |
Орбитальное |
ℓ |
0, 1, 2, …n–1 |
форма орбитали, |
|
|
энергетический |
|||||
|
подуровень |
|||||
|
3 |
Магнитное |
mA |
–ℓ,..,–1,0,+1,..,+ ℓ |
пространственная |
|
|
ориентация |
|||||
|
орбитали |
|||||
|
4 |
Спиновое |
ms |
+½, —½ |
собственный |
|
|
импульс |
|||||
|
электрона |
|||||
Электронные формулы атомов
Чтобы составить электронную формулу атома, необходимо знать следующее:
1. Систему обозначений: nℓх (n – номер энергетического уровня: 1,2,3,…, ℓ – буквенное обозначение подуровня: s, p, d, f; x – число электронов). Примеры: 5s2 – два электрона на s–подуровне пятого энергетического уровня (n = 5, ℓ = 0), 4d8 — восемь электронов на d-подуровне четвертого энергетического уровня (n = 4, ℓ = 2).
2. Последовательность заполнения энергетических подуровней: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s < 5f…
49
(каждый подуровень заполняется только после того, как полностью застроится предыдущий в этом ряду).
3.Максимальную емкость подуровней:
|
S – 2 электрона |
d – 10 электронов |
|
р – 6 электронов |
f – 14 электронов |
Пример: электронная формула атома хлора представляет собой распределение семнадцати электронов данного атома по энергетическим подуровням и имеет вид:
17 Cl 1s2 2s2 2p6 3s2 3p5
Краткая форма записи электронной формулы: электроны, находящие-
ся на полностью застроенных энергетических уровнях, представляются символом соответствующего благородного газа, далее указывается распределение остальных электронов.
Пример: краткая электронная формула атома хлора:
17 Cl [Ne] 3s2 3p5
Распределение электронов по квантовым ячейкам
Квантовые ячейки
s-подуровень
p-подуровень
d-подуровень
f-подуровень
50
В соответствии с правилом Хунда: первоначально каждому электрону предоставляется отдельная квантовая ячейка (неспаренные электроны с параллельными спинами), следующие электроны поступают в уже занятые ячейки, для них значения ms имеют противоположный знак – спаренные электроны).
Обозначения: ↑ ms = + ½, ↓ ms = — ½
Примеры: 6 электронов занимают квантовые ячейки f-подуровня:
↑ ↑ ↑ ↑ ↑ ↑
f-подуровень
для девяти электронов схема приобретает вид:
↑↓ ↑↓ ↑ ↑ ↑ ↑ ↑
f-подуровень
Электронно-графические формулы атомов
|
17Cl |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑ |
||||
|
1s2 |
2s2 |
2p 6 |
3s2 |
3p5 |
Валентные электроны — электроны внешнего энергетического уровня, а также предпоследнего d-подуровня, если он застроен неполностью.
Ядро
Обозначения нуклида:
верхний индекс — массовое число нуклида, нижний индекс — атомный номер соответствующего элемента.
Пример: изотоп хлора:
51
36
17Cl
Сокращенное обозначение: 36Cl
Состав ядра Число протонов – атомный номер, порядковый номер элемента в перио-
дической системе Д. И. Менделеева; Число нейтронов – разность между массовым числом и числом про-
тонов.
Пример: число протонов и нейтронов для изотопа хлора
36
17Cl составляет: число протонов = 17, число нейтронов = 36-17= 19.
Изотопы – один атомный номер, разные атомные массы ( ядро содержит одинаковое число протонов, разное число нейтронов)
Ядерные реакции
В левой и правой части уравнения ядерной реакции должен соблюдаться баланс между:
–суммами массовых чисел (верхних индексов),
–суммами атомных номеров (нижних индексов).
Пример:
|
239 |
1 |
98 |
139 |
1 |
|
94Pu + 0n → 40Zr + 54Xe + 3 0n |
||||
|
Суммарное массовое число: 239 + 1 |
= 98 + 139 + 3·1 |
|||
|
240 = |
240 |
|||
|
Сумма атомных номеров: 94 + 0 = 40 + 54 + 3·0 |
||||
|
94 = |
94 |
Cокращенная форма записи уравнения ядерной реакции:
•слева — исходный нуклид,
•справа – конечный нуклид,
52
• в скобках между ними: частица, вызывающая данное превращение, затем частица, испускаемая в его результате.
Буквенные обозначения: α (альфа-частица), p (протон), n (нейтрон), d (ядро дейтерия – дейтрон) и т.п.
Пример: 23Na (p,n)23Mg для реакции
11Na + 1H → 12Mg + 0n
53
Соседние файлы в папке Доп материалы
- #
- #
18.03.20150 б3Смолова К практич зан по химии.pdf