Слайд 2
ГРАДУИРОВКА СПЕКТРОСКОПА
ОПРЕДЕЛЕНИЕ ДЛИНЫ ВОЛНЫ СПЕКТРАЛЬНЫХ ЛИНИЙ

Слайд 3
Цель работы:
научиться пользоваться спектроскопом, провести его градуировку, исследовать

спектры поглощения и испускания, ознакомиться с элементами качественного спектрального
анализа.
Приборы и принадлежности:
спектроскоп, индукционная катушка, источник постоянного тока на
6 – 12 В, источник света (лампа накаливания), спиртовая горелка, пробирка с раствором КМnО4.
Слайд 5
Ход лучей в спектроскопе
Лучи света выходят из коллиматора
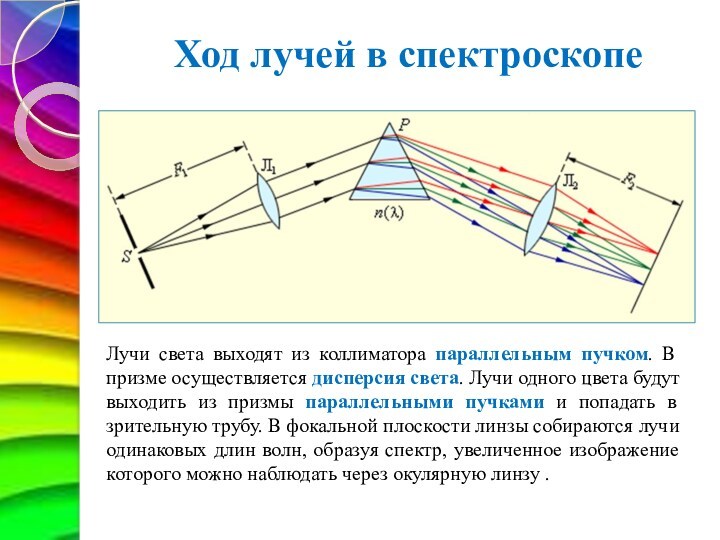
параллельным пучком. В призме осуществляется дисперсия света. Лучи одного
цвета будут выходить из призмы параллельными пучками и попадать в
зрительную трубу. В фокальной плоскости линзы собираются лучи одинаковых длин волн, образуя спектр, увеличенное изображение которого можно наблюдать через окулярную линзу .
Слайд 6
Отсчетный механизм спектроскопа и определение цены деления шкалы
Для

определения относительного положения полос спектра в окулярной трубе спектроскопа
имеется специальный треугольный указатель-маркер, который при помощи микрометрического винта (отсчетного
механизма спектроскопа) можно перемещать и совместить с любой спектральной линией.
Слайд 7
На основную шкалу спектроскопа (горизонтальный винт) нанесены миллиметровые
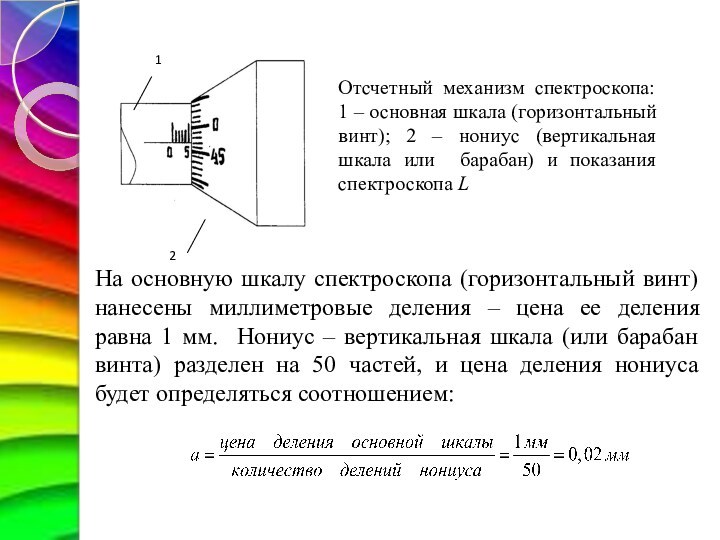
деления – цена ее деления равна 1 мм. Нониус
– вертикальная шкала (или барабан винта) разделен на 50 частей,
и цена деления нониуса будет определяться соотношением:
Слайд 8
Показания спектроскопа L можно найти по формуле:
L

= (N+na)
где N – число миллиметров, отсчитанное вдоль основной
шкалы (горизонтального винта); n – число делений на нониусе (шкале
барабана), а – цена деления нониуса.
Например,
Слайд 9
Градуировка спектроскопа
Шкала спектроскопа позволяет определить только относительное положение

спектральных линий и расстояние между ними, но не длину
волны соответствующих линий. Для того, чтобы с помощью спектроскопа можно
было определить длину волны линий исследуемого спектра, спектроскоп необходимо проградуировать, т.е. установить зависимость между длинами волн спектральных линий, наблюдаемых в поле зрения и делениями шкалы L отсчётного устройства спектроскопа.
Другими словами, проградуировать спектроскоп – значит построить график, у которого на оси Y отложены показания шкалы L отсчётного механизма спектроскопа в миллиметрах, а на оси Х – длина волны λ, нм
Слайд 11
Опыт 1. Градуировка спектроскопа
Расположить лампу дневного света (содержит

пары ртути) перед щелью коллиматора, зажечь лампу.
Лампа помещена
в футляр с отверстиями для исключения слишком большой освещен-ности рабочего
места и поля зрения спектроскопа через линзы.
Слайд 12
Опыт 1. Градуировка спектроскопа
С помощью окуляра добиться четкого

изображения спектра и маркера (треугольный указатель) в поле зрения
окуляра.
Навести маркер-указатель на определенную линию или полосу в спектре, и
провести измерение с отсчетного устройства.
Слайд 13
Опыт 1. Градуировка спектроскопа
Затем, вращая барабан, перевести указатель
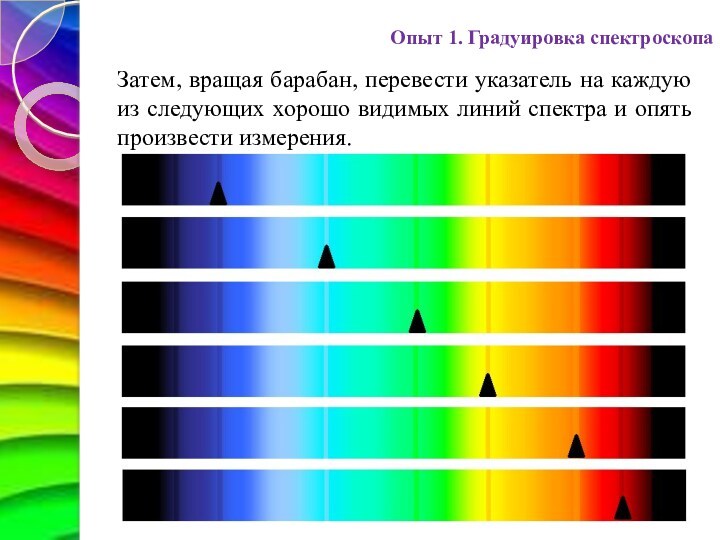
на каждую из следующих хорошо видимых линий спектра и
опять произвести измерения.
Слайд 14
Опыт 1. Градуировка спектроскопа
Таким образом, определить положение всех
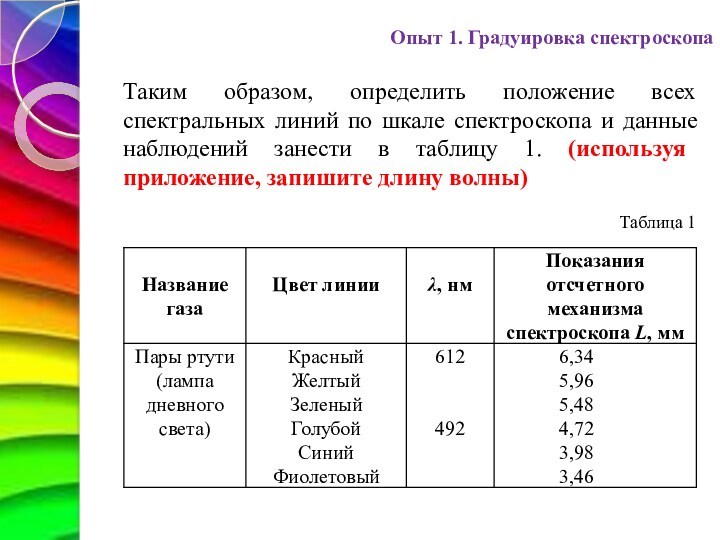
спектральных линий по шкале спектроскопа и данные наблюдений занести
в таблицу 1. (используя приложение, запишите длину волны)
Таблица 1
Слайд 16
Построить градуировочную кривую спектроскопа для лампы дневного света
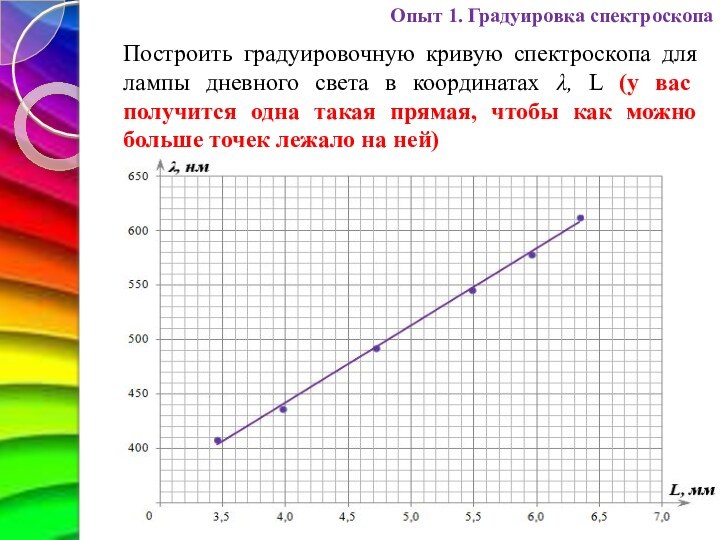
в координатах λ, L (у вас получится одна такая
прямая, чтобы как можно больше точек лежало на ней)
Опыт 1.
Градуировка спектроскопа
Слайд 17
Опыт 2. Исследование спектров испускания
Спиртовую горелку с раство-ром

соли NaCl в спирте поджечь и поместить перед щелью
коллиматора.
Пронаблюдать спектр испускания паров натрия в пламени горелки. (ниже
изображено то, что мы увидим в спектроскопе)
Слайд 18
Опыт 2. Исследование спектров испускания
Определить положение линии спектра
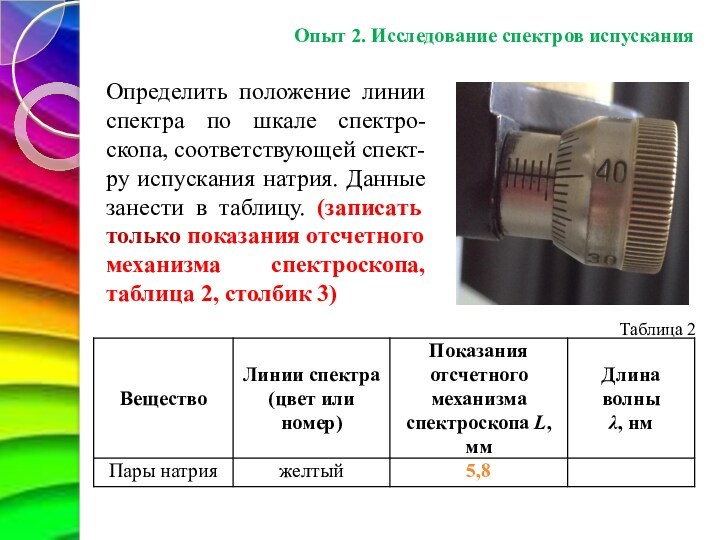
по шкале спектро-скопа, соответствующей спект-ру испускания натрия. Данные занести
в таблицу. (записать только показания отсчетного механизма спектроскопа, таблица 2,
столбик 3)
Таблица 2
Слайд 19
С помощью полученной ранее градуировочной кривой (график у
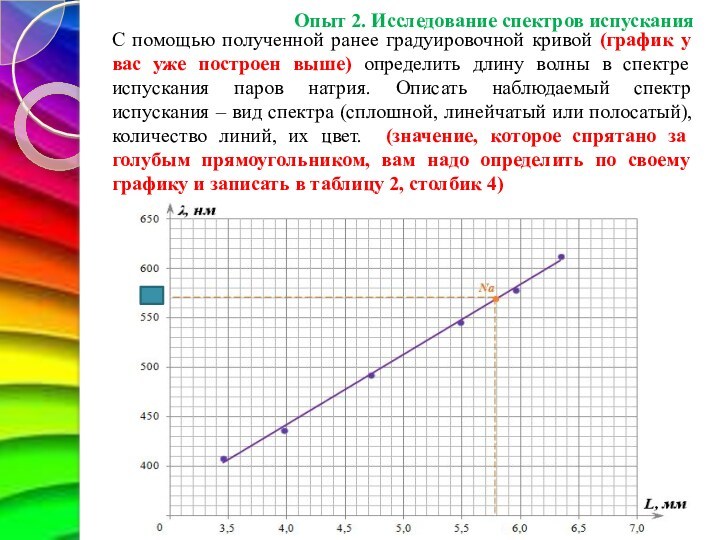
вас уже построен выше) определить длину волны в спектре
испускания паров натрия. Описать наблюдаемый спектр испускания – вид спектра
(сплошной, линейчатый или полосатый), количество линий, их цвет. (значение, которое спрятано за голубым прямоугольником, вам надо определить по своему графику и записать в таблицу 2, столбик 4)
Опыт 2. Исследование спектров испускания
Слайд 20
Опыт 3. Исследование спектров поглощения
Между осветителем (лам-пой накаливания)

и щелью коллиматора поместить ис-следуемое вещество (раст-вор КМnО4). Пронаблюдать
спектр поглощения (темные линии).
Слайд 21
Опыт 3. Исследование спектров поглощения
По шкале спектроскопа определить
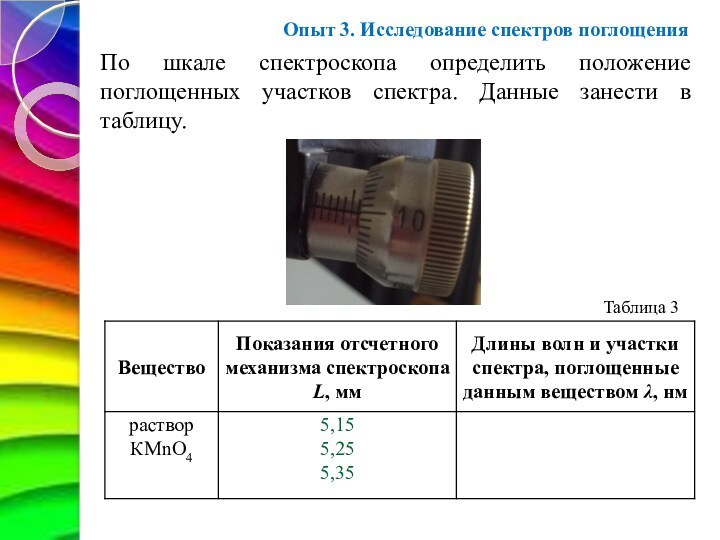
положение поглощенных участков спектра. Данные занести в таблицу.
Таблица 3
Слайд 22
С помощью градуировочной кривой (она уже у вас
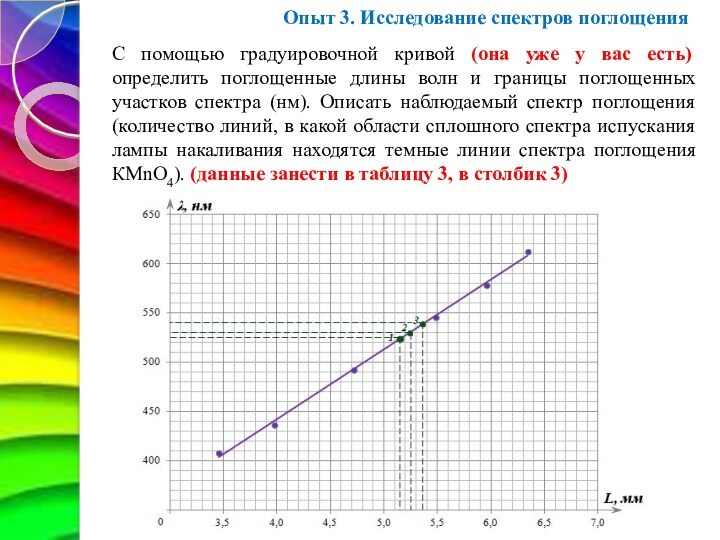
есть) определить поглощенные длины волн и границы поглощенных участков
спектра (нм). Описать наблюдаемый спектр поглощения (количество линий, в какой
области сплошного спектра испускания лампы накаливания находятся темные линии спектра поглощения КМnО4). (данные занести в таблицу 3, в столбик 3)
Опыт 3. Исследование спектров поглощения
Слайд 23
Контрольные вопросы
Из каких составных частей состоит спектроскоп и

каково их назначение?
Вычертить ход лучей в спектроскопе.
Что такое спектр
излучения?
Что такое спектр поглощения?
Объяснить происхождение линейчатых, сплошных и полосатых спектров.
Что
такое спектральный анализ?
Как проградуировать спектроскоп?
Как определить длину волны линии в спектре излучения какого-либо вещества?
Слайд 24
По результатам эксперимента сделать вывод

В
настоящее время определение длин волн
спектральных линий является одним из
наиболее точных физических измерений.
Цель задания заключается в ознакомлении
с методами определения длин волн
спектральных
линий и с применением этих методов к
измерению длин волн нескольких
(56)
спектральных линий исследуемого
вещества. Существует много различных
способов, позволяющих вычислять длины
волн
спектральных
линий с точностью до
0,001 %.
Рассмотрим способы определения длины
волны для призменного спектрографа.
В этом
случае определение длины волны состоит
в сравнении данной длины волны со
стандартными
нормалями, для которых длины волн точно
измерены. Сравнение можно провести
несколькими способами.
1.
Для ориентировочного определения длины
волны можно воспользоваться графической
интерполяцией градуировочной
(дисперсионной) кривой спектрального
прибора или непосредственной
шкалой
длин волн, если последняя имеется в
приборе. С помощью компаратора измеряют
расстояние неизвестных линий до ближайших
известных линий. Затем, пользуясь
дисперсионной кривой, определяют
неизвестные
длины волн. Для получения достаточной
точности нужно иметь в данной области
спектра много известных линий сравнения,
в результате измерения которых получается
много точек на дисперсионной кривой.
Дисперсионную (градуировочную) кривую
в этом случае строят в очень большом
масштабе. Таким способом можно вычислить
длину волны с точностью до 10,5
Å.
2.
Если необходимо добиться большой
точности, то для определения длины волны
прибегают к математической интерполяции.
Если
исследуемая линия находится между двумя
линиями сравнения, расположенными
настолько близко к друг другу, что
участок дисперсионной
кривой
между ними можно с большой точностью
считать прямой линией, то пользуются
линейной интерполяцией.
В
случае линейной интерполяции поступают
следующим образом: пусть имеются две
спектральные линии
и
,
длины волн которых необходимо измерить
(рис. 7а). По обе стороны от них в эталонном
спектре
железа
находят линии, длины волн которых заранее
точно известны,
это нормали длин волн (берутся по атласу
железа). Необходимо на компараторе
измерить расстояние
и
неизвестных
линий
и
от
линий сравнения 1
и расстояние d
между линиями сравнения 1
и 2.
Определение
неизвестной длины волны в случае линейной
интерполяции
основывается на соотношении
(9)
где
коэффициент при
– средняя дисперсия на участке
спектральных линий 1
и 2
. Такой способ вычисления длины волны
вполне пригоден для приборов с
дифракционными решетками. Для призменных
приборов этот способ можно применять,
если (1-2)
не превосходит
50 Å.
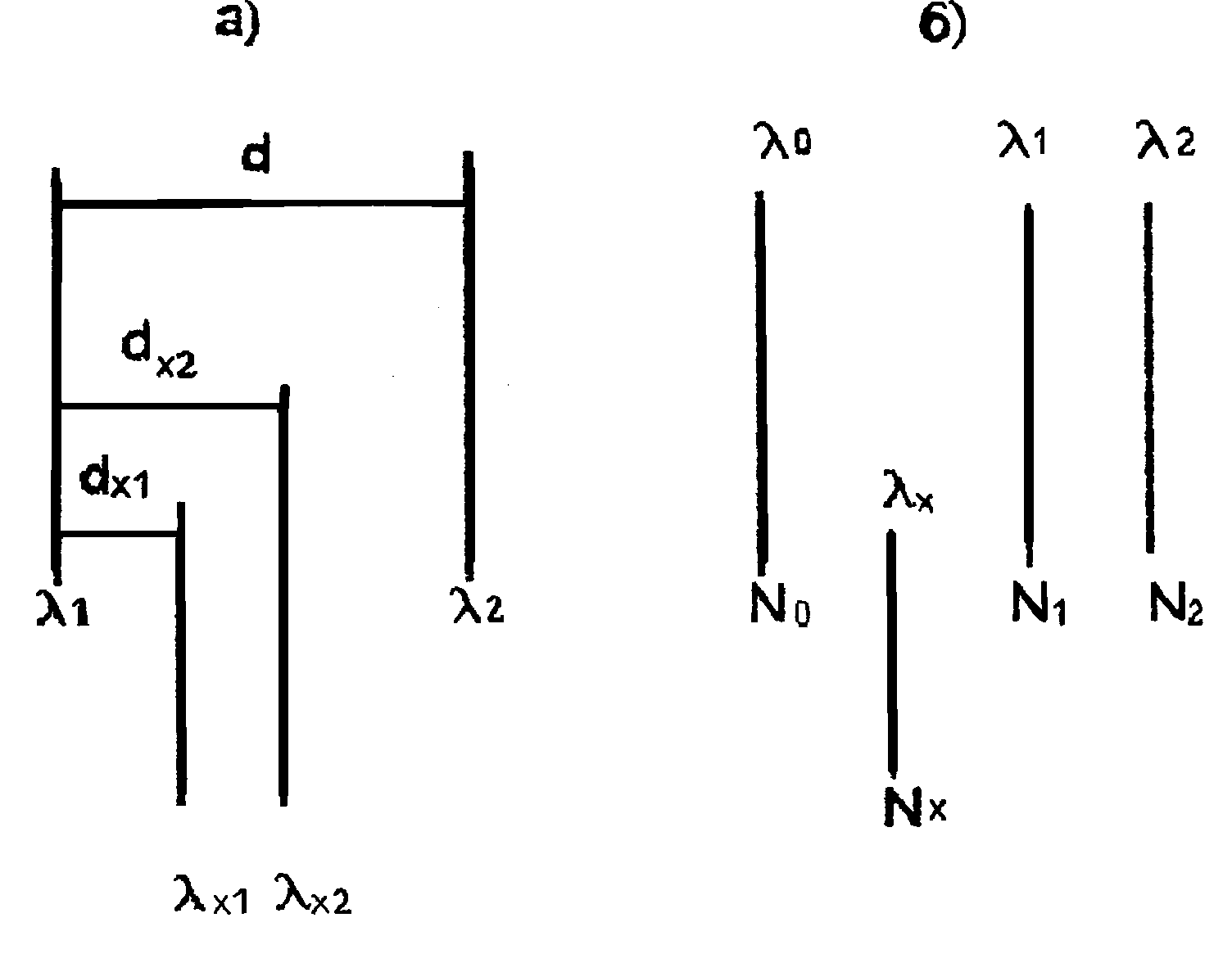
Рис. 7.
Расположение нормалей и измеряемых
длин волн в спектре для линейной (а) и
квадратичной (б) интерполяции
Более
точное определение длины волны можно
производить по интерполяционным формулам
второго порядка (интерполяция отрезком
параболы)
по трём «нормалям» эталонного спектра:
0,
1,
2,
расположенным
в небольшом спектральном участке (рис.
7б). При
этом обычно используют соотношение
, (10)
где
A
и B
– постоянные величины; l
– расстояние между «нормалью»
и измеряемой длиной волны. Для определения
x
следует на компараторе измерить положение
нормалей и неизвестной линии.
Пусть
отсчёты положения этих линий будут N0,
N1,
N2
и Nх.
Так как длины волн всех трех «нормалей»
известны, то согласно интерполяционной
формуле можно составить два уравнения:
;
.
Эти
уравнения дают возможность определить
постоянные А
и В,
входящие в них. Пользуясь далее этими
постоянными, можно вычислить неизвестную
длину волны
по формуле
. (11)
При
анализе погрешностей, возникающих в
процессе измерений и расчетов, следует
иметь в
виду, что
основная неточность возникает при
снятии отсчетов N.
Для компаратора Аббе
N
= ±
0,001 мм.
Легко
показать, что коэффициент А, равный
d/dn,
соответствует линейной дисперсии
спектрального прибора. Это, в частности,
следует из того факта, что формула (11)
является разложением функции x
= f(N)
в ряд
Тейлора
около точки (No,
о
), т.е.
Учитывая
это, можно определить погрешность
При
большей линейной дисперсии прибора
точность в определении x
будет увеличена.
Вычисленная
по формуле
(10) неизвестная
длина волны затем сверяется с табличными
данными. Таким образом можно определить,
какому элементу принадлежит данная
спектральная линия.
Если
же линии сравнения эталонного спектра
расположены на таком расстоянии друг
от друга, что необходимо учитывать
кривизну дисперсионной
кривой, то
при математической интерполяции для
спектров, полученных с призменными
спектрографами, пользуются формулой
Гартмана.
Дисперсионная
формула Гартмана имеет вид
(12)
где
0,
C,
d0
– три постоянные, подбираемые по трём
известным линиям;
и d
–
длина волны
и отсчет компаратора для неизвестной
линии. Эта формула представляет собой
кривую дисперсии призменного спектрографа
с хорошим приближением.
Для
определения постоянных формулы Гартмана
0,
C,
d
производится измерение трёх известных
линий –
1,
2
и 3
(нормалей) и отсчитываются положения
этих линий (d1,d2
и d3)
на компараторе. Составляются три
уравнения, из которых определяются
постоянные
Решение
этих уравнений дает следующие значения
постоянных:
;
.
Получив
численные значения этих постоянных по
формуле Гартмана, можно определить
длину волны x
неизвестной линии по отсчёту для неё.
Экспериментально
по полученному снимку спектра исследуемого
вещества:
1)
определяют длину волны двух спектральных
линий, используя линейную интерполяционную
формулу (9);
2)
вычисляют длину волны нескольких линий
исследуемого вещества, используя формулу
квадратичной интерполяции (11);
3)
по формуле Гартмана определяют длины
волн тех же спектральных линий.
Длины
волн следует подставлять в формулу для
расчёта с точностью до сотых долей
ангстрема.
Контрольные
вопросы к лабораторной работе № 5
-
Как выглядит
оптическая схема спектрографа ИСП-28? -
Какие основные
элементы содеожит любой спектраль-ный
прибор? -
Что является
диспергирующим элементом в спектро-графе
ИСП-28? -
Какую роль выполняют
коллиматорный и камерный объективы? -
Что называется
спектром? -
Для чего при снятии
спектров на ИСП-28 применяется диафрагма
Гартмана? -
Для какой
спектральной области предназначен
ИСП-28? -
Из какого материала
изготовлены призма и линзы спек-трографа? -
Как устроена
призма Корню? -
Чем отличается
линейная дисперсия от угловой? Для чего
вводятся эти понятия?
Редомендуемая
литература
[1], [12], [13], [14].
Таблица 4
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
03.05.2019796.16 Кб2№1.doc
- #
04.05.2019209.92 Кб1№2.doc
- #
- #
10.08.2019237.57 Кб1№3.doc
- #
- #
04.05.2019465.92 Кб3№5.doc
- #
04.05.2019826.37 Кб0№6.doc
- #
10.08.2019283.14 Кб1№7.doc
- #
04.05.2019471.55 Кб2№8.doc
Длина — волна — спектральная линия
Cтраница 1
Длины волн спектральных линий подчиняются строгим, закономерностям и при определенных условиях излучения остаются постоянными. Поэтому длина волны, соответствующая какой-нибудь спектральной линии, или некоторое число этих длин волн может быть принято за естественный эталон длины.
[1]
Длины волн спектральных линий округлены.
[3]
Длина волны спектральной линии является ее важнейшей характеристикой. Однако далеко не всегда удается сразу решить эту задачу. Дело в том, что разные элементы могут иметь линии с близкими длинами волн и требуется дополнительное изучение спектра, прежде чем удается точно установить принадлежность линии. Поэтому нужно подробно рассмотреть, каким образом можно производить идентификацию спектральных линий при качественном анализе.
[4]
Длины волн спектральных линий всех элементов остаются постоянными в обычных источниках света, практически не зависят от условий возбуждения спектра. Возможность спутать спектральные линии разных элементов с близкими длинами волн появляется только из-за того, что точность определения длины волны недостаточно высока.
[5]
Длина волны спектральной линии является ее важнейшей характеристикой. Однако далеко не всегда удается сразу решить эту задачу. Дело в том, что разные элементы могут иметь линии с близкими длинами волн и требуется дополнительное изучение спектра, прежде чем удается точно установить принадлежность линии. Поэтому нужно подробно рассмотреть, каким образом можно производить идентификацию спектральных линий при качественном анализе.
[6]
Длины волн спектральных линий всех элементов остаются постоянными в обычных источниках света, практически не зависят от условий возбуждения спектра. Возможность спутать спектральные линии разных элементов с близкими длинами волн появляется только из-за того, что точность определения длины волны недостаточно высока.
[7]
Длины волн спектральных линий подчиняются строгим закономерностям и при определенных условиях излучения остаются постоянными. Поэтому длина волны, соответствующая какой-нибудь спектральной линии, или некоторое число этих длин волн может быть принято за естественный эталон длины.
[8]
Длины волн спектральных линий обычно измеряются с точностью около 0 001 А при помощи спектрографов, разрешающая сила которых составляет только 0 010 А. Не нарушаются ли при этом какие-нибудь основные законы физики.
[9]
Длину волны спектральной линии измеряют с помощью двух дифракционных решеток. Спектральные максимумы в нулевом и первом порядках имеют вид, представленный на рисунках. На обоих рисунках масштабы одинаковые. У какой решетки больше период и какая решетка обладает большей разрешающей способностью. Оценить приблизительно эти разрешающие способности, считая, что естественная ширина и доплеровская ширина значительно меньше экспериментальной.
[10]
Как длины волн спектральных линий, так и вероятности излучения определяются свойствами атомной системы. Не входя в тонкости, остановимся на основных свойствах излучения атома, главным образом на тех, которые необходимы для уяснения деталей эмиссионного спектрального анализа.
[11]
Вместо длины волны часто употребляемых спектральных линий обычно указывают их буквенные обозначения.
[12]
Определение длин волн спектральных линий; открытие элементов, которым принадлежат эти линии.
[13]
Измерение длин волн спектральных линий основано на том, что между длиной волны спектральной линии К и положением ее на спектрограмме /, отсчитанным от некоторого ( произвольного) начала, за которое может быть ЕЗЯТ, например, нуль шкалы измерительного прибора, существует определенная зависимость.
[14]
Измерение длин волн спектральных линий основано на.
[15]
Страницы:
1
2
3
Линейчатые спектры
-
Темы кодификатора ЕГЭ: линейчатые спектры.
-
Спектр испускания
-
Спектр поглощения
-
Спектральный анализ
-
Линейчатые спектры
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: линейчатые спектры.
Если пропустить солнечный свет через стеклянную призму или дифракционную решётку, то возникнет хорошо известный вам непрерывный спектр (рис. 1)(Изображения на рис. 1, 2 и 3 взяты с сайта www.nanospectrum.ru):
Рис. 1. Непрерывный спектр
Спектр называется непрерывным потому, что в нём присутствуют все длины волн видимого диапазона — от красной границы до фиолетовой. Мы наблюдаем непрерывный спектр в виде сплошной полосы, состоящей из разных цветов.
Непрерывным спектром обладает не только солнечный свет, но и, например, свет электрической лампочки. Вообще, оказывается, что любые твёрдые и жидкие тела (а также весьма плотные газы), нагретые до высокой температуры, дают излучение с непрерывным спектром.
Ситуация качественно меняется, когда мы наблюдаем свечение разреженных газов. Спектр перестаёт быть непрерывным: в нём появляются разрывы, увеличивающиеся по мере разрежения газа. В предельном случае чрезвычайно разреженного атомарного газа спектр становится линейчатым — состоящим из отдельных достаточно тонких линий.
Мы рассмотрим два типа линейчатых спектров: спектр испускания и спектр поглощения.
к оглавлению ▴
Спектр испускания
Предположим, что газ состоит из атомов некоторого химического элемента и разрежен настолько, что атомы почти не взаимодействуют друг с другом. Раскладывая в спектр излучение такого газа (нагретого до достаточно высокой температуры), мы увидим примерно следующую картину (рис. 2):
Рис. 2. Линейчатый спектр испускания
Этот линейчатый спектр, образованный тонкими изолированными разноцветными линиями, называется спектром испускания.
Любой атомарный разреженный газ излучает свет с линейчатым спектром. Более того, для каждого химического элемента спектр испускания оказывается уникальным, играя роль «удостоверения личности» этого элемента. По набору линий спектра испускания можно однозначно сказать, с каким химическим элементом мы имеем дело.
Поскольку газ разрежен и атомы мало взаимодействуют друг с другом, мы можем заключить, что свет излучают атомы сами по себе. Таким образом, атом характеризуется дискретным, строго определённым набором длин волн излучаемого света. У каждого химического элемента, как мы уже сказали, этот набор свой.
к оглавлению ▴
Спектр поглощения
Атомы излучают свет, переходя из возбуждённого состояния в основное. Но вещество может не только излучать, но и поглощать свет. Атом, поглощая свет, совершает обратный процесс — переходит из основного состояния в возбуждённое.
Снова рассмотрим разреженный атомарный газ, но на сей раз в холодном состоянии (при достаточно низкой температуре). Свечения газа мы не увидим; не будучи нагретым, газ не излучает — атомов в возбуждённом состоянии оказывается для этого слишком мало.
Если сквозь наш холодный газ пропустить свет с непрерывным спектром, то можно увидеть что-то вроде этого (рис. 3):
Рис. 3. Линейчатый спектр поглощения
На фоне непрерывного спектра падающего света появляются тёмные линии, которые образуют так называемый спектр поглощения. Откуда берутся эти линии?
Под действием падающего света атомы газа переходят в возбуждённое состояние. При этом оказывается, что для возбуждения атомов годятся не любые длины волн, а лишь некоторые, строго определённые для данного сорта газа. Вот именно эти длины волн газ и «забирает себе» из проходящего света.
Более того, газ изымает из непрерывного спектра ровно те самые длины волн, которые излучает сам! Тёмные линии в спектре поглощения газа в точности соответствуют ярким линиям его спектра испускания. На рис. 4 сопоставлены спектры испускания и поглощения разреженных паров натрия (изображение с сайта www.nt.ntnu.no):
Рис. 4. Спектры поглощения и испускания для натрия
Впечатляющее совпадение линий, не правда ли?
Глядя на спектры испускания и поглощения, физики XIX века пришли к выводу, что атом не является неделимой частицей и обладает некоторой внутренней структурой. В самом деле, что-то ведь внутри атома должно обеспечивать механизм излучения и поглощения света!
Кроме того, уникальность атомных спектров говорит о том, что этот механизм различен у атомов разных химических элементов; стало быть, атомы разных химических элементов должны отличаться по своему внутреннему устройству.
Строению атома будет посвящён следующий листок.
к оглавлению ▴
Спектральный анализ
Использование линейчатых спектров в качестве уникальных «паспортов» химических элементов лежит в основе спектрального анализа — метода исследования химического состава вещества по его спектру.
Идея спектрального анализа проста: спектр излучения исследуемого вещества сопоставляется с эталонными спектрами химических элементов, после чего делается вывод о присутствии или отсутствии того или иного химического элемента в данном веществе. При определённых условиях методом спектрального анализа можно определить химический состав не только качественно, но и количественно.
В результате наблюдения различных спектров были открыты новые химические элементы.
Первыми из таких элементов были цезий и рубидий; они получили название по цвету линий своего спектра (В спектре цезия наиболее выражены две линии небесно-синего цвета, по-латыни называемого caesius. Рубидий же даёт две характерные линии рубинового цвета).
В 1868 году в спектре Солнца были обнаружены линии, не соответствующие ни одному из известных химических элементов. Новый элемент был назван гелием (от греческого гелиос — солнце). Впоследствии гелий был обнаружен в атмосфере Земли.
Вообще, спектральный анализ излучения Солнца и звёзд показал, что все входящие в их состав входят элементы имеются и на Земле. Таким образом, оказалось, что все объекты Вселенной собраны из одного и того же «набора кирпичиков».
Разберем задачи ЕГЭ по темам: Линейчатые спектры, спектры излучения и поглощения.
к оглавлению ▴
Линейчатые спектры
Задача 1
В 1912 г. английским физиком Альфредом Фаулером при изучении излучения вакуумных трубок, заполненных смесью водорода и гелия, была открыта спектральная серия, которую Фаулер ошибочно приписал водороду. Расчёты показывают, что одна из спектральных линий этой серии соответствует переходу электрона в атоме водорода с энергетического уровня с номером n = 3 на энергетический уровень с номером m =1,5 (хотя энергетического уровня с нецелым номером, конечно же, быть не может). Чему была равна длина волны, соответствовавшая данной спектральной линии? Ответ выразите в нанометрах и округлите до целого числа.
Дано:
n=3
m=1,5
Найти:
Решение.
Уровни энергии в атоме водорода определяются формулой: (эВ), где
и т.д. (1)
При переходе с уровня, соответствующего большему значению энергии (n=3) на уровень с меньшим значением энергии (m=1,5) происходит выделение энергии.
В соответствии с формулой (1), можно рассчитать выделившуюся энергию, которая соответствует указанному переходу
После подстановки численных значений получим:
(эВ).
Чтобы найти длину волны, соответствующую указанному излучению, надо воспользоваться формулой Планка:
С учетом перехода с уровня n на уровень m Отсюда необходимо выразить длину волны
Подстановка численных значений дает значение длины волны, соответствовавшая данной спектральной линии. В расчетах необходимо учесть, что 1эВ Дж.
(м) =
(м) = 273 (нм).
Ответ: 273 нм.
Задача 2
На рисунке показаны спектры поглощения трёх смесей неизвестных газов (1, 2 и 3), а также спектры излучения известных газов A и B. Какая из смесей содержит газ A? В качестве ответа запишите число, обозначающую смесь газов.
Решение.
На рисунке представлены линейчатые спектры смесей газов и отдельных газов. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре зависят только от свойств атомов этого вещества, но совершенно не зависят от способа возбуждения свечения атомов. Согласно рисунку, спектральные линии газа А содержатся в смеси газов 3.
Ответ: 3
Задача 3
Какую минимальную скорость должны иметь электроны, чтобы ударом перевести атом водорода из первого энергетического состояния в пятое?
Дано:
n=1
m=5
Найти:
Решение.
Уровни энергии в атоме водорода определяются формулой:
(эВ), где
и т.д.
Для перевода атома водорода из первого энергетического состояния в пятое, ему необходимо сообщить энергию, равную разности этих энергетических состояний.
Рассчитаем значение этой энергии.
(эВ)
В системе «СИ» с учетом того, что 1 эВ Дж.
(Дж).
Электроны, передающие атому водорода эту энергию, должны обладать кинетической энергией не меньшей, чем Дж.
Из последней формулы можно вывести и рассчитать скорость электронов.
масса электрона равна
кг.
(м/с) = 2,14 (Мм/с).
Ответ: 2,14 Мм/с
Благодарим за то, что пользуйтесь нашими материалами.
Информация на странице «Линейчатые спектры» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать необходимые и поступить в ВУЗ или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из разделов нашего сайта.
Публикация обновлена:
08.05.2023
Длина волны всех спектральных линий Решение
ШАГ 0: Сводка предварительного расчета
ШАГ 1. Преобразование входов в базовый блок
Начальная орбита: 3 —> Конверсия не требуется
Конечная орбита: 7 —> Конверсия не требуется
Атомный номер: 17 —> Конверсия не требуется
ШАГ 2: Оцените формулу
ШАГ 3: Преобразуйте результат в единицу вывода
0.00458824468631853 метр —>4588244.68631853 нанометр (Проверьте преобразование здесь)
21 Водородный спектр Калькуляторы
Длина волны всех спектральных линий формула
Длина волны всей спектральной линии = ((Начальная орбита^2)*(Конечная орбита^2))/([R]*(Атомный номер^2)*((Конечная орбита^2)-(Начальная орбита^2)))
λspectral = ((ninitial^2)*(nfinal^2))/([R]*(Z^2)*((nfinal^2)-(ninitial^2)))
Объясните модель Бора.
Модель Бора описывает свойства атомных электронов с помощью набора допустимых (возможных) значений. Атомы поглощают или испускают излучение только тогда, когда электроны скачкообразно переходят между разрешенными или стационарными состояниями. Модель Бора может объяснить линейчатый спектр атома водорода. Излучение поглощается, когда электрон переходит с орбиты с более низкой энергией на орбиту с более высокой энергией; тогда как излучение испускается, когда он движется с более высокой орбиты на более низкую.





