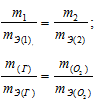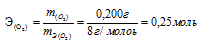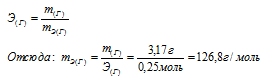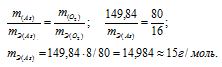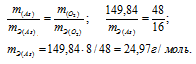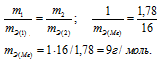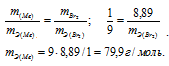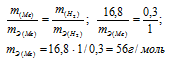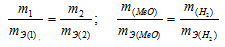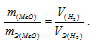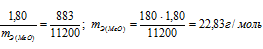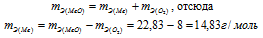для
разных веществ:
7.1.Для
простыходноатомных веществ и
дляодного химического элемента в
сложном веществе:МЭ
= М/п = А/п,
где А –
атомная масса,n– валентность химического элемента.
Например, МЭ(Al)
= 27/3 = 9г /моль (эквивалентов), МЭ(О)
= 16/2 = 8 г/моль;
7.2.Дляпростых
многоатомных (из двух и более атомов)
и сложныхвеществ эквивалентную массу
рассчитывают по общей формулеМЭ
= М/ п.k,
где М –
молярная масса вещества,п –
валентность одного, любого, элемента;
k
– количество атомов этого элемента
в молекуле.
Например, МЭ(О2)
=32/2.2 = 8, г /моль (эквивалентов),
МЭ(N2)
= 28/2.2 = 7, г /моль; МЭ(Al2О3)
= (27.2 + 16.3)/3.2 = (54 + 48)/6 = 102/6 = 17, г/моль.
7.3.Эквивалентная массасложного вещества
равна сумме эквивалентных масс образующих
его химических элементов.
Например, МЭ(Al2О3)
= М(Al)/п(Al) +
М(О)/п(О)= 27/3 + 16/2 = 17
г/моль. При этом fЭ(Al2О3)=
МЭ(Al2О3)/М(Al2О3)=
17 г/моль/102 г/моль = 1/6, Э(Al2О3)=
1/6 моль, число эквивалентов пЭ(Al2О3)
= 6 (6Э в 1 моле вещества
Al2О3).
7.4.Для
вычисления эквивалентных масссложных
веществ разных классовможно
использовать следующие формулы (при
условииполногозамещения
соответствующих функциональных групп
или атомов, ионов, количество которых
указано в формуле
индексом; в противном случае, в
реакцияхнеполногозамещения,
следует учитывать количествопрореагировавшихгрупп, атомов,
ионов):
7.4.1. Эквивалентная масса оксида:
МЭ(окс)
= М(окс)/k
. п =М(окс.)/пЭ
= М(окс). fЭ,
где М(окс) –
молярная масса оксида,k
– количество атомов какого-либо
одного элемента в составе молекулы
оксида,n –
валентность этого элемента;пЭ— число эквивалентов,пЭ
= k . п
эквивалентов Э иfЭ
— фактор эквивалентности оксида,fЭ
= 1/ пЭ.
Например, МЭ(Мп2О7)
= (55.2 + 16.7)/7.2 = 222/14 = 15,8 г/моль (эквивалентов).
7.4.2. Эквивалентная масса основания:
МЭ(осн)=М(осн)/k(ОН)
= М(осн)/пЭ ,
где М(осн.)
– молярная масса,k(ОН)
– кислотность основания, т.е. количество
гидроксидных групп ОН—в молекуле
основания, равное числу эквивалентовпЭ в случаеполного замещения групп ОН—;
принеполном замещении, например,
при недостатке кислоты, пЭ
равно числупрореагировавшихОН—-групп.
Например, МЭ
(Са(ОН)2) = 74/2 = 37
г/моль – в случае полного замещения
обеих
групп ОН—, как в химической
реакции: Са(ОН)2 + 2HCl
= СаCl2 +
2Н2О.
При замещении одной
ОН—–группы МЭ(Са(ОН)2)
= 74/1 = 74 г/моль–
как, например, в
реакции: Са(ОН)2 + HCl
= СаОНCl + Н2О.
7.4.3. Эквивалентная масса кислоты:
МЭ(кисл)
= М(кисл)/
k(Н)=
М(кисл)/пЭ ,
где М(кисл)
– молярная масса,k(Н)– основность кислоты, т.е. количество
атомовНв молекуле кислоты, равное
числу эквивалентов
пЭкислотыпри полном замещении атомов водорода;
в случае ихчастичного замещения– например,при избытке кислоты–пЭ равно числупрореагировавших атомов
Н).
Например, МЭ(Н2SO4)
= 98/2 = 49г /моль,пЭ=
2Э (эквивалентам) – приполном замещениидвухатомов водорода:2NaCl
+ H2SO4
= Na2SO4
+ 2HCl.
При недостатке соли
(избытке кислоты) возможна реакция
замещения только одного атома
водорода:NaCl + H2SO4
= NaНSO4
+ HCl,
и тогда МЭ(Н2SO4)
= 98/1 = 98г /моль,Э(Н2SO4)
=1 моль,пЭ =
1Э.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Как рассчитать эквивалентную массу
Эквивалентной массой, или молярной массой эквивалента, называется количество вещества, взаимодействующее с одним молем водорода или вытесняющие столько же атомов водорода из его соединений. Обозначается эта величина Mэкв, измеряется в г/моль и вычисляется по формулам или экспериментальным путем.

Вам понадобится
- — периодическая система;
- — калькулятор;
- — химическая посуда;
- — разбавленная соляная кислота;
- — навеска металла.
Инструкция
Чтобы найти эквивалентную массу простого вещества, воспользуйтесь формулой:Mэкв = Mа/B, где Mэкв – масса эквивалента;Mа – атомная масса элемента; B – валентность.Например, согласно формуле эквивалентная масса натрия будет равна 22,99 г/моль, а двухвалентной серы – 32/2 = 16 г/моль и т.д. Для сложных веществ молярной массой эквивалента будет называться количество вещества, прореагировавшего без остатка с одним эквивалентом другого вещества, например, водорода.
Помните, что расчет этой величины для разных химических соединений имеет нюансы. Например, при вычислении эквивалентной массы оксидов – складывайте значения эквивалентных масс, составляющих соединение. Допустим, дан оксид цинка. Сначала считаете Mэкв (Zn) = 65/2 =32,5 г/моль. Потом — Mэкв (O) = 16/2 = 8 г/моль. Таким образом, получите эквивалентную массу ZnO равную 40,5 г/моль. А рассчитать массу эквивалента кислоты можно, разделив ее молекулярную массу на количество атомов водорода, содержащихся в ней: Mэкв (H2SO4) = 98/2 = 49 г/моль и т.д.
Для экспериментального определения эквивалентной массы сначала повторите технику безопасности при работе с кислотами и газами. Затем возьмите бюретку, пробирку и воронку. Соедините их между собой резиновыми трубками. Налейте в бюретку дистиллированной воды, с помощью воронки установите ее уровень на нуле.
В пробирку налейте 5 мл соляной кислоты (постарайтесь не замочить стенки). На сухую стенку поместите навеску металла. Следите за тем, чтобы он не упал в кислоту раньше времени. Закройте пробирку пробкой и встряхните. Водород будет вытеснять воду из бюретки. После завершения реакции выровняйте уровень воды в бюретке и воронке. Запишите конечный результат, температуру и давление при проведении опыта.
Определите вытесненный объем водорода, сравнив начальный и конечный уровень воды в бюретке. Приведите полученный результат к нормальным условиям, используя показания барометра и термометра. И затем только рассчитайте массу эквивалента металла, используя формулу:m (металла)/V (водорода при норм.условиях) = Mэкв.(металла)/Vэкв (водорода).
Источники:
- рассчитать молярную массу эквивалента
- ЭКВИВАЛЕНТНАЯ МАССА
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Определить эквивалентную массу
Вычислить фактор эквивалентности и определить эквивалентную массу ортофосфорной кислоты (H3PO4) в реакциях образования гидрофосфата, дигидрофосфата и ортофосфата.
Решение задачи
Напомню, фактор эквивалентности (fэкв) (эквивалент) – число, показывающее какая доля частицы (атома, молекулы) этого вещества равноценна одному иону водорода (H+) в реакциях обмена или одному электрону в окислительно-восстановительных реакциях.
Молярная масса эквивалента – это масса одного моль эквивалента вещества, равная произведению фактора эквивалентности на молярную массу вещества.
Фактор эквивалентности и эквивалентная масса вещества определяются той реакцией в которой данное вещество принимает участие, так как у одного и того же вещества в различных реакциях различны фактор эквивалентности и эквивалентная масса.
Запишем уравнения реакций образования:
А. гидрофосфата
Так как в одной молекуле ортофосфорной кислоты (H3PO4) замещается 2 атома водорода (H), следовательно, фактор эквивалентности (fэкв) ортофосфорной кислоты (H3PO4) равен 1/2:
f экв. (H3PO4) = 1/2
Учитывая, что молярная масса ортофосфорной кислоты (H3PO4) равна 98 г/моль (смотри таблицу Менделеева), определим эквивалентную массу ортофосфорной кислоты (H3PO4):
Б. дигидрофосфата
Так как в одной молекуле ортофосфорной кислоты (H3PO4) замещается 1 атом водорода (H), следовательно, фактор эквивалентности (fэкв) ортофосфорной кислоты (H3PO4) равен 1:
f экв. (H3PO4) = 1
Учитывая, что молярная масса ортофосфорной кислоты (H3PO4) равна 98 г/моль (смотри таблицу Менделеева), определим эквивалентную массу ортофосфорной кислоты (H3PO4):
В. ортофосфата
Так как в одной молекуле ортофосфорной кислоты (H3PO4) замещается 3 атома водорода (H), следовательно фактор эквивалентности (fэкв) ортофосфорной кислоты (H3PO4) равен 1/3:
f экв. (H3PO4) = 1/3
Учитывая, что молярная масса ортофосфорной кислоты (H3PO4) равна 98 г/моль (смотри таблицу Менделеева), определим эквивалентную массу ортофосфорной кислоты (H3PO4):
Ответ:
фактор эквивалентности ортофосфорной кислоты в реакции образования гидрофосфата равен 1/2, молярная масса эквивалента равна 49 г/моль;
фактор эквивалентности ортофосфорной кислоты в реакции образования дигидрофосфата равен 1, молярная масса эквивалента равна 98 г/моль;
фактор эквивалентности ортофосфорной кислоты в реакции образования ортофосфата равен 1/3, молярная масса эквивалента равна 32,667 г/моль.
Эквивалент. Закон зквивалентов. Определение эквивалентной массы вещества
Определение эквивалентной массы вещества
Задача №1
При сгорании 5,00г металла образуется 9,44г оксида металла. Определить эквивалентную массу металла.
Решение:
Из условия задачи следует, что в оксиде металла на 5г металла приходится 4,44г кислорода (9,44 – 5 = 4,44). Согласно закону эквивалентов, массы (объёмы) взаимодействующих веществ пропорциональны их эквивалентным массам. Учитывая, что эквивалентная масса кислорода равна 8 г/моль, составляем пропорцию:
5г металла эквивалентны 4,44г кислорода
mЭ(Ме) г/моль металла эквивалентны 8г/моль кислорода
Откуда mЭ(Ме) = 8 . 5/4,44 = 9,01г/моль.
Ответ: mЭ(Ме) = 9,01г/моль.
Задача №2
Одно и то же количество металла соединяется с 0,200г кислорода и с 3,17г одного из галогенов. Определить эквивалентную массу галогена.
Решение:
I Вариант
Из условия задачи следует, что 0,200г кислорода и 3,17г галогена эквивалентно соединяются с металлом. Согласно закону эквивалентов, массы взаимодействующих веществ пропорциональны их эквивалентным массам. Учитывая, что эквивалентная масса кислорода равна 8 г/моль, составляем пропорцию:
0,200г кислорода эквивалентны 3,17г галогена
mЭ(О2) 8г/моль кислорода эквивалентны mЭ(Г) Х г/моль
Откуда: mЭ(Г) 8 . 3,17/0,200 = 126,8г/моль.
Ответ: mЭ(Г) = 126,8г/моль.
II Вариант
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
Таким образом, количество эквивалентов галогена и кислорода численно равны между собой, что составляет:
Зная количество эквивалентов и массу вещества можно определить эквивалентную массу этого вещества:
Ответ: 126,г/моль.
Задача №3
Масса 1л кислорода равна 1,4г. Сколько литров кислорода расходуется при сгорании 21г магния, эквивалент которого равен 1/2 моля?
Решение:
Находим эквивалентную массу магния: mЭ(Mg) = 1/2M(Mg) =24/2 = 12г/моль. Следовательно, 21г магния составляет 21/2 =1,75 эквивалентной массы Mg. Согласно закону эквивалентов масса израсходованного кислорода составляет 1,75 его эквивалентной массы. Учитывая, что эквивалентная масса кислорода равна 8 г/моль, рассчитаем массу кислорода, расходуемую на сжигание магния: m(O2) = 1,75 . 8 = 14г. Зная, что 1л кислорода по массе составляет 1,4г, рассчитаем объём кислорода расходуемого при сгорании 21г магния, составив пропорцию:
1,4 : 1 = 14 : х;
х = 14 . 1/1,4 = 10л.
Ответ: V(O2) = 10л.
Задача№4
Определить эквивалентные массы металла и серы, если 3,24г металла образует 3,48г оксида и 3,72г сульфида.
Решение:
Из условия задачи следует, что в оксиде металла на 3,24г металла приходится 0,24г кислорода (3,48 – 3,24 = 0,24г). Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам). Так как эквивалентная масса кислорода составляет 8г/моль, то эквивалентную массу металла находим из пропорции:
8 : 0,24 = х : 3,24;
х = 8 . 3,24/0,24 =108г/моль.
В сульфиде металла на 3,24г металла приходится 0,48г серы (3,72 – 3,24 = 0,48г). Эквивалентную массу серы находим из пропорции:
3,24 : 108 = 0,48 : х;
х = 108 . 3,24/0,48 = 16г/моль.
Ответ: mэ(Me) = 108г/моль; mэ(S) = 16г/моль.
Задача№5
Вычислить атомную массу двухвалентного металла и определить, какой это металл, если 8,34г металла окисляются 0,680л кислорода (условия нормальные).
Решение:
Зная, что эквивалентный объём кислорода равен 5,6л/моль, рассчитаем эквивалентную массу металла, составив пропорцию:
8,345 : 0,680 = х : 5,6;
х = 8,34 . 5,6/0,680 = 68,68г/моль.
Атомную массу металла находим, учитывая, что металл двухвалентный, умножением его эквивалентной массы на 2:
М(Ме) = mэ(Ме) . В, где
В – валентность металла; М – молярная масса металла; mэ(Ме) – эквивалентная масса металла.
М(Ме) = 68,68 . 2 = 137,4г/моль.
Определяем, какой это металл по таблице «Периодическая система химических элементов Д.И. Менделеева», учитывая, что его атомная масса составляет 137,4. Такой атомной массе соответствует барий – элемент№56.
Ответ: 137,4; Ba.
Задача№6
Мышьяк образует два оксида, из которых один содержит 65,2% (масс.) As, а другой 75,7% (масс.) As. Определить эквивалентные массы мышьяка в обоих оксидах.
Решение:
а) Находим формулу оксида мышьяка, учитывая, что оксид содержит 65,2% As по массе. Тогда оксид содержит кислорода по массе 34,8% (100 – 65,2 = 34,8). Находим формулу оксид мышьяка:
AsхОу = х : у = 65,2/Ar(As) : 34,8/Ar(O2) = 65,2/74,92 : 34,8/16 = 1 : 2,5 = 2 : 5
Формула оксида будет иметь вид: As2O5.
M(As2O5) = 229,84г/моль.
Находим массу мышьяка и массу кислорода в оксиде:
m(As) = 74,92 . 2 = 149,84г; m(O2) = 16 . 5 = 80г.
Согласно закону эквивалентов массы элементов в оксиде пропорциональны их эквивалентным массам:
б) Подобные расчеты производим, учитывая, что оксид содержит 75,7% As и 24,3% О2 (100 – 75,7 = 24,3) по массе:
AsхОу = х : у = 75,7/74,92 : 24,3/16 = 1,01 : 1,51 = 1 : 1,5 2 : 3
Формула оксида будет иметь вид: As2O3.
M(As2O5) = 197,84г/моль.
m(As) = 74,92 . 2 = 149,84г; m(O2) = 16 . 3 = 48г.
Ответ: а) 15г/моль; 24,97г/моль.
Задача№7
,00г некоторого металла соединяется с 8,89г брома и с 1,78г серы. Найти эквивалентные массы брома и металла, зная, что эквивалентная масса серы равна 16,0 г/моль.
Решение:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их а (объёмам):
Находим эквивалентную массу брома, учитывая, что эквивалентная масса металла равна 9г/моль:
Ответ: 9г/моль; 79,9г/моль.
Задача№8
Эквивалентная масса хлора равна 35,5 г/моль, мольная масса атомов меди равна 63,5 г/моль. Эквивалентная масса хлорида меди равна 99,5 г/моль. Какова формула хлорида меди?
Решение:
Согласно закону эквивалентов:
mэ(соли) = mэ(Cu) + mэ(Cl2).
Отсюда mэ(Cl2) = mэ(соли) — mэ(Cl2) = 99,5 – 35,5 = 64г/моль.
Зная эквивалентные массы хлора и меди можно определить количество их атомов в молекуле соли: mэ(А) = М(А)/mэ(А).
Тогда: CuxCly = x : y = 63,5/63,546 : 35,45/35,5 = 0,992 : 0,999 = 1 : 1
Отсюда CuxCly = CuCl.
Ответ: CuCl.
Задача№9.
Для растворения 16,8г металла потребовалось 14,7г серной кислоты. Определить эквивалентную массу металла и объем выделившегося водорода (условия нормальные).
Решение:
M(H2SO4) =98г/моль.
Находим массу водорода в 14,7г серной кислоты, составив пропорцию: 98 : 2 14,7 : х;
х = 2 . 14,7/98 = 0,3г.
Согласно закону эквивалентов массы взаимодействующих веществ пропорциональны их эквивалентным массам:
Учитывая, что эквивалентный объём водорода равен 11,2л/моль, рассчитаем объём который занимает 0,3г водорода: из пропорции:
1 : 11,2 = 0,3 : х;
х = 11,2 . 0,3/ 1 = 3,36л.
Ответ: mэ(Ме) = 56г/моль; V(H2) = 3,36л.
Задача№10
На восстановление 1,80г оксида металла израсходовано 883 мл водорода, измеренного при нормальных условиях. Вычислить эквивалентные массы оксида и металла.
Решение:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
Так как водород находится в газообразном состоянии, то, соответственно, его количество измеряется в объёмных единицах (мл, л, м3). Мольный объём любого газа при н.у. равен 4л. Отсюда эквивалентный объём водорода равен, молекула которого состоит из двух атомов, т. е. содержит два моля атомов водорода, равен 22,4/2 = 11,2 л/моль или 12000мл/моль.
Отношение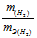
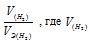
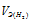
Тогда получим отношение
Находим эквивалентную массу оксида металла:
Согласно закону эквивалентов:
Ответ: 22,83г/моль; 14,83г/моль.
ЭКВИВАЛЕНТНАЯ МАССА (химический эквивалент). Эквивалентная масса элемента — это масса 1 эквивалента элемента; эквивалентом элемента называют такое его количество, которое реагирует с 1 моль атомов водорода или замещает то же количество атомов водорода в химических реакциях. При образовании соединений элементы взаимодействуют друг с другом в количествах, пропорциональных их эквивалентным массам или величинам, кратным этим массам. Для численного выражения эквивалентных масс необходим эталон; в качестве такого эталона приняты атомная масса водорода или ее эквивалент, например атомная масса хлора (Cl–), 1/2 атомной массы кислорода (O2–) или 1/3 атомной массы алюминия (Al3+). Таким образом, эквивалентная масса элемента равна его атомной массе, деленной на его валентность или степень окисления. В настоящее время атомные массы указывают в единицах, отнесенных к массе изотопа углерода с массовым числом 12; этому изотопу приписана масса 12,0000. Тогда атомная масса водорода будет равна 1,00797, хлора – 35,453, кислорода – 15,9994, алюминия – 26,9815. Следовательно, эквивалентная масса элемента – это масса, которая может химически соединяться или замещать в химическом соединении 1,00797 ч. (ч. – часть) водорода, 35,453 ч. хлора, 7,9997 (15,9994:2) ч. кислорода, 8,9938 (26,9815:3) ч. алюминия либо их эквиваленты. При таком определении эквивалентную массу можно найти экспериментально.
Методы определения.
Первые опыты по определению эквивалентных масс провели Дж.Дальтон, Й.Берцелиус, Ж.Дюма, Ж.Стас и другие ученые, но основная заслуга принадлежит здесь Т.Ричардсу, который впервые выполнил тщательные измерения эквивалентных масс с высочайшей точностью. Нагревая чистый перхлорат калия KClO3, превращали его в хлорид калия (KCl), при этом из 100 масс. ч. KClO3 образовывалось 60,835 масс. ч. KCl и 39,165 масс. ч. кислорода. Поскольку одна молекула KClO3 содержит на 3 атома кислорода, т.е. на 47,998 масс. ч., больше, чем KCl, то эквивалентная масса хлорида равна 47,998Ч(60,835:39,165) = 74,555. Далее, известное количество чистого серебра превращали в нитрат серебра, который использовали для осаждения хлорида серебра из раствора при взаимодействии с чистым хлоридом калия. Было установлено, что для полного превращения 74,555 масс. ч., т.е. массового эквивалента хлорида калия KCl, в хлорид серебра, который содержит 35,453 масс. ч. хлора, требуется 107,87 масс. ч. серебра. Эквивалентная масса калия при этом равна 74,555 – 35,453 = 39,102. Аналогично, зная эквивалентную массу серебра и изучая реакции образования им соответствующих галогенидов, например бромида AgBr, можно рассчитать эквивалентную массу галогена (в частности, брома). С использованием эквивалентных масс хлора и брома были определены эквивалентные массы многих металлов. Для нахождения эквивалентной массы какого-либо металла (М) синтезируют его чистый хлорид или бромид MBrx и осаждают галоген в виде галогенида серебра. Зная массы использованного MBrx и полученного AgBr, эквивалентные массы серебра (107,87) и брома (79,999), несложно определить эквивалентную массу металла М, который соединяется с 79,999 масс. ч. брома.
Описанный метод используется для точных расчетов, а для приближенных оценок можно применять другие способы, основанные на измерении объема и расчете массы водорода, выделившегося при растворении металла в кислоте, на определении массы одного металла, вытесняемого известным количеством другого из раствора, на определении состава гидридов или оксидов непосредственно по реакции соединения или аналитическими методами. Эквивалентные массы позволяют не только устанавливать соотношения, в которых элементы соединяются или замещают друг друга, но и точно определять атомные массы.
Кратные эквивалентные массы.
Иногда два элемента соединяются друг с другом в разных соотношениях, образуя два (или более) разных соединения. Например, известны два оксида меди. В одном из них, оксиде меди(II), 31,8 ч. меди соединены с эквивалентной массой, т.е. с 7,9997 масс. ч., кислорода, тогда как в оксиде меди(I) эта же эквивалентная масса кислорода соединена с 63,6 масс. ч. меди. Соответственно эквивалентные массы меди равны 31,8 и 63,6, при этом последняя величина ровно в два раза больше первой, а значит, эквивалентные массы являются кратными величинами. Этот вывод согласуется с ранее высказанным утверждением, что элементы соединяются пропорционально их эквивалентным массам или величинам, кратным этим массам.
Электрохимический эквивалент.
При прохождении через электролит количества электричества 1 F (фарадей) = 96 500 Кл (1 Кл = 1 АЧс) выделяется один химический эквивалент (т.е. эквивалентная масса) любого вещества. Следовательно, масса, выделяемая при прохождении 1 Кл (кулон), равна 1 экв., деленному на 96 500. Эта величина, называемая электрохимическим эквивалентом данного элемента, лежит в основе еще одного метода экспериментального определения эквивалентных масс.
Эквивалентные массы соединений.
Понятие эквивалентной массы было распространено и на соединения; в этом случае эквивалентная масса определяется как масса вещества, кратная эквивалентной массе элемента, являющегося ключевым для данного соединения. Например, для кислот ключевым элементом является водород, образующий в растворе ионы водорода; таким образом, эквивалентная масса кислоты есть масса кислоты, кратная 1,00797 массовым частям водорода, способного образовывать ионы водорода, т.е. водорода, который может быть замещен. Другими словами, эквивалентная масса кислоты равна ее молярной массе, деленной на основность кислоты. Эквивалентная масса основания есть масса основания, которая реагирует с эквивалентной массой любой кислоты и, следовательно, является химическим эквивалентом этой массы. Иначе можно сказать, что эквивалентная масса основания равна его молярной массе, деленной на валентность металла, образующего основание. Для солей эквивалентная масса обычно кратна эквивалентной массе металла, образовавшего эту соль; она равна молярной массе соли, деленной на произведение валентности металла и числа его атомов в молекуле соли. Для эквивалентной массы окислителей и восстановителей можно дать несколько определений. С практической точки зрения наиболее удобно определение, согласно которому эквивалентная масса есть количество вещества, кратное 7,9997 ч. кислорода (или реагирующее с ними) либо его эквиваленту. Другое определение основано на том, что при восстановлении этого количества кислорода происходит перенос одного электрона. В этом случае эквивалентная масса окислителя или восстановителя есть масса, соответствующая массе вещества, принимающего или отдающего один электрон в окислительно-восстановительной реакции.