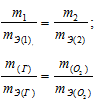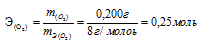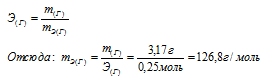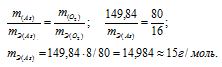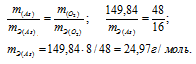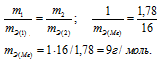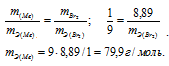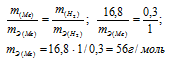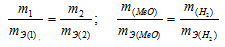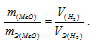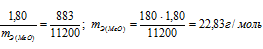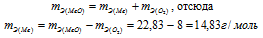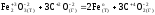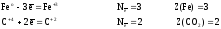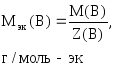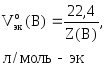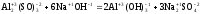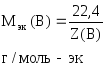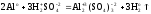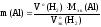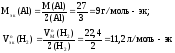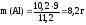Как найти эквивалентную массу
Химические элементы соединяются друг с другом в строго определенных количественных соотношениях. Именно поэтому появились такие понятия, какэквивалент и эквивалентная масса. («Эквивалент» в дословном переводе означает «равный», «равноценный»). Что такое эквивалент в химическом смысле этого слова? Как вычислить эквивалент и (или) эквивалентную массу?
Эквиваленты и эквивалентные массы обычно определяются либо по данным анализа соединений, либо на основании результатов замещения одного элемента другим. Нетрудно понять, что для определения эквивалента (или эквивалентной массы) элемента вовсе необязательно исходить из его соединения с водородом. Эквивалент (эквивалентную массу) можно точно так же вычислить по составу соединения данного элемента с любым другим, эквивалент (эквивалентная масса) которого известен.
Пример. При соединении 1,50 грамма натрия с избытком хлора образовалось 3,81 грамма хлорида натрия. Необходимо найти эквивалентную массу натрия и его эквивалент, если известно, что эквивалентная масса хлора равна 35,45 грамм/моль.Решение. Вычитайте из общей массы образовавшегося продукта исходную массу натрия.
Таким образом, 3, 81 – 1, 50 = 2, 31
То есть, в образовавшемся продукте (в вашем случае хлорид натрия) на 1,50 грамма натрия приходится 2,31 грамма хлора. Из этого следует, что зная эквивалентную массу хлора (35, 45 грамм/моль), вы легко найдете эквивалентную массу натрия по следующей формуле:
35, 45 х 1, 50 / 2, 31 Эквивалентная масса натрия получается равной 23,0 грамм/моль.
Молярная масса натрия также будет равна 23,0 грамм/моль. Из этого следует, что эквивалент натрия равен одному молю (поскольку молярная и эквивалентная массы натрия совпадают).
Понятие об эквивалентах и эквивалентных массах распространяется также и на сложные вещества. Эквивалентом сложного вещества называется такое его количество, которое взаимодействует без остатка с одним эквивалентом водорода.
Как рассчитать эквивалентную массу
Эквивалентной массой, или молярной массой эквивалента, называется количество вещества, взаимодействующее с одним молем водорода или вытесняющие столько же атомов водорода из его соединений. Обозначается эта величина Mэкв, измеряется в г/моль и вычисляется по формулам или экспериментальным путем.

Вам понадобится
- — периодическая система;
- — калькулятор;
- — химическая посуда;
- — разбавленная соляная кислота;
- — навеска металла.
Инструкция
Чтобы найти эквивалентную массу простого вещества, воспользуйтесь формулой:Mэкв = Mа/B, где Mэкв – масса эквивалента;Mа – атомная масса элемента; B – валентность.Например, согласно формуле эквивалентная масса натрия будет равна 22,99 г/моль, а двухвалентной серы – 32/2 = 16 г/моль и т.д. Для сложных веществ молярной массой эквивалента будет называться количество вещества, прореагировавшего без остатка с одним эквивалентом другого вещества, например, водорода.
Помните, что расчет этой величины для разных химических соединений имеет нюансы. Например, при вычислении эквивалентной массы оксидов – складывайте значения эквивалентных масс, составляющих соединение. Допустим, дан оксид цинка. Сначала считаете Mэкв (Zn) = 65/2 =32,5 г/моль. Потом — Mэкв (O) = 16/2 = 8 г/моль. Таким образом, получите эквивалентную массу ZnO равную 40,5 г/моль. А рассчитать массу эквивалента кислоты можно, разделив ее молекулярную массу на количество атомов водорода, содержащихся в ней: Mэкв (H2SO4) = 98/2 = 49 г/моль и т.д.
Для экспериментального определения эквивалентной массы сначала повторите технику безопасности при работе с кислотами и газами. Затем возьмите бюретку, пробирку и воронку. Соедините их между собой резиновыми трубками. Налейте в бюретку дистиллированной воды, с помощью воронки установите ее уровень на нуле.
В пробирку налейте 5 мл соляной кислоты (постарайтесь не замочить стенки). На сухую стенку поместите навеску металла. Следите за тем, чтобы он не упал в кислоту раньше времени. Закройте пробирку пробкой и встряхните. Водород будет вытеснять воду из бюретки. После завершения реакции выровняйте уровень воды в бюретке и воронке. Запишите конечный результат, температуру и давление при проведении опыта.
Определите вытесненный объем водорода, сравнив начальный и конечный уровень воды в бюретке. Приведите полученный результат к нормальным условиям, используя показания барометра и термометра. И затем только рассчитайте массу эквивалента металла, используя формулу:m (металла)/V (водорода при норм.условиях) = Mэкв.(металла)/Vэкв (водорода).
Источники:
- рассчитать молярную массу эквивалента
- ЭКВИВАЛЕНТНАЯ МАССА
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
The most commonly used phrase in chemistry is “equivalent weight,” which is also one of the fundamental concepts in physical chemistry. Equivalent weight commonly referred to as a gram equivalent is the mass of one equivalent or the mass of a particular material that will combine with or replace a specific amount of another substance. To say it another way, the mass of a substance that can displace 1.008 grams of hydrogen or 8.0 grams of oxygen or 35.5 grams of chlorine is its gram equivalent or equivalent weight. Let us study the Equivalent Weight in detail in this article.
What is Equivalent Weight?
Equivalent weight is defined as the ratio of the molecular weight of the solute to the valency of the solute. The equivalent weight of the substance varies according to the reaction it undergoes. The normality of the solution is calculated using the equivalent weight of the substance. The general formula to calculate the equivalent weight is,
Equivalent Weight = Molecular Weight / (n-factor)Valency
How to calculate the Equivalent Weight?
The Equivalent Weight of a compound is the result of dividing the molecular weight by the charge number of that compound.
E = Molecular Weight / n-factor (charge number)
where,
E is Equivalent Weight
Charge number indicates how many protons or hydroxide-equivalents the compound has
The equivalent weight of the compound can be defined as the weight (or mass) of a substance that will include a single reactive proton (or hydrogen ion, H+) or a single reactive hydroxide ion (OH–). The idea of equivalent weight is necessary because some compounds are doubly reactive for every mole present because they have the capacity to supply or receive more than one proton.
Hydrogen has an atomic mass of one (1.008 to be precise). Hydrogen’s valency is always 1. As a result, hydrogen has an equal weight of 1. In the majority of reactions, oxygen has a valency of 2.
Moles
A compound is described as having 6.02 × 1023 distinct particles (atoms or molecules) per unit mole. In fact, there are exactly this many atoms in 12 grams of carbon. The mass of one mole of each element, or its molecular weight (MW), is given in the corresponding box for that element on the periodic table.
Equivalent Weight of Acids and Bases
The equivalent mass of an acid or base in an acid-base reaction is always equal to the mass that contributes to or interacts with one mole of the hydrogen ion (H+). In a similar manner, the mass that supplies or reacts with one gram mole of electrons (e-) produced in the redox reaction is the substance’s equivalent weight.
Knowing an acid’s molecular weight and the charge present in it helps to calculate its equivalent weight.
For example, take sulfuric acid,
H2SO4 + 2OH− → 2H2O + SO42−
Using a periodic table to get each element’s MW and adding it we get 2(1) + (32) + 4(16) = 98.0, and we can determine the acid’s Molecular Weight.
Because the sulfate ion is left with a charge of 2, we get to know that this acid can give two protons.
Hence, the equivalent weight = 98.0/2 = 49.0
Logic is the same for a base. A proton can be taken up by ammonium hydroxide in solution to form an ammonium ion:
NH4OH + H+ = H2O + NH4+
Ammonium hydroxide’s Molecular Weight is calculated as (14) + (4)(1) + (16) + 1 = 35.0
The equivalent Weight for this molecule is 35.0/1 = 35.0 since just one proton is consumed.
How to Calculate Gram-Equivalent Weight?
The number of grams of a substance divided by its equivalent weight is known as a gram equivalent. It can also be written as n moles times the number of charge elements present.
Gram equivalent weight is the equivalent weight given in mass units. The calculated equivalent weight and the gram equivalent weight are equal numerically.
Eq = MW / n
where,
Eq is Equivalent weight
MW is Molecular Weight in grams/mole
n is number of equivalents charge
Also, Read
- Normality
- Molarity
- Difference Between Molarity and Molality
Solved Problems on Equivalent Weight
Question 1: Calculate the Equivalent weight of H2SO4.
Answer:
Two H+ ions are present for every mole of sulfuric acid, or n = 2. Find the total atomic masses of the S, O, and H in your formula by referencing a periodic table:
S = 32.07
O = 16.00
H = 1.01
Add the molecular weight of H2SO4:
32.07 + 4(16.00) + 2(1.01) = 98.08 g/mol
Eq = 98.08 / 2 = 49.04 g/eq.
H2SO4 has a gram equivalent weight of 49.04 g/eq.
Question 2: Calculate the Equivalent weight of NaOH.
Answer:
Since there is just one OH-, there are only one equivalent. Find the total atomic masses of the Na, O, and H in your formula by referencing to periodic table:
Na = 22.99
O = 16.00
H = 1.01
Add the molecular weight of NaOH:
22.99 + 16.00 + 1.01 = 40.00 g/mole
Eq = 40.00 / 1 = 40.00 g/eq
NaOH has a gram equivalent weight of 40.00 g/eq
Question 3: Calculate the Equivalent weight of HCL.
Answer:
Since there is just one H+, there are only one equivalent. Find the total atomic masses of Cl and H in your formula by referencing to periodic table:
Cl = 35.45
H = 1.01
Add the molecular weight of HCL:
35.45 + 1.01 = 36.46 g/mole
Eq = 36.46 / 1 = 36.46 g/eq
HCL has a gram equivalent weight of 36.46 g/eq
Question 4: Calculate the Equivalent weight of Ca(OH)2 →Ca+ + 2 OH–
Answer:
The calcium hydroxide base releases two hydroxyl ions into the environment. Its valency factor, or X value, will therefore be 2.
The calcium hydroxide base has a molecular weight of 74 g/mole.
Equivalent weight = molecular weight / valency
Equivalent weight of calcium hydroxide base= 74 / 2 = 37 g/eq
Therefore, calcium hydroxide has a equivalent weight of 37 g/eq
Question 5: Calculate the Equivalent weight of Al(OH)3 → Al+3 + 3 OH–
Answer:
The aluminum hydroxide base releases three hydroxyl ions. Its valency factor, or X value, will therefore 3.
The aluminum hydroxide base has a molecular weight of 78 g/mol.
Equivalent weight = molecular weight / valency
Equivalent weight of aluminum hydroxide base= 78 / 3 = 26 g/eq.
Therefore, aluminum hydroxide has a equivalent weight of 26 g/eq
FAQs on Equivalent Weight
Question 1: How do you calculate the equivalent weight of acid and base?
Answer:
Divide the molar mass of the base by the quantity of hydroxyl groups to determine the equivalent mass of the base. Divide the molar mass of an acid by the number of protons to determine its equivalent weight.
Question 2: What is the equivalent concentration, and how to calculate it?
Answer:
EW stands for equivalent weight in grams per equivalent. It is computed by dividing the solute’s molecular weight by its equivalents per mole. The amount of H+ ions that an acid contributes to a mole of acid determines how many equivalents are there for acids.
Question 3: What does “equivalent concentration” mean?
Answer:
The molar concentration of a solution (ci), is divided by an equivalency factor (f), to determine its equivalent concentration, or normalcy. Normality = cif
Question 4: What are the factors on which the equivalent weight of any compound depends?
Answer:
The equivalent weight of any compound depends upon the following two factors,
- Molecular weight
- Valency factor
Эквивалент. Закон зквивалентов. Определение эквивалентной массы вещества
Определение эквивалентной массы вещества
Задача №1
При сгорании 5,00г металла образуется 9,44г оксида металла. Определить эквивалентную массу металла.
Решение:
Из условия задачи следует, что в оксиде металла на 5г металла приходится 4,44г кислорода (9,44 – 5 = 4,44). Согласно закону эквивалентов, массы (объёмы) взаимодействующих веществ пропорциональны их эквивалентным массам. Учитывая, что эквивалентная масса кислорода равна 8 г/моль, составляем пропорцию:
5г металла эквивалентны 4,44г кислорода
mЭ(Ме) г/моль металла эквивалентны 8г/моль кислорода
Откуда mЭ(Ме) = 8 . 5/4,44 = 9,01г/моль.
Ответ: mЭ(Ме) = 9,01г/моль.
Задача №2
Одно и то же количество металла соединяется с 0,200г кислорода и с 3,17г одного из галогенов. Определить эквивалентную массу галогена.
Решение:
I Вариант
Из условия задачи следует, что 0,200г кислорода и 3,17г галогена эквивалентно соединяются с металлом. Согласно закону эквивалентов, массы взаимодействующих веществ пропорциональны их эквивалентным массам. Учитывая, что эквивалентная масса кислорода равна 8 г/моль, составляем пропорцию:
0,200г кислорода эквивалентны 3,17г галогена
mЭ(О2) 8г/моль кислорода эквивалентны mЭ(Г) Х г/моль
Откуда: mЭ(Г) 8 . 3,17/0,200 = 126,8г/моль.
Ответ: mЭ(Г) = 126,8г/моль.
II Вариант
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
Таким образом, количество эквивалентов галогена и кислорода численно равны между собой, что составляет:
Зная количество эквивалентов и массу вещества можно определить эквивалентную массу этого вещества:
Ответ: 126,г/моль.
Задача №3
Масса 1л кислорода равна 1,4г. Сколько литров кислорода расходуется при сгорании 21г магния, эквивалент которого равен 1/2 моля?
Решение:
Находим эквивалентную массу магния: mЭ(Mg) = 1/2M(Mg) =24/2 = 12г/моль. Следовательно, 21г магния составляет 21/2 =1,75 эквивалентной массы Mg. Согласно закону эквивалентов масса израсходованного кислорода составляет 1,75 его эквивалентной массы. Учитывая, что эквивалентная масса кислорода равна 8 г/моль, рассчитаем массу кислорода, расходуемую на сжигание магния: m(O2) = 1,75 . 8 = 14г. Зная, что 1л кислорода по массе составляет 1,4г, рассчитаем объём кислорода расходуемого при сгорании 21г магния, составив пропорцию:
1,4 : 1 = 14 : х;
х = 14 . 1/1,4 = 10л.
Ответ: V(O2) = 10л.
Задача№4
Определить эквивалентные массы металла и серы, если 3,24г металла образует 3,48г оксида и 3,72г сульфида.
Решение:
Из условия задачи следует, что в оксиде металла на 3,24г металла приходится 0,24г кислорода (3,48 – 3,24 = 0,24г). Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам). Так как эквивалентная масса кислорода составляет 8г/моль, то эквивалентную массу металла находим из пропорции:
8 : 0,24 = х : 3,24;
х = 8 . 3,24/0,24 =108г/моль.
В сульфиде металла на 3,24г металла приходится 0,48г серы (3,72 – 3,24 = 0,48г). Эквивалентную массу серы находим из пропорции:
3,24 : 108 = 0,48 : х;
х = 108 . 3,24/0,48 = 16г/моль.
Ответ: mэ(Me) = 108г/моль; mэ(S) = 16г/моль.
Задача№5
Вычислить атомную массу двухвалентного металла и определить, какой это металл, если 8,34г металла окисляются 0,680л кислорода (условия нормальные).
Решение:
Зная, что эквивалентный объём кислорода равен 5,6л/моль, рассчитаем эквивалентную массу металла, составив пропорцию:
8,345 : 0,680 = х : 5,6;
х = 8,34 . 5,6/0,680 = 68,68г/моль.
Атомную массу металла находим, учитывая, что металл двухвалентный, умножением его эквивалентной массы на 2:
М(Ме) = mэ(Ме) . В, где
В – валентность металла; М – молярная масса металла; mэ(Ме) – эквивалентная масса металла.
М(Ме) = 68,68 . 2 = 137,4г/моль.
Определяем, какой это металл по таблице «Периодическая система химических элементов Д.И. Менделеева», учитывая, что его атомная масса составляет 137,4. Такой атомной массе соответствует барий – элемент№56.
Ответ: 137,4; Ba.
Задача№6
Мышьяк образует два оксида, из которых один содержит 65,2% (масс.) As, а другой 75,7% (масс.) As. Определить эквивалентные массы мышьяка в обоих оксидах.
Решение:
а) Находим формулу оксида мышьяка, учитывая, что оксид содержит 65,2% As по массе. Тогда оксид содержит кислорода по массе 34,8% (100 – 65,2 = 34,8). Находим формулу оксид мышьяка:
AsхОу = х : у = 65,2/Ar(As) : 34,8/Ar(O2) = 65,2/74,92 : 34,8/16 = 1 : 2,5 = 2 : 5
Формула оксида будет иметь вид: As2O5.
M(As2O5) = 229,84г/моль.
Находим массу мышьяка и массу кислорода в оксиде:
m(As) = 74,92 . 2 = 149,84г; m(O2) = 16 . 5 = 80г.
Согласно закону эквивалентов массы элементов в оксиде пропорциональны их эквивалентным массам:
б) Подобные расчеты производим, учитывая, что оксид содержит 75,7% As и 24,3% О2 (100 – 75,7 = 24,3) по массе:
AsхОу = х : у = 75,7/74,92 : 24,3/16 = 1,01 : 1,51 = 1 : 1,5 2 : 3
Формула оксида будет иметь вид: As2O3.
M(As2O5) = 197,84г/моль.
m(As) = 74,92 . 2 = 149,84г; m(O2) = 16 . 3 = 48г.
Ответ: а) 15г/моль; 24,97г/моль.
Задача№7
,00г некоторого металла соединяется с 8,89г брома и с 1,78г серы. Найти эквивалентные массы брома и металла, зная, что эквивалентная масса серы равна 16,0 г/моль.
Решение:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их а (объёмам):
Находим эквивалентную массу брома, учитывая, что эквивалентная масса металла равна 9г/моль:
Ответ: 9г/моль; 79,9г/моль.
Задача№8
Эквивалентная масса хлора равна 35,5 г/моль, мольная масса атомов меди равна 63,5 г/моль. Эквивалентная масса хлорида меди равна 99,5 г/моль. Какова формула хлорида меди?
Решение:
Согласно закону эквивалентов:
mэ(соли) = mэ(Cu) + mэ(Cl2).
Отсюда mэ(Cl2) = mэ(соли) — mэ(Cl2) = 99,5 – 35,5 = 64г/моль.
Зная эквивалентные массы хлора и меди можно определить количество их атомов в молекуле соли: mэ(А) = М(А)/mэ(А).
Тогда: CuxCly = x : y = 63,5/63,546 : 35,45/35,5 = 0,992 : 0,999 = 1 : 1
Отсюда CuxCly = CuCl.
Ответ: CuCl.
Задача№9.
Для растворения 16,8г металла потребовалось 14,7г серной кислоты. Определить эквивалентную массу металла и объем выделившегося водорода (условия нормальные).
Решение:
M(H2SO4) =98г/моль.
Находим массу водорода в 14,7г серной кислоты, составив пропорцию: 98 : 2 14,7 : х;
х = 2 . 14,7/98 = 0,3г.
Согласно закону эквивалентов массы взаимодействующих веществ пропорциональны их эквивалентным массам:
Учитывая, что эквивалентный объём водорода равен 11,2л/моль, рассчитаем объём который занимает 0,3г водорода: из пропорции:
1 : 11,2 = 0,3 : х;
х = 11,2 . 0,3/ 1 = 3,36л.
Ответ: mэ(Ме) = 56г/моль; V(H2) = 3,36л.
Задача№10
На восстановление 1,80г оксида металла израсходовано 883 мл водорода, измеренного при нормальных условиях. Вычислить эквивалентные массы оксида и металла.
Решение:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
Так как водород находится в газообразном состоянии, то, соответственно, его количество измеряется в объёмных единицах (мл, л, м3). Мольный объём любого газа при н.у. равен 4л. Отсюда эквивалентный объём водорода равен, молекула которого состоит из двух атомов, т. е. содержит два моля атомов водорода, равен 22,4/2 = 11,2 л/моль или 12000мл/моль.
Отношение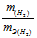
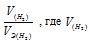
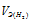
Тогда получим отношение
Находим эквивалентную массу оксида металла:
Согласно закону эквивалентов:
Ответ: 22,83г/моль; 14,83г/моль.
Обозначение
nэк(В),
единицы измерения моль-эк.
Если известна масса вещества и молярная
масса эквивалентов, то количество
вещества эквивалентов рассчитывают по
формуле:
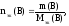
где
m(В)
– масса вещества, г;
Мэк(В)
– молярная масса эквивалентов вещества,
г/моль-эк.
Для
газообразных веществ можно рассчитать
nэк(В),
зная объем газа, который он имеет при
н.у.:
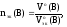
где
Vo(В)
– объем газа при н.у., л;
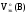
объем эквивалентов газа при н.у., л/моль-эк
Между
количеством вещества эквивалентов
nэк(В)
и количеством вещества n(В)
существует простая зависимость :
nэк(В)
= n(В)
· Z(В)
(23)
Пример.
Рассчитать Z(В),
Мэк(В) всех веществ, принимающих участие
в реакциях а) и б), а так же
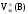
а)
Fe2O3
(т)
+ 3CO(г)
= 2Fe(т)
+ 3CO2(г)
б)
Al2(SO4)3
+ 6NaOH = 2Al(OH)3
+ 3Na2SO4
Решение.
Прежде всего необходимо определить к
какому типу реакций (обменная или
окислительно — восстановительная)
относится данная реакция, для чего
рассчитывают степени окисления атомов
или групп атомов в формульных единицах
всех веществ.
Реакция
а)
является
окислительно-восстановительной.
Находим
атомы, которые изменяют степени окисления,
и выписываем их, с учетом числа в составе
одной формульной единицы и числа отданных
и принятых электронов:
а)
для реагентов
б)
для продуктов
Расчеты
всех величин приведены в таблице 5.
Таблица
5
|
ФЕ |
|
Z(B) |
M(B), |
|
|
|
Fe2O3 |
6 |
6 |
160,0 |
26,7 |
— |
|
CO |
2 |
2 |
28,0 |
14,0 |
11,2 |
|
Fe |
3 |
3 |
56,0 |
18,7 |
— |
|
CO2 |
2 |
2 |
44,0 |
22,0 |
11,2 |
Реакция
б)
является
обменной, т.к. степени окисления атомов
и групп атомов в ходе реакции не
изменяются. Далее необходимо выбрать
те части формульных единиц (положительно
или отрицательно заряженных) по которым
будет производится расчет суммарного
заряда замещающихся ионов, а далее –
Z(B)
и Мэк(В). Расчеты приведены в таблице 6.
Таблица
6.
|
ФЕ |
Замещаю- щиеся ионы |
qi |
Ni |
Z(В)= |
М(В), г/моль |
|
|
Al2(SO4)3 |
SO4–2 |
–2 |
3 |
3·2=6 |
342,0 |
57,0 |
|
NaOH |
Na+ |
+1 |
1 |
1·1=1 |
40,0 |
40,0 |
|
Al(OH)3 |
OH– |
–1 |
3 |
3·1=3 |
78,0 |
26,0 |
|
Na2SO4 |
Na+ |
+1 |
2 |
2·1=2 |
142,0 |
71,0 |
6. Закон эквивалентов.
Согласно
закону эквивалентов все
вещества реагируют и образуются в
эквивалентных количествах.
Например,
для реакции
2CO
+ O2
= 2CO2
(24)
nэк(CO)
= nэк(O2)=nэк(CO2)
(25)
Для
реакции в общем виде:
nAA
+ nBB
= nCC
+ nDD
, (26)
где
A,B
– реагенты;
C,D
– продукты реакции;
nA,nB,nC,nD
– стехиометрические коэффициенты,
закон
эквивалентов
имеет вид:
nэк(A)
= nэк(B)
= nэк(C)
= nэк(D)
(27)
Т.е.
количество вещества эквивалентов всех
участвующих в реакции (26) веществ
(реагентов А и В и образовавшихся
продуктов C
и D)
одинаковы. Поэтому, если количество
вещества эквивалентов одного из веществ
(реагента или продукта) известно по
условию задачи, то определены и nэк
всех остальных веществ, участвующих в
реакции, и необходимость их расчета
отпадает. В этом состоит преимущество
проведения расчетов по закону эквивалентов.
Для
любой химической реакции (см. уравнение
реакции в общем виде (26)) соблюдается
условие (27), которое также может быть
представлено следующим образом:
n(А)
· Z(A)=
n(В)
· Z(B)=
n(С)
· Z(C)=
n(D)
· Z(D)
(28)
Условие
(28) упрощает определение эквивалентного
числа в сложных реакциях.
Пример.
Определить Z(Cr2(SO4)3)
в обменной реакции, выраженной уравнением
Cr2(SO4)3
+ 12KOH = 2K3[Cr(OH)6]
+ 3K2SO4
Решение.
Для приведенной реакции запишем условие
(28):
n(
Cr2(SO4)3)
· Z(Cr2(SO4)3)=
n(
KOH) · Z(KOH)
Из
уравнения реакции:
n(
Cr2(SO4)3)
= 1 n(KOH)
= 12
Поскольку
Z(KOH)
= 1 (не может быть другим, см. табл. 2), то
Если
известны массы веществ, участвующих в
реакции, то используя уравнения (21) и
(27) можно записать:
(29)
или
(30)
Уравнение
(30) является математическим выражением
закона эквивалентов.
Если
одно из веществ уравнения (26), например
B,
находится в газообразном состоянии и
известен его объем при н.у., то количество
вещества эквивалентов этого газа можно
рассчитать по уравнению (22), а математическая
запись закона эквивалентов для веществ
A
и B
будет иметь вид:
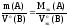
Пример.
Рассчитать массу алюминия, вступившего
в реакцию с разбавленной серной кислотой,
если в результате реакции образуется
10,2 л водорода (н.у.).
Решение.
Запишем уравнение реакции и укажем
степени окисления атомов и заряды ионов:
Реакция
окислительно-восстановительная. Находим
атомы, которые изменяют степени окисления,
и выписываем их, с учетом числа в составе
одной формульной единицы и числа отданных
и принятых электронов:
Alo
–
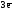
Al+3 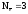
H2o
–
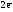
2H+1 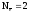
= 2
Согласно
закону эквивалентов:
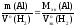
Отсюда
выражаем массу алюмиия:
Рассчитаем
Мэк(Al)
и
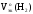
Подставив
полученные значения Мэк(Al)
и
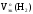
а так жеVo(H2),
рассчитаем массу алюминия:
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #