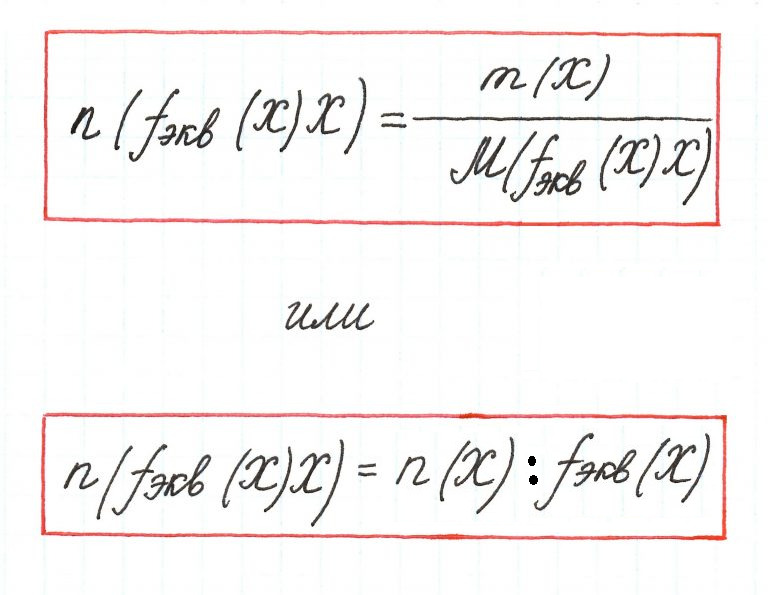Следует учитывать, что эквивалент одного
и того же вещества может меняться в
зависимости от того, в какую реакцию
оно вступает. Эквивалент элемента также
может быть различным в зависимости от
вида соединения, в состав которого он
входит. Эквивалентом может являться
как сама молекула или какая-либо другая
формульная единица вещества, так и ее
часть.
Рассмотрим реакцию, протекающую по
уравнению:
H3PO4
+ 2KOH = K2HPO4
+ 2H2O.
В ходе этой реакции только два атома
водорода замещаются на атомы калия
(кислота проявляет основность, равную
2). С другой стороны, на взаимодействие
с одной молекулой ортофосфорной кислотой
расходуется два иона ОН– щелочи,
следовательно, на взаимодействие с ½
молекулы кислоты потребуется один ион
ОН–. Эквивалентом кислоты является
½Н3РО4, а эквивалентом щелочи
частица КОН.
Число, показывающее, какая часть молекулы
или другой частицы вещества соответствует
эквиваленту, называется фактором
эквивалентности (fЭ).Фактор эквивалентности – это безразмерная
величина, которая меньше, либо равна 1.
Формулы расчета фактора эквивалентности
приведены в таблице 2.
Таким образом, сочетая фактор
эквивалентности и формульную единицу
вещества, можно составить формулу
эквивалента какой-либо частицы, где
фактор эквивалентности записывается
как химический коэффициент перед
формулой частицы:
Эквивалент = fЭ
∙ (формульная единица вещества)
(1.7)
В
примере, рассмотренном выше, фактор
эквивалентности для кислоты, соответственно,
равен ½, а для щелочи КОН – 1.
Между
H3PO4и КОН также могут происходить и другие
реакции. При этом кислота будет иметь
разные значения фактора эквивалентности:
H3PO4
+ 3KOH = K3PO4
+ 3H2O
fЭ(H3PO4)
= 1/3
H3PO4
+ KOH = KН2PO4
+ H2O
fЭ(H3PO4)
= 1.
Эквивалент, как частица, может быть
охарактеризован молярной массой
(молярным объемом) и определенным
количеством веществаэ.
Молярная масса эквивалента(МЭ)
– это масса одного моля эквивалентов,
г/моль. Она равна произведению молярной
массы вещества на фактор эквивалентности:
МЭ = М ·
fЭ.
(1.8)
Молярная масса эквивалента сложного
вещества равна сумме молярных масс
эквивалентов образующих его составных
частей, например:
МЭ(оксида) = МЭ(элемента)
+ МЭ(О),
МЭ(кислоты) = МЭ(Н)
+ МЭ(кислотного
остатка),
МЭ(основания) = МЭ(Ме)
+ МЭ(ОН),
МЭ(соли) = МЭ(Ме)
+ МЭ(кислотного
остатка).
Газообразные вещества, кроме молярной
массы эквивалента, имеют молярный
объем эквивалента(другой термин –
эквивалентный объем,VЭ)
– объем, занимаемый молярной массой
эквивалента или объем одного моля
эквивалентов (размерность –
дм3/моль).
При н.у. получаем:
(1.9)
Эквивалентный
объем водорода при н.у. равен Voэ(Н2)
= 22,4/2 = = 11,2 дм3/моль (объем 1 г
газа при н.у.), соответственно Voэ(О2)
= 22,4/4 = = 5,6 дм3/моль.
Пример.
Определить фактор эквивалентности и
эквивалент у солей: а) ZnCl2,
б) КНСО3, в) (MgOH)2SO4.
Решение: Согласно формулам, приведенным
в таблице 1.2:
Таблица 1.2
Расчет фактора эквивалентности
|
Частица |
Фактор эквивалентности |
Пример |
|
|
В реакциях обмена |
Элемент |
где В(Э) – валентность |
|
|
Простое вещество |
где n(Э) |
fЭ(H2) fЭ(O2) fЭ(O3) |
|
|
Оксид |
где n(Э) |
fЭ(Cr2O3) fЭ(H2O) fЭ(P2O5) |
|
|
Кислота |
где n(H+) |
fЭ(H2SO4) (если основность fЭ(H2SO4) (если основность |
|
|
Основа-ние |
где n(ОH–) |
fЭ(Cu(OH)2) fЭ(Cu(OH)2) (если |
|
|
Соль |
где n(Ме) |
fЭ(Cr2(SO4)3) fЭ(Cr2(SO4)3) |
|
|
В ОВР |
где ne– |
MnO4– fЭ(MnO4–) |
а) ZnCl2(средняя соль)
.
fЭ(ZnCl2)
= 1/2, поэтому эквивалентомZnCl2является частица 1/2ZnCl2;
б) КНСО3(кислая соль)
,
fЭ(КНСО3)
= 1, поэтому эквивалентом КНСО3является частица КНСО3;
в) (MgOH)2SO4(основная соль)
.
fЭ(
(MgOH)2SO4
) = 1/2, поэтому эквивалентом(MgOH)2SO4является частица 1/2(MgOH)2SO4.
Из закона эквивалентов следует, что
массы (или объемы) реагирующих и
образующихся веществ пропорциональны
молярным массам (молярным объемам) их
эквивалентов. Для любых двух веществ,
связанных законом эквивалентов, можно
записать:
,
,
,
(1.10)
где m1иm2 – массы
реагентов и (или) продуктов реакции,
г;
и
–
молярные массы эквивалентов реагентов
и (или) продуктов реакции,
г/моль;V1,V2– объемы
реагентов и (или) продуктов реакции,
дм3;,
–
молярные объемы эквивалентов реагентов
и (или) продуктов реакции,
дм3/моль.
Соседние файлы в папке ХИМИЯ
- #
- #
Материалы из методички: Сборник задач по теоретическим основам химии для студентов заочно-дистанционного отделения / Барботина Н.Н., К.К. Власенко, Щербаков В.В. – М.: РХТУ им. Д.И. Менделеева, 2007. -155 с.
Эквивалент. Закон эквивалентов
Эквивалент – реальная или условная частица вещества Х, которая в данной кислотно-основной реакции или реакции обмена эквивалентна одному иону водорода Н+ (одному иону ОН— или единичному заряду), а в данной окислительно-восстановительной реакции эквивалентна одному электрону.
Фактор эквивалентности fэкв(X) – число, показывающее, какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода или одному электрону в данной реакции, т.е. доля, которую составляет эквивалент от молекулы, иона, атома или формульной единицы вещества.
Наряду с понятием “количество вещества”, соответствующее числу его моль, используется также понятие количество эквивалентов вещества.
Закон эквивалентов: вещества реагируют в количествах, пропорциональных их эквивалентам. Если взято n(экв1) моль эквивалентов одного вещества, то столько же моль эквивалентов другого вещества n(экв2) потребуется в данной реакции, т.е.
n(экв1) = n(экв2) (2.1)
При проведении расчетов необходимо использовать следующие соотношения:
1. Молярная масса эквивалента вещества X равна его молярной массе, умноженной на фактор эквивалентности:
Мэкв(X) = М(X)× fэкв(X). (2.2)
2. Количество эквивалентов вещества X определяется делением его массы на молярную массу эквивалента:
nэкв(X) = m(X)/Мэкв(X). (2.3)
3. Объём моль-эквивалента газа Х при н.у. равен молярному объёму газа, умноженному на фактор эквивалентности:
Vэкв(X) = V(X) × fэкв(X) = 22,4× fэкв(X). (2.4)
4. Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов составляющих это вещество атомов (ионов).
5. Молярная масса эквивалента оксида равна молярной массе эквивалента элемента плюс молярная масса эквивалента кислорода.
6. Молярная масса эквивалента гидроксида металла равна молярной массе эквивалента металла плюс молярная масса эквивалента гидроксила, например:
М[½Са(ОН)2] = 20 + 17 = 37 г/моль.
7. Молярная масса эквивалента сульфата металла равна молярной массе эквивалента металла плюс молярная масса эквивалента SO42-, например,
М(½ СаSO4) = 20 + 48 = 68 г/моль.
Эквивалент в кислотно-основных реакциях
На примере взаимодействия ортофосфорной кислоты со щелочью с образованием дигидро-, гидро- и среднего фосфата рассмотрим эквивалент вещества H3PO4.
H3PO4 + NaOH = NaH2PO4 + H2O, fэкв(H3PO4) =1.
H3PO4 + 2NaOH = Na2HPO4 + 2H2O, fэкв(H3PO4) =1/2.
H3PO4 + 3NaOH = Na3PO4 + 3H2O, fэкв(H3PO4) =1/3.
Эквивалент NaOH соответствует формульной единице этого вещества, так как фактор эквивалентности NaOH равен единице. В первом уравнении реакции молярное соотношение реагентов равно 1:1, следовательно, фактор эквивалентности H3PO4 в этой реакции равен 1, а эквивалентом является формульная единица вещества H3PO4.
Во втором уравнении реакции молярное отношение реагентов H3PO4 и NaOH составляет 1:2, т.е. фактор эквивалентности H3PO4 равен 1/2 и её эквивалентом является 1/2 часть формульной единицы вещества H3PO4 .
В третьем уравнении реакции количество веществ реагентов относятся друг к другу как 1:3. Следовательно, фактор эквивалентности H3PO4 равен 1/3, а её эквивалентом является 1/3 часть формульной единицы вещества H3PO4.
Таким образом, эквивалент вещества зависит от вида химического превращения, в котором принимает участие рассматриваемое вещество.
Следует обратить внимание на эффективность применения закона эквивалентов: стехиометрические расчёты упрощаются при использовании закона эквивалентов, в частности, при проведении этих расчётов отпадает необходимость записывать полное уравнение химической реакции и учитывать стехиометрические коэффициенты. Например, на взаимодействие без остатка 0,25 моль-экв ортофосфата натрия потребуется равное количество эквивалентов вещества хлорида кальция, т.е. n(1/2CaCl2) = 0,25 моль.
Эквивалент в окислительно-восстановительных реакциях
Фактор эквивалентности соединений в окислительно-восстановительных реакциях равен:
fэкв(X) = 1/n, (2.5)
где n – число отданных или присоединенных электронов.
Для определения фактора эквивалентности рассмотрим три уравнения реакций с участием перманганата калия:
2KMnO4 + 5Na2SO3 + 3H2SO4 = 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O.
2KMnO4 + 2Na2SO3 + H2O = 2Na2SO4 + 2MnO2 + 2KOH.
2KMnO4 + Na2SO3 + 2NaOH = Na2SO4 + K2MnO4 + Na2MnO4 + H2O.
В результате получаем следующую схему превращения KMnO4.
в кислой среде: Mn+7 + 5e = Mn+2
в нейтральной среде: Mn+7 + 3e = Mn+4
в щелочной среде: Mn+7 + 1e = Mn+6
Схема превращений KMnO4 в различных средах
Таким образом, в первой реакции fэкв(KMnO4) = 1/5, во второй – fэкв(KMnO4) = 1/3, в третьей – fэкв(KMnO4) = 1.
Следует подчеркнуть, что фактор эквивалентности дихромата калия, реагирующего в качестве окислителя в кислой среде, равен 1/6:
Cr2O72- + 6e + 14H+ = 2 Cr3+ + 7H2O
Примеры решения задач
Задача 1. Определить фактор эквивалентности сульфата алюминия, который взаимодействует со щелочью.
Решение. В данном случае возможно несколько вариантов ответа:
Al2(SО4)3 + 6 KOH = 2 Аl(ОН)3 + 3 K2SО4, fэкв(Al2(SО4)3) = 1/6,
Al2(SО4)3 + 8 KOH(изб) = 2 K[Al(OH)4 ] + 3 K2SО4, fэкв (Al2(SО4)3) = 1/8,
Al2(SО4)3 + 12KOH(изб) = 2K3[Al(OH)6] + 3K2SО4, fэкв (Al2(SО4)3) = 1/12.
Задача 2. Определить факторы эквивалентности Fe3О4 и KCr(SO4)2 в реакциях взаимодействия оксида железа с избытком хлороводородной кислоты и взаимодействия двойной соли KCr(SO4)2 со стехиометрическим количеством щёлочи КОН с образованием гидроксида хрома (III).
Решение.
Fe3О4 + 8 НСl = 2 FeСl3 + FeСl2 + 4 Н2О, fэкв(Fe3О4) = 1/8,
KCr(SO4)2 + 3 КОН = 2 K2SO4 + Сr(ОН)3, fэкв(KCr(SO4)2) = 1/3.
Задача 3. Определить факторы эквивалентности и молярные массы эквивалентов оксидов CrО, Cr2О3 и CrО3 в кислотно-основных реакциях.
CrО + 2 HCl = CrCl2 + H2О; fэкв(CrО) = 1/2,
Cr2О3 + 6 HCl = 2 CrCl3 + 3 H2О; fэкв(Cr2О3) = 1/6,
CrО3 – кислотный оксид. Он взаимодействует со щёлочью:
CrО3 + 2 KОH = K2CrО4 + H2О; fэкв(CrО3) = 1/2.
Молярные массы эквивалентов рассматриваемых оксидов равны:
Мэкв(CrО) = 68(1/2) = 34 г/моль,
Мэкв(Cr2О3) = 152(1/6) = 25,3 г/моль,
Мэкв(CrО3) = 100(1/2) = 50 г/моль.
Задача 4. Определить объём 1 моль-экв О2, NH3 и H2S при н.у. в реакциях:
4 NH3 + 3 О2 2 N2 + 6 H2О;
4 NH3 + 5 О2 4 NO + 6 H2О;
2 H2S + 3 О2 2 SО2 + 2 H2О.
Решение.
Vэкв(О2) = 22,4× 1/4 = 5,6 л.
Vэкв(NH3) = 22,4× 1/3 = 7,47 л – в первой реакции.
Vэкв(NH3) = 22,4× 1/5 = 4,48 л – во второй реакции.
В третьей реакции для сероводорода Vэкв(H2S)=22,4 1/6 = 3,73 л.
Задача 5. 0,45 г металла вытесняют из кислоты 0,56 л (н.у.) водорода. Определить молярную массу эквивалента металла, его оксида, гидроксида и сульфата.
Решение.
nэкв(Ме) = nэкв(Н2) = 0,56:(22,4× 1/2) = 0,05 моль.
Мэкв(X) = m(Ме)/nэкв(Мe) = 0,45:0,05 = 9 г/моль.
Мэкв(МеxOy) = Мэкв(Ме) + Мэкв(O2) = 9 + 32× 1/4 = 9 + 8 = 17 г/моль.
Мэкв(Ме(OH)y) = Мэкв(Ме) + Мэкв(OH—) = 9+17 = 26 г/моль.
Мэкв(Меx(SO4)y) = Мэкв(Ме) + Мэкв(SO42-) = 9 + 96× 1/2 = 57 г/моль.
Задача 6. Рассчитать массу перманганата калия, необходимую для окисления 7,9 г сульфита калия в кислой и нейтральной средах.
Решение.
fэкв(K2SО3) = 1/2 (в кислой и нейтральной среде).
Мэкв(K2SО3) = 158× 1/2 = 79 г/моль.
nэкв (KMnO4) = nэкв(K2SО3) = 7,9/79 = 0,1 моль.
В кислой среде Мэкв(KMnO4) = 158·1/5 = 31,6 г/моль, m(KMnO4) = 0,1·31,6 = 3,16 г.
В нейтральной среде Мэкв (KMnO4) = 158·1/3 = 52,7 г/моль, m(KMnO4) = 0,1·52,7 =5,27 г.
Задача 7. Рассчитать молярную массу эквивалента металла, если оксид этого металла содержит 47 мас.% кислорода.
Решение.
Выбираем для расчётов образец оксида металла массой 100 г. Тогда масса кислорода в оксиде составляет 47 г, а масса металла – 53 г.
В оксиде: nэкв (металла) = nэкв(кислорода). Следовательно:
m(Ме):Мэкв(Ме) = m(кислорода):Мэкв(кислорода);
53:Мэкв(Ме) = 47:(32·1/4). В результате получаем Мэкв(Ме) = 9 г/моль.
Задачи для самостоятельного решения
2.1. Молярная масса эквивалента металла равна 9 г/моль. Рассчитать молярную массу эквивалента его нитрата и сульфата.
Ответ: 71 г/моль; 57 г/моль.
2.2. Молярная масса эквивалента карбоната некоторого металла составляет 74 г/моль. Определить молярные массы эквивалентов этого металла и его оксида.
Ответ: 44 г/моль; 52 г/моль.
2.3. Рассчитать объём 1 моля эквивалента сероводорода (н.у.), который окисляется до оксида серы (IV).
2.4. Определить молярную массу эквивалента Ni(OH)Cl в реакциях:
Ni(OH)Cl + H2S = NiS + HCl + H2O;
Ni(OH)Cl + NaOH = Ni(OH)2 + NaCl.
Ответ: 55,6 г/моль; 111,2 г/моль.
2.5. При взаимодействии 4,8 г неизвестного металла и 13 г цинка с соляной кислотой выделяется одинаковый объём водорода. Вычислить молярные массы эквивалентов металла, его оксида и его хлорида.
Ответ: МЭ(металла)=12 г/моль; МЭ(оксида)=20 г/моль, МЭ(хлорида)=47,5 г/моль.
2.6. Рассчитать молярные массы эквивалентов металла и его гидроксида, если хлорид этого металла содержит 79,7 мас.% хлора, а молярная масса эквивалента хлора равна 35,5 г/моль.
Ответ: МЭ(металла)=9 г/моль; МЭ(оксида)=26 г/моль.
2.7. Какой объём 0,6 М раствора H2O2 пойдёт на окисление 150 мл 2н. раствора FeSO4 в реакции:
H2O2 + 2 FeSO4 + H2SO4 = Fe2(SO4)3 + 2 H2O.
2.8. Определить объём хлора (н.у), необходимый для окисления 100 мл 0,5н раствора K2MnO4.
2.9. 0,66 г кислоты требуются для нейтрализации 10 мл 1М раствора КОН. Найти молярные массы эквивалентов кислоты и ее кальциевой соли в обменной реакции.
Ответ: МЭ(кислоты)=66 г/моль; МЭ(соли)=85 г/моль.
2.10. Бромид металла в результате обменной реакции полностью переведен в сульфат, при этом масса уменьшилась в 1,47 раз. Найти молярную массу эквивалента металла. Определить какой это металл.
Ответ: МЭ(металла)=20 г/моль; Са.
Как рассчитать фактор эквивалентности по уравнению
Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н + или ОН – , в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества. Например, рассмотрим следующую реакцию:
В ходе этой реакции только два атома водорода замещаются на атомы калия, иначе, в реакцию вступают два иона Н + (кислота проявляет основность 2). Тогда по определению эквивалентом H 3 PO 4 будет являться условная частица 1/2 H 3 PO 4, т.к. если одна молекула H 3 PO 4 предоставляет два иона Н + , то один ион Н + дает половина молекулы H 3 PO 4.
С другой стороны, на реакцию с одной молекулой ортофосфорной кислотой щелочь отдает два иона ОН – , следовательно, один ион ОН – потребуется на взаимодействие с 1/2 молекулы кислоты. Эквивалентом кислоты является условная частица 1/2Н3РО4, а эквивалентом щелочи частица КОН.
Число, показывающее, какая часть молекулы или другой частицы вещества соответствует эквиваленту, называется фактором эквивалентности ( f Э). Фактор эквивалентности – это безразмерная величина, которая меньше, либо равна 1. Формулы расчета фактора эквивалентности приведены в таблице 1.1.
Таким образом, сочетая фактор эквивалентности и формульную единицу вещества, можно составить формулу эквивалента какой-либо частицы, где фактор эквивалентности записывается как химический коэффициент перед формулой частицы:
f Э (формульная единица вещества) º эквивалент
В примере, рассмотренном выше, фактор эквивалентности для кислоты, соответственно, равен 1/2, а для щелочи КОН равен 1.
Между H 3 PO 4 и КОН также могут происходить и другие реакции. При этом кислота будет иметь разные значения фактора эквивалентности:
Следует учитывать, что эквивалент одного и того же вещества может меняться в зависимости от того, в какую реакцию оно вступает. Эквивалент элемента также может быть различным в зависимости от вида соединения, в состав которого он входит. Эквивалентом может являться как сама молекула или какая-либо другая формульная единица вещества, так и ее часть.
Таблица 1.1 – Расчет фактора эквивалентности
Частица
Фактор эквивалентности
Примеры
Элемент
,
где В(Э) – валентность элемента
Простое вещество
,
где n (Э) – число атомов элемента (индекс в химической формуле), В(Э) – валентность элемента
f Э (O3) = 1/(3 × 2) = 1/6
Оксид
,
где n (Э) – число атомов элемента (индекс в химической формуле оксида), В(Э) – валентность элемента
f Э (P2O5) = 1/(2 × 5) = 1/10
Кислота
,
где n ( H + ) – число отданных в ходе реакции ионов водорода (основность кислоты)
f Э ( H 2 SO 4 ) = 1/1 = 1 (основность равна 1)
(основность равна 2)
Основание
,
где n (О H – ) – число отданных в ходе реакции гидроксид-ионов (кислотность основания)
f Э ( Cu ( OH )2) = 1/1 = 1 (кислотность равна 1) или
(кислотность равна 2)
,
где n (Ме) – число атомов металла (индекс в химической формуле соли), В(Ме) – валентность металла; n (А) – число кислотных остатков, В(А) – валентность кислотного остатка
f Э ( Cr 2 ( SO 4 )3) = 1/(3 × 2) = 1/6 (расчет по кислотному остатку)
Частица в окислительно-восстановительных реакциях
,
где – число электронов, участвующих в процессе окисления или восстановления
Fe 2+ + 2 ® Fe 0
MnO4 – + 8H + + 5 ® ® Mn 2+ + 4H2O
f Э ( MnO 4 – ) = 1/5
,
где z – заряд иона
f Э ( SO 4 2– ) = 1/2
Пример. Определите фактор эквивалентности и эквивалент у солей: а) ZnCl 2, б) КНСО3, в) ( MgOH )2 SO 4.
Решение: Для расчетов воспользуемся формулами, приведенными в таблице 1.1.
а) ZnCl 2 (средняя соль):
.
f Э( ZnCl 2) = 1/2, поэтому эквивалентом ZnCl 2 является частица 1/2 ZnCl 2.
б) КНСО3 (кислая соль):
.
f Э(КНСО3) = 1, поэтому эквивалентом КНСО3 является частица КНСО3.
в) ( MgOH )2 SO 4 (основная соль):
.
f Э ( ( MgOH )2 SO 4 ) = 1/2, поэтому эквивалентом ( MgOH )2 SO 4 является частица 1/2( MgOH )2 SO 4.
Эквивалент, как частица, может быть охарактеризован молярной массой (молярным объемом) и определенным количеством вещества n э. Молярная масса эквивалента (МЭ) – это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности:
МЭ = М × f Э.
Молярная масса эквивалента имеет размерность «г/моль».
Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов образующих его составных частей , например:
МЭ(соли) = МЭ(Ме) + МЭ(кислотного остатка).
Газообразные вещества помимо молярной массы эквивалента имеют молярный объем эквивалента ( или V Э) – объем, занимаемый молярной массой эквивалента или объем одного моль эквивалента . Размерность « л/моль » . При н.у. получаем:
Закон эквивалентов был открыт в 1792 г. И. Рихтером. Современная формулировка закона: вещества реагируют и образуются согласно их эквивалентам . Все вещества в уравнении реакции связаны законом эквивалентов, поэтому:
n э(реагента1) = … = n э(реагента n ) = n э (продукта1) = … = n э (продукта n )
Из закона эквивалентов следует, что массы (или объемы) реагирующих и образующихся веществ пропорциональны молярным массам (молярным объемам) их эквивалентов. Для любых двух веществ, связанных законом эквивалентов, можно записать:
или или ,
где m 1 и m 2 – массы реагентов и (или) продуктов реакции , г ;
, – молярные массы эквивалентов реагентов и (или) продуктов реакции , г/моль ;
V 1, V 2 – объемы реагентов и (или) продуктов реакции , л ;
, – молярные объемы эквивалентов реагентов и (или) продуктов реакции , л/моль .
Эквивалент. Закон эквивалентов
Материалы портала onx.distant.ru
Эквивалент. Закон эквивалентов
Эквивалент – реальная или условная частица вещества Х, которая в данной кислотно-основной реакции или реакции обмена эквивалентна одному иону водорода Н + (одному иону ОН — или единичному заряду), а в данной окислительно- восстановительной реакции эквивалентна одному электрону.
Фактор эквивалентности fэкв(X) – число, показывающее, какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода или одному электрону в данной реакции, т.е. доля, которую составляет эквивалент от молекулы, иона, атома или формульной единицы вещества.
Наряду с понятием “количество вещества”, соответствующее числу его моль, используется также понятие количество эквивалентов вещества.
Закон эквивалентов: вещества реагируют в количествах, пропорциональных их эквивалентам. Если взято n(экв1) моль эквивалентов одного вещества, то столько же моль эквивалентов другого вещества n(экв2) потребуется в данной реакции, т.е.
При проведении расчетов необходимо использовать следующие соотношения:
1. Молярная масса эквивалента вещества X равна его молярной массе, умноженной на фактор эквивалентности:
2. Количество эквивалентов вещества X определяется делением его массы на молярную массу эквивалента:
3. Объём моль-эквивалента газа Х при н.у. равен молярному объёму газа, умноженному на фактор эквивалентности:
4. Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов составляющих это вещество атомов (ионов).
5. Молярная масса эквивалента оксида равна молярной массе эквивалента элемента плюс молярная масса эквивалента кислорода.
6. Молярная масса эквивалента гидроксида металла равна молярной массе эквивалента металла плюс молярная масса эквивалента гидроксила, например:
М[½Са(ОН)2] = 20 + 17 = 37 г/моль.
7. Молярная масса эквивалента сульфата металла равна молярной массе эквивалента металла плюс молярная масса эквивалента SO4 2- , например,
М(½ СаSO4) = 20 + 48 = 68 г/моль.
Эквивалент в кислотно-основных реакциях
На примере взаимодействия ортофосфорной кислоты со щелочью с образованием дигидро-, гидро- и среднего фосфата рассмотрим эквивалент вещества H3PO4.
Эквивалент NaOH соответствует формульной единице этого вещества, так как фактор эквивалентности NaOH равен единице. В первом уравнении реакции молярное соотношение реагентов равно 1:1, следовательно, фактор эквивалентности H3PO4 в этой реакции равен 1, а эквивалентом является формульная единица вещества H3PO4.
Во втором уравнении реакции молярное отношение реагентов H3PO4 и NaOH составляет 1:2, т.е. фактор эквивалентности H3PO4 равен 1/2 и её эквивалентом является 1/2 часть формульной единицы вещества H3PO4 .
В третьем уравнении реакции количество веществ реагентов относятся друг к другу как 1:3. Следовательно, фактор эквивалентности H3PO4 равен 1/3, а её эквивалентом является 1/3 часть формульной единицы вещества H3PO4.
Таким образом, эквивалент вещества зависит от вида химического превращения, в котором принимает участие рассматриваемое вещество.
Следует обратить внимание на эффективность применения закона эквивалентов: стехиометрические расчёты упрощаются при использовании закона эквивалентов, в частности, при проведении этих расчётов отпадает необходимость записывать полное уравнение химической реакции и учитывать стехиометрические коэффициенты. Например, на взаимодействие без остатка 0,25 моль-экв ортофосфата натрия потребуется равное количество эквивалентов вещества хлорида кальция, т.е. n(1/2CaCl2) = 0,25 моль.
Эквивалент в окислительно-восстановительных реакциях
Фактор эквивалентности соединений в окислительно-восстановительных реакциях равен:
где n – число отданных или присоединенных электронов.
Для определения фактора эквивалентности рассмотрим три уравнения реакций с участием перманганата калия:
В результате получаем следующую схему превращения KMnO4.
в кислой среде: Mn +7 + 5e = Mn +2
в нейтральной среде: Mn +7 + 3e = Mn +4
в щелочной среде: Mn +7 + 1e = Mn +6
Схема превращений KMnO4 в различных средах
Таким образом, в первой реакции fэкв(KMnO4) = 1/5, во второй – fэкв(KMnO4) = 1/3, в третьей – fэкв(KMnO4) = 1.
Следует подчеркнуть, что фактор эквивалентности дихромата калия, реагирующего в качестве окислителя в кислой среде, равен 1/6:
Примеры решения задач
Задача 1. Определить фактор эквивалентности сульфата алюминия, который взаимодействует со щелочью.
Решение. В данном случае возможно несколько вариантов ответа:
Задача 2. Определить факторы эквивалентности Fe3О4 и KCr(SO4)2 в реакциях взаимодействия оксида железа с избытком хлороводородной кислоты и взаимодействия двойной соли KCr(SO4)2 со стехиометрическим количеством щёлочи КОН с образованием гидроксида хрома (III).
Задача 3. Определить факторы эквивалентности и молярные массы эквивалентов оксидов CrО, Cr2О3 и CrО3 в кислотно-основных реакциях.
CrО3 – кислотный оксид. Он взаимодействует со щёлочью:
Молярные массы эквивалентов рассматриваемых оксидов равны:
Мэкв(CrО) = 68(1/2) = 34 г/моль,
Задача 4. Определить объём 1 моль-экв О2, NH3 и H2S при н.у. в реакциях:
Vэкв(NH3) = 22,4× 1/3 = 7,47 л – в первой реакции.
Vэкв(NH3) = 22,4× 1/5 = 4,48 л – во второй реакции.
В третьей реакции для сероводорода Vэкв(H2S)=22,4 1/6 = 3,73 л.
Задача 5. 0,45 г металла вытесняют из кислоты 0,56 л (н.у.) водорода. Определить молярную массу эквивалента металла, его оксида, гидроксида и сульфата.
Задача 6. Рассчитать массу перманганата калия, необходимую для окисления 7,9 г сульфита калия в кислой и нейтральной средах.
fэкв(K2SО3) = 1/2 (в кислой и нейтральной среде).
В кислой среде Мэкв(KMnO4) = 158·1/5 = 31,6 г/моль, m(KMnO4) = 0,1·31,6 = 3,16 г.
В нейтральной среде Мэкв (KMnO4) = 158·1/3 = 52,7 г/моль, m(KMnO4) = 0,1·52,7 =5,27 г.
Задача 7. Рассчитать молярную массу эквивалента металла, если оксид этого металла содержит 47 мас.% кислорода.
Выбираем для расчётов образец оксида металла массой 100 г. Тогда масса кислорода в оксиде составляет 47 г, а масса металла – 53 г.
В оксиде: nэкв (металла) = nэкв(кислорода). Следовательно:
53:Мэкв(Ме) = 47:(32·1/4). В результате получаем Мэкв(Ме) = 9 г/моль.
Задачи для самостоятельного решения
2.1. Молярная масса эквивалента металла равна 9 г/моль. Рассчитать молярную массу эквивалента его нитрата и сульфата.
Ответ: 71 г/моль; 57 г/моль.
2.2. Молярная масса эквивалента карбоната некоторого металла составляет 74 г/моль. Определить молярные массы эквивалентов этого металла и его оксида.
Ответ: 44 г/моль; 52 г/моль.
2.3. Рассчитать объём 1 моля эквивалента сероводорода (н.у.), который окисляется до оксида серы (IV).
Ответ: 3,73 л.
2.4. Определить молярную массу эквивалента Ni(OH)Cl в реакциях:
Ni(OH)Cl + NaOH = Ni(OH)2 + NaCl.
Ответ: 55,6 г/моль; 111,2 г/моль.
2.5. При взаимодействии 4,8 г неизвестного металла и 13 г цинка с соляной кислотой выделяется одинаковый объём водорода. Вычислить молярные массы эквивалентов металла, его оксида и его хлорида.
Ответ: МЭ(металла)=12 г/моль; МЭ(оксида)=20 г/моль, МЭ(хлорида)=47,5 г/моль.
2.6. Рассчитать молярные массы эквивалентов металла и его гидроксида, если хлорид этого металла содержит 79,7 мас.% хлора, а молярная масса эквивалента хлора равна 35,5 г/моль.
Ответ: МЭ(металла)=9 г/моль; МЭ(оксида)=26 г/моль.
2.7. Какой объём 0,6 М раствора H2O2 пойдёт на окисление 150 мл 2н. раствора FeSO4 в реакции:
Ответ: 250 мл.
2.8. Определить объём хлора (н.у), необходимый для окисления 100 мл 0,5н раствора K2MnO4.
Ответ: 0,56 л.
2.9. 0,66 г кислоты требуются для нейтрализации 10 мл 1М раствора КОН. Найти молярные массы эквивалентов кислоты и ее кальциевой соли в обменной реакции.
Ответ: МЭ(кислоты)=66 г/моль; МЭ(соли)=85 г/моль.
2.10. Бромид металла в результате обменной реакции полностью переведен в сульфат, при этом масса уменьшилась в 1,47 раз. Найти молярную массу эквивалента металла. Определить какой это металл.
Ответ: МЭ(металла)=20 г/моль; Са.
Как правильно рассчитывать фактор эквивалентности элементов и веществ
Фактор эквивалентности хрома в соединениях
Задача 232.
Определите эквивалент хрома в следующих соединениях: Cr2O3; CrO3.
Решение:
Эквмвалент = fЭ — фактор эквивалентности элемента (число, показывающее, какая часть молекулы или другой частицы вещества соответствует одному эквиваленту). Эквивалент элемента в оксиде определяется по формуле:
B(Э) — валентность хрома.
Определение фактора эквивалентности оксидов. кислот, оснований и солей
Задача 233.
Определите химические эквиваленты и молярные массы эквивалентов следующих веществ: В2О3; NaOH; H2SO3; NaAl(SO4)2.
Решение:
Молярная масса эквивалента вещества (МЭ) – это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности:
МЭ = М . fЭ, где
М — молярная масса вещества.
а) В2О3
Фактор эквивалентности оксида рассчитывается по формуле:
fЭ = 1/[(nЭ) . B(Э)], где
n(Э) – число атомов элемента (индекс в химической формуле оксида), В(Э) – валентность элемента.
fЭ(B2O3) = 1/(2 . 3) = 1/6, поэтому эквивалентом B2O3 является частица 1/2B2O3.
Зная фактор эквивалентности оксида бора, рассчитаем молярну массу эквивалента данного оксида1, получим:
МЭ(B2O3) = М(B2O3) . fЭ(B2O3) = 69,6182 г/моль . 1/6 = 11,6 г/моль.
б) NaOH
Фактор эквивалентности основания рассчитывается по формуле:
где n(ОH–) – число отданных в ходе реакции гидроксид-ионов (кислотность основания).
fЭ(NaOH) = 1/1 = 1 (кислотность равна 1), поэтому эквивалентом NaOH является частица 1NaOH.
Зная фактор эквивалентности гидроксида натрия, рассчитаем молярну массу эквивалента данного основания2, получим:
МЭ(NaOH) = М(NaOH) . fЭ(NaOH) = 40 г/моль . 1 = 40 г/моль.
в) H2SO3
Фактор эквивалентности кислоты рассчитывается по формуле:
n(H + ) – число отданных в ходе реакции ионов водорода (основность кислоты).
fЭ(H2SO3) = 1/2 (основность равна 2), поэтому эквивалентом H2SO3 является частица 1/2H2SO3.
Зная фактор эквивалентности сернистой кислоты, рассчитаем молярну массу эквивалента данной кислоты3, получим:
МЭ(H2SO3) = М(H2SO3) . fЭ(H2SO3) = 82 г/моль . 1/2 = 40 г/моль.
г) NaAl(SO4)2
М[NaAl(SO4)2] = 242 г/моль.
Фактор эквивалентности соли рассчитывается по формуле:
fЭ = 1/[n(Ме) . B(Me)] = 1/[n(A) . B(A)], где
n(Ме) – число атомов металла (индекс в химической формуле соли), В(Ме) – валентность металла; n(А) – число кислотных остатков, В(А) – валентность кислотного остатка.
Фактор эквивалентности сложной соли можно рассчитать по формуле:
fЭ = 1/<[n(Ме)1 . B(Me)2] + [n(Ме)1 . B(Me)2]> = 1/[n(A) . B(A)], где
n(Ме)1 и n(Ме)2 – число атомов металлов (первого и второго), В(Ме)1 и В(Ме)2 – валентности металлов (первого и второго); n(А) – число кислотных остатков, В(А) – валентность кислотного остатка.
fЭ[NaAl(SO4)2] = 1/<[n(Ме)1 . B(Me)2] + [n(Ме)1 . B(Me)2]> =
= 1/[n(A) . B(A)] = 1/[n(A) . B(A)] = 1[(1 . 1) / (1 . 3)] = 1/(2 . 2) = 1/4, поэтому эквивалентом NaAl(SO4)2 является частица 1/4NaAl(SO4)2.
Зная фактор эквивалентности сульфат алюмииния-наатрия, рассчитаем молярну массу эквивалента данной соли4, получим:
МЭ[NaAl(SO4)2] = М[NaAl(SO4)2] . fЭ[NaAl(SO4)2] = 242 г/моль . 1/4 = 60,5 г/моль.
Определение числа молей и числа эквивалентов в гидроксие титана (III)
Задача 234.
Определите число молей и число эквивалентов в 80 гидроксид титана (III) Ti(OH)3.
Решениие:
m[Ti(OH)3] = 80 г;
М[Ti(OH)3] = 98,89 г/моль ≈ 99 г/моль.
Фактор эквивалентности основания рассчитывается по формуле:
fЭ = 1/n(OH – ), где
где n(ОH – ) – число отданных в ходе реакции гидроксид-ионов (кислотность основания).
fЭ[Ti(OH)3] = 1/3 (кислотность равна 3), поэтому эквивалентом Ti(OH)3 является частица 1/3Ti(OH)3.
1. Определим число молей, получим:
2. Определим число эквивалентов, получим:
nfЭ[Ti(OH)3] = n[Ti(OH)3] . fЭ[Ti(OH)3] = 0,8 . 1/3 = 0,269 ≈ 0,27.
Определение объема эквивалентов хлора
Задача 235.
Определите объем 3,3 эквивалентов Cl2 (н.у.).
Решение:
Vm = 22,4 л/моль;
Молярный объем эквивалента (VmЭ или VЭ) – объем, занимаемый молярной массой эквивалента или объем одного моль эквивалента рассчитаем по формуле:
VЭ = fЭ . Vm = fЭ . 22,4, где
fЭ — фактор эквиваленттности газообразного вещества, Vm — молярный объем газообразного вещества (равен 22,4 л/моль).
Фактор эквивалентности простого вещества определяется по формуле:
1/[n(Э) . В(Э)], где
n(Э) – число атомов элемента (индекс в химической формуле), В(Э) – валентность элемента.
fЭ(Cl2) = 1/(2 . 1) = 1/2;
VЭ(Cl2) = fЭ . Vm = 1/2 . 22,4 = 11,2 л/моль.
Зная количество эквивалентов хлора [nfЭ(Cl2) = 3,3] и VЭ(Cl2), рассчитаем его объем, получим:
V(Cl2) = nfЭ(Cl2) . VЭ(Cl2) = 3,3(1/2) . 22,4 = 36,96 л.
Рассчет молярной массы эквивалента металла, образующегося при реакции с соляной кислотой
Задача 236.
Рассчитайте молярную массу эквивалента металла и определите какой это металл, если при взаимодействии 1 г его с разбавленной соляной кислотой выделяется водород объемом 220 мл, измеренный при давлении 740 мм. рт. ст. и температуре 21 o С. Каков фактор эквивалентности данного метала?
Решение:
Ввычислим объем водорода при нормальных условиях, используя формулу Клапейрона-Менделеева:
PV/T = PoVo/To, где Ро = 760 мм рт. ст., То = 273 К, V = 0,22 л, Р = 740 мм рт. ст. Т = 294 К, Vo = ?
Vo = PVTo/PoТ = (740 . 0,22 . 273)/(760 . 294) = 0,1989 л.
Рассчитаем количество эквивалентов водорода, получим:
nfЭ(Н2) = V/VЭ(Н2) = 0,1989/11,2 = 0,01776 мольэкв.
Согласно закону эквивалентов следует, вещества реагируют в эквивалентных количествах, то число эквивалентов (молей эквивалентов) металла столько же, т.е. nfЭ(Me) = 0,01776 мольэкв. Следовательно, 1 г металла составляет 0,01776 мольэкв.
Тогда
Вычислим молярную массу эквивалента металла, получим:
МЭ(Ме) = m(Ме)/nfЭ(Me) = 1/0,0178 = 56,306 г/моль.
Если валентность металла Z(Ме) = 1, то М(Ме) = МЭ . (Ме) = 56, 306г/моль — одновалентного металла с такой молярной массой нет (смотри таблицу Менделеева).
Если Z(Ме) = 2, то М(Ме) = 2МЭ(Ме) = 112,712 г/моль ≈ 112 г/иоль – двухвалентный металл с такой молярной массой есть — кадмий.
Фактор эквивалентности кадмия рассчитаем по формуле:
B(Э) — валентность кадмия.
1 Формула определения молярной массы эквивалента оксида:
МЭ(оксида) = МЭ(элемента) + МЭ(О) = МЭ(элемента) + 8, где
молярная масса эквивалента оксида;
МЭ(элемента) — молярная масса эквивалента элемента;
МЭ(О) — молярная масса эквивалента кислорода, 8 г/моль.
————————————————
2 Формула определения молярной массы эквивалента основания:
МЭ(основания) = МЭ(Ме) + МЭ(ОН) = МЭ(Ме) + 17, где
МЭ(основания) — молярная масса эквивалента основания;
МЭ(элемента) — молярная масса эквивалента металла;
МЭ(ОН) — молярная масса эквивалента гидроксид-иона, 17 г/моль.
————————————————
3 Формула определения молярной массы эквивалента кислоты:
МЭ(кислоты) = МЭ(Н) + МЭ(кислотного остатка) = 1 + МЭ(кислотного остатка), где
МЭ(кислоты) — молярная масса эквивалента кислоты;
МЭ(Н) — молярная масса эквивалента водорода, 1 г/моль;
МЭ(кислотного остатка) — молярная масса эквивалента кислотного остатка.
————————————————
4 Формула определения молярной массы эквивалента соли:
МЭ(соли) = МЭ(Ме) + МЭ(кислотного остатка), где
МЭ(соли) — молярная масса эквивалента соли;
МЭ(Ме) — молярная масса эквивалента металла;
МЭ(кислотного остатка) — молярная масса эквивалента кислотного остатка.
http://buzani.ru/zadachi/obshchaya-khimiya/1847-opredelenie-faktora-ekvivalentnosti-zadacha-232-236
Химический эквивалент является одним из основных понятий в химии. Эта характеристика вещества, несмотря на свою простоту, часто достаточно запутанна и вызывает ряд затруднений.
Содержание:
1 Химический эквивалент и фактор эквивалентности
1.1 Химический эквивалент в реакциях обмена
1.2 Химический эквивалент в окислительно-восстановительных реакциях
2 Молярная масса эквивалента
3 Химический эквивалент и количественный анализ. Закон эквивалентов
4 Химический эквивалент элемента и сложного вещества
В знаменитом толковом словаре русского языка С.И. Ожегова эквивалент трактуется как «нечто равноценное другому, вполне заменяющее его». Что это значит? Например, книга стоит 500 рублей. Таким образом, 500 рублей – это денежный эквивалент данной книги.
Понятие «эквивалент» в химии относится к реакциям окислительно-восстановительным, ионного обмена, используется при определении концентрации раствора, в реакциях электро-аналитических методов анализа.
Эквивалент является безразмерной величиной.
Химический эквивалент и фактор эквивалентности
Химический эквивалент в реакциях обмена
Разберемся с понятием «химический эквивалент» на примере реакции обмена.
Например, карбонат натрия Na2CO3 и соляная кислота HCl, взаимодействуя между собой, приведут к образованию разных продуктов реакции.
Здесь оба исходных вещества (Na2CO3 и HCl) реагируют друг с другом в соотношении 1:1, т.е. на одну частицу соли приходится одна частица кислоты. Это и есть эквивалентные количества реагирующих веществ. Химическим эквивалентом карбоната натрия в данном случае является одна частица Na2CO3, а эквивалентом соляной кислоты будет одна молекула HCl.
В другом случае оба вещества взаимодействуют иначе:
Исходные вещества реагируют в соотношениях 1:2. То есть с одной частицей соли взаимодействуют 2 молекулы кислоты. Что же здесь будет являться эквивалентом? При определении эквивалента принято сравнивать количество частиц исходного вещества с одним ионом (или атомом) водорода, с которым это исходное вещество может провзаимодействовать (или заместить) в реакции.
В данном случае ионы (атомы) водорода входят в состав соляной кислоты. Тогда в пересчете на одну молекулу HCl (или что то же самое, на один ион Н+), с ней будет реагировать только половина частицы (1/2 часть) Na2CO3. То есть соотношение реагирующих веществ будет 1/2:1. Таким образом, в данной реакции химическим эквивалентом соли является половина частицы Na2CO3. Химическим эквивалентом кислоты является одна молекула HCl.
Очевидно, что в реальности половины частицы Na2CO3 не существует. Поэтому говорят об условной частице вещества, когда определяют ее эквивалент.
Итак, химический эквивалент – это реальная или условная частица вещества, которая в данной химической реакции может прореагировать (или заместить) один атом (или ион) водорода или прореагировать с одним эквивалентом любого другого вещества.
Фактор эквивалентности ƒэкв – количественная характеристика эквивалента, он используется в расчетах.
Фактор эквивалентности показывает, какая доля частицы вещества прореагировала (заместила) в данной химической реакции один ион (атом) водорода.
Так, в первом случае, ƒэкв(Na2CO3)=1, а во втором – ƒэкв(Na2CO3)=1/2. Для соляной кислоты в обоих случаях ƒэкв(HCl)=1.
Рассмотрим другой пример реакции обмена: взаимодействие фосфорной кислоты и гидроксида калия. Определим ее эквивалент и фактор эквивалентности по отношению к одному эквиваленту гидроксида калия.
Фосфорная кислота H3PO4 является многоосновной кислотой. Для подобных кислот (двух- и трехосновных) необходимо учитывать стехиометрию конкретных реакций.
В данном случае одна молекула фосфорной кислоты реагирует с одной частицей гидроксида калия. Поэтому эквивалентом является одна молекула H3PO4. И тогда ее ƒэкв (H3PO4)=1.
А здесь одна молекула фосфорной кислоты реагирует с двумя частицами гидроксида калия. То есть в реакции участвует половина молекулы H3PO4. Это и есть ее эквивалент, который численно выражается фактором эквивалентности ƒэкв(H3PO4)=1/2.
Одна молекула H3PO4 реагирует с тремя частицами КОН. Таким образом, эквивалентом фосфорной кислоты здесь будет одна треть молекулы H3PO4. Тогда фактор эквивалентности ƒэкв(H3PO4)=1/3.
Определение эквивалента и фактора эквивалентности в реакциях обмена для оснований, солей также зависит от стехиометрии реакции.
Химический эквивалент в окислительно-восстановительных реакциях
В окислительно-восстановительных реакциях (ОВР), в отличие от реакций обмена, происходит переход электронов от одного вещества к другому, изменяются степени окисления окислителя и восстановителя. Именно эти процессы и важны при определении эквивалента и фактора эквивалентности в ОВР.
Рассмотрим примеры. Начнем с самого простого.
Взаимодействие водорода и кислорода с образованием воды – это окислительно-восстановительная реакция. В ней восстановителем является водород Н2, а окислителем – О2.
При определении эквивалентов в ОВР ориентируются на то, какая часть частицы принимает или отдает 1 (один) электрон.
Запишем еще раз каждую из полуреакций. Для восстановителя:
Одна молекула Н2 отдает 2ē. Тогда половина молекулы Н2 (а это один атом Н) отдаст 1ē. Следовательно, эквивалентом восстановителя в данной реакции будет половина (1/2 часть) молекулы Н2. И фактор эквивалентности ƒэкв(H2)=1/2.
Для окислителя:
Одна молекула О2 принимает 4ē. Тогда четверть этой молекулы (а это половина атома О) примет 1ē. Следовательно, эквивалентом окислителя в данной реакции будет 1/4 часть молекулы О2 (это условная частица, поскольку реально 1/4 часть молекулы О2 не существует). И фактор эквивалентности ƒэкв(О2)=1/4.
Рассмотрим еще один пример. Так, KMnO4 является сильным окислителем и в любых ОВР всегда проявляет только окислительные свойства. Эквивалент KMnO4 будет отличаться в зависимости от того, в какой ОВР участвует это вещество.
Реакция между сульфитом натрия и перманганатом калия протекает в кислой среде. Из полуреакции восстановления видим, что один ион MnO4— принимает 5ē для перехода в ион Mn2+. Тогда 1ē может принять условная частица, представляющая одну пятую часть (1/5) иона MnO4—. Таким образом, эквивалентом окислителя в данной реакции будет одна пятая часть (1/5) KMnO4. Для окислителя фактор эквивалентности составит ƒэкв(KMnO4)=1/5.
С тем же сульфитом натрия перманганат калия в нейтральной среде реагирует иначе.
Как ясно из приведенной полуреакции восстановления, одна третья часть (1/3) иона MnO4— принимает 1ē. Фактор эквивалентности окислителя в этом случае составит ƒэкв(KMnO4)=1/3.
Взаимодействие сульфита натрия и перманганата калия осуществляется и в щелочной среде:
В данном случае эквивалентом является одна частица KMnO4, поскольку, согласно полуреакции восстановления, речь идет о принятии 1ē. И фактор эквивалентности окислителя в таком случае составляет ƒэкв(KMnO4)=1.
Таким образом, в случае окислительно-восстановительных реакций эквивалентом является реальная или условная частица вещества, которая в данной ОВР эквивалентна 1 (одному) электрону. Эквивалент и фактор эквивалентности в ОВР не определяются стехиометрией реакции в отличие от реакций ионного обмена.
Молярная масса эквивалента
Молярная масса эквивалента (или эквивалентная масса) – это масса одного моля эквивалента вещества.
Обозначается следующим образом:
И выражается, как и молярная масса, в г/моль, поскольку фактор эквивалентности является безразмерной величиной.
Вернемся к примерам, рассмотренным выше.
В данной реакции ƒэкв (H3PO4)=1. Это в том числе означает, что фосфорная кислота вступает в реакцию в количестве 1 моль. Тогда масса 1 моль эквивалента этого вещества соответствует (и равна) его молярной массе: 98 г/моль. Можно сделать вывод, что в данном случае:
В другой реакции гидроксида калия и фосфорной кислоты:
Фактор эквивалентности кислоты ƒэкв (H3PO4)=1/2. Тогда:
И в третьем случае:
Фактор эквивалентности кислоты ƒэкв (H3PO4)=1/3. Тогда:
Как видим, в зависимости от стехиометрии реакции молярная масса эквивалента вещества будет принимать различные значения. Так, для фосфорной кислоты это 98 г/моль, 49г/моль и 32,66 г/моль. В этом заключается отличие молярной массы эквивалента от молярной массы вещества, которая всегда постоянна, не зависимо от типа реакции (обмена, ОВР) и ее стехиометрии.
Итак, молярная масса эквивалента равна произведению фактора эквивалентности и молярной массы вещества:
Химический эквивалент и количественный анализ. Закон эквивалентов
В количественном анализе широко применяются еще два понятия, связанных с химическим эквивалентом.
Количество вещества эквивалента – количество вещества, в котором частицами являются эквиваленты.
Единицей измерения является моль. Вычисляется по формуле:
Молярная концентрация эквивалента (или нормальная концентрация, Сн) представляет собой количество вещества эквивалента, содержащееся в одном литре (или дм3) раствора (моль/л, или моль/дм3).
Иногда запись единиц измерения нормальной концентрации моль/л, или моль/дм3, заменяют более простой записью: н. Например, 0,2 моль/л записывают как 0,2 н.
Если в 1 л (1дм3) раствора содержится 1 моль эквивалентов вещества, то такой раствор называется нормальным. Если содержится 0,1 моль – децинормальным, 0,01 моль – сантинормальным, 0,001 моль – миллинормальным и т.д.
Пример 1. Какова нормальная концентрация раствора H2C2O4∙2H2O, полученного растворением 1,73334 г ее в мерной колбе вместимостью 250 мл?
Пример 2. Какую массу KMnO4 следует взять для приготовления 2 л раствора с С(1/5KMnO4) = 0,02 моль/л?
Используя нормальные концентрации, легко посчитать, какие объемы веществ должны быть смешаны, чтобы те прореагировали полностью, т.е. без остатка. Либо, зная объемы прореагировавших без остатка веществ, можно определить их концентрации.
Согласно закону эквивалентов (И.В. Рихтер), утверждающему, что вещества реагируют между собой в строго определенных (эквивалентных) количествах:
Пример 3. Определите нормальную концентрацию раствора гидроксида калия, если на полное взаимодействие 15,00 мл его раствора израсходовано 18,70 мл раствора соляной кислоты с нормальной концентрацией 0,078моль/л.
Химический эквивалент элемента и молярная масса эквивалента сложного вещества
Если речь не идет о конкретной химической реакции, то посчитать эквивалент и эквивалентную массу элемента или сложного вещества можно, воспользовавшись несколькими способами. Приведем наиболее простые из них.
Химический эквивалент элемента
Химический эквивалент элемента представляет количество элемента, способное полностью соединяться с одним атомом (ионом) водорода или замещать столько же их в химических реакциях.
Так, в молекуле хлороводорода HCl на атом Н приходится один атом Cl. В связи с этим:
У сероводорода H2S 2 атомам Н соответствует 1 атом S. Следовательно, 1 атому Н будет соответствовать 1/2 атома S. И тогда:
Аммиак NH3 характеризуется тем, что в его молекуле 3 атома водорода соединяются с 1 атомом азота. В пересчете на один атом водорода это будет 1/3 атома азота. Поэтому:
Как не трудно заметить из приведенных примеров,
фактор эквивалентности для элементов равен единице, деленной на валентность элемента:
Молярная масса эквивалента сложного вещества
Основными классами сложных веществ являются оксиды, основания, кислоты и соли.
Поскольку не будем останавливаться на факторе эквивалентности в данном случае, молярную массу эквивалента обозначим упрощенно: Мэ.
Для оксидов рассчитывается по формуле:
Например:
Для оснований:
Например:
Для кислот:
Например:
Для солей:
Например:
Подведем итог.
Химический эквивалент – это частица вещества, реальная или условная. Количественным выражением эквивалента является фактор эквивалентности. Для определения эквивалентов веществ в реакции обмена необходимо учитывать ее стехиометрию, а в окислительно-восстановительной реакции – число отданных или принятых веществом электронов.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
Как определить фактор эквивалентности
Химический эквивалент — это частица вещества, которая принимает (отдает) один водород-ион или гидроксил-ион, принимает (отдает) один электрон в окислительно-восстановительных реакциях, а также реагирует с одним атомом водорода или одним эквивалентом другого вещества. Число, показывающее, какая часть молекулы вещества соответствует ее эквиваленту, называется фактором эквивалентности, который может быть либо равным единице, либо меньше ее.

Инструкция
Рассмотрите, например, реакции гидроксида натрия с ортофосфорной кислотой. В зависимости от того, в каких соотношениях были взяты исходные вещества, могу образовываться разные продукты. NaOH + H3PO4 = NaH2PO4 + H2O2NaOH + H3PO4 = Na2HPO4 + 2H2O3NaOH + H3PO4 = Na3PO4 + 3H2O
В первом случае на каждую молекулу щелочи, вступающую в реакцию, приходится одна молекула кислоты. Следовательно, фактор эквивалентности едкого натра равен 1, а фактор эквивалентности кислоты также равен 1.
Во втором случае одна молекула кислоты вступает во взаимодействие с двумя молекулами щелочи. То есть на одну молекулу едкого натра приходится 1/2 молекулы кислоты. Таким образом фактор эквивалентности щелочи по-прежнему равен 1, а фактор эквивалентности кислоты теперь равен 1/2.
Соответственно, в третьем случае, фактор эквивалентности едкого натра равен 1, а кислоты — 1/3, поскольку на одну молекулу щелочи приходится три молекулы кислоты.
Для разных классов химических соединений существуют соответствующие формулы расчета фактора эквивалентности. Например, для элемента он рассчитывается так: 1/В, где В – валентность элемента в том или ином соединении. Вот, например, основной оксид хрома – Cr2O3. В этом соединении хром имеет валентность, равную 3. Следовательно, его Фэ (фактор эквивалентности) равен 1/3. А если вы рассмотрите бихромат калия (он же – калий двухромовокислый), имеющий формулу K2Cr2O7, то здесь уже валентность хрома равна 6, следовательно, его Фэ будет составлять 1/6.
Если речь идет о простом веществе, то есть таком, молекулы которого состоят из атомов только одного элемента, то его фактор эквивалентности вычисляется по формуле 1/ВхN, где В – валентность элемента, а N – количество его атомов в молекуле. Легко можно увидеть, что, например, кислород и озон, хоть в их состав входит только один элемент, будут иметь разные Фэ. У кислорода, имеющего формулу молекулы О2, он будет равен 1/4, а у озона с формулой О3, соответственно, 1/6.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.