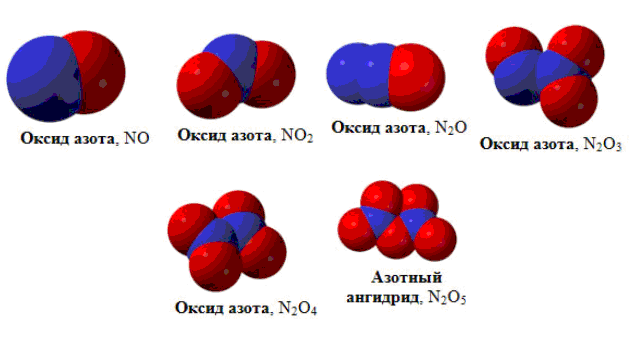
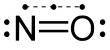Азот проявляет положительные степени окисления от (+1) до (+5) и образует соединения с кислородом:
N2O
— оксид азота((I)),
NO
— оксид азота((II)),
N2O3
— оксид азота((III)),
NO2
— оксид азота((IV)),
N2O5
— оксид азота((V)).
Первые четыре вещества при обычных условиях представляют собой газы, а
N2O5
— твёрдое вещество. Все оксиды азота ядовиты.
Бесцветный оксид азота((II)) образуется в реакции азота с кислородом при высоких температурах:
Этот оксид является также продуктом каталитического окисления аммиака:
Oксид азота((II)) легко окисляется при комнатной температуре. При этом образуется бурый газ с неприятным запахом — оксид азота((IV)):
Обрати внимание!
Оксид азота((I)) и оксид азота((II)) относятся к несолеобразующим оксидам. Они не реагируют с водой, кислотами и основаниями.
Другие оксиды являются солеобразующими (кислотными). Оксиду азота((III)) соответствует слабая азотистая кислота
HNO2
, оксиду азота((V)) — сильная азотная кислота
HNO3
. Oксид азота((IV)) при растворении в воде образует две кислоты одновременно — азотную и азотистую:
В присутствии кислорода реакция между оксидом азота((IV)) и водой протекает иначе, и образуется только азотная кислота:
Оксид азота((II)) и оксид азота((IV)) — промежуточные вещества при получении азотной кислоты.
ответы
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
похожие вопросы 5
Формула оксида азота
Определение и формула оксида азота
Известно несколько оксидов азота, в которых азот имеет разные степени окисления.
Оксид диазота
Химическая формула –
Молярная масса равна г/моль.
Другие названия — «Веселящий газ», закись азота.
Физические свойства – в обычных условиях бесцветный термически устойчивый газ.
Несолеобразующий оксид, слабый окислитель и слабый восстановитель.
Химические свойства оксида диазота
- При нагревании выше
разлагается на азот и кислород:
- Реагирует с металлами при нагревании
:
- Вступает в реакции окисления-восстановления:
Получение
Один из способов получения закиси азота основан на разложении нитрата аммония при :
Монооксид азота
Формула –
Молярная масса равна г/моль.
Физические свойства – бесцветный газ, голубая жидкость.
В твердом состоянии полностью димеризован, термически устойчивый.
Несолеобразующий оксид, слабый окислитель и слабый восстановитель, плохо растворяется в воде.
Химические свойства монооксида азота
- При нагревании выше
разлагается на азот и кислород:
- Реагирует с водородом при нагревании
:
- Вступает в реакции окисления-восстановления:
Получение
Один из способов получения закиси азота основан на взаимодействии аммиака с кислородом при в присутствии катализатора:
Триоксид азота
Формула –
Молярная масса равна г/моль.
Физические свойства – синяя жидкость, термически неустойчивая.
В твердом состоянии имеет голубоватый цвет.
Солеобразующий оксид.
Химические свойства триоксида азота
- При комнатной температуре разлагается на
и
:
- Реагирует с
с образованием нитрита натрия:
- Вступает в реакции окисления-восстановления:
Получение
Один из способов получения триоксида азота основан на взаимодействии диоксида азота с водой:
Диоксид азота
Формула –
Молярная масса равна г/моль.
Физические свойства – бурый газ, в жидком состоянии димер бесцветен, в твердом состоянии белый.
Хорошо растворяется в холодной воде и реагирует с ней.
Сильный окислитель.
Химические свойства диоксида азота
- При нагревании разлагается на
и
:
- Реагирует с
с образованием нитрита и нитрата натрия:
- Вступает в реакции окисления-восстановления:
Получение
Один из способов получения триоксида азота основан на взаимодействии диоксида азота с водой:
Пентаоксид азота
Формула –
Молярная масса равна г/моль.
Физические свойства – белое твердое вещество, бесцветный газ и бесцветная жидкость.
При нагревании возгоняется и плавится.
Солеобразующий оксид, ангидрид азотной кислоты.
Химические свойства пентаоксида азота
- При комнатной температуре за 10 часов разлагается на
и
:
- Реагирует с
с образованием нитрата натрия:
- Вступает в реакции окисления-восстановления:
Получение
Один из способов получения пентаоксида азота основан на взаимодействии реакции:
Примеры решения задач
From Wikipedia, the free encyclopedia
This article is about a molecule of one nitrogen atom and one oxygen atom. For other chemical combinations of nitrogen and oxygen, see nitrogen oxide. For the use of nitric oxide as a medication or in biology, see Biological functions of nitric oxide.

|
||
|
||
| Names | ||
|---|---|---|
| IUPAC name
Nitrogen monoxide[1] |
||
| Systematic IUPAC name
Oxidonitrogen(•)[2] (additive) |
||
| Other names
Nitrogen oxide |
||
| Identifiers | ||
|
CAS Number |
|
|
|
3D model (JSmol) |
|
|
| 3DMet |
|
|
| ChEBI |
|
|
| ChEMBL |
|
|
| ChemSpider |
|
|
| DrugBank |
|
|
| ECHA InfoCard | 100.030.233 |
|
| EC Number |
|
|
|
Gmelin Reference |
451 | |
|
IUPHAR/BPS |
|
|
| KEGG |
|
|
|
PubChem CID |
|
|
| RTECS number |
|
|
| UNII |
|
|
| UN number | 1660 | |
|
CompTox Dashboard (EPA) |
|
|
|
InChI
|
||
|
SMILES
|
||
| Properties | ||
|
Chemical formula |
NO | |
| Molar mass | 30.006 g·mol−1 | |
| Appearance | Colourless gas | |
| Density | 1.3402 g/L | |
| Melting point | −164 °C (−263 °F; 109 K) | |
| Boiling point | −152 °C (−242 °F; 121 K) | |
|
Solubility in water |
0.0098 g / 100 ml (0 °C) 0.0056 g / 100 ml (20 °C) |
|
|
Refractive index (nD) |
1.0002697 | |
| Structure | ||
|
Molecular shape |
linear (point group C∞v) | |
| Thermochemistry | ||
|
Std molar |
210.76 J/(K·mol) | |
|
Std enthalpy of |
90.29 kJ/mol | |
| Pharmacology | ||
|
ATC code |
R07AX01 (WHO) | |
| License data |
|
|
|
Routes of |
Inhalation | |
| Pharmacokinetics: | ||
|
Bioavailability |
good | |
|
Metabolism |
via pulmonary capillary bed | |
|
Biological half-life |
2–6 seconds | |
| Hazards | ||
| Occupational safety and health (OHS/OSH): | ||
|
Main hazards |
[4] |
|
| GHS labelling: | ||
|
Pictograms |
    [3][4] [3][4]
|
|
|
Signal word |
Danger | |
|
Hazard statements |
H270, H280, H314, H330[3][4] | |
|
Precautionary statements |
P220, P244, P260, P280, P303+P361+P353+P315, P304+P340+P315, P305+P351+P338+P315, P370+P376, P403, P405[3][4] | |
| NFPA 704 (fire diamond) |
3 0 3 OX |
|
| Lethal dose or concentration (LD, LC): | ||
|
LC50 (median concentration) |
315 ppm (rabbit, 15 min) 854 ppm (rat, 4 h) 2500 ppm (mouse, 12 min)[5] |
|
|
LCLo (lowest published) |
320 ppm (mouse)[5] | |
| Safety data sheet (SDS) | External SDS | |
| Related compounds | ||
|
Related nitrogen oxides |
Dinitrogen pentoxide
Dinitrogen tetroxide |
|
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Nitric oxide (nitrogen oxide or nitrogen monoxide[1]) is a colorless gas with the formula NO. It is one of the principal oxides of nitrogen. Nitric oxide is a free radical: it has an unpaired electron, which is sometimes denoted by a dot in its chemical formula (•N=O or •NO). Nitric oxide is also a heteronuclear diatomic molecule, a class of molecules whose study spawned early modern theories of chemical bonding.[6]
An important intermediate in industrial chemistry, nitric oxide forms in combustion systems and can be generated by lightning in thunderstorms. In mammals, including humans, nitric oxide is a signaling molecule in many physiological and pathological processes.[7] It was proclaimed the «Molecule of the Year» in 1992.[8] The 1998 Nobel Prize in Physiology or Medicine was awarded for discovering nitric oxide’s role as a cardiovascular signalling molecule.[9]
Nitric oxide should not be confused with nitrogen dioxide (NO2), a brown gas and major air pollutant, or with nitrous oxide (N2O), an anesthetic gas.[6]
Reactions[edit]
With di- and triatomic molecules[edit]
Upon condensing to a liquid, nitric oxide dimerizes to dinitrogen dioxide, but the association is weak and reversible. The N–N distance in crystalline NO is 218 pm, nearly twice the N–O distance.[6]
Since the heat of formation of •NO is endothermic, NO can be decomposed to the elements. Catalytic converters in cars exploit this reaction:
- 2 NO → O2 + N2
When exposed to oxygen, nitric oxide converts into nitrogen dioxide:
- 2 NO + O2 → 2 NO2
This reaction is thought to occur via the intermediates ONOO• and the red compound ONOONO.[10]
In water, nitric oxide reacts with oxygen to form nitrous acid (HNO2). The reaction is thought to proceed via the following stoichiometry:
- 4 NO + O2 + 2 H2O → 4 HNO2
Nitric oxide reacts with fluorine, chlorine, and bromine to form the nitrosyl halides, such as nitrosyl chloride:
- 2 NO + Cl2 → 2 NOCl
With NO2, also a radical, NO combines to form the intensely blue dinitrogen trioxide:[6]
- NO + NO2 ⇌ ON−NO2
Organic chemistry[edit]
The addition of a nitric oxide moiety to another molecule is often referred to as nitrosylation. The Traube reaction[11] is the addition of a two equivalents of nitric oxide onto an enolate, giving a diazeniumdiolate (also called a nitrosohydroxylamine).[12] The product can undergo a subsequent retro-aldol reaction, giving an overall process similar to the haloform reaction. For example, nitric oxide reacts with acetone and an alkoxide to form a diazeniumdiolate on each α position, with subsequent loss of methyl acetate as a by-product:[13]
This reaction, which was discovered around 1898, remains of interest in nitric oxide prodrug research. Nitric oxide can also react directly with sodium methoxide, ultimately forming sodium formate and nitrous oxide by way of an N-methoxydiazeniumdiolate.[14]
Coordination complexes[edit]
Nitric oxide reacts with transition metals to give complexes called metal nitrosyls. The most common bonding mode of nitric oxide is the terminal linear type (M−NO).[6] Alternatively, nitric oxide can serve as a one-electron pseudohalide. In such complexes, the M−N−O group is characterized by an angle between 120° and 140°. The NO group can also bridge between metal centers through the nitrogen atom in a variety of geometries.
Production and preparation[edit]
In commercial settings, nitric oxide is produced by the oxidation of ammonia at 750–900 °C (normally at 850 °C) with platinum as catalyst in the Ostwald process:
- 4 NH3 + 5 O2 → 4 NO + 6 H2O
The uncatalyzed endothermic reaction of oxygen (O2) and nitrogen (N2), which is effected at high temperature (>2000 °C) by lightning has not been developed into a practical commercial synthesis (see Birkeland–Eyde process):
- N2 + O2 → 2 NO
Laboratory methods[edit]
In the laboratory, nitric oxide is conveniently generated by reduction of dilute nitric acid with copper:
- 8 HNO3 + 3 Cu → 3 Cu(NO3)2 + 4 H2O + 2 NO
An alternative route involves the reduction of nitrous acid in the form of sodium nitrite or potassium nitrite:
- 2 NaNO2 + 2 NaI + 2 H2SO4 → I2 + 2 Na2SO4 + 2 H2O + 2 NO
- 2 NaNO2 + 2 FeSO4 + 3 H2SO4 → Fe2(SO4)3 + 2 NaHSO4 + 2 H2O + 2 NO
- 3 KNO2 + KNO3 + Cr2O3 → 2 K2CrO4 + 4 NO
The iron(II) sulfate route is simple and has been used in undergraduate laboratory experiments. So-called NONOate compounds are also used for nitric oxide generation.
Detection and assay[edit]
Nitric oxide (white) in conifer cells, visualized using DAF-2 DA (diaminofluorescein diacetate)
Nitric oxide concentration can be determined using a chemiluminescent reaction involving ozone.[15] A sample containing nitric oxide is mixed with a large quantity of ozone. The nitric oxide reacts with the ozone to produce oxygen and nitrogen dioxide, accompanied with emission of light (chemiluminescence):
- NO + O3 → NO2 + O2 + hν
which can be measured with a photodetector. The amount of light produced is proportional to the amount of nitric oxide in the sample.
Other methods of testing include electroanalysis (amperometric approach), where ·NO reacts with an electrode to induce a current or voltage change. The detection of NO radicals in biological tissues is particularly difficult due to the short lifetime and concentration of these radicals in tissues. One of the few practical methods is spin trapping of nitric oxide with iron-dithiocarbamate complexes and subsequent detection of the mono-nitrosyl-iron complex with electron paramagnetic resonance (EPR).[16][17]
A group of fluorescent dye indicators that are also available in acetylated form for intracellular measurements exist. The most common compound is 4,5-diaminofluorescein (DAF-2).[18]
Environmental effects[edit]
Main article: NOx
Acid rain deposition[edit]
Nitric oxide reacts with the hydroperoxyl radical (HO•
2) to form nitrogen dioxide (NO2), which then can react with a hydroxyl radical (•OH) to produce nitric acid (HNO3):
- •NO + HO•
2 → •NO2 + •OH - •NO2 + •OH → HNO3
Nitric acid, along with sulfuric acid, contributes to acid rain deposition.
Ozone depletion[edit]
•NO participates in ozone layer depletion. Nitric oxide reacts with stratospheric ozone to form O2 and nitrogen dioxide:
- •NO + O3 → NO2 + O2
This reaction is also utilized to measure concentrations of •NO in control volumes.
Precursor to NO2[edit]
As seen in the acid deposition section, nitric oxide can transform into nitrogen dioxide (this can happen with the hydroperoxy radical, HO•
2, or diatomic oxygen, O2). Symptoms of short-term nitrogen dioxide exposure include nausea, dyspnea and headache. Long-term effects could include impaired immune and respiratory function.[19]
Biological functions[edit]
NO is a gaseous signaling molecule.[20] It is a key vertebrate biological messenger, playing a role in a variety of biological processes.[21] It is a bioproduct in almost all types of organisms, including bacteria, plants, fungi, and animal cells.[22]
Nitric oxide, an endothelium-derived relaxing factor (EDRF), is biosynthesized endogenously from L-arginine, oxygen, and NADPH by various nitric oxide synthase (NOS) enzymes.[23] Reduction of inorganic nitrate may also make nitric oxide.[24] One of the main enzymatic targets of nitric oxide is guanylyl cyclase.[25] The binding of nitric oxide to the heme region of the enzyme leads to activation, in the presence of iron.[25] Nitric oxide is highly reactive (having a lifetime of a few seconds), yet diffuses freely across membranes. These attributes make nitric oxide ideal for a transient paracrine (between adjacent cells) and autocrine (within a single cell) signaling molecule.[24] Once nitric oxide is converted to nitrates and nitrites by oxygen and water, cell signaling is deactivated.[25]
The endothelium (inner lining) of blood vessels uses nitric oxide to signal the surrounding smooth muscle to relax, resulting in vasodilation and increasing blood flow.[24] Sildenafil (Viagra) is a drug that uses the nitric oxide pathway. Sildenafil does not produce nitric oxide, but enhances the signals that are downstream of the nitric oxide pathway by protecting cyclic guanosine monophosphate (cGMP) from degradation by cGMP-specific phosphodiesterase type 5 (PDE5) in the corpus cavernosum, allowing for the signal to be enhanced, and thus vasodilation.[23] Another endogenous gaseous transmitter, hydrogen sulfide (H2S) works with NO to induce vasodilation and angiogenesis in a cooperative manner.[26][27]
Nasal breathing produces nitric oxide within the body, while oral breathing does not.[28][29]
Occupational safety and health[edit]
In the U.S., the Occupational Safety and Health Administration (OSHA) has set the legal limit (permissible exposure limit) for nitric oxide exposure in the workplace as 25 ppm (30 mg/m3) over an 8-hour workday. The National Institute for Occupational Safety and Health (NIOSH) has set a recommended exposure limit (REL) of 25 ppm (30 mg/m3) over an 8-hour workday. At levels of 100 ppm, nitric oxide is immediately dangerous to life and health.[30]
Explosion hazard[edit]
Liquid nitrogen oxide is very sensitive to detonation even in the absence of fuel, and can be initiated as readily as nitroglycerin. Detonation of the endothermic liquid oxide close to its b.p. (-152°C) generated a 100 kbar pulse and fragmented the test equipment. It is the simplest molecule that is capable of detonation in all three phases. The liquid oxide is sensitive and may explode during distillation, and this has been the cause of industrial accidents.[31] Gaseous nitric oxide detonates at about 2300 m/s, but as a solid it can reach a detonation velocity of 6100 m/s.[32]
References[edit]
Notes
- ^ a b Nomenclature of Inorganic Chemistry, IUPAC Recommendations (PDF). International Union of Pure and Applied Chemistry. 2005. p. 69.
- ^ «Nitric Oxide (CHEBI:16480)». Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ^ a b c «Nitrogen monoxide — Registration Dossier — ECHA». Retrieved 2020-11-02.
- ^ a b c d «Safety Data Sheet — Nitric Oxide, compressed — Registration Dossier» (PDF). Retrieved 2020-11-02.
- ^ a b «Nitric oxide». Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ a b c d e Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Hou, Y. C.; Janczuk, A.; Wang, P. G. (1999). «Current trends in the development of nitric oxide donors». Current Pharmaceutical Design. 5 (6): 417–441. doi:10.2174/138161280506230110111042. PMID 10390607.
- ^ Culotta, Elizabeth; Koshland, Daniel E. Jr. (1992). «NO news is good news». Science. 258 (5090): 1862–1864. Bibcode:1992Sci…258.1862C. doi:10.1126/science.1361684. PMID 1361684.
- ^ «The Nobel Prize in Physiology or Medicine 1998». NobelPrize.org. Retrieved 2022-06-17.
- ^ Galliker, Benedikt; et al. (2009). «Intermediates in the Autoxidation of Nitrogen Monoxide». Chemistry — A European Journal. 15 (25): 6161–6168. doi:10.1002/chem.200801819. ISSN 0947-6539. PMID 19437472.
- ^
- ^ Arulsamy, Navamoney; Bohle, D. Scott (2006). «Synthesis of Diazeniumdiolates from the Reactions of Nitric Oxide with Enolates». J. Org. Chem. 71 (2): 572–581. doi:10.1021/jo051998p. PMID 16408967.
- ^ Traube, Wilhelm (1898). «Ueber Synthesen stickstoffhaltiger Verbindungen mit Hülfe des Stickoxyds». Justus Liebig’s Annalen der Chemie (in German). 300: 81–128. doi:10.1002/jlac.18983000108.
- ^ Derosa, Frank; Keefer, Larry K.; Hrabie, Joseph A. (2008). «Nitric Oxide Reacts with Methoxide». The Journal of Organic Chemistry. 73 (3): 1139–1142. doi:10.1021/jo7020423. PMID 18184006.
- ^ Fontijn, Arthur; Sabadell, Alberto J.; Ronco, Richard J. (1970). «Homogeneous chemiluminescent measurement of nitric oxide with ozone. Implications for continuous selective monitoring of gaseous air pollutants». Analytical Chemistry. 42 (6): 575–579. doi:10.1021/ac60288a034.
- ^ Vanin, A; Huisman, A; Van Faassen, E (2002). Iron dithiocarbamate as spin trap for nitric oxide detection: Pitfalls and successes. Methods in Enzymology. Vol. 359. pp. 27–42. doi:10.1016/S0076-6879(02)59169-2. ISBN 9780121822620. PMID 12481557.
- ^ Nagano, T; Yoshimura, T (2002). «Bioimaging of nitric oxide». Chemical Reviews. 102 (4): 1235–1270. doi:10.1021/cr010152s. PMID 11942795.
- ^ Kojima H, Nakatsubo N, Kikuchi K, Kawahara S, Kirino Y, Nagoshi H, Hirata Y, Nagano T (1998). «Detection and imaging of nitric oxide with novel fluorescent indicators: diaminofluoresceins». Anal. Chem. 70 (13): 2446–2453. doi:10.1021/ac9801723. PMID 9666719.
- ^ «Centers for Disease Control and Prevention». NIOSH. 1 July 2014. Retrieved 10 December 2015.
- ^ Liu, Hongying; Weng, Lingyan; Yang, Chi (2017-03-28). «A review on nanomaterial-based electrochemical sensors for H2O2, H2S and NO inside cells or released by cells». Microchimica Acta. 184 (5): 1267–1283. doi:10.1007/s00604-017-2179-2. ISSN 0026-3672. S2CID 21308802.
- ^ Weller, Richard, Could the sun be good for your heart? TedxGlasgow. Filmed March 2012, posted January 2013
- ^ Roszer, T (2012) The Biology of Subcellular Nitric Oxide. ISBN 978-94-007-2818-9
- ^ a b Perez, Krystle M.; Laughon, Matthew (November 2015). «Sildenafil in Term and Premature Infants: A Systematic Review». Clinical Therapeutics. 37 (11): 2598–2607.e1. doi:10.1016/j.clinthera.2015.07.019. ISSN 0149-2918. PMID 26490498.
- ^ a b c Stryer, Lubert (1995). Biochemistry (4th ed.). W.H. Freeman and Company. p. 732. ISBN 978-0-7167-2009-6.
- ^ a b c T., Hancock, John (2010). Cell signalling (3rd ed.). Oxford: Oxford University Press. ISBN 9780199232109. OCLC 444336556.
- ^ Szabo, Csaba; Coletta, Ciro; Chao, Celia; Módis, Katalin; Szczesny, Bartosz; Papapetropoulos, Andreas; Hellmich, Mark R. (2013-07-23). «Tumor-derived hydrogen sulfide, produced by cystathionine-β-synthase, stimulates bioenergetics, cell proliferation, and angiogenesis in colon cancer». Proceedings of the National Academy of Sciences of the United States of America. 110 (30): 12474–12479. Bibcode:2013PNAS..11012474S. doi:10.1073/pnas.1306241110. ISSN 1091-6490. PMC 3725060. PMID 23836652.
- ^ Altaany, Zaid; Yang, Guangdong; Wang, Rui (July 2013). «Crosstalk between hydrogen sulfide and nitric oxide in endothelial cells». Journal of Cellular and Molecular Medicine. 17 (7): 879–888. doi:10.1111/jcmm.12077. ISSN 1582-4934. PMC 3822893. PMID 23742697.
- ^ Yasuda, Yoshifumi; Itoh, Tomonori; Miyamura, Miharu; Nishino, Hitoo (1997). «Comparison of Exhaled Nitric Oxide and Cardiorespiratory Indices between Nasal and Oral Breathing during Submaximal Exercise in Humans». Japanese Journal of Physiology. 47 (5): 465–470. doi:10.2170/jjphysiol.47.465. ISSN 0021-521X. PMID 9504133. Retrieved 2022-11-17.
- ^ Dahl, Melissa (2011-01-11). «‘Mouth-breathing’ gross, harmful to your health». NBC News. Retrieved 2021-09-06.
{{cite web}}: CS1 maint: url-status (link) - ^ «Nitric oxide». National Institute for Occupational Safety and Health. Retrieved 2015-11-20.
- ^ «Bretherick’s Handbook of Reactive Chemical Hazards | ScienceDirect». www.sciencedirect.com. Retrieved 2022-02-23.
- ^ Ribovich, John; Murphy, John; Watson, Richard (1975-01-01). «Detonation studies with nitric oxide, nitrous oxide, nitrogen tetroxide, carbon monoxide, and ethylene». Journal of Hazardous Materials. 1 (4): 275–287. doi:10.1016/0304-3894(75)80001-X. ISSN 0304-3894.
Further reading
- Butler A. and Nicholson R.; «Life, death and NO.» Cambridge 2003. ISBN 978-0-85404-686-7.
- van Faassen, E. E.; Vanin, A. F. (eds); «Radicals for life: The various forms of Nitric Oxide.» Elsevier, Amsterdam 2007. ISBN 978-0-444-52236-8.
- Ignarro, L. J. (ed.); «Nitric oxide:biology and pathobiology.» Academic Press, San Diego 2000. ISBN 0-12-370420-0.
External links[edit]
- International Chemical Safety Card 1311
- «Nitric oxide and its role in health and diabetes». 21 October 2015.
- Microscale Gas Chemistry: Experiments with Nitrogen Oxides
- Your Brain Boots Up Like a Computer – new insights about the biological role of nitric oxide.
- Assessing The Potential of Nitric Oxide in the Diabetic Foot
- New Discoveries About Nitric Oxide Can Provide Drugs For Schizophrenia
- Nitric Oxide at the Chemical Database
- «Immediately Dangerous to Life or Health Concentrations (IDLH): Nitric oxide». National Institute for Occupational Safety and Health. 2 November 2018.
1. Положение азота в периодической системе химических элементов
2. Строение атома азота
3. Физические свойства и нахождение в природе
4. Строение молекулы
5. Соединения азота
6. Способы получения
7. Химические свойства
7.1. Взаимодействие с простыми веществами
7.1.1. Взаимодействие с галогенами
7.1.2. Взаимодействие с серой и кремнием
7.1.3. Взаимодействие с водородом и фосфором
7.1.4. Взаимодействие с азотом
7.1.5. Взаимодействие с активными металлами
Аммиак
1. Строение молекулы и физические свойства
2. Способы получения
3. Химические свойства
3.1. Взаимодействие с серной кислотой
3.2. Взаимодействие с азотной кислотой
3.3. Взаимодействие с солями
Соли аммония
Способы получения солей аммония
Химические свойства солей аммония
Оксиды азота
1. Оксид азота (I)
2. Оксид азота (II)
3. Оксид азота (III)
4. Оксид азота (IV)
5. Оксид азота (V)
Азотная кислота
1. Строение молекулы и физические свойства
2. Способы получения
3. Химические свойства
3.1. Диссоциация азотной кислоты
2.3. Взаимодействие с основными и амфотерными оксидами и гидроксидами
2.4. Вытеснение более слабых кислот из солей
2.5. Взаимодействие с металлами
2.6. Взаимодействие с неметаллами
2.7. Окисление сложных веществ
2.8. Взаимодействие с белками
Азотистая кислота
Соли азотной кислоты — нитраты
Соли азотистой кислоты — нитриты
Азот
Положение в периодической системе химических элементов
Азот расположен в главной подгруппе V группы (или в 15 группе в современной форме ПСХЭ) и во втором периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение азота
Электронная конфигурация азота в основном состоянии:
Атом азота содержит на внешнем энергетическом уровне 3 неспаренных электрона и одну неподеленную электронную пару в основном энергетическом состоянии. Следовательно, атом азота может образовать 3 связи по обменному механизму и 1 связь по донорно-акцепторному механизму. Таким образом, максимальная валентность азота в соединениях равна IV. Также характерная валентность азота в соединениях — III.
Степени окисления атома азота – от -3 до +5. Характерные степени окисления азота -3, 0, +1, +2, +3, +4, +5.
Физические свойства и нахождение в природе
Азот в природе существует в виде простого вещества газа N2. Нет цвета, запаха и вкуса. Молекула N2 неполярная, следовательно, в воде азот практически нерастворим.
Азот – это основной компонент воздуха (79% по массе). В земной коре азот встречается в основном в виде нитратов. Входит в состав белков, аминокислот и нуклеиновых кислот в живых организмах.
Строение молекулы
Связь между атомами в молекуле азота – тройная, т.к. у каждого атома в молекуле по 3 неспаренных электрона. Одна σ-связь (сигма-связь) и две — π-связи.
Структурная формула молекулы азота:
Структурно-графическая формула молекулы азота: N≡N.
Схема перекрывания электронных облаков при образовании молекулы азота:
Соединения азота
Типичные соединения азота:
| Степень окисления | Типичные соединения |
| +5 | оксид азота (V) N2O5
азотная кислота HNO3 нитраты MeNO3 |
| +4 | оксид азота (IV) NO2 |
| +3 | оксид азота (III)
азотистая кислота нитриты MeNO2 |
| +2 | оксид азота (II) NO |
| +1 | оксид азота (I) |
| -3 | аммиак NH3
нитриды металлов MeN бинарные соединения азота с неметаллами |
Способы получения азота
1. Азот в лаборатории получают при взаимодействии насыщенных растворов хлорида аммония и нитрита натрия. Образующийся в результате реакции обмена нитрит аммония легко разлагается с образованием азота и воды. В колбу наливают раствор хлорида аммония, а капельную воронку раствор нитрита натрия. При приливании нитрита натрия в колбу начинается выделение азота. Собирают выделяющийся азот в цилиндр. Горящая лучинка в атмосфере азота гаснет.
NaNO2 + NH4Cl → NH4NO2 + NaCl
NH4NO2 → N2 + 2H2O
Суммарное уравнение процесса:
NaNO2 + NH4Cl → N2 + NaCl + 2H2O
Видеоопыт взаимодействия нитрита натрия с хлоридом аммония можно посмотреть здесь.
Азот также образуется при горении аммиака:
4NH3 + 3O2 → 2N2 + 6H2O
2. Наиболее чистый азот получают разложением азидов щелочных металлов.
Например, разложением азида натрия:
2NaN3 → 2Na + 3N2
3. Еще один лабораторный способ получения азота — восстановление оксида меди (II) аммиаком при температуре ~700 °C:
3CuO + 2NH3 → 3Cu + N2 + 3H2O
В промышленности азот получают, буквально, из воздуха. При промышленном производстве очень важно, чтобы сырье было дешевым и доступным. Воздуха много и он пока бесплатный.
Используются различные способы выделения азота из воздуха — адсорбционная технология, мембранная и криогенная технологии.
Адсорбционные методы разделения воздуха на компоненты основаны на разделения газовых сред в азотных установках лежит явление связывания твёрдым веществом, называемым адсорбентом, отдельных компонентов газовой смеси.
Основным принципом работы мембранных систем является разница в скорости проникновения компонентов газа через вещество мембраны. Движущей силой разделения газов является разница парциальных давлений на различных сторонах мембраны.
В основе работы криогенных установок разделения воздуха лежит метод разделения газовых смеси, основанный на разности температур кипения компонентов воздуха и различии составов находящихся в равновесии жидких и паровых смесей.
Химические свойства азота
При нормальных условиях азот химически малоактивен.
1. Азот проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому азот реагирует с металлами и неметаллами.
1.1. Молекулярный азот при обычных условиях с кислородом не реагирует. Реагирует с кислородом только при высокой температуре (2000оС), на электрической дуге (в природе – во время грозы):
N2 + O2 ⇄ 2NO – Q
Процесс эндотермический, т.е. протекает с поглощением теплоты.
1.2. При сильном нагревании (3000оС-5000оС или действие электрического разряда) образуется атомарный азот, который реагирует с серой, фосфором, мышьяком, углеродом с образованием бинарных соединений:
2С + N2 → N≡C–C≡N
Молекулярный азот, таким образом, не реагирует с серой, фосфором, мышьяком, углеродом.
1.3. Азот взаимодействует с водородом при высоком давлении и высокой температуре, в присутствии катализатора. При этом образуется аммиак:
N2 + ЗН2 ⇄ 2NH3
Этот процесс экзотермический, т.е. протекает с выделением теплоты.
1.4. Азот реагирует с активными металлами: с литием при комнатной температуре, кальцием, натрием и магнием при нагревании. При этом образуются бинарные соединения-нитриды.
Например, литий реагирует с азотом с образованием нитрида лития:
N2 + 6Li → 2Li3N
2. Со сложными веществами азот практически не реагирует из-за крайне низкой реакционной способности.
Взаимодействие возможно только в жестких условиях с активными веществами, например, сильными восстановителями.
Например, азот окисляет гидрид лития:
N2 + 3LiH → Li3N + NH3
Аммиак
Строение молекулы и физические свойства
В молекуле аммиака NH3 атом азота соединен тремя одинарными ковалентными полярными связями с атомами водорода:
Геометрическая форма молекулы аммиака — правильная треугольная пирамида. Валентный угол H-N-H составляет 107,3о:
У атома азота в аммиаке на внешнем энергетическом уровне остается одна неподеленная электронная пара. Эта электронная пара оказывает значительное влиение на свойства аммиака, а также на его структуру. Электронная структура аммиака — тетраэдр , с атомом азота в центре:
Аммиак – бесцветный газ с резким характерным запахом. Ядовит. Весит меньше воздуха. Связь N-H — сильно полярная, поэтому между молекулами аммиака в жидкой фазе возникают водородные связи. При этом аммиак очень хорошо растворим в воде, т.к. молекулы аммиака образуют водородные связи с молекулами воды.
Способы получения аммиака
В лаборатории аммиак получают при взаимодействии солей аммония с щелочами. Поск
ольку аммиак очень хорошо растворим в воде, для получения чистого аммиака используют твердые вещества.
Например, аммиак можно получить нагреванием смеси хлорида аммония и гидроксида кальция. При нагревании смеси происходит образование соли, аммиака и воды:
2NH4Cl + Са(OH)2 → CaCl2 + 2NH3 + 2Н2O
Тщательно растирают ступкой смесь соли и основания и нагревают смесь. Выделяющийся газ собирают в пробирку (аммиак — легкий газ и пробирку нужно перевернуть вверх дном). Влажная лакмусовая бумажка синеет в присутствии аммиака.
Видеоопыт получения аммиака из хлорида аммония и гидроксида кальция можно посмотреть здесь.
Еще один лабораторный способ получения аммиака – гидролиз нитридов.
Например, гидролиз нитрида кальция:
Ca3N2 + 6H2O → ЗСа(OH)2 + 2NH3
В промышленности аммиак получают с помощью процесса Габера: прямым синтезом из водорода и азота.
N2 + 3Н2 ⇄ 2NH3
Процесс проводят при температуре 500-550оС и в присутствии катализатора. Для синтеза аммиака применяют давления 15-30 МПа. В качестве катализатора используют губчатое железо с добавками оксидов алюминия, калия, кальция, кремния. Для полного использования исходных веществ применяют метод циркуляции непровзаимодействовавших реагентов: не вступившие в реакцию азот и водород вновь возвращают в реактор.
Более подробно про технологию производства аммиака можно прочитать здесь.
Химические свойства аммиака
1. В водном растворе аммиак проявляет основные свойства (за счет неподеленной электронной пары). Принимая протон (ион H+), он превращается в ион аммония. Реакция может протекать и в водном растворе, и в газовой фазе:
:NH3 + H2O ⇄ NH4+ + OH–
Таким образом, среда водного раствора аммиака – щелочная. Однако аммиак – слабое основание. При 20 градусах один объем воды поглощает до 700 объемов аммиака.
Видеоопыт растворения аммиака в воде можно посмотреть здесь.
2. Как основание, аммиак взаимодействует с кислотами в растворе и в газовой фазе с образованием солей аммония.
Например, аммиак реагирует с серной кислотой с образованием либо кислой соли – гидросульфата аммония (при избытке кислоты), либо средней соли – сульфата аммония (при избытке аммиака):
NH3 + H2SO4 → NH4HSO4
2NH3 + H2SO4 → (NH4)2SO4
Еще один пример: аммиак взаимодействует с водным раствором углекислого газа с образованием карбонатов или гидрокарбонатов аммония:
NH3 + H2O + CO2 → NH4HCO3
2NH3 + H2O + CO2 → (NH4)2CO3
Видеоопыт взаимодействия аммиака с концентрированными кислотами – азотной, серной и и соляной можно посмотреть здесь.
В газовой фазе аммиак реагирует с летучим хлороводородом. При этом образуется густой белый дым – это выделяется хлорид аммония.
NH3 + HCl → NH4Cl
Видеоопыт взаимодействия аммиака с хлороводородом в газовой фазе (дым без огня) можно посмотреть здесь.
3. В качестве основания, водный раствор аммиака реагирует с растворами солей тяжелых металлов, образуя нерастворимые гидроксиды.
Например, водный раствор аммиака реагирует с сульфатом железа (II) с образованием сульфата аммония и гидроксида железа (II):
FeSO4 + 2NH3 + 2H2O → Fe(OH)2 + (NH4)2SO4
4. Соли и гидроксиды меди, никеля, серебра растворяются в избытке аммиака, образуя комплексные соединения – амминокомплексы.
Например, хлорид меди (II) реагирует с избытком аммиака с образованием хлорида тетрамминомеди (II):
4NH3 + CuCl2 → [Cu(NH3)4]Cl2
Гидроксид меди (II) растворяется в избытке аммиака:
4NH3 + Cu(OH)2 → [Cu(NH3)4](OH)2
5. Аммиак горит на воздухе, образуя азот и воду:
4NH3 + 3O2 → 2N2 + 6H2O
Если реакцию проводить в присутствии катализатора (Pt), то азот окисляется до NO:
4NH3 + 5O2 → 4NO + 6H2O
6. За счет атомов водорода в степени окисления +1 аммиак может выступать в роли окислителя, например в реакциях с щелочными, щелочноземельными металлами, магнием и алюминием. С металлами реагирует только жидкий аммиак.
Например, жидкий аммиак реагирует с натрием с образованием амида натрия:
2NH3 + 2Na → 2NaNH2 + H2
Также возможно образование Na2NH, Na3N.
При взаимодействии аммиака с алюминием образуется нитрид алюминия:
2NH3 + 2Al → 2AlN + 3H2
7. За счет азота в степени окисления -3 аммиак проявляет восстановительные свойства. Может взаимодействовать с сильными окислителями — хлором, бромом, пероксидом водорода, пероксидами и оксидами некоторых металлов. При этом азот окисляется, как правило, до простого вещества.
Например, аммиак окисляется хлором до молекулярного азота:
2NH3 + 3Cl2 → N2 + 6HCl
Пероксид водорода также окисляет аммиак до азота:
2NH3 + 3H2O2 → N2 + 6H2O
Оксиды металлов, которые в электрохимическом ряду напряжений металлов расположены справа — сильные окислители. Поэтому они также окисляют аммиак до азота.
Например, оксид меди (II) окисляет аммиак:
2NH3 + 3CuO → 3Cu + N2 + 3H2O
Соли аммония
Соли аммония – это соли, состоящие из катиона аммония и аниона кислотного остатка.
Способы получения солей аммония
1. Соли аммония можно получить взаимодействием аммиака с кислотами. Реакции подробно описаны выше.
2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями.
Например, хлорид аммония реагирует с нитратом серебра:
NH4Cl + AgNO3 → AgCl + NH4NO3
3. Средние соли аммония можно получить из кислых солей аммония. При добавлении аммиака кислая соль переходит в среднюю.
Например, гидрокарбонат аммония реагирует с аммиаком с образованием карбоната аммония:
NH4НCO3 + NH3 → (NH4)2CO3
Химические свойства солей аммония
1. Все соли аммония – сильные электролиты, почти полностью диссоциируют на ионы в водных растворах:
NH4Cl ⇄ NH4+ + Cl–
2. Соли аммония проявляют свойства обычных растворимых солей –вступают в реакции обмена с щелочами, кислотами и растворимыми солями, если в продуктах образуется газ, осадок или образуется слабый электролит.
Например, карбонат аммония реагирует с соляной кислотой. При этом выделяется углекислый газ:
(NH4)2CO3 + 2НCl → 2NH4Cl + Н2O + CO2
Соли аммония реагируют с щелочами с образованием аммиака.
Например, хлорид аммония реагирует с гидроксидом калия:
NH4Cl + KOH → KCl + NH3 + H2O
Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки.
3. Соли аммония подвергаются гидролизу по катиону, т.к. гидроксид аммония — слабое основание:
NH4Cl + Н2O ↔ NH3 ∙ H2O + HCl
NH4+ + HOH ↔ NH3 ∙ H2O + H+
4. При нагревании соли аммония разлагаются. При этом если соль не содержит анион-окислителя, то разложение проходит без изменения степени окисления атома азота. Так разлагаются хлорид, карбонат, сульфат, сульфид и фосфат аммония:
NH4Cl → NH3 + HCl
NH4HCO3 → NH3 + CO2 + H2O
(NH4)2SO4 → NH4HSO4 + NH3
NH4HS → NH3 + H2S
Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония:
NH4NO2 → N2 + 2H2O
190 – 245° C:
NH4NO3 → N2O + 2H2O
При температуре 250 – 300°C:
2NH4NO3 → 2NO + 4H2O
При температуре выше 300°C:
2NH4NO3 → 2N2 + O2 + 4H2O
Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР):
(NH4)2Cr2O7 → Cr2O3 + N2 + 4H2O
Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Видеоопыт разложения дихромата аммония можно посмотреть здесь.
Оксиды азота
| Оксиды азота | Цвет | Фаза | Характер оксида |
| N2O Оксид азота (I), закись азота, «веселящий газ» | бесцветный | газ | несолеобразующий |
| NO Оксид азота (II) | бесцветный | газ | несолеобразующий |
| N2O3 Оксид азота (III), азотистый ангидрид | синий | жидкость | кислотный |
| NO2 Оксид азота (IV), диоксид азота, «лисий хвост» | бурый | газ | кислотный (соответствуют две кислоты) |
| N2O5 Оксид азота (V), азотный ангидрид | бесцветный | твердый | кислотный |
Оксид азота (I)
Оксид азота (I) – это несолеобразующий оксид. Малые концентрации закиси азота вызывают лёгкое опьянение (отсюда название — «веселящий газ»). При вдыхании чистого газа быстро развиваются состояние опьянения и сонливость. Закись азота обладает слабой наркотической активностью, в связи с чем в медицине её применяют в больших концентрациях. В смеси с кислородом при правильном дозировании (до 80 % закиси азота) вызывает хирургический наркоз.
Строение молекулы оксида азота (I) нельзя описать методом валентных связей. Так как оксид азота (I) состоит из двух, так называемых резонансных структур, которые переходят одна в другую:
Общую формулу в таком случае можно задать, обозначая изменяющиеся связи в резонансных структурах пунктиром:
Получить оксид азота (I) в лаборатории можно разложением нитрата аммония:
NH4NO3 → N2O + 2H2O
Химические свойства оксида азота (I):
1. При нормальных условиях оксид азота (I) инертен. При нагревании проявляет свойства окислителя. Оксид азота (I) при нагревании окисляет водород, аммиак, металлы, сернистый газ и др. При этом азот восстанавливается в простое вещество.
N2O + H2 → N2 + H2O
N2O + Mg → N2 + MgO
N2O + 2Cu → N2 + Cu2O
3N2O + 2NH3 → 4N2 + 3H2O
N2O + H2O + SO2 → N2 + H2SO4
Еще пример: оксид азота (I) окисляет углерод и фосфор при нагревании:
N2O + C → N2 + CO
5N2O + 2Р → 5N2 + Р2O5
2. При взаимодействии с сильными окислителями N2O может проявлять свойства восстановителя.
Например, N2O окисляется раствором перманганата в серной кислоте:
5N2O + 3H2SO4 + 2KMnO4 → 10NO + 2MnSO4 + K2SO4 + 3H2O
Оксид азота (II)
Оксид азота (II) – это несолеобразующий оксид. В нормальных условиях это бесцветный ядовитый газ, плохо растворимый в воде. На воздухе коричневеет из-за окисления до диоксида азота. Сжижается с трудом; в жидком и твёрдом виде имеет голубой цвет.
Способы получения.
1. В лаборатории оксид азота (II) получают действием разбавленной азотной кислоты (30%) на неактивные металлы.
Например, при действии 30 %-ной азотной кислоты на медь образуется NO:
3Cu + 8HNO3(разб.) → 3Cu(NO3)2 + 2NO + 4H2O
Также NO можно получить при окислении хлорида железа (II) или иодоводорода азотной кислотой:
3FeCl2 + NaNO3 + 4HCl → 3FeCl3 + NaCl + NO + 2H2O
2HNO3 + 6HI → 2NO + I2 + 4H2O
2. В природе оксид азота (II) образуется из азота и кислорода под действием электрического разряда, например, во время грозы:
N2 + O2 → 2NO
3. В промышленности оксид азота (II) получают каталитическим окислением аммиака:
4NH3 + 5O2 → 4NO + 6H2O
Химические свойства.
1. Оксид азота (II) легко окисляется под действием окислителей.
Например, горит в атмосфере кислорода:
2NO + O2 → 2NO2
Оксид азота (II) легко окисляется под действием хлора или озона:
2NO + Cl2 → 2NOCl
NO + O3 → NO2 + O2
2. В присутствии более сильных восстановителей проявляет свойства окислителя. В атмосфере оксида азота (II) могут гореть водород, углерод и т.п.
Например, оксид азота (II) окисляет водород и сернистый газ:
2NO + 2H2 → N2 + 2H2O
2NO + 2SO2 → 2SO3 + N2
Оксид азота (III)
Оксид азота (III), азотистый ангидрид – кислотный оксид. За счет азота со степенью окисления +3 проявляет восстановительные и окислительные свойства. Устойчив только при низких температурах, при более высоких температурах разлагается.
Способы получения: можно получить при низкой температуре из оксидов азота:
NO2 + NO ↔ N2O3
Химические свойства:
1. Оксид азота (III) взаимодействует с водой с образованием азотистой кислоты:
N2O3 + H2O ↔ 2HNO2
2. Оксид азота (III) взаимодействует с основаниями и основными оксидами:
Например, оксид азота (III) реагирует с гидроксидом и оксидом натрия с образованием нитрита натрия и воды:
N2O3 + 2NaOH → 2NaNO2 + H2O
N2O3 + Na2O → 2NaNO2
Оксид азота (IV)
Оксид азота (IV) — бурый газ. Очень ядовит! Для NO2 характерна высокая химическая активность.
Способы получения.
1. Оксид азота (IV) образуется при окислении оксида азота (I) и оксида азота (II) кислородом или озоном:
2NO + O2 → 2NO2
2. Оксид азота (IV) образуется при действии концентрированной азотной кислоты на неактивные металлы.
Например, при действии концентрированной азотной кислоты на медь:
4HNO3(конц.) + Cu → Cu(NO3)2 + 2NO2 + 2H2O
3. Оксид азота (IV) образуется также при разложении нитратов металлов, которые в ряду электрохимической активности расположены правее магния (включая магний) и при разложении нитрата лития.
Например, при разложении нитрата серебра:
2AgNO3 → 2Ag + 2NO2 + O2
Химические свойства.
1. Оксид азота (IV) реагирует с водой с образованием двух кислот — азотной и азотистой:
2NO2 + H2O → HNO3 + HNO2
Если растворение NO2 в воде проводить в избытке кислорода, то образуется только азотная кислота:
4NO2 + 2H2O + O2 → 4HNO3
Поскольку азотистая кислота неустойчива, то при растворении NO2 в теплой воде образуются HNO3 и NO:
3NO2 + H2O → 2HNO3 + NO
2. При растворении оксида азота (IV) в щелочах образуются нитраты и нитриты:
2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O
4NO2 + 2Ca(OH)2 → Ca(NO2)2 + Ca(NO3)2 + 2H2O
В присутствии кислорода образуются только нитраты:
4NO2 + 4NaOH + O2 → 4NaNO3 + 2H2O
3. Оксид азота (IV) – сильный окислитель. В атмосфере оксида азота (IV) горят фосфор, уголь, сера, оксид серы (IV) окисляется до оксида серы (VI):
2NO2 + 2S → N2 + 2SO2
2NO2 + 2C → N2 + 2CO2
10NO2 + 8P → 5N2 + 4P2O5
NO2 + SO2 → SO3 + NO
4. Оксид азота (IV) димеризуется:
2NO2 ⇄ N2O4
Оксид азота (V)
N2O5 – оксид азота (V), ангидрид азотной кислоты – кислотный оксид.
Получение оксида азота (V).
1. Получить оксид азота (V) можно окислением диоксида азота:
2NO2 + O3 → N2O5 + O2
2. Еще один способ получения оксида азота (V) – обезвоживание азотной кислоты сильным водоотнимающим веществом, оксидом фосфора (V):
2HNO3 + P2O5 → 2HPO3 + N2O5
Химические свойства оксида азота (V).
1. При растворении в воде оксид азота (V) образует азотную кислоту:
N2O5 + H2O → 2HNO3
2. Оксид азота (V), как типичный кислотный оксид, взаимодействует с основаниями и основными оксидами с образованием солей-нитратов.
Например, оксид азота (V) реагирует с гидроксидом натрия:
N2O5 + 2NaOH → 2NaNO3 + H2O
Еще пример: оксид азота (V) реагирует с оксидом кальция:
N2O5 + CaO → Ca(NO3)2
3. За счет азота со степенью окисления +5 оксид азота (V) – сильный окислитель.
Например, он окисляет серу:
2N2O5 + S → SO2 + 4NO2
4. Оксид азота (V) легко разлагается при нагревании (со взрывом):
2N2O5 → 4NO2 + O2
Азотная кислота
Строение молекулы и физические свойства
Азотная кислота HNO3 – это сильная одноосновная кислота-гидроксид. При обычных условиях бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении). Азотная кислота смешивается с водой во всех соотношениях. На свету частично разлагается.
Валентность азота в азотной кислоте равна IV, так как валентность V у азота отсутствует. При этом степень окисления атома азота равна +5. Так происходит потому, что атом азота образует 3 обменные связи и одну донорно-акцепторную, является донором электронной пары.
Поэтому строение молекулы азотной кислоты можно описать резонансными структурами:
Обозначим дополнительные связи между азотом и кислородом пунктиром. Этот пунктир по сути обозначает делокализованные электроны. Получается формула:
Способы получения
В лаборатории азотную кислоту можно получить разными способами:
1. Азотная кислота образуется при действии концентрированной серной кислоты на твердые нитраты металлов. При этом менее летучая серная кислота вытесняет более летучую азотную.
Например, концентрированная серная кислота вытесняет азотную из кристаллического нитрата калия:
KNO3 + H2SO4(конц) → KHSO4 + HNO3
2. В промышленности азотную кислоту получают из аммиака. Процесс осуществляется стадийно.
1 стадия. Каталитическое окисление аммиака.
4NH3 + 5O2 → 4NO + 6H2O
2 стадия. Окисление оксида азота (II) до оксида азота (IV) кислородом воздуха.
2NO + O2 → 2NO2
3 стадия. Поглощение оксида азота (IV) водой в присутствии избытка кислорода.
4NO2 + 2H2O + O2 → 4HNO3
Химические свойства
Азотная кислота – это сильная кислота. За счет азота со степенью окисления +5 азотная кислота проявляет сильные окислительные свойства.
1. Азотная кислота практически полностью диссоциирует в водном растворе.
HNO3 → H+ + NO3–
2. Азотная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например, азотная кислота взаимодействует с оксидом меди (II):
CuO + 2HNO3 → Cu(NO3)2 + H2O
Еще пример: азотная кислота реагирует с гидроксидом натрия:
HNO3 + NaOH → NaNO3 + H2O
3. Азотная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов, сульфитов).
Например, азотная кислота взаимодействует с карбонатом натрия:
2HNO3 + Na2CO3 → 2NaNO3 + H2O + CO2
4. Азотная кислота частично разлагается при кипении или под действием света:
4HNO3 → 4NO2 + O2 + 2H2O
5. Азотная кислота активно взаимодействует с металлами. При этом никогда не выделяется водород! При взаимодействии азотной кислоты с металлами окислителем всегда выступает азот +5. Азот в степени окисления +5 может восстанавливаться до степеней окисления -3, 0, +1, +2 или +4 в зависимости от концентрации кислоты и активности металла.
металл + HNO3 → нитрат металла + вода + газ (или соль аммония)
С алюминием, хромом и железом на холоду концентрированная HNO3 не реагирует – кислота «пассивирует» металлы, т.к. на их поверхности образуется пленка оксидов, непроницаемая для концентрированной азотной кислоты. При нагревании реакция идет. При этом азот восстанавливается до степени окисления +4:
Fe + 6HNO3(конц.) → Fe(NO3)3 + 3NO2 + 3H2O
Al + 6HNO3(конц.) → Al(NO3)3 + 3NO2 + 3H2O
Золото и платина не реагируют с азотной кислотой, но растворяются в «царской водке» – смеси концентрированных азотной и соляной кислот в соотношении 1 : 3 (по объему):
HNO3 + 3HCl + Au → AuCl3 + NO + 2H2O
Концентрированная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (IV), азот восстанавливается минимально:
4HNO3(конц.) + Cu → Cu(NO3)2 + 2NO2 + 2H2O
С активными металлами (щелочными и щелочноземельными) концентрированная азотная кислота реагирует с образованием оксида азота (I):
10HNO3 + 4Ca → 4Ca(NO3)2 + 2N2O + 5H2O
Разбавленная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (II).
8HNO3 (разб.) + 3Cu → 3Cu(NO3)2 + 2NO + 4H2O
С активными металлами (щелочными и щелочноземельными), а также оловом и железом разбавленная азотная кислота реагирует с образованием молекулярного азота:
12HNO3(разб) + 10Na → 10NaNO3 + N2 + 6H2O
При взаимодействии кальция и магния с азотной кислотой любой концентрации (кроме очень разбавленной) образуется оксид азота (I):
10HNO3 + 4Ca → 4Ca(NO3)2 + 2N2O + 5H2O
Очень разбавленная азотная кислота реагирует с металлами с образованием нитрата аммония:
10HNO3 + 4Zn → 4Zn(NO3)2 + NH4NO3 + 3H2O
Таблица. Взаимодействие азотной кислоты с металлами.
| Азотная кислота | ||||
| Концентрированная | Разбавленная | |||
| с Fe, Al, Cr | с неактивными металлами и металлами средней активности (после Al) | с щелочными и щелочноземельными металлами | с неактивными металлами и металлами средней активности (после Al) | с металлами до Al в ряду активности, Sn, Fe |
| пассивация при низкой Т | образуется NO2 | образуется N2O | образуется NO | образуется N2 |
6. Азотная кислота окисляет и неметаллы (кроме кислорода, водорода, хлора, фтора и некоторых других). При взаимодействии с неметаллами HNO3 обычно восстанавливается до NO или NO2, неметаллы окисляются до соответствующих кислот, либо оксидов (если кислота неустойчива).
Например, азотная кислота окисляет серу, фосфор, углерод, йод:
6HNO3 + S → H2SO4 + 6NO2 + 2H2O
Безводная азотная кислота – сильный окислитель. Поэтому она легко взаимодействует с красным и белым фосфором. Реакция с белым фосфором протекает очень бурно. Иногда она сопровождается взрывом.
5HNO3 + P → H3PO4 + 5NO2 + H2O
5HNO3 + 3P + 2H2O → 3H3PO4 + 5NO
Видеоопыт взаимодействия фосфора с безводной азотной кислотой можно посмотреть здесь.
4HNO3 + C → CO2 + 4NO2 + 2H2O
Видеоопыт взаимодействия угля с безводной азотной кислотой можно посмотреть здесь.
10HNO3 + I2 → 2HIO3 + 10NO2 + 4H2O
7. Концентрированная азотная кислота окисляет сложные вещества (в которых есть элементы в отрицательной, либо промежуточной степени окисления): сульфиды металлов, сероводород, фосфиды, йодиды, соединения железа (II) и др. При этом азот восстанавливается до NO2, неметаллы окисляются до соответствующих кислот (или оксидов), а металлы окисляются до устойчивых степеней окисления.
Например, азотная кислота окисляет оксид серы (IV):
2HNO3 + SO2 → H2SO4 + 2NO2
Еще пример: азотная кислота окисляет йодоводород:
6HNO3 + HI → HIO3 + 6NO2 + 3H2O
Азотная кислота окисляет углерод до углекислого газа, т.к. угольная кислота неустойчива.
3С + 4HNO3 → 3СО2 + 4NO + 2H2O
Сера в степени окисления -2 окисляется без нагревания до простого вещества, при нагревании до серной кислоты.
Например, сероводород окисляется азотной кислотой без нагревания до молекулярной серы:
2HNO3 + H2S → S + 2NO2 + 2H2O
При нагревании до серной кислоты:
2HNO3 + H2S → H2SO4 + 2NO2 + 2H2O
8HNO3 + CuS → CuSO4 + 8NO2 + 4H2O
Соединения железа (II) азотная кислота окисляет до соединений железа (III):
4HNO3 + FeS → Fe(NO3)3 + NO + S + 2H2O
8. Азотная кислота окрашивает белки в оранжево-желтый цвет («ксантопротеиновая реакция»).
Ксантопротеиновую реакцию проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую.
Видеоопыт обнаружения белков с помощью азотной кислоты можно посмотреть здесь.
Азотистая кислота
Азотистая кислота HNO2 — слабая, одноосновная, химически неустойчивая кислота.
Получение азотистой кислоты.
Азотистую кислоту легко получить вытеснением из нитритов более сильной кислотой.
Например, соляная кислота вытесняет азотистую кислоту из нитрита серебра:
AgNO2 + HCl → HNO2 + AgCl
Химические свойства.
1. Азотистая кислота HNO2 существует только в разбавленных растворах, при нагревании она разлагается:
3HNO2 → HNO3 + 2NO + H2O
без нагревания азотистая кислота также разлагается:
2HNO2 → NO2 + NO + H2O
2. Азотистая кислота взаимодействует с сильными основаниями.
Например, с гидроксидом натрия:
HNO2 + NaOH → NaNO2 + H2O
3. За счет азота в степени окисления +3 азотистая кислота проявляет слабые окислительные свойства. Окислительные свойства HNO2 проявляет только при взаимодействии с сильными восстановителями.
Например, HNO2 окисляет иодоводород:
2HNO2 + 2HI → 2NO + I2 + 2H2O
Азотистая кислота также окисляет иодиды в кислой среде:
2НNO2 + 2KI + 2H2SO4 → K2SO4 + I2 + 2NO + 2H2O
Азотистая кислота окисляет соединения железа (II):
2HNO2 + 3H2SO4 + 6FeSO4 → 3Fe2(SO4)3 + N2 + 4H2O
4. За счет азота в степени окисления +3 азотистая кислота проявляет сильные восстановительные свойства. Под действием окислителей азотистая кислота переходит в азотную.
Например, хлор окисляет азотистую кислоту до азотной кислоты:
HNO2 + Cl2 + H2O → HNO3 + 2HCl
Кислород и пероксид водорода также окисляют азотистую кислоту:
2HNO2 + O2 → 2HNO3
HNO2 + H2O2 → HNO3 + H2O
Соединения марганца (VII) окисляют HNO2:
5HNO2 + 2HMnO4 → 2Mn(NO3)2 + HNO3 + 3H2O
Соли азотной кислоты — нитраты
Нитраты металлов — это твердые кристаллические вещества. Большинство очень хорошо растворимы в воде.
1. Нитраты термически неустойчивы, причем все они разлагаются на кислород и соединение, характер которого зависит от положения металла (входящего в состав соли) в ряду напряжений металлов:
- Нитраты щелочных и щелочноземельных металлов (до Mg в электрохимическом ряду) разлагаются до нитрита и кислорода.
Например, разложение нитрата натрия:
2KNO3 → 2KNO2 + O2
Исключение – литий.
Видеоопыт разложения нитрата калия можно посмотреть здесь.
- Нитраты тяжелых металлов (от Mg до Cu, включая магний и медь) и литий разлагаются до оксида металла, оксида азота (IV) и кислорода:
Например, разложение нитрата меди (II):
2Cu(NO3)2 → 2CuO + 4NO2 + O2
- Нитраты малоактивных металлов (правее Cu) – разлагаются до металла, оксида азота (IV) и кислорода.
Например, нитрат серебра:
2AgNO3 → 2Ag + 2NO2 + O2
Исключения:
Нитрит железа (II) разлагается до оксида железа (III):
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2
Нитрат марганца (II) разлагается до оксида марганца (IV):
Mn(NO3)2 → MnO2 + 2NO2
2. Водные растворы не обладают окислительно-восстановительными свойствами, расплавы – сильные окислители.
Например, смесь 75% KNO3, 15% C и 10% S называют «черным порохом»:
2KNO3 + 3C + S → N2 + 3CO2 + K2S
Соли азотистой кислоты — нитриты
Соли азотистой кислоты устойчивее самой кислоты, и все они ядовиты. Поскольку степень окисления азота в нитритах равна +3, то они проявляют как окислительные свойства, так и восстановительные.
Кислород, галогены и пероксид водорода окисляют нитриты до нитратов:
2KNO2 + O2 → 2KNO3
KNO2 + H2O2 → KNO3 + H2O
KNO2 + H2O + Br2 → KNO3 + 2HBr
Лабораторные окислители — перманганаты, дихроматы — также окисляют нитриты до нитратов:
5KNO2 + 3H2SO4 + 2KMnO4 → 5KNO3 + 2MnSO4 + K2SO4 + 3H2O
3KNO2 + 4H2SO4 + K2Cr2O7 → 3KNO3 + Cr2(SO4)3 + K2SO4 + 4H2O
В кислой среде нитриты выступают в качестве окислителей.
При окислении йодидов или соединений железа (II) нитриты восстанавливаются до оксида азота (II):
2KNO2 + 2H2SO4 + 2KI → 2NO + I2 + 2K2SO4 + 2H2O
2KNO2 + 2FeSO4 + 2H2SO4 → Fe2(SO4)3 + 2NO + K2SO4 + 2H2O
При взаимодействии с очень сильными восстановителями (алюминий или цинк в щелочной среде) нитриты восстанавливаются максимально – до аммиака:
NaNO2 + 2Al + NaOH + 6H2O → 2Na[Al(OH)4] + NH3
Смесь нитратов и нитритов также проявляет окислительные свойства. Например, смесь нитрата и нитрита калия окисляет оксид хрома (III) до хромата калия:
3KNO2 + Cr2O3 + KNO3 → 2K2CrO4 + 4NO