Удельная газовая
постоянная однородного газа, заменяющего
смесь, называется газовой постоянной
смеси Rсм,
Дж / (кг·К):

или окончательно
.
Через мольные доли
газовая постоянная смеси вычисляется
следующим образом:
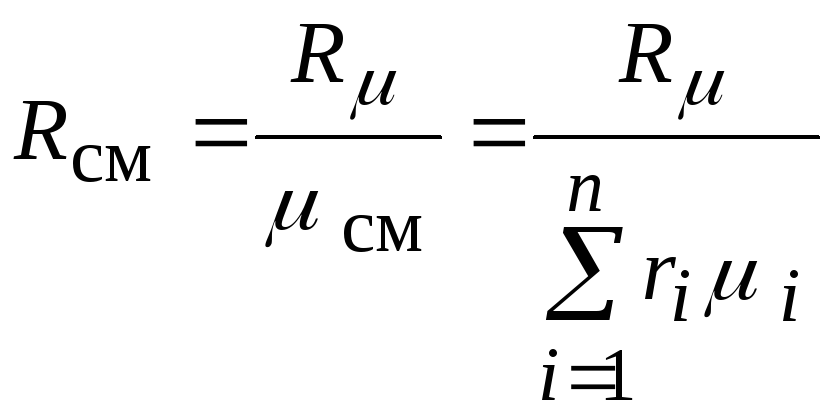
или окончательно

С использованием
можно получить формулу для вычисления
парциального давления идеального газа
через его массовую долю.
Т. к. и
,
то разделив эти
выражения друг на друга получим:
,
откуда
Из последнего
выражения можно получить удобную
формулу, связывающую мольные и массовые
доли идеального газа.
Т. к. ,
то
1.4.8. Плотность смеси газов
Плотность однородного
газа, заменяющего
смесь, называется плотностью смеси:
В справочниках
обычно приводится без объяснений
следующая формула для плотности смеси:
В то же время в
технической литературе встречаются
формулы вида
С вычислением
плотности смеси через плотности
компонентов связано наибольшее число
студенческих ошибок. Дело в том, что
значение плотности
-го
компонента можноформальнополучить из двух формул:
и
Т.
к.
,
то значенияи
заметно отличаются друг от друга.
Проясним вопрос
с вычислением плотности смеси.
По определению
и
,
тогда.
Но
и
Т.
о. в последней формуле плотность i-го
газавычисляется как плотность этого газа,
находящегося в количествекилограммовв объеме
(парциальном объеме) при давлении
смеси
и температуре смеси .
Такое толкование
плотности компонентов смеси используется,
в частности, при расчетеобъемов
продуктов сгорания топлива.
Если плотность
i-го газа в смеси
вычислять через его парциальное давление
,
то
Т.
о. в этой формуле плотность i-го
газа— это плотность газа массой
,
находящегося вобъеме (объем
смеси) при его парциальном давлении и температуре
(температуре смеси).
Такое толкование
плотности компонентов смеси, в частности,
используется при определении абсолютной
и относительной влажности воздуха.
1.4.9. Энтропия смеси идеальных газов
Как указано в
параграфе 1.4.1., энтропия 1 кг
—
компонентной смеси идеальных газов
(удельная энтропия смеси)Sсм
, Дж / (К · кг), определяется по
следующей формуле:
,
где: —
энтропия 1 кгi-го газа.
Из
курса общей термодинамики известно:
,
где: —
массовая изобарная теплоемкостьi-го
газа.
Окончательно
удельная энтропия
-компонентной
смеси может быть вычислена по следующей
формуле:
1.4.10. Теплоемкость газовой смеси
По определению,
теплоемкость — это количество теплоты,
которое необходимо для изменения
температуры единицы количества вещества
(
)
на один градус.
Т. к. температура
всех газов в смеси одинакова, то
теплоемкость смеси, складывается из
теплоемкостей всех компонентов, взятых
в долях, соответствующих способу задания
смеси:
— массовая (удельная)
теплоемкость, Дж / (кг·К);
— мольная теплоемкость,
Дж / (кмоль·К);
— объемная
теплоемкость, Дж / (м3·К).
где: — массовая, мольная и объемная теплоемкостиi-го компонента.
Газовая постоянная смеси газов.
- Газовая постоянная смешанного газа Смешанный газ следует уравнению состояния-pV = mRT и R = pV / mT. Из Формулы (3-2″) n = gtRi / R и 2G / = ZgiRi / R = 1, из которых^ Р = организации стандартов Ирана ’= ^ + g2R2 + … + гнрн. ■(3-3)) Газовая постоянная смешанного газа равна сумме массовой доли каждого газа и произведения этой
газовой постоянной. Еще одно уравнение, определяющее газовую постоянную смеси Р = 2giRi-Ф 8314.2(г,/ ^ + ГДж {он + … + г меня. по известной средней молекулярной массе смеси. <Р = 8314.2 / С.%(3-5) Таким образом, газовая постоянная смеси определяется уравнением, по которому вводится средняя молекулярная масса, а газовая постоянная
Газовая постоянная смеси может быть определена
Людмила Фирмаль
отдельных газов определяется тем же уравнением, но там вводится фактическая молекулярная масса каждого газа. Если указан объемный состав смеси, (3-2 ’) gi =(RiRiYi и Xg,= RZn / Rt = 1. И затем… R—V = 1 KrJR, + rJR,+; • • + rn! Дипломированная медсестра.) •(3-6))Средняя молекулярная масса газовой смеси Средняя молекулярная масса является условной величиной, которая относится
к однородному газу, в котором число молекул и общая масса равны числу молекул и массе смешанного газа. Если известна газовая постоянная смеси、 С-8314.2 / Р•. (3-7) И. Я — = 8314.2%/?+ 2 + … + gntfn). Газовая постоянная Rlt R2t …Заменив Rn величиной из уравнения Клапейрона, получим формулу средней молекулярной массы, если смесь задана массовой долей. х = л / (&//ИИ + gjpt + … + W-(3: 8) Если
- смесь указана в объемной доле, то из Формулы (3-6): Р = H2rJRi = 8314.2 / 2rf | если. С / ? ’8 314,2 / Форекс ’ И затем… •[Л= Srijij = rjfij +Г2[Л2+ … +Гпсп. (3-9) Средняя молекулярная масса газовой смеси равна сумме продуктов объемной доли по молекулярной массе отдельных газов, входящих в состав смеси.Парциальное давление Если известны основные параметры газа, то парциальное давление
газа можно определить по массовой доле уравнения Клапейрона. Л = п =(3-10) В. г-н р. Привет.. чтобы найти парциальное давление каждого газа при определении смеси по объемной доле. ПТВ = ПВЛ и Pi = Р ^ = РТП. (3-11) Парциальное давление каждого газа равно произведению полного давления смешанного газа на объемную долю. Формула (3-
Вы можете использовать закон Бойля-Марриотта
Людмила Фирмаль
11)обычно используется при техническом расчете и испытаниях теплового оборудования. Объемная доля газа определяется специальным прибором — газоанализатором. Управление вопросами и примерами в главе 3 1.Что такое смешанный газ? 2.Дайте Далтону формулировку закона. • * 3.Что называется парциальным давлением?
4.Что называется массой, объемом и молярной долей? 5.Так называемая частичная, или. Ты убавил громкость? Какова связь между удельным объемом, плотностью, молекулярной массой и постоянной газа? 7.Почему молекулярная масса смеси называется средней молекулярной массой? * 8.Как. Пересчет массового состава в объем и пересчет объема в объем? 9., Как определяется газовая
постоянная смеси по массовой доле и объемной доле? — В J0.Как парциальное давление газа в смеси определяется массовой долей и объемной долей? 11.Как определяется средняя молекулярная масса смеси газов? Пример 3-1.Если мы предположим, что объем сухого воздуха составляет 21% 02 и 79% N2, мы получим среднюю молекулярную массу сухого воздуха. По Формуле (3-9)、 = РЛ іх +
r2fx3= 32-0.210 + 28.016-0.79 = 28.93 Пример 3-2 определяет газовую постоянную, плотность и парциальное давление смеси, состоящей из 20 массовых долей воздуха и 1 массовой доли легкого газа. Плотность легкого газа при температуре 273°К и давлении 101325 ″ Li2 ″ равна 0,52 кг Газовая постоянная легкого газа определяется по формуле Клапейрона. U1325 = 7и Джей!(Кг-град). J 0,52-273 В и’
Газовая постоянная воздуха составляет 287.04 Дж! Это хорошая идея. Газовая постоянная смешанного газа определяется по формуле (3-3): R = + g2R2= 287.04-20 / 21 + 714-1 / 21 = 306.3 j /(кг> град). Плотность смеси определяется уравнением Клапейрона: p = p / RT = 101325:306,30-273 = 1,21 кг / М9.Парциальное давление определяется по формуле (3-11). = 101325 — = 90100 nCl Ри Р. 21,306. 3 ′ Парциальное давление газа лампы = = — — — — ^- =11225 Н(м G2 G62 I 21 306.30
Смотрите также:
Решение задач по термодинамике
Поскольку значение газовой постоянной компонента смеси может быть определено по его молярной массе, т. е. Ri = 8314/М , то выражение (3.14) принимает вид [c.124]
При первом способе смешения объем газовой смеси равен сумме объемов газа, из которых состоит смесь. Пусть, например, имеются два резервуара (рис. 3-23), в каждом из которых заключен какой-нибудь газ. Если эти резервуары соединены трубопроводом, на котором установлена задвижка, то через некоторый промежуток времени после открытия ее вследствие теплового движения молекул образуется равномерно распределенная по всему объему смесь при этом предполагается, что смешиваемые газы не могут вступать в химическое взаимодействие. Состав полученной смеси нетрудно определить, если найти количества газов, взятые для смешения. По известному составу можно найти молекулярную массу, газовую постоянную, теплоемкость смеси, объемный состав ее. [c.146]
Осм / см = Ох + / 2 + — + 0 / , +. .. + G / , откуда получаем значение газовой постоянной газовой смеси [c.38]
T. e. газовая постоянная газовой смеси равна сумме произведений весовой доли каждого составляющего газа на его газовую постоянную. [c.38]
Ri — газовая постоянная t-ro компонента к, R — отношение теплоемкостей и газовая постоянная газовой смеси рабочего тела [c.84]
Удельная газовая постоянная паровоздушной смеси Кем и величина Ь [c.177]
Ri — газовые постоянные компонентов смеси. [c.19]
С помощью этого определения можно получить выражение для Re через газовые постоянные компонентов смеси. Теперь мы рассмот- [c.270]
Газовая постоянная сухого воздуха воза = 29,27, а газовая постоянная паровоздушной смеси, как выводится в курсе термодинамики, равна [c.315]
Газовая постоянная R смеси проще всего определяется из уравнения [c.31]
В цилиндре действительного двигателя уменьшение давления выхлопа характеризуется линией 4—1 (см. фиг. 8. 1), количество газа в этом процессе все время убывает. Следовательно, так как продукты горения в горючую смесь не обращаются, то цикл разомкнут между точками 4 1. Процесс между этими точками заменен на диаграммах (фиг. 8. 2 и 8. 3) изохорным процессом с отводом от рабочего агента тепла в холодильник, причем количество рабочего агента принимается за постоянное и неизменное по составу во всех процессах цикла. Такая замена возможна в обеих диаграммах потому, что газовые постоянные горючей смеси и продуктов горения по величине незначительно отличаются одна от другой, работа каждого процесса 1—2 как на фиг. 8. I, так и на фиг.. 8.2 равна нулю и действительное количество тепла д , отдаваемое продуктами сгорания воздуху при переходе от состояния 4 к состоянию 1 (см. фиг. 8. 1), равно количеству тепла д , отнимаемому от рабочего агента при изохорном переходе от состояния 4 к состоянию 1 (фиг. 8.3), т. е. д 2=д2. [c.160]
Введенное на основе формальных соображений в уравнение (51) число Всм можно назвать газовой постоянно 11 смеси. Так как [c.38]
Смесь идеальных газов является тоже идеальным газом и подчиняется уравнениям Клапейрона и Клапейрона—Менделеева. Газовую постоянную для смеси газов можно найти, если известен состав смеси и газовые постоянные ее компонентов. [c.31]
Пример 1-11. Определить газовую постоянную горючей смеси, состоящей из 1,3 м воздуха и 1 ж генераторного газа, если удельный вес последнего при 0° С и 760 м.н рт. ст. равен 1,2 кг м . Объемные содержания воздуха и газа [c.34]
Иэ уравнений (6.9) и (6.10) очевидно, что газовая постоянная R смеси определяется равенством [c.93]
Таким образом, газовая постоянная для смеси [c.41]
Задач.а 4 (стр. 55). Газовая постоянная для смеси газов, согласно уравнению (44), Rm = Из объемных долей fi весовые доли gi можно получить по [c.383]
Все зависимости, полученные выше для идеальных газов, справедливы и для их смесей, если в них подставлять газовую постоянную, молекулярную массу и теплоемкость смеси. [c.40]
Поскольку в соответствии с (1.6) / ,= = 8314/)Xi, то из (4.46) следует, что газовая постоянная смеси Дж/(кг-К) имеет вид [c.41]
Выразим формально газовую постоянную смеси R по формуле (1.6), введя кажущуюся молекулярную массу смеси ц,. [c.41]
Газовая постоянная смеси / = 0,1803-189 + 0,075-462 + 0,0196-260 + + 0,7251-297 = 289 Дж/(кг-К). [c.218]
В книге приводятся результаты теоретического и экспериментального исследования процесса термодиффузионного разделения в газовых смесях в стационарных и нестационарных условиях. Рассматриваются различные методы описания явления термодиффузии в газовых смесях. Описываются принципы стационарного и нестационарного метода экспериментального определения термодиффузионной постоянной. Рассматривается влияние термодиффузии и диффузионной теплопроводности на кондуктивный и конвективный перенос тепла. Найден вклад неидеальности компонент газовой смеси в характеристики процесса термодиффузионного разделения. В приложении приводятся экспериментальные и расчетные данные по термодиффузионной постоянной бинарных смесей газов. [c.208]
В технике очень часто приходится иметь дело с газообразными веществами, представляющими механическую смесь отдельных газов, например, доменный и светильный газ, отходящие газы из котельных установок, двигателей внутреннего сгорания, реактивных двигателей и других тепловых установок. Воздух также представляет собой газовую смесь, состоящую из азота, кислорода, углекислого газа, водяных паров и одноатомных газов. Поэтому для решения практических задач необходимо уметь определять основные параметры газовой смеси газовую постоянную, среднюю молекулярную массу, парциальные давления и др. [c.30]
Таким образом, задачей расчета газовой смеси является определение на основании заданного состава смеси средней молекулярной массы, или газовой постоянной, смеси газов, после чего получение всех остальных параметров можно произвести по уравнению состояния для смеси. [c.31]
Соотношения между массовыми н объемными долями. Между удельными объемами, плотностями, молекулярными массами и газовыми постоянными какого-нибудь газа и всей смеси в целом на основании закона Авогадро и уравнения Клапейрона — Менделеева существует следующая зависимость [c.32]
Газовая постоянная смеси газов [c.33]
Газовая постоянная смеси газов равна сумме произведений массовых долей каждого газа на его газовую постоянную. [c.33]
Другое уравнение для определения газовой постоянной смеси [c.33]
Газовую постоянную смеси можно определить по известной средней молекулярной массе смеси [c.33]
Следовательно, газовая постоянная смеси определяется по уравнению, в которое вводится средняя молекулярная масса, а газовая постоянная отдельного газа определяется по тому же уравнению, но в него вводится действительная молекулярная масса каждого газа. [c.33]
Средняя молекулярная масса представляет собой условную величину и относится к такому однородному газу, у которого число молекул и общая масса равны числу молекул и массе смеси газов. Если известна величина газовой постоянной смеси, то [c.34]
Величину gJRf называют газовой постоянной данной смеси. [c.103]
Природный газ Грознефти имеет следующий объемный состав метан СН4 — 49,0%, этан СгНе—11,0%, пропан СзНз—17,0%, бутан С4Н10—15,0%, пентан С5Н12 —4,0%, углекислоты СО2—1%, азота N2 — 3,0%. Этот газ смешивается с воздухом в пропорции 1 кг газа на 15 кг воздуха, имеющего массовый состав кислорода О2 — 23,2% и азота N2 — 76,8%. Определить молекулярный вес, газовую постоянную полученной смеси, а также плотность ее при давлении 780 мм рт. ст. и температуре 37° С. [c.16]
R Ыок=МгЯ1 — универсальная газовая постоянная Газовая постоянная для смеси, Н = Щ [c.425]
Рассмотрим уравнение состояния газовой смссн, возникаюшей в результате диссоциации двухатомной молекулы. Это уравнение можно получить, если воспользоваться зависимостями для определения давления р н газовой постоянной R смеси газов, а также парциального давле1гия компонента рс [c.60]
Из описания принципа работы поршневых д. в. с. видно, что в них по существу не происходит круговых процессов, так как газообразные продукты горения после расширения и отдачи с помощью поршня энергии нл коленчатый вал удаляются из цилиндра двигателя, а на их место поступает свежая порция горючей смеси, химический состав которой в результате последующего процесса сгорания меняется. Однако условно можно говорить о круговом процессе работы двигателя внутреннего сгорания, если не принимать в расчет химических изменений и определять его КПД по формуле tij = AJqi, подставляя работу Лц и расход теплоты Qi, равные их теоретическим значениям для двигателя. Допускаемая при этом неточность мала, так как, несмотря на коренное изменение химического состава рабочего тела при сгорании, газовые постоянные горючей смеси и продуктов горения незначительно отличаются одна от другой. [c.148]
Продукты сгорания по выходе из сепаратора состоят из сухих продуктов в количестве (Су — 1 о) и водяных паров в количестве (1 0 — ). Газовая постоянная этой смеси определяется по обн еизвестной формуле [c.48]
Газовая постоянная смеси газов. Просуммировав уравнения (4.42) для всех компоисм- [c.41]
c.46
]
Справочник машиностроителя Том 6 Издание 2 (0) — [
c.2
,
c.46
]