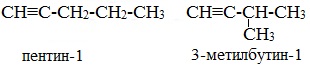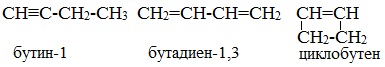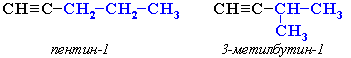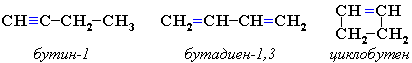Алкины – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
Получение алкинов
Гомологический ряд алкинов
Все алкины имеют общие или похожие физические и химические свойства. Схожие по строению алкины, которые отличаются на одну или несколько групп –СН2–, называют гомологами. Такие алкины образуют гомологический ряд.
Первый представитель гомологического ряда алкенов – этин (ацетилен) C2H2, или СH≡СH.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь.
| Название алкина | Формула алкина |
| Этин (ацетилен) | C2H2 |
| Пропин | C3H4 |
| Бутин | C4H6 |
| Пентин | C5H8 |
| Гексин | C6H10 |
| Гептин | C7H12 |
Общая формула гомологического ряда алкинов CnH2n-2.
Первые три члена гомологического ряда алкинов – газы, начиная с C5Н8 по С16Н30 – жидкости, начиная с С17Н32 — твердые вещества.
Алкины плохо растворимы в воде и хорошо растворимы в органических растворителях.
Строение алкинов
Рассмотрим особенности строения алкинов на примере ацетилена.
В молекуле ацетилена присутствуют химические связи C–H и С≡С.
Связь C–H ковалентная слабополярная одинарная σ-связь. Связь С≡С – тройная, ковалентная неполярная, одна из связей σ, еще две: π-связи. Атомы углерода при тройной связи образуют по две σ-связи и две π-связи. Следовательно, гибридизация атомов углерода при тройной связи в молекулах алкинов – sp:
При образовании σ-связи между атомами углерода происходит перекрывание sp-гибридных орбиталей атомов углерода:
При образовании π-связи между атомами углерода происходит перекрывание негибридных орбиталей атомов углерода:
Две sp-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому две гибридные орбитали атомов углерода при тройной связи в алкинах направлены в пространстве под углом 180о друг к другу:
Изображение с сайта orgchem.ru
Это соответствует линейному строению молекулы.
Например, молекуле ацетилена C2H2 соответствует линейное строение.
Изображение с сайта orgchem.ru
Молекулам алкинов с большим числом атомов углерода соответствует пространственное строение.
Например, в молекуле пропина присутствует атом углерода в sp3-гибридном состоянии, в составе метильного фрагмента СН3. Такой фрагмент имеет тетраэдрическое строение.
Изомерия алкинов
Для алкинов характерна структурная и пространственная изомерия.
Структурная изомерия
Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
Изомеры с различным углеродным скелетом и с формулой С5Н8 — пентин-1 и 3-метилбутин-1
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Алкины являются межклассовыми изомерами с алкадиенами. Общая формула алкинов и алкадиенов — CnH2n-2.
Межклассовые изомеры с общей формулой С4Н6 — бутин-1 и бутадиен
Изомеры с различным положением тройной связи отличаются положением тройной связи в углеродном скелете.
Изомеры положения тройной связи, которые соответствуют формуле С5Н8 — пентин-1 и пентин-2
Пространственная изомерия
Для некоторых алкинов также характерна оптическая изомерия.
Алкины, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров. В молекуле алкина должен присутствовать асимметрический атом углерода (атом углерода, связанный с четырьмя различными заместителями).
Цис-транс-изомерия для алкинов не характерна, так как по тройной связи вращение возможно.
Номенклатура алкинов
В названиях алкинов для обозначения тройной связи используется суффикс -ИН.
Например, алкин на рисунке называется бутин-2
Для простейших алкинов применяются также исторически сложившиеся (тривиальные) названия:
| Название алкина | Формула алкина |
| Ацетилен | CH≡CH |
| Пропин | CH≡C−CH3 |
| Бутин-1 | CH≡C−СH2−CH3 |
Радикалы, содержащие тройную связь, также носят тривиальные названия:
| Формула радикала | Тривиальное название |
| CH≡C− | этинил |
| CH≡C−CH2− | пропаргил |
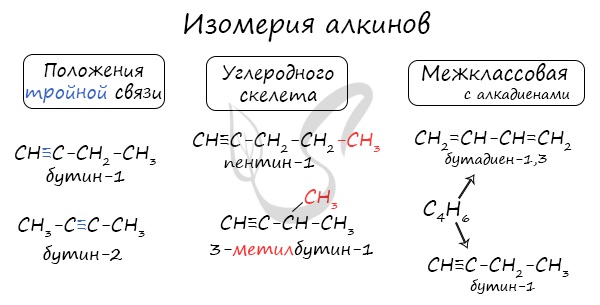
Изомерия алкинов
Для алкинов характерна структурная изомерия. Первые два члена гомологического ряда – этин и пропин – изомеров не имеют.
1. Изомерия углеродного скелета (начиная с С5Н8):
2. Изомерия положения тройной связи (начиная с С4Н6):
3. Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с С4Н6:
Пространственная изомерия относительно тройной связи в алкинах не проявляется, т.к. заместители могут располагаться только одним способом — вдоль линии связи.
Алкины (ацетиленовые углеводороды)
Изомерия алкинов
Структурная изомерия
- Изомерия положения тройной связи, начиная с С4Н6:
- Изомерия углеродного скелета, начиная с С5Н8:
- Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с С4Н6:
Пространственная изомерия относительно тройной связи в алкинах не проявляется, так как заместители могут располагаться только одним способом – вдоль линии связи.
Тем не менее, пространственные изомеры алкинов могут существовать при наличии соответствующих структурных признаков в углеводородном радикале, связанном с тройной связью. Например,
поворотная изомерия молекул HC≡C–CH2–CH3 (бутин-1) при вращении по σ-связи С(3)–С(4);
оптическая изомерия соединения HC≡C–*CH(CH3)–CH2CH3 (3-метилпентин-1), содержащего асимметрический атом *C, и т.п.
Алкины — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну тройную связь С≡С.
Каждая такая связь содержит одну сигма-связь (σ-связь) и две пи-связи (π-связи).
Алкины также называют ацетиленовыми углеводородами. Первый член гомологического ряда — этин — CH≡CH (ацетилен).
Общая формула их гомологического ряда — CnH2n-2.
Номенклатура и изомерия алкинов
Названия алкинов формируются путем добавления суффикса «ин» к названию алкана с соответствующим числом: этин, пропин, бутин и т.д.
При составлении названия алкина важно учесть, что главная цепь атомов углерода должна обязательно содержать тройную связь. Нумерация
атомов углерода в ней начинается с того края, к которому ближе тройная связь. В конце названия указывают атом углерода у которых
начинается тройная связь.

Для алкинов характерна изомерия углеродного скелета, положения тройной связи, межклассовая изомерия с алкадиенами.
Пространственная геометрическая изомерия для них невозможна, ввиду того, что каждый атом углерода, прилежащий к тройной связи,
соединен только с одним единственным заместителем.
Некоторые данные, касающиеся алкинов, надо выучить:
- В молекулах алкинов присутствуют тройные связи, длина которых составляет 0,121 нм
- Тип гибридизации атомов углерода — sp
- Валентный угол (между химическими связями) составляет 180°
Получение алкинов
Ацетилен получают несколькими способами:
- Пиролиз метана
- Синтез Бертло
- Разложение карбида кальция
При нагревании метана до 1200-1500 °C происходит димеризация молекул метана, в ходе чего отщепляется водород.
2CH4 → (t) CH≡CH + 3H2
Осуществляется напрямую, из простых веществ. Протекает на вольтовой (электрической) дуге, в атмосфере водорода.
2C + H2 → (t, вольтова дуга) CH≡CH
В результате разложения карбида кальция образуется ацетилен и гидроксид кальция II.
CaC2 + 2H2O → CH≡CH + Ca(OH)2
Получение гомологов ацетилена возможно в реакциях дегидрогалогенирования дигалогеналканов, в которых атомы галогена
расположены у одного атома углерода или у двух соседних атомов.

Химические свойства алкинов
Алкины — ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны.
- Гидрирование
- Галогенирование
- Гидрогалогенирование
- Реакция Кучерова
- Окисление
- Реакция Н.Д. Зелинского (тримеризация ацетилена)
- Димеризация ацетилена
- Образование солей алкинов
Водород присоединяется к атомам углерода, образующим тройную связь. Пи-связи (π-связи) рвутся, остается единичная сигма-связь (σ-связь).
CH≡C-CH3 + H2 → (t, Ni) CH2=CH-CH3 (в реакции участвует 1 моль водорода)
CH2=CH-CH3 + H2 → (t, Ni) CH3-CH2-CH3 (в реакции участвует 1 моль водорода)
CH≡CH + 2H2 → (t, Ni) CH3-CH3 (в реакции участвует 2 моль водорода)
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная
вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.

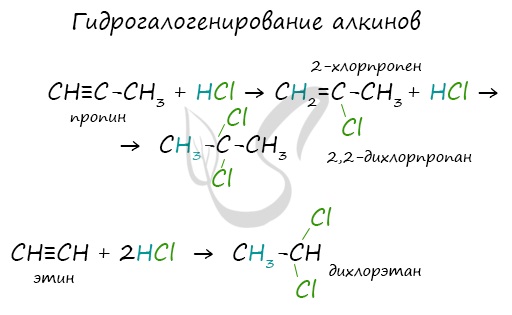
Алкины вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а
атом галогена — к наименее гидрированному атому углерода.
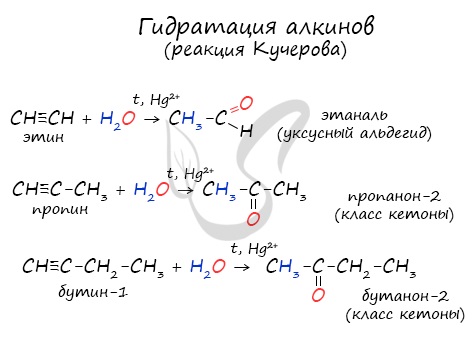
Реакцией Кучерова называют гидратацию ацетиленовых соединений с образованием карбонильных соединений. Открыта русским
химиком М.Г. Кучеровым в 1881 году. Катализатор — соли ртути Hg2+.
Только в реакции с ацетиленом образуется уксусный альдегид. Во всех остальных реакциях (с гомологами ацетилена) образуются
кетоны.
При горении алкины, как и все органические соединения, сгорают с образование углекислого газа и воды — полное окисление.
2CH≡CH + 5O2 → 4CO2 + 2H2O
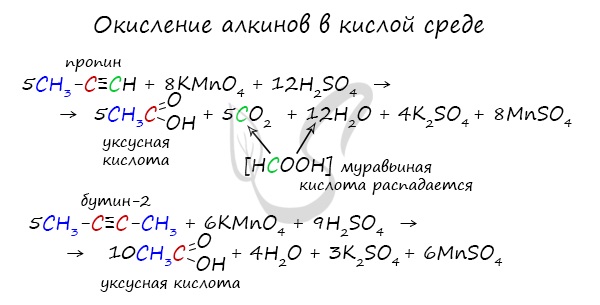
Сильные окислители (особенно в подкисленной среде) способны разрывать молекулы алкинов в самом слабом месте — в месте тройной связи.
Так, при окислении пропина, образуется уксусная кислота и муравьиная кислота, окисляющаяся до угольной кислоты, которая распадается на
углекислый газ и воду.
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический
углеводород — бензол.

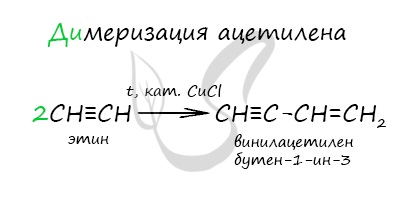
Димеризация ацетилена происходит при наличии катализатора — солей меди I. В результате реакции две молекулы ацетилена соединяются,
образуя винилацетилен.
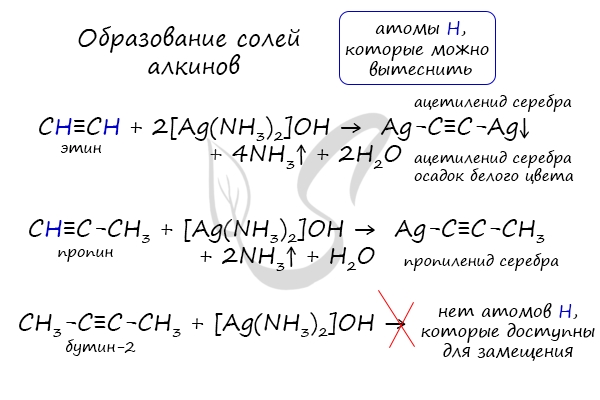
В случае если тройная связь прилежит к краевому атому углерода, то имеющийся у данного атома водород может быть замещен атомом металла.
Если тройная связь спрятана внутри молекулы, то образование солей невозможно.
Реакция аммиачного раствора серебра и ацетилена — качественная реакция, в ходе которой выпадает осадок ацетиленида серебра.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Для алкинов характерны следующие виды структурной изомерии:
- изомерия углеродной цепи;
- изомерия положения тройной связи;
- межклассовая изомерия с диеновыми углеводородами;
- межклассовая изомерия с циклоалкенами.
В молекулах структурных изомеров атомы углерода соединяются в разном порядке. Молекулы могут иметь линейное или разветвлённое строение. Тройная связь в молекулах может располагаться в разных местах.
У ацетилена изомеры отсутствуют, а с увеличением числа атомов углерода количество структурных изомеров возрастает.
В таблице приведены формулы некоторых изомеров, имеющих состав
C5H8
.
|
Структурная формула изомера |
Название |
|
|
пентин-(1) |
|
|
пентин-(2) |
|
|
(3)-метилбутин-(1) |
|
|
пентадиен-(1),(2) |
|
|
пентадиен-(1),(3) |
|
|
(3)-метилциклобутен |