Изомеры – это вещества, имеющие одинаковый состав (число атомов каждого типа), но разное взаимное расположение атомов – разное строение.
Изомерия – это явление существования веществ с одинаковым составом, но различным строением.
Например, формуле C4H10 соответствуют два изомерных соединения н-бутан с линейным углеродным скелетом и изобутан (2-метилбутан) с разветвленным скелетом:
При этом температура кипения н-бутана –0,5оС, а изобутана –11,4оС.
Виды изомерии
Различают два основных вида изомерии: структурную и пространственную (стереоизомерию).
Структурные изомеры отличаются друг от друга взаимным расположением атомов в молекуле; стереоизомеры — расположением атомов в пространстве.
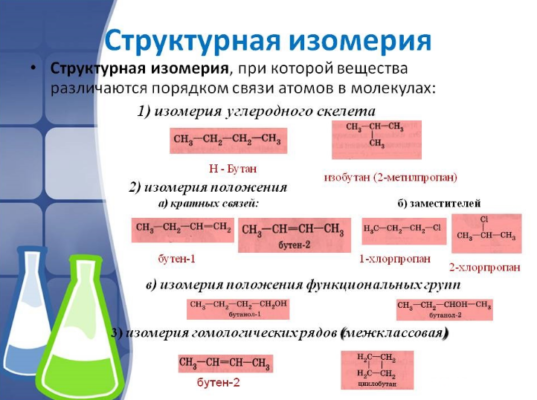
Структурная изомерия
Структурные изомеры – соединения с одинаковым составом, но различным порядком связывания атомов, т.е. с различным химическим строением. Молекулярная формула у структурных изомеров одинаковая, а структурная различается.
1. Изомерия углеродного скелета: вещества различаются строением углеродной цепи, которая может быть линейная или разветвленная.
Например, молекулярной формуле С5Н12 соответствуют три изомера:
2. Изомерия положения обусловлена различным положением кратной связи, функциональной группы или заместителя при одинаковом углеродном скелете молекул.
2.1. Изомерия положения функциональной группы. Например, существует два изомерных предельных спирта с общей формулой С3Н8О: пропанол-1 (н-пропиловый спирт) пропанол-2 (изопропиловый спирт):
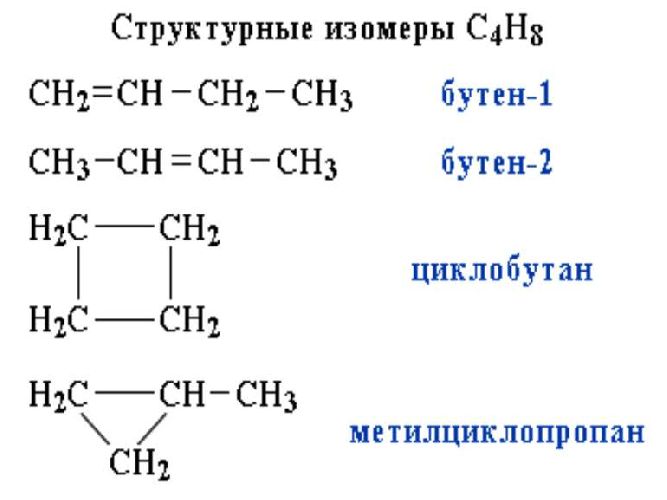
2.2. Изомерия положения кратной связи может быть вызвана различным положением кратной (двойной или тройной) связи в непредельных соединениях. Например, в бутене-1 и бутене-2:
2.3. Межклассовая изомерия – ещё один вид структурной изомерии, когда вещества из разных классов веществ имеют одинаковую общую формулу.
Например, формуле С2Н6О соответствуют: спирт (этанол) и простой эфир (диметиловый эфир):
Пространственная изомерия
Пространственные изомеры – это вещества с одинаковым составом и химическим строением, но с разным пространственным расположением атомов в молекуле. Виды пространственной изомерии – геометрическая (цис—транс) и оптическая изомерия.
1. Геометрическая изомерия (или цис-транс-изомерия).
Геометрическая изомерия характерна для соединений, в которых различается положение заместителей относительно плоскости двойной связи или цикла. Например, для алкенов и циклоалканов.
Двойная связь не имеет свободного вращения вокруг своей оси.
Поэтому заместители у атомов углерода при двойной связи могут быть расположены либо по одну сторону от плоскости двойной связи (цис-изомер), либо по разные стороны от плоскости двойной связи (транс-изомер). При этом никаким вращением нельзя получить из цис-изомера транс-изомер, и наоборот.
Например, бутен-2 существует в виде цис— и транс-изомеров
1,2-Диметилпропан также образует цис-транс-изомеры:
Геометрические изомеры различаются по физическим свойствам (температура кипения и плавления, растворимость, дипольный момент и др.). Например, температура кипения цис-бутена-2 составляет 3,73 оС, а транс-бутена-2 0,88оС.
При этом цис—транс-изомерия характерна для соединений, в которых каждый атом углерода при двойной связи С=С (или в цикле) имеет два различных заместителя.
Например, в молекуле бутена-1 CH2=CH-CH2-CH3 заместители у первого атома углерода при двойной связи (два атома водорода) одинаковые, и цис—транс-изомеры бутен-1 не образует. А вот в молекуле бутена-2 CH3—CH=CH-CH3 заместители у каждого атома углерода при двойной связи разные (атом водорода и метильная группа CH3), поэтому бутен-2 образует цис— и транс-изомеры.
Таким образом, для соединений вида СH2=СHR и СR2=СHR’ цис—транс-изомерия не характерна.
2. Оптическая изомерия
Оптические изомеры – это пространственные изомеры, молекулы которых соотносятся между собой как предмет и несовместимое с ним зеркальное изображение.
Оптическая изомерия свойственна молекулам веществ, имеющих асимметрический атом углерода.
Асимметрический атом углерода — это атом углерода, связанный с четырьмя различными заместителями.
Такие молекулы обладают оптической активностью — способностью к вращению плоскости поляризации света при прохождении поляризованного луча через раствор вещества.
Например, оптические изомеры образует 3-метилгексан:
Два основных понятия органической химии — гомологи и изомеры.
Гомологи — вещества, имеющие сходное строение и свойства, но различающиеся по составу на одну или несколько групп
CH2
.
Изомеры — вещества, имеющие одинаковый состав, но разное строение и свойства.
Изомеры могут различаться порядком соединения атомов в молекуле (химическим строением) или расположением атомов в пространстве. Поэтому различают структурную и пространственную изомерию.
Этот вид изомерии может быть обусловлен разным строением углеродного скелета, положением кратных связей или функциональных групп. Также есть межклассовая изомерия.
|
Изомерия углеродного скелета |
CH3−CH2−CH2−CH3 бутан |
изобутан |
|
Изомерия положения заместителей |
()CH3−CH2−CH2Cl()
(1)-хлорпропан |
() CH3−CHCl−CH3 () (2)-хлорпропан |
|
Изомерия положения кратных связей |
CH2=CH−CH2−CH3 бутен-(1) |
CH3−CH=CH−CH3 бутен-(2) |
|
Изомерия положения функциональных групп |
CH3−CH2−CH2−OH пропанол-(1) |
пропанол-(2) |
|
Межклассовая изомерия |
CH3−CH2−OH этанол |
CH3−O−CH3 диэтиловый эфир |
Пространственная изомерия
По расположению атомов в пространстве выделяют оптическую (энантиомерию) и геометрическую (цис-транс) изомерию.
Оптические изомеры являются зеркальным отражением друг друга. Оптические изомеры существуют в том случае, если в молекуле есть хотя бы один атом углерода, связанный с четырьмя разными группами. Такой атом называют оптически активным.
Геометрические изомеры отличаются расположением групп атомов относительно двойной связи: у цис-изомеров одинаковые группы атомов находятся с одной стороны, а у транс-изомеров — по разные стороны от двойной связи
C=C
. Этот вид изомерии возможен, если каждый из атомов, соединённых двойной связью, связан с разными атомами или группами атомов.
|
Оптическая изомерия (энантиомерия) |
(2)-бром-(2)-хлорэтанол |
(2)-бром-(2)-хлорэтанол |
|
Геометрическая изомерия (цис-транс-изомерия) |
цис-бутен-(2) |
|
Изомерия

4.6
Средняя оценка: 4.6
Всего получено оценок: 566.
4.6
Средняя оценка: 4.6
Всего получено оценок: 566.
Явление, при котором образуются соединения одинаковые по количеству атомов, но разные по структуре или пространственному расположению атомов, называется изомерией. Изомеры отличаются физическими и химическими свойствами. Изомерия свойственна всем органическим соединениям.
Классификация
Изомерия бывает двух типов:
- структурная – соединения отличаются строением молекул;
- пространственная – одинаковые по составу и строению вещества различаются пространственным расположением атомов.
Описание каждого типа представлено в таблице.
|
Изомерия |
Вид |
Определение |
|
Структурная |
Углеродного скелета |
Изомеры отличаются положением метильной группы -СН3 в углеродной цепи (может присоединяться к любому атому углерода) |
|
Положения |
Изомеры отличаются по положению:
|
|
|
Межклассовая |
Из-за расположения функциональной группы образуется вещество другого класса: CH3-CH2-OH (этанол) и CH3-O-CH3 (диметиловый эфир) |
|
|
Пространственная |
Оптическая или зеркальная |
Изомеры зеркально отражают друг друга |
|
Геометрическая |
Изомеры отличаются положением радикалов относительно плоскости. Характерна для классов веществ, содержащих двойные связи, а также для циклических соединений. Бывает двух типов:
|
Чем больше атомов углерода в молекуле, тем больше изомеров может образовывать соединение.
Номенклатура
Названия изомеров состоят из трёх частей:
- номер атома углерода, к которому присоединены дополнительные группы;
- название группы;
- название главной цепи.
За главную цепь принимается самая длинная цепочка атомов углерода. Например, если к цепи из пяти атомов углерода присоединена цепочка из двух атомов углерода, главной считается пятиуглеродная цепь.
Отсчёт атомов начинается с конца с разветвлением или большим количеством разветвлений. Структурная формула изомерии помогает наглядно определить, какой атом является первым.
Примеры изомеров с названиями:
- СН3-СН(СН3)-СН2-СН2-СН3 – 2-метилпентан (метильная группа находится у второго атома углерода);
- СН3-СН2-СН(СН3)-СН2-СН3 – 3-метилпентан;
- СН3-СН(СН3)-СОН – 2-метилпропаналь.
Изомеры имеют одинаковую молекулярную формулу, но разные структурные формулы.
Что мы узнали?
Из урока химии 10 класса узнали о явлении изомерии. Изомеры – соединения с одинаковым количеством атомов, но с разным строением или пространственным положением. При структурной изомерии меняется положение в углеродной цепи двойной связи, метильной группы или радикала. Пространственная изомерия бывает двух типов – оптическая (зеркальная) и геометрическая. Структурные названия изомеров обуславливаются положением функциональных групп и радикалов.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Тайсон Коняхин
5/5
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 566.
А какая ваша оценка?
Органическая химия — раздел, который вызывает больше всего вопросов. Сложность заключается в первую очередь в огромном количестве веществ: ученым известно более миллиона. Но не нужно пугаться. В органике соединения поделены на классы, свойства внутри которых очень похожи. Выучив общие реакции для каждой группы веществ, вы сможете с легкостью решать задания. Первая тема в рамках подготовки к ЕГЭ — изомерия и номенклатура органических соединений. В статье мы разберем основы этого раздела. Более подробно материал рассматривается на подготовительных курсах. Там изучаются все сложные вопросы органической химии, поэтому выпускники набирают высокие баллы на ЕГЭ.
Изомерия
Первый вопрос, который мы рассмотрим — изомерия органических соединений в химии. Под этим термином понимают явление существования веществ-изомеров. Изомеры — это соединения, имеющие одинаковый качественный и количественный состав (то есть молекулярную формулу), но разное строение и свойства (то есть структурную формулу).
Для начала разберемся в формулах органических соединений. Молекулярная показывает только тип атомов и их количество. Например, C5H10OH. Структурная отражает взаимное расположение атомов в молекуле. Приведенная молекулярная формула может принадлежать сразу нескольким веществам, так как гидроксильная группа может располагаться у разных атомов. Под формулой может скрываться пентанол-1 CH3-CH2-CH2-CH2-CH2-OH, пентанол-2 CH3-CH2-CH2-CH(OH)-CH3 или пентанол-3 CH3-CH2-CH(OH)-CH2-CH3. Эти вещества, имеющие разное взаимное расположение атомов, и называются изомерами.
Различают два вида изомерии — пространственную и структурную. Структурная изомерия подразумевает различный порядок расположения атомов в молекуле. Делится на несколько типов:
- углеродного скелета. Различное расположение радикалов в молекуле: СН3— СН2-СН2-СН2-CH3 (н-пентан) и СН3-СН2-СН(CH3)-CH3 (2-метилбутан);
- положения кратной связи. Двойные и тройные связи могут располагаться у разных атомов. Изомерами являются бутен-1 СН2=СН-СН2-СН3 и бутен-2 СН3-СН=СН2-СН3;
- положения функциональной группы. Пример — уже рассмотренный выше пентанол;
- межклассовая. Иногда под одной формулой скрываются вещества разных классов. Такими изомерами являются алкины и алкадиены, алкены и циклоалканы, спирты и простые эфиры, альдегиды и кетоны, сложные эфиры и карбоновые кислоты. Пример: метилацетат CH3-COO-CH3 и пропановая кислота CH3-CH2-COOH;
- взаимного расположения заместителей. Характерна для циклических соединений (аренов, циклоалканов, циклов с кратными связями). Когда в кольцо вносится второй заместитель, он может располагаться в одном из трех положений: орто (у соседних атомов углерода), мета (через один атом) и пара (напротив друг друга). Это касается ароматических соединений. В циклоалканах заместители обозначают цифрами, например, 1,2-диметилциклобутан;
- метамерия. Связана с разным положением гетероатома в молекуле. Гетероатом — это азот, сера, кислород. Такими изомерами могут быть амины, например, этиламин СН3–СН2–NH2 и диметиламин СН3–NH–СН3;
- таутомерия. Это явление, при котором два изомера легко переходят друг в друга. В таком случае вещество состоит сразу из нескольких молекул, устанавливается равновесие, которое смещается под действием внешних факторов. Пример веществ — пропанон и пропенол-2.
Вторым типом изомерии в органике является пространственная. Она связана с различным взаимным расположением атомов в молекуле. При этом сама структура остается прежней. Оптическая изомерия возникает при вращении атомов вокруг кратной связи. Она характерна для алкенов и алкинов. Аналогичное явление обнаружено у циклов с несколькими заместителями. В цис-изомерах одинаковые группы атомов расположены по одну сторону кратной связи или цикла, в транс — по разные стороны.
Оптическая изомерия характеризуется различным расположением молекул относительно одного атома. Это должен быть ассиметричный углерод — с четырьмя разными заместителями. Он называется хиральным центром. Изомеры являются зеркальным отражением друг друга, как правая и левая рука. Это дает им разные химические свойства.
Номенклатура
Переходим к классификации и номенклатуре органических соединений в химии. В рамках этой темы нужно понимать, какие классы соединений существуют и как их называть. В органике используется систематическая номенклатура ИЮПАК. Основа названия — корень, обозначающий самую длинную углеродную цепь. Первые 10 веществ в гомологическом ряду:
-
С1 — мет-;
-
С2 — эт-;
-
С3 — проп-;
-
С4 — бут-;
-
С5 — пент-;
-
С6 — гекс-;
-
С7 — гепт-;
-
С8 — окт-;
-
С9 — нон-;
-
С10 — дек-.
Далее идет суффикс. Самая простая номенклатура у углеводородов. Алканы имеют суффикс -ан (пропан), алкены — -ен (пропен), алкины — -ин (пропин). Если кратных связей 2 и больше, перед суффиксом добавляется соответствующая цифра — ди, три, тетра, пента и т.д. (бутадиен). У циклических соединений добавляется приставка цикло- (циклопропан). Суффиксами обозначают также наличие заместителей. Для этого используется -ил (этил). Расположение заместителя указывается цифрой, реже используются греческие буквы альфа, бета, гамма. Важный момент: за начало цепочки берется тот конец, у которого ближе кратная связь. Если ее нет, то учитывается близость заместителя. Названия аренов исходят от первого представителя — бензола. К нему добавляются соответствующие заместители, например, 1,2-диметилбензол.
В номенклатуру органических соединений в химии входят и функциональные группы. При нумерации атомов за начало принимается тот конец, ближе к которому располагается группа. Самая старшая указывается в суффиксе, остальные в приставке. Обозначения групп в порядке старшинства:
|
Класс |
Формула |
Название в приставке |
Название в суффиксе |
Пример |
|
Карбоновые кислоты |
-COOH |
карбокси- |
-овая кислота |
CH3COOH этановая кислота карбоксиэтан |
|
Сульфокислоты |
-SO3H |
сульфо- |
-сульфокислота |
CH3-SO3H Сульфометан Метилсульфокислота |
|
Нитрил |
-CN |
циано- |
-нитрил |
CH3-CN цианометан метилнитрил |
|
Альдегиды |
-CHO |
оксо- |
-аль |
CH3-CHO этаналь 1-оксоэтан |
|
Кетоны |
-CO |
оксо- |
-он |
CH3-CO-CH3 пропанон 2-оксопропан |
|
Спирты |
-OH |
гидрокси- |
-ол |
CH3OH метанол гидроксиметан |
|
Амины |
-NH2 |
амино- |
-амин |
CH3-CH2-NH2 этиламин аминоэтан |
|
Простые эфиры |
-OR |
алкокси- |
— |
CH3-O-CH3 алкоксиэтан |
|
Галогениды |
-F, -Cl, -Br, -I |
фтор-, хлор-, бром-, йод- |
-фторид, -хлорид, -бромид, -йодид |
CH3-Cl метилхлорид хлорметан |
|
Нитросоединения |
-NO2 |
нитро- |
— |
CH3-NO2 Нитрометан |
Пример названия
Мы разобрали изомерию и номенклатуру. Попробуем назвать сложное органическое вещество.
-
Определяем главную цепь. В этом случае возьмем за основу бензольное кольцо. У него есть группа -OH, поэтому в названии можем использовать корень -фенол.
-
Нумеруем атомы. Первым будет углерод с группой -OH, потому что мы взяли за основу фенол. Старшим заместителем является карбоксильная группа, но она находится напротив, то есть на равном расстоянии с обеих сторон. Следующий по старшинству заместитель — CH2Cl, он будет вторым. Далее идем по циклу.
-
Называем все заместители. CH2Cl — хлорметил, CH2-CH2-COOH — карбоксипропил, NO2 — нитрогруппа.
-
Записываем название соединения. Все группы указываются в алфавитном порядке. Не забываем указывать, около какого атома они стоят: 4-карбоксипропил-5-нитро-2-хлорметилфенол.
Итак, мы разобрались в классификации, изомерии и номенклатуре органических соединений. Это основы химии, поэтому представленный материал нужно знать наизусть. Обязательно решайте типовые задания из ЕГЭ по химии и тренируйтесь называть сложные вещества. Тема показалась вам трудной? Запишитесь на подготовительные курсы. Там преподаватели ответят на вопросы и разберут все сложные моменты. Желаем вам успехов на итоговой аттестации!
Изомерия (от греческих слов
«изос» – «равный» и «мерос» – «часть», «доля») — явление существования химических соединений — изомеров, — одинаковых по
составу и молекулярной массе, но различающихся по строению или расположению
атомов в пространстве и по свойствам.
Термин «изомерия» вёл в химию Й. Берцелиус
в 1830 году, а подлинное объяснение этот термин получил во второй половине 19
века на основе теории химического строения А. М. Бутлерова и стереохимического
учения Я. Вант-Гоффа.
Например, вам известно, что молекулярная формула бутана – С4Н10.
Бутан, в молекуле которого атомы расположены в виде линейной цепочки, называют
нормальным бутаном, а бутан, цепь атомов углерода которого разветвлена,
называют изобутаном. Эти два вещества имеют одинаковую молекулярную формулу, но
различаются по строению, а значит, и по свойствам.
Например, молекулярной формуле C2H6O соответствуют два
вещества с разными структурными формулами – этиловый спирт и
диметиловый эфир. Они также имеют одинаковый состав, по разное строение и
свойства. Этиловый спирт – жидкость, которая реагирует с металлическим
натрием с выделением водорода, кипит при +78,5 0С. При тех же
условиях диметиловый эфир – газ, не реагирующий с натрием, кипит при -23 0С.
Существуют два основных типа изомерии. Это структурная и пространственная.
Структурные изомеры – это изомеры, имеющие различный порядок
соединения атомов в молекуле.
Пространственные изомеры – это изомеры, которые имеют одинаковые
заместители у каждого атома углерода, но отличаются их взаимным расположением в
пространстве.
Различают три вида структурной изомерии. Это изомерия углеродного
скелета, обусловленная различным порядком связи атомов углерода, изомерию
положения, обусловленную различным положением функциональных групп или
кратных связей при одинаковой углеродной цепи.
Изомерия углеродного скелета характерна для любых классов
органических соединений. Например, для вещества С4Н10 изомерами
будут бутан и 2-метилпропан, для С5Н8 – это пентин и
3-метилбутин-1, для С5Н10О2 – это пентановая
кислота и 2-метилбутановая кислота, 3-метилбутановая кислота, для С5Н12О
– это пентанол-1 и 2-метилбутанол-1, для С4Н8О2
– это пропилметаноат и изопропилметаноат.
Если рассмотреть изомерию положения кратной связи или функциональной
группы, то существуют структурные изомеры с одинаковым углеродным скелетом,
которые отличаются положением кратных связей (двойных и тройных) или
функциональных групп.
Например, изомерия положения кратных связей характерна для алкенов,
алкинов и диенов. Так, изомерами по отношению друг к другу будут бутен-1 и
бутен-2, бутин-1 и бутин-2, бутадиен-1,2 и бутадиен-1,3. Изомерия положения
функциональных групп характерна для спиртов и аминов. Так пропанол-1 и
пропанол-2 будут по отношению к друг другу изомерами, как и
бутанамин-1 и бутанамин-2, α-аминопропановая кислота и
β-аминопропановая кислота.
В межклассовой изомерии вещества относятся к различным классам
органических соединений, как этанол и диметиловый эфир имеют общую формулу – С2Н6О
или бутин-1 и бутадиен-1,3, относящиеся к классам алкинов и диенов, а также
этановая кислота и метилметаноат (то есть насыщенные одноосновные карбоновые
кислоты и сложные эфиры).
Различают два вида пространственной изомерии: геометрическую и
оптическую. Геометрическая изомерия характерна для соединений с двойной
углерод-углеродной связью. Так для молекулы бутена-2 характерно 2 изомера:
цис-изомер и транс-изомер. У цис-изомера одинаковые
группы атомов находятся по одну сторону от плоскости, а у транс-изомера
– по разные стороны.
Другим примером пространственных изомеров являются циклические α- и
β-формы глюкозы, различающиеся положением гидроксильных групп у первого
атома углерода.
Оптической изомерией обладают только те вещества, у которых есть асимметрический,
или хиральный атом (от греческого хирос – «рука», «образец
несимметричной фигуры»), то есть это атом, который связан с четырьмя различными
заместителями. Оптические изомеры являются зеркальным изображением друг друга,
подобно двум ладоням и несовместимы. Так, молочная кислота, или
2-оксипропановая кислота, существует в виде двух оптических изомеров, потому
что она содержит 1 асимметрический атом углерода.
Оптическая изомерия называется также энантиомерией (от
греческого enantios – «противоположный» и meros –
«часть»), а оптические изомеры – энантиомерами. У
хиральных молекул возникают изомерные пары, в которых молекулы изомеров
различаются пространственной организацией, точно также, как предмет и его
зеркальное отражение. Пара таких изомеров имеют, как правило, одинаковые
химические и физические свойства, но разную оптическую активность: если один
изомер вращает плоскость поляризованного света по часовой стрелке, то другой –
обязательно против. Тогда один изомер называют правовращающим, а второй –
левовращающим.