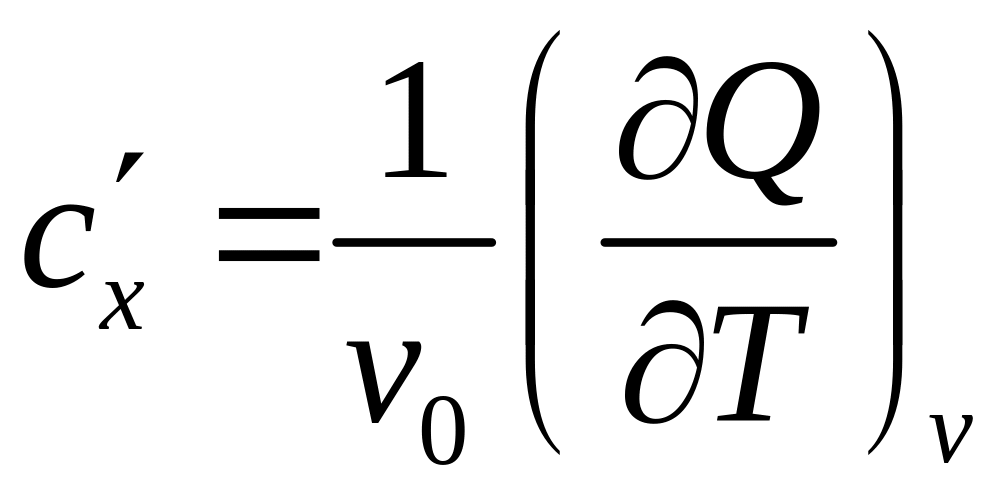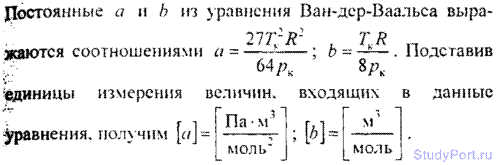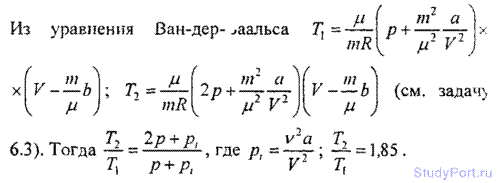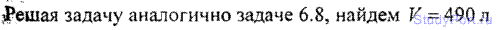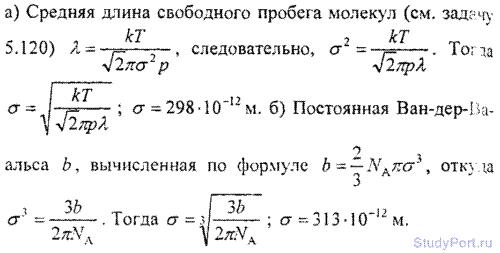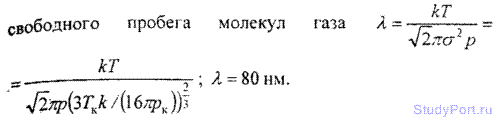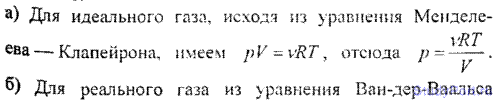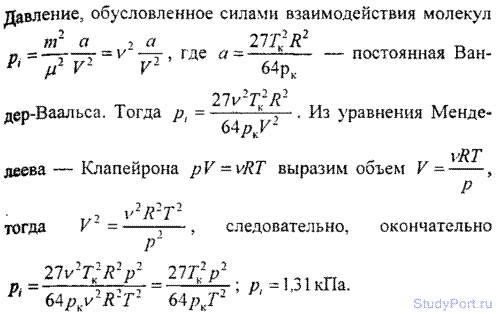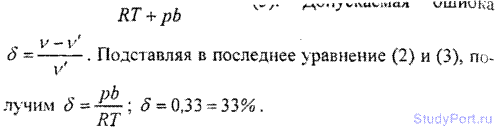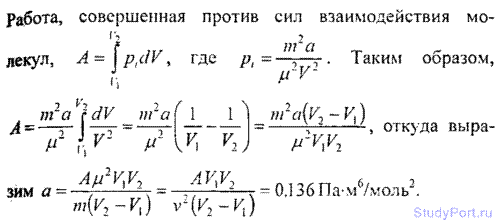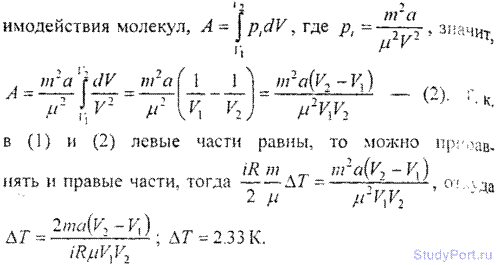-
Уравнение состояния идеального газа
Уравнение Клапейрона
,
или
.
Это
уравнение записано для 1
кг
идеального газа. Умножая обе части
уравнения на молекулярный вес, выраженный
в кг
,
получим уравнение, записанное для 1
кмоля
идеального газа
,
где
– объем 1
кмоля
;
– универсальная
газовая постоянная
или
– уравнение
Менделеева-Клайперона.
Тогда
газовая постоянная
для конкретного газа находится как:
.
При
нормальных физических условиях (НФУ)
ртутного столба,
объем 1 кмоль любого газа составляет
.
Задача
2.1.
Определить
температуру газа, если при
объем 0,5 кмоля составляет
.
Решение.
Находим объем 1
кмоля при заданных условиях
.
Подставляем это
значение в формулу Менделеева-Клайперона,
имеем
.
Задача
2.2.
Найти
плотность метана при НФУ.
Решение.
,
,
.
Задача
2.3.
По
трубопроводу
подается аммиак при давлении
и температуре
.
Скорость потока
.
Найти массовый расход газа.
Решение.
,
,
,
.
Задача
2.4.
Давление
водяных паров в комнате
.
Температура воздуха
.
Объем комнаты
.
Найти массу пара.
Решение.
Водяной
пар при данном парциальном давлении и
температуре находится в перегретом
состоянии и по свойствам близок к
идеальному газу.
;
;
;
.
-
Теплоемкость
Теплоемкостью
тела называется отношение количества
теплоты, подведенной или отведенной в
определенном термодинамическом процессе,
к изменению его температуры.
,
где
х
– параметр, сохраняющийся постоянным
в течение процесса, например
.
Данное уравнение определяет истинную
теплоемкость газа. Различают следующие
виды удельной теплоемкости:
Удельная
массовая теплоемкость:

Удельная объемная
теплоемкость:
;
,
где
– удельный объем при нормальных
физических условиях;
Удельная
молярная теплоемкость:
,
где
– число кмолей вещества.
Теплоемкости
и
для идеального газа связаны следующими
соотношениями:
– показатель
адиабаты;
– уравнение Майера.
Из
этих двух уравнений имеем для идеального
газа:
;
.
Теплоемкость
в политропном процессе с показателем
политропы
.
Кроме
истинных теплоемкостей в расчетах
употребляют средние теплоемкости
,
равные отношению количества теплоты
выделившейся в конечном процессе 1-2 к
конечному изменению температуры
.
.
Здесь
учитываем, что
.
Теплоемкость
(истинная и средняя) является функцией
температуры. Для технических расчетов
часто принимают линейную зависимость
теплоемкости от температуры
.
В
таблице приведены формулы для средней
мольной теплоемкости при
для некоторых газов. Эти данные могут
быть также приведены в табличном виде.
|
Газ |
|
|
Азот |
28,97+0,002566 |
|
Водород |
28,78+0,001117 |
|
Кислород |
29,56+0,003404 |
|
Воздух |
28,09+0,002412 |
|
Водяной пар |
32,85+0,00544 |
Если
требуется найти расход теплоты для
нагрева газа от
до
,
пользуясь вышеуказанными средними
теплоемкостями, тогда определяют теплоты
и
,
необходимые для нагрева газа от
до
и от
до
.
,
.
Средняя
теплоемкость в пределах от
до
определяется как:
.
Данные
об истинной и средней теплоемкости
различных газов в интервале температур
приводятся в таблицах.
Задача
3.1.
В
баллоне объемом 20 л содержится воздух
при давлении
и температуре
.
Сколько нужно подвести к нему теплоты,
чтобы температура достигла
?
Теплоемкость
воздуха считать постоянной.
Решение.
Рассматривается
изохорный процесс
.
Для
воздуха:
.
Количество
воздуха в баллоне:
.
Количество
подведенного тепла:
.
Здесь
учтено, что
.
Задача
3.2.
По
экспериментальным данным молярная
теплоемкость аммиака при
,
а при
.
Определить линейную зависимость
теплоемкости от температуры.
Решение.
Примем
зависимость в виде:
.
Запишем
эту зависимость для двух температур:
Решая
совместно эти уравнения относительно
А и В, получим:
.
Искомая
зависимость:
.
Задача
3.3.
Воздух
в теплоизолированной трубе нагревается
электрическим током
и
на
.
Объемный расход воздуха
.
Давление 1 бар, температура воздуха на
входе
.
Найти удельную массовую теплоемкость
воздуха
.
Решение.
Рассматривается
подвод теплоты к потоку при
.
Находим массовый расход воздуха:
.
Мощность
электрического нагревателя:
.
Уравнение
тепловой мощности:
,
откуда
.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Страница 1 из 2
6.1. В каких единицах системы СИ выражаются постоянные а и b, входящие в уравнение Ван-дер-Ваальса?
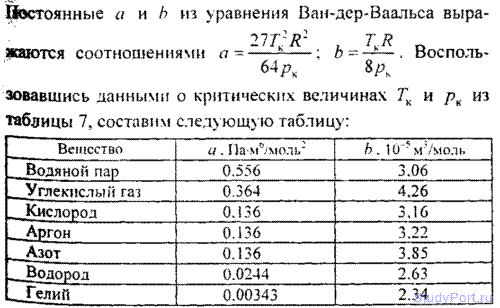
6.2. Пользуясь данными о критических величинах Тк и pк для некоторых газов (смотри таблицу), найти для них постоянные а и b , входящие в уравнение Ван-дер-Ваальса.
6.3. Какую температуру Т имеет масса m = 2 г азота, занимающего объем V = 820cm3 при давлении p = 0,2 МПа? Газ рассматривать как: а) идеальный; б) реальный.
6.4. Какую температуру Т имеет масса m = 3,5 г кислорода занимающего объем F=90cm3 при давлении p = 2,8МПа? Газ рассматривать как: а) идеальный; б) реальный.
6.5. Масса m = 10 г гелия занимает объем V = 100 см3 при давлении p = 100 МПа. Найти температуру Т газа, считая его: а) идеальным; б) реальным.
6.6. Количество v = 1 кмоль углекислого газа находится при температуре t = 100° С. Найти давление p газа, считая его:
а) реальным; б) идеальным. Задачу решить для объемов V1 = 1 м3
и V2= 0,05 м3.
6.7. В закрытом сосуде объемом V = 0,5 м3 находятся коли-
чество v = 0.6 кмоль углекислого газа при давлении p = 3 МПа.
Пользуясь уравнением Ван-дер-Ваальса, найти, во сколько раз надо увеличить температуру газа, чтобы давление увеличилось вдвое.
6.8. Количество v = 1 кмоль кислорода находится при температуре t=21°C и давлении p = 10МПа. Найти объем V газа,
считая, что кислород при данных условиях ведет себя как реальный газ.
6.9. Количество v = 1 кмоль азота находится при температуре t = 27°C и давлении p = 5МПа. Найти объем V газа, считая, что азот при данных условиях ведет себя как реальный газ.
6.10. Найти эффективный диаметр а молекулы кислорода, считая известными для кислорода критические значения Тк и pк.
6.11. Найти эффективный диаметр а молекулы азота двумя способами: а) по данному значению средней длины свободного пробега молекул при нормальных условиях ? = 95 нм; б) по известному значению постоянной b в уравнении Ван-дер-Ваальса.
6.12. Найти среднюю длину свободного пробега ? молекул углекислого газа при нормальных условиях. Эффективный диаметр б молекулы вычислить, считая известными для углекислого газа критические значения Tk и pk.
6.1З. Найти коэффициент диффузии D гелия при температуре t = 17° С и давлении p = 150 КПа. Эффективный диаметр атома б вычислить, считая известными для гелия критические значения Тk и pk.
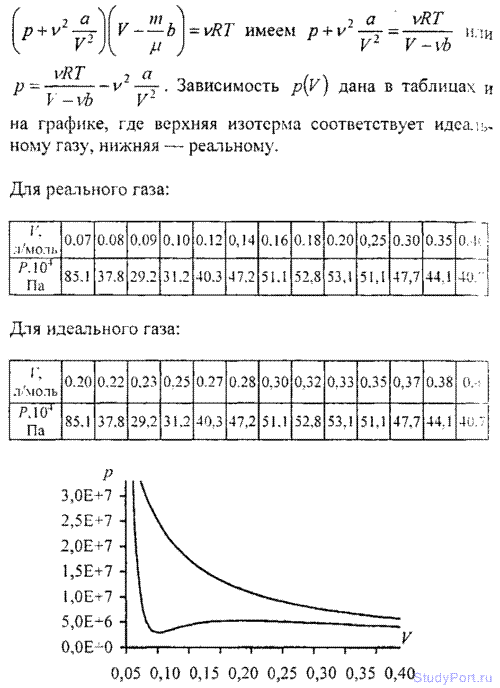
6.14. Построить изотермы p = f(v) для количества v = 1 кмоль углекислого газа при температуре t = 0° С. Газ рассматривать как: а) идеальный; б) реальный. Значения V (в л/моль) для реального газа взять следующие: 0,07, 0,08, 0,10, 0,12, 0,14, 0,16, 0,18, 0,20, 0,25, 0,30, 0,35 и 0,40; для идеального газа — в интервале 0,2 < V < 0,4 л/моль.
6.15. Найти давление p1, обусловленное силами взаимодействия молекул, заключенных в количестве v = 1 кмоль газа при нормальных условиях. Критическая температура и критическое давление этого газа равны Тk = 417 К и pk = 7,7 МПа.
6.16. Для водорода силы взаимодействия между молекулами незначительны; преимущественную роль играют собственные размеры молекул. Написать уравнение состояния такого полуидеального газа. Какую ошибку мы допустим при нахождении количества водорода v, находящегося в некотором объеме при температуре t = 0° С и давлении p = 280 МПа, не учитывая собственного объема молекул?
6.17. В сосуде объемом V = 10 л находится масса m = 0,25 кг азота при температуре t = 27° С. Какую часть давления газа составляет давление, обусловленное силами взаимодействия молекул? Какую часть объема сосуда составляет собственный объем молекул?
6.18. Количество v = 0.5 кмоль некоторого газа занимает объ-ем V1=1m3. При расширении газа до объема V2 = 1.2 м3 была
совершена работа против сил взаимодействия молекул A =5,684 кДж. Найти постоянную а, входящую в уравнение Ван-дер-Ваал ьса.
6.19. Масса m = 20 кг азота адиабатически расширяется в вакуум от объема V1 = 1 м3 до объема V2 = 1 м3. Найти понижение
температуры dT при этом расширении, считая известной для азота постоянную а, входящую в уравнение Ван-дер-Ваальса (смотри ответ 6.2).
6.20. Количества v = 0,5 кмоль трехатомного газа адиабатически расширяется в вакуум от объема V1 = 0,5 м3 до объема V2 = 3 м3. Температура газа при этом понижается на dT = 122 К. Найти постоянную а. входящую в уравнение Ван-дер-Ваальса.
Как найти число молекул в газе
Молекула — это электрически нейтральная частица, обладающая всеми химическими свойствами, присущими данному конкретному веществу. В том числе и газам: кислороду, азоту, хлору и т.д. Как можно определить количество молекул газа?

Инструкция
Если вам необходимо подсчитать, сколько молекул кислорода содержится в 320 граммах этого газа при нормальных условиях, прежде всего, определите, какое количество молей кислорода заключено в этом количестве. По таблице Менделеева, можно увидеть, что округленная атомная масса кислорода – 16 атомных единиц. Поскольку молекула кислорода – двухатомная, масса молекулы составит 32 атомные единицы. Следовательно, количество молей 320/32 = 10.
Дальше вам поможет универсальное число Авогадро, названное в честь ученого, предположившего, что равные объемы идеальных газов при постоянных условиях содержат одинаковые количества молекул. Оно обозначается символом N(A) и очень велико – приблизительно составляет 6,022*10(23). Умножьте это число на вычисленное количество молей кислорода и вы узнаете, что искомое количество молекул в 320 граммах кислорода – 6,022*10(24).
А если вам известно давление кислорода, а также объем, занимаемый им, и температура? Как вычислить количество его молекул при таких данных? И тут нет ничего сложного. Надо лишь записать универсальное уравнение Менделеева-Клапейрона для идеальных газов:
PV = RTM/m
Где P – давление газа в паскалях, V – его объем в кубических метрах, R – универсальная газовая постоянная, M – масса газа, а m – его молярная масса.
Cлегка преобразуя это уравнение, вы получите:
M = PVm/RT
Поскольку у вас есть все необходимые данные (давление, объем, температура заданы изначально, R = 8,31, а молярная масса кислорода = 32 грамма/моль), вы элементарно найдете массу газа при данном объеме, давлении и температуре. А дальше задача решается точно так же, как и в вышеописанном примере: N(A)M/m. Произведя вычисления, вы узнаете, сколько молекул кислорода содержится при заданных условиях.
Можно еще более упростить решение, поскольку в полученной дроби N(A)PVm/RTm молярные массы сокращаются, и остается: N(A)PV/RT. Подставив в формулу известные вам величины, вы получите ответ.
Видео по теме
Полезный совет
Ни один реальный газ (включая кислород), конечно же, не является идеальным, поэтому уравнение Менделеева-Клапейрона можно использовать для расчетов лишь при условиях, не очень сильно отличающихся от нормальных.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
На практике часто встречаются такие изменения состояния газа, когда одновременно изменяются все три параметра – объем VV, давление pp и температура TT. В таких случаях зависимость между параметрами определяется уравнением состояния газа.
Уравнение Клапейрона
Рассмотрим процесс, в результате которого газ перешел из нормального состояния с параметрами V0V_0, p0p_0, T0T_0 в состояние с другими параметрами V1V_1, p1p_1, T1T_1.
Такой переход от начального к конечному состоянию газа можно осуществить с помощью двух известных процессов (например, сначала изобарического, а затем изотермического) по схеме:
I.V0,p0,T0;V′,p0,T;V′=V0TT0I.{{V}_{0}},{{p}_{0}},{{T}_{0}};{V}’,{{p}_{0}},T;{V}’={{V}_{0}}frac{T}{{{T}_{0}}}
II.V′,p0,T;V,p,T;p0V′=pVII.{V}’,{{p}_{0}},T;V,p,T;{{p}_{0}}{V}’=pV
Исключив из двух полученных уравнений объем V′V’ для промежуточного состояния газа, получим
pVT=p0V0T0frac{pV}{T}=frac{{{p}_{0}}{{V}_{0}}}{{{T}_{0}}}
то есть получим уравнение:
pV=ВТpV = ВТ.
Это уравнение вывел французский ученый Б. П. Э. Клапейрон в 1834 году. Постоянная BB в нем – постоянная зависимости от природы газа и его количества. Эту постоянную, рассчитанную для единицы массы газа, называют удельной газовой постоянной B0B_0.
В качестве примера вычислим удельный газовую постоянную для воздуха. Объем 1 кг воздуха – удельный объем воздуха в нормальных условиях (давление 1,013 · 105 Па и температура 273,15 К)
V0=1ρ0=11,293(м3кг){{V}_{0}}=frac{1}{{{rho }_{0}}}=frac{1}{1,293}(frac{{{м}^{3}}}{кг})
Отсюда:
B0=p0V0T0=p0V0273=1,013⋅1051,293⋅273=287,1(Джкг⋅К){{B}_{0}}=frac{{{p}_{0}}{{V}_{0}}}{{{T}_{0}}}=frac{{{p}_{0}}{{V}_{0}}}{273}=frac{1,013cdot {{10}^{5}}}{1,293cdot 273}=287,1(frac{Дж}{кгcdot К})
Аналогично вычислено, что удельная газовая постоянная для водорода равна 4125, для кислорода – 295,7; для азота – 296,7 Дж / (кг · К) и т. д.
Преобразования Менделеева
В 1874 г. русский химик Д. И. Менделеев, воспользовавшись законом Авогадро, предоставил уравнение Клапейрона в более удобном для использования виде. При этом оказалось целесообразным рассчитывать постоянную для газов, взятых в количестве 1 моль или 1 кмоль:
Rm=p0V0mT0=1,013⋅105⋅0,0224273=8,31(Джмоль⋅K){{R}_{m}}=frac{{{p}_{0}}{{V}_{0m}}}{{{T}_{0}}}=frac{1,013cdot {{10}^{5}}cdot 0,0224}{273}=8,31(frac{Дж}{мольcdot K})
Постоянную RmR_m (или просто RR) называют универсальной газовой постоянной. Уравнение состояния в расчете на 1 моль идеального газа имеет вид, аналогичный уравнению Клапейрона:
pV=RmTpV={{R}_{m}}T
В таком виде уравнения состояния идеального газа называют уравнением Клапейрона-Менделеева.
Кроме единицы количества вещества – моль – разрешается применять кратные и дольные от ее величины. В пересчете на кмоль RR составит:
R=1,013⋅105⋅22,4273=8,31⋅103(Джкмоль⋅K)R=frac{1,013cdot {{10}^{5}}cdot 22,4}{273}=8,31cdot {{10}^{3}}(frac{Дж}{кмольcdot K})
В расчете на 1 кмоль идеального газа уравнение записывают так:
pV=RTpV = RT,
а для любой массы mm – так:
pV=mμRTpV=frac{m}{mu }RT
где μμ – масса, которую имеет кмоль газа.
Для удобства расчетов преимущественно пользуются именно этой формой уравнения.
По данному уравнению легко находим зависимость плотности газа от давления и температуры, а именно:
mV=μpRTfrac{m}{V}=frac{mu p}{RT},
ρ=μpRTrho =frac{mu p}{RT}
Таковы в общем виде эмпирические закономерности в свойствах идеального газа.
Физическая суть постоянной
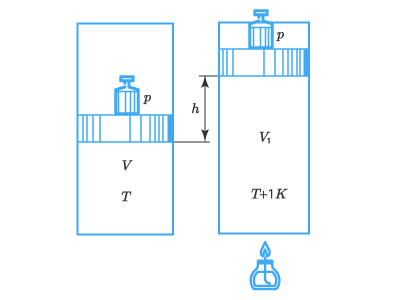
Для выяснения физической сути постоянной RR представим 1 кмоль газа под поршнем в некоем цилиндре:
При этом давление в нем составляет рр, температура – ТТ, а площадь поршня SS.
Повысим температуру газа внутри цилиндра от ТТ до (Т+1КТ + 1 К). Газ расширяется и выполняет работу, поднимая поршень на высоту hh. Эта работа составит:
А=pShА = pSh,
но Sh=ΔVSh = ΔV – прирост объема газа при расширении;
поэтому А=pΔVА = pΔV.
Данное выражение определяет работу газа в изобарическом процессе.
Применив уравнение Клапейрона-Менделеева к начальному и конечному состояниям газа, получим:
pV=RT;pV1=R(T+1K)pV=RT;p{{V}_{1}}=R(T+1K)
Отняв от второго уравнения первое, получим:
p(V1−V)=R;R=pΔVp({{V}_{1}}-V)=R;R=pDelta V
Сопоставим данное равенство с уравнением работы по подъему и найдем, что R=АR = А, то есть универсальная газовая постоянная численно равна работе расширения одного кмоль газа при изобарическом нагревании на 1К1 К.
Тест по теме: “Уравнение Клапейрона-Менделеева”
В этой статье мы коснемся нескольких краеугольных понятий в химии, без которых совершенно невозможно
решение задач. Старайтесь понять смысл физических величин, чтобы усвоить эту тему.
Я постараюсь приводить как можно больше примеров по ходу этой статьи, в ходе изучения вы увидите множество примеров
по данной теме.

Относительная атомная масса — Ar
Представляет собой массу атома, выраженную в атомных единицах массы. Относительные атомные массы указаны в периодической
таблице Д.И. Менделеева. Так, один атом водорода имеет атомную массу = 1, кислород = 16, кальций = 40.
Относительная молекулярная масса — Mr
Относительная молекулярная масса складывается из суммы относительных атомных масс всех атомов, входящих в состав вещества.
В качестве примера найдем относительные молекулярные массы кислорода, воды, перманганата калия и медного купороса:
Mr (O2) = (2 × Ar(O)) = 2 × 16 = 32
Mr (H2O) = (2 × Ar(H)) + Ar(O) = (2 × 1) + 16 = 18
Mr (KMnO4) = Ar(K) + Ar(Mn) + (4 × Ar(O)) = 39 + 55 + (4 * 16) = 158
Mr (CuSO4*5H2O) = Ar(Cu) + Ar(S) + (4 × Ar(O)) + (5 × ((Ar(H) × 2) +
Ar(O))) = 64 + 32 + (4 × 16) + (5 × ((1 × 2) + 16)) = 160 + 5 * 18 = 250
Моль и число Авогадро
Моль — единица количества вещества (в системе единиц СИ), определяемая как количество вещества, содержащее столько же структурных единиц
этого вещества (молекул, атомов, ионов) сколько содержится в 12 г изотопа 12C, т.е. 6 × 1023.
Число Авогадро (постоянная Авогадро, NA) — число частиц (молекул, атомов, ионов) содержащихся в одном моле любого вещества.

Больше всего мне хотелось бы, чтобы вы поняли физический смысл изученных понятий. Моль — международная единица количества вещества, которая
показывает, сколько атомов, молекул или ионов содержится в определенной массе или конкретном объеме вещества. Один моль любого вещества
содержит 6.02 × 1023 атомов/молекул/ионов — вот самое важное, что сейчас нужно понять.
Иногда в задачах бывает дано число Авогадро, и от вас требуется найти, какое вам дали количество вещества (моль). Количество вещества в химии
обозначается N, ν (по греч. читается «ню»).
Рассчитаем по формуле: ν = N/NA количество вещества 3.01 × 1023 молекул воды и 12.04 × 1023 атомов углерода.
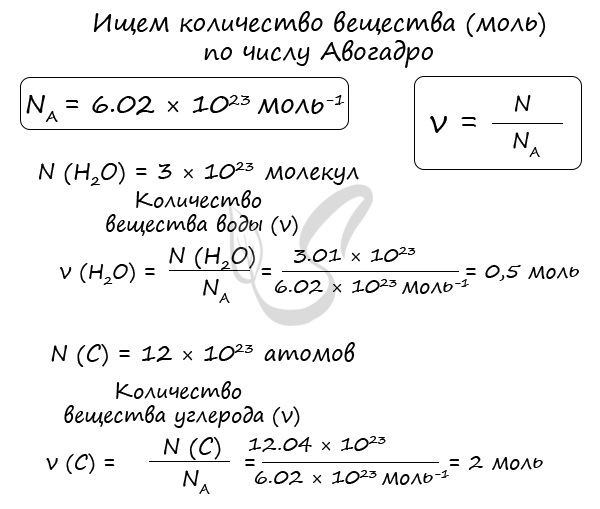
Мы нашли количества вещества (моль) воды и углерода. Сейчас это может показаться очень абстрактным, но, иногда не зная, как найти
количество вещества, используя число Авогадро, решение задачи по химии становится невозможным.
Молярная масса — M
Молярная масса — масса одного моля вещества, выражается в «г/моль» (грамм/моль). Численно совпадает с изученной нами ранее
относительной молекулярной массой.
Рассчитаем молярные массы CaCO3, HCl и N2
M (CaCO3) = Ar(Ca) + Ar(C) + (3 × Ar(O)) = 40 + 12 + (3 × 16) = 100 г/моль
M (HCl) = Ar(H) + Ar(Cl) = 1 + 35.5 = 36.5 г/моль
M (N2) = Ar(N) × 2 = 14 × 2 = 28 г/моль
Полученные знания не должны быть отрывочны, из них следует создать цельную систему. Обратите внимание: только что мы рассчитали
молярные массы — массы одного моля вещества. Вспомните про число Авогадро.
Получается, что, несмотря на одинаковое число молекул в 1 моле (1 моль любого вещества содержит 6.02 × 1023 молекул),
молекулярные массы отличаются. Так, 6.02 × 1023 молекул N2 весят 28 грамм, а такое же количество молекул
HCl — 36.5 грамм.
Это связано с тем, что, хоть количество молекул одинаково — 6.02 × 1023, в их состав входят разные атомы, поэтому и
массы получаются разные.

Часто в задачах бывает дана масса, а от вас требуется рассчитать количество вещества, чтобы перейти к другому веществу в реакции.
Сейчас мы определим количество вещества (моль) 70 грамм N2, 50 грамм CaCO3, 109.5 грамм HCl. Их молярные
массы были найдены нам уже чуть раньше, что ускорит ход решения.

ν (CaCO3) = m(CaCO3) : M(CaCO3) = 50 г. : 100 г/моль = 0.5 моль
ν (HCl) = m(HCl) : M(HCl) = 109.5 г. : 36.5 г/моль = 3 моль
Иногда в задачах может быть дано число молекул, а вам требуется рассчитать массу, которую они занимают. Здесь нужно использовать
количество вещества (моль) как посредника, который поможет решить поставленную задачу.
Предположим нам дали 15.05 × 1023 молекул азота, 3.01 × 1023 молекул CaCO3 и 18.06 × 1023 молекул
HCl. Требуется найти массу, которую составляет указанное число молекул. Мы несколько изменим известную формулу, которая поможет нам связать
моль и число Авогадро.

Теперь вы всесторонне посвящены в тему. Надеюсь, что вы поняли, как связаны молярная масса, число Авогадро и количество вещества.
Практика — лучший учитель. Найдите самостоятельно подобные значения для оставшихся CaCO3 и HCl.
Молярный объем
Молярный объем — объем, занимаемый одним молем вещества. Примерно одинаков для всех газов при стандартной температуре
и давлении составляет 22.4 л/моль. Он обозначается как — VM.
Подключим к нашей системе еще одно понятие. Предлагаю найти количество вещества, количество молекул и массу газа объемом
33.6 литра. Поскольку показательно молярного объема при н.у. — константа (22.4 л/моль), то совершенно неважно, какой газ мы
возьмем: хлор, азот или сероводород.
Запомните, что 1 моль любого газа занимает объем 22.4 литра. Итак, приступим к решению задачи. Поскольку какой-то газ
все же надо выбрать, выберем хлор — Cl2.


Моль (количество вещества) — самое гибкое из всех понятий в химии. Количество вещества позволяет вам перейти и к
числу Авогадро, и к массе, и к объему. Если вы усвоили это, то главная задача данной статьи — выполнена 

Относительная плотность и газы — D
Относительной плотностью газа называют отношение молярных масс (плотностей) двух газов. Она показывает, во сколько раз одно вещество
легче/тяжелее другого. D = M (1 вещества) / M (2 вещества).
В задачах бывает дано неизвестное вещество, однако известна его плотность по водороду, азоту, кислороду или
воздуху. Для того чтобы найти молярную массу вещества, следует умножить значение плотности на молярную массу
газа, по которому дана плотность.
Запомните, что молярная масса воздуха = 29 г/моль. Лучше объяснить, что такое плотность и с чем ее едят на примере.
Нам нужно найти молярную массу неизвестного вещества, плотность которого по воздуху 2.5

Предлагаю самостоятельно решить следующую задачку (ниже вы найдете решение): «Плотность неизвестного вещества по
кислороду 3.5, найдите молярную массу неизвестного вещества»

Относительная плотность и водный раствор — ρ
Пишу об этом из-за исключительной важности в решении
сложных задач, высокого уровня, где особенно часто упоминается плотность. Обозначается греческой буквой ρ.
Плотность является отражением зависимости массы от вещества, равна отношению массы вещества к единице его объема. Единицы
измерения плотности: г/мл, г/см3, кг/м3 и т.д.
Для примера решим задачку. Объем серной кислоты составляет 200 мл, плотность 1.34 г/мл. Найдите массу раствора. Чтобы не
запутаться в единицах измерения поступайте с ними как с самыми обычными числами: сокращайте при делении и умножении — так
вы точно не запутаетесь.

Иногда перед вами может стоять обратная задача, когда известна масса раствора, плотность и вы должны найти объем. Опять-таки,
если вы будете следовать моему правилу и относится к обозначенным условным единицам «как к числам», то не запутаетесь.
В ходе ваших действий «грамм» и «грамм» должны сократиться, а значит, в таком случае мы будем делить массу на плотность. В противном случае
вы бы получили граммы в квадрате 
К примеру, даны масса раствора HCl — 150 грамм и плотность 1.76 г/мл. Нужно найти объем раствора.

Массовая доля — ω
Массовой долей называют отношение массы растворенного вещества к массе раствора. Важно заметить, что в понятие раствора входит
как растворитель, так и само растворенное вещество.
Массовая доля вычисляется по формуле ω (вещества) = m (вещества) / m (раствора). Полученное число будет показывать массовую долю
в долях от единицы, если хотите получить в процентах — его нужно умножить на 100%. Продемонстрирую это на примере.

Решим несколько иную задачу и найдем массу чистой уксусной кислоты в широко известной уксусной эссенции.
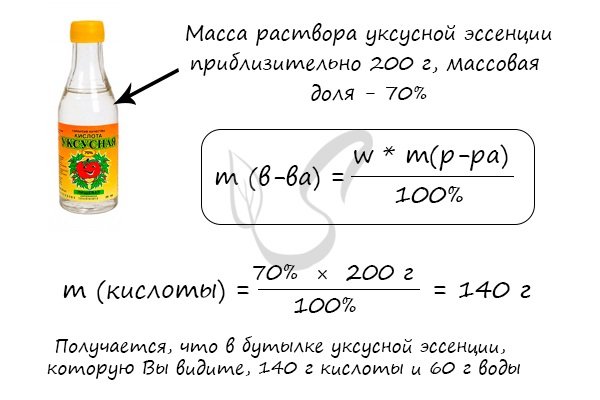
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.