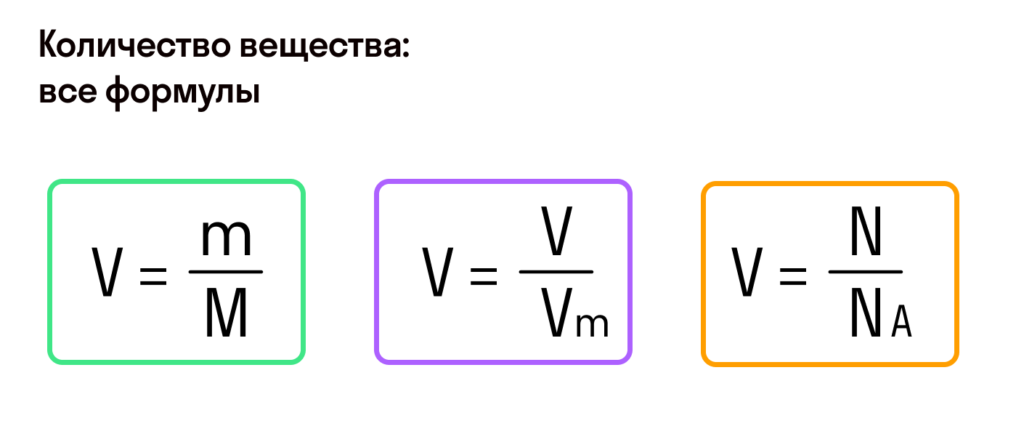
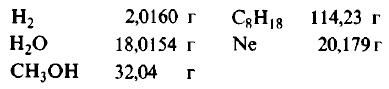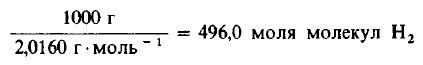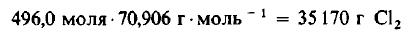Итак, количество вещества в химии обозначается греческой буквой «ню».
Помню, как в 9-м классе мой учитель физики Игорь Юрьевич учил меня правильно писать букву «ню». До этого она у меня получалась немного коряво.
Но поскольку на БВ не проходят греческие буквы, я буду обозначать количество вещества латинской буквой v. Латинская v очень похожа на греческую «ню».
Рассмотрим следующие случаи.
1) Если нам известно количество частиц вещества, то количество вещества можно найти по формуле:
v = n/NA
где
v — количество вещества;
n — количество частиц вещества. Это безразмерная величина, то есть это просто число. Правда, это число бывает очень большим, например, 5*(10^24).
NA — постоянная Авогадро. Постоянная Авогадро представляет собой универсальную константу. NA = 6,022*(10^23) моль^(–1).
2) Если нам известна масса вещества, то количество вещества находится по следующей формуле:
v = m/M
где
v — количество вещества;
m — масса вещества;
M — молярная масса вещества находится по химической формуле вещества, при помощи периодической системы Д. И. Менделеева, путём суммирования атомных масс всех входящих в молекулу атомов с учётом имеющихся индексов.
3) Если нам известен объём газообразного вещества, то мы можем найти количество вещества газа по такой формуле:
v = V/Vm
где
v — количество вещества;
V — объём газа;
Vm — молярный объём газов. Молярный объём газов — это универсальная константа. Vm = 22,414 л/моль = 22414 м3/моль.
Повторюсь, что формула v = V/Vm верна только для газов!
Наконец, рассмотрим Ваш случай.
Вам по условию даны объём и объёмная доля.
Я рискну предположить, что у Вас задача примерно такого рода:
«Объём газовой смеси составляет 240 л. Объёмная доля кислорода в смеси равна 45%. Вычислите количество вещества кислорода в смеси».
Такая задача решается в два действия.
1) Находим объём кислорода:
V (O2) = V0 * ф / 100 = 240 л * 45 / 100 = 108 л.
(Ф — это объёмная доля, она обозначается греческой буквой «фи». Вместо неё приходится писать русскую ф).
2) Находим количество вещества кислорода. Кислород — это газ, значит, мы имеем право воспользоваться формулой v = V/Vm.
v (O2) = V/Vm = 108 л : 22,414 л/моль = 4,818 моль. Округление произведено до тысячных.
Моль — условное количество вещества
Добавлено: 3 октября 2021 в 12:58

Химия — наука, изучающая взаимодействие веществ на атомном и молекулярном уровнях. Эти процессы значительно отличаются от привычного нам макроуровня и поэтому требуют специфических подходов, в том числе к «подсчету» и «взвешиванию».
Школьный курс химии включает понятия «моль» и «молярной массы». Они кажутся сложными, но если разобраться, то вы без труда поймете сущность этих понятий и научитесь ими пользоваться при решении задач.
Моль
Понятие «моль» попытаемся разобрать и, самое главное, понять на примере всем знакомой реакции взаимодействия кислорода и водорода. Когда одна молекула O2 соединяется с двумя молекулами H2, получается две молекулы H2O:
- O2 + 2H2 = 2H2O
То есть, чтобы максимально полно провести химическую реакцию, мы должны взять на каждую молекулу кислорода две молекулы водорода. Итак, у нас есть 100 г кислорода.
Сколько понадобится водорода для протекания процесса? И тут возникает первый вопрос: сколько молекул в 100 г кислорода? Наверное, миллиарды или даже миллиарды миллиардов? И сколько их в 100 г водорода? Уж точно в не в 2 раза меньше.
Как вообще подсчитать молекулы, ведь они бывают совершенно разными, «тяжелыми» и «легкими». Этими вопросами задавались и люди, закладывавшие основу современной химической науки.
Был найден простой выход, который помогает легко и изящно решить проблему. Химики решили взять за единицу измерения не одну молекулу, а определенное их количество, причем очень большое. Таким образом эта единица измерения приводит микроуровень к макроуровню. Она называется «моль».
Моль — это количество вещества из 6,02214076⋅1023 атомов или молекул. Оно не имеет физического смысла и изначально было привязано к массе определенного количества (12 граммов) углерода-12, но позже переопределено, как и многие другие единицы системы СИ.
В школьных расчетах количество структурных единиц в моле, которое также называется постоянной Авогадро, обычно округляют до 6,022⋅1023 и обозначают NA.
С этой величиной связано другое химическое понятие — «количество вещества», то есть количество структурных единиц в определенной его порции. Оно обозначается буквой ν (ню).
Примеры
В стакане содержится 2 моль воды. Сколько молекул воды находится в стакане?
- N = ν⋅ NA =2 ⋅ 6,022⋅1023 = 12,044⋅1023 молекул воды.
Также можно решить обратную задачу. Сколько молей вещества составляют 24,088⋅1023 молекул воды?
- ν⋅ = N / NA = 24,088⋅1023 / 6,022⋅1023 = 4 моля.
Что называется молярной массой
Итак, мы поняли, что моль — условное количество вещества, выбранное для удобства химиков. Это даже не миллиарды миллиардов, как мы предположили ранее, а миллиарды триллионов, что никак не облегчает задачу подсчета этих структурных единиц.
Как же все-таки узнать, сколько атомов или молекул в 100 граммах того или иного вещества? Теперь хорошо бы связать количество вещества и его массу, ведь это не одно и то же. Нам поможет «молярная масса» — 1 моль вещества или 6,022⋅1023 структурных единиц этого вещества.
Итак, масса вещества равна массе порции вещества m к количеству молекул ν в его порции:
- М = m / ν.
Вооружившись этим знанием, мы можем переводить граммы в число молекул и наоборот. При этом следует учесть, что молярная масса численно идентична молекулярной массе (то есть массе молекулы), выраженной в атомных единицах массы, и относительной молекулярной массе.
Пример
Найдем массу 5 моль воды.
Чтобы решить эту задачу, обратимся к формуле молярной массы и выразим из нее массу:
- m = М ⋅ ν
В этой формуле мы знаем количество вещества ν = 5 моль, а молярную массу сложной молекулы нужно определить, как сумму молярных масс составляющих ее химических элементов:
- M (H2O) = 2 ⋅M (H) + M (O)
Где взять молярные массы кислорода и водорода (в соединение входит два атома водорода, поэтому его молярную массу умножаем на 2)?
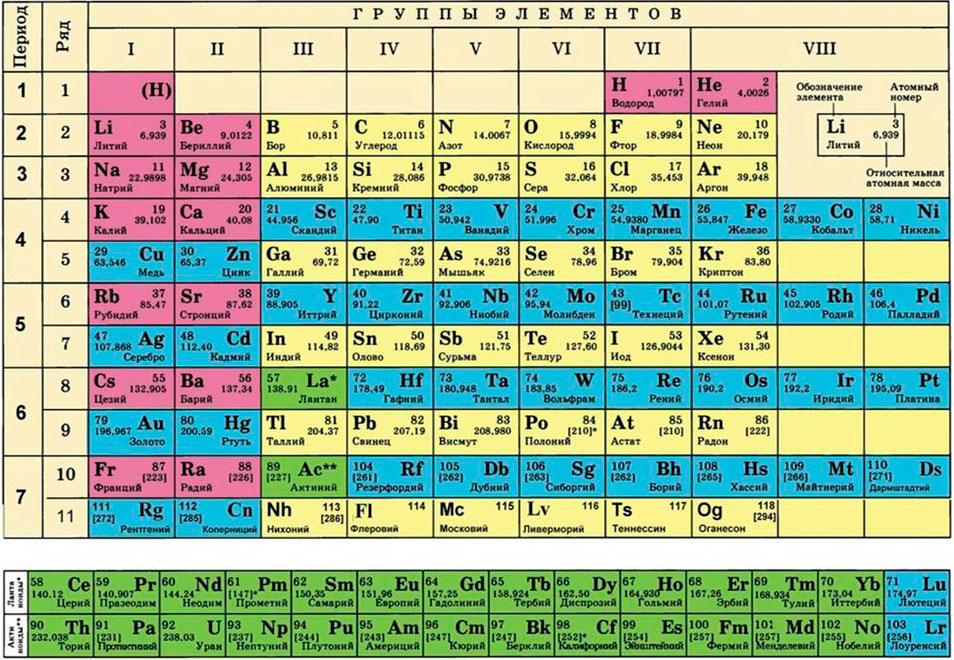
Для этого нам понадобится таблица Менделеева и значение «относительной атомной массы», которая, как мы уже знаем, идентична молекулярной. Это значение приведено для каждого химического элемента и для водорода равно 1,00797 (то есть близко к 1), для углерода — близко к 6, для кислорода — около 16.
Подставим соответствующие значения в исходную формулу и получим:
- M (H2O) = 2 ⋅M (H) + M (O) = 2 ⋅ 1 + 16 = 18 г/моль.
То есть вес 1 моль воды составляет 18 граммов. Теперь можем подсчитать массу 5 моль воды:
- m = М ⋅ ν = 18 ⋅ 5 = 90 г.
Аналогичным образом мы можем подсчитать количество вещества, которое содержится в определенном образце заданной массы. Для примера возьмем оксид алюминия Al2O3 и узнаем, сколько моль в 400 граммах этого вещества. Для этого выразим количество вещества через молярную массу и подставим исходные данные:
- ν = m / М = 400 / (2 ⋅ М (Al) + 3 ⋅ (O)) = 400 / (2 ⋅ 75 + 3 ⋅ 16) = 400 / (150 + 48) = 400 / 198 ≈ 2,02 моль.
Занимайтесь на курсах ЕГЭ и ОГЭ в паре TwoStu и получите максимум баллов на экзамене:

Эксперт по подготовке к ЕГЭ, ОГЭ и ВПР
Задать вопрос
Закончил Московский физико-технический институт (Физтех) по специальности прикладная физика и математика. Магистр физико-математических наук. Преподавательский стаж более 13 лет. Соучредитель курсов ЕГЭ и ОГЭ в паре TwoStu.
Читайте также:
Вчера обещал объяснить это доступным языком. Вещь важная для понимания химии. Если один раз понять, то потом уже не забудешь.
Химия имеет свой язык, как и любая наука. 2H2 + O2 → 2H2O — на химическом языке запись реакции образования воды из простых веществ, водорода (H) и кислорода (O). Маленькие цифры относятся к количеству атомов (Они стоят после символа химического элемента), большие — к количеству молекул. Из уравнения видно что две молекулы водорода соединяются с одной молекулой кислорода и в результате выходит две молекулы воды. Внимание — это очень важно понять! Соединяются именно молекулы с молекулами, не «грамм с граммом», а молекула с молекулой.
Эта пропорция сохранится всегда:
| 2 молекулы водорода | соединятся с одной молекулой кислорода | и получится | 2 молекулы воды |
| 200 молекул водорода | соединятся с 100 молекул кислорода | и получится | 200 молекулы воды |
| 2000 молекул водорода | соединятся с 1000 молекул кислорода | и получится | 2000 молекулы воды |
| 2 миллиона молекул водорода | соединятся с миллионом молекул кислорода | и получится | 2 миллиона молекул воды |
Всё бы хорошо, но есть две проблемы. Первая — в реальной жизни мы не сможем отмерить один миллион молекул кислорода или водорода. Мы сможем отмерить один грамм или одну тонну реактивов. Вторая — молекулы очень маленькие. В одном стакане воды их 6,7·1024 штук. Или, в обычной записи 6,7 триллионов триллионов (именно так — почти семь триллионов раз по триллиону молекул). Оперировать такими цифрами неудобно.
Какой же выход? Молекулы ведь тоже имеют массу, пускай очень маленькую. Мы просто берём массу одной молекулы, умножаем на количество молекул и получаем нужную нам массу. Договорились так — берём очень большое количество молекул (600 миллиардов триллионов штук) и изобретаем для этого количества специальную единицу измерения моль. Как для 12 штук чего-либо есть специальное название «дюжина», и когда говорят о «десяти дюжинах», то имеют в виду 120 штук. 5 дюжин яиц = 60 штук. Так и с молями. 1 моль — это 600 миллиардов триллионов молекул или, в математической нотации, 6,02·1023 молекул. То есть когда нам говорят «1 моль» водорода, мы знаем что речь идёт о 600 миллиардах триллионов молекул водорода. Когда говорят о 0,2 молях воды, то мы понимаем что речь идёт 120 миллиардах триллионов молекул воды.
Ещё раз — моль это просто такая счётная единица, только специально для молекул. Как «десяток», «дюжина» или «миллион», только гораздо больше.
Продолжая таблицу выше, можно написать:
| 2 моля водорода | соединятся с одним молем кислорода | и получится | 2 моля воды |
| 20 молей водорода | соединятся с 10 молями кислорода | и получится | 20 молей воды |
| 1000 молей водорода | соединятся с 500 молями кислорода | и получится | 1000 молей воды |
Первую проблему мы решили, писать 1 моль или 2 моля гораздо удобнее чем 600 миллиардов триллионов молекул или 1,2 триллиона триллионов молекул. Но для одного удобства не стоило огород городить. Вторая проблема, как помним, переход от количества молекул (не считать же их поштучно!) к массе вещества, к тому что мы можем отмерить на весах. Такое количество молекул в одном моле (оно ведь немного странное, некруглое — 6,02·1023 молекул) выбрано неспроста. Один моль молекул углерода весит ровно 12 грамм.
Понятно что все молекулы разные. Есть большие и тяжелые — в них может быть много атомов, или не очень много, но зато сами атомы тяжелые. А есть маленькие и легкие молекулы. Для каждого атома и для многих молекул есть в справочниках таблицы с их молярной массой. То есть с весом одного моля таких молекул (если нет, можно легко самим посчитать, сложив молярные массы всех атомов, из которых составлена молекула). Молярная масса измеряется в грамм/моль (сколько грамм весит один моль, то есть сколько грамм весят 6,02·1023 молекул). Мы помним ведь что моль — просто счётная единица. Ну как если бы в справочнике писали — 1 дюжина куриных яиц весит 600 грамм, а 1 дюжина страусиных весит 19 килограмм. Дюжина — просто количество (12 штук), а сами яйца, куриное или страусиное, весят по-разному. И дюжина таких или других яиц тоже по-разному весит.
Так и с молекулами. 1 моль маленьких и лёгких молекул водорода весит 2 грамма, а 1 моль больших молекул серной кислоты — 98 грамм. 1 моль кислорода весит 32 грамма, 1 моль воды — 18 грамм. Вот картинка для примера, где видны маленькие молекулы водорода и большие молекулы кислорода. Эта картинка — графическое отображение реакции 2H2 + O2 → 2H2O.
Продолжаем заполнять таблицу:
| 2 моля водорода | соединятся с одним молем кислорода | и получится | 2 моля воды |
| 4 грамма водорода (т.к. 1 моль водорода весит два грамма) | соединятся с 32 граммами кислорода | и получится | 36 грамм воды |
Видите переход от количества молекул к их массе? Видите что выполняется закон сохранения вещества? 4 грамма + 32 грамма дали 36 грамм.
Теперь мы можем решать простые задачи по химии. Вот самая примитивная: Было 100 молекул кислорода и 100 молекул водорода. Что произойдёт в результате реакции? Мы знаем что на 1 молекулу кислорода нужно 2 молекулы водорода. Поэтому прореагируют все 100 молекул водорода (и образуется 100 молекул воды), а вот кислород прореагирует не весь, ещё 50 молекул останется. Кислород в избытке.
Молекулы штуками, как я уже сказал выше, никто не считает. Вещества обычно отмеряют граммами. Теперь задача из школьного учебника: есть 10 г. водорода и 64 г. кислорода, что будет если их смешать? Мы для начала должны перевести массы в моли (то есть в количество молекул или количество вещества, как говорят химики). 10 г. водорода — это 5 моль водорода (1 моль водорода весит 2 грамма). 64 г. кислорода — это 2 моля (1 моль весит 32 грамма). Мы знаем что на 1 моль кислорода при реакции уходит 2 моля водорода. Значит, в нашем случае прореагирует весь кислород (2 моля) и 4 моля водорода из пяти. Получится 4 моля воды и ещё останется один моль водорода.
Переведём ответ снова в граммы. Прореагирует весь кислород (64 грамма) и 8 грамм водорода (4 моля * 2 г/моль). 1 моль водорода останется не прореагировавшим (это 2 грамма) и получится 72 грамма воды (4 моля * 18 г/моль). Закон сохранения вещества опять выполняется — 64 + 10 = 72 + 2.
Думаю что теперь уже всем должно быть понятно. 1 моль — просто количество молекул. Молярная масса — это масса одного моля. Она нужна для того чтобы переходить от массы вещества (с которой мы работаем в реальном мире) к количеству молекул, или количеству вещества, нужному для реакций.
Снова повторимся:
а) вещества реагирует в соотношении n молекул одного к m молекул другого. Это пропорция будет одинаковой и для 100 молекул исходного вещества, и для ста триллионов, или для ста триллионов триллионов.
б) для удобства, чтобы не считать молекулы штуками, придумали специальную счётную единицу — моль, то есть сразу 6,02·1023 молекул. Количество этих молей называют обычном «количество вещества»
в) моль каждого вещества весит по-разному, т.к. молекулы и атомы, из которых состоит вещества, сами весят по-разному. Масса одного моля вещества называется его молярной массой. Ещё один пример — обычные и силикатные кирпичи весят по-разному. Если мы проведём аналогию, то «вес тысячи кирпичей» — это «молярная масса» (с тем отличием что молекул не 1000, а больше). Масса этой «тысячи кирпичей» разная для силикатных и обычных кирпичей.
г) весь этот огород городим для того чтобы легко можно было переходить от массы реактивов к количеству вещества (количеству молекул, количеству молей) и обратно. А переходить туда/обратно нужно потому что в реальном мире мы отмеряем реактивы граммами, а химические реакции идут пропорционально не массе, а количеству молекул.
P.S. Химикам и прочим — я здесь специально многое упрощал. Не нужно мне объяснять что 12 грамм весит не 1 моль углерода, а 1 моль молекул изотопа С12, или про то что вместо «молекул» нужно было бы писать «структурных единиц» (молекул, ионов, атомов…), специально не упомянул что 1 моль газа занимает одинаковый объём при одинаковых условиях и ещё про многое другое
Что мне не нравилось в учебниках — только формальное определение моля, без указания смысла этого понятия и для чего это нужно.
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·1023 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·1023 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·1023).
Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·1023 атомов. Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·1023 молекул. Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
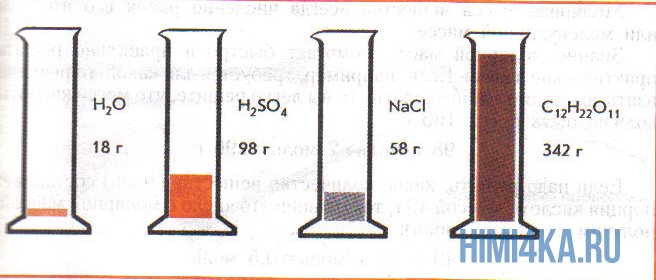
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·1023; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·1023 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·1023 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·1023 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·1023 × 0,25 = 1,505·1023 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·1023 молекул/моль, что равно 2,99·1026 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
Рассчитать объем кислорода.
Рассчитать объем кислорода (газа) при нормальных условиях, если известна его масса, можно по формуле: V = m · Vm / M = ν · Vm. Рассчитать объем кислорода (газа), если известна его масса, температура и давление, можно по формуле: V = m · R · T / (p · M) = ν · R · T / p.
Химическая формула кислорода O₂.
Расчет объема кислорода (газа)
Теория расчета объема газа
Пример: Рассчитайте объем для 1 кг кислорода, для 160 г кислорода, для 6 г кислорода
Пример: Рассчитайте объем для 2 моль кислорода, для 3 моль кислорода, для 5 моль кислорода
Рассчитать объем газа: азота, водорода, воздуха, гелия, озона, кислорода, углекислого газа, хлора
Рассчитать объем кислорода (газа) при нормальных условиях:
Рассчитать объем кислорода (газа):
Теория:
Рассчитать объем кислорода (газа) при нормальных условиях, если известна его масса, можно по формуле:
V = m · Vm / M = ν · Vm,
где
V – объем газа, л,
ν – количество вещества, моль,
Vm – молярный объем газа, л/моль, Vm = 22,4 л/моль,
ν = m / M,
m – масса газа, г,
М – молярная масса газа, г/моль,
M(О₂) = 2·16 = 32 г/моль,
Нормальные условия: 0 оС (или 273,15 К), 101,325 кПа или 1 атм.
Рассчитать объем кислорода (газа), если известна его масса, температура и давление, можно по формуле:
V = m · R · T / (p · M) = ν · R · T / p,
где
V – объем газа, л,
ν – количество вещества, моль,
ν = m / M,
m – масса газа, г,
М – молярная масса газа, г/моль,
M(О₂) = 2·16 = 32 г/моль,
R – универсальная газовая постоянная, R ≈ 8,314 Дж/(моль⋅К),
T – термодинамическая температура, К.
P – давление, кПа.
Пример: Рассчитайте объем для 1 кг кислорода, для 160 г кислорода, для 8 г кислорода:
Рассчитайте объем для 1 кг кислорода при нормальных условиях.
V = m · Vm / M = 1 000 грамм · 22,4 л/моль / 32 г/моль = 700 литров.
Рассчитайте объем для 1 кг кислорода при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = m · R · T / p · M = 1 000 грамм · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа · 32 г/моль) = 2 625,405 литров или 2,625405 м3.
Рассчитайте объем для 160 г кислорода при нормальных условиях.
V = m · Vm / M = 160 грамм · 22,4 л/моль / 32 г/моль = 112 литров.
Рассчитайте объем для 160 г кислорода при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = m · R · T / p · M = 160 грамм · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа · 32 г/моль) = 420,064 литров.
Рассчитайте объем для 8 г кислорода при нормальных условиях.
V = m · Vm / M = 8 грамм · 22,4 л/моль / 32 г/моль = 5,6 литров.
Рассчитайте объем для 8 г кислорода при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = m · R · T / p · M = 8 грамм · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа · 32 г/моль) = 21,003 литра.
Пример: Рассчитайте объем для 2 моль кислорода, для 3 моль кислорода, для 5 моль кислорода:
Рассчитайте объем для 2 моль кислорода при нормальных условиях.
V = ν · Vm = 2 моль · 22,4 г/моль = 44,8 литров.
Рассчитайте объем для 2 моль кислорода при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = ν · R · T / p = 2 моль · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа) = 168,025 литров.
Рассчитайте объем для 3 моль кислорода при нормальных условиях.
V = ν · Vm = 3 моль · 22,4 г/моль = 67,2 литров.
Рассчитайте объем для 3 моль кислорода при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = ν · R · T / p = 3 моль · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа) = 252,038 литра.
Рассчитайте объем для 5 моль кислорода при нормальных условиях.
V = ν · Vm = 5 моль · 22,4 г/моль = 112 литров.
Рассчитайте объем для 5 моль кислорода при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = ν · R · T / p = 5 моль · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа) = 420,064 литров.
Рассчитать объем газа: азота, водорода, воздуха, гелия, озона, кислорода, углекислого газа, хлора
Коэффициент востребованности
4 157