Найти массу, плотность или объем онлайн
На данной странице калькулятор поможет найти плотность, массу или объем вещества онлайн. Для расчета введите значения в калькулятор.
Объем, масса и плотность
Найти
Масса:
Объем:
Плотность:
Ответы:
Формула для нахождения массы тела через плотность и объем:
m — масса; V — объем; p — плотность.
Формула для нахождения объема тела через плотность и массу:
m — масса; V — объем; p — плотность.
Формула для нахождения плотности тела через объем и массу:
m — масса; V — объем; p — плотность.
Калькулятор
Как найти количество молекул через плотность?
Но зато, зная плотность вещества и массу одной молекулы, можно определить число молекул в 1 м3 вещества, которое другим путем подсчитать нельзя. Чтобы найти число молекул в 1 м3, нужно плотность вещества разделить на массу одной его молекулы, массу же молекулы определяют опытным путем.
Как найти количество вещества Если дан объем?
Выразим из формулы молярного объёма n : n ( X ) = V ( X ) V m — химическое количество газа можно вычислить, если его объём разделить на молярный объём.
Как найти массу если есть объем?
Вес можно рассчитать по формуле: m=V*p, где р – плотность, V – объем материала. Например, 10 м3 речного песка весят 13 тонн. Если известна масса материала, то объем можно узнать по формуле: V = m/ p.
Как вычислить молярную массу вещества?
Молярная масса в Международной системе СИ измеряется в кг/моль, хотя обычно эту величину выражают в грамм/моль. Эта величина обозначается английской буквой M, а формула молярной массы выглядит следующим образом: M=m/v, где m – масса вещества, а v – количество вещества.
Как найти плотность по массе и объему?
плотность = масса объём ρ = m V , где m — масса, V — объём. Основной единицей плотности вещества является кг м 3 .
Как найти количество вещества через массовую долю?
Перемножив массовую долю с массой раствора: m = m(р-ра) × ω.
…
Для его нахождения нужно основываться на условии задачи, так как вычислить количество вещества можно по трём формулам:
- По массе. n=m/M — Массу вещества (в граммах) разделить на его молярную массу (в г/моль).
- По объёму. …
- По числу молекул.
14.02.2019
Как найти количество вещества через концентрацию?
Количество растворенного вещества : = c•V, где c – молярная концентрация растворенного вещества в моль/л, V – объем раствора в л. где m(р-ра) – масса раствора в г, – массовая доля растворенного вещества.
Как определить количество моль вещества?
Количество молей вещества n находят из отношения массы m этого вещества (г) к его молярной массе М (г/моль). Например, число молей в m г воды составляет: n = m/18.
Как найти массу силу тяжести?
Формула силы тяжести Fт=m*g, где m-масса тела, g-ускорение свободного падения. Для тела массой m=400 г =0.4 кг сила тяжести составит Fт=0.4*10=4 Н. Формула силы тяжести: F=mg, где m- масса тела, g-Н/кг.
Как найти массу и объем газа?
Vm=M/p, где Vm – молярный объем, М – молярная масса, а p – плотность вещества. Рис. 2.
Как найти массу вещества в растворе?
Масса раствора определяется по формуле m (раствора)= m (масса растворенного вещества)/ w (массовая доля растворенного вещества). Или m = r (плотность раствора — г/см3) * V (объем раствора).
Как найти молярную массу пример?
Молярная масса вещества равна сумме молярных масс элементов, входящих в состав его молекул. Например, молярная масса метана CH4 определяется следующим образом: М(CH4) = M(C) + 4·M(H) = 12 + 4 = 16 г/моль. Это означает, что 16 г CH4 содержат 6,02·1023 молекул (1 моль).
Что такое относительная атомная масса вещества?
Относи́тельная а́томная ма́сса (устаревшее название — атомный вес) — значение массы атома, выраженное в атомных единицах массы, определяется как отношение массы атома данного элемента к 1⁄12 массе нейтрального атома изотопа углерода 12C.
Что такое масса вещества?
Масса молекул (масса вещества) – это та же самая масса тела, которая ранее рассматривалась в разделе «Механика». Это самая обычная масса. Логично, что нам захочется узнать не только массу всех молекул, но и количество этих молекул в веществе.
Основные формулы для решения задач по химии
05-Авг-2012 | комментариев 450 | Лолита Окольнова
Все, все основные задачи по химии решаются с помощью
нескольких основных понятий и формул.
У всех веществ разная масса, плотность и объем. Кусочек металла одного элемента может весить во много раз больше, чем точно такого же размера кусочек другого металла.
Моль (количество моль)
обозначение: моль, международное: mol — единица измерения количества вещества. Соответствует количеству вещества, в котором содержится NA частиц (молекул, атомов, ионов). Поэтому была введена универсальная величина — количество моль. Часто встречающаяся фраза в задачах — «было получено… моль вещества»
NA = 6,02 · 1023
NA — число Авогадро. Тоже «число по договоренности». Сколько атомов содержится в стержне кончика карандаша? Несколько миллионов. Оперировать такими величинами не удобно. Поэтому химики и физики всего мира договорились — обозначим 6,02 · 1023 частиц (атомов, молекул, ионов) как 1 моль вещества.
1 моль = 6,02 · 1023 частиц
Это была первая из основных формул для решения задач.
Молярная масса вещества
Молярная масса вещества — это масса одного моль вещества. Обозначается как M
Есть еще молекулярная масса — Mr
Находится по таблице Менделеева — это просто сумма атомных масс вещества.
Например, нам дана серная кислота — H2SO4. Давайте посчитаем молярную массу вещества: атомная масса H =1, S-32, O-16.
Mr(H2SO4)=1•2+32+16•4=98 гмоль.
Вторая необходимая формула для решения задач —
формула массы вещества:
Т.е., чтобы найти массу вещества, необходимо знать количество моль (n), а молярную массу мы находим из Периодической системы.
Закон сохранения массы — масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ.
Если мы знаем массу (массы) веществ, вступивших в реакцию, мы можем найти массу (массы) продуктов этой реакции. И наоборот.
Третья формула для решения задач по химии —
объем вещества:
Откуда взялось число 22.4? Из закона Авогадро:
в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул.
Согласно закону Авогадро, 1 моль идеального газа при нормальных условиях (н.у.) имеет один и тот же объём Vm = 22,413 996(39) л
Т.е., если в задаче нам даны нормальные условия, то, зная количество моль (n), мы можем найти объем вещества.
Итак, основные формулы для решения задач по химии
Число Авогадро NA
6,02 · 1023 частиц
Количество вещества n (моль)
n=mM
n=V22.4 (лмоль)
Масса вещества m (г)
m=n•Mr
Объем вещества V(л)
V=n•22.4 (лмоль)
или вот еще удобная табличка:
Это формулы. Часто для решения задач нужно сначала написать уравнение реакции и (обязательно!) расставить коэффициенты — их соотношение определяет соотношение молей в процессе.
В ОГЭ и ЕГЭ по химии задач , в которых нужно было бы найти только объем массу кол-во моль нет — это обычно ЧАСТЬ решения задачи. Однако, чтобы легко решать более сложные задачи, нужно тренироваться на таких вот небольших упражнениях.
Находим количество вещества по массе
1 Какое количество вещества алюминия содержится в образце металла массой 10.8 г?2 Какое количество вещества содержится в оксиде серы (VI) массой 12 г?
3 Определите количество моль брома, содержащееся в массе 12.8 г.
Находим массу по количеству вещества:
4. Определите массу карбоната натрия количеством вещества 0.25 моль.Объем по количеству вещества:
5. Какой объем будет иметь азот при н.у., если его количество вещества 1.34 моль?6. Какой объем занимают при н.у. 2 моль любого газа?
Ответы:/p>
- 0.4 моль
- 0.15 моль
- 0.08 моль
- 26.5 г
- 30 л
- 44.8 л
Категории:
|
Обсуждение: «Основные формулы для решения задач по химии»
(Правила комментирования)
Онлайн калькулятор поможет перевести объём в массу и наоборот массу перевести в объём. Для произведения расчетов необходимо знать объём (в см3, дм3, м3, мл, л на выбор) и плотность (в г/см3, г/м3, кг/см3, кг/м3, т/м3, кг/л на выбор).
Определить плотность некоторых веществ можно в таблице под калькулятором.
Формула для перевода объёма в массу: M = V × P
Формула для перевода массы в объём: V = M / P
Где: M — масса; V — объем; P — плотность.
×
Пожалуйста напишите с чем связна такая низкая оценка:
×
Для установки калькулятора на iPhone — просто добавьте страницу
«На главный экран»
Для установки калькулятора на Android — просто добавьте страницу
«На главный экран»
Формула массы через плотность и объем является одной из базовых формул физики, изучаемых в рамках школьной программы еще в седьмом классе. Она пригодится в решении многих задач.
Формула зависимости массы от объема и плотности
Для того, чтобы найти плотность жидкости или твердого вещества, существует базовая формула: плотность равна массе, поделенной на объем.
Записывается это так:
ρ = m / V
И из нее можно вывести еще две формулы.
Формулу для объема тела:
V = m / ρ
А также формулу для расчета массы:
m = V * ρ
Как видите, запомнить последнюю очень легко: это единственная формула, где две единицы нужно умножить.
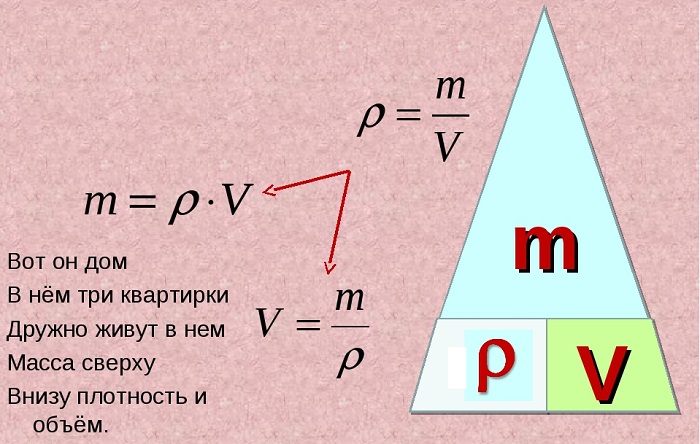
Для запоминания этой зависимости можно использовать рисунок в виде «пирамидки», разделенной на три секции, в вершине которой находится масса, а в нижних углах – плотность и объем.
Несколько иначе обстоят дела с газами. Рассчитать их вес гораздо сложнее, так как у газов нет постоянной плотности: они рассеиваются и занимают весь доступный им объем.
Для этого пригодится понятие молярной массы, которую можно найти, сложив массу всех атомов в формуле вещества при помощи данных из периодической таблицы.
Вторая единица, которая нам понадобится – количество вещества в молях. Его можно вычислить по уравнению реакции. Подробнее об этом можно узнать в рамках курса химии.
Другой способ нахождения мольного количества – через объем газа, который нужно поделить на 22,4 литра. Последнее число – это объемная постоянная, которую стоит запомнить.
В итоге, зная две предыдущие величины, мы можем определить массу газа:
m = n * M,
где M – это молярная масса, а n – количество вещества.
Результат получится в граммах, поэтому для решения физических задач важно не забыть перевести его в килограммы, поделив на 1000. Числа в этой формуле часто могут оказываться достаточно сложными, поэтому для вычислений может понадобиться калькулятор.
Еще один нестандартный случай, с которым можно столкнуться – необходимость найти плотность раствора. Для этого существует формула средней плотности, построенная аналогично формулам других средних величин.
Для двух веществ посчитать ее можно так:
(m1 + m2) / V1 + V2.
Также из этой формулы можно вывести несколько других в зависимости от того, какие из величин известны по условию задачи.
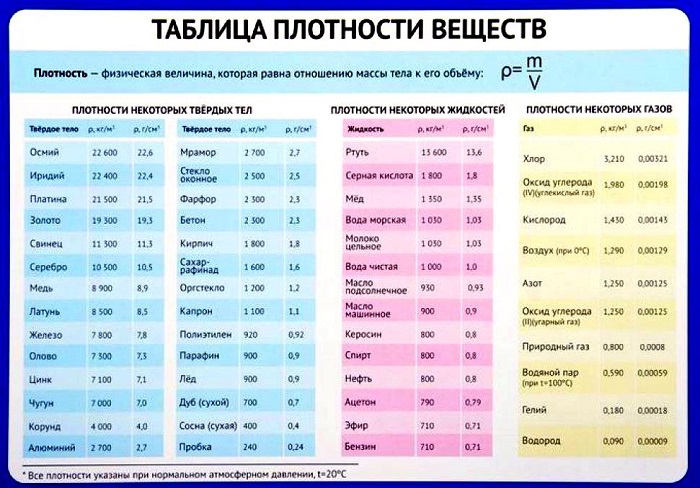
Таблица плотности некоторых веществ
Плотность многих веществ известна заранее и легко находится по соответствующей таблице.
В работе с ней важно обращать внимание на размерности и не забывать о том, что все данные собраны при нормальных условиях: комнатной температуре в 20 градусов Цельсия, а также определенном давлении, влажности воздуха и так далее.
Плотности других, более редких веществ можно найти онлайн.
Как минимум одно из значений плотности стоит запомнить, так как оно часто появляется в задачах. Это плотность воды – 1000 кг/м3 или 1 г/см3.
Примеры решения задач
Задача 1
Условие: имеется алюминиевый брусок со сторонами 3, 5 и 7 сантиметров. Какова его масса?
Решение:
Найдем объем бруска:
V = a * b * c;
V = 3 * 5 * 7 = 105 см3;
Табличное значение плотности алюминия: 2800 кг/м3 или 2,8 г/см3;
Вычислим массу бруска:
m = V * ρ;
m = 105 * 2,8 = 294 г.
Ответ: m = 294 г.
Задача 2
Задача по смежной теме.
Условие: сколько энергии потребуется для того, чтобы довести воду комнатной температуры (20 градусов Цельсия) из стакана (ёмкость 200 мл) до температуры кипения?
Решение:
Найдем недостающую информацию: температура кипения воды t2 = 100 градусов Цельсия, удельная теплоемкость воды с = 4200 Дж/кг * С, плотность воды 1 г/см3, 1 мл воды = 1 см3;
Найдем массу воды:
m = V * ρ;
m = 200 * 1 = 200 г = 0,2 кг;
Найдем энергию:
Q = c * m * (t2 – t1);
Q = 4200 * 0,2 * (100 – 20) = 67200 Дж = 67,2 кДж.
Ответ: Q = 67,2 кДж.
Задача 3
Задача с молярной массой.
Условие: найдите массу CO2 при объеме в 5,6 л.
Решение:
Найдем молярную массу CO2 :
M = 12 + 16 * 2 = 44 г/моль;
Найдем количество вещества через объем:
n = 5,6 / 22,4 = 0,25 моль;
Найдем массу:
m = n * M;
m = 0,25 * 44 = 11 г.
Ответ: m = 11 г.