Речь в статье пойдет о КПД различных циклов, проводимых с газом. При этом давайте помнить, что внутренняя энергия изменяется тогда, когда изменяется температура, а в адиабатном процессе передачи тепла не происходит, то есть для совершения работы в таком процессе газ «изыскивает внутренние резервы». Кроме того, работа численно равна площади под кривой процесса, а работа за цикл — площади внутри цикла.
Задача 1.
На рисунке представлена диаграмма цикла с одноатомным идеальным газом. Участки и
— адиабаты. Вычислите КПД
данной тепловой машины и максимально возможный КПД
.
К задаче 1
КПД тепловой машины можно вычислить как
Машина получает тепло только на участке AB, и, так как работы здесь не совершается, то можно вычислить количество теплоты, полученное газом, как увеличение его внутренней энергии:
Работа численно равна площади, ограниченной циклом. Поэтому
Участк и
по условию – адиабаты, то есть передачи тепла газу на этих участках не происходит, следовательно, работа будет совершена за счет «внутренних резервов» — то есть внутренней энергии. Нужно, следовательно, найти, как она изменилась.
Задачу можно решить двумя способами. Во-первых, просто определить температуры в точках и
,
и
, это легко сделать из данных графика с помощью уравнения Менделеева-Клапейрона, и затем посчитать
. Но, так как
, а
,то изменение внутренней энергии будет равно
Определим максимальный КПД. Посчитаем его как КПД цикла Карно. Максимальная температура газа будет достигнута в точке , а минимальная – в точке
:
Ответ: ,
.
Задача 2.
Над идеальным одноатомным газом проводят цикл, включающий изобару, изохору, изотерму, при этом работа газа за цикл равна кДж. В процессе изотермического сжатия (3-1) внешние силы совершают над газом положительную работу
кДж. Найдите КПД данной тепловой машины.
К задаче 2
Работа газа в процессе 1-2– площадь под линией процесса 1-2. Работа внешних сил – площадь под циклом (под линией 3-1). Поэтому полная работа за цикл – это разность работы газа и работы внешних сил, площадь, ограниченная линиями цикла. Она будет равна 5 кДж.
Работа газа в процессе 1-2, таким образом, равна 8 кДж. А поскольку процесс изобарный, то кДж. Тогда КПД
Ответ: .
Задача 3.
КПД тепловой машины, работающей по циклу, включающему изотермический (1-2) и адиабатный (3-1) процессы, равен , причем работа, совершенная 2 моль одноатомного идеального газа в изотермическом процессе
кДж. Найдите разность
максимальной и минимальной температур газа в цикле.
К задаче 3
Полная площадь под кривой процесса 1-2 равна кДж. При этом, так как КПД машины 25%, то площадь внутри цикла равна
, а под кривой 3-1 —
. В процессе 1-2 изменения внутренней энергии не было, так как температура не менялась, а в процессе 3-1 газу не передавали тепло, следовательно, работа совершена за счет внутренней энергии. Т.е.
Ответ: 500 K.
На этой странице вы узнаете
- В чем прелесть фазовых переходов?
- Что лучше выбрать: Mercedes или BMW?
Люди научились летать в космос, покорять недра Земли и погружаться в глубины океана. Эти и другие достижения возможны благодаря способности извлекать максимум пользы из имеющихся ресурсов,а именно получать тепловую энергию различными доступными способами. Сегодня мы разберем задачи, которые заставят тепловые процессы играть на нашей стороне.
Тепловые машины и их КПД
Рекомендация: перед тем как приступить к выполнению задач неплохо было бы повторить тему «Уравнение состояния идеального газа» . Но ключевую теорию, на которой основано решение задач, сейчас разберем вместе.
Вспомним, что фазовые переходы — это переход из одного агрегатного состояния в другое. При этом может выделяться большое количество теплоты.
Именно благодаря этому они и стали такими полезными для нас. Например, в ядерных реакторах воду используют в качестве рабочего тела, то есть она нагревается вследствие энергии, полученной из ядерных реакций, доходит до температуры кипения, а затем под большим давлением уже в качестве водяного пара воздействует на ротор генератора, который вращается и дает нам электроэнергию! На этом основан принцип работы атомных электростанций.
А самый простой пример фазового перехода — образование льда на лужах в морозные ноябрьские дни. Правда о выделении тепла здесь речи не идет.
Мы не почувствуем, как испарится капелька у нас на руке, потому что это не требует много тепла от нашего тела. Но мы можем наблюдать, как горят дрова в мангале, когда мы жарим шашлык, потому что выделяется огромное количество теплоты. А зачем мы вообще рассматриваем эти фазовые переходы? Все дело в том, что именно фазовые переходы являются ключевым звеном во всех процессах, где нас просят посчитать КПД, от них нашему рабочему телу и подводится теплота нагревателя.

Человечество придумало такие устройства, которые могут переработать тепловую энергию в механическую.
Тепловые двигатели, или тепловые машины, — устройства, способные преобразовывать внутреннюю энергию в механическую.
Их устройство довольно просто: они на входе получают какую-то энергию (в основном — энергию сгорания топлива), а затем часть этой теплоты расходуется на совершение работы механизмом. Например, в автомобилях часть энергии от сгоревшего бензина идет на движение. Схематично можно изобразить так:
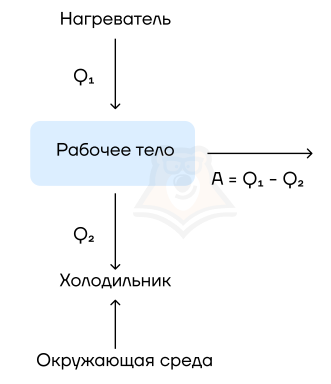
Рабочее тело — то, что совершает работу — принимает от нагревателя количество теплоты Q1, из которой A уходит на работу механизма. Остаток теплоты Q2 рабочее тело отдает холодильнику, по сути — это потеря энергии.
Физика не была бы такой загадочной, если б все в ней было идеально. Как и в любом процессе или преобразовании, здесь возможны потери, зачастую очень большие. Поэтому «индикатором качества» машины является КПД, с которым мы уже сталкивались в механике:
Коэффициент полезного действия (КПД) тепловой машины — это отношение полезной работы двигателя к энергии, полученной от нагревателя.
(eta) — КПД,
A — работа газа (Дж),
Q1 — количество теплоты, полученное от нагревателя (Дж).
Мы должны понимать, что КПД на практике никогда не получится больше 1, поскольку всегда будут тепловые потери.
Полезную работу можно расписать как Q1 — Q2 (по закону сохранения энергии). Тогда формула примет вид:
(eta = frac{Q_1 — Q_2}{Q_1} = 1 — frac{Q_2}{Q_1})
Давайте попрактикуемся в применении данной формулы на задаче номер 9 из ЕГЭ.
Задача. Тепловая машина, КПД которой равен 60%, за цикл отдает холодильнику 100 Дж. Какое количество теплоты за цикл машина получает от нагревателя? (Ответ дайте в джоулях).
Решение:
Давайте сначала вспомним нашу формулу для КПД:
(eta = frac{Q_1 — Q_2}{Q_1}),
где (Q_1) — это теплота, которую тело получает от нагревателя, (Q_2) — теплота, которая подводится к холодильнику.
Тогда отсюда можно вывести искомую теплоту нагревателя:
(eta Q_1 =Q_1-Q_2)
(eta Q_1 — Q_1= -Q_2)
(Q_1=frac{- Q_2}{eta-1}=frac{-100}{0,6-1}=250 Дж).
Ответ: 250 Дж
Цикл Карно
Мы знаем, что потери — это плохо, поэтому должны предотвращать их. Как это сделать? Нам ничего делать не нужно, за нас уже все сделал Сади Карно, французский физик, разработавший цикл, в котором машины достигают наивысшего КПД. Этот цикл носит его имя и состоит из двух изотерм и двух адиабат. Рассмотрим, как этот цикл выглядит в координатах p(V).
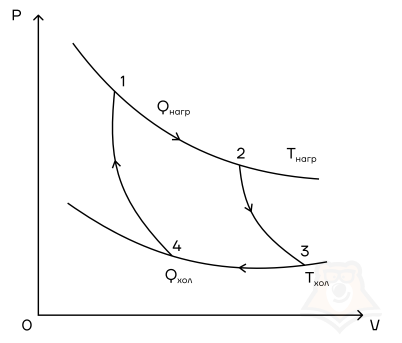
- Температура верхней изотермы 1-2 — температура нагревателя (так как теплота в данном процессе подводится).
- Температура нижней изотермы 3-4 — температура холодильника (так как теплота в данном процессе отводится).
- 2-3 и 4-1 — это адиабатические расширение и сжатие соответственно, в них газ не обменивается теплом с окружающей средой.
Цикл Карно — цикл идеальной тепловой машины, которая достигает наивысшего КПД.
Формула, по которой можно рассчитать ее КПД выражается через температуры:
T1 — температура нагревателя,
T2 — температура холодильника.
Не то круто, что красиво, а то, что по Карно работает! Поэтому присматривайте такой автомобиль, у которого высокий КПД.
Интересно, что максимальный уровень КПД двигателя внутреннего сгорания автомобилей на данный момент всего около 43%. По официальным заявлениям компания Nissan Motor с 2021 года испытывает прообраз двигателя нового поколения с планируемым КПД 50%.
Приступим к задачам
Задачи на данную тему достаточно часто встречаются в задании 27 из КИМа ЕГЭ. Давайте разберем некоторые примеры.
Задание 1. Одноатомный газ совершает циклический процесс, как показано на рисунке. На участке 1–2 газ совершает работу A12 = 1520 Дж. Участок 3–1 представляет собой адиабатный процесс. Количество теплоты, отданное газом за цикл холодильнику, равно |Qхол| = 4780 Дж. Найдите работу газа |A13| на адиабате, если количество вещества постоянно.
Решение:
Шаг 1. Первое, с чего лучше начинать задачи по термодинамике — исследование процессов.
Посмотрим на участок 1-2 графика: продолжение прямой проходит через начало координат, поэтому график функционально можно записать, как p = aV, где a — какое-то число, константа. Графиком является не изотерма, поскольку график изотермы в координатах p-V — гипербола. Из уравнения Менделеева-Клапейрона следует: (frac{pV}{T} = const). Отсюда можно сделать вывод, что возрастает температура, так как растут давление и объем. Температура и объем растут, значит, увеличивается и внутренняя энергия и объем соответственно.
Участок 2-3: процесс изохорный, поскольку объем постоянен, следовательно, работа газом не совершается. Рассмотрим закон Шарля: (frac{p}{T} = const). Давление в этом процессе растет, тогда растет и температура, поскольку дробь не должна менять свое значение. Делаем вывод, что внутренняя энергия тоже увеличивается.
Участок 3-1: адиабата по условию, то есть количество теплоты в этом переходе равна нулю из определения адиабатного процесса. Работа газа отрицательна, так как газ уменьшает объем.
Оформим все данные в таблицу.
Определим знаки Q, используя первый закон термодинамики: Q = ΔU + A.

Из этих данных сразу видно, что количество теплоты, отданное холодильнику — это количество теплоты в процессе 2-3.
Шаг 2. Первый закон термодинамики для процесса 1-2 запишется в виде:
Q12 = ΔU12 + A12.
Работа A12 — площадь фигуры под графиком процесса, то есть площадь трапеции:
(A_{12} = frac{p_0 + 2p_0}{2} * V0 =frac{3p_0V_0}{2}).
Запишем изменение внутренней энергии для этого процесса через давление и объем. Мы выводили эту формулу в статье «Первое начало термодинамики»:
(Delta U_{12} = frac{3}{2}(2p_0 * 2V_0 — p_0V_0) = frac{9p_0V_0}{2}).
Заметим, что это в 3 раза больше работы газа на этом участке:
(Delta U_{12} = 3A_{12} rightarrow Q_{12} = 4A_{12}).
Шаг 3. Работа цикла — площадь фигуры, которую замыкает график, тогда . A = A12 — |A31|. С другой стороны, работа цикла вычисляется как разность между энергиями нагревателя и холодильника: A = Q12 — |Q31|.
Сравним эти формулы:
Q12 -|Q31| = A12 — |A31|,
подставим выражения из предыдущего пункта:
4A12 — |Q31| = A12 — |A31| (rightarrow) |A31| = -3A12 + |Q31| = -31520 + 4780 = 220 Дж.
Ответ: 220 Дж
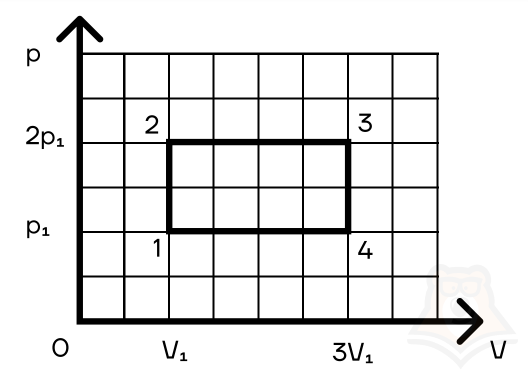
Задание 2. Найти КПД цикла для идеального одноатомного газа.
Решение:
Шаг 1. КПД цикла определим по формуле: (eta = frac{A}{Q}), где Q — количество теплоты от нагревателя, а А — работа газа за цикл. Найдем А как площадь замкнутой фигуры: A = (2p1 — p1)(3V1 — V1) = 2p1V1.
Шаг 2. Найдем процесс, который соответствует получению тепла от нагревателя. Воспользуемся теми же приемами, что и в прошлой задаче:
Посмотрим на участок 1-2 графика: давление растет, объем не меняется. По закону Шарля (frac{p}{T} = const) температура тоже растет. Работа газа равна 0 при изохорном процессе, а изменение внутренней энергии положительное.
2-3: давление не меняется, растет объем, а значит, работа газа положительна. По закону Гей-Люссака (frac{V}{T} = const) температура тоже растет, растет и внутренняя энергия.
3-4: давление уменьшается, следовательно, и температура уменьшается. При этом процесс изохорный и работа газа равна 0.
4-1: давление не меняется, объем и температура уменьшаются — работа газа отрицательна и внутренняя энергия уменьшается.
Оформим данные в таблицу:
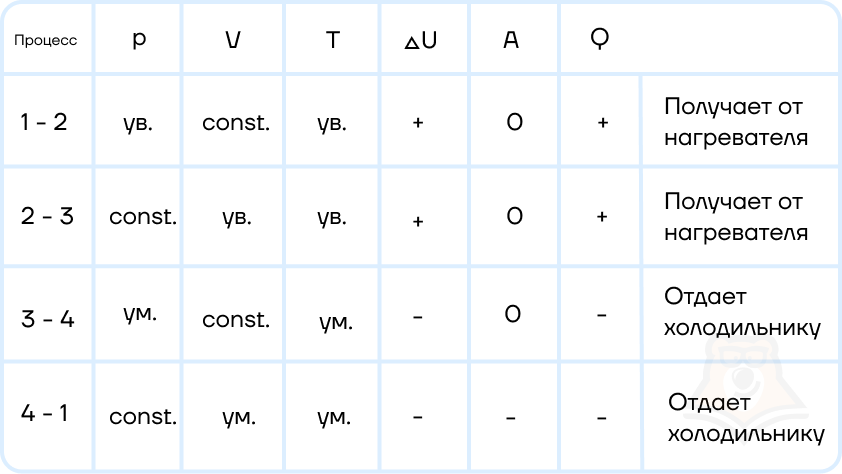
Отметим, что необходимое Q = Q12 + Q23.
Шаг 3. Запишем первый закон термодинамики для процессов 1-2 и 2-3:
(Q_{12} = U_{12} + A_{12} = Delta U_{12} = frac{3}{2}(2p_1V_1 -p_1V_1) = frac{3}{2}p_1V_1).
(Q_{23} = Delta U_{23} + A_{23}), работу газа найдем как площадь под графиком: A23 = 2p1(3V1 — V1) = 4p1V1.
(Delta U_{12} = frac{3}{2}(2p_1 * 3V_1 — 2p_1V_1) = 6p_1V_1).
(Q_{23} = Delta U_{23} + A_{23} = 10p_1V_1).
Шаг 4. Мы готовы считать КПД: (eta = frac{A}{Q} = frac{A}{Q_{12} + Q_{23}} = frac{2p_1V_1}{frac{3}{2}p_1V_1 + 10p_1V_1} = frac{4}{23} approx 0,17).
Ответ: 17%
Теперь вас не должно настораживать наличие графиков в условиях задач на расчет КПД тепловых машин. Продолжить обучение решению задач экзамена вы можете в статьях «Применение законов Ньютона» и «Движение точки по окружности».
Фактчек
- Тепловые двигатели — устройства, способные преобразовывать внутреннюю энергию в механическую.
- Тепловая машина принимает тепло от нагревателя, отдает холодильнику, а рабочим телом совершает работу.
- Коэффициент полезного действия (КПД) тепловой машины — это отношение полезной работы двигателя к энергии, полученной от нагревателя.
(eta = frac{A}{Q_1} = frac{Q_1 — Q_2}{Q_1} = 1 — frac{Q_2}{Q_1}) - Цикл Карно — цикл с максимально возможным КПД: (eta = frac{T_1 — T_2}{T_1} = 1 — frac{T_2}{T_1})
- Не забываем, что работа считается, как площадь фигуры под графиком.
Проверь себя
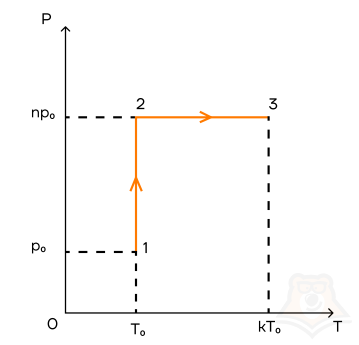
Задание 1.
1 моль идеального газа переходит из состояния 1 в состояние 2, а потом — в состояние 3 так, как это показано графике. Начальная температура газа равна T0 = 350 К. Определите работу газа при переходе из состояния 2 в состояние 3, если k = 3, а n = 2.
- 5672 Дж
- 4731 Дж
- 5817 Дж
- 6393 Дж
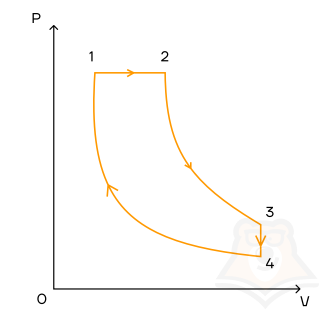
Задание 2.
1 моль идеального одноатомного газа совершает цикл, который изображен на pV-диаграмме и состоит из двух адиабат, изохоры, изобары. Модуль отношения изменения температуры газа при изобарном процессе ΔT12 к изменению его температуры ΔT34 при изохорном процессе равен 1,5. Определите КПД цикла.
- 0,6
- 0,5
- 0,8
- 1
Задание 3.
В топке паровой машины сгорело 50 кг каменного угля, удельная теплота сгорания которого равна 30 МДж/кг. При этом машиной была совершена полезная механическая работа 135 МДж. Чему равен КПД этой тепловой машины? Ответ дайте в процентах.
- 6%
- 100%
- 22%
- 9%
Задание 4.
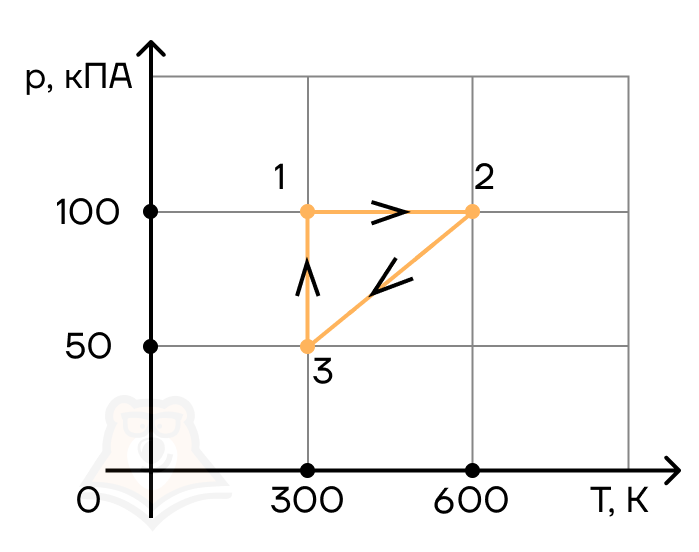
С двумя молями одноатомного идеального газа совершают циклический процесс 1–2–3–1 (см. рис.). Чему равна работа, совершаемая газом на участке 1–2 в этом циклическом процессе?
- 4444 Дж
- 2891 Дж
- 4986 Дж
- 9355 Дж
Ответы:1 — 3; 2 — 1; 3 — 4; 4 — 3.
Цикл
Карно—
это обратимый круговой процесс, состоящий
из двух адиабатических и двух изотермических
процессов. В процессе Карно термодинамическая
система выполняет механическую работу
и обменивается теплотой с
двумя тепловыми резервуарами, имеющими
постоянные, но различающиеся температуры.
Резервуар с более высокой температурой
называется нагревателем, а с более
низкой температурой — холодильником.
КПД
для идеального газа—
Вычислим
КПД цикла Карно для идеального газа.
При изотермическом процессе внутренняя
энергия идеального газа остаётся
постоянной. Поэтому количество полученной
газом теплоты равно
работе ,
совершаемой газом при переходе из
состояния 1 в состояние 2.(рис 2)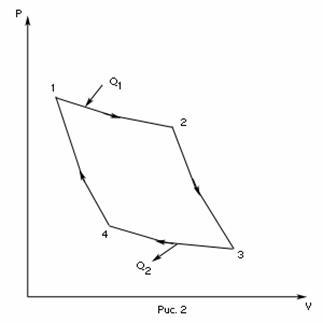
,
где –
масса идеального газа в тепловой машине.
Количество
отдаваемой холодильнику теплоты равно
работе ,
затраченной на сжатие газа при переходе
его из состояния 3 в состояние 4. Эта
работа равна
.
Для
того чтобы цикл был замкнутым, состояние
1 и 4 должны лежать на одной и той же
адиабате. Отсюда вытекает условие
.
Аналогично
для состояний 2 и 3 должно вытекать
условие
.
Разделив
одно соотношение на другое, приходим к
условию замкнутости цикла
.
Теперь
подставляя и
в
выражение для КПД, получим
.
(2)
В
результате получим формулу для КПД
цикла Карно:
26. Барометрическая формула. Распределение Больцмана.
При
выводе основного уравнения
молекулярно-кинетической теории газов
и максвелловского распределения молекул
по скоростям делалось предположение,
что внешние силы не действуют на молекулы
газа, поэтому молекулы равномерно
распределены по объему. Но молекулы
любого газа находятся в потенциальном
поле тяготения Земли. Сила тяжести, с
одной стороны, и тепловое движение
молекул — с другой, приводят газ к
некоторому стационарному состоянию,
при котором давление газа с высотой
уменьшается.
Выведем
закон изменения давления с высотой,
предполагая при этом, что масса всех
молекул одинакова, поле тяготения
однородно и температура постоянна.
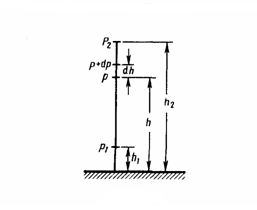
Рис.1
Если
атмосферное давление на высоте h равно
р (рис. 1), то на высоте h+dh оно равно p+dp
(при dh>0 dp<0, так как давление с высотой
уменьшается). Разность давлений р и p+dp
равна весу газа, заключенного в объеме
цилиндра высотой dh с основанием площадью
1 м2:
где
ρ — плотность газа на высоте h (dh настолько
мало, что при изменении высоты в этом
интервале плотность газа можно считать
постоянной). Значит,
(1)
Зная
уравнение состояния идеального газа
pV=(m/M) RT (m — масса газа, М — молярная масса
газа), находим, что
Подставив
это выражение в (1), получим
или
С
изменением высоты от h1 до
h2 давление
изменяется от р1 до
р2 (рис.
67), т. е.
или
(2)
Выражение
(2) называется барометрической
формулой.
Она позволяет вычислить атмосферное
давление в зависимости от высоты или,
измеряя давление, найти высоту: Так как
высоты считаются относительно уровня
моря, где давление считается нормальным,
то выражение (2) может быть представлено
в виде
(3)
где
р — давление на высоте h.
Прибор
для определения высоты над земной
поверхностью называется высотомером (или альтиметром).
Его работа основана на применении
формулы (3). Из этой формулы следует, что
чем тяжелее газ, тем давление с высотой
убывает тем быстрее.
Барометрическую
формулу (3) можно преобразовать, если
воспользоваться формулой p=nkT:
где
n – концентрация молекул на высоте h,
n0 –
то же, на высоте h=0. Так как M=m0NA (NA –
постоянная Авогадро, m0 –
масса одной молекулы), a R=kNA,
то
(4)
где
m0gh=P
— потенциальная энергия молекулы в
поле тяготения, т. е.
(5)
Выражение
(5) называется распределением
Больцмана для
внешнего потенциального поля. Из него
видно, что при постоянной температуре
плотность газа больше там, где меньше
потенциальная энергия его молекул.
Если
частицы находятся в состоянии хаотического
теплового движения и имеют одинаковую
массу и , то распределение Больцмана
(5) применимо в любом внешнем потенциальном
поле, а не только в поле сил тяжести.
Соседние файлы в предмете Физика
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
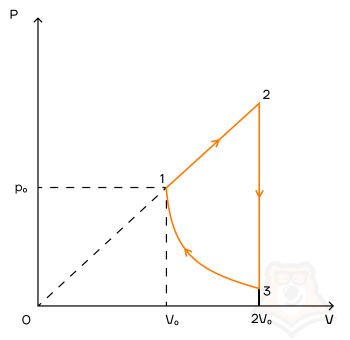
Условие задачи:
Задача №5.5.54 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
(eta-?)
Решение задачи:
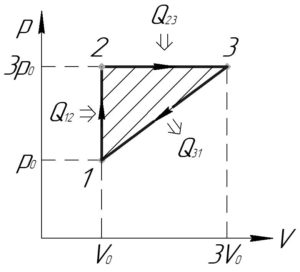
[eta = frac{A}{{{Q_н}}};;;;(1)]
Работу цикла (A) численно равна площади фигуры цикла в координатах p-V, при этом если цикл обходится по часовой стрелке, то работа цикла будет положительной (как у нас). Фигура цикла представляет собой прямоугольный треугольник, поэтому:
[A = frac{1}{2}left( {3{p_0} – {p_0}} right)left( {3{V_0} – {V_0}} right)]
[A = 2{p_0}{V_0};;;;(2)]
Теперь нужно определить процессы в цикле, в которых теплота подводилась к газу. Запишем первый закон термодинамики:
[Q = Delta U + A;;;;(3)]
Также запишем формулу для определения изменения внутренней энергии одноатомного идеального газа (Delta U):
[Delta U = frac{3}{2}nu RDelta T;;;;(4)]
Запишем уравнение Клапейрона-Менделеева для точек 1-3:
[left{ begin{gathered}
{p_0}{V_0} = nu R{T_1} ;;;;(5)hfill \
3{p_0}{V_0} = nu R{T_2} ;;;;(6)hfill \
3{p_0} cdot 3{V_0} = nu R{T_3} ;;;;(7)hfill \
end{gathered} right.]
Рассмотрим изохорный процесс 1-2 ((V=const)), работа газа (A_{12}) в таком процессе равна нулю. Тогда количество теплоты (Q_{12}) по формуле (3), учитывая формулу (4), равно:
[{Q_{12}} = frac{3}{2}nu RDelta {T_{12}};;;;(8)]
Так как давление в процессе 1-2 растёт, значит растёт и температура, то есть (Delta T_{12}>0). Поэтому, согласно формуле (8) (Q_{12}>0), то есть теплота в процессе 1-2 подводилась к газу. Учитывая формулы (5) и (6), формула (8) примет вид:
[{Q_{12}} = frac{3}{2}left( {3{p_0}{V_0} – {p_0}{V_0}} right) = 3{p_0}{V_0};;;;(9)]
Теперь рассмотрим изобарный процесс 2-3 ((p=const)). Работа газа (A_{23}) в таком процессе равна:
[{A_{23}} = 3{p_0}left( {3{V_0} – {V_0}} right) = 3{p_0} cdot 3{V_0} – 3{p_0}{V_0}]
Учитывая уравнения (6) и (7), имеем:
[{A_{23}} = nu RDelta {T_{23}}]
Количество теплоты (Q_{23}) по формуле (3), учитывая формулу (4), равно:
[{Q_{23}} = frac{3}{2}nu RDelta {T_{23}} + nu RDelta {T_{23}}]
[{Q_{23}} = frac{5}{2}nu RDelta {T_{23}};;;;(10)]
Так как объем в процессе 2-3 увеличивается, то по закону Гей-Люссака увеличивается и температура ((Delta T_{23}>0)). Поэтому, согласно формуле (10) (Q_{23}>0), то есть теплота в процессе 2-3 к газу подводилась. Учитывая формулы (6) и (7), формула (10) примет вид:
[{Q_{23}} = frac{5}{2}left( {3{p_0} cdot 3{V_0} – 3{p_0}{V_0}} right) = 15{p_0}{V_0};;;;(11)]
Так как в процессах 1-2 и 2-3 теплота подводится, значит в процессе 3-1 она отводится, так как хотя бы в одном из процессов цикла она должна отводится. Поэтому количество теплоты (Q_н), полученное от нагревателя, равно:
[{Q_н} = {Q_{12}} + {Q_{23}}]
Подставим в эту формулу выражения (9) и (11), тогда:
[{Q_н} = 3{p_0}{V_0} + 15{p_0}{V_0}]
[{Q_н} = 18{p_0}{V_0};;;;(12)]
В формулу (1) для определения КПД (eta) подставим выражения (2) и (12):
[eta = frac{{2{p_0}{V_0}}}{{18{p_0}{V_0}}} = frac{2}{{18}} = 0,111 = 11,1% ]
Ответ: 11,1%.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
5.5.53 В некотором процессе газу сообщено 900 Дж теплоты, а его внутренняя энергия
5.5.55 В идеальном тепловом двигателе за счёт каждого килоджоуля энергии, полученной
5.5.56 Холодильник идеального теплового двигателя имеет температуру 27 C. Как изменится
2 начало термодинамики.
- Постулат Клаузиуса: «Невозможен процесс, единственным результатом которого являлась бы передача тепла от более холодного тела к более горячему»[1] (такой процесс называется процессом Клаузиуса).
- Постулат Томсона (Кельвина): «Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара» (такой процесс называется процессом Томсона).
Тепловые машины.
Идеальная тепловая машина — машина, в которой произведённая работа и разница между количеством подведённого и отведённого тепла равны. Работа идеальной тепловой машины описывается циклом Карно.
При работе часть тепла Q1 передается от нагревателя к рабочему телу, а затем часть энергии Q2 передается холодильнику, который охлаждает машину. КПД тепловой машины считается по формуле ((Q1-Q2)/Q1)х100.
Периодически действующий двигатель, совершающий работу за счет получаемого извне тепла, называется тепловой машиной.
Циклические процессы.
Как правило, любая тепловая машина (двигатель) использует циклический процесс. Ее
рабочее тело
, т.е. термодинамическая система, преобразующая часть полученного тепла в работу, периодически через цикл приходит в начальное состояние.
Так как в результате циклического процесса внутренняя энергия не изменяется, т.е. , то из первого начала термодинамики следует, что совершенная за цикл работа равна площади петли цикла на диаграмме p-V и она же равна разности полученной и отданной за цикл теплоты: A=Q1-Q2.
равен отношению произведенной за цикл работы к полученному от нагревателя теплу: Заметим, что тепло распространяется от нагретого тела к холодному, но не наоборот:
.
Это утверждает
формулировка Клаузиуса
второго начала термодинамики: невозможны такие процессы, единственным результатом которых был бы переход тепла от холодного тела к нагретому.
КПД циклического процесса.
КПД теплово́го дви́гателя — отношение совершённой полезной работы двигателя, к энергии, полученной от нагревателя. КПД теплового двигателя может быть вычислен по следующей формуле
,
где — количество теплоты, полученное от нагревателя,
— количество теплоты, отданное холодильнику. Наибольшим КПД среди циклических машин, оперирующих при заданных температурах горячего источника T1 и холодного T2, обладают тепловые двигатели, работающие по циклу Карно; этот предельный КПД равен
.
Цикл Карно.
Цикл Карно является обратимым циклическим процессом с двумя источниками теплоты, имеющими разные, но постоянные температуры. Так как температуры источников тепла постоянные, а процессы получения и отдачи рабочим веществом тепла должны быть обратимыми, то эти процессы могут быть только изотермическими. При этом температура рабочего вещества в цикле должна, очевидно, меняться без теплообмена с окружающей средой, т.е. в адиабатных условиях. Поэтому цикл Карно состоит из двух обратимых изотермических и двух обратимых адиабатных процессов, чередующихся между собой.
Цикл Карно осуществляется рабочим веществом следующим образом (рис. 1).
| рис. 1 |
Рабочее вещество, расширяясь изотермически от состояния до состояния
, получает количество тепла
от горячего источника, имеющего температуру на бесконечно малую величину
большую, чем температура рабочего вещества (обратимость), т. е.
. При этом, если в качестве рабочего вещества взять идеальный газ, то он производит работу (2.7.22), равную количеству полученного тепла
:
| (4.11.1) |
В состоянии 2 к рабочему веществу прекращается подвод тепла и затем в обратимом адиабатном процессе расширения до объема температура рабочего вещества уменьшается до температуры T2 , которая на бесконечно малую величину dT больше температуры холодного источника
Далее рабочее вещество изотермически
обратимо сжимается от объема V3 до объема V4. При этом рабочее вещество (идеальный газ) отдает холодному источнику количество тепла
| (4.11.2) |
Откуда находим
| (4.11.3) |
Наконец, замыкающим цикл процессом является обратимый адиабатный процесс, в котором рабочее вещество возвращается в начальное состояние 1.
Вычислим КПД цикла Карно. По определению КПД любого цикла
| (4.11.4) |
Подставляя выражения (4.11.1) и (4.11.3) в (4.11.4), получим
| (4.11.5) |
Из последнего выражения видно, что КПД цикла не зависит от количества рабочего вещества . Уравнение адиабаты идеального газа
запишем для двух адиабатных процессов 23 и 41:
| (4.11.6) |
| (4.11.7) |
Откуда находим
| (4.11.8) |
Подставив последнее выражение в (4.11.5), будем иметь:
| (4.11.9) |
Таким образом, КПД цикла Карно, произведенного с идеальным газом, определяется только температурами T1 (горячего) и T2 (холодного) источников тепла. При этом тем больше, чем больше разность между T1 и T2 . КПД цикла Карно равен 1 в двух практически недостижимых случаях: когда
или, когда T2 =0 . Если КПД цикла равен единице, то из выражения (4.11.4) следует, что Q2=0 , т. е. все тепло Q1 , полученное от горячего источника, преобразуется в работу, что запрещено вторым началом термодинамики. Следовательно, КПД никакого цикла, в том числе и цикла Карно, не может быть равен единице.
Теплота сгорания топлива.
Теплота́ сгора́ния — это количество выделившейся теплоты при полном сгорании массовой (для твердых и жидких веществ) или объёмной (для газообразных) единицы вещества. Измеряется в джоулях или калориях. Теплота сгорания, отнесённая к единице массы или объёма топлива, называется удельной теплотой сгорания (дж или кал на 1 кг, м³ или моль).
Уде́льная теплота́ сгора́ния то́плива — физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг или объёмом 1 м³.
Удельная теплота сгорания измеряется в Дж/кг (Дж/м³) или калория/кг (калория/м³). Для экспериментального измерения этой величины используются методы калориметрии.