Физические свойства
Литий — это щелочной металл, серебристо-белого цвета. Самый легкий из металлов, мягкий, низкая температура плавления.
Способ получения
Литий получают в промышленности электролизом расплава хлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси):
2LiCl = 2Li + Cl2
Качественная реакция
Качественная реакция на литий — окрашивание пламени солями лития в карминно-красный цвет.
Химические свойства
Литий — активный металл; на воздухе реагирует с кислородом и азотом, и покрывается оксидно-нитридной пленкой. Воспламеняется при умеренном нагревании; окрашивает пламя газовой горелки в темно-красный цвет.
1. Литий — сильный восстановитель. Поэтому он реагирует почти со всеми неметаллами.
1.1. Литий легко реагирует с галогенами с образованием галогенидов:
2Li + I2 = 2LiI
1.2. Литий реагирует с серой с образованием сульфида лития:
2Li + S = Li2S
1.3. Литий активно реагирует с фосфором и водородом. При этом образуются бинарные соединения — фосфид лития и гидрид лития:
3Li + P = Li3P
2Li + H2 = 2LiH
1.4. С азотом литий реагирует при комнатной температуре с образованием нитрида:
6Li + N2 = 2Li3N
1.5. Литий реагирует с углеродом с образованием карбида:
2Li + 2C = Li2C2
1.6. При взаимодействии с кислородом литий образует оксид.
4Li + O2 = 2Li2O
2. Литий активно взаимодействует со сложными веществами:
2.1. Литий бурно реагирует с водой. Взаимодействие лития с водой приводит к образованию щелочи и водорода. Литий реагирует бурно, но без взрыва.
2Li0 + H2+O = 2Li+OH + H20
Видеоопыт: взаимодействие щелочных металлов с водой можно посмотреть здесь.
2.2. Литий взаимодействует с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой) со взрывом. При этом образуются соль и водород.
Например, литий бурно реагирует с соляной кислотой:
2Li + 2HCl = 2LiCl + H2↑
2.3. При взаимодействии лития с концентрированной серной кислотой выделяется сероводород.
Например, при взаимодействии лития с концентрированной серной кислотой образуется сульфат лития, диоксид серы и вода:
2Li + 3H2SO4(конц.) = 2LiHSO4 + SO2↑ +2H2O
2.4. Литий реагирует с азотной кислотой:
3Li + 4HNO3(разб.) = 3LiNO3 + NO↑ +2H2O
2.5. Литий может реагировать даже с веществами, которые проявляют очень слабые кислотные свойства. Например, с аммиаком, ацетиленом (и прочими терминальными алкинами), спиртами, фенолом и органическими кислотами.
Например, при взаимодействии лития с аммиаком образуются амиды и водород:
2Li + 2NH3 = 2LiNH2 + H2 ↑
2.6. В расплаве литий может взаимодействовать с некоторыми солями. Обратите внимание! В растворе литий будет взаимодействовать с водой, а не с солями других металлов.
Например, литий взаимодействует в расплаве с хлоридом алюминия :
3Li + AlCl3 → 3LiCl + Al
| Литий | |
|---|---|
| Очень лёгкий, очень мягкий металл серебристо-белого цвета | |

Литий |
|
| Название, символ, номер | литий / Lithium (Li), 3 |
| Атомная масса (молярная масса) |
[6,938; 6,997]а. е. м. (г/моль) |
| Электронная конфигурация | [He] 2s1 |
| Радиус атома | 145 пм |
| Ковалентный радиус | 134 пм |
| Радиус иона | 76 (+1e) пм |
| Электроотрицательность | 0,98 (шкала Полинга) |
| Электродный потенциал | -3,06В |
| Степени окисления | +1 |
| Энергия ионизации (первый электрон) |
519,9 (5,39) кДж/моль (эВ) |
| Плотность (при н. у.) | 0,534 г/см³ |
| Температура плавления | 453,69 K (180,54 °C, 356,97 °F) |
| Температура кипения | 1613 K (1339,85 °C, 2443,73 °F) |
| Уд. теплота плавления | 2,89 кДж/моль |
| Уд. теплота испарения | 148 кДж/моль |
| Молярная теплоёмкость | 24,86 Дж/(K·моль) |
| Молярный объём | 13,1 см³/моль |
| Структура решётки | кубическая объёмноцентрированная |
| Параметры решётки | 3,490 Å |
| Температура Дебая | 400 K |
| Теплопроводность | (300 K) 84,8 Вт/(м·К) |
| Номер CAS | 7439-93-2 |
Литий (Li, лат. lithium) — химический элемент первой группы, второго периода периодической системы с атомным номером 3. Как простое вещество представляет собой мягкий щелочной металл серебристо-белого цвета.
Содержание
- 1 История и происхождение названия
- 2 Физические свойства
- 3 Химические свойства
- 4 Нахождение в природе
- 4.1 Геохимия лития
- 4.2 Месторождения
- 4.3 Изотопы лития
- 4.4 В космосе
- 5 Получение
- 5.1 Добыча
- 6 Применение
- 6.1 Термоэлектрические материалы
- 6.2 Химические источники тока
- 6.3 Лазерные материалы
- 6.4 Окислители
- 6.5 Дефектоскопия
- 6.6 Пиротехника
- 6.7 Сплавы
- 6.8 Электроника
- 6.9 Металлургия
- 6.9.1 Металлургия алюминия
- 6.10 Ядерная энергетика
- 6.10.1 Литий-6
- 6.10.2 Литий-7
- 6.11 Сушка газов
- 6.12 Медицина
- 6.13 Смазочные материалы
- 6.14 Регенерация кислорода в автономных аппаратах
- 6.15 Силикатная промышленность
- 6.16 Прочие области применения
- 7 Биологическое значение лития
- 8 Цены
История и происхождение названия
Литий был открыт в 1817 году шведским химиком и минералогом Иоганном Арфведсоном сначала в минерале петалите (Li,Na)[Si4AlO10], а затем в сподумене LiAl[Si2O6] и в лепидолите K2Li3Al5[Si6O20](F,OH)4. Металлический литий впервые получил Гемфри Дэви в 1818 году.
Своё название литий получил из-за того, что был обнаружен в «камнях» (греч. λίθος — камень). Первоначально назывался «литион», современное название было предложено Берцелиусом.
Физические свойства
Литий — серебристо-белый металл, мягкий и пластичный, твёрже натрия, но мягче свинца. Его можно обрабатывать прессованием и прокаткой.
При комнатной температуре металлический литий имеет кубическую объёмноцентрированную решётку (координационное число 8), пространственная группа I m3m, параметры ячейки a = 0,35021 нм, Z = 2. Ниже 78 К устойчивой кристаллической формой является гексагональная плотноупакованная структура, в которой каждый атом лития имеет 12 ближайших соседей, расположенных в вершинах кубооктаэдра. Кристаллическая решётка относится к пространственной группе P 63/mmc, параметры a = 0,3111 нм, c = 0,5093 нм, Z = 2.
Из всех щелочных металлов литий характеризуется самыми высокими температурами плавления и кипения (180,54 и 1340 °C, соответственно), у него самая низкая плотность при комнатной температуре среди всех металлов (0,533 г/см³, почти в два раза меньше плотности воды). Вследствие своей низкой плотности литий всплывает не только в воде, но и, например, в керосине.
Маленькие размеры атома лития приводят к появлению особых свойств металла. Например, он смешивается с натрием только при температуре ниже 380 °C и не смешивается с расплавленными калием, рубидием и цезием, в то время как другие па́ры щелочных металлов смешиваются друг с другом в любых соотношениях.
Карминово-красное окрашивание пламени солями лития
Химические свойства
Литий является щелочным металлом, однако относительно устойчив на воздухе. Литий является наименее активным щелочным металлом, с сухим воздухом (и даже с сухим кислородом) при комнатной температуре практически не реагирует. По этой причине литий является единственным щелочным металлом, который не хранят в керосине (к тому же плотность лития столь мала, что он будет в нём плавать); он может непродолжительное время храниться на воздухе.
Во влажном воздухе медленно реагирует с азотом и другими газами, находящимися в воздухе, превращаясь в нитрид Li3N, гидроксид LiOH и карбонат Li2CO3.
6Li + N2 ⟶ 2Li3N
2Li + 2H2O ⟶ 2LiOH + H2
Поэтому длительно литий хранят в петролейном эфире, парафине, газолине и/или минеральном масле в герметически закрытых жестяных коробках.
В кислороде при нагревании горит, превращаясь в оксид Li2O.
4Li + O2 ⟶ 2Li2O
Интересная особенность лития в том, что в интервале температур от 100 °C до 300 °C он покрывается плотной оксидной плёнкой и в дальнейшем не окисляется. В отличие от остальных щелочных металлов, дающих стабильные надпероксиды и озониды; надпероксид и озонид лития — нестабильные соединения.
В 1818 немецкий химик Леопольд Гмелин установил, что литий и его соли окрашивают пламя в карминово-красный цвет, это является качественным признаком для определения лития. Температура самовоспламенения находится в районе 300 °C. Продукты горения раздражают слизистую оболочку носоглотки.
Спокойно, без взрыва и возгорания, реагирует с водой, образуя LiOH и H2.
-
- 2Li + 2H2O → 2LiOH + H2
Реагирует также с этиловым спиртом (с образованием этанолята):
2Li + 2C2H5OH ⟶ 2C2H5OLi + H2
Вступает в реакцию с водородом (при 500—700 °C) с образованием гидрида лития:
2Li + H2 ⟶ 2LiH
Реагирует с аммиаком при нагревании, при этом сначала образует амид лития (220 °C), а затем имид лития (400 °C):
2Li + 2NH3 ⟶ 2LiNH2 + H2
2Li + NH3 ⟶ Li2NH + H2
Реагируя с галогенами (с йодом — только при нагревании, выше 200 °C) образует соответствующие галогениды:
2Li + F2 ⟶ 2LiF
2Li + Cl2 ⟶ 2LiCl
2Li + Br2 ⟶ 2LiBr
2Li + I2 ⟶ 2LiI
При 130 °C реагирует с серой с образованием сульфида:
2Li + S ⟶ Li2S
В вакууме при температуре выше 200 °C реагирует с углеродом (образуется ацетиленид):
2Li + 2C ⟶ Li2C2
При 600—700 °C литий реагирует с кремнием с образованием силицида:
4Li + Si ⟶ Li4Si
Химически растворим в жидком аммиаке (−40 °C), образуется синий раствор.
В водном растворе ион лития имеет самый низкий стандартный электродный потенциал (−3,045 В) из-за малого размера и высокой степени гидратации иона лития.
Металлический литий вызывает ожоги при попадании на влажную кожу, слизистые оболочки и в глаза.
Нахождение в природе
Геохимия лития
Литий по геохимическим свойствам относится к крупноионным литофильным элементам, в числе которых калий, рубидий и цезий. Содержание лития в верхней континентальной коре составляет 21 г/т, в морской воде 0,17 мг/л.
Основные минералы лития — слюда лепидолит — KLi1,5Al1,5[Si3AlO10](F, OH)2 и пироксен сподумен — LiAl[Si2O6]. Когда литий не образует самостоятельных минералов, он изоморфно замещает калий в широко распространённых породообразующих минералах.
Месторождения лития приурочены к редкометалльным гранитным интрузиям, в связи с которыми развиваются литиеносные пегматиты или гидротермальные комплексные месторождения, содержащие также олово, вольфрам, висмут и другие металлы. Стоит особо отметить специфические породы онгониты — граниты с магматическим топазом, высоким содержанием фтора и воды и исключительно высокими концентрациями различных редких элементов, в том числе и лития.
Другой тип месторождений лития — рассолы некоторых сильносолёных озёр.
Месторождения
Месторождения лития известны в Чили, Боливии (Солончак Уюни — крупнейшее в мире), США, Аргентине, Конго, Китае (озеро Чабьер-Цака), Бразилии, Сербии, Австралии.
В России более 50 % запасов сосредоточено в редкометалльных месторождениях Мурманской области.
Изотопы лития
Основная статья: Изотопы лития
Природный литий состоит из двух стабильных изотопов: 6Li (7,5 %) и 7Li (92,5 %); в некоторых образцах лития изотопное соотношение может быть сильно нарушено вследствие природного или искусственного фракционирования изотопов. Это следует иметь в виду при точных химических опытах с использованием лития или его соединений. У лития известны 7 искусственных радиоактивных изотопов (4Li − 12Li) и два ядерных изомера (10m1Li и 10m2Li). Наиболее устойчивый из них, 8Li, имеет период полураспада 0,8403 с. Экзотический изотоп 3Li (трипротон), по-видимому, не существует как связанная система.
7Li является одним из немногих изотопов, возникших при первичном нуклеосинтезе (то есть в период от 1 секунды до 3 минут после Большого Взрыва) в количестве не более 10−9 от всех элементов. Некоторое количество изотопа 6Li, как минимум в десять тысяч раз меньшее, чем 7Li, также образовано в первичном нуклеосинтезе.
Примерно в десять раз больше 7Li образовались в звёздном нуклеосинтезе. Литий является промежуточным продуктом реакции ppII, но при высоких температурах активно преобразуется в два ядра гелия-4 (через 8Be).
В космосе
Аномально высокое содержание лития наблюдается в звёздных образованиях, состоящих из красного гиганта (или сверхгиганта), внутри которого находится нейтронная звезда — объектах Ландау — Торна — Житкова.
Также имеется большое количество звёзд-гигантов с необычно высоким содержанием лития, что объясняется попаданием лития в атмосферу звёзд при поглощении ими экзопланет-гигантов.
Получение
- Сырьё
Исходным сырьём для лития служат два источника: минеральное сырьё (например, сподумен) и солевые растворы из соляных озёр, богатые солями лития. В обоих случаях результатом работы является карбонат лития Li2CO3.
Сподумен (силикат лития и алюминия) можно перерабатывать несколькими способами. Например, спеканием с сульфатом калия получают растворимый сульфат лития, который осаждают из раствора содой:
- Li2SO4 + Na2CO3 ⟶ Li2CO3↓ + Na2SO4 .
Солевые растворы предварительно выпаривают. В солевых растворах содержится хлорид лития LiCl. Однако вместе с ним содержатся большие количества других хлоридов. Для увеличения концентрации лития из выпаренного раствора осаждают карбонат лития Li2CO3, например по схеме
- 2LiCl + Na2CO3 ⟶ Li2CO3↓ + 2NaCl.
- Получение металла
Металлический литий чаще всего получают электролизом расплава солей или восстановлением из оксида.
- Электролиз
При электролизе используется хлорид лития. Его получают из карбоната по схеме:
- Li2CO3 + 2HCl ⟶ 2LiCl + H2O + CO2.
Поскольку температура плавления хлорида лития близка к температуре кипения лития, применяют эвтектическую смесь с хлоридом калия или бария, что понижает температуру расплава и позволяет избавиться от необходимости улавливать пары металла. Расход электроэнергии до 14 кВт∙ч на 1 кг лития. На другом электроде получают газообразный хлор.
- Восстановление
Поскольку литий — активный металл, его восстановление из оксидов или галогенидов возможно только при немедленном удалении лития из зоны реакции. В противном случае невозможно сместить баланс реакции в нужную сторону. Литий удаляют из зоны реакции путём поддержания температур, при которых литий испаряется и покидает зону реакции в виде паров. Другие реагенты при этом должны оставаться в расплаве. Для восстановления используются кремний или алюминий, например:
- 2Li2O + Si ⟶ 4Li↑ + SiO2
- Рафинирование
Полученный литий очищают методом вакуумной дистилляции, последовательно выпаривая разные металлы из сплава при определённых температурах.
Добыча
В 2015 году в мире добыли 32,5 тыс. тонн лития и его соединений в пересчёте на металл. Крупнейшие страны по добыче — Австралия, Чили и Аргентина. В России собственная добыча лития была полностью утрачена после распада СССР, но в 2017 году Россия запустила экспериментальную установку, позволяющую добывать литий из бедных руд с небольшими затратами.
Большая часть добывается из естественных водных линз в толще соляных озёр, в насыщенных соляных растворах которых концентрируется хлорид лития. Раствор выкачивается и выпаривается на солнце, полученная смесь солей перерабатывается. Содержание лития в растворе колеблется от 0,01 % до 1 %. Также значительная доля добычи приходится на минеральное сырьё, например, минерал сподумен.
Применение
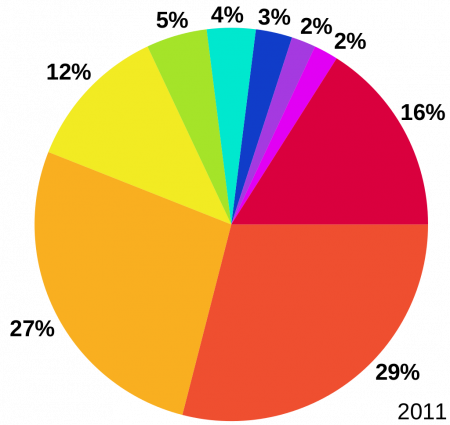
Оценка использования лития в мире в 2011 году: Керамика и стекло (29 %) Источники тока (27 %) Смазочные материалы (12 %) Непрерывная разливка стали (5 %) Регенерация кислорода (4 %) Полимеры (3 %) Металлургия алюминия (2 %) Фармацевтика (2 %) другое (16 %)
Термоэлектрические материалы
Сплав сульфида лития и сульфида меди — эффективный полупроводник для термоэлектропреобразователей (ЭДС около 530 мкВ/К).
Химические источники тока
Из лития изготовляют аноды химических источников тока (аккумуляторов, например, литий-хлорных аккумуляторов) и гальванических элементов с твёрдым электролитом (например, литий-хромсеребряный, литий-висмутатный, литий-окисномедный, литий-двуокисномарганцевый, литий-иодсвинцовый, литий-иодный, литий-тионилхлоридный, литий-оксидванадиевый, литий-фторомедный, литий-двуокисносерный элементы), работающих на основе неводных жидких и твёрдых электролитов (тетрагидрофуран, пропиленкарбонат, метилформиат, ацетонитрил).
Кобальтат лития и молибдат лития показали лучшие эксплуатационные свойства и энергоёмкость в качестве положительного электрода литиевых аккумуляторов.
Гидроксид лития используется как один из компонентов для приготовления электролита щелочных аккумуляторов. Добавление гидроксида лития к электролиту тяговых железо-никелевых, никель-кадмиевых, никель-цинковых аккумуляторных батарей повышает их срок службы в 3 раза и ёмкость на 21 % (за счёт образования никелатов лития).
Алюминат лития — наиболее эффективный твёрдый электролит (наряду с цезий-бета-глинозёмом).
Лазерные материалы
Монокристаллы фторида лития используются для изготовления высокоэффективных (КПД 80 %) лазеров на центрах свободной окраски и для изготовления оптики с широкой спектральной полосой пропускания.
Окислители
Перхлорат лития используют в качестве окислителя.
Дефектоскопия
Сульфат лития используют в дефектоскопии.
Пиротехника
Нитрат лития используют в пиротехнике для окрашивания огней в красный цвет.
Сплавы
Сплавы лития с серебром и золотом, а также медью являются очень эффективными припоями. Сплавы лития с магнием, скандием, медью, кадмием и алюминием — новые перспективные материалы в авиации и космонавтике (из-за их лёгкости). На основе алюмината и силиката лития создана керамика, затвердевающая при комнатной температуре и используемая в военной технике, металлургии, и, в перспективе, в термоядерной энергетике. Огромной прочностью обладает стекло на основе литий-алюминий-силиката, упрочняемого волокнами карбида кремния. Литий очень эффективно упрочняет сплавы свинца и придаёт им пластичность и стойкость против коррозии.
Электроника
Триборат лития-цезия используется как оптический материал в радиоэлектронике. Кристаллические ниобат лития LiNbO3 и танталат лития LiTaO3 являются нелинейными оптическими материалами и широко применяются в нелинейной оптике, акустооптике и оптоэлектронике.
Литий также используется при наполнении осветительных газоразрядных металлогалогеновых ламп.
Гидроксид лития добавляют в электролит щелочных аккумуляторов для увеличения срока их службы.
Металлургия
В чёрной и цветной металлургии литий используется для раскисления и повышения пластичности и прочности сплавов. Литий иногда применяется для восстановления методами металлотермии редких металлов.
Металлургия алюминия
Карбонат лития является важнейшим вспомогательным веществом (добавляется в электролит) при выплавке алюминия, и его потребление растёт с каждым годом пропорционально объёму мировой добычи алюминия (расход карбоната лития 2,5—3,5 кг на тонну выплавляемого алюминия).
- Легирование алюминия
Введение лития в систему легирования позволяет получить новые сплавы алюминия с высокой удельной прочностью.
Добавка лития снижает плотность сплава и повышает модуль упругости. При содержании лития до 1,8 % сплав имеет низкое сопротивление коррозии под напряжением, а при 1,9 % сплав не склонен к коррозионному растрескиванию. Увеличение содержания лития до 2,3 % способствует возрастанию вероятности образования рыхлот и трещин. Механические свойства при этом изменяются: пределы прочности и текучести возрастают, а пластические свойства снижаются.
Наиболее известны системы легирования Al-Mg-Li (пример — сплав 1420, применяемый для изготовления конструкций летательных аппаратов) и Al-Cu-Li (пример — сплав 1460, применяемый для изготовления ёмкостей для сжиженных газов).
Ядерная энергетика
Изотопы 6Li и 7Li обладают разными ядерными свойствами (сечение поглощения тепловых нейтронов, продукты реакций) и сфера их применения различна. Гафниат лития входит в состав специальной эмали, предназначенной для захоронения высокоактивных ядерных отходов, содержащих плутоний.
Литий-6
Применяется в термоядерной энергетике.
При облучении нуклида 6Li тепловыми нейтронами получается радиоактивный тритий 3H:
- 36Li + 01n → 13H + 24He
Благодаря этому литий-6 может применяться как замена радиоактивного, нестабильного и неудобного в обращении трития как в военных (термоядерное оружие), так и в мирных (управляемый термоядерный синтез) целях. В термоядерном оружии обычно применяется дейтерид лития-6 6LiD.
Перспективно также использование лития-6 для получения гелия-3 (через тритий) с целью дальнейшего использования в дейтерий-гелиевых термоядерных реакторах.
Литий-7
Применяется в ядерных реакторах. Благодаря очень высокой удельной теплоёмкости и низкому сечению захвата тепловых нейтронов жидкий литий-7 (часто в виде сплава с натрием или цезием) служит эффективным теплоносителем. Фторид лития-7 в сплаве с фторидом бериллия (66 % LiF + 34 % BeF2) носит название «флайб» (FLiBe) и применяется как высокоэффективный теплоноситель и растворитель фторидов урана и тория в высокотемпературных жидкосолевых реакторах, и для производства трития.
Соединения лития, обогащённые по изотопу лития-7, применяются на реакторах PWR для поддержания водно-химического режима, а также в деминерализаторе первого контура. Ежегодная потребность США оценивается в 200—300 кг, производством обладают лишь Россия и Китай.
Сушка газов
Высокогигроскопичные бромид LiBr и хлорид лития LiCl применяются для осушения воздуха и других газов.
Медицина
Основная статья: Препараты лития
Соли лития обладают нормотимическими и другими лечебными свойствами. Поэтому они находят применение в медицине.
Смазочные материалы
Стеарат лития («литиевое мыло») используется в качестве загустителя для получения пастообразных высокотемпературных смазок машин и механизмов. См. напр.: Литол, ЦИАТИМ-201.
Регенерация кислорода в автономных аппаратах
Гидроксид лития LiOH, пероксид Li2O2 применяются для очистки воздуха от углекислого газа; при этом последнее соединение реагирует с выделением кислорода (например, 2Li2O2 + 2CO2 → 2Li2CO3 + O2), благодаря чему используется в изолирующих противогазах, в патронах для очистки воздуха на подлодках, на пилотируемых космических аппаратах и т. д.
Силикатная промышленность
Литий и его соединения широко применяют в силикатной промышленности для изготовления специальных сортов стекла и покрытия фарфоровых изделий.
Прочие области применения
Соединения лития используются в текстильной промышленности (отбеливание тканей), пищевой (консервирование) и фармацевтической (изготовление косметики).
Весьма перспективно использовать литий в качестве наполнителя поплавка батискафов — этот металл имеет плотность, почти в два раза меньшую, чем вода (точнее, 534 кг/м³), это значит, что один кубический метр лития может удерживать на плаву почти на 170 кг больше, чем один кубический метр бензина. Однако литий — щелочной металл, активно реагирующий с водой, следует каким-то образом надёжно разделить эти вещества, не допустить их контакта.
Из лития изготавливают аноды химических источников тока (например, литий-хлорных аккумуляторов) и гальванических элементов с твёрдым электролитом (например, литий-хромсеребряный, литий-висмутатный, литий-окисномедный, литий-двуокисномарганцевый, литий-иодсвинцовый, литий-иодный, литий-тионилхлоридный, литий-оксидванадиевый, литий-фторомедный, Литий-двуокисносерный элементы), работающих на основе неводных жидких и твёрдых электролитов (тетрагидрофуран, пропиленкарбонат, метилформиат, ацетонитрил). Кобальтат лития и молибдат лития показали лучшие эксплуатационные свойства и энергоёмкость в качестве положительного электрода литиевых аккумуляторов. Гидроксид лития используется как один из компонентов для приготовления электролита щелочных аккумуляторов. Добавление гидроксида лития к электролиту тяговых железо-никелевых, никель-кадмиевых, никель-цинковых аккумуляторных батарей повышает их срок службы в 3 раза и ёмкость на 21 % (за счёт образования никелатов лития). Алюминат лития — наиболее эффективный твёрдый электролит (наряду с цезий-бета-глинозёмом). Триборат лития-цезия используется как оптический материал в радиоэлектронике. Кристаллические ниобат лития LiNbO3 и танталат лития LiTaO3 являются нелинейными оптическими материалами и широко применяются в нелинейной оптике, акустооптике и оптоэлектронике. Литий также используется при наполнении осветительных газоразрядных металлогалогеновых ламп. Гидроксид лития добавляют в электролит щелочных аккумуляторов для увеличения срока их службы.
Биологическое значение лития
Литий в небольших количествах необходим организму человека (порядка 100 мкг/день для взрослых). Преимущественно в организме находится в щитовидной железе, лимфоузлах, сердце, печени, лёгких, кишечнике, плазме крови, надпочечниках.
Литий принимает участие в важных процессах:
- участвует в углеводном и жировом обменах;
- поддерживает иммунную систему;
- предупреждает возникновение аллергии;
- снижает нервную возбудимость.
Препараты лития широко используются в терапии психических расстройств.
Выделяется литий преимущественно почками.
Цены
По состоянию на конец 2007 — начало 2008 года, цены на металлический литий (чистота 99 %) составляли 63—66 долларов за 1 кг.
Литий
Ли́тий (лат. Lithium; обозначается символом Li) — элемент главной подгруппы первой группы, второго периода периодической системы химических элементов таблицы Менделеева, с атомным номером 3. Простое вещество литий (CAS-номер: 7439-93-2) — мягкий щелочной металл серебристо-белого цвета.
История и происхождение названия
Литий был открыт в 1817 году шведским химиком и минералогом А. Арфведсоном сначала в минерале петалите (Li,Na)[Si4AlO10], а затем в сподумене LiAl[Si2O6] и в лепидолите KLi1.5Al1.5[Si3AlO10](F,OH)2. Металлический литий впервые получил Гемфри Дэви в 1825 году.
Своё название литий получил из-за того, что был обнаружен в «камнях» (греч. λίθος — камень). Первоначально назывался «литион», современное название было предложено Берцелиусом.
Нахождение в природе
Геохимия лития
Литий по геохимическим свойствам относится к крупноионным литофильным элементам, в числе которых калий, рубидий и цезий. Содержание лития в верхней континентальной коре составляет 21 г/т, в морской воде 0,17 мг/л.
Основные минералы лития — слюда лепидолит — KLi1.5Al1.5[Si3AlO10] (F, OH)2 и пироксен сподумен — LiAl [Si2O6]. Когда литий не образует самостоятельных минералов, он изоморфно замещает калий в широко распространенных породообразующих минералах.
Месторождения лития приурочены к редкометалльным гранитным интрузиям, в связи с которыми развиваются литиеносные пегматиты или гидротермальные комплексные месторождения, содержащие также олово, вольфрам, висмут и другие металлы. Стоит особо отметить специфические породы онгониты — граниты с магматическим топазом, высоким содержанием фтора и воды, и исключительно высокими концентрациями различных редких элементов, в том числе и лития.
Другой тип месторождений лития — рассолы некоторых сильносоленых озёр.
Месторождения
Месторождения лития известны в России (более 50% запасов страны сосредоточено в редкометальных месторождениях Мурманской области), Боливии, Аргентине, Мексике, Афганистане, Чили, США, Канаде, Бразилии, Испании, Швеции, Китае, Австралии, Зимбабве, Конго.
Получение
В настоящее время для получения металлического лития его природные минералы или разлагают серной кислотой (кислотный способ), или спекают с CaO или CaCO3 (щелочной способ), или обрабатывают K2SO4 (солевой способ), а затем выщелачивают водой. В любом случае из полученного раствора выделяют плохо растворимый карбонат лития Li2CO3, который затем переводят в хлорид LiCl. Электролиз расплава хлорида лития проводят в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси).
2LiCl = 2Li + Cl2
В дальнейшем полученный литий очищают методом вакуумной дистилляции.
Физические свойства
Литий — серебристо-белый металл, мягкий и пластичный, твёрже натрия, но мягче свинца. Его можно обрабатывать прессованием и прокаткой.
Из всех щелочных металлов литий характеризуется самыми высокими температурами плавления и кипения (180,54 и 1340 °C, соответственно), у него самая низкая плотность при комнатной температуре среди всех металлов (0,533 г/см³, почти в два раза меньше плотности воды).
Маленькие размеры атома лития приводят к появлению особых свойств металла. Например, он смешивается с натрием только при температуре ниже 380 °C и не смешивается с расплавленными калием, рубидием и цезием, в то время как другие па́ры щелочных металлов смешиваются друг с другом в любых соотношениях.
Химические свойства
Литий является щелочным металлом, однако относительно устойчив на воздухе. Литий является наименее активным щелочным металлом, с сухим воздухом (и даже с сухим кислородом) при комнатной температуре практически не реагирует. По этой причине литий является единственным щелочным металлом, который не хранится в керосине (к тому же плотность лития столь мала, что он будет в нём плавать) и может непродолжительное время храниться на воздухе.
Во влажном воздухе медленно реагирует с азотом, находящимся в воздухе, превращаясь в нитрид Li3N, гидроксид LiOH и карбонат Li2CO3. В кислороде при нагревании горит, превращаясь в оксид Li2O. Есть интересная особенность, что в интервале температур от 100 °C до 300 °C литий покрывается плотной оксидной плёнкой, и в дальнейшем не окисляется.
В 1818 немецкий химик Леопольд Гмелин установил, что литий и его соли окрашивают пламя в карминово-красный цвет, это является качественным признаком для определения лития. Температура возгорания находится около 300 °C. Продукты горения раздражают слизистую оболочку носоглотки.
Спокойно, без взрыва и возгорания, реагирует с водой, образуя LiOH и H2. Реагирует также с этиловым спиртом (с образованием алкоголята), с водородом (при 500—700 °C) с образованием гидрида лития, с аммиаком и с галогенами (с иодом — только при нагревании). При 130 °C реагирует с серой с образованием сульфида. В вакууме при температуре выше 200 °C реагирует с углеродом (образуется ацетиленид). При 600—700 °C литий реагирует с кремнием с образованием силицида. Химически растворим в жидком аммиаке (−40 °C), образуется синий раствор.
Литий хранят в петролейном эфире, парафине, газолине и/или минеральном масле в герметически закрытых жестяных коробках. Металлический литий вызывает ожоги при попадании на влажную кожу, слизистые оболочки и в глаза.
Источник: Википедия
Другие заметки по химии
Литий
Литий — химический элемент 2-го периода, 1-й группы в периодической системе Менделеева. Данное название получил от собственного местонахождения (в «камнях», от греч. λίθος), в дальнейшем название видоизменялось. Представляет собой щелочной металл с атомным номером 3.
Изотопы
Литий природного происхождения состоит из двух изотопов: 6Li и 7Li, являющихся стабильными. 7Li входит в несчетно малое число изотопов, произошедших при таком процессе, как нуклеосинтез. Также, у лития существует 7 радиоактивных изотопов искусственного происхождения и 2 атомных изомера. Большей устойчивость среди них обладает 8Li.
Физические свойства лития
- Мягкий и пластичный металл с серебряно-белым окрасом
- Имеет способность к обработке прессом или прокатом
- При нормальных условиях имеет кристаллическую решетку в виде куба
- Температура плавления-180,54°С, кипения-1340 °C
- Низкая плотность
- Из-за малых размеров атома, литий имеет специфические свойства смешивания с другими металлами.
Химические свойства
Литий является самым неактивным среди щелочных металлов, оттого при комнатной температуре почти не вступает в реакции даже с воздухом (сухим). С тесанием долгого времени и только во влажном воздухе взаимодействует с азотом и прочими газами. При нагревании вступает в реакцию с кислородом, образуя оксид лития. Интересен и тот факт, что в пределах температур от 100°С до 300°С литий покрывается плотным слоем оксидный пленки, что позволяет ему не окисляться в дальнейшем. Качественные реакции заключаются в том, что литий и его соединения придают пламени красноватый оттенок. Спокойно протекает реакция лития с водой. Реагирует с рядом веществ: водород, аммиак и галогены (в большинстве случаев только при наличии определенной температуры). Взаимодействует и с такими веществами, как сера,углерод и кремний. Реагирует также с этиловым спиртом.
Геохимия лития
По степени распространенности относится к литофильным элементам (составляющие ~93 % массы земной коры и ~97 % массы солевого состава океанической воды). Основные его минералы — пироксен сподумен и слюда лепидолит. В случае, если литий не образовывает отдельные минералы, он в широких масштабах замещает калий в породообразующих минералах.
Его месторождениями является не только земля, но и рассолы немногих озёр. Также, необычайно высока концентрация лития в звездных образованиях, состоящих из сверхгиганта.
Широко применение лития в данных сферах:
- Как источник тока
- Материалы для смазки
- Регенерация кислорода
- Металлургия алюминия
- Фармацевтика
- Керамика и стекло
- Полимеры
- Безостановочная разливка стали
- Окислители
- Пиротехника
- Сплавы
- Электроника и радиоэлектроника
- Ядерная энергетика
- Сушка газов
- Медицина
- Текстильная промышленность
- Пищевая промышленность.
Биологическая роль лития
Так как литий участвует во многих важнейших для человека биологических процессах, его наличие в организме как микроэлемента незаменимо и достигает до 200 мкг/день для взрослого человека. В большей степени располагается в лимфоузлах, сердце, печени, кишечнике, щитовидной железе, лёгких, надпочечниках и в плазме крови.
Процессы, в которых литий принимает активное участие:
- Понижает уровень нервной возбудимости
- Поддерживает в норме иммунную систему
- Предупреждает возникновение аллергии
- Принимает участие в обменах углеродами и жирами
Помимо этого, литейные препараты нашли весьма обширное применение в профилактике и лечении психических расстройств. Выведение же лития из организма человека происходит главным образом через почки.
По материалам сайта chemicalportal.ru
Ли́тий (от греч. λίθος – камень; лат. Lithium), Li, химический элемент I группы короткой формы (1-й группы длинной формы) периодической системы, атомный номер 3, атомная масса 6,941 а. е. м.; относится к щелочным металлам. Природный литий состоит из двух стабильных изотопов 6Li (7,59 %) и 7Li (92,41 %), для которых сечения захвата тепловых нейтронов сильно различаются (9,45·10–26 м2 и 3,3·10–30 м2 соответственно). Искусственно получены радиоизотопы с массовыми числами 4–11. Литий открыт в 1817 г. шведским химиком А. Арфведсоном в минерале петалите. Металлический литий впервые получен в 1818 г. Г. Дэви.
Распространённость в природе
Содержание лития в земной коре составляет 6,5·10–3 % по массе; в свободном состоянии вследствие высокой химической активности не встречается. Литий накапливается преимущественно в пегматитах. Близость ионных радиусов Li+, Fe2+ и Mg2+ обусловливает вхождение Li+ в решётки магнезиально-железистых силикатов – пироксенов и амфиболов; литий содержится в виде изоморфной примеси в слюдах и др. Все минералы лития (силикаты, фосфаты и др.) редкие. Основные минералы: сподумен LiAl[Si2O6], лепидолит KLi1,5Al1,5[Si3AlO10](F,OH)2, петалит LiAl[Si4O10] и амблигонит LiAl[PO4](F,OH). Основные промышленные источники лития – пегматиты редких и рассеянных элементов (около 60 %) и рапа некоторых соляных озёр (до 40 %).

Свойства
Конфигурация внешней электронной оболочки атома лития 2s1; в соединениях проявляет степень окисления +1; энергия ионизации Li0→Li+ 5,392 эВ, электроотрицательность по Полингу 0,98; атомный радиус 145 пм, ионный радиус Li+ (в скобках приведены координационные числа) 73 пм (4); 90 пм (6); 106 пм (8).
Компактный литий – серебристо-белый металл, быстро покрывающийся тёмно-серым налётом, состоящим из нитрида Li3N и оксида Li2O. При обычной температуре литий кристаллизуется в кубической объёмноцентрированной решётке; при температуре ниже –193 °C решётка гексагональная плотноупакованная; tпл 180,54 °C, tкип 1342 °C; самый лёгкий металл, плотность 0,534 г/см3 (25 °C); при 298 К температурный коэффициент линейного расширения 5,6·10–5 К–1, теплопроводность 85 Вт/(м·К), удельное электрическое сопротивление 9,4·10–8 Ом·м. Литий парамагнитен.
Литий – мягкий и пластичный металл, хорошо обрабатывается прессованием и прокаткой, легко протягивается в проволоку, твёрдость по Бринеллю 5 МПа (твёрже других щелочных металлов). Пары́ лития окрашивают пламя в тёмно-красный цвет.
Многие химические реакции лития протекают менее энергично, чем у других щелочных металлов. С сухим воздухом литий практически не реагирует при комнатной температуре, окисляется только при нагревании. Во влажном воздухе образуется преим. Li3N, при влажности воздуха более 80 % – LiOH и Li2CO3. С сухим O2 при комнатной температуре не реагирует, при нагревании горит голубым пламенем с образованием Li2O (пероксид Li2O2 получают только косвенным путём). С водой реагирует менее энергично, чем другие щелочные металлы, при этом образуется гидроксид LiOH и выделяется H2. Расплав лития при контакте с водой взрывается. Разбавленные минеральные кислоты энергично растворяют литий. В жидком аммиаке растворяется, образуя синий раствор. Литий непосредственно соединяется с F2, Cl2, Br2, при нагревании также и с I2, образуя галогениды (важнейший – хлорид лития LiCl). При нагревании (500 °С) взаимодействует с H2, образуя лития гидрид LiH, с серой – сульфид Li2S. С азотом литий медленно реагирует при комнатной температуре, энергично – при 250 °С с образованием нитрида Li3N. С фосфором литий непосредственно не взаимодействует, в специальных условиях могут быть получены фосфиды Li3P, LiP, Li2P2. Нагревание лития с углеродом приводит к образованию карбида Li2C2. Бинарные соединения лития – Li2O, LiH, Li3N, Li2C2, LiCl и др. и LiOH очень реакционноспособны; при нагревании или плавлении они разрушают многие металлы, фарфор, кварц и др. Литий легко сплавляется со многими металлами (кроме Fe и Ni), образуя твёрдые растворы (с Mg, Zn, Al) или интерметаллиды (с Ag, Hg, Mg, Al и др.). Литий образует многочисленные литийорганические соединения, что определяет его важную роль в органическом синтезе.
Мелкая крошка лития вызывает ожоги влажной кожи и глаз. Загоревшийся литий засыпают NaCl или содой. Хранят литий в герметически закрытых жестяных коробках под слоем пастообразной массы из парафина и минеральные масла.
Наиболее важные соединения лития: лития карбонат Li2CO3 (бесцветные кристаллы с плотностью 2110 кг/м3 и tпл 732 °С, плохо растворимые в воде; используют для получения других соединений лития, а также в производстве ситаллов, керамики, электроизоляционного фарфора, эмалей, глазурей, в пиротехнике, в чёрной металлургии, в качестве добавки в электролит алюминиевых электролизёров и пр.); лития хлорид LiCl (бесцветные гигроскопичные кристаллы с плотностью 2070 кг/м3 и tпл 610 °С, растворимые в воде и во многих органических растворителях; используют как высаливающий и дегидратирующий агент, в промышленности – для получения металлического лития электролизом, для кондиционирования воздуха, в производстве флюсов для плавки металлов и пр.); лития фторид LiF (бесцветные кристаллы с плотностью 2600 кг/м3 и tпл 849 °С; используют как материал термолюминесцентных дозиметров, как оптический материал, компонент электролитов, эмалей, глазурей и пр.); лития гидроксид LiOH (бесцветные кристаллы с плотностью 1440 кг/м3 и tпл 473 °С, менее растворимы в воде, чем гидроксиды других щелочных металлов; используют как добавки к электролиту щелочных аккумуляторов, в качестве реагента для получения, например, олеатов, стеаратов и пальмитатов – компонентов консистентных смазок для авиации и военной техники с рабочим интервалом от –50 до +150 °С, как поглотитель CO2 на подводных лодках, самолётах и космических кораблях); лития ниобат (метаниобат лития) LiNbO3 (бесцветные кристаллы с плотностью 4628 кг/м3 и tпл 1260 °С; монокристаллы LiNbO3 выращивают по методу Чохральского и используют в качестве преобразователей энергии и звукопроводов, элементов модуляторов и другого в электрооптике, модуляторов лазерного излучения, пироэлектрических приёмников лучистой энергии и др.).
Получение
Соединения лития получают в результате гидрометаллургической переработки концентратов – продуктов обогащения литиевых руд. Основной промышленный минерал лития – сподумен – перерабатывают по известковому, сульфатному, сернокислотному и щёлочно-солевому методам. По известковому методу сподумен разлагается известняком при 1150–1200 °С:
Li2O⋅Al2O3⋅4SiO2+8CaCO3=Li2O⋅Al2O3+4(2CaO⋅SiO2)+8CO2.Li₂O· Al₂O₃· 4SiO₂ + 8CaCO_3= Li₂O· Al₂O₃ +4(2CaO·SiO₂) +8CO₂. Спек выщелачивают водой в присутствии избытка извести, при этом алюминат лития Li2O·Al2O3 разлагается: Li2O⋅Al2O3+Ca(OH)2=2LiOH+CaO⋅Al2O3.Li₂O·Al₂O₃ + Ca(OH)₂=2LiOH +CaO·Al₂O₃.По сульфатному методу сподумен (и другие алюмосиликаты) спекают с K2SO4 (при 1050–1100 °С): Li2O⋅Al2O3⋅4SiO2+K2SO4=Li2SO4+K2O⋅Al2O3⋅4SiO2,Li₂O· Al₂O₃· 4SiO₂ + K₂SO₄= Li₂SO₄ + K₂O· Al₂O₃· 4SiO₂,сульфат лития растворяют в воде и из раствора содой осаждают карбонат лития: Li2SO4+Na2CO3=Li2CO3+Na2SO4.Li₂SO₄ +Na₂CO₃=Li₂CO₃ +Na₂SO₄.По сернокислотному способу получают раствор сульфата лития, затем карбонат; реакция применима только для β-модификации сподумена. При щёлочно-солевом методе после разложения сподумена смесью CaCO3 и CaCl2 в раствор переходит LiCl.
Металлический литий получают электролизом расплавленной смеси LiCl и KCl при 400–460 °С с последующей очисткой от примесей (Na, K, Mg, Ca, Al, Fe) вакуумной дистилляцией, ректификацией или зонной плавкой. Металлический литий получают также вакуум-термическим восстановлением алюмината лития (алюминием при температуре 1150–1200 °С и давлении 15–66 Па), Li2O (кремнием или алюминием в присутствии CaO при температуре 950–1000 °С и давлении 0,1 Па), сподумена (ферросилицием в присутствии CaCO3 при температуре 1050–1150 °С и давлении 1,3–4,4 Па). Объём мирового производства лития около 7·106 т/год.
Применение
Важнейшая область применения лития – ядерная энергетика. Изотоп 6Li – единственный промышленный источник для производства трития. Жидкий литий используют в качестве теплоносителя в урановых реакторах, расплавленный 7LiF – как растворитель U и Th в гомогенных реакторах. Дейтерид 6Li – основа термоядерного оружия. Литий применяют в производстве анодов для химических источников тока на основе неводных и твёрдых электролитов; как компонент сплавов с Mg и Al, антифрикционных сплавов (баббитов), сплавов с Si для изготовления катодов в электровакуумных приборах; для раскисления, дегазации, рафинирования Cu, медных, цинковых и никелевых сплавов; как катализатор полимеризации (например, изопрена), ацетилирования и др. Соединения лития (например, карбонат) применяются для лечения психических заболеваний.
Дата публикации: 1 августа 2022 г. в 12:05 (GMT+3)