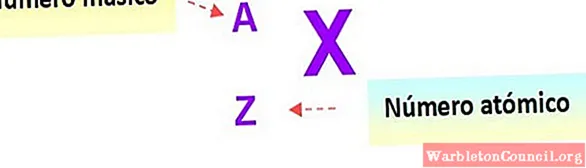Характеристика азота
Положение в ПСХЭ
Азот (N) располагается во 2 периоде, в V группе, главной подгруппе, имеет порядковый номер 7.
Атомные числа
A (массовое число) = 14
P (число протонов) = 7
N (число нейтронов) = A — Z = 14 — 7 = 7
ē (число электронов) = 7
Электронное строение атома
N
+7
2
5
7N 1s2 2s2 2p3
Валентные электроны
| 7N | ↑↓ | ↑ | ↑ | ↑ | ||
| 2s | 2p |
Степени окисления
минимальная: -3
максимальная: +5
Свойства простого вещества
Азот – p-элемент, неметалл.
Высший оксид
N2O5 – оксид азота (V).
Проявляет кислотные свойства:
N2O5 + 2NaOH ⟶ 2NaNO3 + H2O
Высший гидроксид
HNO3 – азотная кислота.
Проявляет кислотные свойства:
HNO3 + NaOH ⟶ NaNO3 + H2O
Водородное соединение
NH3
Химия
Опубликовано 28/06/2020
Задание по химии:
Каково массовое число ядра атома азота 14(7)N? Какова масса ядра в а.е.м (с точностью до целых чисел)?
Вот правильное решение:
Массовое число ядра атома азота 14 (7) N равна 14. Масса ядра так же равна 14 а.е.м.
Поделитесь мнением
Ваш электронный адрес не будет опубликован, комментарий появится после модерации.
Сохраните мое имя и адрес электронной почты в этом браузере, для последующих комментариев.
Привет всем! Нужен ваш совет, как отвечать…
Изобразите силы, действующие на тело, когда оно плавает на поверхности жидкости. (Подробнее…)
ГДЗФизикаПерышкин А.В.Школа7 класс
Содержание
- Примеры массовых чисел
- Водород
- Кислород
- Углерод
- Уран
- Как получить массовое число?
- Обозначения для атомов
- Изотопы
- Изотопы углерода
- Таблица природных изотопов углерода
- Примеры работы
- — Пример 1
- Ответить
- — Пример 2
- Ответить
- Ссылки
В массовое число Массовое число атома — это сумма количества протонов и количества нейтронов в ядре. Эти частицы взаимозаменяемо обозначаются именем нуклоны, поэтому массовое число представляет их количество.
Пусть N — количество присутствующих нейтронов, а Z — количество протонов, если мы назовем A массовым числом, тогда:
А = N + Z
Примеры массовых чисел
Вот несколько примеров массовых чисел для хорошо известных элементов:
Водород
Самый стабильный и многочисленный атом водорода также самый простой: 1 протон и один электрон. Поскольку ядро водорода не имеет нейтронов, верно, что A = Z = 1.
Кислород
В ядре кислорода 8 нейтронов и 8 протонов, поэтому A = 16.
Углерод
Жизнь на Земле основана на химии углерода, легкого атома с 6 протонами в ядре плюс 6 нейтронов, поэтому A = 6 + 6 = 12.
Уран
Этот элемент, намного тяжелее предыдущих, хорошо известен своими радиоактивными свойствами. В ядре урана 92 протона и 146 нейтронов. Тогда его массовое число A = 92 + 146 = 238.
Как получить массовое число?
Как упоминалось ранее, массовое число A элемента всегда соответствует сумме числа протонов и числа нейтронов, содержащихся в его ядре. Это тоже целое число, но … есть ли какое-нибудь правило относительно соотношения между двумя величинами?
Посмотрим: все перечисленные элементы легкие, кроме урана. Атом водорода, как мы уже сказали, самый простой. В нем нет нейтронов, по крайней мере, в его наиболее распространенной версии, а в кислороде и углероде есть равное количество протонов и нейтронов.
То же самое происходит и с другими легкими элементами, такими как азот, еще один очень важный для жизни газ, который имеет 7 протонов и 7 нейтронов. Однако по мере того, как ядро становится более сложным, а атомы становятся тяжелее, количество нейтронов увеличивается с другой скоростью.
В отличие от легких элементов, уран с 92 протонами имеет примерно в 1 ½ раза больше нейтронов: 1 ½ x 92 = 1,5 x 92 = 138.
Как видите, это довольно близко к 146 — количеству нейтронов, которое он имеет.
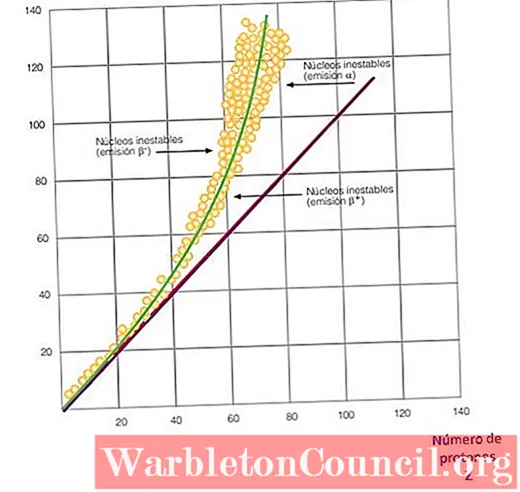
Все это становится очевидным на кривой на рисунке 2. Это график зависимости N от Z, известный каккривая ядерной устойчивости. Там вы можете увидеть, как легкие атомы имеют такое же количество протонов, что и нейтроны, и как с Z = 20 количество нейтронов увеличивается.
Таким образом, большой атом становится более стабильным, так как избыток нейтронов уменьшает электростатическое отталкивание между протонами.
Обозначения для атомов
Очень полезная запись, которая быстро описывает тип атома, следующая: символ элемента и соответствующие атомные и массовые числа записываются, как показано ниже на этой диаграмме:
В этих обозначениях атомы в предыдущих примерах будут:
Иногда используются другие более удобные обозначения, в которых для обозначения атома используются только символ элемента и массовое число, без атомного номера. Таким образом, 12 6C просто записывается как углерод-12, 16 8Или кислород — 16 и так далее для любого элемента.
Изотопы
Число протонов в ядре определяет природу элемента. Например, каждый атом, ядро которого содержит 29 протонов, является атомом меди, несмотря ни на что.
Предположим, атом меди по какой-то причине теряет электрон, это все равно медь. Однако теперь это ионизированный атом.
Атомному ядру сложнее получить или потерять протон, но в природе это может происходить. Например, внутри звезд более тяжелые элементы непрерывно образуются из легких элементов, поскольку звездное ядро ведет себя как термоядерный реактор.
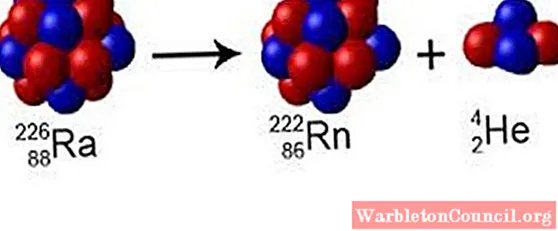
И прямо здесь, на Земле, есть феномен радиоактивный распад, в котором некоторые нестабильные атомы изгоняют нуклоны и излучают энергию, превращаясь в другие элементы.
Наконец, существует вероятность того, что атом определенного элемента имеет другое массовое число, в данном случае это изотоп.
Хороший пример — всем известный углерод-14 или радиоуглерод, который используется для датировки археологических объектов и как биохимический индикатор. Это тот же углерод с идентичными химическими свойствами, но с двумя дополнительными нейтронами.
Углерод-14 менее распространен, чем углерод-12, стабильный изотоп, а также радиоактивен. Это означает, что со временем он распадается, выделяя энергию и частицы, пока не станет стабильным элементом, которым в его случае является азот.
Изотопы углерода
Углерод существует в природе как смесь нескольких изотопов, наиболее распространенными из которых являются уже упомянутые 126С или углерод-12. А кроме углерода-14 есть 136C с дополнительным нейтроном.
Это обычное явление в природе, например, известно 10 стабильных изотопов олова. С другой стороны, из бериллия и натрия известен только один изотоп.
Каждый изотоп, природный или искусственный, имеет разную скорость превращения. Таким же образом можно создавать искусственные изотопы в лаборатории, которые, как правило, нестабильны и радиоактивно распадаются за очень короткий период долей секунды, в то время как для других требуется гораздо больше времени, равное возрасту Земли или больше.
Таблица природных изотопов углерода
| Изотопы углерода | Атомный номер Z | Массовое число A | Изобилие% |
|---|---|---|---|
| 12 6 C | 6 | 12 | 98.89 |
| 13 6 C | 6 | 13 | 1.11 |
| 14 6 C | 6 | 14 | Следы |
Примеры работы
— Пример 1
В чем разница между137 N и 147 N?
Ответить
Оба являются атомами азота, так как их атомный номер равен 7. Однако один из изотопов с A = 13 имеет на один нейтрон меньше, а 147 N — самый распространенный изотоп.
— Пример 2
Сколько нейтронов находится в ядре атома ртути, обозначаемого как 20180 Hg?
Ответить
Поскольку A = 201 и Z = 80, а также зная, что:
А = Z + N
N = А — Я = 201 — 80 = 121
И делается вывод, что в атоме ртути 121 нейтрон.
Ссылки
- Коннор, Н. Что такое нуклон — Структура атомного ядра — Определение. Получено с: period-table.org.
- Найт, р. 2017. Физика для ученых и инженерии: стратегический подход. Пирсон.
- Сирс, Земанский. 2016. Университетская физика с современной физикой. 14-го. Ред. Том 2.
- Типпенс, П. 2011. Физика: концепции и приложения. 7-е издание. Макгроу Хилл.
- Википедия. Массовое число. Получено с: en.wikipedia.org.
Классы
Все классы
- 7
- 8
- 9
Предметы
Все предметы
- Русский язык
- Английский язык
- Алгебра
- Геометрия
- Физика
войтирегистрация
- Ответкин
- Решебники
- 7 класс
- Физика
- Пёрышкин (сборник задач)
- Номер задания №1849
Назад к содержанию
ГДЗ (готовое домашние задание из решебника) на Номер задания №1849 по учебнику Физика. 7-9 классы. Сборник задач к учебникам / А.В. Перышкин — 9ое издание. Экзамен, 2013-2017г.
Условие
Каково массовое число ядра атома азота 14(7)N? Какова масса ядра в а.е.м (с точностью до целых чисел)?
Решение 1
Другие задачи из этого учебника
Популярные решебники

Издатель: А. В. Перышкин, Дрофа, 2013-2019г

Издатель: А. В. Перышкин, Экзамен, 2013-2017г.
Сообщить об ошибке
Выберите тип ошибки:
Решено неверно
Опечатка
Плохое качество картинки
Опишите подробнее
в каком месте ошибка
Ваше сообщение отправлено
и скоро будет рассмотрено
ОК, СПАСИБО