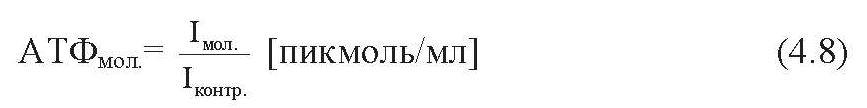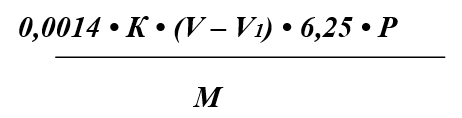Цель:
овладение методами количественного
определения массовой доли белка и
проведение сравнительного анализа
полученных данных.
Задание:
1.
Определить содержание массовой доли
белка в представленных образцах сырья
и пищевых продуктов различными
количественными методами.
2. Провести
математическую обработку полученных
данных.
3.
Провести сравнительный анализ полученных
данных, представленных в виде сводной
таблицы.
4. Сделать заключение
о проделанной работе.
Теоретические сведения
Среди азотистых веществ, входящих в
состав пищевых продуктов, важнейшая
роль принадлежит белкам. Их основное
значение заключается в незаменимости
другими компонентами пищи. Белки
составляют основу процессов
жизнедеятельности организма.
Необходимость их постоянного обновления
лежит в основе обмена веществ.
Белки в организме выполняют структурную
(построение тканей и клеточных
компонентов) и функциональную (ферменты,
гормоны, дыхательные пигменты и др.)
роль.
Дефицит белка в пищевом рационе повышает
восприимчивость организма к
инфекционным заболеваниям, нарушает
процессы кроветворения, обмен липидов,
витаминов и др. У детей при белковой
недостаточности замедляются рост и
умственное развитие.
Длительный избыток белка в питании
также отрицательно сказывается на
жизнедеятельности организма, вызывая
перевозбудимость нервной системы,
нарушение обменных процессов, перегрузку
печени и почек.
В ежедневном рационе взрослого человека
белки должны составлять около 14% общей
калорийности, сочетаясь в определенном
соотношении с другими пищевыми веществами.
Известно, что растительные белки
усваиваются организмом не полностью
по сравнению с животными. Так, белки
молока и яиц усваиваются на 96%, белки
рыбы и мяса — на 95%, белки хлеба из муки
пшеничной I и II
сортов — на 85%, белки картофеля, хлеба
из обойной муки, бобовых— на 70%. Учитывая,
что растительные белки менее полноценны
по составу незаменимых аминокислот,
чем животные, потребление определенного
количества животных белков совершенно
необходимо. Для взрослого человека доля
животных белков в среднем должна
составлять около 55% общего количества
белка в рационе.
Массовую долю белка в пищевых продуктах
определяют по количеству общего азота
методом Кьельдаля. С развитием фото- и
спектрофотометрии были разработаны
методы количественного определения
белка, основанные на его способности
давать окрашенные соединения с .некоторыми
реагентами. Среди них следует отметить
метод Лоури, биуретовый метод. Находят
применение также физико-химические
методы, в основу которых ‘положены
специфические свойства белка: образование
различной степени помутнения в зависимости
от концентрации белка в растворе
сульфосалициловой кислоты (нефелометрический
метод), способность белка адсорбировать
некоторые красители и другие
свойства белка.
Все перечисленные методы могут быть
отнесены к ускоренным. При относительно
небольших затратах времени они
характеризуются достаточно высокой
точностью и простотой определения.
Порядок выполнения работы
Порядок
определения массовой доли белка по
методу Къельдаля (арбитражный) способом
отгона и титрования
Сущность
метода:
Предназначен
для определения содержания белка в
блюде или рационе с целью контроля его
энергетической ценности. Сущность
метода состоит в разрушении органического
вещества навески концентрированной
серной кислотой в присутствии катализаторов
(сульфата меди (II) и сульфата калия).
Выделившийся в результате реакции азот
улавливается серной кислотой, и образуется
сульфат аммония. При добавлении едкого
натра выделяется аммиак, который отгоняют
в раствор серной кислоты и оттитровывают.
Для пересчета на содержание белка
количество азота, содержащегося в
навеске, умножают на соответствующий
коэффициент. Коэффициенты пересчета
выведены на основании процентного
содержания азота в отдельных видах
продуктов.
Проведение
испытаний
Приготовление
минерализата: Навеску в количестве
0,3-0,5гр. взвешивают с точностью до
0,0001гр., затем количественно переносят
её в колбу Къельдаля, доливают 10 см3
концентрированной H2SO4
(ρ=1,84гр/см3)
и в качестве катализатора добавляют
катализатор, состоящий из смеси сульфата
меди (II) и сульфата калия. Колбу Къельдадя
закрывают воронкой и ставят на систему
для минерализации (рис. 8).
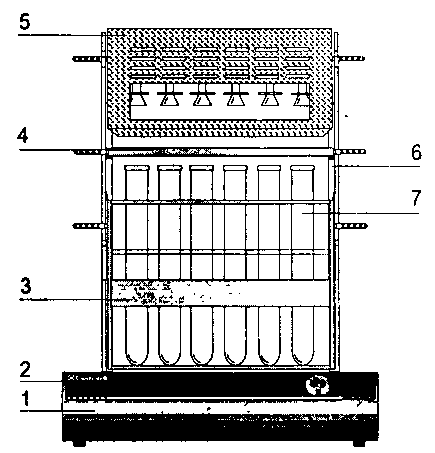
Рисунок 8 — Установки для
минерализации TURBOTHERM
1 — Нагревательный блок
2 — Панель управления
3 — Вставной штатив для реакционных
сосудов
4 — Каплеулавливающий поддон
5 — Вытяжная система
6 — Двухъярусная стойка
7 – Колбы Къельдаля для
минерализации
Нагревание
продолжают до тех пор, пока жидкость в
колбе не станет однородной. Внутренние
стенки колбы должны быть чистыми, что
достигается осторожным взбалтыванием
содержимого колбы для смывания со стенок
темных, обугленных частиц. По окончании
сжигания содержимое колбы охлаждают.
Отгон.
После минерализации количественно
переносят минерализат в мерную колбу
на 100см3,
охлаждают, доводят содержимое колбы до
метки дистиллированной безаммиачной
водой. Отгон минерализата производят
паром (до 150см3)
на системе «Vopodest»
(рис. 10). Для этого в реактор наливают
20см3
минерализата, в приемник — 30см3
0,02н H2SO4,
добавляют 2-3капли смешенного индикатора
и запускают прибор. Окончание отгона
можно проверить по реакции дистиллята
по лакмусовой бумаге — реакция должна
быть нейтральной.
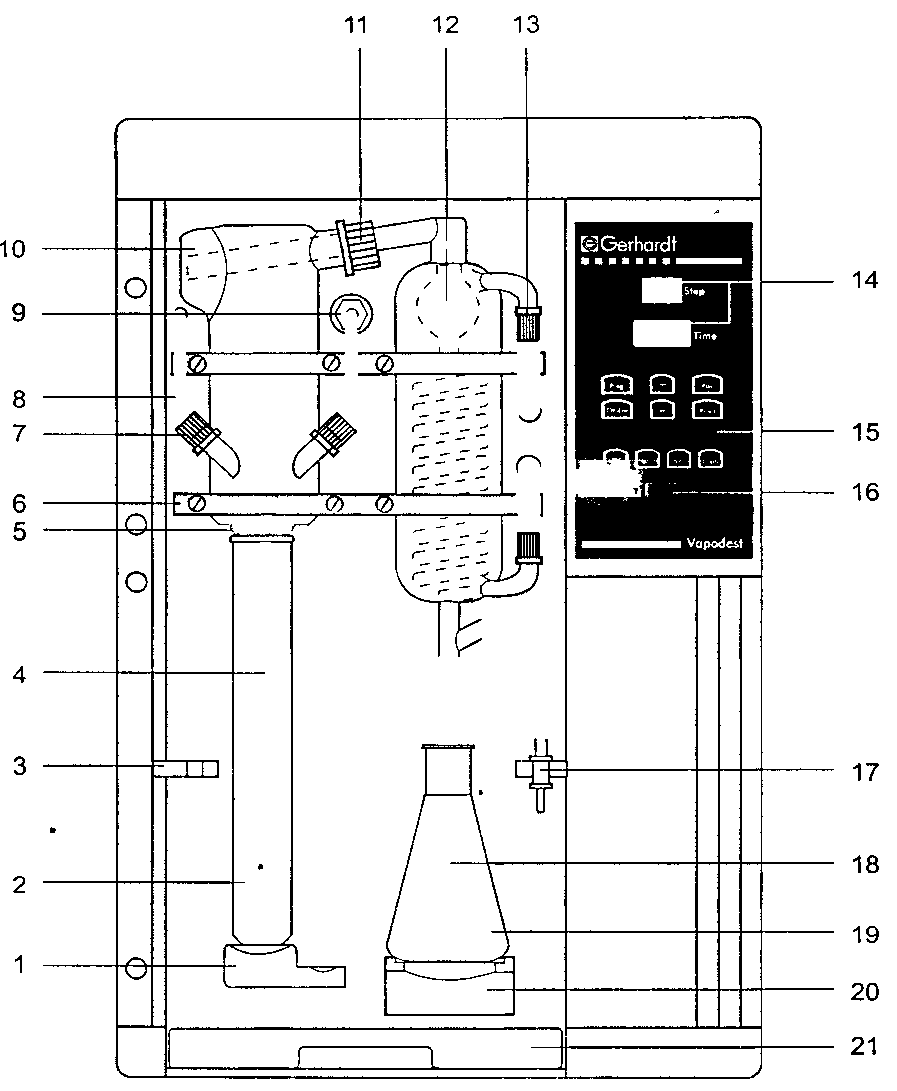
Рисунок 10 — Установка для
отгонки Vapodest-30
1 — Прижимное устройство для
установки колбы или пробирки; 2 — Пробирка
KTG/KMT,
250/100 мл или колба Къельдаля на 500/750 мл с
широким горлом; 3 — Держатель для шланга
входа водяного пара; 4 — Шланг входа
водяного пара, тефлон; 5 — Конический
уплотнитель; 6 — Зажим для стеклоизделий;
7 — Резьбовое соединение деталей Ø 18 мм
с силиконовой прокладкой; 8 — Шланг ввода
раствора NaOH,
тефлон; 9 — Резьбовое соединение шланга
ввода водяного пара с парогенератором;
10 — Каплеулавливающая насадка, стекло;
11 — Резьбовое соединение деталей Ø 32мм
с силиконовой прокладкой; 12 — Холодильник
для конденсации паров; 13 — Резьбовое
соединение деталей Ø 14мм; 14 — Дисплей;
15 — Клавиатура, химически стойкий пластик;
16 — Сетевой выключатель; 17 — Клапан
вентиляции; 18 — Шланг выхода дистиллята,
8/12 мм, силикон; 19 — Приемная емкость,
обычно коническая колба; 20 — Основание
для установки приемной емкости; 21 —
Поддон для сбора пролитой жидкости
Титрование.
Избыток кислоты оттитровывают 0,02н КОН
до перехода окраски в грязно- зеленый
цвет.
Контрольный
опыт выполняют так же, как прописано
выше, но без навески продукта. В качестве
навески добавляют 10мл. воды.
Расчетная
формула:
,
где
V1
– количество 0,02 КОН, пошедшее на
титрование в контрольном опыте, см3;
V2
– количество 0,02 КОН, пошедшее на
титрование в рабочем опыте, см3;
К
– поправочный коэффициент для 0,02н КОН;
В
– эквивалентное количество искомого
вещества (азота) в гр. или мг., которое
эквивалентно реагирует с 1см3
титруемого раствора (0,02н КОН);
V3
– объем колбы разведения, см3;
V4
– объем вытяжки, взятое на отгон, см3;
m
– масса навески, гр.;
100
– пересчет на 100 гр. продукта
Коэффициент
В рассчитывается по формуле:
(мг/см3)
(гр/см3),
где:
Е
– грамм-эквивалент вещества (азота);
N
– нормальность титруемого раствора
(0,02н КОН)
Для
определения содержания белка в блюде
полученное количество азота в граммах
умножают на соответствующий коэффициент.
В среднем коэффициент пересчета азота
на содержание белка в животных пищевых
продуктах равен 6,25, в растительных
продуктах — 5,5 – 6,0.
О
принятом коэффициенте должно быть
указано в рабочем журнале и в бланке
результатов анализа.
Порядок
определения массовой доли белка по
методу Къельдаля фотометрическим
способом
Сущность
метода:
Метод
основан на минерализации пробы по
Къельдалю и фотометрическом измерении
интенсивности окраски индофенолового
синего, которая пропорциональна
количеству аммиака в минерализате.
Проведение
испытаний
Приготовление
минерализата: Навеску в количестве
0,3-0,5гр. взвешивают с точностью до
0,0001гр., затем количественно переносят
её в колбу Къельдаля, доливают 10 см3
концентрированной H2SO4
(ρ=1,84гр/см3) и в качестве катализатора
добавляют 1,0см3
33% пергидроля. Колбу Къельдаля закрывают
воронкой и ставят на систему для
минерализации (рисунок 2). Пергидроль
добавляют на протяжении всего процесса
минерализации. Минерализация считается
законченной, если раствор в колбе
Къельдаля перестает темнеть при
добавлении пергидроля.
Приготовление
пробы:
В
мерную колбу на 50см3
вносят 2-4см3
минерализата, приливают ¾ объема колбы
безаммиачной дистиллированной воды,
затем 1см3
50% раствора сегнетовой соли и 2см3
реактива Несслера, доливают безаммиачной
дистиллированной водой до метки и через
15 минут фотоколориметрируют при длине
волны 480-490нм.
За
окончательный результат принимают
среднее арифметическое результатов
трех параллельных определений. Расхождение
между параллельными определениями не
должно превышать 0,1% по содержанию азота.
Приготовление
стандартной шкалы:
Шкалы
готовят непосредственно перед
колориметрированием в мерных колбах
на 50см3.
В колбы вносят 0,2,4,6,8,10,12,14см3
стандартного раствора хлористого
аммония, приливают ¾ объема колбы
безаммиачной дистиллированной воды,
затем вносят 1см3
50% раствора сегнетовой соли. Для
предупреждения выпадения в осадок ионов
кальция и магния, взбалтывают колбу.
Далее вносят 2см3
реактивы Несслера, объем колбы доводят
до метки безаммиачной дистиллированной
водой и перемешивают. Окраска развивается
в течение 15 минут. Через 30 мин. определяют
оптическую плотность растворов на
спектрофотометре при длине волны
480-490нм или фотоэлектроколориметре с
синим светофильтром. Стабильность
окраски растворов сохраняется в течение
одного часа. Температура реактивов при
проведении цветной реакции должна быть
не ниже 20°C.
По
полученным значениям строят график
зависимости концентрации азота (С) от
оптической плотности (Д)
Расчетная
формула:
,
где:
С
– концентрация азота, определенная по
калибровочному графику и соответствующая
оптической плотности, мг/см3;
V1
– объем колбы разведения, см3;
V2
– объем минерализата, взятого на
колориметрирование, см3
m
– навеска пробы, г
100
— пересчет на 100гр. продукта
Для
определения содержания белка в блюде
полученное количество азота в граммах
умножают на соответствующий коэффициент.
В среднем коэффициент пересчета азота
на содержание белка в животных пищевых
продуктах равен 6,25, в растительных
продуктах — 5,5 – 6,0.
О
принятом коэффициенте должно быть
указано в рабочем журнале и в бланке
результатов анализа.
Контрольные вопросы:
-
Каково значение белков для организма
человека? -
Каков принцип определения белка по
методу Къельдаля? -
В чем заключается способ определения
белка по методу Къельдаля способом
отгона и титрования? -
В чем заключается способ определения
белка по методу Къельдаля фотометрическим
способом? -
Каковы достоинства и недостатки способа
определения белка по методу Къельдаля?
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Текущая страница: 3 (всего у книги 6 страниц) [доступный отрывок для чтения: 1 страниц]
4.4. Определение массовой доли белков 44
ГОСТ 23327-98 Молоко и молочные продукты. Метод измерения массовой доли общего азота по Кьельдалю и определение массовой доли белка. ГОСТ 25179-90 «Молоко. Методы определения белка»
[Закрыть]
Белки – высокомолекулярные органические соединения, построенные из аминокислот. К основным белкам молока относятся казеин, глобулин и альбумин. Содержание белков в коровьем молоке колеблется от 2,8 до 3,8 %, в среднем, оно составляет 3,2 %, в том числе казеина около 82 %, на долю сывороточных белков приходится 15-22 % от общего количества белков молока. Молочные белки имеют важное пищевое и технологическое значение, от количественного содержания белков зависит выход сыра, творога и других белковых продуктов. Для контроля содержания белков в молоке применяют следующие методы: – метод Кьельдаля. Метод основан на сжигании органических компонентов пробы молока в колбе Кьельдаля с серной кислотой. По количеству освобождающегося при этом азота в виде аммиака, определяемого титрованием, вычисляют содержание азотистых веществ.
– колориметрический метод. Метод основан на способности белков молока при рН ниже изоэлектрической точки, связывать кислые красители (амидо черный) вследствие образования нерастворимого комплекса. При этом интенсивность окраски раствора уменьшается обратно пропорционально количеству белка. После удаления осадка измеряют оптическую плотность раствора оставшегося красителя и по эмпирической формуле определяют массовую долю белка в молоке.
– метод формольного титрования. Метод основан на реакции щелочных аминогрупп белка с формалином, при этом образуется метиламиновая кислота и, соответственно, повышается титруемая кислотность молока, по приросту которой определяют массовую долю белка в молоке.
– рефрактометрический. Метод основан на установлении разности показателя преломления луча света, проходящего через молоко и выделенную из него (после осаждения казеина хлористым кальцием) сыворотку.
– расчетный. При выводе расчетной формулы для определения белка в молоке (Бм) исходили из постоянства соотношения между составными частями молока. Белок: лактоза: зола = 9: 13: 2.
Определение массовой доли белков в молоке колориметрическим методом
Методика может быть реализована на универсальных фотоколориметрах типа КФК (2М, 3М, 5М), СФ-16 со светофильтрами для выделения спектральной области 590-600 нм, а также приборах «Про-Милк МК-2» фирмы Foss-Electric (Дания) и «Про-о-Мат-Ш» фирмы Funke-Gerber (Германия).
Приборы и реактивы. Весы лабораторные, рН-метр лабораторный, центрифуга молочная с частотой вращения 1000 об/мин., баня водяная с температурой 60-80 °C, термометр ртутный, кюветы кварцевые рабочей длины 10 мм, стаканчики химические стеклянные вместимостью 50 и 100 см3, пробирки стеклянные, фильтровальная бумага или фильтры бумажные (розовая лента), пипетки вместимостью 1, 2 и 20 см3, колбы мерные вместимостью 200 и 2000 см3, колбы химические вместимостью 500 и 750 см3, раствор сине-черного красителя в цитратной буферной смеси (рН 2,3).
Приготовление реактивов. Реактив 1 (буферный раствор). Взвешивают 31,7 г лимонной кислоты и 8,4 г (12-водного) или 3,4 г безводного ортофосфата натрия. Реактивы помещают в колбу и добавляют в нее 400 см3 дистиллированной воды. Содержимое нагревают до температуры около 70 °C, перемешивают до полного растворения и охлаждают до 20оС.
Реактив 2 (раствор красителя). Навеску 4,6 г красителя «амидо черный 10 Б» помещают в колбу и добавляют в нее 200 см3 воды, нагревают до 70 °C и перемешивают до растворения красителя. Раствор отфильтровывают через бумажный фильтр в мерную колбу вместимостью 2000 см3. Фильтр промывают водой до удаления следов красителя. Затем в эту колбу переносят реактив 1. Содержимое колбы охлаждают и доливают водой до метки, закрывают резиновой пробкой и перемешивают содержимое путем многократного переворачивания колбы. Если рН раствора не соответствует 2,3 ± 0,1, то добавляют, соответственно, концентрированную серную кислоту или гидроксид натрия.
Техника анализа. В стеклянную пробирку пипеткой вносят 1 см3 молока, приливают 20 см3 раствора красителя, закрыв пробирку резиновой пробкой, перемешивают ее содержимое, переворачивая пробирку от 2 до 10 раз, не встряхивая. Пробирку помещают в центрифугу и центрифугируют в течение 20 мин. Затем отбирают пипеткой 1см3 надосадочной жидкости, помещают в мерную колбу вместимостью 50 см3, доливают до метки дистиллированной водой и перемешивают содержимое. Аналогичным способом разбавляют рабочий раствор красителя в 50 раз. Он должен иметь оптическую плотность 0,82 ± 0,02, если она не соответствует данному значению, то добавляют буферный раствор или раствор красителя.
На фотоэлектроколориметре или спектрофотометре в кювете с длиной рабочей грани 10 мм при 590-600 нм измеряют оптическую плотность разбавленного раствора красителя по отношению к разбавленной надосадочной жидкости. Массовую долю белка (%) вычисляют по формуле (34.3):
Б = 7,78 D – 1,34 (4.3)
где D – оптическая плотность;
7,78 и 1,34 – эмпирические коэффициенты.
Определение массовой доли белков методом формольного титрования
Метод применяют для контроля массовой доли белка в молоке кислотностью не более 22°Т. Консервирование проб молока не допускается.
Приборы и реактивы. Пипетки вместимостью 20 и 50 см3, пипетки градуированные вместимостью 1 и 5 см3, стаканы химические или колбы вместимостью 150-200 см3, бюретка для титрования вместимостью 25 см3. Гидроксид натрия 0,1 н и 40 %-ный растворы, приготовленные на прокипяченной дистиллированной воде, 2 %-ный спиртовой раствор фенолфталеина, формалин технический 37-40 %-ный (нейтрализованный), 2,5 %-ный раствор сульфата кобальта, вода дистиллированная, свободная от углекислого газа.
Нейтрализация формалина. К 50 см3 формалина добавляют 3-4 капли раствора фенолфталеина и затем по каплям приливают сначала 40 %-ный, а в завершение 0,1 н раствор гидроксида натрия до появления слабо-розового окрашивания.
Приготовление эталона окраски. В колбочку для титрования или химический стакан отмеривают 20 мл молока и добавляют 0,5 мл 2,5 %-ного сульфата кобальта.
Техника анализа. В химический стакан или колбу для титрования пипеткой отмеривают 20 см3 молока и добавляют 0,25 см3 (10-12 капель) раствора фенолфталеина, а затем оттитровывают 0,1 н раствором гидроксида натрия из бюретки до появления слабо-розовой окраски, соответствующей контрольному эталону. Затем вносят 4 см3 нейтрализованного формалина, перемешивают круговыми движениями и через 1 мин вторично титруют до такой же окраски, как и при первом титровании.
Массовая доля (%) общего количества белков в молоке равна количеству 0,1 н раствора щелочи, израсходованного на титрование в присутствии формалина, умноженному на коэффициент 0,959 (4.4):
Б = 0,959 • N (4.4)
где N -количество щелочи, пошедшей на титрование.
Определение массовой доли белков рефрактометрическим методом
Массовую долю белков в молоке данным методом определяют на рефрактометрах типа АМ и ИРФ-464.
Приборы и реактивы. Рефрактометр, водяная баня закрытого типа, электроплита, центрифуга молочная, пипетки вместимостью 5 см3, флаконы для лекарственных средств типа ФО вместимостью 10 см3, 4 %-ный раствор кальция хлористого, вода дистиллированная.
Проведение анализа. В 3 флакона отмеривают по 5 см3 молока и добавляют по 6 капель раствора хлорида кальция. Флаконы закрывают пробками и перемешивают содержимое. Флаконы помещают в водяную баню так, чтобы уровень воды достигал половины высоты флаконов, закрывают крышкой, доводят до кипения и кипятят не менее 10 мин. Не открывая бани, сливают воду через отверстия в крышке и наливают в баню холодную воду для охлаждения. Флаконы энергично встряхивают и разрушают белковый сгусток. После чего их помещают в центрифугу и центрифугируют не менее 10 мин. Образовавшуюся прозрачную сыворотку отбирают пипеткой и наносят 1-2 капли на измерительную призму рефрактометра. Закрывают измерительную призму осветительной.
Наблюдая в окуляр рефрактометра, специальным корректором убирают окрашенность границы света и тени. Снимают показания оптической плотности сыворотки (Бс) по шкале «Белок» не менее 3 раз и вычисляют среднее арифметическое. Удаляют сыворотку с призмы рефрактометра, промывают водой и вытирают фильтровальной бумагой. Помещают на измерительную призму 2 капли исследуемого молока и также снимают показания (не менее 3 раз) по шкале «Белок» – Бм. Массовую долю белка в молоке Б (%) вычисляют по формуле (4.5):
Б = Бм – Бс (4.5) где Бм и Бс – оптическая плотность молока и выделенной из него безбелковой сыворотки.
Определение массовой доли белков расчетным методом (приблизительно)
Бм = 0,075 Жм + 0,098 А + 0,085 (4.6)
где Жм – массовая доля жира в молоке, %;
А – плотность молока, °А;
0,075, 0,098, 0,085 – эмпирические коэффициенты.
4.5. Рефрактометрический метод определения лактозы в молоке
Данным методом на рефрактометрах типа АМ-2, ИРФ, РЛ или РЛП возможно определение лактозы в молочной сыворотке.
Метод основан на способности безбелковой сыворотки, преломлять проходящий через нее свет в зависимости от концентрации лактозы.
Приборы и реактивы. Рефрактометр типа АМ-2, ИРФ или РЛ-2, водяная баня с навинчивающейся крышкой для флаконов, медицинские флакончики с резиновыми пробками, пипетка вместимостью 5 см3, капельница, вата хирургическая, бумага фильтровальная, стеклянная палочка с опаянным концом, 4 %-ный раствор хлорида кальция, вода дистиллированная.
Подготовка к анализу. Подготовка к анализу заключается в получении безбелковой сыворотки из исследуемого молока. В медицинский флакончик отмеривают 5 см3 молока и добавляют 5 капель хлорида кальция. Флакончик закрывают пробкой и перемешивают. Затем для полного осаждения белков флаконы ставят в кипящую водяную баню (с завинченной крышкой) на 10 мин. После чего воду из бани сливают через отверстия в крышке и флаконы охлаждают под проточной водой. Затем стеклянной трубкой или пипеткой с ватным тампоном в нижней части отбирают немного сыворотки, фильтруя ее через вату.
Техника анализа на рефрактометрах типа АМ-2 или ИРФ. На измерительную призму рефрактометра наносят 1-2 капли прозрачной сыворотки. Закрывают измерительную призму осветительной. Наблюдая в окуляр рефрактометра, специальным корректором убирают расплывчатость и окрашенность на границе света и тени. Снимают показания по шкале «Белок» (Xi) Удаляют сыворотку с призмы рефрактометра, промывают водой и вытирают фильтровальной бумагой.
Затем на призму наносят 1-2 капли дистиллированной воды и также снимают показания по шкале белок (Х2). Массовую долю лактозы (Л) в процентах находят по формуле (4.7):
Л = X1 -Х2; (4.7)
где: Х1 – показание по шкале «Белок» для сыворотки, %;
Х2 – показание по шкале «Белок» для дистиллированной воды, %
Техника анализа на рефрактометре РЛ-2. Рефрактометр РЛ-2 имеет две шкалы: «показатель преломления» в пределах 1,33-1,54 и «содержание сухих веществ по сахарозе» до 95 %. Рефрактометр на «0» устанавливают при 20 °C. Перед работой камеры призм рефрактометра присоединяют штуцерами к ультратермостату и пропускают воду с температурой 17,5 °C в течение 1015 мин. Затем проверяют установку нуля. На нижнюю призму наносят 2 капли дистиллированной воды, закрывают верхней и устанавливают окуляр на резкость видимости по шкале и визирной линии (представляющей собой три штриха). Окуляр перемещают до совмещения визирной линии с границей светотени. Она должна совпадать с нулевым делением шкалы сухих веществ и с делением nD=1,333.
Призмы насухо вытирают и на поверхность нижней призмы наносят 2 капли прозрачной сыворотки. Наблюдая в окуляр, вращением рукоятки устанавливают поле зрения на фокус (ясную видимость), устраняют расплывчатость и радужность окраски границы светотени. Передвижением окуляра добиваются полного совпадения граничной линии с визирным указателем и отсчитывают показатель преломления сыворотки по левой шкале рефрактометра. Затем по таблице (Приложение Г) устанавливают массовую долю молочного сахара.
4.6. Определение механической загрязненности молока 55
ГОСТ 8218-89 «Молоко. Метод определения чистоты»
[Закрыть]
Метод основан на отделении механической примеси из дозированной пробы молока путем процеживания через фильтр и визуального сравнения наличия механической примеси на фильтре с образцом сравнения (эталоном).
Приборы и материалы. Приборы разных конструкций (типа «Рекорд» и др.) с диаметром фильтрующей поверхности 27-30 мм, ватные фильтры лабораторные, фланель (отбеленная).
Техника анализа. На сетку прибора кладут ватный или фланелевый фильтр в виде кружка и закрепляют. Пробу молока объемом 250 см3, подогретую до температуры (35±5)°С, тщательно перемешивают и пропускают через приготовленный фильтр. По окончании фильтрования фильтр помещают на лист пергамента и просушивают на воздухе. В зависимости от количества механической примеси на фильтре молоко подразделяют на три группы (таблица 4.3).
Таблица 4.3 – Определение группы чистоты молока
6 Цвет фильтра должен соответствовать цвету молока в соответствии с требованиями стандарта. При изменении цвета фильтра молоко, независимо от количества имеющейся на фильтре механической примеси, относят к третьей группе чистоты.
4.7. Методы определения микробной обсемененности молока 66
ГОСТ Р 53430-2009 Молоко и продукты переработки молока. Методы микробиологического анализа. ГОСТ Р 52415-2005 «Молоко натуральное коровье – сырье. Люминесцентный метод определения количества мезофильных аэробных и факультативно анаэробных микроорганизмов»
[Закрыть]
Пробы для микробиологических исследований отбирают в стерильную посуду с помощью специальных приспособлений с соблюдением правил асептики. Инвентарь для отбора проб перед использованием стерилизуют фламбированием (протирание ватой, смоченной спиртом, с последующим обжиганием на огне) или в автоклаве. Стерильные колбы с пробами закрывают стерильными пробками, горлышко посуды и пробку обертывают бумагой и обвязывают. Отобранные пробы следует исследовать не позднее 4 ч с момента взятия, при условии хранения или транспортирования при температуре не выше 6 °C.
Определение бактериальной обсемененности молока может быть проведено путем непосредственного посева молока на питательную среду (чашечный метод) или по редуктазной пробе.
Эта проба является косвенным показателем микробного загрязнения сырого молока. В процессе жизнедеятельности бактерии выделяют в окружающую среду наряду с другими окислительно-восстановительными ферментами анаэробные дегидразы, по старой классификации называемые редуктазами. Существует зависимость между количеством мезофильных аэробных и факультативно-анаэробных микроорганизмов (КМАФАнМ) в молоке и содержанием в нем редуктаз, что дает возможность использовать редуктазную пробу как косвенный показатель уровня бактериальной обсемененности сырого молока.
Метод основан на восстановлении резазурина окислительновосстановительными ферментами, выделяемыми в молоко микроорганизмами. По продолжительности изменения окраски резазурина оценивают бактериальную обсемененность сырого молока.
Определение микробной обсемененности молока редуктазными пробами
Приборы и реактивы. Редуктазник или водяная баня с терморегулятором, пробирки диаметром 20 мм и высотой 180 мм, пипетки вместимостью 1 и 20 см3, рабочий раствор резазурина (готовится из основного).
Основной раствор: 100 мг резазурина растворяют в 200 см3 прокипяченной и охлажденной дистиллированной воды. Срок хранения не более 20 сут. при 3-5 °C.
Рабочий раствор готовят из основного разбавлением прокипяченной и охлажденной дистиллированной водой в соотношении 1: 10. Срок хранения не более 7 сут.
Техника анализа. Пробу с резазурином следует проводить не ранее чем через 2 ч после доения. В пробирки наливают по 1 см3 рабочего раствора резазурина и по 10 см3 исследуемого сырого молока, закрывают резиновыми пробками и смешивают путем медленного трехкратного переворачивания пробирок.
Пробирки помещают в редуктазник с температурой воды (37 ±1) °С. Вода в редуктазнике или водяной бане после погружения пробирок с сырым молоком должна доходить до уровня жидкости в пробирке или быть немного выше. Температуру (37 ±1) °С поддерживают в течение всего времени определения. Пробирки с сырым молоком и резазурином на протяжении анализа должны быть защищены от света прямых солнечных лучей (редуктазник должен быть плотно закрыт крышкой).
Время погружения пробирок в редуктазник считают началом анализа. Показания снимают через 1 ч. Появление окрашивания молока в этих пробирках при встряхивании не учитывают.
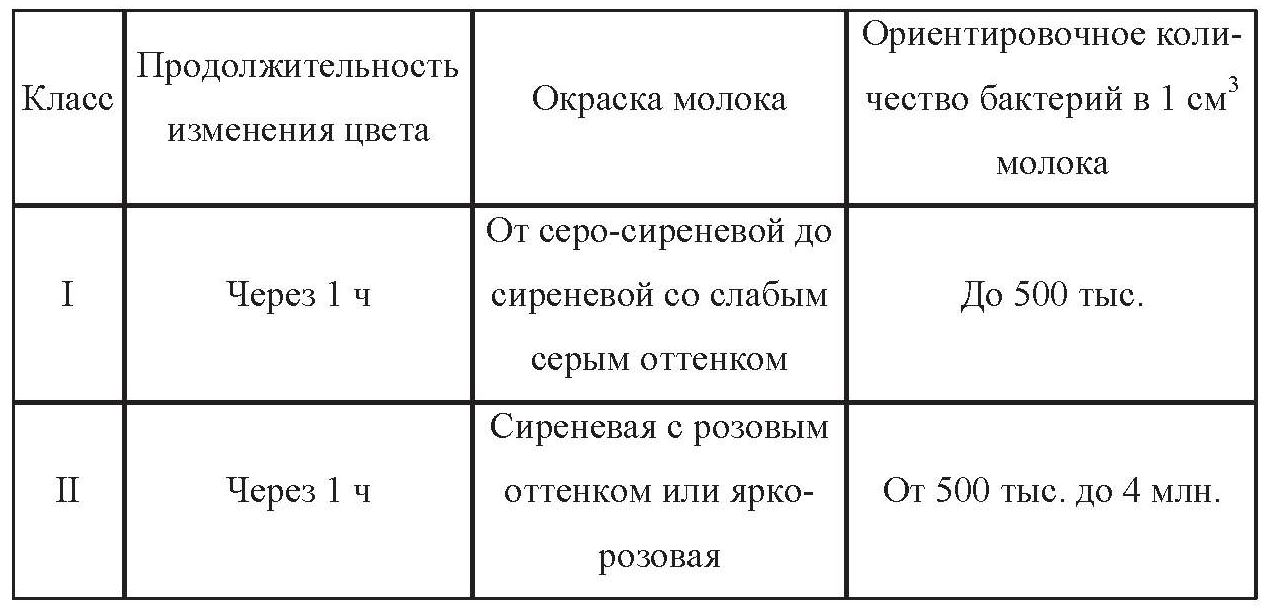
По истечении 1 ч пробирки вынимают из редуктазника, осторожно переворачивают. Пробирки с молоком, имеющим окраску от серо-сиреневой до сиреневой со слабым серым оттенком, оставляют в редуктазнике еще на 30 мин. В зависимости от продолжительности обесцвечивания или изменения цвета молоко относят к одному из классов в соответствии с таблицей 4.4.
Таблица 4.4 – Определение бактериальной обсемененности и класса молока по редуктазной пробе с резазурином
Примечания: 1. Для оценки качества сырого молока при бактериальной обсемененности до 100 тыс. в 1 см3 используют посев на чашки Петри.
2. При бактериальной обсемененности сырого молока до 300 тыс. время выдержки проб составляет 1,5 ч. Окраска сырого молока – от серо-сиреневой до сиреневой со слабым серым оттенком.
3. Цвет сырого молока от бледно-розового до белого через 1 ч выдержки свидетельствует о бактериальной обсемененности свыше 4 млн. жизнеспособных клеток.
Цветовая шкала для определения класса сырого молока по редуктазной пробе с резазурином представлена в приложении Д.
Определение микробной обсемененности молока биолюминесцентным методом
Метод основан на растворении соматических клеток, белка и жира молока АТФ-реагентом; фильтровании полученного образца через бактериальный мембранный фильтр; растворении отфильтрованных микроорганизмов реагентом на основе диметилсульфоксида; расчете концентрации АТФ микроорганизмов в полученном растворе по его биолюминесценции и определении количества микроорганизмов в 1 см3 молока.
Приборы и реактивы: люминометр, обеспечивающий измерение люминесценции в диапазоне длин волн от 400 до 700 нм; люминонометрическая кювета (типа фильтраветы); штатив для фильтравет; шприц медицинский вместимостью 5 см3; наконечник резиновый к медицинскому шприцу; фильтровальная бумага; пипетки автоматические вместимостью 0,02 см3, 0,1 см3 и 1 см3; наконечники к автоматическим пипеткам стерильные; баня водяная, позволяющая поддерживать температуру (45 ± 1)oC. Реагенты: флакон № 1 – АТФ-реагент ЛЮМТЕК, лиофильно высушенный; флакон № 2 – раствор для реконструкции АТФ-реагента; флакон № З – АТФ-контроль, лиофилизованный; флакон № 4 – реагент для разрушения бактериальных клеток, раствор; флакон № 5 – реагент для предобработки молока, лиофилизованный; флакон № 6 – промывочный раствор. Внимание! Реагенты следует хранить в холодильнике при температуре от 0 до 6 °C.
Для получения воспроизводимых результатов анализа молока необходимо соблюдать меры предосторожности, принятые при работе в микробиологической лаборатории, в частности: перед проведением анализа поверхность лабораторного стола обработать 70 % этанолом; использовать автоматические пипетки и стерильные наконечники к ним; для выполнения каждой операции использовать новый стерильный наконечник; после анализа каждого образца молока штативы для фильтравет, фланцевый наконечник шприца, пинцет и автоматические пипетки стерилизовать 70 % этанолом.
Подготовка реагентов к анализу. Во флакон № 1 внести 2 мл раствора из флакона № 2, выдержать 30 мин перед использованием. Полученный раствор АТФ-реагента можно хранить при комнатной температуре в течение рабочего дня, а при 4 °C – в течение 2-3 дней.
Во флакон № 3 внести 1 мл раствора из флакона № 4, перемешать. Полученный раствор АТФ контроля имеет концентрацию АТФ 10 пикомоль/мл. Полученный раствор следует использовать в течение одного рабочего дня.
Проверка АТФ-реагента по АТФ-контролю. Поместить фильтравету с помощью пинцета в кюветное отделение люминометра. Внести в нее 0,02 мл раствора АТФ-контроля из флакона №З и 0,05 мл раствора из флакона № 2, перемешать, добавить 0,05 мл раствора АТФ-реагента из флакона № 1, быстро перемещать и измерить биолюминесцентный сигнал. Повторить измерения еще раз и найти среднее значение биолюминесцентного сигнала для АТФ-контроля (IK0HmpX Если измеренные значения различаются более, чем на 20 %, то необходимо провести третье измерение и усреднить два наиболее близких значения.
Техника анализа. Образец анализируемого молока объемом 50 мл довести до комнатной температуры и тщательно перемешать. Внести 1 мл молока во флакон № 5 с реагентом для предобработки молока и тщательно перемешать. Закрыть флакон, поместить его в водяную баню (45 ± 0,5)оС на 10 мин. Поместить в штатив для фильтравет с помощью пинцета фильтровальную полоску и установить на неё две фильтраветы.
Внести в одну фильтравету 0,2 мл предобработанного молока и продавить его на фильтровальную бумагу, создавая избыточное давление с помощью шприца с резиновым наконечником. Сдвинуть фильтровальную полоску так, чтобы под фильтраветой оказался сухой участок полоски. Внести в ту же фильтравету две капли промывочного раствора из флакона № 6 и продавить его в фильтровальную полоску, создавая избыточное давление с помощью шприца с резиновым наконечником.
Поместить фильтравету с помощью пинцета в кюветное отделение люминометра и внести в нее 0,02 мл раствора из флакона № 4. Добавить через 1-2 мин в ту же фильтравету 0,05 мл раствора из флакона № 2, перемещать, затем добавить 0,05 мл АТФ-реагента из флакона № 1, быстро перемещать и измерить максимальный биолюминесцентный сигнал (IМ0Д).
Повторить операции со второй фильтраветой. Найти среднее значение биолюминесцентного сигнала для образца молока (IМ0Д). Если измеренные значения (I различаются более, чем на 20 %, то необходимо провести третье измерение и усреднить два наиболее близких значения.
Рассчитать концентрацию АТФ в молоке по формуле (4.8):
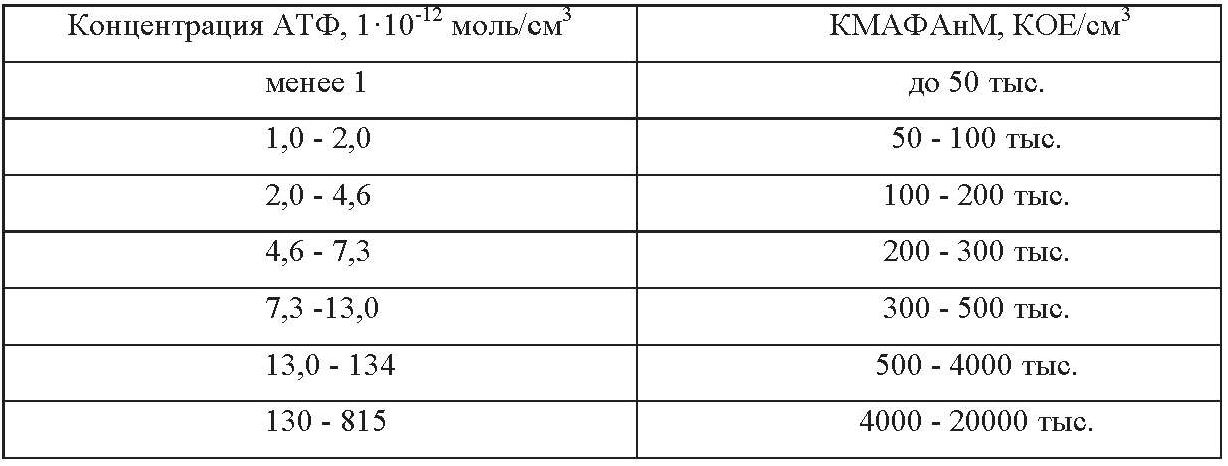
Определить величину КМАФАнМ по таблице 4.5, приведенной ниже.
Таблица 4.5 – Определение КМАФАнМ в сыром молоке биолюминесцентным методом
Определение содержания белков.
Цель работы. Овладеть методами определения содержания белков в пищевых продуктах.
Теоретическое обоснование. Белки — это высокомолекулярные органические соединения,
построенные из аминокислот, соединенных между собой пептидными связями. Роль белков в организме человека
чрезвычайно важна, так как они участвуют в важнейших процессах в организме. Необходимость их постоянного
обновления лежит в основе обмена веществ. Белки в организме выполняют структурную (входят в состав
тканей и клеток) и функциональную (ферменты, гормоны и др.) роль.
Потребление белков должно быть оптимальным, так как и недостаток, и избыток белков в пище вреден для
человека. Потребность взрослого человека составляет в среднем 100 г белка в сутки. По составу белковые
вещества в пище должны быть примерно на 2/3 животного происхождения и на 1/3 — растительного. Белками
богаты мясо, рыба, яйца, молоко, злаковые и бобовые культуры.
Массовую долю белка в пищевых продуктах определяют различными методами:
Наиболее точным является метод Къельдаля, который заключается в окислении (сжигании) органических
веществ концентрированной серной кислотой при кипячении в присутствии катализатора. Содержание белка
определяют по количеству азота. Метод Къельдаля длительный и трудоемкий, требует высокой квалификации
работающего.
В связи с этим широко применяются физико-химические (ускоренные) методы количественного определения
белка, основанные на специфических свойствах белка:
- способности адсорбировать некоторые красители (метод Юди);
- способности пептидных связей белка образовывать комплексное окрашенное соединение с ионами меди в
щелочном растворе (биуретовый); - способности активных групп различных аминогрупп, входящих в состав полипептидной цепи белка, давать
характерные реакции (метод Лоури) и др. Преимущество этих методов в том, что они отличаются достаточно
высокой точностью, простотой и быстротой определения.
Оборудование и техническое оснащение лабораторной работы.
Прибор нагревательный для сжигания навесок; прибор для перегонки с каплеуловителем; колбы Къельдаля;
колбы конические; цилиндры мерные; бюретки вместимостью; капельница. Мука, раствор КОН; сегнетова соль;
дистиллированная вода; раствор СиSО4; СС14; раствор КОН; сульфосалициловая
кислота; мерные колбы, пробки для колб; пипетки; весы; механический встряхиватель; центрифуга;
фотоэлектроколориметр; фотоэлектрический нефелометр.
Содержание и порядок выполнения лабораторной работы:
Метод Къельдаля.
Навеску из гомогенной массы берут с таким расчетом, чтобы в пробе содержалось примерно 20…25 мг
азота. Метод основан на сжигании органических компонентов пробы пищи в присутствии серной кислоты.
Выделяющийся при этом азот улавливается серной кислотой и образуется сульфат аммония. При добавлении
едкого натра выделяется аммиак, который отгоняют в раствор серной кислоты. Выделившийся аммиак
определяют титрованием. Для ускорения сжигания применяют катализатор: смесь серно-кислой меди и
серно-кислого натрия.
Аппаратура, материалы, реактивы. Прибор нагревательный для сжигания навесок; прибор для
перегонки с каплеуловителем; колбы Къельдаля вместимостью 100 см3 с грушевидной стеклянной
пробкой; колбы конические вместимостью 250 см3; цилиндры мерные на 25, 50, 100
см3; бюретки вместимостью 25 см3 с ценой деления 0,1 см3; капельница.
Серная кислота плотностью 1,84 г/см3, 33 %-ный раствор гидроокиси натрия, 0,05 моль/дм3
раствор серной кислоты, смешанный индикатор (к 25 см3 0,1 %-ного раствора метиленового
голубого добавляют 3 см3 0,02 %-ного спиртового раствора метилового красного), лакмусовая
бумага.
Методика анализа. В колбу Къельдаля переносят навеску, которую берут на аналитических весах в
лодочку из алюминиевой фольги или подпергаментной бумаги, добавляют цилиндром 20 см3 серной
кислоты, вливая ее постепенно по стенкам колбы и смывая частицы продукта. В колбу добавляют катализатор
(0,5 г серно-кислой меди и 7,5 г серно-кислого натрия), устанавливают ее в наклонном положении в
вытяжном шкафу в нагревательный прибор, приливают 1 см3 этилового спирта. Колбу закрывают
грушевидной стеклянной пробкой и осторожно нагревают. При образовании пены в первый период окисления
колбу следует снять с нагревательного прибора и дать пене осесть, а затем продолжить нагревание, следя
за тем, чтобы пена не попала в горло колбы. После прекращения пенообразования нагрев усиливают. Степень
нагревания считают достаточной, когда кипящая кислота конденсируется в средней части горлышка колбы
Къельдаля.
Время от времени содержимое колбы перемешивают, смывая частицы со стенок колбы. Нагревание продолжают
до тех пор, пока жидкость не станет бесцветной (слегка голубоватой) и совершенно прозрачной. Содержимое
колбы охлаждают, осторожно по стенке добавляют 50 см3 дистиллированной воды, перемешивают и
охлаждают.
В коническую колбу вместимостью 250 см3 пипеткой отмеривают 40 см3 0,05
моль/дм3 серной кислоты, добавляют четыре капли индикатора, перемешивают и погружают
наконечник, соединенный с холодильником, в кислоту на 1,5…2 см.
В перегонную колбу переносят содержимое колбы Къельдаля, ополаскивая ее несколько раз, 100…150
см3 дистиллированной воды, опускают красную лакмусовую бумажку и соединяют с холодильником с
помощью каплеуловителя. Отмеривают цилиндром 80 см3 33 %-ного раствора гидроокиси натрия и
через делительную воронку вливают его в перегонную колбу. Сразу же после добавления щелочи закрывают
кран делительной воронки для предотвращения потерь аммиака. Содержимое колбы нагревают до кипения, при
этом необходимо избегать пенообразования. Продолжают перегонку до тех пор, пока жидкость не станет
вскипать толчками. Нагрев регулируют таким образом, чтобы продолжительность дистилляции была не менее 20
мин. Перед окончанием перегонки опускают коническую колбу так, чтобы конец наконечника оказался над
поверхностью раствора серной кислоты, и продолжают перегонку еще 1…2 мин. Нагревание прекращают. В
коническую колбу смывают небольшими порциями дистиллированной воды остатки раствора серной кислоты с
внутренней и внешней поверхностей наконечника. Дистиллят титруют 0,1 моль/дм3 раствором
гидроокиси натрия до перехода окраски из фиолетовой в зеленую.
Параллельно проводят контрольный анализ, добавив в колбу Кьельдаля вместо навески 5 см3
дистиллированной воды. Контрольный опыт проводят в каждой серии определений количества белка и при
каждой замене реактивов.
Массу белка (X, г) вычисляют с точностью до третьего знака по формуле:
где:
0,0014 — количество азота, эквивалентное 1 см3 0,05 моль/дм3 раствора серной
кислоты, г;
К — поправочный коэффициент 0,1 моль/дм3 раствора гидроокиси натрия;
V — объем 0,1 моль/дм3 раствора гидроокиси натрия, использованный на титрование 0,05
моль/дм3 раствора серной кислоты в контрольном опыте,
см3; V1 = 6,25 — коэффициент пересчета азота на белок;
Р — масса обеда или рациона, г, в рабочем опыте;
m — масса навески, г.
При исследовании проводят не менее трех определений, по результатам которых рассчитывают среднее
арифметическое. Фактическое содержание белка в обеде (рационе) сравнивают с теоретическим, рассчитанным
по таблицам химического состава пищевых продуктов с учетом потерь при тепловой обработке.
Определение массовой доли белка биуретовым методом.
Специфической реакцией на содержание белка является биуретовая реакция, так как ее дают полипептидные
связи. Она получила свое название от производного мочевины — биурета, который образует в щелочном
растворе медного купороса окрашенное комплексное соединение. Интенсивность окрашивания пропорциональна
содержанию пептидных связей, а следовательно, и концентрации белка в растворе.
Биуретовую реакцию дают все белки, пептоны и полипептиды, начиная с тетрапептидов.
Эта реакция длительное время использовалась как качественная реакция на белок. В дальнейшем она стала
применяться для количественного определения белка в различных объектах. Биуретовый метод применяют в
различных модификациях, различающихся условиями экстрагирования белка, способами внесения биуретового
реактива и техникой колориметрирования.
Ниже приводится биуретовый метод определения массовой доли белка в муке в модификации Дженнингса.
Материалы, реактивы, оборудование. Мука (объект исследования); 10 н. раствор КОН; сегнетова
соль; дистиллированная вода; 4%-ный раствор СиSО4; СС14; 0,05 н. раствор КаОН;
сульфосалициловая кислота; мерные колбы вместимостью 1000 см3‘ мерные цилиндры; конические
колбы вместимостью 250-300 см3; пробки для колб; бюретки; пипетки; мерная колба вместимостью
50 см3; весы; механический встряхиватель; центрифуга; фотоэлектроколориметр;
фотоэлектрический нефелометр.
Приготовление биуретового реактива. Для приготовления реактива берут 15 см3 10 н.
раствора КОН и 25 г сегнетовой соли, взятой с точностью ±0,01 г, и растворяют примерно в 900
см3 дистиллированной воды в мерной колбе вместимостью 1000 см3. К этому раствору
медленно добавляют при постоянном перемешивании 30 см3 4%-го раствора Си8О4,
отмеренных цилиндром. Объем колбы доводят дистиллированной водой до метки.
Методика анализа. Взвешивают около 1,5 г муки с точностью ±0,001 г и помещают в сухую
коническую колбу вместимостью 250-300 см3. Отмеривают под тягой цилиндром с ценой деления 0,1
см3 2 см3 четыреххлористого углерода для извлечения жира из образца и добавляют
пипеткой 100 см3 биуретового реактива. Закрытую пробкой колбу встряхивают на механическом
встряхивателе в течение 60 мин, а затем центрифугируют в течение 10 мин при частоте вращения 4500
мин-1. Прозрачный центрифугат помещают в кюветы фотоэлектроколориметра с толщиной слоя
раствора 5 мм. Измерение оптической плотности производят при длине волны 550 нм.
По величине оптической плотности белковой вытяжки с помощью калибровочной кривой определяют массовую
долю белка в навеске я (мг). Калибровочная кривая представляет собой зависимость между массой белка в
навеске муки (мг) и оптической плотностью раствора.
Рассчитывают массовую долю белка (% к массе сухих веществ).
Построение калибровочной кривой. Для построения калибровочной кривой подбирают
образцы муки с различной массовой долей белка в диапазоне, встречающемся в реальных условиях (от 8 до 20
%). Интервал в содержании белка в используемых образцах должен находиться в пределах не более 1 %.
Количество образцов должно быть не менее 10. С увеличением их числа точность определений возрастает.
Затем приведенным выше биуретовым методом определяют оптическую плотность белковых вытяжек всех
образцов. При построении кривой на оси абсцисс откладывают величины оптической плотности, а на оси
ординат — массовую долю белка в навеске (мг).
Определение массовой доли белка нефелометрическим методом.
Метод основан на измерении интенсивности светового потока, рассеянного твердыми или коллоидными
частицами, находящимися в растворе во взвешенном состоянии. По интенсивности светорассеяния,
определяемой на фотоэлектроколориметре, судят о концентрации исследуемого вещества. В настоящее время
широко применяют фотоэлектрические нефелометры. Растворы высокомолекулярных соединений, например
растворы белков, при определенных условиях в присутствии некоторых химических реагентов способны
опалесцировать. Одним из таких реагентов является сульфосалициловая кислота. Концентрация белка в этом
случае может быть определена по интенсивности опалесценции.
Продукты гидролиза белка — пептоны, аминокислоты и другие азотсодержащие вещества не опалесцируют.
Экспериментальной проверкой установлено, что нефелометрический метод с использованием сульфосалициловой
кислоты отличается быстротой, высокой точностью, простотой и хорошей Корреляцией по сравнению с методом
Кьельдаля.
Методика анализа. Взвешивают 0,5 г исследуемой муки с точностью
±0,001 и помещают в коническую колбу вместимостью 250-300 см3. В колбу из бюретки
добавляют 50 см 0,05 н. раствора гидроксида натрия. Закрытую пробкой колбу встряхивают на механическом
встряхивателе в течение 15 мин. Затем вытяжку центрифугируют в течение 10 мин при частоте вращения 6000
мин-1. Прозрачный центрифугат в количестве 5 см3 пипеткой переносят в мерную колбу
на 50 см3 и содержимое колбы доводят до метки сульфосалициловой кислотой.
Получение правильных результатов при нефелометрическом методе анализа в значительной мере зависит от
методики получения суспензии, в частности от порядка и скорости смешивания растворов. Поэтому после
добавления сульфосалициловой кислоты колбу быстро переворачивают 2-3 раза (не более), раствор
наливают в кювету с толщиной слоя 5 мм и измеряют величину оптической плотности раствора при длине волны
550 нм. Замеры следует проводить сразу после добавления кислоты, так как частицы белка быстро
агрегируют.
Количество белка определяют по калибровочной кривой, построенной для этого метода и представляющей
зависимость между массой белка в навеске (мг) и оптической плотностью раствора. Построение калибровочной
кривой ведут аналогично описанному выше.
Запись в лабораторном журнале проводят точно так же, как в биуретовом методе. По полученным данным
делают заключение о содержании белка в муке.
Требования к отчету по лабораторной работе. Лабораторные записи необходимо вести
аккуратно, поэтапно, в соответствии с порядком выполнения лабораторной работы. Заносить тему,
цель, материалы и оборудование, необходимые в лабораторной работе, основные этапы проведения опытов и
результаты в виде тезисов, либо в табличном или графическом виде, а также с необходимыми рисунками.
Контрольные вопросы:
- Перечислите основные методы определения белка в пищевых продуктах?
- На чем основан метод Къельдаля?
- По какой формуле вычисляют количество белка Х (в г.)?
- Что такое биуретовая реакция определения белков?
- Как проводиться нефелометрический метод определения белков?