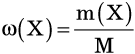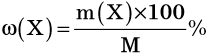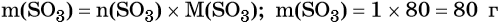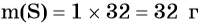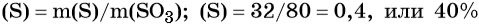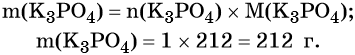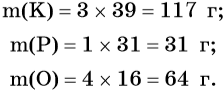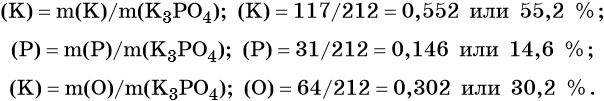Я считаю, что это задание несложное, ведь ребята уже умеют считать относительную молекулярную массу и массовую долю. Относительная молекулярная масса — это сумма относительных атомных масс всех элементов, входящих в состав данного вещества, с учётом индексов (количества атомов одного элемента). Массовая доля — это отношение относительной атомной массы элемента с учётом индекса к относительной молекулярной массе вещества, умноженное на 100%. А теперь считаем и называем вещества:
а) SnO₂ — оксид олова(II).
б) Al₂O₃ — оксид алюминия.
в) СаО — оксид кальция.
д) Р₂О₅ — оксид фосфора(V).
Вот и всё решение. Долго, но не сложно.
Рассчитайте массовые доли элементов в оксидах: а)
S
n
O
2
; б)
A
l
2
O
3
; в) CaO; г)
P
2
O
5
. Назовите все вещества.
reshalka.com
ГДЗ Химия 8 класс класс Габриелян. §14. Проверьте свои знания. Номер №2
Решение а
Дано:
S
n
O
2
Найти:
ω(Sn) − ?
ω(O) − ?
Решение:
Mr(
S
n
O
2
) = 119 + 2 * 16 = 151
ω(Sn) = 119 : 151 * 100% = 78,81%
ω(O) = 32 : 151 * 100% = 21,19%
Ответ:
S
n
O
2
− оксид олова (IV); ω(Sn) = 78,81%; ω(O) = 21,19%
Решение б
Дано:
A
l
2
O
3
Найти:
ω(Al) − ?
ω(O) − ?
Решение:
Mr(
A
l
2
O
3
) = 2 * 27 + 3 * 16 = 102
ω(Al) = 54 : 102 * 100% = 52,9%
ω(O) = 48 : 102 * 100% = 47,1%
Ответ:
A
l
2
O
3
− оксид алюминия; ω(Al) = 52,9%; ω(O) = 47,1%
Решение в
Дано:
CaO
Найти:
ω(Ca) − ?
ω(O) − ?
Решение:
Mr(CaO) = 40 + 16 = 56
ω(Ca) = 40 : 56 * 100% = 71,4%
ω(O) = 16 : 56 * 100% = 28,6%
Ответ: CaO − оксид кальция; ω(Ca) = 71,4%; ω(O) = 28,6%
Решение г
Дано:
P
2
O
5
Найти:
ω(P) − ?
ω(O) − ?
Решение:
Mr(
P
2
O
5
) = 3 * 31 + 5 * 16 = 142
ω(P) = 62 : 142 * 100% = 43,7%
ω(O) = 80 : 142 * 100% = 56,3%
Ответ:
P
2
O
5
− оксид фосфора(V); ω(P) = 43,7%; ω(O) = 56,3%
найди число атомов каждого элемента в молекуле оксида углерода, если массовая доля углерода в нём равна (42,86) %, а массовая доля кислорода — (57,14) %.
1. Примем массу оксида равной (100) г. Масса углерода в такой порции равна (42,86) г, а масса кислорода — (57,14) г.
2. Находим относительные атомные массы элементов в Периодической таблице:
3. Обозначаем число атомов углерода как (x), а число атомов кислорода — (y), и записываем отношение масс:
.
4. Получаем выражение:
5. Находим отношение (x : y):
.
В молекуле оксида углерода на (1) атом углерода приходится (1) атом кислорода.
Вычисление массовой доли химического элемента в веществе
Одним из основных законов химии является закон постоянства состава вещества (рассмотрен ранее в уроке 5).
На основании данного закона проводятся различные практически значимые вычисления, в том числе вычисления массовой доли химического элемента в веществе.
Массовой долей вещества ω(X) называют отношение массы данного вещества в системе к массе всей системы. Для некоего вещества X:
где ω(Х) — массовая доля вещества Х, m(X) — его масса; M — масса всей системы.
Массовая доля является величиной безразмерной. Ее выражают в долях от единицы или в процентах, если долю от единицы умножить на 100:
В качестве системы может выступать как молекула химического соединения, так и смесь, раствор и т. д. Рассмотрим несколько типовых заданий.
Пример 1. Рассчитайте массовую долю серы в оксиде серы (VI).
Решение: Молярная масса оксида серы (VI) M(SO3) = 80 г/моль, атомная масса серы в этом соединении 32 г/ моль. Для расчётов выбираем образец оксида серы количеством вещества 1 моль. Масса этого вещества составит:
Исходя из формулы SO3 можно заключить, что в 1 моль SO3 будет содержаться 1 моль серы, масса которой составит:
Тогда массовая доля серы в оксиде серы (VI) будет равна:
Ответ: 0,4, или 40%.
Пример 2. Рассчитайте массовые доли элементов в фосфате калия K3PO4.
Решение: Молярная масса M(K3PO4) = 212 г/моль. Для расчётов выбираем образец фосфата калия количеством вещества 1 моль. Масса этого вещества составит:
Исходя из формулы K3PO4 можно заключить, что в 1 моль этого соединения будет содержаться 3 моль калия, 1 моль фосфора и 4 моль кислорода, масса которых составит:
Определим массовые доли элементов:
Тренировочные задания
1. Количественное содержание элементов калия, серы и кислорода в сульфите калия равно
1) 20,2; 30,4; 49,4
2) 49,4; 20,2; 30,4
3) 30,4; 49,4; 20,2
4) 49,4; 30,4; 20,2
2. Количественное содержание элементов бария, серы и кислорода в сульфите бария равно
1) 63,1; 22,1; 14,8
2) 63,1; 14,8; 22,1
3) 14,8; 22,1; 63,1
4) 22,1; 63,1; 14,8
3. Количественное содержание элементов кальция, фосфора и кислорода в фосфате кальция равно
1) 20,0; 41,3; 38,7
2) 38,7; 20,0; 41,3
3) 38,7; 41,3; 20,0
4) 41,3; 38,7; 20,0
4. Количественное содержание элементов натрия, фосфора и кислорода в фосфате натрия равно
1) 42,1; 18,9; 39,0
2) 18,9; 39,0; 42,1
3) 39,0; 42,1; 18,9
4) 18,9; 42,1; 39,0
5. Количественное содержание элементов калия, фосфора и кислорода в фосфате калия равно
1) 14,6; 30,2; 55,2
2) 30,2; 55,2; 14,6
3) 55,2; 14,6; 30,2
4) 55,2; 30,2; 14,6
6. Количественное содержание элементов алюминия, серы и кислорода в сульфате алюминия равно
1) 15,8; 56,1; 28,1
2) 28,1; 56,1; 15,8
3) 56,1; 15,8; 28,1
4) 15,8; 28,1; 56,1
7. Количественное содержание элементов кальция, углерода и кислорода в карбонате кальция равно
1) 18,0; 48,0; 40,0
2) 48,0; 40,0 18,0
3) 40,0; 48,0; 12,0
4) 40,0 12,0; 48,0
8. Количественное содержание элементов алюминия, фосфора и кислорода в фосфате алюминия равно
1) 22,1; 25,4; 52,5
2) 22,1; 52,5; 25,4
3) 52,5; 25,4; 22,1
4) 25,4; 52,5; 22,1
9. Количественное содержание элементов кальция, азота и кислорода в нитрате кальция равно
1) 24,4; 17,1; 58,5
2) 17,1; 58,5; 24,4
3) 58,5; 24,4; 17,1
4) 24,4; 58,5; 24,4
10. Количественное содержание элементов магния, азота и кислорода в нитрате магния равно
1) 16,2; 64,9; 18,9
2) 16,2; 18,9; 64,9
3) 18,9; 64,9; 16,2
4) 64,9; 16,2; 18,9
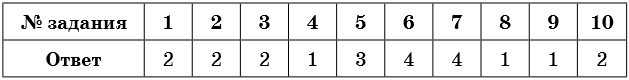
Ответы
ГДЗ (готовое домашние задание из решебника) на § 14 №2, Номера по учебнику Химия. 8 класс. Учебник для общеобразовательных организаций / О.С. Габриелян, И.Г. Остроумов, С.А. Сладков. Просвещение, 2019-2021г.
2. Рассчитайте массовые доли элементов в оксидах: а) SnO2; б) А1203; в) СаО; г) P2O5. Назовите все вещества.
А) M(SnO2)=Ar(Sn)+2Ar(O)=119+2•16= 151
w(Sn)=(Ar(Sn))/M(SnO_2 ) •100%= 119/151•100%=78,81%
w(O)=(2Ar(O))/M(SnO_2 ) •100%= 32/151•100%=21,19%
Б) M(Al2O3)=2Ar(Al)+3Ar(O)=2•27+3•16= 102
w(Al)=(2Ar(Al))/M(Al_2 O_3 ) •100%= 54/102•100%=52,9%
w(O)=(3Ar(O))/M(Al_2 O_3 ) •100%= 48/102•100%=47,1%
В) M(CaO)=Ar(Ca)+Ar(O)=40+16= 56
w(Ca)=(Ar(Ca))/M(CaO) •100%= 40/56•100%=71,4%
w(O)=(Ar(O))/M(CaO) •100%= 16/56•100%=28,6%
Г) M(P2O5)=2Ar(P)+5Ar(O)=3•31+5•16= 142
w(P)=(2Ar(P))/M(P_2 O_5 ) •100%= 62/142•100%=43,7%
w(O)=(5Ar(O))/M(P_2 O_5 ) •100%= 80/142•100%=56,3%