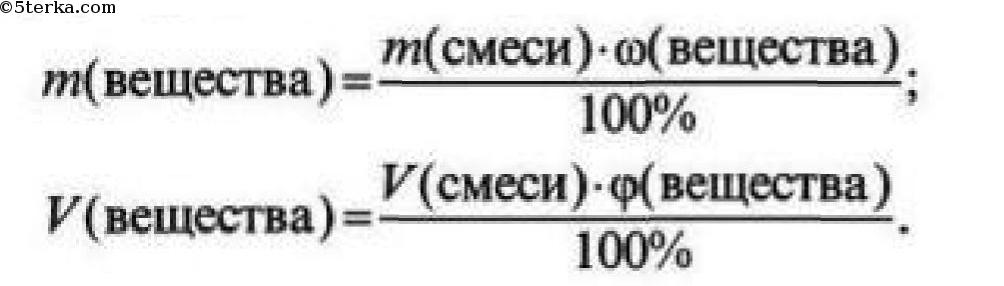Каждое вещёство наряду с основным компонентом включает то или иное количество примесей. Именно поэтому абсолютно чистых веществ в природе не существует.
Образец (вещество, навеску), содержащий примеси, принято называть техническим (технически чистым). Его массу обозначают mтехн, массу примесей — mприм, а массу основного (чистого) вещества — mчист.
Обрати внимание!
(=) mчист (+)
mприм
.
Содержание примесей в техническом образце обычно указывается с помощью массовой доли, которую выражают в долях от единицы или в процентах:
Сумма массовых долей примесей
ωприм
и основного вещества
ωчист
равна (1) ((100) %):
(+) ωчист (=) (1) ((100) %).
При проведении расчётов по уравнениям химических реакций, если исходное вещество содержит определённую долю примесей, придерживаются алгоритма:
1. если необходимо, записывают уравнение химической реакции.
2. Находят массу чистого вещества.
Её можно рассчитать по формуле:
mчист (=) mтехн (·) ωчист (=) mтехн (·) ((1 -) ωприм )
— либо используя пропорцию. При этом mтехн соответствует (100) %, а mчист — (x) %.
3. Определяют химическое количество чистого вещества по формуле:
n=mM.
4. Подчёркивают формулы интересующих веществ в уравнении реакции.
Под этими формулами записывают химические количества вступивших в реакцию и образовавшихся веществ (коэффициенты перед веществами в уравнении реакции). Над формулами веществ указывают известную величину (найденное по формуле химическое количество чистого вещества), а также неизвестную, которую обозначают за (x) — (химическое количество образующегося продукта реакции или вступившего в реакцию исходного вещества).
5. Составляют пропорцию и находят неизвестную величину.
6. Если необходимо, рассчитывают по формуле массу продукта реакции или массу вступившего в реакцию вещества:
m=n⋅M.
Обрати внимание!
Если необходимо найти объём газообразного вещества ( при н. у.) — используют формулу: V(вещ)=Vm⋅n(вещ); Vm=22,4 л/моль.
Вычисли массу негашёной извести
CaO
, которую получили при обжиге известняка массой (300) г, если массовая доля примесей в нём равна (0,08) ((8) %).
1. Запиши уравнение химической реакции:
2. Определи массовую долю чистого карбоната кальция в известняке и найди массу соли:
ωчист (=) (1) (-) ωприм (= 1 — 0,08 = 0,92).
(0,92) — массовая доля (в долях от единицы) карбоната кальция в известняке.
mчист (=) mтехн (·) ωчист (= 300 · 0,92 = 276) г.
(276) г — масса чистого карбоната кальция в известняке.
3. Определи химическое количество чистого вещества:
моль.
4. (2,76) моль (x) моль
(1) моль (1) моль
5. Составь пропорцию и найди неизвестную величину:
(2,76) моль — химическое количество образовавшейся негашёной извести.
6. Определи массу негашёной извести:
г.
Ответ: (m()CaO()) (=) (154,56) г.
I.
Определение массы (объема) вещества по
известной массе другого вещества, содержащего определенную долю примесей.
Помните: 1.Особенность данного типа задач в том, что сначала
необходимо вычислить массу чистого вещества в смеси.
2. В условии
задачи в роли смеси может выступать руда, технический образец вещества, раствор.
Порядок решения задачи:
1) Прочитайте задачу, запишите краткое условие.
2)
Определите
массу чистого вещества по формуле: mв-ва= mсмеси * ωв-ва.
3) Напишите уравнение реакции.
4) Найдите количества веществ, данных в задаче,
по уравнению и по условию.
5) Произведите необходимые расчёты и запишите
ответ.
Образец решения:
Рассчитайте объем водорода, выделившегося при взаимодействии с соляной
кислотой 325 г цинка, содержащего 20% примесей.
Д
а н о:
Р е ш е н и е:
mтехнич.(Zn)= 325 г
1) mтехнич.(Zn)=
325 г ω (Zn)= 100%-20%=80% (0,8);
ωприм.=
20% (0,2) m (Zn)=
325 * 0,8 = 260 г
V(Н2)= ?
n (Zn)
= 260г : 65 г/моль = 4 моль.
по условию:
4
моль Х
моль
2)
Zn
+ 2HCl = ZnCl2 +
H2
: 1 моль
1 моль
Х= 4 моль
V(Н2) = Vm * n(Н2); V(Н2) = 22,4 л/моль * 4 моль =
89,6 л.
Ответ: V(Н2) =89,6 л.
Алгоритм
решения задач на примеси.
II.
Определение массовой доли примесей (или
массовой доли чистого вещества в смеси) по массе (объёму) продуктов реакции.
Помните: 1) сначала выполняются действия по уравнению
реакции;
2) для
определения массовой доли примесей применяем формулу:
ωприм.
= mприм./mсмеси.
Порядок решения задачи:
1) Прочитайте задачу, запишите краткое условие.
2) Составьте уравнение химической реакции.
3) Рассчитайте массу чистого вещества,
необходимого для реакции по уравнению реакции.
4) Вычислите массу примесей в образце по условию.
5) Вычислите массовую долю примесей по формуле: ωприм.
= mприм./mсмеси.
Образец решения:
Определите массовую долю примесей в техническом образце карбида
кальция, если из 200 г его получили 56 л ацетилена.
Д
а н о: Р е ш
е н и е: пусть х г – масса чистого
вещества
CaC2.
mтехнич.(CaC2)=200г
1)по условию: х г 56л
V(С2Н2)
= 56 л
CaC2
+
2Н2О = С2Н2 + Са(ОН)2
ωприм = ?
1 моль 1 моль
М=64г/моль Vm=22.4л/моль
по уравнению: m=64 г V= 22,4 л ,
тогда х г/64 г= 56 л/22,4 л;
х = 160 г.
2) определяем массу примесей в образце:
mприм.= 200 – 160 = 40 г.
3) определяем массовую долю примесей:
ωприм = 40 г/ 200 г = 0,2 (или 20%).
Ответ: ωприм =
20%.
В этой статье мы коснемся нескольких краеугольных понятий в химии, без которых совершенно невозможно
решение задач. Старайтесь понять смысл физических величин, чтобы усвоить эту тему.
Я постараюсь приводить как можно больше примеров по ходу этой статьи, в ходе изучения вы увидите множество примеров
по данной теме.

Относительная атомная масса — Ar
Представляет собой массу атома, выраженную в атомных единицах массы. Относительные атомные массы указаны в периодической
таблице Д.И. Менделеева. Так, один атом водорода имеет атомную массу = 1, кислород = 16, кальций = 40.
Относительная молекулярная масса — Mr
Относительная молекулярная масса складывается из суммы относительных атомных масс всех атомов, входящих в состав вещества.
В качестве примера найдем относительные молекулярные массы кислорода, воды, перманганата калия и медного купороса:
Mr (O2) = (2 × Ar(O)) = 2 × 16 = 32
Mr (H2O) = (2 × Ar(H)) + Ar(O) = (2 × 1) + 16 = 18
Mr (KMnO4) = Ar(K) + Ar(Mn) + (4 × Ar(O)) = 39 + 55 + (4 * 16) = 158
Mr (CuSO4*5H2O) = Ar(Cu) + Ar(S) + (4 × Ar(O)) + (5 × ((Ar(H) × 2) +
Ar(O))) = 64 + 32 + (4 × 16) + (5 × ((1 × 2) + 16)) = 160 + 5 * 18 = 250
Моль и число Авогадро
Моль — единица количества вещества (в системе единиц СИ), определяемая как количество вещества, содержащее столько же структурных единиц
этого вещества (молекул, атомов, ионов) сколько содержится в 12 г изотопа 12C, т.е. 6 × 1023.
Число Авогадро (постоянная Авогадро, NA) — число частиц (молекул, атомов, ионов) содержащихся в одном моле любого вещества.

Больше всего мне хотелось бы, чтобы вы поняли физический смысл изученных понятий. Моль — международная единица количества вещества, которая
показывает, сколько атомов, молекул или ионов содержится в определенной массе или конкретном объеме вещества. Один моль любого вещества
содержит 6.02 × 1023 атомов/молекул/ионов — вот самое важное, что сейчас нужно понять.
Иногда в задачах бывает дано число Авогадро, и от вас требуется найти, какое вам дали количество вещества (моль). Количество вещества в химии
обозначается N, ν (по греч. читается «ню»).
Рассчитаем по формуле: ν = N/NA количество вещества 3.01 × 1023 молекул воды и 12.04 × 1023 атомов углерода.
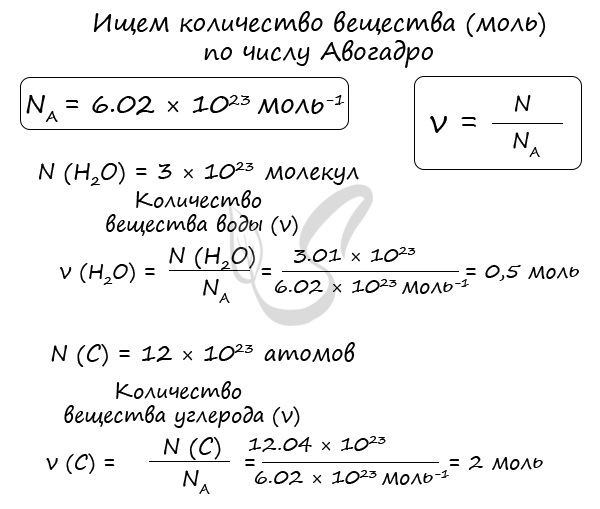
Мы нашли количества вещества (моль) воды и углерода. Сейчас это может показаться очень абстрактным, но, иногда не зная, как найти
количество вещества, используя число Авогадро, решение задачи по химии становится невозможным.
Молярная масса — M
Молярная масса — масса одного моля вещества, выражается в «г/моль» (грамм/моль). Численно совпадает с изученной нами ранее
относительной молекулярной массой.
Рассчитаем молярные массы CaCO3, HCl и N2
M (CaCO3) = Ar(Ca) + Ar(C) + (3 × Ar(O)) = 40 + 12 + (3 × 16) = 100 г/моль
M (HCl) = Ar(H) + Ar(Cl) = 1 + 35.5 = 36.5 г/моль
M (N2) = Ar(N) × 2 = 14 × 2 = 28 г/моль
Полученные знания не должны быть отрывочны, из них следует создать цельную систему. Обратите внимание: только что мы рассчитали
молярные массы — массы одного моля вещества. Вспомните про число Авогадро.
Получается, что, несмотря на одинаковое число молекул в 1 моле (1 моль любого вещества содержит 6.02 × 1023 молекул),
молекулярные массы отличаются. Так, 6.02 × 1023 молекул N2 весят 28 грамм, а такое же количество молекул
HCl — 36.5 грамм.
Это связано с тем, что, хоть количество молекул одинаково — 6.02 × 1023, в их состав входят разные атомы, поэтому и
массы получаются разные.

Часто в задачах бывает дана масса, а от вас требуется рассчитать количество вещества, чтобы перейти к другому веществу в реакции.
Сейчас мы определим количество вещества (моль) 70 грамм N2, 50 грамм CaCO3, 109.5 грамм HCl. Их молярные
массы были найдены нам уже чуть раньше, что ускорит ход решения.

ν (CaCO3) = m(CaCO3) : M(CaCO3) = 50 г. : 100 г/моль = 0.5 моль
ν (HCl) = m(HCl) : M(HCl) = 109.5 г. : 36.5 г/моль = 3 моль
Иногда в задачах может быть дано число молекул, а вам требуется рассчитать массу, которую они занимают. Здесь нужно использовать
количество вещества (моль) как посредника, который поможет решить поставленную задачу.
Предположим нам дали 15.05 × 1023 молекул азота, 3.01 × 1023 молекул CaCO3 и 18.06 × 1023 молекул
HCl. Требуется найти массу, которую составляет указанное число молекул. Мы несколько изменим известную формулу, которая поможет нам связать
моль и число Авогадро.

Теперь вы всесторонне посвящены в тему. Надеюсь, что вы поняли, как связаны молярная масса, число Авогадро и количество вещества.
Практика — лучший учитель. Найдите самостоятельно подобные значения для оставшихся CaCO3 и HCl.
Молярный объем
Молярный объем — объем, занимаемый одним молем вещества. Примерно одинаков для всех газов при стандартной температуре
и давлении составляет 22.4 л/моль. Он обозначается как — VM.
Подключим к нашей системе еще одно понятие. Предлагаю найти количество вещества, количество молекул и массу газа объемом
33.6 литра. Поскольку показательно молярного объема при н.у. — константа (22.4 л/моль), то совершенно неважно, какой газ мы
возьмем: хлор, азот или сероводород.
Запомните, что 1 моль любого газа занимает объем 22.4 литра. Итак, приступим к решению задачи. Поскольку какой-то газ
все же надо выбрать, выберем хлор — Cl2.


Моль (количество вещества) — самое гибкое из всех понятий в химии. Количество вещества позволяет вам перейти и к
числу Авогадро, и к массе, и к объему. Если вы усвоили это, то главная задача данной статьи — выполнена 

Относительная плотность и газы — D
Относительной плотностью газа называют отношение молярных масс (плотностей) двух газов. Она показывает, во сколько раз одно вещество
легче/тяжелее другого. D = M (1 вещества) / M (2 вещества).
В задачах бывает дано неизвестное вещество, однако известна его плотность по водороду, азоту, кислороду или
воздуху. Для того чтобы найти молярную массу вещества, следует умножить значение плотности на молярную массу
газа, по которому дана плотность.
Запомните, что молярная масса воздуха = 29 г/моль. Лучше объяснить, что такое плотность и с чем ее едят на примере.
Нам нужно найти молярную массу неизвестного вещества, плотность которого по воздуху 2.5

Предлагаю самостоятельно решить следующую задачку (ниже вы найдете решение): «Плотность неизвестного вещества по
кислороду 3.5, найдите молярную массу неизвестного вещества»

Относительная плотность и водный раствор — ρ
Пишу об этом из-за исключительной важности в решении
сложных задач, высокого уровня, где особенно часто упоминается плотность. Обозначается греческой буквой ρ.
Плотность является отражением зависимости массы от вещества, равна отношению массы вещества к единице его объема. Единицы
измерения плотности: г/мл, г/см3, кг/м3 и т.д.
Для примера решим задачку. Объем серной кислоты составляет 200 мл, плотность 1.34 г/мл. Найдите массу раствора. Чтобы не
запутаться в единицах измерения поступайте с ними как с самыми обычными числами: сокращайте при делении и умножении — так
вы точно не запутаетесь.

Иногда перед вами может стоять обратная задача, когда известна масса раствора, плотность и вы должны найти объем. Опять-таки,
если вы будете следовать моему правилу и относится к обозначенным условным единицам «как к числам», то не запутаетесь.
В ходе ваших действий «грамм» и «грамм» должны сократиться, а значит, в таком случае мы будем делить массу на плотность. В противном случае
вы бы получили граммы в квадрате 
К примеру, даны масса раствора HCl — 150 грамм и плотность 1.76 г/мл. Нужно найти объем раствора.

Массовая доля — ω
Массовой долей называют отношение массы растворенного вещества к массе раствора. Важно заметить, что в понятие раствора входит
как растворитель, так и само растворенное вещество.
Массовая доля вычисляется по формуле ω (вещества) = m (вещества) / m (раствора). Полученное число будет показывать массовую долю
в долях от единицы, если хотите получить в процентах — его нужно умножить на 100%. Продемонстрирую это на примере.

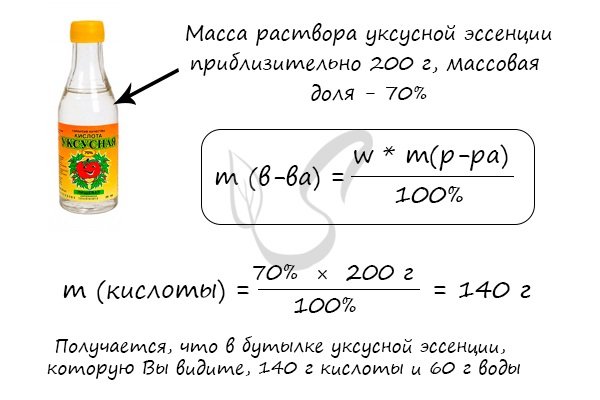
Решим несколько иную задачу и найдем массу чистой уксусной кислоты в широко известной уксусной эссенции.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Вычисление массы или
объема продукта реакции по известной массе или объему исходного вещества,
содержащего определенную массовую долю примесей (в %)
При
решении задач этого типа необходимо вначале рассчитать массу или объем чистого
вещества, которое содержится в исходной смеси, а потом решать как обычную
задачу по химическому уравнению. Массу чистого вещества (как и объем) можно
вычислить двумя способами.
С
п о с о б 1. Массу чистого вещества (или объем) определяют по формуле:
w (чист.
в-ва) = 100 % – w (примеси),
w (чист.
в-ва) =
m (чист.
в-ва) = m (смеси) · w (чист. в-ва)
Способ 2. Вначале определяют массу примеси:
m (примеси)
= m (смеси) · w (примеси), а затем вычитают ее из
массы смеси: m (чист. в-ва) = m (смеси) – m (примеси).
П р и м е р 1. На завод было
доставлено 50 т фосфорита, содержащего 35 % пустой породы. Определите
массу фосфата кальция в природном фосфорите.
Решение.
С п о с о б 1. Массовая доля фосфата
кальция в руде составляет:
w (Ca3(PO4)2)
= 100 % – 35 % = 65 %,
m (Ca3(PO4)2)
= 50 · 0,65 = 32,5 (т).
Способ
2. m (примеси) = 50 т · 0,35 = 17,5 т, тогда
m (Ca3(PO4)2)
= 50 т – 17,5 т = 32,5 т.
П р и м е р 2. Определите, какой
объем ацетилена можно получить из карбида кальция массой 10 кг, массовая
доля примесей в котором 15 %.
Решение.
1.
Определяем массу примесей:
m (примеси)
= 10 · 0,15 = 1,5 (кг)
2.
Масса чистого карбида кальция равна
m (CaC2)
= 10 – 1,5 = 8,5 (кг).
3.
Составляем уравнение реакции:
0,133 моль х моль
CaC2
+ 2H2O = C2H2
+ Ca(OH)2
1 моль 1 моль
4.
Рассчитываем ν (CaC2):
ν (CaC2)
= =
0,133 моль
5.
По уравнению реакции определяем ν (C2Н2):
ν (CaC2)
= ν (C2Н2) Þ
ν (C2Н2) = 0,133 моль
6.
Определяем объем ацетилена:
V (C2Н2)
= ν (C2Н2) · VM
= 0,133 моль · 22,4 м3/моль = 2,979 м3.
П р и м е р 3. Вычислите, какая масса
фосфорита с массовой долей примесей 12 % необходима для получения фосфора
массой 200 кг.
Решение.
х моль 6,452 моль
Ca3(PO4)2
+ 3SiO2 + 5C 3CaSiO3 + 2P
+ 5CO
1 моль 2 моль
1.
Определяем ν (P)
: ν (P) = =
6,452 (моль).
2.
По уравнению реакции определяем ν (Ca3(PO4)2)
чистого:
ν (Ca3(PO4)2)
: ν (P) = 1 : 2 Þ
ν (Ca3(PO4)2) = =
3,226 (моль).
3.
Находим массу чистого фосфата кальция, необходимую для получения фосфора массой
200 кг:
m (Ca3(PO4)2)
= ν (Ca3(PO4)2)
· М
= 3,226 · 310 = 1000 (кг).
4.
Находим массовую долю чистого фосфата кальция:
w (Ca3(PO4)2) =
100 % – w (примесей) = 100 % – 12 % = 88 %.
5.
Определяем массу фосфорита, необходимую для получения фосфора массой
200 кг:
w (Ca3(PO4)2)
=
Þ
m (фосфорита) = = 1136,4 (кг).
П р и м е р 4. При взаимодействии
кальцинированной соды массой 10,8 г с избытком соляной кислоты получили
оксид углерода (IV) объемом 2,24 л (н. у.). Вычислите массовую долю
(%) примесей в кальцинированной соде.
Решение.
х моль 0,1 моль
Na2CO3
+ 2HCℓ = 2NaCℓ + H2O + CO2
1 моль 1 моль
1.
Находим количество вещества СО2:
ν (СО2)
= =
0,1 (моль)
2.
Вычисляем массу Na2CO3 в кальцинированной соде.
Из
уравнения реакции следует:
ν (Na2CO3)
: ν (СО2) = 1 : 1 Þ
ν (Na2CO3) = 0,1 моль, тогда
m (Na2CO3)
= ν (Na2CO3)
· М (Na2CO3)
= 0,1 · 106 = 10,6 (г).
3.
Находим массу примесей в кальцинированной соде:
m (прим.)
= m (кальц. сода) – m (Na2CO3) = 10,8 – 10,6 =
0,2 (г)
4.
Вычисляем массовую долю примесей:
w примесей
= =
0,018, или 1,8 %.
Реши самостоятельно:
1. Определите массу NaOH, которую
можно получить при взаимодействии соды с известковым молоком, полученным из
5 кг известняка, содержащего 80 % CaCO3. (3,2 кг.)
2.
Вычислите объем (в м3) оксида углерода (IV) и массу жженой извести
(CaO), которые можно получить при обжиге 500 кг известняка, содержащего
92 % карбоната кальция. (257,6 кг CaO и 103 м3 СО2.)
3.
Какая масса раствора с массовой долей серной кислоты 70 % потребуется для
получения фосфорной кислоты из фосфорита массой 200 кг, содержащего
70 % Ca3(PO4)2? (189,7 кг.)
4.
При взаимодействии 5,0 г технического магния с избытком соляной кислоты
выделилось 3,36 л водорода (н. у.). Вычислите массовую долю (в %)
чистого магния в техническом магнии. (72,0 %.)
5.
Оксид углерода (IV), полученный при сжигании угля массой 50 г, пропустили
через раствор гидроксида бария. Какая масса осадка образовалась, если
массовая доля углерода в угле составляет 96 %? (788 г.)
6.
Песок массой 2 кг сплавили с избытком гидроксида калия, получив в
результате реакции силикат калия массой 3,82 кг. Определите выход продукта
реакции, если массовая доля оксида кремния (IV) в песке равна 90 %. (82,7 %.)
7.
При сгорании технической серы массой 10 г выделился газ, который
пропустили через избыток раствора гидроксида натрия. В реакцию вступил
гидроксид натрия массой 24 г. Определите массовую долю серы в техническом
продукте. (96 %.)
8.
Вычислите массу раствора кислоты с массовой долей HCℓ 30 %,
затраченную на растворение цинка массой 200 г с массовой долей примесей
35 %. (487 г.)
9.
Для обжига сульфида цинка массой 2 т с массовой долей негорючих веществ
3 % израсходовали 6000 м3 воздуха. Определите объемные
доли газов в образовавшейся газовой смеси. (83,1 % N2;
7,76 % SO2; 9,14 % О2.)
10.
Вычислите, какая масса магнетита Fe3O4, содержащего
10 % примесей, необходима для получения железа массой 4 т. (6,134 т.)
11.
При действии на мрамор массой 10,5 г соляной кислотой выделился оксид
углерода (IV) объемом 2,24 л (н. у.). Определите массовую долю (%)
карбоната кальция в мраморе. (95,24 %.)
12.
При прокаливании на воздухе пирита массой 5 кг получен оксид серы (IV)
массой 5,12 кг. Определите массовую долю FeS2 в пирите.
(96 %.)
13.
Вычислите число атомов углерода и кислорода в карбонате кальция массой
11 кг, в котором находится 9,1 % примесей, не содержащих
углерод и кислород. (6 · 1022 атомов углерода; 1,8 · 1023
атомов кислорода.)
14.
Вычислите число атомов цинка и хлора в хлориде цинка массой 42,5 г, в
котором находится 20 % примесей, не содержащих цинк и хлор. (1,5 · 1023
атомов цинка; 3 · 1023 атомов хлора.)
15.
Массовая доля ZnS в цинковой обманке составляет 97 %. Определите, какой
объем сероводорода образуется из 500 кг цинковой обманки. (112 м3.)
16.
Какое количество бензола можно получить из ацетилена, выделившегося при
обработке водой карбида кальция массой 42,8 г с массовой долей примесей
18,4 %? Массовая доля выхода бензола составляет 30 %. (0,054 моль.)
17.
Из карбида кальция массой 7,5 г с массовой долей примесей 4 %
получили ацетилен, который был превращен в альдегид по реакции Кучерова. Какая
масса серебра выделится при взаимодействии всего полученного альдегида с
аммиачным раствором оксида серебра? (24,3 г.)
18.
Природный газ объемом 235,8 л (н. у.) использовали для получения
ацетилена. Объемная доля метана в газе составляет 95 %. Определите объем
образовавшегося ацетилена (н. у.), если его выход составил 60 %. (67,2 л.)
19. Вычислите
массу раствора с массовой долей гидроксида натрия 10 %, необходимую для
полной нейтрализации продукта сгорания природного газа объемом 23,33 л
(н. у.). Объемная доля метана составляет 96 %. (800 г.)
20. Какой объем
природного газа (н. у.) потребуется для получения муравьиной кислоты
массой 69 г путем каталитического окисления метана? Объемная
доля метана в природном газе составляет 98 %. (34,28 л.)
21. Образец технического карбида алюминия массой
16 г обработали избытком воды. Определите объем газа (н. у.), который
получили, если массовая доля примесей в карбиде составляет 10 %, а выход
продукта реакции равен 75 %. (5,04 л.)
№3. Доля (массовая или объемная) примесей — это безразмерная величина, которая показывает отношение массы (объема) примесей к общей массе (объему) смеси.
Чтобы найти массу (объем) чистого вещества, если известна массовая (объемная) доля примесей, необходимо:
1) из 100% вычесть массовую (объемную) долю примесей и найти массовую (объемную) долю чистого вещества;
2) по формуле рассчитать массу (объем) чистого вещества:
Источник:
Решебник
по
химии
за 11 класс (О.С. Габриелян, 2007 год),
задача №3
к главе «§12 Состав вещества. Смеси».
Все задачи
← 2 Что называют массовой (объемной) долей компонента смеси? Как ее рассчитывают?
4 Не производя расчета, укажите, в каком из оксидов, формулы которых Fe2O3 и Fe3O4, содержание железа выше. Ответ подтвердите расчетами. →
Комментарии