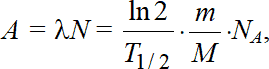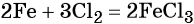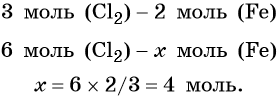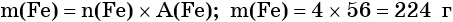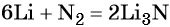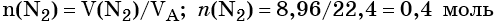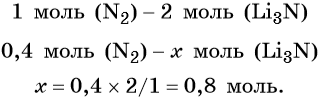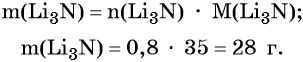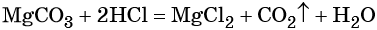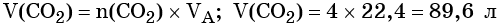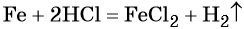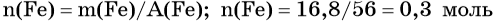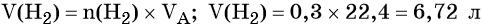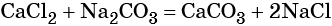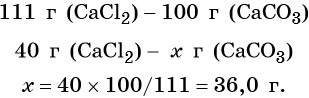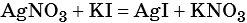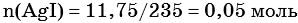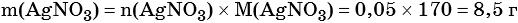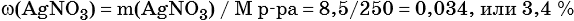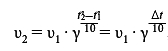В химии гравиметрия («весовой анализ») является арбитражным аналитическим методом. Какими бы ни были методы анализа, применяемые в настоящее время (сейчас получили распространение физико-химические и физические методы), все они так или иначе, применительно к задачам количественного анализа, сводятся к необходимости использовать некоторые исходные вещества в качестве эталонов. Последние могут быть изготовлены с использованием, в конечном итоге, аналитических весов.
Но в ядерной физике и радиохимии гравиметрический метод совершенно не распространен главным образом вследствие того, что в подавляющем числе радиоаналитических задач (и, тем более, в радиоэкологии) имеют дело с такими массами радиоактивных веществ, которые находятся за пределом чувствительности даже наилучших весов. Тем не менее помимо установления абсолютной активности радионуклидов, что выполняется инструментально, бывает необходимо знать и их массу (концентрацию). Это достигается элементарным расчетом на основе соотношения (1.10):
где m – масса радионуклида (г), M – молярная масса радионуклида (г/моль);
NA = 6,022045•1023 моль-1 – постоянная Авогадро.
Отсюда следует:

(Здесь активность выражается в беккерелях, а период полураспада в секундах).
По этой формуле можно рассчитать массу, например, одного кюри любого радионуклида. Так, 1Kи 238 U (T1/2 = 4,5•109 лет) имеет массу около трех тонн, 1 Kи226Ra (T1/2= 1600 лет) – 1 г (это так и должно быть, т.к. один грамм именно этого изотопа радия в свое время был выбран за эталон одного кюри).
В то же время масса короткоживущих радионуклидов, имеющих T1/2 порядка нескольких лет или суток (не говоря уж о тех, период полураспада которых исчисляется секундами или долями секунды), в аналитическом смысле может оказаться настолько незначительной, эфемерной, почти нереальной, что ей нельзя будет приписать проявление каких бы то ни было макроскопических термодинамически фиксируемых свойств. Иными словами, химические (в общем случае термодинамические) характеристики любой фазы, в которую включается (или ею утрачивается, отдается) радиоактивный микрокомпонент, не могут измениться сколько-нибудь заметным образом, т.к. уровень концентрации этой примеси (выражаемый в процентах или в мольных долях) не более значим, чем уровень любых других практически неустранимых загрязнений, присутствующих даже в самых чистых химических препаратах.
Вот такие массы веществ и соответствующие им концентрации в радиохимической литературе получили название «невесомые количества», «микроколичества», или даже «ультрамикроколичества». А само вещество в таких количествах обычно называют микрокомпонентом.
С явлением радиоактивности (точнее – с экспоненциальным характером ее проявления) связан распространенный паралогизм – убежденность некоторых людей в том, что по истечении десяти периодов полураспада любой радионуклид практически распадается полностью.
Проанализируем справедливость этого утверждения. В соответствии с (1.11): N/N0 = 2 – n = 2–10 = 1/1024. При этом распалось (N0 – N) атомов:
Nрасп = N0 – N = N0 (1–1/1024).
Последнее выражение дает основание для высказывания двух суждений.
1) С одной стороны, 1–1/1024 ? 1, т.е. Nрасп ? N0, что соответствует итогу «радионуклид практически распался весь». Казалось бы, это утверждение в какой-то степени приемлемо, т.к. равенство Nрасп ? N0 выполняется с погрешностью (погрешность вычисления) менее 0,1%, о чем многие проектировщики могут только мечтать.
2) Но, с другой стороны, из того факта, что значение некоторой физической величины уменьшилось на три порядка, вовсе не вытекает следствие, что данную величину можно приравнять нулю. Это всего лишь «психологический софизм», поскольку здесь соединились два независимых сравнения, причем одно в процессе рассуждений подменяется другим.
В первом случае признается имеющим смысл фраза, что «0,00098 гораздо меньше (пренебрежимо меньше) единицы». Но и во втором случае оставшееся число атомов, N, тоже необходимо сравнить с каким-то другим эталоном, репером, нормой и т.п., но отнюдь не с единицей.
Скорей всего N и A, которые «остались» (Nост и Aост) после истечения 10 T1/2, нужно сравнивать с существующими нормами или потребностями. Если оценивается вредная сторона носителя радиоактивности, то сравнение должно происходить, например, с санитарными нормами (Aн). Здесь возможны различные ситуации:
Aн > Aост и даже Aн >> Aост, либо наоборот Aн<Aост, Aн << Aост (обычно в подобных сравнениях фигурируют удельные величины). Понятно, что житейские и юридические выводы, следующие отсюда, будут абсолютно различными. При этом совсем не исключено, что соотношение Aн << Aост может оставаться в силе не только по истечению 10 T1/2, но и после прошествия гораздо большего отрезка времени.
Таким образом, психологическому аспекту экспоненциальной зависимости редко отдают должное, она таит в себе ряд паралогизмов и не вписывается в интуицию человека. Эта зависимость наглядна только при сравнении ее с некоторым соответствующим пределом (нормой, репером, эталоном и т.п.).
У закона радиоактивного распада как у зависимости экспоненциального характера есть еще одна особенность, касающаяся временного поведения долгоживущих радионуклидов. В связи с этим рассмотрим один характерный пример.
Период полураспада урана-238 равен 4,5·109 лет. Какова убыль его активности вследствие распада за конкретный, но незначительный по сравнению с периодом полураспада интервал времени, например, за миллион лет?
Эта убыль, выражаемая в долях единицы, отнесенная к начальному значению активности, равна:
Положим t = 106 лет и преобразуем равенство следующим образом:
Обоснованно полагая ? величиной очень малой в сравнении с единицей, ограничимся первым линейным членом разложения логарифмической функции в ряд: ln(1 – ?) ? – ? . Тогда ? = (0,692•106/4,5·109) = 1,5 · 10–4 или 0,015%. Таким образом, активность урана-238 как функция времени может быть независимо рассмотрена в двух временных масштабах.
1) В геохронологическом масштабе времени (отрезки времени, сопоставимые, например, с возрастом Земли, признаваемым в космогонии) этот радионуклид значимо изменял свою активность. Так, если возраст Земли в настоящее время оценивается величиной порядка нескольких миллиардов лет, то с момента возникновения нашей планеты как тела Солнечной системы до наших дней активность содержащегося в геосфере урана-238 уменьшилась практически вдвое.
2) В технологическом (антропном) масштабе (отрезки времени, сопоставимые с интервалом, протекшим с момента возникновения Homo Sapiens, и гораздо меньшие), как только что было показано выше, активность этого радионуклида (и, естественно, всех других, обладающих такими же значительными периодами полураспада) может быть рассматриваема как практически независимая от времени: 
Иными словами, обсуждение зависимости активности долгоживущих радионуклидов от времени имеет смысл и сопряжено с практически полезными расчетами только тогда, когда четко определен масштаб времени, в соответствии с которым это обсуждение проводится.
Данный текст является ознакомительным фрагментом.
Вычисление количества вещества, массы или объема вещества по количеству веществ, массе или объему одного из реагентов или продуктов реакции
Основой для проведения количественных расчётов в химии является закон сохранения массы. Согласно этому закону масса реагентов равна массе продуктов реакции.
Отсюда следует, что для любой химической реакции массы реагентов и продуктов реакции относятся между собой как молярные массы веществ, умноженные на их стехиометрические коэффициенты.
Для расчёта по химическим уравнениям можно использовать два эквивалентных способа: через количество вещества или через пропорцию. Подчеркнём ещё раз: официального запрета на использование метода пропорций при решении задач на ОГЭ и ЕГЭ нет!
Для определения массы (или количества вещества) продуктов реакции или исходных веществ по уравнениям химических реакций вначале составляют уравнение химической реакции и устанавливают стехиометрические коэффициенты; затем определяют молярную массу, массу и количество вещества известных реагентов химической реакции; составляют и решают пропорцию, в которую в зависимости от условий задачи вводят числовые значение величин: молярные массы, массы, количества веществ или их объёмы (для газов).
При этом в одном столбце пропорций должны находиться одинаковые характеристики вещества с одной и той же размерностью.
Пример 1. Масса железа, вступившего в реакцию с 6 моль хлора, равна _________ г. (Ответ запишите с точностью до целого числа.)
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что 3 моль Cl2 реагируют с 2 моль Fe, т. е.:
Определяем массу железа:
Пример 2. Масса нитрида лития, образовавшегося в результате его реакции с азотом объёмом 8,96 л, равна_______________ г.
Решение. Составляем уравнение химической реакции:
Определяем количество вещества азота, вступившего в реакцию:
Из уравнения реакции следует, что из 1 моль N2 образуется 2 моль Li3N, т. е.:
Определим массу Li3N:
Пример 3. Объём углекислого газа, образовавшегося в результате разложения карбоната магния количеством вещества 4 моль избытком соляной кислоты, равен________ л.
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что количество вещества углекислого газа и карбоната магния равны между собой, т. е. n(CO2) = 4 моль.
Определим V(CO2):
Пример 4. Объём водорода, который выделится при растворении 16,8 г железа в избытке разбавленной соляной кислоты, равен _________ л.
Решение. Составляем уравнение химической реакции:
Определим количество вещества железа:
Количество вещества железа и водорода в данном уравнении реакции равны между собой. Следовательно, количество вещества водорода также равно 0,3 моль.
Вычислим объём водорода:
Пример 5. Масса осадка, который образуется в результате взаимодействия 40,0 г хлорида кальция с избытком карбоната натрия, равна _________г.
Решение. Составляем уравнение реакции:
Согласно уравнению химической реакции составим пропорцию и решим её:
Пример 6. 250 г раствора нитрата серебра смешали с избытком раствора йодида калия. Выпал осадок массой 11,75 г. Вычислите массовую долю нитрата серебра в исходном растворе.
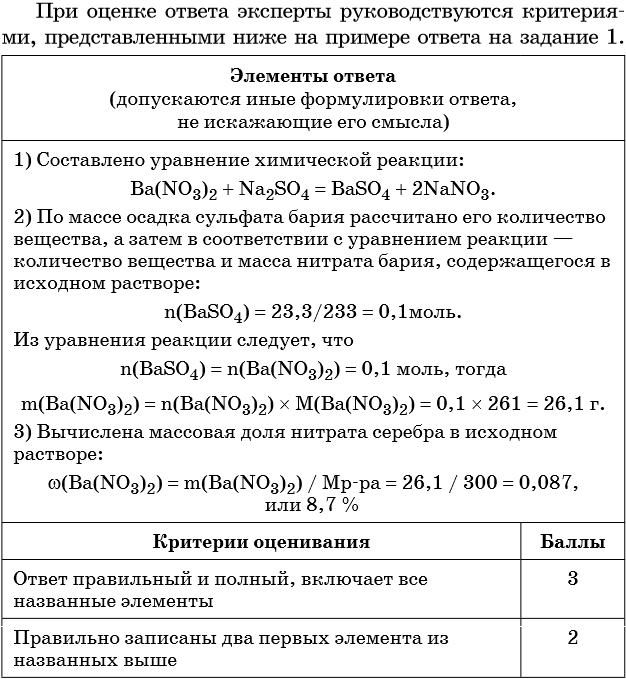
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысла)
1) Составлено уравнение химической реакции:
2) По массе осадка йодида серебра рассчитано его количество вещества, а затем в соответствии с уравнением реакции — количество вещества и масса нитрата серебра, содержащегося в исходном растворе:
Из уравнения реакции следует, что n(AgI) = n(AgNO3) = 0,05 моль, тогда:
3) Вычислена массовая доля нитрата серебра в исходном растворе:
| Критерии оценивания | Баллы |
| Ответ правильный и полный, включает все названные элементы | 3 |
| Правильно записаны два первых элемента из названных выше | 2 |
| Правильно записан один из названных выше элементов (1-й или 2-й) | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
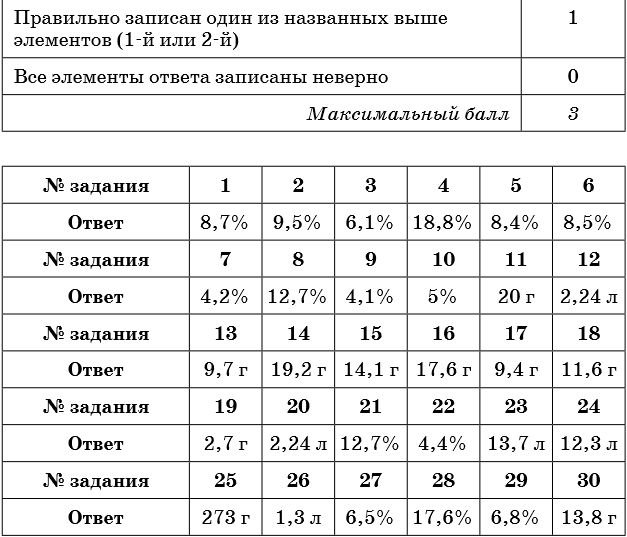
Тренировочные задания
1. К 300 г раствора нитрата бария прибавили избыток раствора сульфата натрия. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
2. К 150 г раствора сульфата натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
3. К 300 г раствора силиката натрия прибавили избыток раствора нитрата кальция. Масса выпавшего осадка составила 12,0 г. Определите концентрацию соли в исходном растворе.
4. К 150 г раствора карбоната калия прибавили избыток раствора соляной кислоты. При этом выделился газ объёмом 3,36 л (н. у.). Определите концентрацию соли в исходном растворе.
5. К 250 г раствора гидрокарбоната натрия прибавили избыток раствора бромоводородной кислоты. При этом выделился газ объёмом 5,6 л. Определите концентрацию соли в исходном растворе.
6. К 50 г раствора карбоната натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
7. К 200 г раствора хлорида бария прибавили избыток раствора карбоната калия. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
8. К 200 г раствора хлорида железа (II) прибавили избыток раствора гидроксида калия. Масса выпавшего осадка составила 18,0 г. Определите концентрацию соли в исходном растворе.
9. К 400 г раствора нитрата свинца прибавили избыток раствора йодида натрия. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
10. К 300 г раствора йодида натрия прибавили избыток раствора нитрата свинца. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
11. Определите массу осадка, который выпадет при взаимодействии 150 г 14,8%-ного раствора хлорида кальция с избытком раствора карбоната натрия.
12. Определите объём газа (н. у.), который выделится при взаимодействии 120 г 8,8%-ного раствора карбоната натрия с избытком раствора соляной кислоты.
13. Определите массу соли, которая выпадет в осадок при взаимодействии 140 г 13,5%-ного раствора нитрата цинка с избытком раствора сульфида натрия.
14. Определите массу осадка, который выделится при взаимодействии 200 г 18,8%-ного раствора нитрата меди с избытком раствора сульфида натрия.
15. Определите массу осадка, который выпадет при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора хлорида цинка.
16. Определите массу осадка, который выделится при взаимодействии 200 г 12,7%-ного раствора хлорида железа (II) с избытком раствора сульфида натрия.
17. Определите массу осадка, который выделится при взаимодействии 50 г 17%-ного раствора нитрата серебра с избытком раствора бромида калия.
18. Определите массу осадка, который образуется при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора нитрата кальция.
19. Определите массу осадка, который образуется при взаимодействии 50 г 5,8%-ного раствора хлорида магния с избытком раствора фосфата натрия.
20. Определите объём газа, который выделится при взаимодействии 200 г 6,9%-ного раствора карбоната калия с избытком раствора соляной кислоты.
21. Оксид фосфора (V) массой 21,3 г растворили в растворе гидроксида калия, в результате чего был получен раствор средней соли массой 500 г. Определите концентрацию фосфата калия в конечном растворе.
22. Раствор хлорида железа (II) полностью прореагировал со 120 г раствора гидроксида натрия, в результате чего образовалось 6,0 г осадка. Определите массовую долю гидроксида натрия в исходном растворе.
23. Какой объём аммиака (н. у.) может полностью прореагировать со 150 г 20%-ного раствора серной кислоты с образованием средней соли?
24. В 200 г 20%-ного раствора соляной кислоты растворили магний до прекращения выделения газа. Определите объём выделившегося при этом водорода (н. у.).
25. Аммиак объёмом 10 л (н. у.) пропустили через раствор серной кислоты с массовой долей 8% до образования средней соли. Определите массу исходного раствора.
26. Определите объём сероводорода (н. у.), который необходимо пропустить через 130 г 6%-ного раствора хлорида меди (II) до полного осаждения сульфида меди (II).
27. Сероводород объёмом 3,36 л (н. у.) пропустили через раствор гидроксида натрия, в результате чего получили 180 г раствора сульфида натрия. Определите массовую долю соли в полученном растворе.
28. Алюминий массой 8,1 г может нацело прореагировать с 250 г раствора серной кислоты. Определите массовую долю серной кислоты в исходном растворе.
29. К 250 г раствора нитрата серебра добавили раствор хлорида калия до прекращения выделения осадка, масса которого составила 14,35 г. Определите массовую долю нитрата серебра в исходном растворе.
30. К 300 г 5%-ного раствора хлорида магния добавили избыток раствора фосфата калия. Вычислите массу выпавшего при этом осадка.
Ответы
Алгоритм 1
Вычисление массы вещества по известной массе другого
вещества, участвующего в реакции
Пример. Вычислите массу кислорода, выделившегося в результате разложения
порции воды массой 9 г.
Последовательность выполнения действий
С помощью соответствующих обозначений запишем условие задачи, найдем молярные массы веществ, о которых идет речь в условии задачи
Дано:
m(Н20) = 9г
m(О2) = ? г
М(Н2О) = 18 г/моль
М(О2) = 32 г/моль
Найдем количество вещества, масса которого дана в условии задачи
Решение:
n=
Запишем уравнение реакции. Расставим коэффициенты
2Н2О = 2Н2?+ О2?
Над формулой в уравнении реакции запишем найденное значение количества вещества, а под формулами веществ — стехиометрические соотношения, отображаемые химическим уравнением
0,5 моль ? моль
2Н2О = 2Н2 + О2
2 моль 1 моль
Вычислим количество вещества, массу которого требуется найти. Для этого составляем пропорцию


Следовательно, n(O2) = 0,25 моль
Найдем массу вещества, которую требуется вычислить
m(O2)= n(O2)·M(O2)
m(O2) = 0,25 моль • 32 г/моль = 8 г
Запишем ответ
Ответ: m(О2) = 8 г
Как найти массу по термохимическому уравнению
Алгоритм 8
Расчеты по термохимическим уравнениям. Вычисление массы вещества по известному количеству теплоты
Пример. По термохимическому уравнению
С + О2 = СО2 + 412 кДж вычислите массу сгоревшего угля, если количество теплоты, выделившееся в результате реакции, составляет 82,4 кДж.
С помощью соответствующих обозначений запишем условие задачи, найдем молярную массу вещества, о котором идет речь в условии задачи
Запишем термохимическое уравнение реакции. Обозначим вопросительным знаком количество вещества, массу которого надо
найти, и надпишем количество теплоты, записанное в условии задачи. Под формулой вещества обозначим молярное соотношение, вытекающее из уравнения реакции. Вычислим количество вещества, массу которого требуется найти.
Решение:
Для этого составим пропорцию
х/1=82,4/412, откуда х= 0,2.
Следовательно, n(С)=0,2 моль
Перейдем от количества вещества к массе вещества. Для этого используем молярную массу вещества
химэко
Меню сайта
Категории каталога
| 8 класс [27] |
| 9 класс [16] |
| 10 класс [30] |
| 11 класс [5] |
| Экзамен [4] |
| Лаборатория [7] |
| Опорные конспекты [0] |
| Переменка [6] |
| НОТ школьника [9] |
| Решение задач [9] |
| Творческие работы учащихся [3] |
| Учебные пособия [5] |
Форма входа
Приветствую Вас Гость!
Поиск
Друзья сайта
Наш опрос
Статистика
Термохимические уравнения включают в себя кроме химических формул тепловой эффект реакции. Числовое значение в уравнении реакции строго соответствует количествам веществ, участников реакции, т.е. коэффициентам. Благодаря этому соответствию, можно установить пропорциональные отношения между количеством вещества или массой и количеством теплоты в этой реакции.
Например: Термохимическое уравнение разложения малахита
Мы видим, что на разложение 1 моля малахита необходимо израсходовать 47 кДж, при этом образуется 2 моля оксида меди, 1 моль воды и 1 моль углекислого газа. Если мы затратим энергии в 2 раза больше, мы сумеем разложить 2 моля малахита, при этом получим 4 моля оксида меди, 2 моля воды и 2 моля углекислого газа.
Аналогично можно установить пропорциональные отношения, используя коэффициенты и молярные массы участников реакции. 47 кДж энергии затратится на разложение 94 г малахита, при этом выделится 160 г оксида меди, 18 г воды и 44 г углекислого газа. Пропорция несложная, но, используя массовые числа, учащиеся часто допускают расчетные ошибки, поэтому я рекомендую решать задачи с пропорциями через количество вещества.
Задача 1. Определите количество теплоты, которое выделится при образовании 120 г MgO в результате реакции горения магния, с помощью термохимического уравнения.
2 Mq + O 2 = 2 MqO + 1204 кДж
1) Определяем количества оксида магния, используя формулу для нахождения количества вещества через массу.
n ( MqO ) = 120г/ 40 г/моль = 3 моль
2) Составляем пропорцию с учетом коэффициентов в уравнении реакции
Расчёты по термохимическим уравнениям
Теоретический материал представлен на страницах:
Любая химическая реакция сопровождается поглощением или выделением энергии. Термохимические уравнения показывают соотношение между кол-вом веществ, вступающих в реакцию, и кол-вом энергии, которую выделяют, либо поглощают эти вещества в процессе химической реакции.
Главное отличие термохимического уравнения от молекулярного заключается в том, что кроме формул и коэффициентов, в нем указывается еще и кол-во энергии (теплоты реакции), относящееся к числу молей реагирующих веществ, соответствующему коэффициентам в уравнении реакции.
Теплота реакции (тепловой эффект) обозначается буквой Q (измеряется в кДж), и записывается в конце уравнения. Знак «плюс» перед числом обозначает выделившееся кол-во энергии, знак «минус» — кол-во поглощенной энергии.
Реакции, протекающие с выделением энергии, называются экзотермическими; с поглощением энергии — эндотермическими.
Если известна масса одного из двух реагирующих веществ, на основе термохимического уравнения можно определить кол-во теплоты реакции.
Пример 1 . Определить теплоту реакции горения 320 г серы.
- Согласно уравнения реакции, при сгорании 1 моля серы выделяется 297 кДж энергии, нам надо узнать, сколько энергии выделится при сгорании 320 г серы.
- Для решения задачи необходимо составить и решить простую пропорцию:
- Переходим от молей к граммам:
- В пропорции заменяем моли на граммы:
Если известно кол-во выделенной (поглощенной) теплоты в ходе реакции, можно определить массы прореагировавших веществ.
Пример 2 . Определить кол-во сгоревшего угля, если в ходе горения было выделено 33520 кДж энергии.
- Согласно уравнения реакции, при сгорании 1 моль углерода (масса 1 моль С = 12 г) выделилсь 402,24 кДж энергии.
- Составляем и решаем пропорцию:
Пример 3 . При горении 1 л метана (н.у) выделяется 39 кДж энергии. Составить термохимическое уравнение реакции и вычислить тепловой эффект.
Пример 4 . При горении 2,4 г магния (н.у) выделяется 60,12 кДж энергии. Составить термохимическое уравнение реакции.
Пример 5 . Два моля аммиака образуются в результате взаимодействия 1 моля азота с тремя молями водорода. Необходимо составить уравнение термохимической реакции, в ходе которой выделяется 92 кДж тепла, а все вещества, участвующие в реакции, являются газами.
Это очень простая задача, решение которой указано в условии.
Второй вариант записи термохимического уравнения.
Пример 6 . Составить термохимическое уравнение эндотермической реакции образования двухвалентного оксида азота из азота и кислорода с поглощением 180 кДж энергии. Записать это уравнение для образования 1 моля NO.
Первая часть задания не вызывает трудностей:
В этом термохимическом уравнении 2 моля оксида азота образуется при взаимодействии 1 моля азота и 1 моля кислорода. Для того, чтобы переписать данное уравнение для 1 моля оксида азота, необходимо все коэффициенты и кол-во теплоты разделить на 2:
Пример 7 . При образовании 50 г карбоната кальция (CaCO3) выделилось 80 кДж энергии. Определить тепловой эффект реакции разложения одного моля карбоната кальция.
- Определяем кол-во энергии, выделяемое при образовании 1 моля CaCO3 (М(CaCO3)=100 г/моль):
- Термохимическое уравнение реакции образования 1 моль карбоната кальция имеет вид:
- Термохимическое уравнение реакции разложения 1 моль карбоната кальция имеет вид:
- Q=-160 кДж
Пример 8 . Рассчитать кол-во выделенной энергии при образовании 2 л аммиака при н.у.
- Согласно термохимического уравнения — 1 моль аммиака образовался из полумоля азота и полутора молей водорода. Составляем пропорцию:
Пример 9 . Рассчитать тепловой эффект реакции:
- На основании первого следствия из закона Гесса:
- Теплоты образования простых веществ равны нулю:
- Теплоты образования сложных веществ берем из таблицы:
- Подставляем числовые значения в уравнение:
- Термохимическое уравнение реакции будет иметь вид:
Пример 10 . Рассчитать тепловой эффект реакции:
- Тепловой эффект реакции будем рассчитывать по формуле, вытекающей из второго следствия закона Гесса:
- Тепловые эффекты сгорания C2H4 и C2H6 можно взять из приведенных выше термохимический уравнений.
- Тепловой эффект сгорания водорода можно вычислить из термохимического уравнения образования 1 моля воды (теплоту образования воды берем из таблицы):
- Подставляем численные значения в формулу:
- Термохимическое уравнение реакции будет иметь вид:
Пример 11 . Определить скорость изменения реакции синтеза аммиака при а) увеличении концентрации исходных веществ в 2 раза; б) уменьшении давления в реакционной смеси в 2 раза:
- Записываем кинетическое уравнение данной реакции:
- Если концентрации исходных веществ будут увеличены в 2 раза, кинетическое уравнение примет вид:
- Составляем отношение и решаем его:
- Увеличение концентрации исходных веществ в 2 раза приведет к ускорению скорости реакции в 16 раз.
- Исходя из того факта, что концентрации газов пропорциональны давлению (при уменьшении давления в 2 раза концентрации также уменьшатся в 2 раза), логично предположить, что при снижении в 2 раза давления скорость протекания реакции снизится в 16 раз. Убедимся в этом, составив соотношение кинетических уравнений.
- Исхдное кинетическое уравнение:
- Для удобства чтения формул сделаем подстановку:
- Кинетическое уравнение при снижении давления в 2 раза:
- Соотошение:
- При уменьшении давления в реакционной смеси в 2 раза скорость протекания реакции уменьшится в 16 раз.
Пример 12 . Определить скорость изменения реакции с температурным коэффициентом 4 (γ=4) при повышении температуры с 10°C до 30°C.
Для решения задачи воспользуемся правилом Вант-Гоффа, которое выражается следующей математической формулой:
Все, что нам нужно сделать — подставить численные значения в формулу и провести расчеты:
При повышении температуры с 10 до 30 градусов Цельсия скорость реакции увеличится в 16 раз.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
источники:
http://himekoscho.ucoz.ru/load/termokhimicheskie_uravnenija/27-1-0-130
http://prosto-o-slognom.ru/chimia_primery/005-termochimicheskie_uravneniya.html
Вам понадобится:
- значение массы
- Значение скорости
- Значение силы
- Время
#1
Кроме школьных уроков физики, такие задачи запросто могут пригодиться в жизни. К примеру, нужно точно рассчитать массу груза без использования весов на складе, или точно вычислить время, за которое груз будет перенесен и скорость, с которой будет совершено это действие. Решить задачу такого рода можно только с помощью использовании второго закона Ньютона. Именно базовый закон динамики позволяет нам узнать, как найти массу, зная скорость. Второй закон Ньютона гласит, что сила равна произведению массы на ускорение, где сила измеряется в Ньютонах, масса в килограммах, а ускорение — в метрах на секунду в квадрате.
#2
Естественно, что для того, чтобы найти неизвестный множитель, нужно разделить на известный множитель. В таком случае, масса будет равна частному от деления силы на ускорение. Левую часть уравнения будет довольно просто рассчитать, ведь абсолютно все догадаются, как рассчитать массу вещества с помощью весов. Далее нам нужно заменить неизвестную величину каким-либо отношением с известными величинами. Мы можем запросто заменить ускорение частным от деления скорости на время, ведь скорость мы знаем изначально, а время мы можем запросто засечь с помощью секундной стрелки часов.
#3
Если предмет полый, то имеет смысл также узнать, как определить массу воздуха внутри него, потому что порой это может немного изменить окончательные подсчеты. Стоит помнить, что если или время посчитано в минутах, или скорость задана в километрах в час, то все это нужно перевести в стандартную международную систему измерения СИ, по которой время измеряется в секундах, скорость в метрах в секунду, а масса, как физическая величина, измеряется в килограммах. Из m=F/a и a=V/t в случае подстановки второй формулы в первую следует, что m=F/V/t, а следовательно мы можем получить m=Ft/V, благодаря правилу деления на дробь.
#4
Далее, чтобы найти массу предмета нужно просто подставить заранее переведенные в общую систему значения силы, времени и скорости и решить это уравнение относительно m. Массы чрезмерно малых предметов вычисляются совсем по-другому. Например, если нужно узнать, как найти массу ядра атома какого-либо вещества, то стоит обратиться за значением к периодической таблице Менделеева. Но для всех предметов, больших чем атомы и молекулы, действует способ описанный выше, который еще в далеком семнадцатом веке открыл великий физик Исаак Ньютон.