Условие задачи:
Определить молярную массу газа, если его плотность при нормальных условиях равна 0,09 кг/м3.
Задача №4.1.16 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
(rho=0,09) кг/м3, (M-?)
Решение задачи:
Запишем уравнение Клапейрона-Менделеева:
[pV = frac{m}{M}RT;;;;(1)]
Плотность газа (rho), как и любого другого вещества, находят по формуле:
[rho = frac{m}{V}]
Тогда формула (1) примет следующий вид:
[p = frac{rho }{M}RT]
Выразим отсюда искомую молярную массу газа (M):
[M = frac{{rho RT}}{p}]
Напомним, что при нормальных условиях давление (p) равно 100 кПа, а температура (T) – 0° C или 273 К.
Универсальная газовая постоянная равна 8,31 Дж/(моль·К).
Считаем ответ:
[M = frac{{0,09 cdot 8,31 cdot 273}}{{100 cdot {{10}^3}}} = 0,002;кг/моль = 2;г/моль]
По полученной молярной массе легко догадаться, что это водород H2.
Ответ: 2 г/моль.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
4.1.15 В лабораторных условиях создан высокий вакуум, то есть очень малое давление
4.1.17 Найти число молекул в 2 кг углекислого газа
4.1.18 Во сколько раз масса молекулы углекислого газа CO2 больше массы молекулы аммиака NH3
Найти массу, плотность или объем онлайн
На данной странице калькулятор поможет найти плотность, массу или объем вещества онлайн. Для расчета введите значения в калькулятор.
Объем, масса и плотность
Найти
Масса:
Объем:
Плотность:
Ответы:
Формула для нахождения массы тела через плотность и объем:
m — масса; V — объем; p — плотность.
Формула для нахождения объема тела через плотность и массу:
m — масса; V — объем; p — плотность.
Формула для нахождения плотности тела через объем и массу:
m — масса; V — объем; p — плотность.
Калькулятор
Масса через плотность и объем, формула
Масса тела выражается через плотность и объем следующей формулой:
Масса тела — есть произведение плотности вещества из которого состоит тело на его объем.
[ m = ρV ]
Здесь:
V — объем тела (м³),
m — масса тела, (килограмм),
ρ — плотность вещества, (кг/м³).
Вычислить, найти массу твердых тел или жидкостей через плотность и объем по формуле (1)
Выберите вещество ▼
| ρ (плотность вещества, x103 кг/м³) |
| V (объем тела, м³) |
Вычислить
нажмите кнопку для расчета
Вычислить, найти массу газа через плотность и объем по формуле (1)
Выберите вещество ▼
| ρ (плотность газа, кг/м³) |
| V (объем газа, м³) |
Вычислить
нажмите кнопку для расчета
Масса через плотность и объем |
стр. 443 |
|---|
Формула массы через плотность и объем является одной из базовых формул физики, изучаемых в рамках школьной программы еще в седьмом классе. Она пригодится в решении многих задач.
Формула зависимости массы от объема и плотности
Для того, чтобы найти плотность жидкости или твердого вещества, существует базовая формула: плотность равна массе, поделенной на объем.
Записывается это так:
ρ = m / V
И из нее можно вывести еще две формулы.
Формулу для объема тела:
V = m / ρ
А также формулу для расчета массы:
m = V * ρ
Как видите, запомнить последнюю очень легко: это единственная формула, где две единицы нужно умножить.
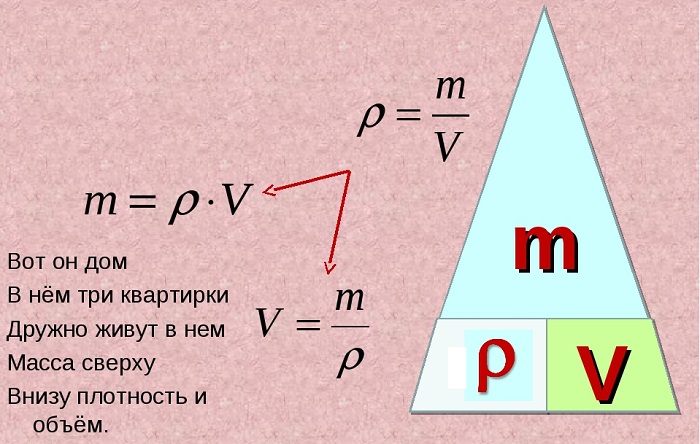
Для запоминания этой зависимости можно использовать рисунок в виде «пирамидки», разделенной на три секции, в вершине которой находится масса, а в нижних углах – плотность и объем.
Несколько иначе обстоят дела с газами. Рассчитать их вес гораздо сложнее, так как у газов нет постоянной плотности: они рассеиваются и занимают весь доступный им объем.
Для этого пригодится понятие молярной массы, которую можно найти, сложив массу всех атомов в формуле вещества при помощи данных из периодической таблицы.
Вторая единица, которая нам понадобится – количество вещества в молях. Его можно вычислить по уравнению реакции. Подробнее об этом можно узнать в рамках курса химии.
Другой способ нахождения мольного количества – через объем газа, который нужно поделить на 22,4 литра. Последнее число – это объемная постоянная, которую стоит запомнить.
В итоге, зная две предыдущие величины, мы можем определить массу газа:
m = n * M,
где M – это молярная масса, а n – количество вещества.
Результат получится в граммах, поэтому для решения физических задач важно не забыть перевести его в килограммы, поделив на 1000. Числа в этой формуле часто могут оказываться достаточно сложными, поэтому для вычислений может понадобиться калькулятор.
Еще один нестандартный случай, с которым можно столкнуться – необходимость найти плотность раствора. Для этого существует формула средней плотности, построенная аналогично формулам других средних величин.
Для двух веществ посчитать ее можно так:
(m1 + m2) / V1 + V2.
Также из этой формулы можно вывести несколько других в зависимости от того, какие из величин известны по условию задачи.
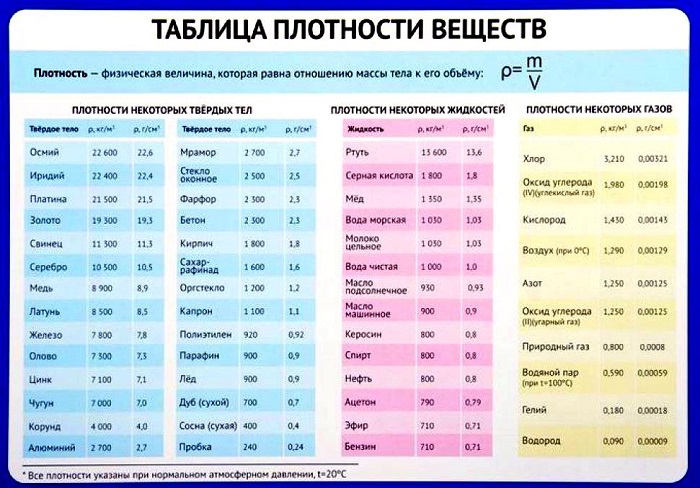
Таблица плотности некоторых веществ
Плотность многих веществ известна заранее и легко находится по соответствующей таблице.
В работе с ней важно обращать внимание на размерности и не забывать о том, что все данные собраны при нормальных условиях: комнатной температуре в 20 градусов Цельсия, а также определенном давлении, влажности воздуха и так далее.
Плотности других, более редких веществ можно найти онлайн.
Как минимум одно из значений плотности стоит запомнить, так как оно часто появляется в задачах. Это плотность воды – 1000 кг/м3 или 1 г/см3.
Примеры решения задач
Задача 1
Условие: имеется алюминиевый брусок со сторонами 3, 5 и 7 сантиметров. Какова его масса?
Решение:
Найдем объем бруска:
V = a * b * c;
V = 3 * 5 * 7 = 105 см3;
Табличное значение плотности алюминия: 2800 кг/м3 или 2,8 г/см3;
Вычислим массу бруска:
m = V * ρ;
m = 105 * 2,8 = 294 г.
Ответ: m = 294 г.
Задача 2
Задача по смежной теме.
Условие: сколько энергии потребуется для того, чтобы довести воду комнатной температуры (20 градусов Цельсия) из стакана (ёмкость 200 мл) до температуры кипения?
Решение:
Найдем недостающую информацию: температура кипения воды t2 = 100 градусов Цельсия, удельная теплоемкость воды с = 4200 Дж/кг * С, плотность воды 1 г/см3, 1 мл воды = 1 см3;
Найдем массу воды:
m = V * ρ;
m = 200 * 1 = 200 г = 0,2 кг;
Найдем энергию:
Q = c * m * (t2 – t1);
Q = 4200 * 0,2 * (100 – 20) = 67200 Дж = 67,2 кДж.
Ответ: Q = 67,2 кДж.
Задача 3
Задача с молярной массой.
Условие: найдите массу CO2 при объеме в 5,6 л.
Решение:
Найдем молярную массу CO2 :
M = 12 + 16 * 2 = 44 г/моль;
Найдем количество вещества через объем:
n = 5,6 / 22,4 = 0,25 моль;
Найдем массу:
m = n * M;
m = 0,25 * 44 = 11 г.
Ответ: m = 11 г.
давления (1-е за единицу)
1 2,5 4
плотности (1-я за единицу)
1 2,53 4,1
рост плотности от давления отличается от линейной зависимости (и в условии оговорено, что газ не идеальный) значит надо брать не Клайперона, а Ван-дер-Ваальса или какую-нибудь экзотику вроде Дитеричи или Бертло, но в двух последних вместо молярной массы или молярного объёма фигурируют совсем другие характеристики газа.
Так что придётся к Ван-дер-Ваальсу обращаться. Там под V фигурирует молярный обём (молярная масса, делённая на плотность), но получается система из трёх уравнений, причём молярный объём аж в кубе
(p+a/V^2) (V-b) = RT. Молярную массу обозначу за M, плотность за ro
pM^3/ro^3 — bpM^2/ro^2 + aM/ro — ab — RTM^2/ro^2 =0 и так три раза для разных (но известных) p и ro.
u,w,x,y,z константы, которые можно вычислить
u1 M^3 — b w1 M^2 + a x1 M -ab -y1 M^2 = 0
u2 M^3 — b w2 M^2 + a x2 M -ab -y2 M^2 = 0
u3 M^3 — b w3 M^2 + a x3 M -ab -y3 M^2 = 0
можно из первого вычесть второе, из второго третье, из третьего первое, член ab исчезнет
a и b линейно входят, можно из первого ур-я выразить а через b и M, из второго, подставив а, выразить b через M, в третьем уже избавиться от а и b, получив что-то жуткое относительно M, но вполне считаемое численными методами.
То есть молекулярную массу узнать можно, но «почему-то» не хочется.
По одной молекулярной массе узнать газ. Может можно, может нет, зависит от конкретной массы, а если смесь, то вообще говорить не о чем.
СO2 -> 12+2*16=44
С3 H8 -> 12*3 +8 = 44
Учитывая наработки авторов предыдущих ответов, я бы выбрал молярную массу кислорода, но двухатомные газы почти идеальные. Значит надо взять многоатомный с той же молярной массой. Однозначно подходит метанол. Муравьиный спирт не в водном растворе и так должен быть газообразным, а уж при давлениях меньше атмосферы тем более.