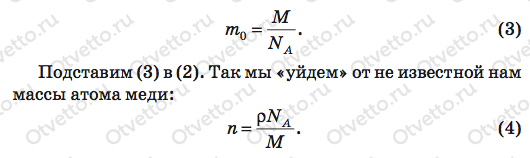|
Какая атомная масса у меди?kohno более года назад
Абдигапар более года назад Чтобы определить атомную массу меди сначала найдем по таблице Менделеева относительную атомную массу меди.ArCu = 63,546. Далее используя число Авогадро определяем массы одного атома: 63,546/6,022*10^23 = 10,55*10^-23 = 1,055*10^-22 г. Ответ: 1,055*10^-22 г комментировать
в избранное
ссылка
отблагодарить Руслан Кипер более года назад Атомную массу меди можно посмотреть в таблице Менделеева. Там ее значение 63,546 атомных единиц массы. В школьных учебниках ее часто сокращают до 64 а.е.м., а при более точных расчетах берут 63,5 а.е.м. комментировать
в избранное
ссылка
отблагодарить Знаете ответ? |
Refer to the explanation.
In order to determine the mass of one atom of an element, you must determine its molar mass, which is its atomic weight on the periodic table in g/mol, and you need to know the relationship between moles and the number of atoms: #»1 mol of atoms»# = #6.022xx10^23# #»atoms»#. Then divide the molar mass by #6.022xx10^23# #»atoms/mol»#.
Example:
What is the mass of one copper #(«Cu»)# atom?
Solution:
The atomic weight of copper is #»63.456 u»#, so its molar mass is #»63.456g/mol»#.
Divide the molar mass by #6.022xx10^23# #»atoms/mol»#.
#(63.456″g»/color(red)cancel(color(black)(«mol»)))/(6.022xx10^23″atoms»/color(red)cancel(color(black)(«mol»)))=1.054xx 10^(-22)# #»g/atom»#
The mass of one Cu atom is #1.054xx10^(-22)# #»g»#.
Не знаю как выше у человека столько получилось, по-моему так решается все это:
V=m/M=N/Na — колличество вещества равно массе вещества деленной на молярную массу вещества, равно числу атомов деленное на число авогадро.
Отсюда получаем что масса атомов равна: m=M*N/Na
Следовательно масса одного амтома: m=64*1/6.02*20^23= 10.63 * 10 ^ -23 грамма
Ну в кг то будет 10.63 * 10 ^ -26 кг
Или вот вариант решения через пропорцию, если так вам легче будет:
Mr(Cu) — Na
m(X) — N
m(1атома) = 64*1/6,02*10^23 = 10.6312*10^-23 грамм
2021-12-17
Какова масса меди, если в ней содержится 1 г электронов (масса электрона составляет 1/1840 а. е. м.)?
Решение:
Составим последовательный план решения задачи: масса одной атомной единицы массы (в граммах) $rightarrow$ масса одного электрона (в граммах) $rightarrow$ число электронов, масса которых составляет 1 г $rightarrow$ число атомов $Cu (n)$, содержащее это число электронов $rightarrow$ число молей $Cu$, содержащих $n$ атомов $Cu$ $rightarrow$ масса $Cu$ (в граммах), содержащая 1 г электронов.
1) Рассчитаем массу 1 а. е. м. (в граммах). Для этого сначала рассчитаем массу одного атома углерода $^{12} C$:
масса $6,02 cdot 10^{23}$ атомов углерода $^{12} C$ равна 12 г
масса 1 атома углерода $^{12} C$ равна $x$ г
Составляем пропорцию:
$6,02 cdot 10^{23} : 12 = 1:x$, отсюда $x =| frac{12}{6,02 cdot 10^{23}} г$
Далее по определению «углеродной» единицы (1 а. е. м. равна 1/12 массы атома углерода $^{12} C$) имеем:
$1 а. е. м. = frac{1}{12} cdot frac{12 г}{6,02 cdot 10^{23}} = frac{1}{6,02 cdot 10^{23}} г$
2) Рассчитаем массу 1 электрона (в граммах), исходя из условия задачи:
$m (bar{e}) = frac{1}{1840} frac{1}{6,02 cdot 10^{23} } г$
3) Определим число электронов массой 1 г:
масса 1 электрона составляет $frac{1}{1840 cdot 6,02 cdot 10^{23} } г$
масса $y$ электронов составляет 1 г
$y = 1840 cdot 6,02 cdot 10^{23}$ электронов
4) Определим число атомов меди ($n$), содержащих в себе $y$ электронов. Порядковый номер меди — 29, следовательно, 1 атом содержит 29 электронов.
1 атом $Cu$ содержит 29 электронов
$n$ атомов $Cu$ содержат $1840 cdot 6,02 cdot 10^{23}$ электронов
Решаем пропорцию, получаем:
$n = frac{1840 cdot 6,02 cdot 10^{23} }{29}$ атомов $Cu$
5) Определим количество вещества меди $z$ (в молях), содержащее $n$ атомов меди:
1 моль $Cu$ содержит $6,02 cdot 10^{23}$ атомов $Cu$
$z$ моль $Cu$ содержат $frac{1840 cdot 6,02 cdot 10^{23}}{29}$ атомов $Cu$
Решим пропорцию, получим:
$z = frac{1840}{29} моль$
6) Определим, наконец, какая масса меди содержит 1 г электронов:
масса 1 моль $Cu$ составляет 64 г
масса $frac{1840}{29}$ моль $Cu$ составляет $m$ г
$1:64 = frac{1840}{29} : m; m = frac{1840 cdot 64}{29} = 4070; m = 4070 г$
Ответ: 4,07 кг меди содержат 1 г электронов.
Задача: Определить число атомов в 1 м3 меди. Молярная масса меди М = 0,0635 кг/моль, ее плотность ρ = 900 кг/м3.
Пояснение: Обозначим V объем меди, M — ее молярную массу, ρ — плотность меди, m0 — массу каждого атома, NA — число Авогадро, N — число атомов меди в объеме V.
Концентрацию атомов n найдем, разделив плотность меди ρ , т.е. массу единицы объема меди, на массу каждого атома меди m0:
Массу каждого атома меди определим, разделив массу атомов в одном моле, т.е. ее атомную массу М, на число атомов в одном моле, т.е. на число Авогадро NА:
Теперь подставим правую часть равенства (4) вместо концентрации n в формулу (1). Так мы решим задачу в общем виде:
Ответ: N = 8,5 · 1027.