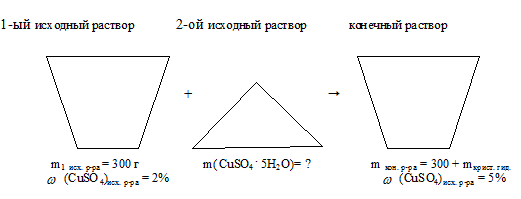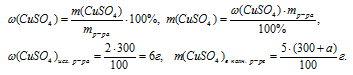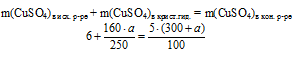Кристаллогидраты — это сложные вещества, которые содержат в кристаллической решетке молекулы воды.
Многие соединения (чаще всего соли) выкристаллизовываются из водных растворов в виде кристаллогидратов.
Например, медный купорос:
CuSO4·5H2O
Кристаллогидраты растворяются в воде, при этом протекают сложные физико-химические процессы, но, если говорить про конечный результат, вещество диссоциирует, а кристаллизационная вода отделяется и попадает в раствор. Условно процесс растворения можно записать в виде уравнения:
CuSO4·5H2O → CuSO4 + 5H2O
Но в ЕГЭ по химии лучше не записывать растворение кристаллогидрата, как химическую реакцию!
Названия кристаллогидратов, которые могут встретиться в ЕГЭ по химии:
CuSO4·5H2O — медный купорос, пентагидрат сульфата меди (II)
Na2CO3 × 10H2O — кристаллическая сода, декагидрат карбоната натрия
ZnSO4 × 7H2O — цинковый купорос, гептагидрат сульфата цинка
Как решать задачи на кристаллогидраты?
Рассмотрим приемы, которые можно использовать при решении задач на кристаллогидраты, на примере.
1. В 300 мл воды растворили 7,6 г CuSO4·5H2O (медного купороса). Определите массовую долю CuSO4 в образовавшемся растворе.
Для определения массы соли в составе кристаллогидрата по массе кристаллогидрата можно использовать два способа.
Первый способ.
В составе кристаллогидрата медного купороса на одну частицу кристаллогидрата приходится одна частица сульфата меди (II). На две частицы кристаллогидратов тогда приходится две частицы сульфата меди и т.д. Аналогично на 1 порцию (моль) частиц кристаллогидрата приходится 1 порция (1 моль) частиц сульфата меди (II).
То есть молярное соотношение (отношение количества вещества) кристаллогидрата CuSO4·5H2O и сульфата меди (II) равно CuSO4 1:1
n(CuSO4·5H2O):n(CuSO4) = 1:1
Или:
n(CuSO4·5H2O) = n(CuSO4)
Находим молярные массы гидрата и сульфата меди (II):
М(CuSO4·5H2O) = 64 + 32 + 64 + 5·18 = 250 г/моль
М(CuSO4) = 64 + 32 + 64 = 160 г/моль
Количество вещества кристаллогидрата:
n(CuSO4·5H2O) = m/M = 7,6/250 = 0,0304 моль
n(CuSO4) = n(CuSO4·5H2O) = 0,0304 моль
Масса сульфата меди в составе кристаллогидрата:
m(CuSO4) = M·n = 160 г/моль·0,0304 моль = 4,864 г
Второй способ.
Определим массовую долю сульфата меди в составе кристаллогидрата:
ω(CuSO4) = М(CuSO4)/М(CuSO4·5H2O) = 160 г/моль/250 г/моль = 0,64 или 64%
Тогда массу сульфата меди в образце кристаллогидрата массой 7,6 г можно определить, зная массовую долю сульфата меди:
m(CuSO4) = ω(CuSO4) · m(CuSO4·5H2O) = 0,64 · 7,6 г = 4,864 г
Масса исходной воды:
m(H2O) = ρ·V = 1 г/мл · 300 мл = 300 г
Массу раствора сульфата меди (II) находим по принципу материального баланса: складываем все материальные потоки, которые пришли в систему, вычитаем уходящие материальные потоки.
mр-ра(CuSO4) = m(CuSO4·5H2O) + m(H2O) = 7,6 г + 300 г = 307,6 г
Массовая доля сульфата меди (II) в конечном растворе:
ω(CuSO4) = m(CuSO4)/mр-ра(CuSO4) = 4,864 г/307,6 г = 0,0158 или 1,58%
Ответ: ω(CuSO4) = 0,0158 или 1,58%
2. Какую массу железного купороса (FeSO4•7H2O) надо взять, чтобы приготовить 1,25 л раствора сульфата железа с массовой долей 9%, если плотность этого раствора 1,086 г/мл?
Масса конечного раствора сульфата железа:
mр-ра(FeSO4) = ρ·V = 1,086 г/мл·1250 мл = 1357,5 г
Масса сульфата железа в этом растворе:
m(FeSO4) = ω(FeSO4) · mр-ра(FeSO4) = 1357,5 г · 0,09 = 122,175 г
n(FeSO4) = m(FeSO4)/M(FeSO4) = 122,175 г/152 г/моль = 0,804 моль
Молярное соотношение (отношение количества вещества) кристаллогидрата FeSO4•7H2O и сульфата железо (II) равно FeSO4 1:1
n(FeSO4•7H2O):n(FeSO4 ) = 1:1
Отсюда:
n(FeSO4•7H2O) = n(FeSO4 ) = 0,804 моль
Масса кристаллогидрата:
m(FeSO4•7H2O) = n(FeSO4•7H2O) · M(FeSO4•7H2O) = 0,804 моль · 278 г/моль = 223,45 г
Ответ: m(FeSO4•7H2O) = 223,45 г
3. В растворе хлорида алюминия с ω(AlCl3) = 2% растворили 100 г кристаллогидрата AlCl3·6H2O. Вычислите, какой стала массовая доля AlCl3 в полученном растворе, если объём раствора 1047 мл, а его плотность 1,07 г/мл.
Масса конечного раствора хлорида алюминия:
mр-ра,2(AlCl3) = ρ·V = 1,07 г/мл·1047 мл = 1120,29 г
Тогда масса исходного раствора хлорида аммония:
mр-ра,1(AlCl3) = mр-ра,2(AlCl3) – m(AlCl3·6H2O) = 1120,29 г – 100 г = 1020,29 г
Масса хлорида алюминия в исходном растворе:
m1(AlCl3) = ω1(AlCl3) · mр-ра,1(AlCl3) = 0,02 · 1020,29 г = 20,4 г
Массовая доля хлорида алюминия в кристаллогидрате:
ω(AlCl3) = М(AlCl3)/М(AlCl3·6H2O) = 133,5 г/моль/241,5 г/моль = 0,5528 или 55,28%
Масса хлорида алюминия в кристаллогидрате:
mв к/г(AlCl3) = ω(AlCl3) · m(AlCl3·6H2O) = 100 г · 0,5528 = 55,28 г
Общая масса хлорида алюминия в конечном растворе:
m2(AlCl3) = mв к/г(AlCl3) + m1(AlCl3) = 55,28 г + 20,4 г = 75,68 г
Массовая доля хлорида алюминия в конечно растворе:
ω2(AlCl3) = m2(AlCl3)/mр-ра,2(AlCl3) = 75,68 г/1120,29 г = 0,068 или 6,8%
Ответ: ω2(AlCl3) = 0,068 или 6,8%
4. Вычислите массы FeSO4·7H2O (железного купороса) и воды, необходимые для приготовления 500 г раствора с массовой долей FeSO4 7%.
Ответ: m(FeSO4·7H2O) = 64 г; m(H2O) = 436 г.
5. Вычислите объём воды и массу кристаллогидрата Na2SO4·10H2O (глауберовой соли), которые требуются для приготовления 500 г раствора с массовой долей Na2SO4 15%.
Ответ: m(Na2SO4·10H2O) = 170,45 г; V(H2O) = 329,55 мл.
6. Какую массу кристаллогидрата Na2SO4·10H2O необходимо растворить в 400 мл воды, чтобы получить раствор с ω(Na2SO4) = 10%?
7. Нужно приготовить 320 г раствора с ω(CuSO4) = 12%. Рассчитайте массу кристаллогидрата CuSO4·5H2O и массу раствора с ω1(CuSO4) = 8%, которые потребуются для приготовления заданного раствора.
Ответ: m(CuSO4·5H2O) = 22,86 г; m8% р-ра = 297,14 г.
8. Вычислите, какую массу кристаллогидрата AlCl3·6H2O нужно растворить в 1 кг раствора хлорида алюминия с массовой долей AlCl3 2%, чтобы получить раствор с массовой долей AlCl3 3%.
Ответ: m(AlCl3·6H2O) = 19,2 г.
9. Сколько граммов кристаллогидрата Na2SO4·10H2O необходимо добавить к 100 мл раствора сульфата натрия с массовой долей Na2SO4 8% и плотностью 1,07 г/мл, чтобы удвоить массовую долю Na2SO4 в растворе?
Ответ: m(Na2SO4·10H2O) = 30,6 г.
10. Какую массу CuSO4·5H2O (медного купороса) нужно растворить в 1 кг раствора сульфата меди(II) с массовой долей CuSO4 5%, чтобы получить раствор с массовой долей CuSO4 10%?
Ответ: m(CuSO4·5H2O) = 92,6 г.
11. Вычислите массу CuSO4·5H2O (медного купороса), необходимую для приготовления 5 л раствора с массовой долей CuSO4 8% (плотность раствора 1,084 г/мл)? Рассчитайте молярную концентрацию CuSO4 в этом растворе.
Ответ: m(CuSO4·5H2O) = 677,5 г; c(CuSO4) = 0,54 моль/л.
12. Массовая доля кристаллизационной воды в кристаллогидрате сульфата натрия (Na2SO4·xH2O) составляет 55,9%. Определите формулу кристаллогидрата. Вычислите массовую долю сульфата натрия в растворе, полученном при
растворении 80,5 г данного кристаллогидрата в 2 л воды.
Ответ: Na2SO4·10H2O; ω(Na2SO4) = 1,7%.
13. К раствору сульфата железа(II) с массовой долей FeSO4 10% добавили 13,9 г кристаллогидрата этой соли. Получили раствор массой 133,9 г, с массовой долей FeSO4 14,64%. Определите формулу кристаллогидрата.
14. После растворения 13,9 г кристаллогидрата сульфата железа(II) (FeSO4·xH2O) в 86,1 г воды массовая доля FeSO4 в растворе оказалась равной 7,6%. Определите формулу кристаллогидрата.
15. При охлаждении 200 мл раствора сульфата магния с ω(MgSO4) = 24% (плотность раствора 1,270 г/мл) образовался осадок кристаллогидрата MgSO4·7H2O массой 61,5 г. Определите массовую долю MgSO4 в оставшемся
растворе.
Ответ: ω2(MgSO4) = 12,73%.
16. При охлаждении 400 мл раствора сульфата меди(II) с массовой долей CuSO4 25% (плотность раствора 1,19 г/мл) образовался осадок кристаллогидрата CuSO4·5H2O массой 50 г. Определите массовую долю CuSO4 в оставшемся растворе.
17. При охлаждении 500 г раствора сульфата железа(II) с массовой долей FeSO4 35% выпало в осадок 150 г кристаллогидрата FeSO4·7H2O. Определите массовую долю FeSO4 в оставшемся растворе.
18. Медный купорос (CuSO4 × 5H2O) массой 25 г растворили в воде и получили раствор с массовой долей соли 10%. К этому раствору добавили 8,4 г железа и после завершения реакции ещё 100 г 9,8%-ного раствора серной кислоты. Определите массовую долю соли в полученном растворе.
19. Медный купорос (CuSO4 × 5H2O) массой 100 г растворили в воде и получили раствор с массовой долей соли 20%. К этому раствору добавили 32,5 г цинка и после завершения реакции ещё 560 г 40%-ного раствора гидроксида калия. Определите массовую долю гидроксида калия в полученном растворе.
20. К 20%-ному раствору соли, полученному при растворении в воде 50 г медного купороса (CuSO4 × 5H2O), добавили 14,4 г магния. После завершения реакции к полученной смеси прибавили 146 г 25%-ного раствора хлороводородной кислоты. Определите массовую долю хлороводорода в образовавшемся растворе. (Процессами гидролиза пренебречь.)
21. Нитрид натрия массой 8,3 г растворили в 490 г 20%-ного раствора серной кислоты. К полученному раствору добавили 57,2 г кристаллической соды (Na2CO3 × 10H2O). Определите массовую долю кислоты в конечном растворе. Учитывать образование только средних солей.
22. Медный купорос (CuSO4 × 5H2O) массой 12,5 г растворили в воде и получили раствор с массовой долей соли 20%. К этому раствору добавили 5,6 г железа и после завершения реакции еще 117 г 10%-ного раствора сульфида натрия. Определите массовую долю сульфида натрия в конечном растворе.
23. Медный купорос (CuSO4 × 5H2O) массой 37,5 г растворили в воде и получили раствор с массовой долей соли 20%. К этому раствору добавили 11,2 г железа и после завершения реакции ещё 100 г 20%-ного раствора серной кислоты. Определите массовую долю соли в полученном растворе.
24. При растворении в воде 57,4 г цинкового купороса (ZnSO4 × 7H2O) получили 20%-ный раствор соли. К полученному раствору добавили 14,4 г магния. После завершения реакции к полученной смеси прибавили 292 г 25%-ного раствора хлороводородной кислоты. Определите массовую долю кислоты в образовавшемся растворе. (Процессами гидролиза пренебречь.)
25. При растворении 25 г медного купороса (CuSO4 × 5H2O) в воде был получен 20%-ный раствор соли. К этому раствору добавили измельчённую смесь, образовавшуюся в результате прокаливания порошка алюминия массой 2,16 г с оксидом железа(III) массой 6,4 г. Определите массовую долю сульфата меди(II) в полученном растворе.
26. При растворении в воде 57,4 г цинкового купороса (ZnSO4 × 7H2O) получили 10%-ный раствор соли. К полученному раствору добавили 14,4 г магния. После завершения реакции к полученной смеси прибавили 240 г 30%-ного раствора гидроксида натрия. Определите массовую долю гидроксида натрия в образовавшемся растворе. (Процессами гидролиза пренебречь.)
27. Свинцовый сахар ((CH3COO)2Pb × 3H2O) массой 37,9 г растворили в воде и получили 10%-ный раствор соли. К этому раствору добавили 7,8 г цинка и после завершения реакции добавили еще 156 г 10%-ного раствора сульфида натрия. Определите массовую долю сульфида натрия в конечном растворе.
28. Медный купорос (CuSO4 × 5H2O) массой 25 г растворили в воде и получили раствор с массовой долей соли 10%. К этому раствору добавили 19,5 г цинка и после завершения реакции ещё 240 г 30%-ного раствора гидроксида натрия. Определите массовую долю гидроксида натрия в полученном растворе.
29. При растворении в воде 114,8 г цинкового купороса (ZnSO4 × 7H2O) получили 10%-ный раствор соли. К полученному раствору добавили 12 г магния. После завершения реакции к полученной смеси прибавили 365 г 20%-ного раствора хлороводородной кислоты. Определите массовую долю кислоты в образовавшемся растворе. (Процессами гидролиза пренебречь.)
30. Медный купорос (CuSO4 × 5H2O) массой 50 г растворили в воде и получили раствор с массовой долей соли 10%. К этому раствору добавили 19,5 г цинка и после завершения реакции ещё 200 г 30%-ного раствора гидроксида натрия. Определите массовую долю гидроксида натрия в полученном растворе.
Ответ: w(NaOH) = 3,8%
31. Медный купорос (CuSO4 × 5H2O) массой 50 г растворили в воде и получили раствор с массовой долей соли 16%. К этому раствору добавили 26 г цинка и после завершения реакции ещё 320 г 20%-ного раствора гидроксида натрия. Определите массовую долю гидроксида натрия в полученном растворе.
32. Фосфид кальция массой 18,2 г растворили в 182,5 г 20%-ного раствора соляной кислоты. К полученному раствору добавили 200,2 г кристаллической соды (Na2CO3 × 10H2O). Определите массовую долю карбоната натрия в конечном растворе.
Ответ: w(Na2CO3) = 6%
Задачи на состав и определение формулы кристаллогидратов:
- Вычислите массовую долю бария в кристаллогидрате гидроксида бария, в котором число атомов водорода в 1,8 раз больше числа атомов кислорода.
- Имеется смесь равных масс гептагидрата гидрофосфата натрия и дигидрата дигидрофосфата натрия. Сколько в это смеси приходится атомов кислорода на один атом фосфора?
- Число атомов водорода, равное числу Авогадро, содержится в 21,9 г кристаллогидрата ацетата цинка. Установите формулу кристаллогидрата.
- В некоторой порции пентагидрата сульфата меди содержится 0,25 моль воды. Вычислите массу этой порции кристаллогидрата.
- В какой массе дигидрата сульфата кальция содержится число электронов, равное числу Авогадро?
- Вычислите число атомов и число электронов 14г гептагидрата сульфата никеля (II).
- Рассчитайте массу атомов водорода, содержащихся в 143 моногидрата ацетата меди.
- В некоторой порции кристаллогидрата сульфата желез (III) число атомов кислорода в 15 раз больше числа Авогадро, а число атомов железа точно соответствует числу Авогадро. Выведите формулу кристаллогидрата.
- В 0,250 моль кристаллогидрата разница между массой кристаллизационной воды и массой беводной соли равна 59,5. Массовая доля кристаллизационной воды составляет 28,83%. Вычислите относительную молекулярную массу кристаллогидрата.
- В кристаллогидрате, образованном средней солью металла, массовая доля кристаллизационной воды равна 50,0%. Вычислите массу водорода, содержащегося в 100 г этого кристаллогидрата.
- В кристаллогидрате, образованном солью бескислородной кислоты, массовая доля соли равна 0,755. Вычислите массу кислорода, содержащегося в 1.00 г этого кристаллогидрата.
- В некоторой порции кристаллогидрата ацетата магния находится 9,632∙1023 атомов углерода и 3,371∙1024 атомов водорода. Вычислите число атомов кислорода, находящихся в этой порции кристаллогидрата.
- В некоторой порции кристаллогидрата ацетата бария находится 4,816∙1023 атомов углерода и 8,428∙1023 атомов кислорода. Вычислите число атомов водорода, находящихся в этой порции кристаллогидрата.
14. В 0,250 моль дигидрата ацетата металла 2А-группы содержится 1,535∙1025 электронов. Установите, какой металл входит в состав кристаллогидрата.
Задачи на реакции с участием кристаллогидратов:
- Оксид меди (II) массой 16 г обработали 40 мл 5,0 %-го раствора серной кислоты (ρ=1,03 г/см3). Полученный раствор отфильтровали, фильтрат упарили. Определите массу полученного кристаллогидрата.
- Декагидрат карбоната натрия обработали раствором азотной кислоты массой 150 г, при этом выделилось 2,67 л углекислого газа (н.у.). Вычислите массовую долю азотной кислоты в исходном растворе.
- К сульфиду калия массой 3,30 г, находящемуся в водном растворе, добавили 0,02 моль гексагидрата хлорида меди. Вычислите массу образовавшегося осадка.
- При растворении 27,2 г смеси железа и оксида железа (II) в серной кислоте и выпаривании раствора досуха образовалось 111,2 г железного купороса — гептагидрата сульфата железа (II). Определите количественный состав исходной смеси.
- Какую массу медного купороса необходимо добавить к 150 г 12%-ного раствора гидроксида натрия, чтобы щёлочь полностью прореагировала?
- 7,5 г медного купороса (пентагидрат сульфата меди) растворили в 142,5 воды. К полученному раствору добавили 150 мл 10 %-ного раствора гидроксида калия (плотность 1,1 г/мл). Определить состав полученного раствора в массовых процентах.
- Какую массу декагидрата карбоната натрия необходимо растворить в 130 г 10%-ного раствора хлорида алюминия, чтобы полностью осадить гидроксид алюминия? Определить состав раствора (в массовых процентах) после отделения осадка.
8. В 1 л воды растворили 57,2 г кристаллической соды (декагидрат карбоната натрия). Через полученный раствор пропустили 1,12 л углекислого газа. Найти массовые доли веществ в полученном растворе.
Задачи на материальный баланс и растворы с участием кристаллогидратов:
- Медный купорос массой 12,5 г; растворили в 87,5 мл воды. Вычислите массовую долю (в %) сульфата меди (II) в полученном растворе.
- В 200 г раствора сульфата меди (II) с массовой долей соли 4% растворили 50 г медного купороса. Вычислите массовую долю (в %) сульфата меди (II) в полученном растворе.
- В 5 л воды растворили дигидрат хлорида бария массой 250 г. Вычислите массовую долю (в %) безводной соли в полученном растворе.
- В 135,6 г воды растворили глауберову соль массой 64,4 г. Рассчитайте массовую долю (в %) безводной соли в полученном растворе.
- Необходимо приготовить 2 л 0,1 М водного раствора сульфата меди (II). Какая масса медного купороса потребуется для этого?
- Выпарили досуха 0,5 л 15-процентного раствора сульфата натрия (плотность 1,14 г/см3). Вычислите массу полученных кристаллов, учитывая, что соль выделяется в виде кристаллогидрата — декагидрата сульфата натрия.
- До какого объема надо разбавить 500 мл 20-процентного раствора хлорида натрия (плотность 1,152 г/мл), чтобы получить 4,5-процентный раствор плотностью 1,029 г/мл?
- Смешали 500 мл 32 — процентного раствора азотной кислоты плотностью 1,2 г/мл и один литр воды. Вычислите массовую долю (в %) азотной кислоты в полученном растворе.
- Рассчитайте объем 25% раствора сульфата цинка (плотность 1,3 г/мл), который необходимо разбавить водой для получения 0,5 М раствора этой соли объемом 4л.
- Декагидрат карбоната натрия массой 0,05 кг растворили в воде объемом 0,15 л. Вычислите массовую долю безводной соли в полученном растворе.
- В воде объемом 0,157 м3 растворили медный купорос массой 43 кг. Вычислите массовую долю безводной соли в полученном растворе.
- Какую массу дигидрата фторида калия можно получить из 450 г 25,0%-го раствора фторида калия?
- Массовая доля безводной соли в кристаллогидрате равна 64%. Какую массу кристаллогидрата нужно взять для приготовления 150 г 50%-го раствора соли?
- В каком количестве вещества воды следует растворить 100 г декагидрата карбоната натрия для получения раствора с массовой долей соли, равной 10,0%?
- Из какой массы 25,0%-го раствора карбоната натрия выпало при охлаждении 10 г декагидрата, если в результате этого массовая доля соли в растворе уменьшилась в два раза?
- В каком объеме воды следует растворить 0,3 моль пентагидрата сульфата меди (II) для получения 12%-го раствора?
- Рассчитайте, сколько г FeSO4×7H2O и воды потребуется для приготовления 200 мл 18 мас % раствора сульфата железа (II) с плотностью 1,19 г/мл.
- Кристаллогидрат фосфата натрия Nа3РО4×12Н2О количеством вещества 1 моль растворили в 75 моль воды. Плотность получившегося раствора оказалась равной 1,098 г/мл. Вычислите молярную концентрацию ионов натрия в этом растворе.
- В 225 г 25,5%-го раствора бромида кальция растворили гексагидрат бромида кальция массой 50,0 г. Вычислите массовые доли веществ в получившемся растворе.
- Из 500 г 15,0%-го раствора сульфита натрия при охлаждении выпало 25,2 г гептагидрата сульфита натрия. Рассчитайте массовую долю соли в полученном растворе.
- Из 250 г 17,0%-го раствора карбоната натрия при охлаждении выпало 28,6 г декагидрата карбоната натрия. Рассчитайте массовую долю соли в полученном растворе.
- В 20,0 г 5,00%-го раствора гидроксида натрия растворили 4 г тетрагидрата гидроксида натрия, при этом плотность полученного раствора стала равной 1,11 г/мл. Вычислите молярную концентрацию полученного раствора.
- К 2% раствору хлорида алюминия добавили 100 г кристаллогидрата АlСl3∙6Н2О. Найдите концентрацию полученного раствора, объем которого составил 1047 мл, а плотность 1,07 г/мл.
- Сколько граммов кристаллогидрата СuSО4∙5Н2О и какой объем раствора сульфата меди, содержащего 5 мас.% СuSО4 и имеющего плотность 1,045 г/мл, надо взять для приготовления 400 мл раствора сульфата меди, содержащего 7 мас.% СuSО4 и имеющего плотность 1,06 г/см3?
- Сколько граммов кристаллогидрата Nа2СО3∙10 Н2О надо добавить к 400 мл раствора карбоната натрия, содержащего 5 мас.% Na2СО3 и имеющего плотность 1,05 г/см , чтобы получить 16 мас.% раствор, плотность которого 1,17 г/см ?
- Какой объем 5% раствора сульфата натрия надо взять, чтобы растворение в нем 150 г кристаллогидрата Nа2SO4∙10Н2О привело к образованию 14% раствора? Плотности растворов Nа2SО4 равны, соответственно, 1,044 и 1,131 г/мл.
- Алюмокалиевые квасцы КАl(SО4)2∙12Н2О количеством вещества 10 ммоль растворили в 10 моль воды. Вычислите массовые доли сульфата калия и сульфата алюминия в образовавшемся растворе.
- В каком количестве вещества воды следует растворить 100 г декагидрата карбоната натрия для получения раствора с массовой долей соли, равной 10,0%?
- Из какой массы 25,0%-го раствора карбоната натрия выпало при охлаждении 10 г декагидрата, если в результате этого массовая доля соли в растворе уменьшилась в два раза?
- Из 500 г 15,0%-го раствора сульфита натрия при охлаждении выпало 25,2 г гептагидрата сульфита натрия. Рассчитайте массовую долю соли в полученном растворе.
- Из 250 г 17,0%-го раствора карбоната натрия при охлаждении выпало 28,6 г декагидрата карбоната натрия. Рассчитайте массовую долю соли в полученном растворе.
- В 20,0 г 5,00%-го раствора гидроксида натрия растворили 4 г тетрагидрата гидроксида натрия, при этом плотность полученного раствора стала равной 1,11 г/мл. Вычислите молярную концентрацию полученного раствора.
- Какую массу дигидрата фторида калия можно получить из 450 г 25,0%-го раствора фторида калия?
- Какую массу кристаллогидрата сульфата хрома (III), кристаллизующегося с 18 молекулами воды, можно получить из 80 мл раствора с концентрацией сульфата хрома 0,8 моль/л?
Кристаллогидраты

4.6
Средняя оценка: 4.6
Всего получено оценок: 88.
4.6
Средняя оценка: 4.6
Всего получено оценок: 88.
Выделить растворённое вещество из раствора можно путём выпаривания воды. В некоторых случаях образуются гидраты в кристаллическом виде или кристаллогидраты. Они содержат молекулы воды, которые называются кристаллизационной водой.
Общее описание
Кристаллогидраты образуются благодаря взаимодействию катионов кристаллической решётки вещества с молекулами воды. Это возможно, если связь между катионами и анионами кристалла более слабая.
К кристаллогидратам в первую очередь относятся соли. Типичными кристаллогидратами являются природные минералы – гипс, карналлит, алебастр, бура. Также кристаллогидраты образуют кислоты и основания.
Название вещества зависит от количества молекул воды. Для этого используют приставки, обозначающие число:
- 1 – моно;
- 2 – ди;
- 3 – три;
- 4 – тетра;
- 5 – пента;
- 6 – гекса;
- 7 – гепта;
- 8 – окта;
- 9 – нона;
- 10 – дека.
Например, кристаллогидрат FeSO4, содержащий одну молекулу воды, называется моногидрат сульфата железа (II). Если в кристаллогидрате семь молекул воды, он называется гептагидрат сульфата железа (II).
Вода из кристаллогидрата в большинстве случаев удаляется ступенчато. Например, при нагревании медного купороса, он переходит в тригидрат, затем в моногидрат. При нагревании до 250°С медный купорос полностью обезвоживается до сульфата меди (II).
Формула кристаллогидрата состоит из двух частей. Сначала записывается формула вещества. Через точку (знак умножения) указывается количество молекул воды. Например, ZnSO4 ∙ 7H2O, CuSO4 ∙ H2O, Na2CO3·10H2O, H2SO4 · H2O.
Расчёт массы вещества
При прокаливании кристаллогидраты разлагаются на сухое вещество и воду. Чтобы вычислить массовую долю вещества используется следующая формула:
ω(сух. в-ва) = m(сух. в-ва) / m(кр-та).
Для расчёта массовой доли воды применяется схожая формула:
ω(H2O) = m(H2O) / m(кр-та).
Рассмотрим решение задачи с применением формулы.
Необходимо вычислить массовую долю кристаллизационной воды в тригидрате нитрата меди (II) (Cu(NO3)2 ∙ 3H2O).
Решение:
Сначала запишем молярные массы воды и нитрата меди (II):
- M (Cu(NO3)2) = 187,5 г/моль;
- M (H2O) = 18 г/моль.
В 1 моле кристаллогидрата содержится 1 моль нитрата меди (II) и 3 моль воды, поэтому получаем по формуле m = n ∙ M массу воды и массу соли в кристаллогидрате:
- m (H2O) = 3 ∙ 18 = 54 г;
- m (Cu(NO3)2) = 1 ∙ 187,5 = 187,5 г.
Высчитаем общую массу вещества:
m (Cu(NO3)2 ∙ 3H2O) = 187,5 + 54 = 241,5 г.
Остаётся вычислить массовую долю воды:
ω(H2O) = m(H2O) / m(кр-та) = 54 / 241,5 = 0,22 или 22 %.
Ответ: массовая доля воды в тригидрате нитрата меди (II) 22 %.
Некоторые вещества невозможно обезводить без разложения. Например, соединение BeC2O4·H2O устойчиво только в форме кристаллогидрата.
Что мы узнали?
Кристаллогидратами называются вещества, содержащие молекулы воды за счёт их притяжения катионами кристаллической решётки. В формуле кристаллогидратов, а также в названии вещества указывается количество воды. Например, CuSO4 ∙ H2O – моногидрат сульфата меди (II). Если известны массы воды и сухого вещества, можно вычислить их массовую долю.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
Пока никого нет. Будьте первым!
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 88.
А какая ваша оценка?
Расчеты с участием кристаллогидратов и их свойства
При подготовке к экзаменам по химии, будь то ЕГЭ или ДВИ, мы неизбежно встречаемся с кристаллогидратами. Давайте разберемся, что это такое. Начнем с процесса кристаллизации. Когда мы охлаждаем горячий насыщенный раствор какой-либо соли, то ее растворимость начинает снижаться. Условному избытку соли некуда деваться, поэтому он выпадает в осадок. В зависимости от условий (скорость охлаждения, чистота раствора, тип вещества), при которых мы проводим процесс, осадок может получиться аморфным или кристаллическим. Иногда могут получиться крупные сформированные кристаллы правильной формы. Такие кристаллы часто содержат в себе не только растворенное вещество, но и молекулы растворителя. Эти молекулы встроены в решетку кристалла и не удаляются оттуда без внешних воздействий. Такие кристаллические вещества называют кристаллосольватами (solvent – растворитель). Если растворителем была вода, как в большинстве экзаменационных заданий, то будет кристаллогидрат. Отметим основные особенности и свойства кристаллогидратов.
1) Состав кристаллогидратов в большинстве случаев вполне определен и выражается отношением числа формульных единиц соли (или иного соединения) и кристаллизационной воды. Например, запись Fe2(SO4)3·9H2O означает, что в составе таких кристаллов на 1 моль кристаллогидрата приходится 1 моль безводного сульфата железа (III) и 9 моль кристаллизационной воды:
n(Fe2(SO4)3) = n(Fe2(SO4)3·9H2O)
n(H2O крист.) = 9n(Fe2(SO4)3·9H2O)
2) При растворении в воде кристаллогидрата образуется просто водный раствор самой соли. Говорить о растворе кристаллогидрата по этой причине не совсем верно. Будет раствор соли. Также важно отметить, что фраза «при растворении в воде кристаллогидрата Х был получен 10%-ный раствор» означает именно 10%-ный раствор относительно безводной соли, а не кристаллогидрата. Будьте внимательны!
3) В названии кристаллогидратов отражают само вещество и количество и молекул воды. Например, кристаллы Fe2(SO4)3·9H2O можно назвать нонагидрат сульфата железа (III) или сульфат железа (III) девятиводный (редко). По тому же принципу Cu(NO3)2·3H2O – тригидрат нитрата меди (II), NiSO4·7H2O – гептагидрат сульфата никеля, Ba(OH)2·8H2O – октагидрат гидроксида бария. Также существуют тривиальные названия для некоторых кристаллогидратов. Например, CuSO4·5H2O – медный купорос, FeSO4·7H2O – железный купорос, KAl(SO4)2·12H2O – алюмокалиевые квасцы и т.д.
4) При нагревании кристаллогидраты разлагаются. Возможно два варианта: обезвоживание или гидролиз. В рамках ЕГЭ и ДВИ может встретиться первый вариант. Приведем пару примеров:
CuSO4·5H2O = CuSO4 + 5H2O
MgSO4·7H2O = MgSO4 + 7H2O
При более сильном нагревании разложение может пойти дальше, зависит от свойств самой безводной соли. В таком случае можно записать суммарное уравнение процесса:
4Fe(NO3)2·9H2O = 2Fe2O3 + 8NO2 + O2 + 36H2O
5) (на ЕГЭ пока не встречалось) При образовании кристаллогидрата он забирает часть воды из раствора на собственное формирование. Например, если при охлаждении сформировалось 0,2 моль CuSO4·5H2O, то раствор при этом потерял 1 моль воды:
n(H2O крист.) = 5n(CuSO4·5H2O) = 5·0,2 = 1 моль
Справедливо и то, что при растворении кристаллогидрата вся его кристаллизационная вода перейдет в раствор.
Рассмотрим несколько задач с участием кристаллогидратов. Все из них будут полезны при подготовке к ДВИ, а многие и для ЕГЭ. Тем более, что формулировка задания 33 постоянно меняется и пополняется новыми идеями)
Задача №1
Неизвестный кристаллогидрат нитрата меди (II) содержит 22,31% воды по массе. Установите формулу кристаллогидрата.
Решение:
Пусть формульная единица кристаллогидрата содержит х молекул кристаллизационной воды. Тогда его формула будет Cu(NO3)2·xH2O. Молярная масса такого вещества будет равна:
M(Cu(NO3)2·xH2O) = 64 + 14·2 + 16·6 + 18х = 188 + 18х г/моль
Выразим массовую долю воды в кристаллогидрате:
ω(H2O) = M(xH2O)/M(Cu(NO3)2·xH2O)·100% = 22,31%
ω(H2O) = 18х/(188 + 18х)·100% = 22,31%
18х/(188 + 18х) = 0,2231
18х = 41,94 + 4,016х
х = 3
Ответ: Cu(NO3)2·3H2O
Задача №2
Массовая доля протонов в кристаллогидрате хлорида марганца равна 50%. Установите формулу кристаллогидрата.
Решение:
Пусть формульная единица кристаллогидрата содержит х молекул кристаллизационной воды. Тогда его формула будет MnCl2·xH2O. Молярная масса такого вещества будет равна:
M(MnCl2·xH2O) = 55 + 35,5·2 + 18х = 126 + 18х г/моль
В составе атома марганца содержится 25 протонов, хлора – 17, кислорода – 8, водорода – 1. Тогда в составе одной формульной единицы будет:
N(p) = 25 + 17·2 + 10х = 59 + 10х
На 1 моль кристаллогидрата приходится (59 + 10х) моль протонов. Их масса будет равна:
m(p) = n(p)·M(p) = 59 + 10х г
Выразим массовую долю воды в кристаллогидрате:
ω(р) = m(p)/m(MnCl2·xH2O)·100% = 50%
ω(p) = (59 + 10х )/( 126 + 18х)·100% = 50%
(59 + 10х )/( 126 + 18х) = 0,5
59 + 10х = 63 + 9х
х = 4
Ответ: MnCl2·4H2O
Задача №3
Отношение количеств электронов в безводном сульфате натрия и его кристаллогидрате равно 7:17. Установите формулу кристаллогидрата.
Решение:
Пусть формульная единица кристаллогидрата содержит х молекул кристаллизационной воды. Тогда его формула будет Na2SO4·xH2O. В составе атома натрия содержится 11 электронов, серы – 16, кислорода – 8, водорода – 1. Тогда в составе одной формульной единицы будет:
N(e) = 11·2 + 16 + 8·4 + 10x = 70 + 10x
В формульной единице сульфата натрия будет 70 электронов. Тогда составим уравнение:
70/(70 + 10х) = 7/17
1190 = 490 + 70х
х = 10
Ответ: Na2SO4·10H2O
Задача №4
Навеску кристаллогидрата перхлората магния разделили на две равные части. Первую нагревали в вакууме до постоянной массы, затем растворили полученную безводную соль в 50 мл воды, что привело к образованию раствора с массовой долей соли 4,27%. Вторую часть растворили 50 мл воды что привело к образованию раствора с массовой долей соли 4,183%. Установите формулу кристаллогидрата.
Решение:
Пусть было х г безводной соли. Вычислим массу соли в первом растворе:
ω(Mg(ClO4)2) = m(Mg(ClO4)2)/m(р-ра)·100%
m(p-pa) = m(H2O доб.) + m(Mg(ClO4)2)
m(H2O доб.) = ρ·V = 50 г
х/(50 + х))·100% = 4,27%
х/(50 + х) = 0,0427
х = 2,135 + 0,0427х
х = 2,23
m(Mg(ClO4)2) = 2,23 г
Далее вычислим массу воды во втором растворе:
m(р-ра Mg(ClO4)2) = m(Mg(ClO4)2)/ω(Mg(ClO4)2)·100%
m(р-ра Mg(ClO4)2) = 2,23/4,183%·100% = 53,31 г
m(H2O общ.) = m(p-pa) — m(Mg(ClO4)2) = 53,31 – 2,23 = 51,08 г
Поскольку часть воды в растворе происходит от исходного кристаллогидрата, ее можно найти по разности:
m(H2O крист.) = m(H2O общ.) — m(H2O доб.) = 51,08 – 50 = 1,08 г
Далее вычислим количества безводной соли и кристаллизационной воды:
n(Mg(ClO4)2) = m(Mg(ClO4)2)/M(Mg(ClO4)2) = 2,23/223 = 0,01 моль
n(H2O крист.) = m(H2O)/M(H2O) = 1,08/18 = 0,06 моль
Пусть формульная единица кристаллогидрата содержит х молекул кристаллизационной воды. Тогда его формула будет Mg(ClO4)2·xH2O. Найдем отношение количеств соли и воды:
n(H2O крист.)/n(Mg(ClO4)2) = х/1 = 0,06/0,01 = 6
х = 6
Ответ: Mg(ClO4)2·6H2O
Задача №5
При охлаждении до 0˚С 150 г горячего насыщенного раствора сульфата меди (II) в осадок выпало 42,38 г медного купороса. Определите растворимость сульфата меди (II) при 80˚С. Растворимость сульфата меди (II) при 0˚С равна 18,3 г/100 г воды.
Решение:
Выразим массовую долю сульфата меди в составе медного купороса:
ω(CuSO4) = m(CuSO4)/m(CuSO4·5H2O)·100% = М(CuSO4)/М(CuSO4·5H2O)·100%
ω(CuSO4) = 160/250·100% = 64% или 0,64
Далее вычислим массу безводной соли в составе выпавшего в осадок кристаллогидрата:
m(CuSO4) = m(CuSO4·5H2O)·ω(CuSO4) = 42,38·0,64 = 27,12 г
Пусть в исходном растворе было х г безводной соли. Тогда будет справедлива следующая запись:
(х – 27,12)/(150 – 42,38) = 18,3/118,3
Решим уравнение:
118,3(х – 27,12) = 18,3·107,62
118,3х – 3208,3 = 1969,4
х = 43,8
Вычислим, сколько в горячем растворе было воды:
m(Н2О) = m(р-ра) — m(CuSO4) = 150 – 43,8 = 106,2 г
Определим растворимость безводной соли на 100 г воды:
S(CuSO4) = m(CuSO4)/m(Н2О)·100 = 43,8/106,2·100 = 41,2 г на 100 г воды
Ответ: 41,2 г/100 г воды.
Алгоритм решения задач на приготовление растворов с использованием кристаллогидратов
Кристаллогидраты — это твердые вещества, содержащие в своем составе воду, входящую в состав кристалла в виде целых молекул. Формулу кристаллогидрата записывают, указывая количество молекул кристаллизационной воды, приходящейся на одну единицу вещества. Например, СuSО4 . 5Н2О кристаллогидрат сульфата меди2; Nа2SО4 . 10Н2О — кристаллогидрат сульфата натрия (декагидрат сульфата натрия)3. Некоторые вещества могут образовывать несколько кристаллогидратов. Например:
СоС12 . 6Н2О — розово-красные кристаллы (устойчив до t = 49 °С);
СоС12 . 4Н2О — красные кристаллы (устойчив до t = 58 °С);
СоС12 . 2Н2О — сине-фиолетовые кристаллы (устойчив до t = 90 °С);
СоС12 . Н2О — темно-синие кристаллы (устойчив до t = 140 °С);
СоС12 (безводн.) — бледно-синего цвета (устойчив до t плавл.= 724 °С).
Причем содержание воды в них зависит не только от влажности окружающей среды, но и от температуры. При ее повышении кристаллогидраты часто теряют воду, даже находясь, в равновесии с ней (под слоем воды). Так для хлорида кобальта приведены температуры, выше которых данный кристаллогидрат теряет воду.
При растворении кристаллогидрата образуется самый обычный раствор, где растворенным веществом будет безводная соль, а кристаллизационная вода смешается с водой раствора.
При решении задач с использованием кристаллогидратов следует учитывать кристаллизационную воду, поступающую в раствор.
Задача 1.
Определить массу медного купороса СuSО4 . 5Н2О, который необходимо добавить к 300 г 2%-ного (масс.) раствора СuSО4 в воде для получения 5% -ного раствора.
Дано:
масса исходного раствора: mисх р-ра = 300 г;
массовая доля СuSО4 в исходном р-ре:
массовая доля СuSО4 в конечном р-ре: 
Найти:
массу добавленного кристаллогидрата: m(СuSО4 . 5Н2О)довавл. = ?
Решение:
Отобразим условие задачи в виде рисунка:
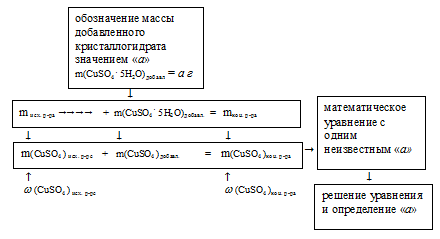
Алгоритм решения будет выглядеть следующим образом:
1. Искомой величиной является масса кристаллогидрата СuSО4 . 5Н2О. Обозначим ее величиной «а». Тогда масса полученного раствора составляет:
mкон. р-ра = mисх. р-ра + mкрист. гид. = (300 + а)
2. Так как кристаллогидрат состоит не из чистой соли, определим массу СuSО4
в «а» г СuSО4 . 5Н2О. Удобнее всего это сделать, используя молярную массу кристаллогидрата.
М(СuSО4 . 5Н2О) = (СuSО4) + 5 .М(Н2О) =
= 64 + 32 + 4 х 16 + 5 х ( 2 х 1 + 16) = 160 + 90 = 250 г/моль.
Составляем пропорцию:
250 г СuSО4 . 5Н2О содержит 160 г СuSО4 (по молярной массе)
а mСuSО4 . 5Н2О содержит х г СuSО4 (по условию)
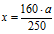
3. Теперь определим массу чистого СuSО4 в исходном и конечном растворах.
Масса чистого СuSО4 в полученном растворе складывалась из суммы масс СuSО4 в исходном растворе и чистого СuSО4 в кристаллогидрате. Отсюда имеем математическое уравнение:
Решая это уравнение, получим: а = 15 г.
Величиной «а» мы обозначали массу кристаллогидрата.
m(СuSО4 . 5Н2О) = 15г.
Ответ: необходимо добавить 15 г СuSО4 . 5Н2О.
Комментарии:
1 При приготовлении растворов часто приходится использовать не чистые вещества, а их кристаллогидраты.
2 Бытовое и промышленное название — медный купорос.
3 Бытовое и промышленное название — глауберова соль.
Задача
Определить массу кристаллогидрата Na2CO3? 10H2O и воды, которые необходимо взять для приготовления раствора массой 540 г. с массовой долей карбоната натрия 15%.
1. Запишите условие задачи с помощью общепринятых обозначений.
Дано:
m р-ра = 540г
ω (Na2CO3) = 30%
m (Na2CO3? 10H2O) = ?
m(Н2О) = ?
Решение:
1. Определите массу карбоната натрия Na2CO3, содержащегося в 540 г. раствора
m в-ва = ω1· m р-ра /100%
m (Na2CO3) = 15% ? 540 г. /100% = 81 г.
2. Сделайте пересчет рассчитанной массы на кристаллогидрат. Для этого рассчитайте молярные массы Na2CO3 и Na2CO3? 10H2O
М (Na2CO3) = 106 г/моль
М (Na2CO3? 10H2O) = 286 г/моль
Отсюда по формуле m = n? M найдите массы Na2CO3 и Na2CO3? 10H2O, приняв количество вещества n равным 1 моль
m (Na2CO3) = 106 г.
m (Na2CO3? 10H2O) = 286 г.
3. Вычислите массу кристаллогидрата, составив отношение:
в 286 г. Na2CO3? 10H2O содержится 106 г. Na2CO3,
а в х г. Na2CO3? 10H2O —————— 81 г. Na2CO3
х = 286? 81/ 106 = 219 г. – масса Na2CO3? 10H2O, необходимая для приготовления раствора.
4. Вычислите массу воды:
m(Н2О) = m р-ра – m в-ва
m(Н2О) = 540 – 219 = 321 г.
5. Запишите ответ:
Ответ: для приготовления раствора потребуется 219 г. Na2CO3? 10H2O и 321 г. воды
I. Расчеты по формулам
В какой массе дигидрата сульфата кальция содержится число электронов, равное числу Авогадро?
В некоторой порции пентагидрата сульфата меди содержится 0,25 моль воды. Вычислите массу этой порции кристаллогидрата.
В некоторой порции кристаллогидрата сульфата желез (III) число атомов кислорода в 15 раз больше числа Авогадро, а число атомов железа точно соответствует числу Авогадро. Выведите формулу кристаллогидрата.
Вычислите число атомов и число электронов в 14 г гептагидрата сульфата никеля (II).
Имеется смесь равных масс гептагидрата гидрофосфата натрия и дигидрата дигидрофосфата натрия. Сколько в это смеси приходится атомов кислорода на один атом фосфора?
Рассчитайте массу атомов водорода, содержащихся в 143 г моногидрата ацетата меди.
Вычислите массовую долю бария в кристаллогидрате гидроксида бария, в котором число атомов водорода в 1,8 раз больше числа атомов кислорода.
В 0,25 моль кристаллогидрата разница между массой кристаллизационной воды и массой безводной соли равна 59,5. Массовая доля кристаллизационной воды составляет 28,83%. Вычислите относительную молекулярную массу кристаллогидрата.
В 2 моль кристаллогидрата разница между массой кристаллизационной воды и массой безводной соли равна 26. Массовая доля кристаллизационной воды составляет 0,468. Вычислите молярную массу кристаллогидрата.
В кристаллогидрате, образованном средней солью металла, массовая доля кристаллизационной воды равна 50,0%. Вычислите массу водорода, содержащегося в 100 г этого кристаллогидрата.
В кристаллогидрате, образованном солью бескислородной кислоты, массовая доля соли равна 0,755. Вычислите массу кислорода, содержащегося в 1.00 г этого кристаллогидрата.
В некоторой порции кристаллогидрата ацетата магния находится 9,632•1023 атомов углерода и 3,371•1024 атомов водорода. Вычислите число атомов кислорода, находящихся в этой порции кристаллогидрата.
В некоторой порции кристаллогидрата ацетата бария находится 4,816*1023 атомов углерода и 8,428*1023 атомов кислорода. Вычислите число атомов водорода, находящихся в этой порции кристаллогидрата.
В 0,25 моль дигидрата ацетата металла 2А-группы содержится 1,535*1025 электронов. Установите, какой металл входит в состав кристаллогидрата.
Какую массу кристаллогидрата сульфата хрома (III), кристаллизующегося с 18 молекулами воды, можно получить из 80 мл раствора с концентрацией сульфата хрома 0,8 моль/л?
Какую массу дигидрата фторида калия можно получить из 450 г 25%-го раствора фторида калия?
II. Задачи на растворы
Определите массовую долю сульфата железа (II) в растворе, полученном при растворении 55,6 г семиводного кристаллогидрата в 344,4 г воды.
Определите количество воды, в котором надо растворить 27,8 г семиводного сульфата железа (II), чтобы получить насыщенный при 50 °С раствор сульфата железа (II) (растворимость соли при этой температуре 48,6 г в 100 г воды).
Определите количество кристаллогидрата MgС12*6H2О, которое нужно растворить в 159,4 г воды, чтобы получить 10%-ный раствор хлорида магния.
Какую массу кристаллогидрата сульфата натрия (кристаллизуется с 10 молекулами воды) можно получить при выпаривании 400 мл 12%-ного раствора плотностью 1,12 г/мл?
4,48 г дигидрата хлорида бария растворили в 15,52 мл воды. К полученному раствору прибавили 4 мл раствора сульфата калия (плотность 1,08 г/мл) с концентрацией 0,32 моль/л. Как изменилась массовая доля хлорида бария в растворе?
Вычислите массовую долю соли в растворе, полученном смешением 0,04 моль нонагидрата нитрата хрома (III) и 1 моль воды.
Алюмокалиевые квасцы КА1(SО4)2*12Н2О количеством вещества 10 ммоль растворили в 10 моль воды. Вычислите массовые доли сульфата калия и сульфата алюминия в образовавшемся растворе.
Кристаллогидрат фосфата натрия Nа3РО4*12Н2О количеством вещества 1 моль растворили в 75 моль воды. Плотность получившегося раствора оказалась равной 1,098 г/мл. Вычислите молярную концентрацию ионов натрия в этом растворе.
В 300 г раствора фосфата натрия с концентрацией 0,32 моль/л (пл. 1,05 г/мл) растворили 25 г кристаллогидрата фосфата натрия (кристаллизуется с 12 молекулами воды). Вычислите массовые доли веществ в получившемся растворе.
В 225 г 25,5%-го раствора бромида кальция растворили гексагидрат бромида кальция массой 50 г. Вычислите массовые доли веществ в получившемся растворе.
В каком объеме воды следует растворить 0,3 моль пентагидрата сульфата меди (II) для получения 12%-го раствора?
В каком количестве вещества воды следует растворить 100 г декагидрата карбоната натрия для получения раствора с массовой долей соли, равной 10%?
Из какой массы 25%-го раствора карбоната натрия выпало при охлаждении 10 г декагидрата, если в результате этого массовая доля соли в растворе уменьшилась в два раза?
Из 500 г 15,0%-го раствора сульфита натрия при охлаждении выпало 25,2 г гептагидрата сульфита натрия. Рассчитайте массовую долю соли в полученном растворе.
Из 250 г 17,0%-го раствора карбоната натрия при охлаждении выпало 28,6 г декагидрата карбоната натрия. Рассчитайте массовую долю соли в полученном растворе.
В 20 г 5%-го раствора гидроксида натрия растворили 4 г тетрагидрата гидроксида натрия, при этом плотность полученного раствора стала равной 1,11 г/мл. Вычислите молярную концентрацию полученного раствора.
Массовая доля безводной соли в кристаллогидрате равна 64%. Какую массу кристаллогидрата нужно взять для приготовления 150 г 50%-го раствора соли?
Сколько граммов кристаллогидрата А1Сl3*6Н2О необходимо растворить в 1000 г 2 мас.% раствора AlС13, чтобы получить 3% раствор?
Для приготовления насыщенного при 50°С раствора СuSO4 было взято 74,8 г Н2О. После охлаждения раствора до 25 °С выпало 15.23 г кристаллогидрата СuSО4*5Н2О, а концентрация СuSО4 в растворе стала равной 18,23 мас.%. Определите концентрацию (в мас.%) исходного раствора СuSО4, насыщенного при 50 °С.
При охлаждении 300 г насыщенного при 40°С раствора FеSО4 (растворимость соли 40,1 г в 100 г воды) до 20°С выпал кристаллогидрат FeSО4*7Н2О, а концентрация FеSО4 в растворе стала равной 20,82 мас.%. Определите массу выпавшего кристаллогидрата.
Растворимость сульфата натрия при 20°С равна 19,2 г Nа2SО4 в 100 г воды. Найдите, какую массу кристаллогидрата Nа2SО4*10Н2О надо добавить к 200 г раствора Na2SO4, содержащего 10 мас.% растворенного вещества, для получения насыщенного при 20°С раствора.
К 2 мас.% раствору хлорида алюминия добавили 100 г кристаллогидрата А1С13*6Н2О. Найдите концентрацию полученного раствора, объем которого составил 1047 мл, а плотность равна 1,07 г/мл.
Сколько граммов кристаллогидрата СuSО4*5Н2О и какой объем раствора сульфата меди, содержащего 5 мас.% СuSО4 и имеющего плотность 1,045 г/мл, надо взять для приготовления 400 мл раствора сульфата меди, содержащего 7 мас.% СuSО4 и имеющего плотность 1,06 г/см3?
Сколько граммов кристаллогидрата Nа2СО3*10 Н2О надо добавить к 400 мл раствора карбоната натрия, содержащего 5 мас.% Na2СОз и имеющего плотность 1,05 г/см , чтобы получить 16 мас.% раствор, плотность которого 1,17 г/см ?
Какой объем 5% раствора сульфата натрия надо взять, чтобы растворение в нем 150 г кристаллогидрата Nа2SO4*10Н2О привело к образованию 14% раствора? Плотности растворов Nа2SО4 равны, соответственно, 1,044 и 1,131 г/мл.
Для приготовления насыщенного при 50°С раствора нитрата никеля было взято 100 г Н2О. После охлаждения раствора до 25°С выпало 152 г кристаллогидрата Ni(NО3)2*6Н2О, а концентрация нитрата никеля в растворе стала равной 50 мас.%. Определите концентрацию исходного раствора Ni(NО3)2, насыщенного при 50°С.
Из раствора, содержащего 40% FeSO4, при охлаждении выпало 50 г его кристаллогидрата (FeSО4*7Н2О), а концентрация FеSО4 в оставшемся растворе стала равна 20% . Найдите массу исходного раствора.
Декагидрат карбоната натрия обработали раствором азотной кислоты массой 150 г, при этом выделилось 2,67 л углекислого газа (н.у.). Вычислите массовую долю азотной кислоты в исходном растворе.
К сульфиду калия массой 3,3 г, находящемуся в водном растворе, добавили 0,02 моль гексагидрата хлорида меди. Вычислите массу образовавшегося осадка.
III. Установление формулы кристаллогидрата
Относительная молекулярная масса кристаллогидрата сульфата железа (II) равна 278. Установите формулу этого кристаллогидрата.
Массовая доля воды в кристаллогидрате ацетата цинка равна 16,4%. Установите формулу кристаллогидрата.
Массовая доля кислорода в кристаллогидрате нитрата железа (III) равна 0,713. Установите формулу кристаллогидрата.
В смеси, в которой количества веществ хлорида натрия и кристаллогидрата бромида натрия равны, массовая доля поваренной соли составляет 29,6%. Установите состав кристаллогидрата бромида натрия.
Число атомов водорода, равное числу Авогадро, содержится в 21,9 г кристаллогидрата ацетата цинка. Установите формулу кристаллогидрата.
Чтобы получить смесь оксида хрома (III) и кристаллогидрата сульфата хрома (III) с равными массовыми долями этих двух соединений, пришлось взять количество вещества оксида в 4,71 раза больше количества вещества кристаллогидрата. Установите состав кристаллогидрата.
Определите состав кристаллогидрата сульфата натрия, если известно, что при нагревании 80,5 г кристаллогидрата до 300°С масса испарившейся воды составила 45 г. Какова концентрация в массовых процентах раствора, полученного при растворении 80,5 г данного кристаллогидрата в 2 л воды?
В смеси, в которой количества веществ хлорида натрия и кристаллогидрата бромида натрия равны, массовая доля поваренной соли составляет 29,6%. Установите состав кристаллогидрата бромида натрия.
К 200 г раствора Zn(NО3)2, содержащего 20 мас.% растворенного вещества, добавили 40 г кристаллогидрата этой соли. Концентрация Zn(NО3)2 в полученном растворе стала равной 27,27 мас.%. Установите формулу кристаллогидрата.
При охлаждении 250 г насыщенного при 70°С раствора йодида бария (растворимость 246,6 г соли в 100 г воды) до 0°С выпало 164,7 г кристаллогидрата, а концентрация ВаI2 в растворе стала равной 62,5 мас.%. Установите формулу кристаллогидрата.
При охлаждении 300 г насыщенного при 60°С раствора нитрата меди (растворимость соли 181,7 г в 100 г воды) до 250С выпало 75 г кристаллогидрата нитрата меди, а концентрация Сu(NО3)2; в растворе стала равной 60,1 мас.%. Установите формулу кристаллогидрата.
К раствору хлорида марганца, содержащему 20% МnС12, добавили 41,3 г кристаллогидрата этой соли. Полученный раствор имеет массу 180 г и содержание хлорида марганца, равное 30 мас.%. Установите формулу кристаллогидрата.
К 500 г раствора хлорида меди, содержащего 15 мас.% СиС12, добавили 153,4 г кристаллогидрата этой соли. Концентрация СиС12 в полученном растворе стала равной 30 мас.%. Установите формулу кристаллогидрата.
При охлаждении 200 г насыщенного при 40°С раствора Na3РO4 (растворимость соли 23,3 г в 100 г воды) до 25°С выпало 40,92 г кристаллогидрата, а концентрация Na3РО4 в растворе стала равной 12,66 мас.%. Установите формулу кристаллогидрата.
К раствору ацетата свинца, содержащему 15% Рb(СН3СОО)2, добавили 20 г кристаллогидрата этой соли. Полученный раствор имеет массу 150 г и содержание ацетата свинца 24,43 мас.%. Установите формулу кристаллогидрата.
Кристаллогидраты — это твердые вещества, содержащие в своем составе воду, входящую в состав кристалла в виде целых молекул. Формулу кристаллогидрата записывают, указывая количество молекул кристаллизационной воды, приходящейся на одну единицу вещества. Например, СuSО4 . 5Н2О кристаллогидрат сульфата меди2; Nа2SО4 . 10Н2О — кристаллогидрат сульфата натрия (декагидрат сульфата натрия)3. Некоторые вещества могут образовывать несколько кристаллогидратов. Например:
СоС12 . 6Н2О — розово-красные кристаллы (устойчив до t = 49 °С);
СоС12 . 4Н2О — красные кристаллы (устойчив до t = 58 °С);
СоС12 . 2Н2О — сине-фиолетовые кристаллы (устойчив до t = 90 °С);
СоС12 . Н2О — темно-синие кристаллы (устойчив до t = 140 °С);
СоС12 (безводн.) — бледно-синего цвета (устойчив до t плавл.= 724 °С).
Причем содержание воды в них зависит не только от влажности окружающей среды, но и от температуры. При ее повышении кристаллогидраты часто теряют воду, даже находясь, в равновесии с ней (под слоем воды). Так для хлорида кобальта приведены температуры, выше которых данный кристаллогидрат теряет воду.
При растворении кристаллогидрата образуется самый обычный раствор, где растворенным веществом будет безводная соль, а кристаллизационная вода смешается с водой раствора.
При решении задач с использованием кристаллогидратов следует учитывать кристаллизационную воду, поступающую в раствор.
Задача 1.
Определить массу медного купороса СuSО4 . 5Н2О, который необходимо добавить к 300 г 2%-ного (масс.) раствора СuSО4 в воде для получения 5% -ного раствора.
Дано:
масса исходного раствора: mисх р-ра = 300 г;
массовая доля СuSО4 в исходном р-ре:
массовая доля СuSО4 в конечном р-ре: 
Найти:
массу добавленного кристаллогидрата: m(СuSО4 . 5Н2О)довавл. = ?
Решение:
Отобразим условие задачи в виде рисунка:
Алгоритм решения будет выглядеть следующим образом:
1. Искомой величиной является масса кристаллогидрата СuSО4 . 5Н2О. Обозначим ее величиной «а». Тогда масса полученного раствора составляет:
mкон. р-ра = mисх. р-ра + mкрист. гид. = (300 + а)
2. Так как кристаллогидрат состоит не из чистой соли, определим массу СuSО4
в «а» г СuSО4 . 5Н2О. Удобнее всего это сделать, используя молярную массу кристаллогидрата.
М(СuSО4 . 5Н2О) = (СuSО4) + 5 .М(Н2О) =
= 64 + 32 + 4 х 16 + 5 х ( 2 х 1 + 16) = 160 + 90 = 250 г/моль.
Составляем пропорцию:
250 г СuSО4 . 5Н2О содержит 160 г СuSО4 (по молярной массе)
а mСuSО4 . 5Н2О содержит х г СuSО4 (по условию)
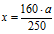
3. Теперь определим массу чистого СuSО4 в исходном и конечном растворах.
Масса чистого СuSО4 в полученном растворе складывалась из суммы масс СuSО4 в исходном растворе и чистого СuSО4 в кристаллогидрате. Отсюда имеем математическое уравнение:
Решая это уравнение, получим: а = 15 г.
Величиной «а» мы обозначали массу кристаллогидрата.
m(СuSО4 . 5Н2О) = 15г.
Ответ: необходимо добавить 15 г СuSО4 . 5Н2О.
Комментарии:
1 При приготовлении растворов часто приходится использовать не чистые вещества, а их кристаллогидраты.
2 Бытовое и промышленное название — медный купорос.
3 Бытовое и промышленное название — глауберова соль.
Кристаллогидраты. Решение расчётных задач.
Помелина Людмила Геннадьевна, учитель химии ГБОУ СОШ № 151
Познавательные задачи:
Показать актуальность выбранной темы
Расширить знания учащихся о кристаллогидратах
Использовать алгебраический метод решения задач
(межпредметная связь с математикой, на экзаменах ЕГЭ решаются подобные задачи)
Для успешной сдачи экзамена в формате ЕГЭ необходимо научиться решать задачи по теме «Растворы», но с применением кристаллогидратов.
Кристаллогидраты — кристаллы, содержащие молекулы воды.
Кристаллогидраты – это те же растворы, поэтому можно рассчитывать массовую долю растворённого вещества
Типичными кристаллогидратами являются многие природные минералы, например, гипс CaSO4·2H2O, карналлит MgCl2·KCl·6H2O.
Медный купорос CuSO4·5H2O ,
железный купорос FeSO4·7H2O,
кристаллическая сода Na2CO3·10H2O.
Кристаллизационная вода уходит из кристаллов при прокаливании.
Например,медный купорос CuSO4·5H2O – голубые кристаллы, а при прокаливании получается белый порошок.
Номенклатура.
Количество воды указывается названием греческих числительных:
2 – дигидрат
3 – тригидрат
4 – тетра, 5 –пента и.т.д.
Например, Na2CO3·10H2O – декагидрат карбоната натрия
Вводим обозначения:
Молярная массакристаллогидрата Mк.г.
Масса кристаллогидрата mк.г.
Молярная масса безводной соли Mб.в
Масса безводной соли mб.в.
Массовая доля безводной соли в кристаллогидратеW =Mб.в. : Mк.г.
Массабезводной солиmб.в.=mк.г. · W
Масса воды в кристаллогидрате mH2O=mк.г. · W(H2O)
Масса кристаллогидрата mк.г. = mб.в. : Wб.в
Массовая доля растворённого вещества
ω(Омега) = mр.в. / mр-ра
mр.в = mр-ра ·ω mр-ра = mр.в / ω
Нахождение массовой доли соли вкристаллогидрате
Задача №1
Определите массовую долю сульфата меди (II)CuSO4 в медном купоросе CuSO4·5H2O
Алгоритм решения
Найти молярные массы безводной соли, т.е.CuSO4 и кристаллогидрата CuSO4·5H2O
М(CuSO4)= 160 г/ моль
М(CuSO4·5H2O) =160+90= 250 г/ моль
Определить массовую долю безводной соли
W =Mб.в. : Mк.г.= 160 :250 = 0,64; 64%
Ответ: 64%
Теперь необходимо научиться переводить любую массу кристаллогидрата в массу безводной соли.
Задача№2
Сколько грамм безводной соли сульфата меди CuSO4 находится в 200 г её кристаллогидрата CuSO4·5H2O
Алгоритм решения.
Найти массовую долю безводной соли
W =Мб.в./Мк.г.= 160 г/ моль : 250 г/ моль = 0,64; 64 %
По массовой доле определить массу mб.в.
mб.в.=mк.г. · W= 200 · 0,64 = 128 г Ответ: 128 г
Нахождение массовой доли и массы воды в кристаллогидрате
Задача №1
Определите массовую долю воды в железном купоросеFeSO4·7H2O
Алгоритм решения.
Найти молярные массы воды иFeSO4·7H2O
М(H2O)= 18г/ моль
М(FeSO4·7H2O) =152+ 18 * 7= 152 +126 =278 г/ моль
Определить массовую долю воды
W =МH2O./Мк.г.= 18 · 7 г/ моль : 278 г/ моль = 0,453; 45,3%
Ответ: 45,3%
Задача №2
Сколько грамм воды находится в 1 кг кристаллогидратаFeSO4·7H2O
Алгоритм решения.
Определить массовую долю воды
W (H2O) =mH2O:Мк.г.= 18*7: 278 = 0,453
По массовой доле воды определить массу воды от данной массы кристаллогидратаFeSO4·7H2O
mH2O= mк.г.· W(H2O) = 1000 г · 0,453 = 453 г
Ответ:453 г
Приготовление раствора
Задача №1 Сколько г. кристаллической соды Na2CO3·10H2O и воды надо взять, чтобы приготовить 572 г 10 % раствора карбоната натрия Na2CO3
Алгоритм решения.
Найти массу безводной соли в 10% растворе
ω =10 %; 0,1 mр.в.= mр-ра * ω= 572 * 0,1 = 57,2 г =mб.в.
Найти массовую долю безводной соли
W =Мб.в./Мк.г.= 106 106 +180) = 0,37
Масса кристаллогидрата
mк.г. = mб.в. : Wб.в = 57,2:0,37 = 154,6 г
Масса воды mH2O = 572 – 154,6 = 417,4г
Ответ: 417,4г
Задача№2Вычислите массу воды, в которой необходимо растворить 56,2 г кристаллогидратаCoSO4 ·7 H2O для получения 12,5 % раствора сульфата кобальта (II)
|
Дано: |
Решение |
|
mк.г. = 56,2 г ω = 12,5% ; 0,125 |
Mб.в (CoSO4 )= 155 г/моль Mк.г. (CoSO4 ·7 H2O) = 281 г/моль W =Мб.в./Мк.г = 155 : 281 = 0,552 Масса mб.в.. = mк.г · Wб.в=56,5·0,552 = 31,19 г Масса раствора mр-ра = mр. в / ω = 31,19 : 0,125=249г m(H2O) = mр-ра — mк.г = 249 – 56,2 = 192,8 г |
|
Найти: m(H2O) |
Ответ:m(H2O)= 192,8 г |
Задача для самостоятельного решения
Какую массу кристаллогидратаCu(NO3)2. 3 H2O нужно растворить в воде объёмом 300 мл для получения раствора с массовой долей нитрата меди 5 %
Ответ: 20,57 г.
Приготовление более концентрированных растворов
Задача №1
Сколько грамм глауберовой соли Na2SO4·10H2O необходимо добавить к 80 г 5% раствора, чтобы увеличить концентрацию солиNa2SO4 в 2 раза
Алгоритм решения.
Мб.в(Na2SO4) = 142 г/ моль , Мк.г(Na2SO4·10H2O) = 322 г/ моль
Найти массовую долю безводной соли в кристаллогидрате
W =Мб.в.:Мк.г= 142: 322 = 0,44
Найти массу безводной соли в 5% растворе соли
ωр-ра1=5 %; 0,05
mр.в.1= mр-ра1 * ω р.в1 = 80· 0,05 = 4 г
Выбираем неизвестное
X – это масса г.добавляемого кристаллогидрата, тогда масса безводной соли будет меньше.mб.в.=mк.г. · Wб.в = x· W= x·0,44
Новая концентрация раствора равна 10% , 0,1
Масса 2 раствора увеличится mр-ра2 = mр-ра1 + mк.г. добав.= 80 +X
Составляем уравнение с одним неизвестным, пользуясь формулой
ωр.в2=mр.в.2 / mр-ра2
0,1 = 4 +x·0,44/80 +X
РешаемX= 11,76 г
Ответ: глауберовой соли Na2SO4·10H2O необходимо добавить 11,76 г
Задача 2
Сколько грамм кристаллогидрата медного купороса надо добавить, чтобы из 20 % раствора массой 240 г получить 30 % раствор.
|
Дано: |
Решение |
|
mр-ра1 = 240 г ωр-ра1 =20%; 0,2 ωр-ра2= 30 %; 0,3 |
Мб.в(CuSO4) = 160 г/ моль Мк.г(CuSO4·5H2O) =250 г/ моль W =Mб.в. : Mк.г.= 160 :250 = 0,64; 64% mр.в.1= mр-ра1·ω р.в1= 240 · 0,2 = 48 г =mб.в. X – это масса г.добавляемогокристаллогидрата, тогда масса безводной соли будет меньше. mб.в.=mк.г. · Wб.в = x· W= x·0,64 mр.в.2=mр.в.1 +x·0,64(добавка) = 48+x·0,64 Новая концентрация раствора равна 30% , 0,3 Масса 2 раствора увеличится: mр-ра2 = mр-ра1 + mк.г. добав.=240 +X Составляем уравнение с одним неизвестным, пользуясь формулой ωр.в2=mр.в.2 / mр-ра2 0,3 = 48+x·0,64 /240 + X X = 70,6 г |
|
Найти: mк.г.(CuSO4·5H2O) |
Ответ: кристаллогидрата медного купороса надо добавить 70,6 г |
Задача для самостоятельного решения
Сколько грамм железного купороса FeSO4·7H2O необходимо добавить к 280 г15% раствора, чтобы увеличить концентрацию солиFeSO4 в 1,5 раза. (65,2 г)
Какую массу медного купороса CuSO4·5H2O и какой объём 7% раствора сульфата меди (II) (плотность раствора ∫ = 1,05 г/ мл) нужно взять для приготовления 2 л. 20 % раствора (плотность раствора ∫ = 1,1 г/ мл)
( 502г и 1617 мл)
Смешали 400 мл 2 % раствора сульфата меди (II) (плотность раствора ∫ = 1,0 г/ мл) и 300 мл 30 % раствора сульфата меди (II) (плотность раствора ∫ = 1,12 г/ мл). К полученному раствору добавили 75 г медного купороса CuSO4·5H2O. Найдите концентрацию полученного раствора. (19,3 %)
4. К 700 мл 5 % раствора сульфата меди (II) (плотность раствора ∫ = 1,05 г/ мл) добавили 25 г медного купороса CuSO4·5H2O. После этого раствор упарили до объёма 300 мл (плотность раствора ∫ = 1,1 г/ мл). Найдите концентрацию полученного раствора.
(15,98 %)
Литература.
О.C. Габриелян, П.В. Решетов, И.Г. Остроумов Задачи по химии и способы их решения. М.: Дрофа, 2004.
Крутецкая Е.Д. Решение усложнённых и комбинированных задач по химии. Рабочая тетрадь.- СПбАППО, 2006.
В, Б. Воловик, Е.Д. Крутецкая Общая и неорганическая химия: Вопросы, упражнения, задачи, тесты. Пособие для средней школы. – СПб: СМИО Пресс,2014.
Приложение
|
Название |
Формула |
|
|
систематическое |
Тривиальное (техническое) |
|
|
Декагидрат карбоната натрия |
Сода техническая |
Na2CO3·10H2O |
|
Пентагидрат сульфата меди (II) |
Медный купорос |
CuSO4·5H2O |
|
Гептагидрат сульфата железа (II) |
Железный купорос |
FeSO4·7H2O |
|
Декагидрат сульфата натрия |
Глауберова соль |
Na2SO4·10H2O |
|
Гептагидрат сульфата магния |
Горькая (английская соль) |
MgSO4·7H2O |
|
Дигидрат сульфата кальция |
гипс |
CaSO4· 2H2O |
Адрес публикации: https://www.prodlenka.org/metodicheskie-razrabotki/223551-metodicheskaja-razrabotka-kristallogidraty-re
Задача 3. Медный купорос (CuSO4·5H2O) массой 12,5 г растворили в воде и получили раствор с массовой долей соли 20%. К этому раствору добавили 5,6 г железа и после завершения реакции еще 117 г 10%-ного раствора сульфида натрия. Определите массовую долю сульфида натрия в конечном растворе.
Источник: Я сдам ЕГЭ. Типовые задания. А.А. Каверина, стр. 210.
Решение:
1. Посчитаем количество веществ сульфата меди (II) в растворе и железа:
M(CuSO4) = 160 г/моль
M(CuSO4·5H2O) = 250 г/моль.
n(CuSO4·5H2O) = 12,5/250 = 0,05 моль
n(CuSO4) =n(CuSO4·5H2O) = 0,05 моль
m(CuSO4 в исходном растворе) = 0,05·160 = 8 г.
n(Fe) = 5,6/56 = 0,1 моль.
2. Запишем уравнение реакции сульфата меди (II) с железом:
| CuSO4 | + | Fe |   → | FeSO4 | + | Cu | |
|---|---|---|---|---|---|---|---|
| Было: | 0,05 моль | 0,1 моль | — | — | |||
| Стало: | — | 0,05 моль | 0,05 моль | 0,05 моль |
3. Рассчитаем исходное количество сульфида натрия:
n(Na2S) = 117·0,1/78 = 0,15 моль
| FeSO4 | + | Na2S |   → | FeS | + | Na2SO4 | |
|---|---|---|---|---|---|---|---|
| Было: | 0,05 моль | 0,15 моль | — | — | |||
| Стало: | — | 0,15-0,05 = 0,1 моль | 0,05 моль | 0,05 моль |
Так как сульфат железа (II) в недостатке, в растворе останется 0,1 моль сульфида натрия.
m(Na2S) = 0,1·78 = 7,8 г.
4. Рассчитаем массу итогового раствор:
m(итогового р-ра) = m(исх. р-ра CuSO4) + m(железа, которое перешло в раствор) + m(р-ра Na2S) — m(Cu) — m(FeS)
m(исх. р-ра CuSO4) = 8/0,2 = 40 г.
m(железа, которое перешло в раствор) = 0,05·56 = 2,8 г.
m(ра-ра Na2S) = 117 г (по условию)
m(Cu) = 0,05·64 = 3,2 г.
m(FeS) = 0,05·88 = 4,4 г.
m(итогового р-ра) = 40 + 2,8 + 117 — 3,2 — 4,4 = 152,2 г.
w(Na2S) = 7,8/152,2 = 0,0512 или 5,1%.
Ответ: w(Na2S) = 5,1%.