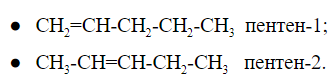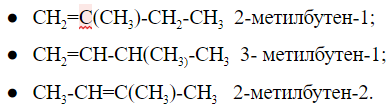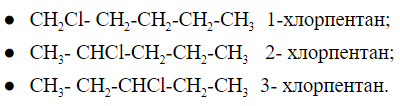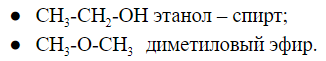Межклассовая изомерия

4.3
Средняя оценка: 4.3
Всего получено оценок: 285.
4.3
Средняя оценка: 4.3
Всего получено оценок: 285.
Один из видов структурной изомерии является межклассовая изомерия. В этом случае образуются изомеры между двумя классами органических веществ.
Изомерия
Вещества, сходные по содержанию и количеству атомов, но разные по структурному или пространственному строению, называются изомерами. Выделяют два типа изомерии:
- структурная;
- пространственная.
Структурная изомерия может происходить:
- по углеродному скелету
- по положению групп, связей или заместителей.
В некоторых случаях при перемещении функциональной группы образуется вещество другого класса. В этом случае говорят о межклассовой изомерии, которая также является структурной изомерией. Например, при перемещении гидроксильной группы из этанола (CH3-CH2-OH) образуется диметиловый эфир (CH3-O-CH3).
Пространственная изомерия показывает, как располагаются атомы углеродной цепочки в пространстве, и бывает двух видов:
- оптическая или зеркальная;
- геометрическая или цис-транс-изомерия.
При оптической изомерии образуются молекулы, будто являющиеся зеркальным отражением друг друга. Цис-транс-изомеры различаются положением заместителей по отношению к плоскости, делящей молекулу пополам. Если по одну сторону находятся одинаковые радикалы, такие изомеры называются цис-изомерами. Если одинаковые радикалы лежат по разным сторонам плоскости, они называются транс-изомерами.
Чем длиннее цепь, тем больше изомеров может образовывать вещество.
Межклассовые изомеры
При перемещении в углеродном скелете функциональной группы образуется новое вещество, которое относится к другому классу органических соединений. При этом у изомеров абсолютно одинаковые общие формулы.
В таблице наглядно показано, между какими классами веществ образуется изомерия, а также приведены примеры межклассовой изомерии.
|
Классы, образующие изомерию |
Общая формула |
Примеры |
|
Алкены и циклоалканы |
CnH2n |
Бутен-1 (CH2=CH-CH2-CH3) и циклобутан (C4H8) |
|
Алкадиены и алкины |
CnH2n-2 |
Бутадиен-1,3 (CH2=CH-CH=CH2) и бутин-1 (CH≡C-CH2-CH3) |
|
Одноатомные спирты и простые эфиры |
CnH2n+2O |
Бутанол-1 (CH3-CH2-CH2-CH2OH) и метилпропиловый эфир (CH3-O-CH2-CH2-CH3) |
|
Альдегиды и кетоны |
CnH2nO |
Бутаналь (CH3-CH2-CH2-COH) и бутанон-2 (CH2-CO-CH2-CH2-CH3) |
|
Карбоновые кислоты и сложные эфиры |
CnH2nO2 |
Бутановая кислота (CH3-CH2-CH2-COOH) и пропилформиат (COOH-CH2-CH2-CH3) |
|
Нитросоединения и аминокислоты |
CnH2n+1NO2 |
Нитробутан (CH3-CH2-CH2-CH2NO2) и альфа-аминобутановая кислота (CH3-CH2-CH-(NH2)COOH) |
Среди всех классов органических веществ алканы не образуют межклассовую изомерию.
Что мы узнали?
Некоторые классы органических веществ могут образовывать межклассовую изомерию при перемещении функциональной группы. Межклассовая изомерия является разновидностью структурной изомерии. Классы, образующие межклассовые изомеры: алкены с циклоалканами, алкадиены с алкинами, одноатомные спирты с простыми эфирами, альдегиды с кетонами, карбоновые кислоты со сложными эфирами, нитросоединения с аминокислотами.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
Пока никого нет. Будьте первым!
Оценка доклада
4.3
Средняя оценка: 4.3
Всего получено оценок: 285.
А какая ваша оценка?
Изомеры – это вещества, имеющие одинаковый состав (число атомов каждого типа), но разное взаимное расположение атомов – разное строение.
Изомерия – это явление существования веществ с одинаковым составом, но различным строением.
Например, формуле C4H10 соответствуют два изомерных соединения н-бутан с линейным углеродным скелетом и изобутан (2-метилбутан) с разветвленным скелетом:
При этом температура кипения н-бутана –0,5оС, а изобутана –11,4оС.
Виды изомерии
Различают два основных вида изомерии: структурную и пространственную (стереоизомерию).
Структурные изомеры отличаются друг от друга взаимным расположением атомов в молекуле; стереоизомеры — расположением атомов в пространстве.
Структурная изомерия
Структурные изомеры – соединения с одинаковым составом, но различным порядком связывания атомов, т.е. с различным химическим строением. Молекулярная формула у структурных изомеров одинаковая, а структурная различается.
1. Изомерия углеродного скелета: вещества различаются строением углеродной цепи, которая может быть линейная или разветвленная.
Например, молекулярной формуле С5Н12 соответствуют три изомера:
2. Изомерия положения обусловлена различным положением кратной связи, функциональной группы или заместителя при одинаковом углеродном скелете молекул.
2.1. Изомерия положения функциональной группы. Например, существует два изомерных предельных спирта с общей формулой С3Н8О: пропанол-1 (н-пропиловый спирт) пропанол-2 (изопропиловый спирт):
2.2. Изомерия положения кратной связи может быть вызвана различным положением кратной (двойной или тройной) связи в непредельных соединениях. Например, в бутене-1 и бутене-2:
2.3. Межклассовая изомерия – ещё один вид структурной изомерии, когда вещества из разных классов веществ имеют одинаковую общую формулу.
Например, формуле С2Н6О соответствуют: спирт (этанол) и простой эфир (диметиловый эфир):
Пространственная изомерия
Пространственные изомеры – это вещества с одинаковым составом и химическим строением, но с разным пространственным расположением атомов в молекуле. Виды пространственной изомерии – геометрическая (цис—транс) и оптическая изомерия.
1. Геометрическая изомерия (или цис-транс-изомерия).
Геометрическая изомерия характерна для соединений, в которых различается положение заместителей относительно плоскости двойной связи или цикла. Например, для алкенов и циклоалканов.
Двойная связь не имеет свободного вращения вокруг своей оси.
Поэтому заместители у атомов углерода при двойной связи могут быть расположены либо по одну сторону от плоскости двойной связи (цис-изомер), либо по разные стороны от плоскости двойной связи (транс-изомер). При этом никаким вращением нельзя получить из цис-изомера транс-изомер, и наоборот.
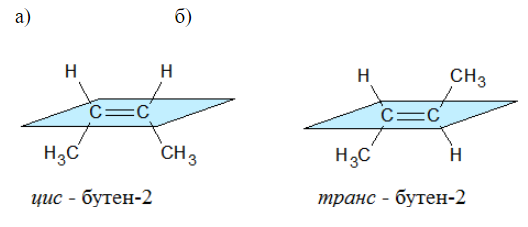
Например, бутен-2 существует в виде цис— и транс-изомеров
1,2-Диметилпропан также образует цис-транс-изомеры:
Геометрические изомеры различаются по физическим свойствам (температура кипения и плавления, растворимость, дипольный момент и др.). Например, температура кипения цис-бутена-2 составляет 3,73 оС, а транс-бутена-2 0,88оС.
При этом цис—транс-изомерия характерна для соединений, в которых каждый атом углерода при двойной связи С=С (или в цикле) имеет два различных заместителя.
Например, в молекуле бутена-1 CH2=CH-CH2-CH3 заместители у первого атома углерода при двойной связи (два атома водорода) одинаковые, и цис—транс-изомеры бутен-1 не образует. А вот в молекуле бутена-2 CH3—CH=CH-CH3 заместители у каждого атома углерода при двойной связи разные (атом водорода и метильная группа CH3), поэтому бутен-2 образует цис— и транс-изомеры.
Таким образом, для соединений вида СH2=СHR и СR2=СHR’ цис—транс-изомерия не характерна.
2. Оптическая изомерия
Оптические изомеры – это пространственные изомеры, молекулы которых соотносятся между собой как предмет и несовместимое с ним зеркальное изображение.
Оптическая изомерия свойственна молекулам веществ, имеющих асимметрический атом углерода.
Асимметрический атом углерода — это атом углерода, связанный с четырьмя различными заместителями.
Такие молекулы обладают оптической активностью — способностью к вращению плоскости поляризации света при прохождении поляризованного луча через раствор вещества.
Например, оптические изомеры образует 3-метилгексан:
Стереоизомерия и стереоизомеры
Сам феномен существования соединений, имеющих одинаковый химический состав (количественный и качественный), но различное строение и, соответственно, разные свойства, называется изомерией (впервые термин был введён в 1830 И. Берцелиусом). Выделяют два её основных вида: пространственную (стереоизомерия) и структурную. К пространственной относятся:
- геометрическая, заключающаяся в пространственном расположении функциональных групп относительно кратных связей. Существуют цис-изомеры, лежащие по одну сторону от заместителя при кратной связи, и транс-изомеры, располагающиеся по разные стороны;
- оптическая, заключающаяся в разном направлении отклонения плоскости поляризации (характерна только для соединений, содержащих несимметричные атомы углерода) и разделяющая изомеры на левовращающие и правовращающие.
Организм чутко реагирует на геометрические и оптические изомеры, к которым относятся большинство нуклеиновых кислот, витаминов, сахаров и гормонов.
Одно и то же вещество в зависимости от своего пространственного строения может оказаться как незаменимым для жизнедеятельности человека реагентом, так и опасным ядом. Невозможным является решение вопросов медицины и биохимии без учёта явления изомерии.
Структурное многообразие
Структурная изомерия основана на различиях в строении химического соединения. Так как, согласно теории Бутлерова, атомы и их группировки в молекуле не существуют изолированно, а оказывают определённое воздействие друг на друга, то даже простейшая перестановка вызывает необратимое изменение свойств вещества. Принято деление структурных различий на четыре типа:
- изменение в углеродном скелете (возможно для углеводородов, содержащих более трёх атомов углерода в цепи);
- изменение положения кратной связи или функциональной группы;
- изомерия «нецельных структур», или метамерия (для молекул, радикалы в которых разделены гетероатомом, — простые и сложные эфиры, тиоспирты и т. д. );
- межклассовая изомерия.
Наиболее критично между собой различаются изомеры последнего вида, так как, несмотря на своё формальное сходство (содержание одного и того же количества атомов, функциональных групп и заместителей) они относятся к различным классам органических соединений.
Примеры межклассовых изомеров
Наиболее доступным способом изучения изомеров между классами органических соединений является составление таблицы, включающей в себя химическую формулу, общую для гомологов обоих классов, и примеры изомерных друг другу веществ.
| Общая формула | Классы | Примеры |
| СnH2n | Циклоалканы и алкены | Циклогептан и 2 -этил 3 — метилбутен-2, циклогексан и гексен-1 |
| CnH2n-2 | Алкины и алкадиены (алкадиеновые или диеновые углеводороды) | Пропин и пропандиен, 2-метилпропин-3 и бутадиен — 1,2 |
| CnH2nO | Альдегиды и кетоны | 2-метилпропаналь и бутанон-2 |
| CnH2nO2 | Сложные эфиры и карбоновые кислоты | Пропилформиат и бутановая кислота |
| CnH2n+2O | Простые эфиры и одноатомные спирты | Диметиловый эфир и этанол |
| CnH2n+1NO2 | Аминокислоты и нитросоединения | Альфааминобутановая кислота и нитробутан |
Для каждого вида изомерии существуют свои способы различения веществ — как по физическим, так и по химическим свойствам. Например, кислоты и эфиры отличаются тем, что первые легко вступают во взаимодействие со щелочами, активными металлами и оксидами, а вторые характеризуются относительной реакционной инертностью.
Кроме того, многие органические соединения обладают специфическим запахом (уксусная кислота — едкий, уксусно-амиловый эфир — эфирный аромат, напоминающий грушу).
Содержание
- 1 Определение
- 2 Структурная изомерия
- 2.1 Изомерия углеродного скелета
- 2.2 Изомерия положения кратной связи
- 2.3 Изомерия положения функциональной группы
- 2.4 Валентная изомерия
- 2.5 Межклассовая изомерия
- 3 Изомерия статическая и динамическая
- 4 Стереоизомерия
- 4.1 Цис-транс — изомерия (геометрическая)
- 4.2 Оптическая изомерия
- 5 Правила построения формул Фишера
- 6 Заключение
Органические соединения с одинаковым качественным и количественным составом – изомеры — могут отличаться по свойствам. Причиной является различное строение, которое определяет отношение веществ к классу соединений.
Чтобы определить класс недостаточно оперировать молекулярной формулой вещества – необходимо знать графическую формулу, которая показывает структурное и пространственное расположение атомов в молекуле.
Определение
Изомеры — это химические соединения с идентичным атомным составом, но различные по строению или пространственному расположению атомов. Изомеры имеют разные химические свойства.
Основные виды изомерии:
- структурные;
- пространственные.
Структурная изомерия
Структурные изомеры – химические вещества, при одинаковом качественном и количественном составе различающиеся порядком расположения атомов – строением вещества.
Выделяют шесть видов структурной изомерии:
Изомерия углеродного скелета
Пентан имеет три структурные формулы изомеров:
Изомерия положения кратной связи
При общей формуле пентен имеет два изомера, различающихся расположением двойной связи:
У изомеров положения кратной связи параллельно может быть изомерия углеродного скелета. Для пентена это:
Общее число структурных изомеров пентена равно пяти, из которого два изомера положения двойной связи и три изомера углеродного скелета.
Изомерия положения функциональной группы
К функциональным группам относятся фрагменты органических соединений, определяющие их свойства.
Для примера: -ОН гидроксильная, -СООН карбоксильная, -NH2 аминогруппа, -CN цианогруппа и другие.
Как выглядит изомерия положения можно рассмотреть на примере пентана и -Cl в качестве функциональной группы:
Хлорпентан имеет 3 положения функциональной группы, которые различаются между собой местом расположения заместителя на углеродной цепи.
Валентная изомерия
Изомеры, которые можно перевести из одного в другой путем перераспределения внутренних связей называют валентными. Внутримолекулярная перегруппировка является не катализируемым и не зависящим от растворителя процессом.
На внутримолекулярные изменения, влияет температура, в случае с бензолом Хюккеля УФ-облучение.
Пример:
бензол – у этого простейшего ароматического углеводорода, известны три валентных изомера:
Бензол Дьюара трансформируется в обычный бензол при t 20°С за 48 часов, при t 90°С для изомеризации достаточно 30 минут.
Преобразование бензола в бензвален (бензол Хюккеля) происходит при его облучении УФ-светом с определенной длиной волны.
Призман – самый нестабильный из изомеров бензола.
Межклассовая изомерия
Соединения, имеющие общую формулу, могут содержать функциональные группы, относящиеся к разным классам соединений.
Общую формулу имеют два вещества:
Изомерия статическая и динамическая
Различают типы изомерии:
- статическая – изомеры образуются в результате химического процесса изомеризации;
- динамическая – несколько изомеров существуют одномоментно и легко переходят друг в друга.
К статической относятся изомерия углеродного скелета, положения кратной связи, функциональной группы, межклассовая и валентная.
Пример динамической изомерии – прототропная таутомерия, при которой обратимая изомеризация происходит за счет перехода протона водорода внутри молекулы.
Это интересно:
Изомеры гексана
Изомеры пентена
Гомологический ряд алкенов
Стереоизомерия
В пространственных изомерах с одинаковой структурной формулой, атомы молекулы ориентированы в пространстве по-разному.
Чем же отличается структурная изомерия от пространственной: первая рассматривает порядок атомов в молекуле на плоскости, а вторая – в объеме.
Стереоизомерия делится на геометрическую (цис-транс) и оптическую.
Цис-транс — изомерия (геометрическая)
Геометрические изомеры присутствуют в веществах, имеющих двойные связи или циклы.
Подразделяют геометрические изомеры относительно плоскости, в которой расположена π-связь или закольцованный цикл.
Изомеры, у которых одинаковые заместители расположены по одну сторону от плоскости называют цис- изомерами.
Соединения, у которых заместители расположены по разные стороны от плоскости π-связь или кольца называют транс- изомерами.
Наглядной иллюстрацией могут служить простейшие геометрические изомеры — бутен-:
Оптическая изомерия
При исследовании веществ с одинаковой структурной формулой на поляриметре было выявлено явление вращения плоскости поляризованного света. Такие вещества получили название оптически активных веществ.
Исследования показали, что молекулы этих веществ хиральны, то есть несовместимы со своим отражением в зеркале. Хиральные вещества присутствуют в виде двух оптических антиподов (энантиомеров), один из которых правовращающий (+), а другой – левовращающий (-).
Определить знак оптического изомера можно с помощью поляриметра.
Причина хиральности состоит в присутствии ассиметрического атома углерода – связанного с четырьмя различными заместителями.
Хиральные молекулы невозможно совместить, так как они зеркально симметричны.
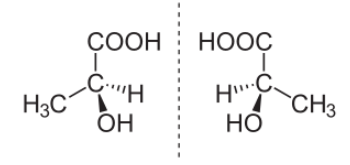
Пример пары стереоизомеров, представляющих зеркальные отражения:
(S)-(+)- Молочная кислота (слева) и (R)-(-)-Молочная кислота (справа).
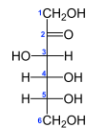
Для изображения оптических изомеров используют проекционные формулы Э.Фишера.
Правила построения формул Фишера
Изображают стереоизомеры с ассиметрическим атомом углерода на плоскости в виде проекционных форм, предложенных в конце XIX века Э.Фишером.
Правила изображения проекции Фишера:
- Углеродный скелет располагается в пространстве вертикально, нумерация атомов углерода идет сверху вниз.
- Горизонтальные связи в проекции направлены к наблюдателю, а вертикальные – от него.
Правила пользования проекциями Фишера имеют ограничения:
- проекция корректна только в плоскости чертежа;
- нельзя разворачивать чертеж на 90° и 270°, так как вертикальные и горизонтальные линии меняются местами;
- допускается разворот на 180°.
Номенклатура стереоизомеров основана на правиле последовательности заместителей при асимметрическом атоме углерода по старшинству (определяется как порядковый номер в Периодической таблице). Учитывается направление уменьшения старшинства: падение по часовой стрелке обозначается как R, против – как S.
Заключение
Все виды изомерии органических соединений делят на две части – структурная изомерия и пространственная.
Изомеры, относящиеся к первой группе, различаются порядком соединения атомов, а ко второй – только их пространственным расположением. Классификация изомеров опирается на различия между ними. Изучение множества структурных и пространственных форм веществ стали возможны благодаря работам А.М.Бутлерова и Я.Г.Вант-Гоффа.
Межклассовая изомерия – примеры
На чтение 3 мин Просмотров 3
Один из видов структурной изомерии является межклассовая изомерия. В этом случае образуются изомеры между двумя классами органических веществ.
Изомерия
Вещества, сходные по содержанию и количеству атомов, но разные по структурному или пространственному строению, называются изомерами. Выделяют два типа изомерии:
- структурная;
- пространственная.
Структурная изомерия может происходить:
- по углеродному скелету
- по положению групп, связей или заместителей.
В некоторых случаях при перемещении функциональной группы образуется вещество другого класса. В этом случае говорят о межклассовой изомерии, которая также является структурной изомерией. Например, при перемещении гидроксильной группы из этанола (CH3-CH2-OH) образуется диметиловый эфир (CH3-O-CH3).
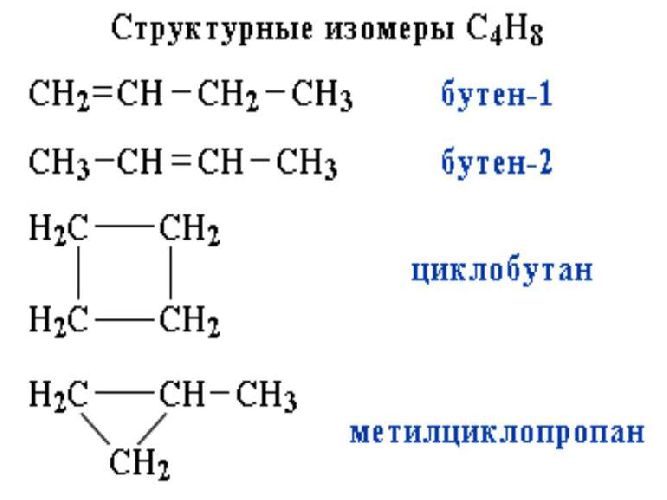
Рис. 1. Примеры структурной изомерии.
Пространственная изомерия показывает, как располагаются атомы углеродной цепочки в пространстве, и бывает двух видов:
- оптическая или зеркальная;
- геометрическая или цис-транс-изомерия.
При оптической изомерии образуются молекулы, будто являющиеся зеркальным отражением друг друга. Цис-транс-изомеры различаются положением заместителей по отношению к плоскости, делящей молекулу пополам. Если по одну сторону находятся одинаковые радикалы, такие изомеры называются цис-изомерами. Если одинаковые радикалы лежат по разным сторонам плоскости, они называются транс-изомерами.
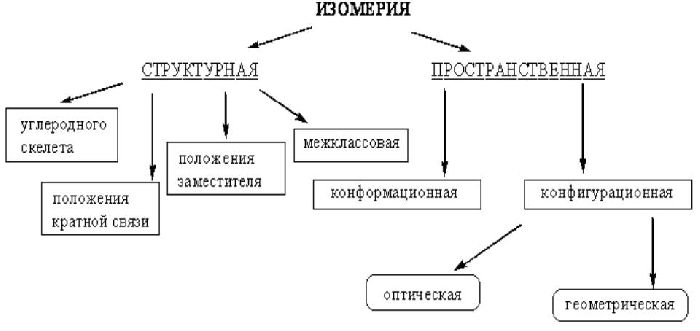
Рис. 2. Схема классификации изомерии.
Чем длиннее цепь, тем больше изомеров может образовывать вещество.
Межклассовые изомеры
При перемещении в углеродном скелете функциональной группы образуется новое вещество, которое относится к другому классу органических соединений. При этом у изомеров абсолютно одинаковые общие формулы.
В таблице наглядно показано, между какими классами веществ образуется изомерия, а также приведены примеры межклассовой изомерии.
|
Классы, образующие изомерию |
Общая формула |
Примеры |
|
Алкены и циклоалканы |
CnH2n |
Бутен-1 (CH2=CH-CH2-CH3) и циклобутан (C4H8) |
|
Алкадиены и алкины |
CnH2n-2 |
Бутадиен-1,3 (CH2=CH-CH=CH2) и бутин-1 (CH≡C-CH2-CH3) |
|
Одноатомные спирты и простые эфиры |
CnH2n+2O |
Бутанол-1 (CH3-CH2-CH2-CH2OH) и метилпропиловый эфир (CH3-O-CH2-CH2-CH3) |
|
Альдегиды и кетоны |
CnH2nO |
Бутаналь (CH3-CH2-CH2-COH) и бутанон-2 (CH2-CO-CH2-CH2-CH3) |
|
Карбоновые кислоты и сложные эфиры |
CnH2nO2 |
Бутановая кислота (CH3-CH2-CH2-COOH) и пропилформиат (COOH-CH2-CH2-CH3) |
|
Нитросоединения и аминокислоты |
CnH2n+1NO2 |
Нитробутан (CH3-CH2-CH2-CH2NO2) и альфа-аминобутановая кислота (CH3-CH2-CH-(NH2)COOH) |
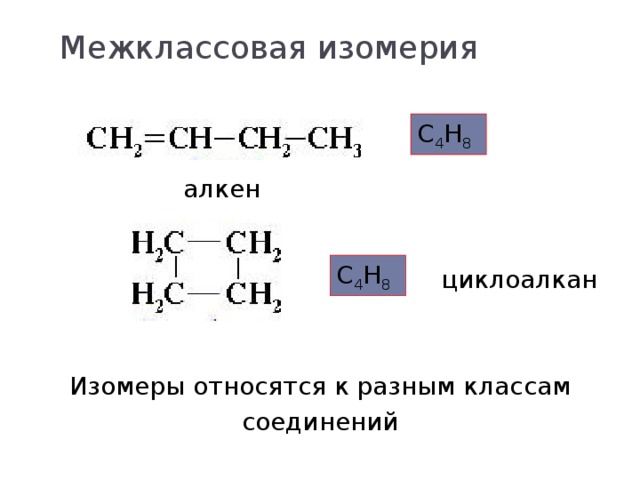
Рис. 3. Примеры межклассовой изомерии.
Среди всех классов органических веществ алканы не образуют межклассовую изомерию.
Что мы узнали?
Некоторые классы органических веществ могут образовывать межклассовую изомерию при перемещении функциональной группы. Межклассовая изомерия является разновидностью структурной изомерии. Классы, образующие межклассовые изомеры: алкены с циклоалканами, алкадиены с алкинами, одноатомные спирты с простыми эфирами, альдегиды с кетонами, карбоновые кислоты со сложными эфирами, нитросоединения с аминокислотами.
Беликова Ирина
Учитель физики, информатики и вычислительной техники. Победитель конкурса лучших учителей Российской Федерации в рамках Приоритетного Национального Проекта «Образование».