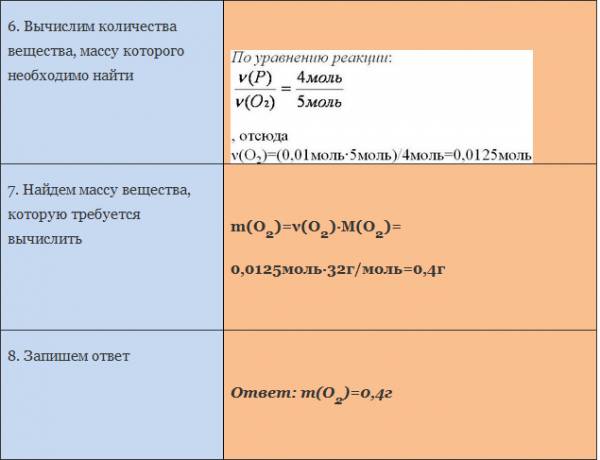
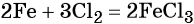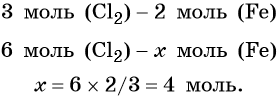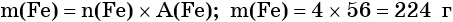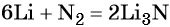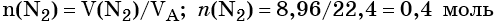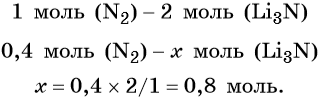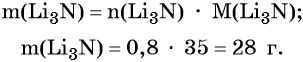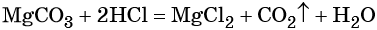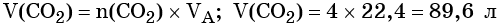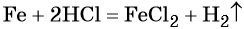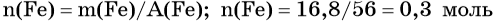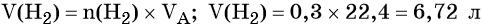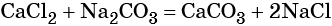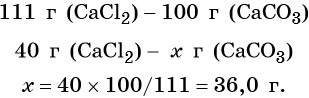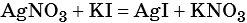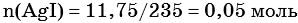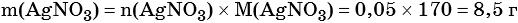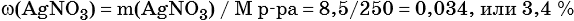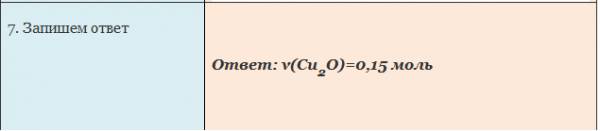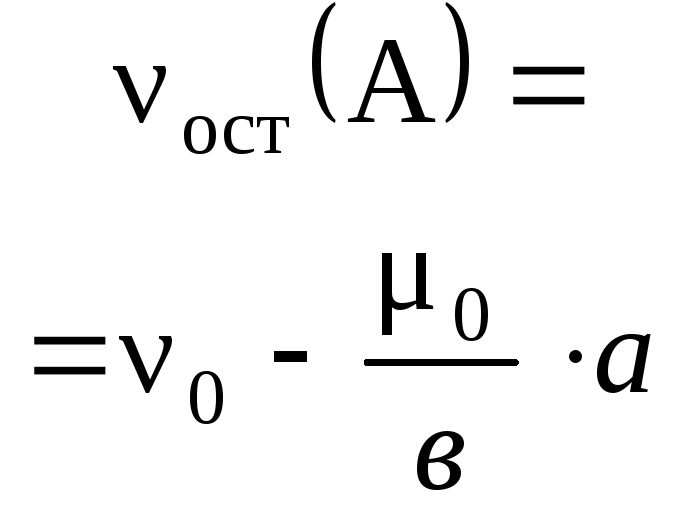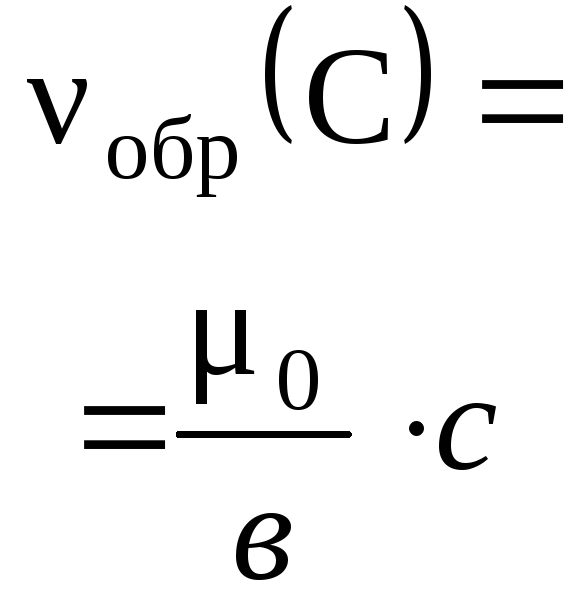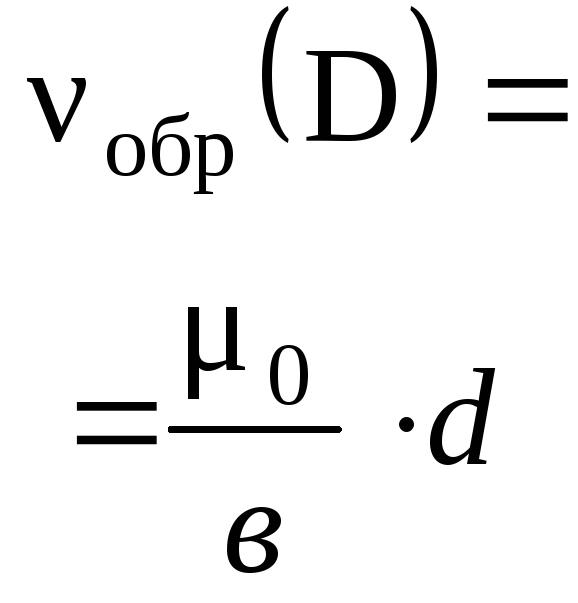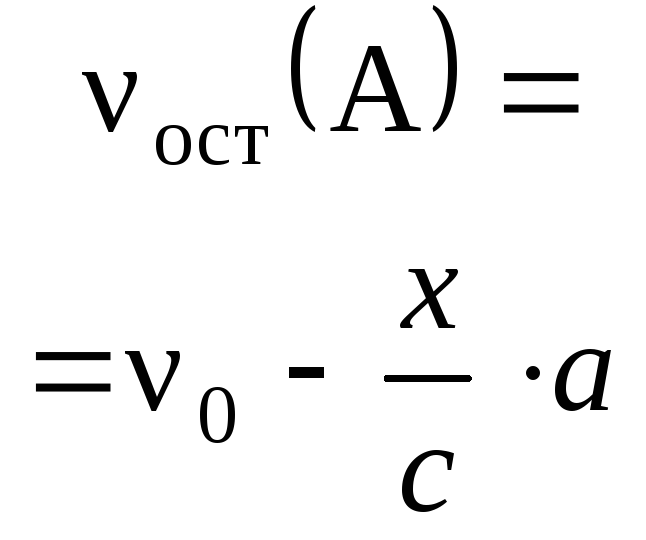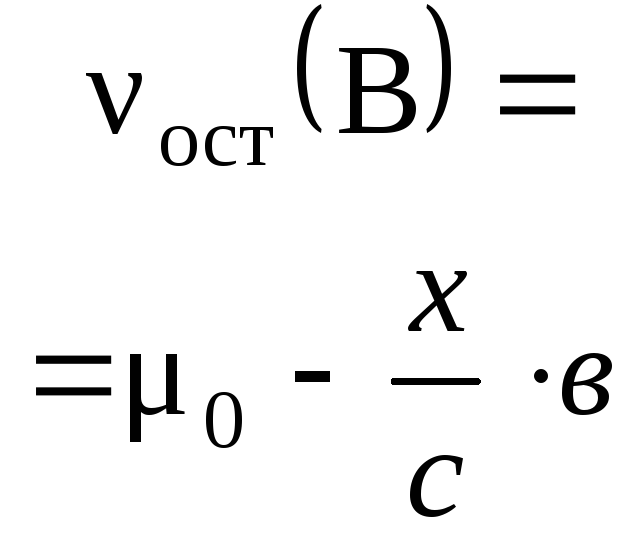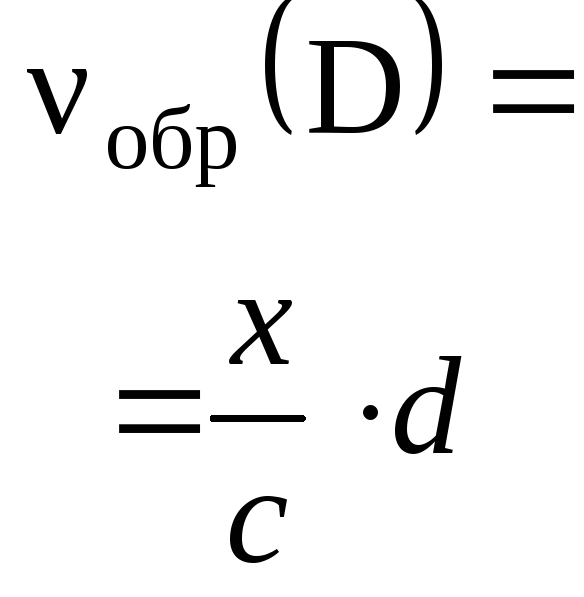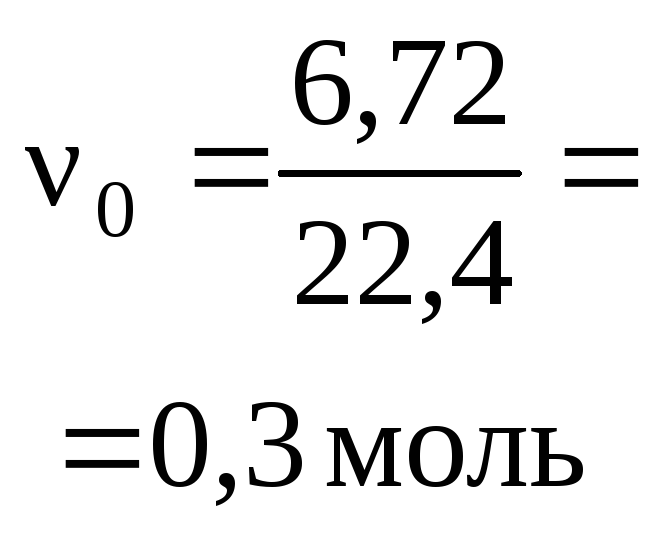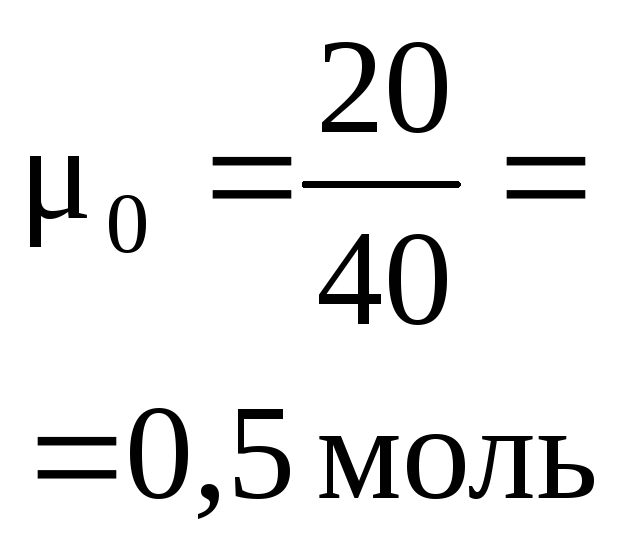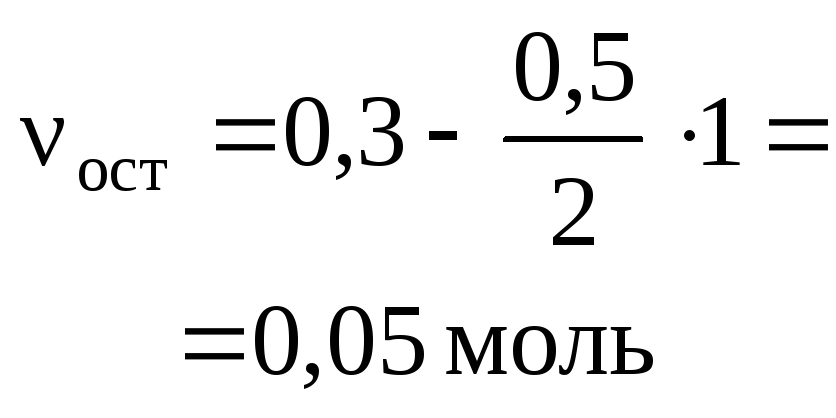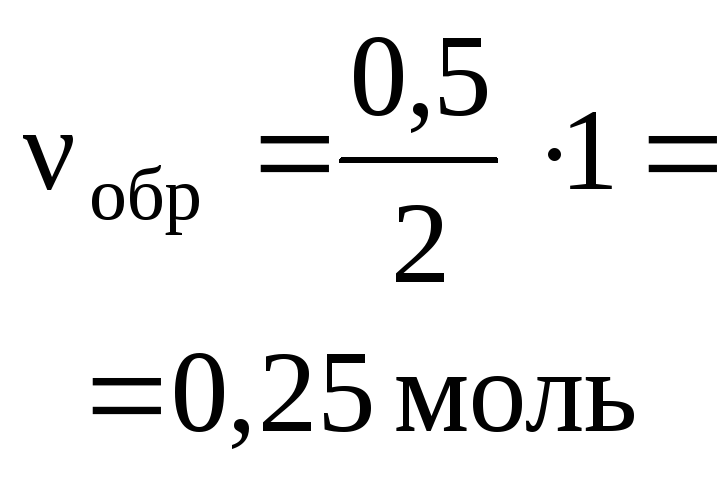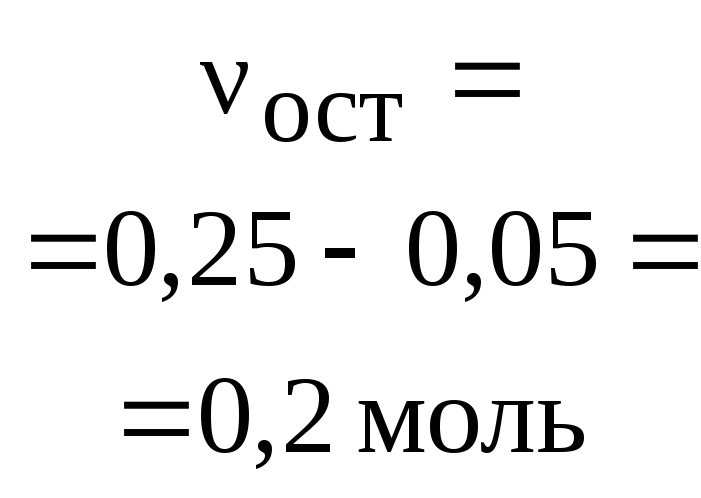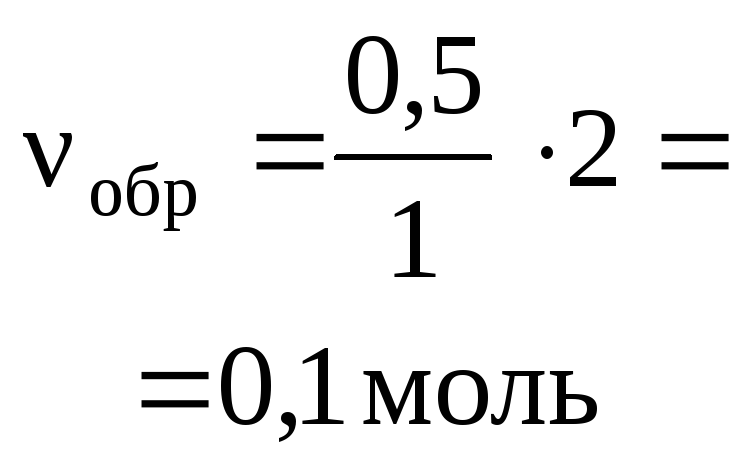Как решать задачи по химии? Как проводить простейшие расчеты по уравнениям химических реакций? Сколько выделяется газа, образуется воды, выпадает осадка или сколько получается конечного продукта реакций? Сейчас мы постараемся разобрать все нюансы и ответить на эти вопросы, которые очень часто возникают при изучении химии.
Решение задач в химии является неотъемлемой частью в изучении этой сложной, но очень интересной науки.
Алгоритм решения задач по химии
- Прочитать условия задачи (если они есть). Да, об этом все знают — как же решить задачу без условий — но все же, для полноты инструкции, мы не могли не указать этот пункт.
- Записать данные задачи. На этом пункте мы не будем заострять внимание, так как требования различных учебных заведений, учителей и преподавателей могут значительно отличаться.
- Записать уравнение реакции. Теперь начинается самое интересное! Здесь нужно быть внимательным! Обязательно необходимо верно расставить коэффициенты перед формулами веществ. Если вы забудете это сделать, то все наши усилия буду напрасны.
- Провести соответствующие расчеты по химическому уравнению. Далее рассмотрим, как же сделать эти самые расчеты.
Для этого у нас есть два пути, как решить задачу по химии. Условно, назовем их правильным (используя понятия количества вещества) и неправильным (используя пропорции). Конечно же, мы бы рекомендовали решать задачи правильным путем. Так как у неправильного пути имеется очень много противников. Как правило, учителя считают, что ученики, решающие задачи через пропорции, не понимают самой сути протекания процессов химических реакций и решают задачи просто математически.
Расчет по уравнениям химических реакций с использованием понятия количества вещества
Суть данного метода, состоит в том, что вещества реагируют друг с другом в строгом соотношении. И уравнение реакции, которое мы записали ранее, дает нам это соотношение. Коэффициенты перед формулами веществ дают нам нужные данные для расчетов.
Для примера, запишем простую реакцию нейтрализации серной кислоты и гидроксида натрия.
H_{2}SO_{4} + NaOH → Na_{2}SO_{4} + H_{2}O
Расставим коэффициенты:
H_{2}SO_{4} + 2NaOH → Na_{2}SO_{4} + 2H_{2}O
Исходя из этого уравнения, мы видим, что одна молекула серной кислоты взаимодействует с двумя молекулами гидроксида натрия. И в результате этой реакции получается одна молекула сульфата натрия и две молекулы воды.
Сейчас мы немного отступим от разбора задач, чтобы познакомиться с основными понятиями, которые пригодятся нам в решении задач по химии.
Рассчитывать количество молекул, например в 98 граммах серной кислоты — это не самое удобное занятие. Числа будут получаться огромными ( ≈ 6,022140857⋅1023 молекул в 98 граммах серной кислоты) . Для этого в химии ввели понятие количества вещества (моль) и молярная масса.
1 Моль (единица измерения количества вещества) — это такое количество атомов, молекул или каких либо еще структурных единиц, которое содержится в 12 граммах изотопа углерода-12. Позднее выяснилось, что в 12 граммах вещества углерод-12 содержится 6,022140857⋅1023 атомов. Соответственно, можно сказать, что 1 моль, это такая масса вещества, в которой содержится 6,022140857⋅1023 атомов (или молекул) этого вещества.
Но ведь молекулы и атомы имеют различный состав и различное строение. Разные атомы содержат разное количество протонов и нейтронов. Соответственно 1 моль для разных веществ будет иметь разную массу, имея при это одинаковое количество молекул ( атомов). Эта масса называется молярной.
Молярная масса — это масса 1 моля вещества.
Используя данные понятия, можно сказать, что 1 моль серной кислоты реагирует с 2 молями гидроксида натрия, и в результате получается 1 моль сульфата натрия и 2 моль воды. Давайте запишем эти данные под уравнением реакции для наглядности.
begin{matrix}H_{2}SO_{4} & + & 2NaOH & → & Na_{2}SO_{4} & + & 2H_{2}O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль end{matrix}
Следом запишем молярные массы для этих веществ
begin{matrix} H_{2}SO_{4} & + & 2NaOH & → & Na_{2}SO_{4} & + & 2H_{2}O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль \ 98 : г& & 40 : г & & 142 : г & & 18 : г end{matrix}
Теперь, зная массу одного из веществ, мы можем рассчитать, сколько нам необходимо второго вещества для полного протекания реакции, и сколько образуется конечных продуктов.
Для примера, решим по этому же уравнению несколько задач.
Задача. Сколько грамм гидроксида натрия (NaOH) необходимо для того, чтобы 49 грамм серной кислоты (H2SO4) прореагировало полностью?
Итак, наши действия: записываем уравнение химической реакции, расставляем коэффициенты. Для наглядности, запишем данные задачи над уравнением реакции. Неизвестную величину примем за Х. Под уравнением записываем молярные массы, и количество молей веществ, согласно уравнению реакции:
begin{matrix}49 : г & & X : г & & & & \ H_{2}SO_{4} & + & 2NaOH & → & Na_{2}SO_{4} & + & 2H_{2}O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль \ 98 : г& & 40 : г & & 142 : г & & 18 : г end{matrix}
Записывать данные под каждым веществом — не обязательно. Достаточно это будет сделать для интересующих нас веществ, из условия задачи. Запись выше дана для примера.
Примерно так должны выглядеть данные, записанные по условиям задачи. Не претендуем на единственно правильное оформление, требования у всех разные. Но так, как нам кажется, смотрится все довольно наглядно и информативно.
Первое наше действие — пересчитываем массу известного вещества в моли. Для этого разделим известную массу вещества (49 грамм) на молярную массу:
4998=0,5 моль серной кислоты
Как уже упоминалось ранее, по уравнению реакции 1 моль серной кислоты реагирует с 2 моль гидроксида натрия. Соответственно с 0,5 моль серной кислоты прореагирует 1 моль гидроксида натрия.
n(NaOH)=0.5*2=1 моль гидроксида натрия
Найдем массу гидроксида натрия, умножив количество вещества на молярную массу:
1 моль * 40 г/моль = 40 грамм гидроксида натрия.
Ответ: 40 грамм NaOH
Как видите, в решении задачи по уравнению реакции нет ничего сложного. Задача решается в 2-3 действия, с которыми справятся ученики начальных классов. Вам необходимо всего лишь запомнить несколько понятий.
Решение задач по химии через пропорцию
Ну и расскажем про второй способ вычислений по уравнениям химических реакций — вычисления через пропорцию. Этот способ может показаться немного легче, так как в некоторых случаях можно пропустить стадию перевода массы вещества в его количество. Чтобы было более понятно, объясню на том же примере.
Так же, как и в прошлом примере, запишем уравнение реакции, расставим коэффициенты и запишем над уравнением и под уравнением известные данные.
Для этого способа, нам так же понадобится записать под уравнением реакции, следом за молярной массой, массу вещества, соответствующую его количеству по уравнению. Если проще, то просто перемножить две строки под уравнением реакции, количество моль и молярную массу. Должно получиться так:
begin{matrix}49 : г & & X : г & & & & \ H_{2}SO_{4} & + & 2NaOH & → & Na_{2}SO_{4} & + & 2H_{2}O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль \ 98 : г& & 40 : г & & 142 : г & & 18 : г \ 98 : г & & 80 : г & & 142 : г & & 36 : г end{matrix}
А теперь внимание, начинается магия! Нас интересует строка данных над уравнением, и самая нижняя строка под уравнением. Составим из этих данных пропорцию.
frac{49}{98} = frac{X}{80}
Далее находим неизвестное значение Х из пропорции и радуемся полученному значению:
Х=49*80/98=40 грамм
Как видим, получается тот же результат. Прежде всего, при решении задач в химии, главное все же — понимание химических процессов. Тогда решение задачи не станет для вас проблемой!
Вычисление количества вещества, массы или объема вещества по количеству веществ, массе или объему одного из реагентов или продуктов реакции
Основой для проведения количественных расчётов в химии является закон сохранения массы. Согласно этому закону масса реагентов равна массе продуктов реакции.
Отсюда следует, что для любой химической реакции массы реагентов и продуктов реакции относятся между собой как молярные массы веществ, умноженные на их стехиометрические коэффициенты.
Для расчёта по химическим уравнениям можно использовать два эквивалентных способа: через количество вещества или через пропорцию. Подчеркнём ещё раз: официального запрета на использование метода пропорций при решении задач на ОГЭ и ЕГЭ нет!
Для определения массы (или количества вещества) продуктов реакции или исходных веществ по уравнениям химических реакций вначале составляют уравнение химической реакции и устанавливают стехиометрические коэффициенты; затем определяют молярную массу, массу и количество вещества известных реагентов химической реакции; составляют и решают пропорцию, в которую в зависимости от условий задачи вводят числовые значение величин: молярные массы, массы, количества веществ или их объёмы (для газов).
При этом в одном столбце пропорций должны находиться одинаковые характеристики вещества с одной и той же размерностью.
Пример 1. Масса железа, вступившего в реакцию с 6 моль хлора, равна _________ г. (Ответ запишите с точностью до целого числа.)
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что 3 моль Cl2 реагируют с 2 моль Fe, т. е.:
Определяем массу железа:
Пример 2. Масса нитрида лития, образовавшегося в результате его реакции с азотом объёмом 8,96 л, равна_______________ г.
Решение. Составляем уравнение химической реакции:
Определяем количество вещества азота, вступившего в реакцию:
Из уравнения реакции следует, что из 1 моль N2 образуется 2 моль Li3N, т. е.:
Определим массу Li3N:
Пример 3. Объём углекислого газа, образовавшегося в результате разложения карбоната магния количеством вещества 4 моль избытком соляной кислоты, равен________ л.
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что количество вещества углекислого газа и карбоната магния равны между собой, т. е. n(CO2) = 4 моль.
Определим V(CO2):
Пример 4. Объём водорода, который выделится при растворении 16,8 г железа в избытке разбавленной соляной кислоты, равен _________ л.
Решение. Составляем уравнение химической реакции:
Определим количество вещества железа:
Количество вещества железа и водорода в данном уравнении реакции равны между собой. Следовательно, количество вещества водорода также равно 0,3 моль.
Вычислим объём водорода:
Пример 5. Масса осадка, который образуется в результате взаимодействия 40,0 г хлорида кальция с избытком карбоната натрия, равна _________г.
Решение. Составляем уравнение реакции:
Согласно уравнению химической реакции составим пропорцию и решим её:
Пример 6. 250 г раствора нитрата серебра смешали с избытком раствора йодида калия. Выпал осадок массой 11,75 г. Вычислите массовую долю нитрата серебра в исходном растворе.
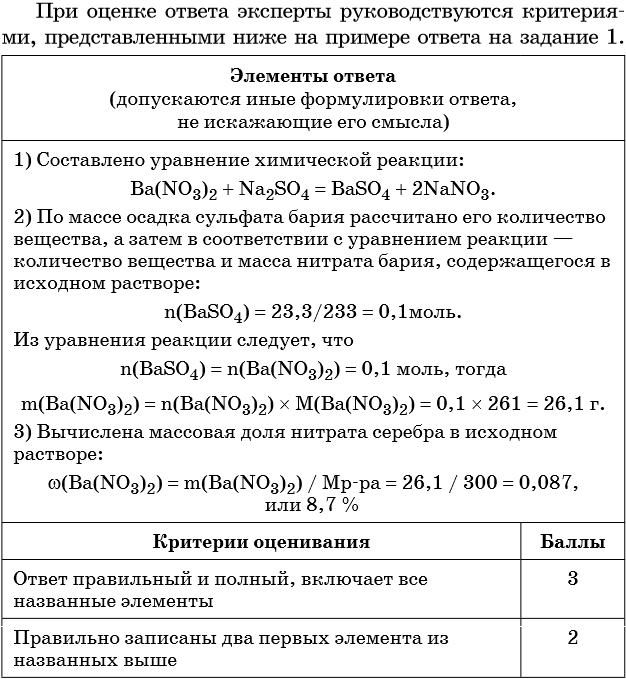
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысла)
1) Составлено уравнение химической реакции:
2) По массе осадка йодида серебра рассчитано его количество вещества, а затем в соответствии с уравнением реакции — количество вещества и масса нитрата серебра, содержащегося в исходном растворе:
Из уравнения реакции следует, что n(AgI) = n(AgNO3) = 0,05 моль, тогда:
3) Вычислена массовая доля нитрата серебра в исходном растворе:
| Критерии оценивания | Баллы |
| Ответ правильный и полный, включает все названные элементы | 3 |
| Правильно записаны два первых элемента из названных выше | 2 |
| Правильно записан один из названных выше элементов (1-й или 2-й) | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
Тренировочные задания
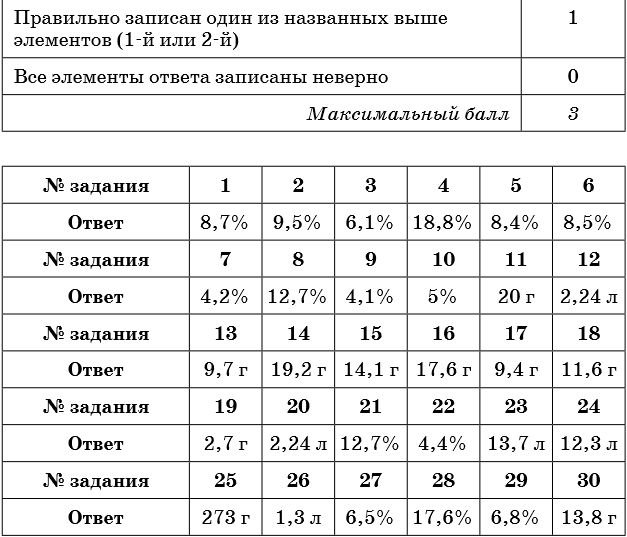
1. К 300 г раствора нитрата бария прибавили избыток раствора сульфата натрия. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
2. К 150 г раствора сульфата натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
3. К 300 г раствора силиката натрия прибавили избыток раствора нитрата кальция. Масса выпавшего осадка составила 12,0 г. Определите концентрацию соли в исходном растворе.
4. К 150 г раствора карбоната калия прибавили избыток раствора соляной кислоты. При этом выделился газ объёмом 3,36 л (н. у.). Определите концентрацию соли в исходном растворе.
5. К 250 г раствора гидрокарбоната натрия прибавили избыток раствора бромоводородной кислоты. При этом выделился газ объёмом 5,6 л. Определите концентрацию соли в исходном растворе.
6. К 50 г раствора карбоната натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
7. К 200 г раствора хлорида бария прибавили избыток раствора карбоната калия. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
8. К 200 г раствора хлорида железа (II) прибавили избыток раствора гидроксида калия. Масса выпавшего осадка составила 18,0 г. Определите концентрацию соли в исходном растворе.
9. К 400 г раствора нитрата свинца прибавили избыток раствора йодида натрия. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
10. К 300 г раствора йодида натрия прибавили избыток раствора нитрата свинца. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
11. Определите массу осадка, который выпадет при взаимодействии 150 г 14,8%-ного раствора хлорида кальция с избытком раствора карбоната натрия.
12. Определите объём газа (н. у.), который выделится при взаимодействии 120 г 8,8%-ного раствора карбоната натрия с избытком раствора соляной кислоты.
13. Определите массу соли, которая выпадет в осадок при взаимодействии 140 г 13,5%-ного раствора нитрата цинка с избытком раствора сульфида натрия.
14. Определите массу осадка, который выделится при взаимодействии 200 г 18,8%-ного раствора нитрата меди с избытком раствора сульфида натрия.
15. Определите массу осадка, который выпадет при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора хлорида цинка.
16. Определите массу осадка, который выделится при взаимодействии 200 г 12,7%-ного раствора хлорида железа (II) с избытком раствора сульфида натрия.
17. Определите массу осадка, который выделится при взаимодействии 50 г 17%-ного раствора нитрата серебра с избытком раствора бромида калия.
18. Определите массу осадка, который образуется при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора нитрата кальция.
19. Определите массу осадка, который образуется при взаимодействии 50 г 5,8%-ного раствора хлорида магния с избытком раствора фосфата натрия.
20. Определите объём газа, который выделится при взаимодействии 200 г 6,9%-ного раствора карбоната калия с избытком раствора соляной кислоты.
21. Оксид фосфора (V) массой 21,3 г растворили в растворе гидроксида калия, в результате чего был получен раствор средней соли массой 500 г. Определите концентрацию фосфата калия в конечном растворе.
22. Раствор хлорида железа (II) полностью прореагировал со 120 г раствора гидроксида натрия, в результате чего образовалось 6,0 г осадка. Определите массовую долю гидроксида натрия в исходном растворе.
23. Какой объём аммиака (н. у.) может полностью прореагировать со 150 г 20%-ного раствора серной кислоты с образованием средней соли?
24. В 200 г 20%-ного раствора соляной кислоты растворили магний до прекращения выделения газа. Определите объём выделившегося при этом водорода (н. у.).
25. Аммиак объёмом 10 л (н. у.) пропустили через раствор серной кислоты с массовой долей 8% до образования средней соли. Определите массу исходного раствора.
26. Определите объём сероводорода (н. у.), который необходимо пропустить через 130 г 6%-ного раствора хлорида меди (II) до полного осаждения сульфида меди (II).
27. Сероводород объёмом 3,36 л (н. у.) пропустили через раствор гидроксида натрия, в результате чего получили 180 г раствора сульфида натрия. Определите массовую долю соли в полученном растворе.
28. Алюминий массой 8,1 г может нацело прореагировать с 250 г раствора серной кислоты. Определите массовую долю серной кислоты в исходном растворе.
29. К 250 г раствора нитрата серебра добавили раствор хлорида калия до прекращения выделения осадка, масса которого составила 14,35 г. Определите массовую долю нитрата серебра в исходном растворе.
30. К 300 г 5%-ного раствора хлорида магния добавили избыток раствора фосфата калия. Вычислите массу выпавшего при этом осадка.
Ответы
Комментарии преподавателя
Соотношение количеств веществ, участвующих в реакции
Коэффициенты в уравнении реакции показывают не только число молекул каждого вещества, но и соотношение количеств веществ, участвующих в реакции. Так, по уравнению реакции: 2H2 + O2 = 2H2O – можно утверждать, что для образования определенного количества воды (например, 2 моль) необходимо столько же моль простого вещества водорода (2 моль) и в два раза меньше моль простого вещества кислорода (1 моль). Приведем примеры подобных расчетов.
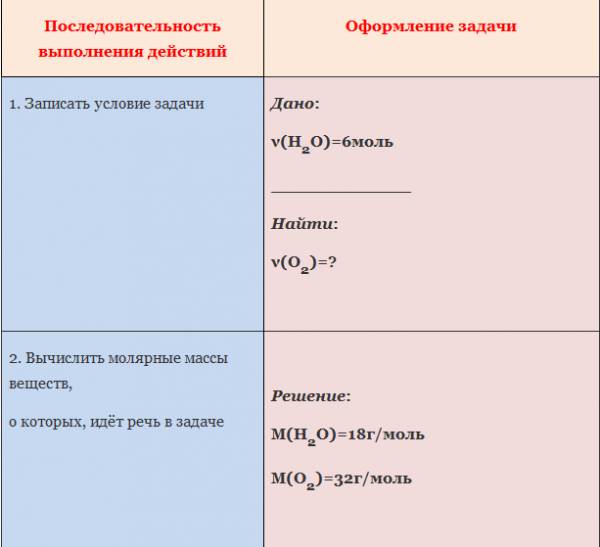
ЗАДАЧА 1. Определим количество вещества кислорода, образующегося в результате разложения 4 моль воды.
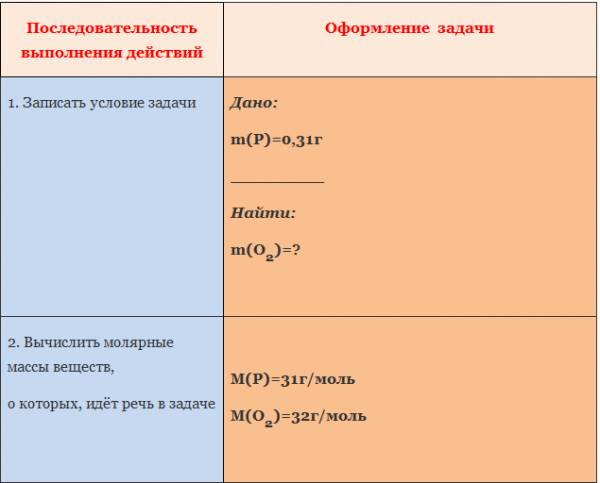
АЛГОРИТМ решения задачи:
1. Составить уравнение реакции
2. Составить пропорцию, определив количества веществ по уравнению реакции и по условию задачи (обозначить неизвестное количество вещества за х моль).
3. Составить уравнение (из пропорции).
4. Решить уравнение, найти х.
Рис. 1. Оформление краткого условия и решения задачи 1
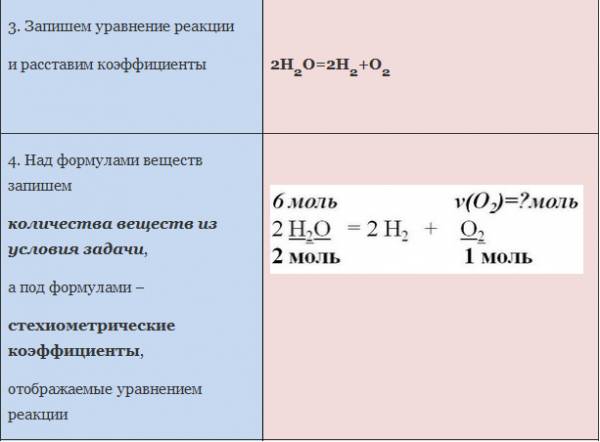
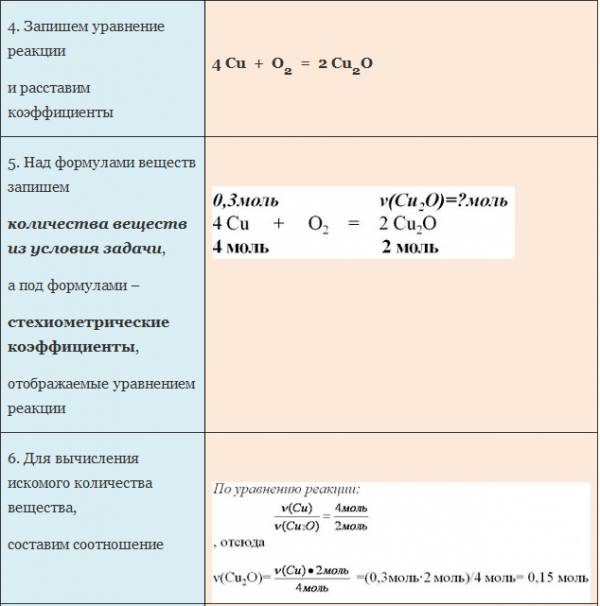
ЗАДАЧА 2. Какое количество кислорода потребуется для полного сжигания 3 моль меди?
Воспользуемся алгоритмом решения задач с использованием уравнения химической реакции.
Рис. 2. Оформление краткого условия и решения задачи 2.
I. Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством кислорода (4Al +3O2=2Al2O3).
2. Вычислите количество вещества оксида натрия, образовавшегося в результате взаимодействия натрия количеством вещества 2,3 моль с достаточным количеством кислорода (4Na+O2=2Na2O).
Алгоритм №1
Вычисление количества вещества по известному количеству вещества, участвующего в реакции.
Пример. Вычислите количество вещества кислорода, выделившегося в результате разложения воды количеством вещества 6 моль.
II. Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите массу серы, необходимую для получения оксида серы (IV) количеством вещества 4 моль (S+O2=SO2).
2. Вычислите массу лития, необходимого для получения хлорида лития количеством вещества 0,6 моль (2Li+Cl2=2LiCl).
Внимательно изучите алгоритм и запишите в тетрадь
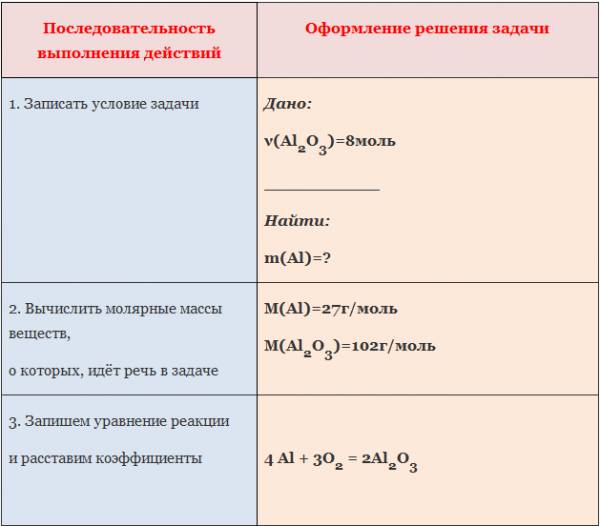
Алгоритм №2
Вычисление массы вещества по известному количеству другого вещества, участвующего в реакции.
Пример: Вычислите массу алюминия, необходимого для получения оксида алюминия количеством вещества 8 моль.
III. Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12,8 г (2Na+S=Na2S).
2. Вычислите количество вещества образующейся меди, если в реакцию с водородом вступает оксид меди (II) массой 64 г (CuO + H2 = Cu + H2O).
Внимательно изучите алгоритм и запишите в тетрадь
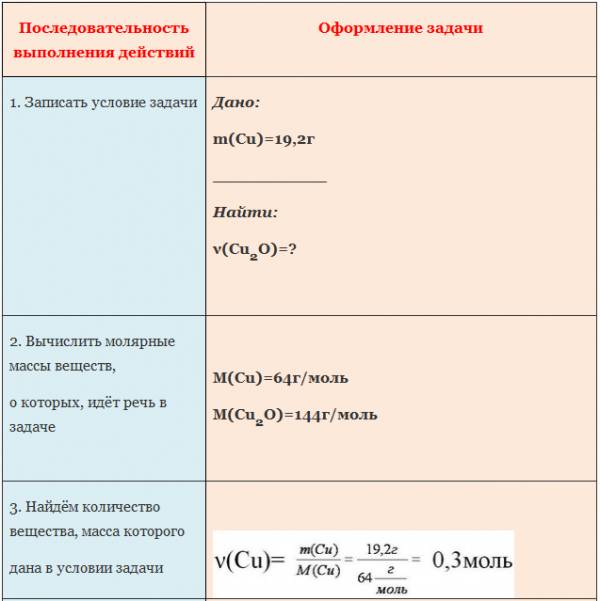
Алгоритм №3
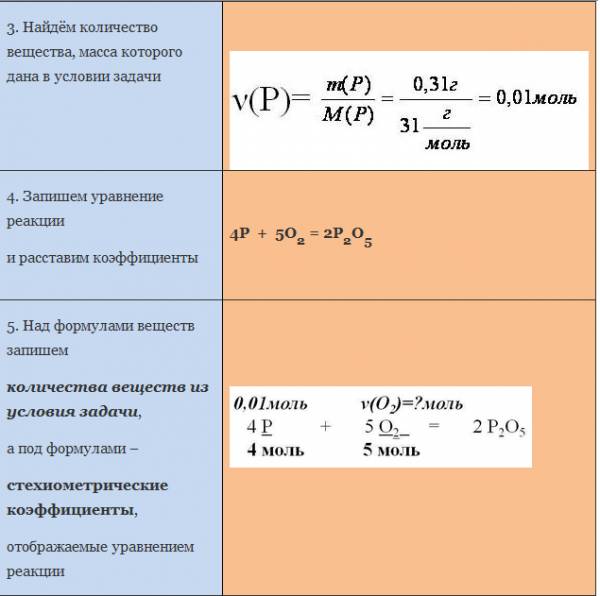
Вычисление количества вещества по известной массе другого вещества, участвующего в реакции.
Пример. Вычислите количество вещества оксида меди (I), если в реакцию с кислородом вступает медь массой 19,2г.
Внимательно изучите алгоритм и запишите в тетрадь
IV. Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите массу кислорода, необходимую для реакции с железом массой 112 г
(3Fe + 4O2=Fe3O4).
Алгоритм №4
Вычисление массы вещества по известной массе другого вещества, участвующего в реакции
Пример. Вычислите массу кислорода, необходимую для сгорания фосфора, массой 0,31г.
*******************************
Мольные соотношения участников реакции
Рассмотрим уравнение реакции образования воды из простых веществ:
2H2 + O2 = 2H2O
Можно сказать, что из двух молекул водорода и одной молекулы кислорода образуется две молекулы воды. С другой стороны, эта же запись говорит о том, что для образования каждых двух молей воды нужно взять два моля водорода один моль кислорода.
Мольное соотношение участников реакции помогает производить важные для химического синтеза расчеты. Рассмотрим примеры таких расчетов.
ЗАДАЧА 1. Определим массу воды, образовавшуюся в результате сгорания водорода в 3,2 г кислорода.
Чтобы решить эту задачу, сначала необходимо составить уравнение химической реакции и записать над ним данные условия задачи.
Если бы мы знали количество вещества вступившего в реакцию кислорода, то смогли бы определить количество вещества воды. А затем, рассчитали бы массу воды, зная ее количество вещества и молярную массу. Чтобы найти количество вещества кислорода, нужно массу кислорода разделить на его молярную массу.
Молярная масса численно равна относительной молекулярной массе. Для кислорода это значение составляет 32. Подставим в формулу: количество вещества кислорода равно отношению 3,2 г к 32 г/моль. Получилось 0,1 моль.
Для нахождения количества вещества воды оставим пропорцию, используя мольное соотношение участников реакции:
на 0,1 моль кислорода приходится неизвестное количество вещества воды, а на 1 моль кислорода приходится 2 моля воды.
Отсюда количество вещества воды равно 0,2 моль.
Чтобы определить массу воды, нужно найденное значение количества воды умножить на ее молярную массу, т.е. умножаем 0,2 моль на 18 г/моль, получаем 3,6 г воды.
Рис. 1. Оформление записи краткого условия и решения Задачи 1
Помимо массы, можно рассчитывать объем газообразного участника реакции (при н.у.), используя известную вам формулу, в соответствие с которой объем газа при н.у. равен произведению количества вещества газа на молярный объем. Рассмотрим пример решения задачи.
ЗАДАЧА 2. Рассчитаем объем кислорода (при н.у.), выделившийся при разложении 27г воды.
Запишем уравнение реакции и данные условия задачи. Чтобы найти объем выделившегося кислорода, нужно найти сначала количество вещества воды через массу, затем по уравнению реакции определить количество вещества кислорода, после чего можно рассчитать его объем при н.у.
Количество вещества воды равно отношению массы воды к ее молярной массе. Получаем значение 1,5 моль.
Составим пропорцию: из 1,5 моля воды образуется неизвестное количество кислорода, из 2 молей воды образуется 1 моль кислорода. Отсюда количество кислорода равно 0,75 моля. Рассчитаем объем кислорода при н.у. Он равен произведению количества кислорода на молярный объем. Молярный объем любого газообразного вещества при н.у. равен 22,4 л/моль. Подставив числовые значения в формулу, получим объем кислорода, равный 16,8 л.
Рис. 2. Оформление записи краткого условия и решения Задачи 2
Зная алгоритм решения подобных задач, можно рассчитать массу, объем или количество вещества одного из участников реакции по массе, объему или количеству вещества другого участника реакции.
ИСТОЧНИКИ
исчтоник конспекта — http://interneturok.ru/ru/school/chemistry/8-klass/bvewestva-i-ih-prevraweniyab/raschety-massy-veschestva-po-uravneniyu-himicheskoy-reaktsii
источник видео — http://www.youtube.com/watch?v=wZbj-o5J5Vs
источник видео — http://www.youtube.com/watch?v=8sPwPk7a7p0
источник видео — http://www.youtube.com/watch?v=ygaarSGQDwE
источник видео — http://www.youtube.com/watch?v=Gv-jZX0wZxE
http://himiknoginsk.ucoz.ru/index/raschety_po_khimicheskim_uravnenijam/0-144
С помощью стехиометрических
коэффициентов схема химической реакции
переходит в ее уравнение, которое в
явном виде отражает закон сохранения
количества атомов каждого вида при
переходе от исходных веществ (реагентов)
к продуктам реакции.
Стехиометрические коэффициенты позволяют
установить связь между количествами
участвующих в реакции веществ на основе
следующего правила:
коэффициенты в химическом уравнении
задают молярные пропорции
(отношения), в которых вступают в реакцию
исходные вещества (реагенты) и образуются
продукты реакции.
Рассмотрим в качестве примера реакцию
синтеза аммиака:
3H2+ N2= 2NH3 ,
для которой согласно приведенному
правилу можно записать
,
где индексы
«пр.» и «обр.» соответствуют количествам
прореагировавших и образовавшихся
веществ. Последнее соотношение можно
представить в ином виде:
а) для веществ H2и N2:
или в другой форме
;
б) для веществ H2и NH3:или
;
в) для веществ N2и NH3:или
.
Легко видеть,
что все пропорции можно объединить и
записать в виде:
=
.
Последнее
равенство является основным расчетным
уравнением, связывающим количества
прореагировавших веществ и образовавшихся
продуктов реакции. При необходимости
в это уравнение можно из условия задачи
ввести массы и объемы участников реакции,
используя обычные соотношения.
Например, для реакции
4FeS2(т) + 11О2= 2Fe2O3(т)
+ 8SO2(г)
основное расчетное
уравнение имеет вид:
и если в него
ввести обычно задаваемые в задачах для
твердых веществ их массы, а для газов –
объемы, то оно примет следующую форму:
Методика вычислений
с использованием основного расчетного
уравнения химической реакции включает
в себя несколько общих моментов:
1) Прежде
всего определяют опорное вещество, по
количеству которого проводят весь
последующий расчет. В условии задачи
для него задана или масса, или объем,
или концентрация, которые, в свою очередь,
позволяют вычислить число молей опорного
вещества. Как правило, это не составляет
большого труда, а исключение относится
к так называемым задачам на избыток и
недостаток, когдаопорное вещество
нужно выбрать издвух исходных.Дело в том, что при приготовлении
реакционной смеси исходные вещества
можно смешивать в любых пропорциях, но
реагировать друг с другом они будут
всегда в строго определенных пропорциях,
которые устанавливают для них
стехиометрические коэффициенты в
уравнении химической реакции. В этих
условиях вполне возможна ситуация,
когда одно из исходных веществ прореагирует
полностью, а часть другого останется
не прореагировавшей и тогда говорят,
что первое вещество взято в недостатке
по отношению ко второму и, наоборот,
второе вещество находится в избытке по
отношению к первому. В данном случае в
качестве опорного вещества следует
выбрать исходное вещество, взятое в
недостатке, поскольку именно его
количество будет определять как окончание
реакции, так и количества образующихся
продуктов.
Как
определить опорное вещество, если в
задаче указаны данные (массы, объемы и
др.) для обоих исходных веществ? Пусть
в реакцию вступают два вещества А и В
аА
+ вВ → продукты реакции ,
а
исходные количества этих веществ 0
(А) и 0
(В) можно
вычислить из условия задачи.
Для
ответа на поставленный вопрос нужно
сравнить два числа
,
где возможны три варианта:
I
вар.
,
тогда исходная реакционная смесь
называется стехиометрической и в
качестве опорного вещества может быть
выбрано любое из них – А или В;
II
вар.
,
тогда вещество А взято в избытке и
опорным будет вещество В;
III
вар.
,
тогда вещество В будет в избытке и
опорным является вещество А.
Окончание необратимых химических
реакций в первом варианте происходит
в момент одновременного исчезновения
обоих исходных веществ, а в двух других
– в момент исчезновения вещества,
взятого в недостатке, причем в конечной
смеси веществ, наряду с продуктами
реакции, будет присутствовать не
прореагировавший остаток вещества,
взятого в избытке.
2)
Из основного расчетного уравнения
вытекает простое
правило определения числа молей
вступивших
в реакцию исходных веществ и образовавшихся
продуктов по числу молей опорного
вещества:
для
определения числа молей прореагировавшего
или образовавшегося в реакции вещества
необходимо число молей опорного вещества
разделить на его стехиометрический
коэффициент и этот результат умножить
на стехиометрический коэффициент
определяемого вещества.
Для
реакции 2Al + 6HCl = 2AlCl3
+ H2,
где
опорным веществом, например, является
алюминий можно записать:
Определив
количества интересующих нас веществ,
легко рассчитать их массы, объемы и
концентрации, то есть те характеристики
участников химической реакции, которые
фигурируют в условии задачи.
Таким
образом, общая схема расчета по уравнению
химической реакции может быть представлена
в виде:
-
Необратимая
реакция.
Пусть
и
начальные количества реагентов А и В и
,
т.е. вещество А взято в избытке, тогда
a
A
+ в
В
= с
С
+
d
D
|
начало реакции: |
(избыток) |
(недостаток) |
0 |
0 |
|
|
окончание |
|
0 |
|
|
-
Обратимая
реакция.
В
этом случае реакция заканчивается
установлением химического равновесия
и равновесная смесь содержит как продукты
реакции, так и остаток исходных веществ.
Пусть к моменту установления равновесия
образовалось, например, х
моль продукта С – это опорное вещество,
то
a
A
+ в
В
с
С
+
d
D
|
Начало |
|
|
0 |
0 |
|
Равновесие: |
|
|
|
|
Пример 1. Раствор, содержащий 20,0 г
гидроксида натрия поглотил 6,72 л
углекислого газа (н. у.). Определите
продукты реакции и их количества.
При
поглощении раствором щелочи кислотных
оксидов (СО2 ,SO2
,P2O5и др.) или водородных соединений (H2Sи др.), которым соответствуют многоосновные
кислоты, на первом этапе при избытке
щелочи всегда образуются средние соли,
которые на втором этапе при наличии
избытка поглощаемого реагента частично
или полностью переходят в кислые соли:
СО2
(газ)
+ 2
NaOH =
Na2CO3
+
Н2О
|
начало реакции: |
|
|
0 |
|
|
|
||||
|
окончание |
|
0 |
|
Остаток
углекислого газа реагирует с карбонатом
натрия:
Na2CO3
+ СО2
(газ)
+
Н2О
=
2
NaHСО3
|
начало реакции: |
0,25 (избыток) |
0,05 (недостаток) |
0 |
|
окончание |
|
0 |
|
Итак,
в растворе присутствует смесь солей:
0,1 моль NaHCO3
и 0,2 моль Na2CO3.
Пример
2. В стакан
с 200 мл раствора фосфорной кислоты с
молярной концентрацией 0,5 моль/л внесли
6 г гидроксида натрия. Определите состав
раствора после окончания реакции.
При
нейтрализации щелочью (NaOH,
KOH,
NH3
и др.) многоосновных кислот происходит
последовательное замещение атомов
водорода на металл или аммонийную группу
и состав продуктов реакции зависит от
соотношения количеств реагентов. В
нашем случае, если
–
образуетсяNaH2PO4
; если 1: 2 , то Na2HPO4
и если 1:
3 , то Na3PO4.
В промежуточных вариантах возникает
смесь солей.
Найдем
исходные количества реагентов:
;
,
– имеет место промежуточный вариант
между 1: 1 и 1: 2 , поэтому реакция идет в
два этапа:
H3PO4
+ NaOH = NaH2PO4
+ H2O
|
начало реакции: |
0,1 (недостаток) |
0,15 (избыток) |
0 |
|
окончание |
0 |
|
0,1 |
далее
остаток щелочи реагирует с NaH2PO4
NaH2PO4
+ NaOH = Na2HPO4
+ H2O
|
начало реакции: |
0,1 (избыток) |
0,05 (недостаток) |
0 |
|
окончание |
|
0 |
0,05 |
Итак,
в растворе после реакции присутствует
смесь солей – по 0,05 моль NaH2PO4
и Na2HPO4
.
Успех в проведении расчетов по цепочкам
химических уравненийв случае, когда
продукт одной реакции является исходным
веществом для другой, зависит от
правильного выбора последовательности
переходов от одного уравнения к другому.
Выбрав согласно условию задачи опорное
вещество, стрелками удобно указать
последовательность расчета, помня при
этом, что вещество, полученное в предыдущей
реакции, в том же количестве используется
в последующей если, естественно, в ходе
всего многостадийного процесса нет
потерь и выход каждой реакции 100 %.
Пример 3.
Сколько литров хлора и водорода (н.у.)
необходимо для получения хлороводорода,
способного нейтрализовать раствор
щелочи, образующийся при растворении
в воде 13,7 г бария.
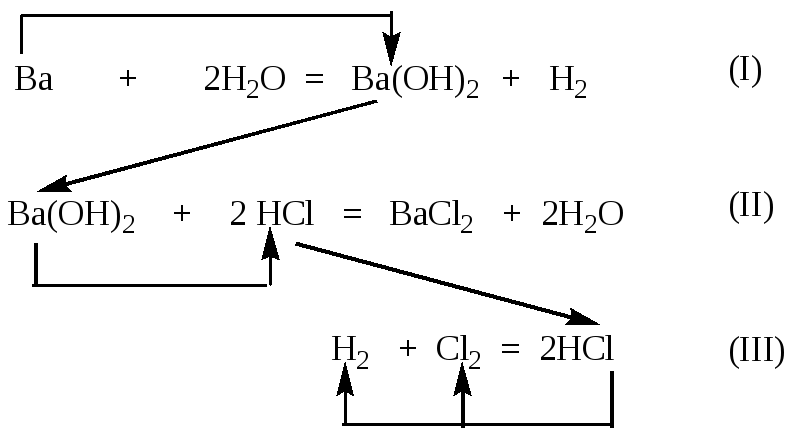
Составим уравнения
всех реакций и стрелками укажем
последовательность расчета:
Опорное вещество барий
и его количество
(Ва) =
.
Цепочка расчетов:
уравнение (I) — (Ba(OH)2/
I) ==>
уравнение (II) — (HCl
/ II)=> уравнение (III) –
(Cl2) =(H2) =,
тогда V(H2)
= V(Cl2) = 0,1 моль· 22,4 л/моль = 2,24 л.
При решении
задач на смеси веществнеобходимо
прежде всего для каждого компонента
смеси отдельно записать все химические
реакции, в которых он может участвовать
в соответствии с условием задачи. В
качестве опорных веществ обычно выбирают
вещества исходной смеси и их количества
(число молей) обозначают как неизвестные
– x, y, z, …., а затем составляют уравнения
материального баланса по количеству,
массе или объему ( для газов) участников
химических реакций, где два последних
необходимо выразить через неизвестные.
Число балансовых уравнений должно быть
равно числу неизвестных. На последнем
этапе решается полученная система
алгебраических уравнений.
Пример 4.При сгорании 13,44 л (н. у.)
смеси водорода, метана и угарного газа
образовалось 8,96 л углекислого газа и
14,4 г воды. Определить количества газов
в смеси.
Уравнения реакций:
2H2+ O2= 2H2O
(I)
CH4
+ 2O2
= CO2
+ 2H2O
(II)
2CO
+ O2 =
2CO2
(III)
Опорные вещества –
CH4, H2и CO; обозначим их
количества
ν(H2)
= x; ν(СH4)
= y; ν(CO) = z.
Составим три
балансовых уравнения по числу неизвестных:
а) баланс по объему
смеси:
V (H2) +
V(CH4) + V(CO) = 13,44 л, введем в него
неизвестные:
xVm+ yVm+ zVm= 13,44 или x + y + z =0,6
моль;
б) баланс по количеству
CO2:
ν(CO2/
II) + ν(CO2/
III) = νобщ.(CO2),
но
;
ν(CO2/
II) = ν(CH4)
= y; ν(CO2/
III) = z,
тогда
y + z = 0,4.
в) баланс по количеству
H2O:
ν(H2O/
I) + ν(H2O/
II) = νобщ.(H2O),
но
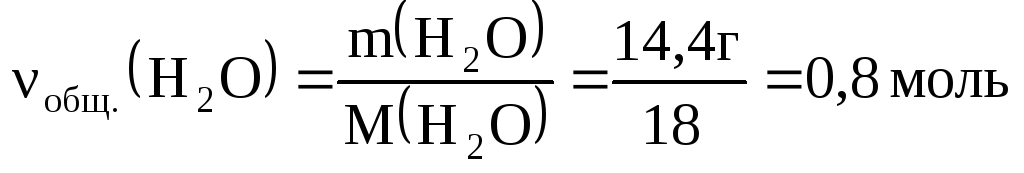
;
,
тогда
x + 2y = 0,8.
Итак, получаем систему
уравнений вида
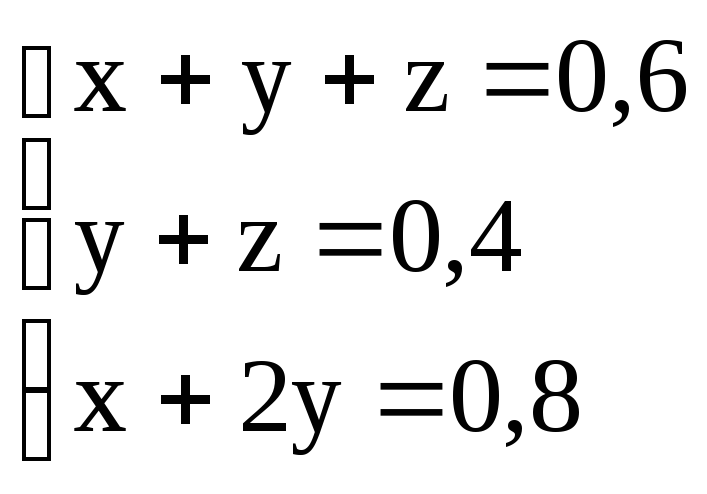
которая легко решается
устно
x = 0,2 моль; y =
0,3 моль; z = 0,1 моль.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Между количествами веществ, участвующих в химической реакции, существует прямо пропорциональная зависимость: чем большее количество одного из веществ принимает участие в данном превращении, тем большее количество других веществ в нём участвует, и наоборот.
Если в химической реакции участвуют вещества (A) и (B), то уравнение реакции имеет вид
(…aA) (+) (…bB), где (a) и (b) — коэффициенты, относящиеся к формулам соответствующих веществ.
Прямо пропорциональную зависимость, существующую между количествами веществ (A) и (B), можно выразить математически:
, отсюда:
n(A)=a⋅n(B)b
или
n(B)=b⋅n(A)a
.
Для того чтобы произвести простейший расчёт по уравнению химической реакции, следует, как правило, сделать четыре шага:
1. написать уравнение химической реакции, упомянутой в условии задачи: (…aA) (+) (…) (…bB).
2. Если в условии задачи не указано количество вещества ((A)), участвующего в превращении, следует, исходя из того, что дано, сделать такой расчёт:
а) если известна масса вещества, его количество можно рассчитать путём деления массы на его молярную массу:
n(A)=m(A)M(A)
.
б) Если известен объём газообразного вещества, измеренный при нормальных условиях (н. у.), количество вещества можно рассчитать путём деления объёма на молярный объём:
n(A)=V(A)Vm
, где
Vm=22,4
л/моль.
в) Если известно число частиц вещества (атомов, молекул или др.), принимающих участие в реакции, его количество можно рассчитать путём деления числа частиц на число Авогадро:
n(A)=N(A)NA
, где
NA=6,02⋅1023
1/моль.
3. Зная количество одного вещества ((A)), участвующего в реакции, можно рассчитать количество второго вещества ((B)), принимающего участие в этой реакции:
n(B)=b⋅n(A)a
.
4. Если требуется рассчитать не количество второго вещества ((B)), а численное значение другой физической величины (его массу, объём газа (н. у.) или др.), следует сделать такой расчёт:
а) чтобы рассчитать массу второго вещества, участвующего в реакции, следует его количество умножить на молярную массу данного вещества:
m(B)=n(B)⋅M(B)
.
б) Чтобы рассчитать объём газа (н. у.), участвующего в химической реакции, нужно его количество умножить на молярный объём:
V(B)=n(B)⋅Vm
.
в) Чтобы рассчитать число частиц (атомов, молекул или др.) второго вещества, принимающего участие в данной химической реакции, нужно его количество умножить на число Авогадро:
N(B)=n(B)⋅NA
.
г) Чтобы рассчитать молярную массу второго вещества, участвующего в химической реакции, следует его массу разделить на количество этого вещества:
M(B)=m(B)n(B)
.
Обрати внимание!
Все вышеупомянутые вычисления можно сделать, не пользуясь расчётными формулами, а составляя пропорции.
Пример:
для того чтобы рассчитать, какое количество вещества содержится в (4,9) г серной кислоты (её молярная масса равна (98) г/моль), следует составить такую пропорцию:
в (98) г серной кислоты содержится (1) моль этого вещества,
а в (4,9) г серной кислоты содержится (x) моль вещества;
.