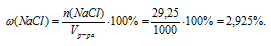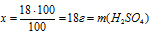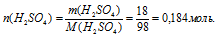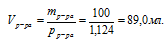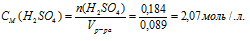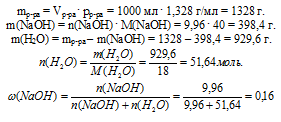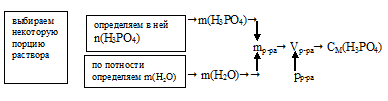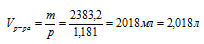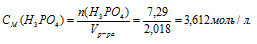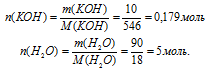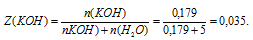Раствор – однородная система, состоящая из растворителя и растворенного в нем вещества (или нескольких). Количественная характеристика определяется концентрацией веществ, входящих в их состав.
Массовая доля
Массовая доля – это отношение массы растворённого вещества к массе всего раствора.
ω(%)=mxmX×100%omega left(% right)= frac{m_{x}}{m_{X}} times 100%
Сколько калия хлорида (в граммах) содержится в 100г 10% раствора?
Решение:
Масса калия хлорида (молярная масса MM для KClKCl 75г/моль):
mKCl=ω×M100%=10%×75100%=7,5m_{KCl}=frac{omega times M}{100%}=frac{10% times 75}{100%}=7,5г
Ответ: 7,5г.
Сколько необходимо добавить натрия гидроксида к 120г 3% раствора этой же соли, что бы концентрация увеличилась в три раза?
Решение:
Масса натрия гироксида исходная (MNaOH=40M_{NaOH}=40 г/моль:
m1NaOH=ω×M100%=3%×40100%=1,2m_{1NaOH}=frac{omega times M}{100%}=frac{3%times 40}{100%}=1,2г
Массовая доля натрия гидроксида в необходимом растворе:
ω2%=ω%×3=3%×3=9%omega _{2}%=omega%times3=3%times3=9%
Масса NaOH в необходимом растворе:
m2NaOH=9%×40100%=3,6m_{2NaOH}=frac{9%times 40}{100%}=3,6г
Необходимое количество рассчитываем как разность:
mNaOH=m2NaOH−m1NaOH=3,6−1,2=2,4m_{NaOH}=m_{2NaOH}-m_{1NaOH}=3,6-1,2=2,4г
Ответ: 2,4г.
Молярная концентрация
Молярная концентрация – количество вещества (в молях) в объеме раствора.
Количество растворенного вещества (в молях) выражается как масса вещества (в граммах), деленная на молярную массу (г/моль).
η=mxMeta =frac{m_{x}}{M}
Молярная концентрация выражается в формуле:
Cx=ηV=η=mxM×VC_{x} = frac{eta }{V} = eta =frac{m_{x}}{M}times V
Определите молярную концентрацию калия иодида. В 120мл воды содержится 15г KI.
Решение:
Выражаем молярную концентрацию (моль/л) KI по формуле ($M_(KI)=$166г/моль):
CKI=mKIMKI×VC_{KI} =frac{m_{KI}}{M_{KI}}times V=15166×0,12=0,01=frac{15}{166}times 0,12=0,01моль/л
Т.к. молярная концентрация выражается в моль/л миллилитры переводим в литры.
Ответ: 3,61 моль/л.
Какая масса лития хлорида содержится в 200мл 3М раствора?
Решение:
Находим количество растворенного лития хлорида (моль):
η=CLiCl×V=3×0,2=0,6eta =C_{LiCl}times V=3times 0,2=0,6г
Выражаем массу M(LiCl)=M_ (LiCl)= 42,3г/моль):
mLiCl=ηLiCl×MLiCl=0,6×42.3=25,4m_{LiCl}=eta_{LiCl} times M_{LiCl}=0,6times 42.3=25,4г
Ответ: 25,4г.
Молярная (мольная) доля
Молярная (мольная) доля – отношения количества вещества в растворе к количеству всех веществ, образующих раствор.
Nx%=nx∑n×100%N_{x}%=frac{n_{x}}{sum{n}}times 100%
Концентрация бария хлорида в 100мл водного раствора равна 20%. Определите его мольную долю.
MBaCl2=208M_{BaCl_{2}}=208моль/л, MH2O=18M_{H_{2}O}=18моль/л.
Решение:
Находим содержание воды:
ωH2O=100%−ωBaCl2=100%−20%=80%omega _{H_{2}O}=100%-omega BaCl_{2}=100%-20%=80%
Т.к. объем раствора равен 100мл, то массы каждого компонента равны значениям массовой доли. Следовательно:
mBaCl2=20m_{BaCl_{2}}=20г
mH2O=80m_{H_{2}O}=80г
Определим количество ηeta для бария хлорида и воды:
ηBaCl2=mBaCl2MBaCl2=20208=0,01eta_{BaCl_{2}}=frac{m_{BaCl_{2}}}{M_{BaCl_{2}}}=frac{20}{208}=0,01моль
ηH2O=mH2OMH2O=2018=1,1eta_{H_{2}O}=frac{m_{H_{2}O}}{M_{H_{2}O}}=frac{20}{18}=1,1моль
Определяем мольную долю NBaCl2N_{BaCl_{2}}:
NBaCl2=ηBaCl2ηBaCl2+ηH2O×100%=0,010,01+0,1×100%=9%N_{BaCl_{2}}=frac{eta BaCl_{2}}{eta BaCl_{2}+eta H_{2}O}times 100%=frac{0,01}{0,01+0,1}times 100%=9%
Ответ: 9%
Молярная концентрация эквивалента
Молярная концентрация эквивалента (нормальность) – число моль эквивалентов в объеме раствора.
C1/z=mxM1/z×VC_{1/z} = frac{m_{x}}{M_{1/z}times V}моль*экв/литр
Фактор эквивалентности f1/zf_{1/z} – показывает часть реальной частицы, составляющую эквивалент.
Молярная масса эквивалента M1/zM_{1/z} – произведение молярной массы и фактора эквивалентности:
M1/z=M×f1/zM_{1/z} = M times f_{1/z}г/моль
Определите молярную концентрацию эквивалента 4.6г серной кислоты, нейтрализованной раствором гидроксида натрия. В результате реакции общий объём составил 100мл.
Решение:
MH2SO4=98M_{H_{2}SO_{4}}=98г/моль, f1/z=1/2f_{1/z=1/2}.
Находим молярную массу эквивалента для серной кислоты:
M1/zH2SO4=MH2SO4×f1/zM_{1/z H_{2}SO_{4}} = M _{H_{2}SO_{4}}times f_{1/z} = 98times 1/2=49$г/моль
Находим нормальность:
C1/zH2SO4=mH2SO4M1/zH2SO4×V=4,649×0,1=0,94C_{1/z H_{2}SO_{4}} = frac{m_{H_{2}SO_{4}}}{M_{1/z H_{2}SO_{4}}times V}=frac{4,6}{49times
0,1}=0,94моль*экв/л
Ответ: 0,94моль*экв/л.
Моляльность
Моляльность – количество вещества в килограмме растворителя.
Сm=ηxmС_{m}=frac{eta _{x}}{m}моль/кг
В 300г воды растворили 20г калия гидроксида. Определите моляльную концентрацию раствора.
Решение:
MKOH=98M_{KOH}=98г/моль.
Находим количество калия гидроксида:
ηKOH=mKOHM=2056=0,36eta _{KOH} = frac{m_{KOH}}{M}=frac{20}{56}=0,36моль
Находим моляльность (граммы переводим в килограммы):
CKOH=ηKOHm=0,360,3=1,2C_{KOH}=frac{eta _{KOH}}{m}=frac{0,36}{0,3}=1,2моль/кг
Ответ: 1,2 моль/кг.
При решении химических задач, при расчётах на работе, да и просто в жизни иногда приходится рассчитывать концентрации. Неважно, будет это школьная теоретическая задача, необходимость приготовить электролит для аккумулятора автомобиля, надобность узнать количество сахара для компота — все расчёты концентраций выполняются по известным формулам, которых не так много. Однако, с этим часто возникают трудности.
Прочитав эту статью, Вы научитесь легко рассчитывать концентрации веществ и при надобности играючи переводить одну концентрацию в другую. В статье приводятся примеры задач с решениями, а в конце приведём справочную табличку с формулами, которую можно распечатать и держать под рукой.
Массовая доля
Начнём с простого, но в то же время нужного способа выражения концентрации компонента в смеси — массовой доли.
Массовая доля есть отношение массы данного компонента к сумме масс всех компонентов. Обозначать её принято буквой w или ω (омега).
Рассчитывается массовая доля по формуле:
Large w_{i}=frac{m_{i}}{m}, ;;;;;(1)
где Large w_{i} — массовая доля компонента i в смеси,
Large m_{i} — масса этого компонента,
m — масса всей смеси.
И сразу разберём на примере:
Задача:
Зимой дороги посыпают песком с солью. Известно, что куча имеет массу 50 кг, и в неё всыпали 1 кг соли и перемешали. Найти массовую долю соли.
Решение:
Масса соли есть Large m_{i} по формуле выше. Масса всей смеси нам пока неизвестна, но найти её легко. Просуммируем массу песка и соли:
Large m = m_{п}+m_{с}= 50 кг + 1 кг = 51 кг
А теперь находим и массовую долю:
Large w_{с} = frac{m_{с}}{m} = 1 кг / 51 кг = 0.0196,
или умножаем на 100% и получаем 1.96%.
Ответ: 0.0196, или 1.96%.
Теперь решим что-то посложнее, и ближе к ЕГЭ.
Задача:
Смешали 200 г раствора глюкозы с массовой концентрацией 25% и 300 г раствора глюкозы с массовой концентрацией 10%. Найти массовую концентрацию полученного раствора, ответ округлить до целых.
Решение:
Обозначим первый и второй растворы соответственно Large m_{1} и Large m_{2}. Массу полученного после смешения раствора обозначим Large m и найдём:
Large m = m_{1} + m_{2} = 200 г + 300 г = 500 г
Массу самой глюкозы в первом и втором растворе обозначим Large m_{гл. 1} и Large m_{гл. 2}. По формуле (1) это будут наши массы компонентов. Массы растворов нам известны, их массовые концентрации тоже. Как найти массу компонента? Очень просто, находим неизвестное делимое умножением (и не забываем, что проценты — это сотые части):
Large m_{гл. 1} = w_{1}cdot m_{1} = 0.25 cdot 200 г = 50 г
Large m_{гл. 2} = w_{2}cdot m_{2} = 0.1 cdot 300 г = 30 г
Таким образом, общая масса глюкозы Large m_{гл}:
Large m_{гл} = m_{гл. 1} + m_{гл. 2} = 50 г + 30 г = 80 г.
Ответ: 80 г.
Задачи на смешение раствором с разными концентрациями одного вещества можно решать с помощью «конверта Пирсона».
Объёмная доля
Часто, когда мы имеем дело с жидкостями и газами, удобно оперировать их объёмами, а не массой. Поэтому, чтобы выражать долю какого-либо компонента в таких смесях (но и в твёрдых тоже вполне можно), пользуются понятием объёмной доли.
Объёмная доля компонента — отношение объёма компонента к сумме объёмов компонентов до смешивания. Объёмная доля измеряется в долях единицы или в процентах. Обычно обозначается греческой буквой φ (фи).
Рассчитывается объёмная доля по формуле:
Large phi_{B}=frac{V_{B}}{sum{V_{i}}}, ; ;;;; (2)
где Large phi_{B} — объёмная доля компонента B;
Large V_{B} — объём компонента B;
Large sum{V_{i}} — сумма объёмов всех компонентов.
Здесь важно понимать, что в формулу по возможности подставляем именно сумму объёмов всех компонентов, а не объём смеси, так как при смешивании некоторых жидкостей суммарный объём уменьшается. Так, если смешать литр воды и литр спирта, два литра аквавита мы не получим — будет примерно 1800 мл. В школьных задачах, как правило, это не так важно, но в уме держим и помним.
Задача:
Смешали 6 объёмов воды и 1 объём серной кислоты. Найти объёмную долю кислоты в полученном растворе.
Решение:
Так как объёмная доля — безразмерная величина, объёмы компонентов в условии задачи могут даваться в любых единицах — литрах, стаканах, баррелях, штофах, сексталях — главное, чтобы в одинаковых. Если не так — переводим одни в другие, если одинаковые — решаем. В нашем условии описаны просто некоторые «объёмы», их и подставляем.
Large phi_{H_{2}SO_{4}} = frac{V_{ H_{2}SO_{4} }} { V_{ H_{2}SO_{4}} + V_{H_{2}O}} = frac{1 : объём}{1 : объём + 6 : объёмов} = frac{1 : объём}{7 : объёмов} = 0.143, : или : 14.3%
Ответ: 14.3 %.
С газами всё обстоит немного интереснее — при не очень больших давлениях и температурах объёмная доля какого-либо газа в газовой смеси равна его мольной доле. (Ведь мы знаем, что молярный объём газов почти равен 22.4 л/моль).
Задача:
Мольная доля кислорода в сухом воздухе составляет 0.21. Найдите объёмную долю азота, если объёмная доля аргона составляет 1%.
Решение:
Внимательный читатель заметил, что мы написали о том, что объёмная и мольная доля для газов в смеси равны. Поэтому, объёмная доля кислорода равна также 0.21, или 21%. Найдём объёмную долю азота:
Large 100% — 21% — 1% = 78%.
Ответ: 78%.
Мольная доля
В тех случаях, когда нам известны количества веществ в смеси, мы можем выразить содержание того или иного компонента с помощью мольной доли.
Мольная доля — отношение количества молей данного компонента к общему количеству молей всех компонентов. Мольную долю выражают в долях единицы. ИЮПАК рекомендует обозначать мольную долю буквой x (а для газов — y).
Находят мольную долю по формуле:
Large x_{B} = frac{n_{B}}{sum{n_{i}}}, ;;;;;(3)
где Large x_{B} — мольная доля компонента B;
Large n_{B} — количество компонента B, моль;
Large sum{n_{i}} — сумма количеств всех компонентов.
Разберём на примере.
Задача:
При неизвестных условиях смешали 3 кг азота, 1 кг кислорода и 0.5 кг гелия. Найти мольную долю каждого компонента полученной газовой смеси.
Решение:
Сначала находим количество каждого из газов (моль):
Large n_{N_{2}} = frac{ m_{N_{2}}}{M_{N_{2}}} = frac {3000 : г}{28 : ^г/_{моль}} = 107.14 : моль
Large n_{O_{2}} = frac{ m_{O_{2}}}{M_{O_{2}}} = frac {1000 : г}{32 : ^г/_{моль}} = 31.25 : моль
Large n_{He} = frac{ m_{He}}{M_{He}} = frac {500 : г}{4 : ^г/_{моль}} = 125 : моль
Затем считаем сумму количеств:
Large sum {n} = 107.14 : моль + 31.25 : моль + 125 : моль = 263.39 : моль
И находим мольную долю каждого компонента:
Large y_{N_{2}} = frac {107.14 : моль}{263.39 : моль} = 0.4068, : или : 40.68 %;
Large y_{O_{2}} = frac {31.25 : моль}{263.39 : моль} = 0.1186, : или : 11.86 %;
Large y_{He} = frac {125 : моль}{263.39 : моль} = 0.4746, : или : 47.46 %;
Проверяем:
Large 40.68 % + 11.86 % + 47.46 % = 100%.
И радуемся правильному решению.
Ответ: 40.68%, 11.86% , 47.46%.
Молярность (молярная объёмная концентрация)
А сейчас рассмотрим, вероятно, самый часто встречающийся способ выражения концентрации — молярную концентрацию.
Молярная концентрация (молярность, мольность) — количество вещества (число молей) компонента в единице объёма смеси. Молярная концентрация в системе СИ измеряется в моль/м³, однако на практике её гораздо чаще выражают в моль/л или ммоль/л.
Также иногда говорят просто «молярность», и обозначают буквой М. Это значит, что, например, обозначение «0.5 М раствор соляной кислоты» следует понимать как «полумолярный раствор соляной кислоты», или 0.5 моль/л.
Обозначают молярную концентрацию буквой c (латинская «цэ»), или заключают в квадратные скобки вещество, концентрация которого указывается. Например, [Na+] — концентрация катионов натрия в моль/л. Кстати, слово «моль» в обозначениях не склоняют — 5 моль/л, 3 моль/л.
Рассчитывается молярная концентрация по формуле:
Large c_{B} = frac{n_{B}}{V} ; ; ;;; (4)
где Large n_{B} — количество вещества компонента B, моль;
Large V — общий объём смеси, л.
Разберём на примере.
Задача:
В пивную кружку зачем-то насыпали 24 г сахара и до краёв заполнили кипятком. А нам зачем-то нужно найти молярную концентрацию сахарозы в полученном сиропе. И кстати, дело происходило в Британии.
Решение:
Молекулярная масса сахарозы равна 342 (посчитайте, может мы ошиблись — C12H22O11). Найдём количество вещества:
Large n_{сахарозы} = frac{24 : г}{342 : г/моль} = 0.0702 моль
Британская пинта (мера объёма такая) равна 0.568 л. Поэтому молярная концентрация находится так:
Large c_{сахарозы} = frac{0.0702 : моль}{0.568 : л} = 0.1236 моль/л
Ответ: 0.1236 моль/л.
Нормальная концентрация (молярная концентрация эквивалента, «нормальность»)
Нормальная концентрация — количество эквивалентов данного вещества в 1 литре смеси. Нормальную концентрацию выражают в моль-экв/л или г-экв/л (имеется в виду моль эквивалентов).
Обозначается нормальная концентрация как сн, сN, или даже c(feq B). Рассчитывается нормальная концентрация по формуле:
Large c_{N} = z cdot c_{B} = z cdot frac{n_{B}}{V}= frac{1}{f_{eq}} cdot frac {n_{B}}{V} ; ;;;; (5)
где Large n_{B} — количество вещества компонента В, моль;
V — общий объём смеси, л;
z — число эквивалентности (фактор эквивалентности Large f_{eq} = 1/z ).
Значение нормальной концентрации для растворов записывают как «н» или «N», а говорят «нормальность» или «нормальный». Например, раствор с концентрацией 0.25 н — четвертьнормальный раствор.
Разберём на примере.
Задача:
Рассчитать нормальность раствора объёмом 1 л, если в нём содержится 40 г перманганата калия. Раствор приготовили для последующего проведения реакции в нейтральной среде.
Решение:
В нейтральной среде перманганат калия восстанавливается до оксида марганца (IV). При этом в окислительно-восстановительной реакции 1 атом марганца принимает 3 электрона (проверьте на любой окислительно-восстановительной реакции перманганата калия с образованием оксида, расставив степени окисления), что означает, что число эквивалентности будет равно 3. Для расчёта концентрации по формуле (5) выше нам ещё не хватает количества вещества KMnO4. найдём его:
Large n_{KMnO_{4}}=frac{m _{KMnO_{4}}}{M _{KMnO_{4}} } = frac{40 : г}{158 г/моль}= 0.253 моль
Теперь считаем нормальную концентрацию:
Large c_{N_{KMnO_{4}}}= z cdot frac{n_{KMnO_{4}}}{V} = 3 cdot frac{0.253 : моль}{1 : л} = 0.759 моль-экв/л
Ответ: 0.759 моль-экв/л.
Таким образом, заметим важное на практике свойство — нормальная концентрация больше молярной в z раз.
Мы не будем рассматривать в данной статье особо экзотические способы выражения концентраций, о них вы можете почитать в литературе или интернете. Поэтому расскажем ещё об одном способе, и на нём остановимся — массовая концентрация.
Моляльная концентрация
Моляльная концентрация (моляльность, молярная весовая концентрация) — количество растворённого вещества (число моль) в 1000 г растворителя.
Измеряется моляльная концентрация в молях на кг. Как и с молярной концентрацией, иногда говорят «моляльность», то есть раствор с концентрацией 0.25 моль/кг можно назвать четвертьмоляльным.
Находится моляльная концентрация по формуле:
Large m_{B} = frac{n_{B}}{m_{A}}, ;;;;; (6)
где Large n_{B} — количество вещества компонента B, моль;
Large m_{A} — масса растворителя, кг.
Казалось бы, зачем нужна такая единица измерения для выражения концентрации? Так вот, у моляльной концентрации есть одно важное свойство — она не зависит от температуры, в отличие, например, от молярной. Подумайте, почему?
Массовая концентрация
Массовая концентрация — отношение массы растворённого вещества к объёму раствора. По рекомендации ИЮПАК, обозначается символом γ или ρ.
Находится массовая концентрация по формуле:
Large rho_{B}=frac{m_{B}}{V}, ;;;;; (7)
где Large m_{B} — масса растворенного вещества, г;
Large V — общий объём смеси, л.
В системе СИ выражается в кг/м3.
Разберём на примере.
Задача:
Рассчитать массовую концентрацию перманганата калия по условиям предыдущей задачи.
Решение:
Решение будет совсем простым. Считаем:
Large rho_{ KMnO_{4} }=frac{m_{ KMnO_{4} }}{V} =frac{40 : г}{1 : л} = 40 г/л.
Ответ: 40 г/л.
Также в аналитической химии пользуются понятием титра по растворенному веществу. Титр по растворенному веществу находится так же, как и массовая концентрация, но выражается в г/мл. Легко догадаться, что в задаче выше титр будет равен 0.04 г/мл (для этого надо умножить наш ответ на 0.001 мл/л, проверьте). Кстати, обозначается титр буквой Т.
А теперь, как обещали, табличка с формулами перевода одной концентрации в другую.
Таблица перевода одной концентрации в другую.
В таблице слева — ВО ЧТО переводим, сверху — ЧТО. Если стоит знак «=», то, естественно, эти величины равны.
| Массовая доля, large omega, % | Мольная доля, large x , % | Объёмная доля, large phi, % | Молярная концентрация, large c, моль/л | Нормальная концентрация, large c_{N} , моль-экв/л | Моляльная концентрация, large m, моль/кг | Массовая концентрация, large rho, г/л | |
| Массовая доля, large omega, % | = | large omega_{B}=LARGE frac{x_{B} cdot M(B)}{sum x_{i} cdot M_{i}} | Для газов: omega = LARGE frac{phi_{A} cdot M(A)}{sum (M_{i} cdot phi_{i})} |
large omega_{B}= LARGE frac{c_{B} cdot M(B)}{rho} | large omega_{B}=LARGE frac{c_{N} cdot M(B)}{rho cdot z} | large omega_{B}= LARGE frac{gamma_{B}}{rho} | |
| Мольная доля, large x , % | large x_{B}=LARGE frac{frac{omega_{B}}{M(B)}}{sum frac{omega_{i}}{M_{i}}} | = | large x_{B}=LARGE frac{m_{B}}{m_{B}+frac{1}{M(A)}} | ||||
| Объёмная доля, large phi, % | Для газов: large phi_{A}=LARGE frac{frac{omega_{A}}{M(A)}}{sum frac{omega_{i}}{M_{i}}} |
= | |||||
| Молярная концентрация, large c, моль/л | large c_{B}=LARGE frac{rho cdot omega_{B}}{M(B)} | = | large c_{B}=Large frac{c_{N}}{z} | ||||
| Нормальная концентрация, large c_{N} , моль-экв/л | large c_{N}=LARGE frac{rho cdot omega_{B} cdot z}{M(B)} | large c_{N}=c_{B} cdot z | = | ||||
| Моляльная концентрация, large m, моль/кг | large m_{B}=Large frac{x_{B}}{M(A)(1-x_{B})} | = | |||||
| Массовая концентрация, large gamma, г/л | large gamma_{B}=rho cdot omega_{B} | = |
Таблица будет пополняться.
Молярная доля — величина, которая характеризует отношение количества молей искомого вещества к общему количеству молей всех веществ, находящихся, например в растворе или смеси газов.
Как-же ее вычислить?
Для вычисления потребуется таблица Менделеева и калькулятор.
Этап 1.
Следует выписать формулы всех веществ и расчитать их молярные массы, используя таблицу Менделеева.
Пример:
Молярная масса воды (H20) равна 18. Почему? Атомная масса водорода (H) равна 1, а атомная масса кислорода (O) равна 16, соответственно 16+1+1=18.
Также, к примеру молярная масса оксида аллюминия (Al2O3) равна 27+27+16+16+16=102 (Атомная масса аллюминия 27, и как сказанно выше, кислорода 16).
Этап 2.
Теперь нужно определить количество молей каждого вещества. Для этого, массу вещества следует разделить на молярную массу.
Этап 3.
Теперь у нас есть сумма молей всех веществ (запишем, как Z) и количество молей искомого вещества (запишем, как n)
Формула для определения молярной доли X=n/Z, где X — искомая молярная доля, Z — сумма всех молей, n — моли искомого вещества.
Раствор
–
гомогенная (однородная) система, состоящая
как минимум из двух компонентов, один
из которых растворитель, другой –
растворенное вещество. То есть состав
раствора = растворитель + растворенное
вещество.
Например,
водный раствор хлорида натрия состоит
из двух компонентов: воды (растворителя)
и хлорида натрия (растворенного вещества).
Существует несколько
способов выражения концентрации
растворов.
Молярная
концентрация, или молярность (СM)
–
количество вещества (ν) растворенного
компонента, содержащееся в 1 литре (дм3)
раствора:
[моль/л], (14)
Молярная
концентрация эквивалентов
(Сэкв),
(нормальная
концентрация или нормальность
N)
– количество вещества эквивалентов
(νэкв)
растворенного компонента, содержащееся
в 1 литре (дм3)
раствора:
Сэкв
(N)
= νэкв
/ V
[моль-экв/л] (15)
Моляльная
концентрация
или
моляльность
(b)
– количество вещества (ν) растворенного
компонента в 1 кг раствора:
[моль/кг], (16)
Массовая
доля
(ω)
–
отношение массы растворенного вещества
(mр.в.)
к массе раствора (mр-ра)
Ее рассчитывают, выражая в долях единицы
или в процентах. Массовая доля, выраженная
в процентах, называется процентной
концентрацией:
(17)
Процентная
концентрация показывает массу
растворенного вещества, содержащегося
в 100 г раствора. Например, ω(KOH)
= 3% означает, что в 100 г этого раствора
содержится 3 г KOH
и
97 г
H2O.
Молярная
доля (Ni)
– отношение количества вещества
растворенного компонента (в-ва)
(или растворителя, р-ля)
к суммарному количеству вещества всех
компонентов раствора. Например, в
системе, состоящей из растворителя и
одного растворенного вещества, молярная
доля растворенного вещества равна:
, (18)
Молярная доля
растворителя:
(19)
Примеры решения задач
Пример 1.
Определить молярную концентрацию
раствора NaOH
с массовой долей 10% и плотностью
=1,1 г/см3.
Р е ш е н и е. 1) Записываем выражение для молярной концентрации раствора NaOh :
2)
10%-ный раствор – это 10г NaOH
в 100г раствора. Находим количество
вещества NaOH,
содержащееся в 10 г:
,
mNaOH
= 10 г, MNaOH
= 23 + 16 +1 = 40 г/моль
,
т.е. 0,25 моль NaOH
содержится в 100 г раствора.
3)
Находим объем раствора массой 100 г:
m=V,
=
0,091 л
4)
Рассчитываем молярную концентрацию:
Ответ:
молярная концентрация раствора гидроксида
натрия с массовой долей 10% составляет
2,74 моль/л
Пример
2. Найти
молярную долю растворенного вещества
в растворе сахарозы с массовой долей
67%.
Р е ш е н и е. 1) Вспомним, что молярная доля растворенного вещества равна:
67%-ный (по массе)
раствор означает, что в 100 г раствора
содержится 67 г сахарозы и 33 г воды.
2) Определяем
количество вещества сахарозы и количество
вещества воды:
в-ва
= 67/342 = 0,196 моль,
р-ля
= 33/18 = 1,83 моль
Следовательно,
молярная доля сахарозы равна:
Ответ: молярная
доля сахарозы в растворе сахарозы с
массовой долей 67% составляет 0,097.
Пример
3.
Какой объем серной кислоты с массовой
долей 96% (плотностью 1,84 г/см3)
и какую массу воды нужно взять для
приготовления 100 мл 15%-ного (по массе)
раствора H2SO4
(
= 1,10 г/см3).
Р е ш е н и е. 1) Найдем массу 100 мл 15% раствора h2so4:
mH2SO4-р-ра
= V
= 1001,10
=110 г.
2)
Из формулы массовой доли находим массу
серной кислоты, содержащейся в этом
растворе:
;
mH2SO4
=
3)
Найдем массу 96% раствора, содержащего
16,5 г H2SO4:
4)
Находим объем 96 %-ного раствора серной
кислоты:
Ответ:
для приготовления 100мл 15%-ного раствора
H2SO4
потребуется 9,3 мл 96%-ного раствора серной
кислоты и 110 – 16,5 = 93,5 г воды.
Соседние файлы в папке ЗКТэССО
- #
- #
- #
- #
- #
- #
- #
- #
- #
Определение массовой доли, молярности и мольной доли
Задача 4.
Определите массовую долю NаС1 в 0,5 М водном растворе (плотность раствора принять равной 1,000 г/мл).
Дано:
молярная концентрация NаС1 в р-ре: См(NаС1) = 0,5 моль/л.;
плотность раствора: рр-ра = 1,000 г/мл.
Найти:
массовую долю NаС1 в растворе.
Решение:
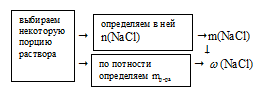
Схематично алгоритм решения можно представить так:
Наиболее удобно выбрать именно объем раствора, т.к. известная концентрация выражена в моль/л. Причем разумнее всего взять объем равный 1 л.
По записи концентрации (0,5 моль/л) видно, что в этом 1 л раствора содержится 0,5 моль чистой соли NаС1.
Определим массу 0,5 моль NаС1:
m(NаС1) = n(NаС1) . М(NаС1) = 0,5 . 58,5 = 29,25 г.
Определим массу раствора:
mр-ра = Vр-ра . pр-ра = 1000мл . 1 г/мл = 1000 г.
Массовую долю NаС1 в растворе определяем, пользуясь соотношением:
Ответ: 
Задача 5.
Определить молярность 18%-ного раствора Н2SО4 в воде (рр-ра = 1,124 г/мл).
Дано:
массовая доля Н2SО4 в растворе: 
плотность раствора: рр-ра = 1,124 г/мл.
Найти:
молярную концентрацию Н2SО4 в растворе.
Решение:
Схематично алгоритм решения можно представить так:
Наиболее удобно выбрать именно массу раствора, т.к. известна массовая доля. Причем разумнее всего взять массу 100 г.
1. Находим массу серной кислоты в выбранной массе раствора:
100 г составляют 100%
х г составляют 18%
в 100 г 18% -ного раствора.
2. Определяем количество вещества в 18 г Н2SО4
3. Используя плотность, находим объем 100 г раствора:
4. Объем переводим в литры, т.к. молярная концентрация измеряется в моль/л: Vр-ра = 89 мл = 0,089 л.
5. Определяем молярную концентрацию:
Ответ: СМ(Н2SО4) = 2,07 моль/л.
Задача 6.
Определите мольную долю NаОН в водном растворе, если его концентрация равна 9,96 моль/л, а плотность 1,328 г/мл.
Дано:
молярная концентрация NаОН в растворе: См(NаОН) = 9,96 моль/л;
плотность раствора: рр-ра = 1,328 г/мл.
Найти:
мольную долю NаОН в растворе.
Решение:
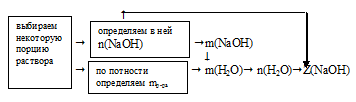
Схематично алгоритм решения можно представить так:
Наиболее удобно выбрать именно объем раствора, т.к. известная концентрация выражена в моль/л. Причем разумнее всего взять объем равный 1 л.
По записи концентрации (9,96 моль/л) видно, что в этом 1 л раствора содержится 9,96 моль чистого NаОН.
Для определения мольной доли NаОН еще необходимо выявить количество вещества (n, моль) воды в выбранной порции раствора (1л). Для этого определим массу раствора и вычтем из нее массу NаОН.
Ответ1: 
Задача 7.
Мольная доля водного раствора Н3РО4 в воде составляет 7,29%(мольн.) Определите молярность этого раствора, если его плотность 1,181 г/мл.
Дано:
мольная доля Н3РО4 в растворе: Z(Н3РО4) = 7,29%;
плотность раствора: рр-ра= 1,181 г/мл.
Найти:
молярную концентрацию Н3РО4 в растворе.
Решение:
Схематично алгоритм решения можно представить так:
Наиболее удобно выбрать такое количество раствора, в котором:
n(Н3РО4) + n(Н2О) = 100 моль.
В этой порции раствора количество вещества Н3РО4 численно совпадает с мольной долей: Z(Н3РО4) = 7,29 моль.
Для определения молярности нам осталось выявить объем выбранной порции раствора. Его можно вычислить, используя плотность раствора. Но для этого необходимо знать его массу. Массу же раствора можно рассчитать исходя из количеств веществ компонентов (Н3РО4 и Н2О) раствора.
1. Выбранная нами порция содержит суммарно 100 моль. Количество вещества Н3РO4 нам известно. Используя эти данные, находим n(Н2О).
п(Н2О) = 100 – 7,29 = 92,71 моль.
2. Определим массу 92,71 моль воды:
m(Н2О) = n(Н2О) . М(Н2О) = 92,71 . 18 = 1669 г.
3. Определим массу 7,29 моль Н3РО4:
m(Н3РO4) = n(Н3РО4) . М(Н3РО4) = 7,29 . 98 = 714,4 г.
4. Находим массу выбранной порции раствора:
mр-ра = m(Н2О) + m(Н3РО4) = 1669 + 714,4 =2383 г.
5. Используя данные о плотности раствора, находим его объем:
6. Теперь определим молярную концентрацию:
Ответ: СМ(Н3РО4) = 3,612моль/л.
Задача 8.
Определите мольные доли веществ в водном растворе КОН, если массовая доля гидроксида калия в нем составляет 10,00%.
Дано:
массовая доля КОН в растворе: 
Найти:
мольную долю КОН и Н2O(в растворе: Z(КОН) = ?; Z(H2O) = ?
Решение:
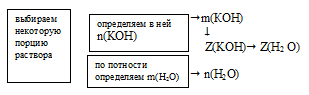
Схематично алгоритм решения можно представить так:
Наиболее удобно выбрать именно массу раствора, т.к. известна массовая доля. Причем разумнее всего взять массу 100 г. В этом случае массы каждого компонента совпадут с численным значением массовой доли:
m(КОН) = 10 г, m(Н2О) = 100 – m(КОН) = 100 – 10 = 90 г.
1. Определим количество вещества (n, моль) воды и КОН.
2. Определяем мольную долю КОН
3. Определяем мольную долю воды:
Z(Н2O) = 1 – Z(КОН) = 1 – 0,035 = 0,965.
Ответ: Z(КОН) = 0,035 (доли от 1) или 3,5%(мольн.);
Задача 9.
Определите массовые доли веществ в водном растворе Н2SО4, если мольная доля серной кислоты в нем составляет 2,000%.
Дано:
мольная доля Н2SО4 в растворе: Z (Н2SО4)= 2,000%;
Найти:
массовые доли Н2SО4 и Н2О в растворе: 

Решение:
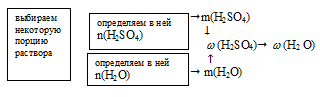
Схематично алгоритм решения можно представить так:
Наиболее удобно выбрать такое количество раствора, в котором n(Н2SО4) + n(Н2О) = 100 моль. В этой порции раствора количество вещества Н2SО4 численно совпадает с мольной долей: nН2SО4= 2 моль.
1. Находим количество вещества воды в выбранной порции
n(Н2О) = 100 моль – 2 моль = 98 моль.
2. Определяем массы Н2SО4 и Н2О по найденным значениям количеств веществ.
m (Н2SО4) = n(Н2SО4) . М(Н2SО4) = 2 . 98 = 196 г.
m(Н2О) = n(Н2О) . М(Н2О) = 98 . 18 = 1764 г.
3. По массам компонентов раствора находим их массовые доли.
Ответ: 

Комментарии;
1 Мольная доля выражена в долях от единицы.