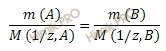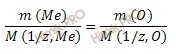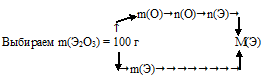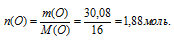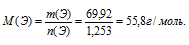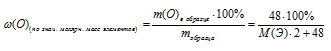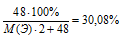При окислении 16,74 грамм двухвалентного металла образовалась 21,54 грамма оксида. Вычислите молярную массу эквивалента металла и его оксида. Чему равна атомная масса металла?
Решение задачи
Согласно закону эквивалентов: массы реагирующих веществ пропорциональны молярным массам эквивалента этих веществ.
По условию задачи оксид образован двухвалентным металлом, следовательно, формулу запишем так MeO.
Исходя из массы оксида металла и массы металла, определим массу кислорода по формуле:
m (O) = m (MeO) – m (Me)
Получаем:
m (O) = 21,54 – 16,74 = 4,8 (г).
Закон эквивалентов в данном случае имеет вид:
Из уравнения находим молярную массу эквивалента металла:
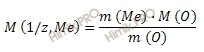
Рассчитаем молярную массу металла по формуле:
Где:
М – молярная масса,
В – валентность,
Э – эквивалентная масса
n – число атомов элемента в соединении.
Получаем:
M (Мe) = 2 ∙ 27,9 = 55,8 (г/моль).
Напомню, что молярная масса вещества, имеющего атомную или металлическую структуру, численно равна относительной атомной массе.
Следовательно, атомная масса металла равна 55,8 г/моль. А металл – железо (Fe).
Учитывая, что молярная масса оксида железа (FeO) равна 71,8 г/моль, найдем молярную массу эквивалента оксида железа (FeO) рассчитаем по формуле:
Получаем:
Э (FeO) = 71,8/2 = 35,9 (г/моль).
Ответ:
молярная масса эквивалента металла равна 27,9 г/моль;
атомная масса металла равна 55,8 г/моль;
молярная масса эквивалента оксида равна 35,9 г/моль.
Определение молярной массы эквивалента металла
Цель работы: усвоить
понятия химического эквивалента,
молярной массы эквивалента, закона
эквивалентов; ознакомиться с
экспериментальным определением молярной
массы эквивалента металла методом
вытеснения водорода из кислоты.
Теоретическая часть
Известно,
что количество вещества определяется
числом структурных единиц (атомов,
молекул, ионов) этого вещества и выражается
в молях.
Моль ()– это единица количества вещества,
содержащая столько же структурных
единиц данного вещества, сколько атомов
содержится в 0,012 кг углерода, состоящего
только из изотопа12С.
Молярная
масса (М) вещества
представляет собой отношение массы
вещества (m) к его количеству (),
а значение молярной массы численно
совпадает с относительной молекулярной
массой вещества или относительной
атомной массой элемента, но измеряется
в г/моль.
Эквивалентом
вещества (э),
вступающего в какую-либо реакцию,
называют такое его количество, которое
приходится на единицу валентности
соответствующего элемента при образовании
им соединения.
Химический
эквивалент и молярная масса эквивалента
представляют собой важнейшие характеристики
элементов, простых и сложных веществ,
учитывая то, что согласно закону
эквивалентов
все вещества взаимодействуют между
собой в эквивалентных количествах.
Единицей
химического эквивалента (э),
так же как и количества вещества является
моль,
а молярная
масса эквивалента (Мэ),
соответственно измеряется в г/моль.
Так,
водород в своих соединениях, как правило,
одновалентен, и его эквивалент равен 1
моль Н или 1/2 моль Н2,
а молярная масса его эквивалента Мэ(Н)
= 1 г/моль.
Кислород
в своих соединениях двухвалентен, тогда
его эквивалент равен 1/2 моль О или 1/4
моль О2,
а молярная масса его эквивалента Мэ(О)
= 8 г/моль.
Железо
в своих соединениях может быть и двух-,
и трехвалентным, тогда его эквивалент
в первом случае будет равен 1/2 моль Fe, а
молярная масса эквивалента Мэ(Fe) = 28
г/моль. Эквивалент железа во втором
случае будет равен 1/3 моль Fe, а молярная
масса эквивалента Мэ(Fe) = 18,6 г/моль.
Следовательно, молярную массу эквивалента
простого вещества можно рассчитать по
формуле:
, (1)
где М(эл-та)
– молярная масса элемента;
В(эл-та)
– валентность элемента.
Молярные
массы эквивалентов сложных веществ
(оксидов, кислот, оснований, солей)
рассчитываются несколько иначе.
Молярная
масса эквивалента оксида
рассчитывается отношением молярной
массы оксида к произведению числа атомов
элемента на его валентность.
,
где М(оксида)
– молярная масса оксида;
n(эл-та) –
число атомов элемента;
В(эл-та) –
валентность элемента.
Для
оксида железа (Ш), например, молярная
масса его будет равна:
Молярная масса
эквивалента кислотырассчитывается
отношением молярной массы кислоты к
числу атомов водорода в кислоте, способных
замещаться в химических реакциях.
,
где М
(кислоты) – молярная масса кислоты;
n
(H) – число замещающихся в химической
реакции атомов водорода.
Для серной
кислоты (H2SO4),
например, молярная масса эквивалента
будет равна:
Молярная
масса эквивалента основания
рассчитывается отношением молярной
массы основания к числу гидроксогрупп.
,
где
М (основания) – молярная масса основания;
n
(OH) – число гидроксогрупп.
Для
гидроксида кальция (Ca(OH)2),
например, молярная масса эквивалента
будет равна:
Молярная
масса эквивалента соли
рассчитывается отношением молярной
массы соли к произведению числа атомов
металла на их валентность.
,
где М
(соли) – молярная масса соли;
n (Ме) –
число атомов металла;
В (Ме) – валентность
металла.
Для
сульфата натрия (Na2SO4),
например, молярная масса эквивалента
будет равна:
Из
закона
эквивалентов
следует, что массы вступающих и
образующихся в результате реакции
веществ прямопропорциональны молярным
массам их эквивалентов:
, (2)
где
m(1)
и Мэ(1)
– масса и молярная масса эквивалента
первого вещества;
m(2)
и Мэ(2)
– масса и молярная масса эквивалента
второго вещества.
Из
следствия из закона Авогадро вытекает
понятие молярный
объем — объем,
который занимает 1 моль любого газа при
нормальных условиях, т.е. при р = 105
Па (1 атм или 760 мм рт. ст.) и Т = 273 К ( 0о
С). Значение
этого объема равно 22,4 л/моль (22400 мл/моль).
Отсюда можно вывести понятие и молярного
объема эквивалента
газа (или эквивалентного объема) –
объема, занимаемого при нормальных
условиях одним эквивалентом (одной
молярной массой эквивалента) газа.
Известно,
что эквивалент водорода равен 1/2 моль
Н2,
тогда молярный объем эквивалента
водорода Vэ(Н2)
= 11,2 л/моль; соответственно Vэ(О2)
= 5,6 л/моль, т.к. эквивалент кислорода
равен 1/4 моль О2.
Если
же в реакции участвуют газы и известны
их объемы, то соотношение (2) можно
представить следующим образом:
(3)
где m(1)
и Мэ(1) –
масса и молярная масса эквивалента
первого вещества;
V(2)
и Vэ(2) –
объем и молярный объем эквивалента
второго вещества.
Следует
иметь ввиду, что объемы, входящие в
соотношение (3), нужно приводить
к нормальным условиям
по формуле объединенного закона
Гей-Люссака – Бойля –Мариотта:
,
откуда(4)
где р,
V, Т –
давление, объем и температура газа при
условиях опыта;
ро,
Vо,
То
– давление, объем и температура газа
при нормальных условиях.
Известны
методы экспериментального определения
молярных масс эквивалентов: 1) метод
прямого определения – молярную массу
эквивалента определяют по данным прямого
синтеза кислородного или водородного
соединения данного элемента; 2)
аналитический метод – производится
точный анализ соединения данного
элемента с любым другим, молярная масса
эквивалента которого известна; 3) метод
вытеснения водорода — используется для
определения молярной массы эквивалента
тех металлов, которые способны вытеснить
водород из разбавленных кислот и щелочей;
4) электрохимический метод – определяется
масса металла, осаждающегося на электроде
при электролизе раствора соли этого
металла. Молярная масса эквивалента
рассчитывается по закону Фарадея: при
прохождении через раствор или расплав
электролита 965000 Кулонов электричества
на электродах выделяется по одному
эквиваленту вещества.
ЭКСПЕРИМЕНТАЛЬНАЯ
ЧАСТЬ
Сущность
экспериментального определения молярной
массы эквивалента металла заключается
в определении объема водорода (приведенного
к нормальным условиям), вытесняемого
из кислоты навеской металла, взятой на
аналитических весах.
Произведением
молярной массы эквивалента металла на
его валентность определяют молярную
массу атома металла.
По
молярной массе атома металла и его
валентности находят местоположение
металла в периодической системе элементов
Д.И.Менделеева, т.е. его название.
По
указанию преподавателя студент взвешивает
на аналитических весах навеску металла
известной валентности.
Прибор
для определения молярной массы эквивалента
изображен на рисунке.
П
еред началом работы прибор следует
проверить на герметичность. Для этого
отсоединяют пробирку А от прибора, через
воронку С заливают водой таким образом,
чтобы уровень воды в бюретке В установился
на нулевом делении или несколько ниже;
избыток воды удалить. Присоединяют
пробирку А на место. Затем поднимают
воронку C вверх и следят за уровнем воды
в бюретке В. Если уровень в последней
непрерывно повышается, то это означает,
что прибор негерметичен и следует
проверить все резиновые соединения.
Если же прибор герметичен, то повышение
уровня воды в бюретке В произойдет
незначительно только в первый момент,
а потом он будет оставаться неизменным.
Убедившись
в герметичности прибора, отсоединяют
пробирку А от прибора и, записав начальный
уровень воды в бюретке В, наливают в
пробирку А 1/4 ее объема соляной кислоты,
приготовленной для определения молярной
массы эквивалента металла соответствующей
валентности.
Держа
пробирку А в положении, близком к
горизонтальному, помещают на сухое
место у отверстия пробирки взвешенный
металл и в таком положении соединяют
пробирку А с бюреткой В, следя за тем,
чтобы металл не упал в кислоту.
Убедившись
вторично
в герметичности прибора путем поднятия
воронки С вверх, стряхивают металл в
кислоту и наблюдают за ходом реакции.
По
окончании реакции (прекращение выделения
пузырьков водорода), устанавливают
уровень воды в бюретке В и воронке С на
одной высоте, перемещая кольцо К с
воронкой С вниз по штативу, и записывают
уровень воды в бюретке В после окончания
опыта. Шкала бюретки В проградуирована
в миллилитрах (мл).
С
помощью барометра определяют величину
атмосферного давления ( ратм ),
термометра – температуру ( t ) воздуха
в помещении (соответственно и температуру
воды в приборе) в момент проведения
опыта.
С
помощью таблицы 1 определяют давление
водяного пара ( рН2Опар ),
соответствующего измеренной температуре
опыта, в мм рт.ст.
Таблица
1
Зависимость
давления водяного пара от температуры
|
t |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
|
рН2Опар |
12,8 |
13,6 |
14,5 |
15,5 |
16,5 |
17,5 |
18,7 |
19,8 |
21,1 |
22,4 |
23,8 |
Порядок расчета
-
Определите
объем выделившегося водорода в результате
опыта. Для этого от значения уровня
воды в бюретке В после окончания опыта
( V2
) следует вычесть значение уровня воды
в бюретке В в начале опыта ( V1
).
V(Н2)
= V2
– V1.
Переведите
значение объема выделившегося в
результате опыта водорода в кубические
дециметры, учитывая, что 1 см3
= 10 –3
дм3.
-
Приведите
экспериментальный объем выделившегося
водорода к нормальным условиям,
воспользовавшись формулой 4. Следует
учесть, что давление внутри бюретки В
складывается из давления водорода и
давления водяного пара внутри объема
бюретки при данной температуре:
ратм
= рН2
+ рН2Опар
, тогда
где ратм
– измеренное атмосферное давление во
время проведения опыта;
рН2Опар –
давление водяного пара при температуре
опыта;
V
(Н2) –
экспериментальный объем водорода;
Т
– температура проведения опыта (К),
равная (273+t);
ро,
То
– давление и температура при нормальных
условиях.
-
Вычислите
молярную массу эквивалента металла, с
точностью до 0,1 г/моль, воспользовавшись
формулой 3:
4. Воспользовавшись
формулой 1, рассчитайте молярную массу
металла и укажите какой это металл.
Результаты
эксперимента представьте в виде таблицы
2.
Таблица
2
|
масса |
pатм, мм |
t, |
V1,, |
V2, |
V(H2), |
pH2Oпар, мм |
V0(H2), |
Мэ |
М |
5. Вычислите
величины абсолютной и относительной
ошибок (Х).
Абсолютная
ошибка:
Хабс.
= М (Ме)
табличное – М
(Ме)
экпериментальное
Относительная
ошибка:
Вопросы для
самоконтроля
1. Что
называется эквивалентом вещества?
-
Что
является единицей эквивалента вещества? -
Какую
размерность имеет молярная масса
эквивалента вещества? -
Какие
значения имеют молярные массы эквивалентов
водорода и кислорода? -
Как
можно рассчитать молярную массу
эквивалента элемента? -
Что
такое молярный объем и молярный объем
эквивалента? -
Какие
значения имеют молярные объемы
эквивалентов водорода и кислорода? -
Как
формулируется закон эквивалентов? -
Почему
при выполнении расчетов в экспериментальной
части работы нужно знать давление
водяного пара? -
Какие
Вы знаете методы экспериментального
определения молярной массы эквивалента
металлов?
Задачи
-
Медь
с кислородом образует два соединения,
в которых содержится 79,9 % меди и 20,1 %
кислорода, и 88,8 % меди и 11,2 % кислорода.
Определите молярные массы эквивалентов
меди в этих соединениях и составьте
формулы этих соединений. -
При
сгорании 3 г магния образовалось 5 г
оксида магния. Рассчитайте молярную
массу эквивалента магния. -
При
взаимодействии 2,4 г углерода с кислородом
образовалось 5,6 г оксида. Определите
молярную массу эквивалента углерода
в этом соединении и напишите уравнение
реакции. -
При
взаимодействии 4 г двухвалентного
металла с кислородом образовалось 5,6
г оксида. Определите, какой это металл
и напишите уравнение реакции. -
При
растворении в соляной кислоте 5,4 г
трехвалентного металла выделилось
6,72 л водорода, измеренного при н.у.
Определите, какой это металл и напишите
уравнение реакции. -
При
взаимодействии одновалентного металла
с 0,2 г водорода образовалось 4,8 г гидрида
металла. Определите, какой это металл
и напишите уравнение этой реакции. -
При
окислении 8 г металла, проявляющего
валентность, равную I, получено 9 г
оксида. Определите, какой это металл и
напишите уравнение данной реакции. -
Рассчитайте
объем водорода, выделившегося при
растворении в соляной кислоте 18 г
металла, молярная масса эквивалента
которого равна 9 г/моль. -
При
взаимодействии 0,9 г трехвалентного
металла с серой образовалось 2,5 г
сульфида металла. Определите, какой
это металл, учитывая, что молярная масса
эквивалента серы в этом соединении 16
г/моль. Напишите уравнение соответствующей
реакции. -
При
окислении 6,4 г серы образовалось 16 г
оксида. Определите молярную массу
эквивалента серы в этом соединении и
напишите уравнение соответствующей
реакции.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Как вычислить эквивалентные массы оксида и металла
Эквивалент – такое количество химического элемента, которое либо связывает, либо замещает один моль атомов водорода. Соответственно, масса одного эквивалента называется эквивалентной массой (Мэ), и выражается в г/моль. Перед учащимися на химии часто ставят задачу определить эквивалентную массу того или иного вещества (соединения). Например, металла и образованного им оксида.

Инструкция
В первую очередь следует запомнить несколько простых правил. Если речь идет о металле, его эквивалентная масса рассчитывается по формуле: Мэ=М/В, где М – атомная масса металла, а В – его валентность. Рассмотрите это правило на конкретных примерах.
Кальций (Са). Его атомная масса 40,08. Округленно примите ее за 40. Валентность равна 2. Следовательно, Мэ(Са) = 40/2 = 20 г/моль. Алюминий (Al). Его атомная масса 26,98. (Округленно 27). Валентность равна 3. Таким образом, Мэ(Al) = 27/3 = 9 г/моль.
Перечисленные способы применимы, если речь идет о чистых металлах. А если они входят в состав какого-либо соединения, например, тех же оксидов? Тут надо запомнить другое правило: эквивалентная масса оксида вычисляется по формуле: Мэ + Мо, где Мо – эквивалентная масса кислорода. Она, соответственно, рассчитывается по уже рассмотренной формуле М/В, то есть 16/2 = 8.
Предположим, у вас есть основной оксид алюминия, Al2O3. Как посчитать его эквивалентную массу? Очень просто: 27/3 + 16/2 = 17 г/моль.
Есть ли другой способ определения эквивалентных масс металла и его оксида? Да, и весьма эффективный. Он основан на так называемом законе эквивалентов, согласно которому все вещества реагируют друг с другом в эквивалентных количествах. Например: металл массой 33,4 грамма вступил в реакцию окисления с кислородом воздуха. В результате получился оксид общей массой 43 грамма. Требуется определить эквивалентные массы самого металла и его оксида.
Сначала вычислите, сколько кислорода соединилось с металлом в ходе этой реакции: 43 – 33,4 = 9,6 грамм. Согласно закону эквивалентов, эта масса во столько же раз больше эквивалентной массы кислорода (которая, напомним, равна 8), во сколько раз эквивалентная масса металла меньше его первоначального количества. То есть 33,4/Мэ(ме) = 9,6/8. Следовательно, Мэ(ме) = 33,4*8/9,6 = 27,833 г/моль, или округленно 27,8 г/моль. Такова эквивалентная масса металла.
Эквивалентную же массу оксида найдите следующим действием: 27,8 + 8 = 35,8 г/моль.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
2022-08-31
Оксид неизвестного металла (II) массой 14,4 г восстановили смесью $H_{2}$ и $CO$. В результате реакции образовалось 1,8 г $H_{2}O$ и 4,4 г $CO_{2}$. Определите неизвестный металл.
Решение:
Рассчитываем количества воды и оксида углерода (IV):
$nu (H_{2}O) = frac{m(H_{2}O)}{M(H_{2}O)}; nu (H_{2}O) = frac{1,8}{18} = 0,1 моль$;
$nu (CO_{2}) = frac{m(CO_{2})}{M(CO_{2})}; nu (CO_{2}) = frac{4,4}{44} = 0,1 моль$.
Оксид металла реагирует с водородом по уравнению
$MeO + H_{2} rightarrow Me + H_{2}O$.
Рассчитываем количество оксида металла, всту-пившего в реакцию с водородом. Согласно уравнению реакции
$nu_{1}(MeO) = nu (H_{2}O); nu_{1}(MeO)) = 0,1 моль$.
Вычисляем количество оксида металла, вступившего в реакцию с оксидом углерода:
$MeO + CO rightarrow Me + CO_{2}$.
Из уравнения реакции следует, что
$nu_{2}(MeO) = nu (CO_{2}); nu_{2}(MeO) = 0,1 моль$.
Рассчитываем общее количество оксида металла:
$nu (MeO) = nu_{1} (MeO)) + nu_{2}(MeO)$;
$nu (MeO) = 0,1 + 0,1 = 0,2 моль$.
Находим молярную массу оксида металла:
$M(MeO) = frac{m(MeO)}{ nu(MeO)}$;
$M(MeO) = frac{14,4}{0,2} = 72 г/моль$.
Вычисляем молярную массу неизвестного металла:
$M(Me) = M(MeO) — M(O)$;
$M(Me) = 72 — 16 = 56 г/моль$.
Металлом с молярной массой 56 г/моль является $Fe$.
Способы определения молекулярной формулы оксида и элемента металла, образующего данный оксид
Задача 115.
Некоторый элемент образует оксид вида Э2О3, где Э — неизвестный элемент. Массовая доля кислорода в нем составляет 30,08% . Определите элемент и формулу оксида.
Дано: формула оксида: Э2О3; массовая доля кислорода в оксиде:
Найти: элемент и формулу оксида.
Решение:
Для выявления неизвестного элемента необходимо определить его молярную массу, по которой, пользуясь Периодической системой Д.И.Менделеева, возможно найти неизвестный элемент.
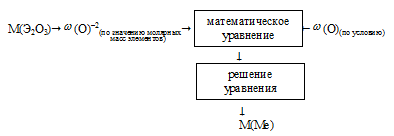
I способ (последовательно-разветвленный алгоритм).
Схематично этот алгоритм можно изобразить так:
1) Произвольно выбираем некоторую массу образца. Наиболее удобная масса — 100 г, т.к. в условии фигурирует массовая доля. Тогда в 100 г Э2О3 содержится 30,08 г кислорода.
2) По разности находим массу неизвестного элемента:
m(Э) = 100 – m(О) = 100 – 30,08 = 69,92 г содержится в выбранном образце Э2О3.
3) Находим количество вещества атомарного кислорода:
4) По известной общей формуле Э2О3 вычисляем количество вещества атомов неизвестного элемента. На каждые 3 моль атомов кислорода приходится 2 моль атомов неизвестного элемента.
Составим пропорцию:
3 моль атомов кислорода приходится на 2 моль атомов Э
1,88 моль атомов кислорода приходится на х моль атомов Э.
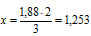
5) Теперь находим молярную массу атомов неизвестного элемента:
По таблице Д. И. Менделеева находим элемент, имеющий молярную массу 55,8 г/моль. Подходит железо. Этот элемент действительно проявляет степень окисления (+3) и образует оксид Fе2О3.
II способ (встречный алгоритм).
Схематично алгоритм можно изобразить таким образом:
Применим предложенный алгоритм.
1) Записываем выражение для молярной массы Э2О3:
М(Э2О3) = М(Э) . 2 + М(О) . 3 = (М(Э) . 2 + 48) г/моль.
2) Выбираем массу образца Э2О3, соответствующую 1 моль вещества. Она составит m(Э2О3) = (M(Э) . 2 + 48) г. Масса кислорода в этом образце будет 48 г.
3) Записываем выражение для массовой доли кислорода в выбранном образце:
4) Приравниваем полученное выражение к значению массовой доли кислорода из условия:
Получили одно уравнение с одним неизвестным М(Э). Решаем его и получаем М(Э) = 55,8 г/моль.
По таблице Д.И. Менделеева находим элемент, имеющий молярную массу 55,8 г/моль. Подходит железо. Этот элемент действительно проявляет степень окисления (+3) и образует оксид Fе2О3.
Ответ: искомый элемент — железо, формула Fе2О3.