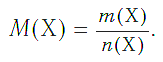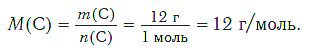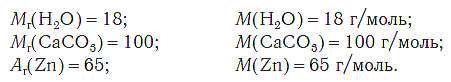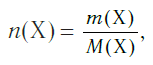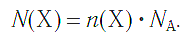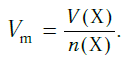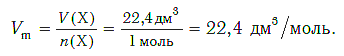Рассчитать объем хлора.
Рассчитать объем хлора (газа) при нормальных условиях, если известна его масса, можно по формуле: V = m · Vm / M = ν · Vm. Рассчитать объем хлора (газа), если известна его масса, температура и давление, можно по формуле: V = m · R · T / (p · M) = ν · R · T / p.
Химическая формула хлора Cl₂.
Расчет объема хлора (газа)
Теория расчета объема газа
Пример: Рассчитайте объем для 35 г хлора
Рассчитать объем газа: азота, водорода, гелия, хлора
Рассчитать объем хлора (газа) при нормальных условиях:
Рассчитать объем хлора (газа):
Теория:
Рассчитать объем хлора (газа) при нормальных условиях, если известна его масса, можно по формуле:
V = m · Vm / M = ν · Vm,
где
V – объем газа, л,
ν – количество вещества, моль,
Vm – молярный объем газа, л/моль, Vm = 22,4 л/моль,
ν = m / M,
m – масса газа, г,
М – молярная масса газа, г/моль,
M(Cl₂) = 2·35,457 = 70,914 г/моль,
Нормальные условия: 0 оС (или 273,15 К), 101,325 кПа или 1 атм.
Рассчитать объем хлора (газа), если известна его масса, температура и давление, можно по формуле:
V = m · R · T / (p · M) = ν · R · T / p,
где
V – объем газа, л,
ν – количество вещества, моль,
ν = m / M,
m – масса газа, г,
М – молярная масса газа, г/моль,
M(Cl₂) = 2·35,457 = 70,914 г/моль,
R – универсальная газовая постоянная, R ≈ 8,314 Дж/(моль⋅К),
T – термодинамическая температура, К.
P – давление, кПа.
Пример: Рассчитайте объем для 35 г хлора:
Рассчитайте объем для 35 г хлора при нормальных условиях.
V = m · Vm / M = 35 грамм · 22,4 л/моль / 70,914 г/моль = 11,055 литров.
Рассчитайте объем для 35 г хлора при 30 градусах Цельсия (303,15 К), давлении 30 кПа.
V = m · R · T / p · M = 35 грамм · 8,314 Дж/(моль⋅К) · 303,15 К / (30 кПа · 70,914 г/моль) = 41,465 литр.
Рассчитать объем газа: азота, водорода, гелия, хлора
Коэффициент востребованности
912
Таблица молярных объёмов химических элементов.
Молярный объём – отношение объёма вещества к его количеству при определенной температуре и давлении.
Молярный объём имеет обозначение Vm.
Молярный объём численно равен объёму одного моля вещества.
Молярный объём в Международной системе единиц (СИ) измеряется в кубических метрах на моль, русское обозначение: м3/моль; международное: m3/mol.
Термин «молярный объём» может быть применён к простым веществам, химическим соединениям и смесям.
Молярный объём зависит от температуры, давления и агрегатного состояния вещества.
Молярный объём вещества вычисляется по формуле:
Vm = V/n = M/ρ,
где
V – объем вещества,
n – количество вещества,
M – молярная масса,
ρ – плотность вещества.
Таблица молярных объёмов химических элементов (1 часть):
| Атомный номер | Химический элемент | Символ | Молярный объём, см3/моль |
| 1 | Водород | H | 11,21 |
| 2 | Гелий | He | 22,42354 |
| 3 | Литий | Li | 12,97383 |
| 4 | Бериллий | Be | 4,8767 |
| 5 | Бор | B | 4,3947 |
| 6 | Углерод | C | 5,314469 – графит,
3,42 – алмаз |
| 7 | Азот | N | 11,196 |
| 8 | Кислород | O | 11,196 |
| 9 | Фтор | F | 11,202 |
| 10 | Неон | Ne | 22,42 |
| 11 | Натрий | Na | 23,74976 |
| 12 | Магний | Mg | 13,984 |
| 13 | Алюминий | Al | 9,993 |
| 14 | Кремний | Si | 12,05386 |
| 15 | Фосфор | P | 16,99054 |
| 16 | Сера | S | 16,35969 |
| 17 | Хлор | Cl | 11,0308 |
| 18 | Аргон | Ar | 22,392 |
| 19 | Калий | K | 45,675584 |
| 20 | Кальций | Ca | 25,85677 |
| 21 | Скандий | Sc | 15,060606 |
| 22 | Титан | Ti | 10,62059 |
| 23 | Ванадий | V | 8,3373977 |
| 24 | Хром | Cr | 7,282 |
| 25 | Марганец | Mn | 7,35449 |
| 26 | Железо | Fe | 7,0923 |
| 27 | Кобальт | Co | 6,6217 |
| 28 | Никель | Ni | 6,58884 |
| 29 | Медь | Cu | 7,12399 |
| 30 | Цинк | Zn | 9,16092 |
Таблица молярных объёмов химических элементов (2 часть):
| 31 | Галлий | Ga | 11,80945 |
| 32 | Германий | Ge | 13,6464 |
| 33 | Мышьяк | As | 13,082 |
| 34 | Селен | Se | 16,3851 |
| 35 | Бром | Br | 25,610256 |
| 36 | Криптон | Kr | 22,34613 |
| 37 | Рубидий | Rb | 55,78838 |
| 38 | Стронций | Sr | 33,315589 |
| 39 | Иттрий | Y | 19,88 |
| 40 | Цирконий | Zr | 14,01075 |
| 41 | Ниобий | Nb | 10,84 |
| 42 | Молибден | Mo | 9,33 |
| 43 | Технеций | Tc | 8,5217 |
| 44 | Рутений | Ru | 8,17057 |
| 45 | Родий | Rh | 8,2655 |
| 46 | Палладий | Pd | 8,851 |
| 47 | Серебро | Ag | 10,282955 |
| 48 | Кадмий | Cd | 12,995 |
| 49 | Индий | In | 15,7 |
| 50 | Олово | Sn | 16,239398 |
| 51 | Сурьма | Sb | 18,181275 |
| 52 | Теллур | Te | 20,4487 |
| 53 | Йод | I | 25,689 |
| 54 | Ксенон | Xe | 22,253 |
| 55 | Цезий | Cs | 70,732 |
| 56 | Барий | Ba | 39,1245 |
| 57 | Лантан | La | 22,6 |
| 58 | Церий | Ce | 20,9472 |
| 59 | Празеодим | Pr | 21,221 |
| 60 | Неодим | Nd | 20,5763 |
Таблица молярных объёмов химических элементов (3 часть):
| 61 | Прометий | Pm | 19,961 |
| 62 | Самарий | Sm | 20,4487964 |
| 63 | Европий | Eu | 28,978642 |
| 64 | Гадолиний | Gd | 19,9 |
| 65 | Тербий | Tb | 19,3363 |
| 66 | Диспрозий | Dy | 19,0 |
| 67 | Гольмий | Ho | 18,7527 |
| 68 | Эрбий | Er | 18,449 |
| 69 | Тулий | Tm | 18,124 |
| 70 | Иттербий | Yb | 26,33789 |
| 71 | Лютеций | Lu | 17,77939 |
| 72 | Гафний | Hf | 13,41 |
| 73 | Тантал | Ta | 10,86774 |
| 74 | Вольфрам | W | 9,55 |
| 75 | Рений | Re | 8,858563 |
| 76 | Осмий | Os | 8,42 |
| 77 | Иридий | Ir | 8,52 |
| 78 | Платина | Pt | 9,249786 |
| 79 | Золото | Au | 10,2 |
| 80 | Ртуть | Hg | 14,821 |
| 81 | Таллий | Tl | 17,247535 |
| 82 | Свинец | Pb | 18,2716 |
| 83 | Висмут | Bi | 21,3681 |
| 84 | Полоний | Po | 22,727272 |
| 85 | Астат | At | 32,94 − предположительно |
| 86 | Радон | Rn | 22,816 |
| 87 | Франций | Fr | нет данных |
| 88 | Радий | Ra | 45,2 |
| 89 | Актиний | Ac | 22,5422 |
| 90 | Торий | Th | 19,791717 |
Таблица молярных объёмов химических элементов (4 часть):
| 91 | Протактиний | Pa | 15,03 |
| 92 | Уран | U | 12,4949559 |
| 93 | Нептуний | Np | 11,5892 |
| 94 | Плутоний | Pu | 12,313 |
| 95 | Америций | Am | 17,77615 |
| 96 | Кюрий | Cm | 18,28275 |
| 97 | Берклий | Bk | 16,71 |
| 98 | Калифорний | Cf | 16,62 |
| 99 | Эйнштейний | Es | нет данных |
| 100 | Фермий | Fm | нет данных |
| 101 | Менделевий | Md | нет данных |
| 102 | Нобелий | No | нет данных |
| 103 | Лоуренсий | Lr | нет данных |
| 104 | Резерфордий (Курчатовий) | Rf | нет данных |
| 105 | Дубний (Нильсборий) | Db | нет данных |
| 106 | Сиборгий | Sg | нет данных |
| 107 | Борий | Bh | нет данных |
| 108 | Хассий | Hs | нет данных |
| 109 | Мейтнерий | Mt | нет данных |
| 110 | Дармштадтий | Ds | нет данных |
Источник: https://www.schoolmykids.com
Коэффициент востребованности
3 877
zubareva45
8 лет назад
Светило науки — 4227 ответов — 26168 раз оказано помощи
Дано:
m(Cl₂) =28,4г.
————————
V(Cl₂) -?
1. Молярный объем Vm=22,4л./моль
2. Молярная масса хлора M(Cl₂)=35,5х2=71г./моль
3. Находим количество вещества n хлора массой 28,4г. по формуле:
n=m ÷M n= 28,4г.÷71г./моль=0,4моль
4. Находим объем хлора по формуле:
V = n x Vm V(Cl₂) = 0,4моль х 22,4л./моль= 8,96л.
5. Ответ: хлор массой 28,4г. займет объем 8,96л.
(5 оценок)
В уроке 9 «Молярная масса и молярный объем» из курса «Химия для чайников» выясним, что подразумевается под молярной массой и молярным объемом; приведем формулы для их вычисления. Напоминаю, что в прошлом уроке «Химическое количество вещества и моль» мы выяснили, что такое химическое количество вещества; рассмотрели моль в качестве единицы количества вещества, а также познакомились с постоянной Авогадро.
Молярная масса
Вы знаете, что одинаковое химическое количество любых веществ содержит одно и то же число структурных единиц. Но у каждого вещества его структурная единица имеет собственную массу. Поэтому и массы одинаковых химических количеств различных веществ тоже будут различны.
Молярная масса — это масса порции вещества химическим количеством 1 моль.
Молярная масса вещества Х обозначается символом M(Х). Она равна отношению массы данной порции вещества m(Х) (в г или кг) к его химическому количеству n(Х) (в моль):
В Международной системе единиц молярная масса выражается в кг/моль. В химии чаще используется дольная единица — г/моль.
Определим молярную массу углерода. Масса углерода химическим количеством 1 моль равна 0,012 кг, или 12 г. Отсюда:
Молярная масса любого вещества, если она выражена в г/моль, численно равна его относительной молекулярной (формульной) массе.
Например:
На рисунке 47 показаны образцы веществ (H2O, CaCO3, Zn), химическое количество которых одно и то же — 1 моль. Как видите, массы разных веществ химическим количеством 1 моль различны.
Молярная масса является важной характеристикой каждого отдельного вещества. Она отражает зависимость между массой и химическим количеством вещества. Зная одну из этих величин, можно определить вторую — массу по химическому количеству:
и, наоборот, химическое количество по массе:
а также число структурных единиц:
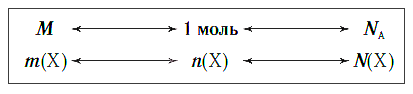
Взаимосвязь между этими тремя характеристиками вещества в любом его агрегатном состоянии можно выразить простой схемой:
Молярный объем
В отличие от твердых и жидких веществ все газообразные вещества химическим количеством 1 моль занимают одинаковый объем (при одинаковых условиях). Эта величина называется молярным объемом и обозначается Vm.
Подобно молярной массе, молярный объем газа равен отношению объема данного газообразного вещества V(Х) к его химическому количеству n(Х):
Так как объем газа зависит от температуры и давления, то при проведении различных расчетов берутся обычно объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимаются температура 0 °С и давление 101,325 кПа.
Установлено, что при нормальных условиях отношение объема любой порции газа к химическому количеству газа есть величина постоянная и равная 22,4 дм3/моль. Другими словами, молярный объем любого газа при нормальных условиях:
Молярный объем — это объем, равный 22,4 дм3, который занимает 1 моль любого газа при нормальных условиях.
Пример 1. Вычислите химическое количество SiO2, масса которого равна 240 г.
Спойлер
[свернуть]
Пример 2. Определите массу серной кислоты H2SO4, химическое количество которой 2,5 моль.
Спойлер
[свернуть]
Пример 3. Сколько молекул CO2 и сколько атомов кислорода содержится в углекислом газе массой 110 г?
Спойлер
[свернуть]
Пример 4. Какой объем занимает кислород химическим количеством 5 моль при нормальных условиях?
Спойлер
[свернуть]
Краткие выводы урока:
- Масса вещества химическим количеством 1 моль называется его молярной массой. Она равна отношению массы данной порции вещества к его химическому количеству.
- Объем газообразных веществ химическим количеством 1 моль при нормальных условиях одинаков и равен 22,4 дм3.
- Величина, равная 22,4 дм3/моль, называется молярным объемом газов.
Надеюсь урок 9 «Молярная масса и молярный объем» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Данный урок был заключительным в главе «Основные химические понятия».
Определите массу хлора (Cl2) (грамм), содержащегося при нормальных условиях в 4,48 литрах хлора (Cl2).
Решение задачи
Учитывая, что хлор (Cl2) – газ желтовато-зеленого цвета, вычислим массу хлора (Cl2), по формуле перерасчета, устанавливающей связь между массой и объемом газа:
Откуда:
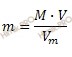
M (Cl2) = 2 ∙ 35,5 = 71 (г/моль).
Найдем массу хлора:
m (Cl2) = 71 ∙ 4.48 / 22,4 = 14,2 (г).
Ответ:
масса хлора (Cl2) равна 14,2 грамма.