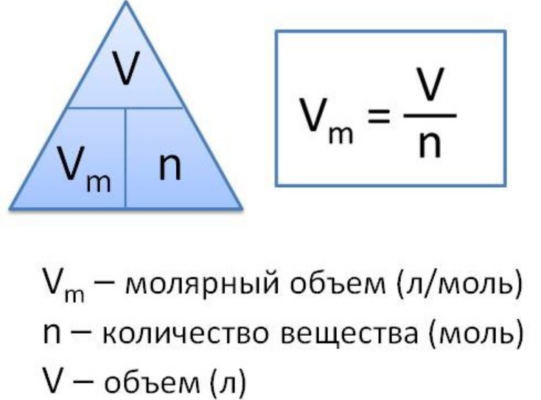
Молярный объем газа

4.3
Средняя оценка: 4.3
Всего получено оценок: 502.
4.3
Средняя оценка: 4.3
Всего получено оценок: 502.
Для того, чтобы узнать состав любых газообразных веществ необходимо уметь оперировать такими понятиями, как молярный объем, молярная масса и плотность вещества. В данной статье рассмотрим, что такое молярный объем, и как его вычислить?
Количество вещества
Количественные расчеты проводят с целью, чтобы в реальности осуществить тот или иной процесс или узнать состав и строение определенного вещества. Эти расчеты неудобно производить с абсолютными значениями массы атомов или молекул из-за того, что они очень малы. Относительные атомные массы также в большинстве случаев невозможно использовать, так как они не связаны с общепринятыми мерами массы или объема вещества. Поэтому введено понятие количество вещества, которое обозначается греческой буквой v (ню) или n. Количество вещества пропорционально числу содержащихся в веществе структурных единиц (молекул, атомных частиц).
Единицей количества вещества является моль.
моль – это такое количество вещества, которое содержит столько же структурных единиц, сколько атомов содержится в 12 г изотопа углерода.
Масса 1 атома равна 12 а. е. м., поэтому число атомов в 12 г изотопа углерода равно:
Na= 12г/12*1,66057*10в степени-24г=6,0221*10 в степени 23
Физическая величина Na называется постоянной Авогадро. Один моль любого вещества содержит 6,02*10 в степени 23 частиц.
Молярный объем газа
Молярный объем газа – это отношение объема вещества к количеству этого вещества. Эту величину вычисляют при делении молярной массы вещества на его плотность по следующей формуле:
Vm=M/p,
где Vm – молярный объем, М – молярная масса, а p – плотность вещества.
В международной системе Си измерение молярного объема газообразных веществ осуществляется в кубических метрах на моль (м3 /моль)
Молярный объем газообразных веществ отличается от веществ, находящихся в жидком и твердом состоянии тем, что газообразный элемент количеством 1 моль всегда занимает одинаковый объем (если соблюдены одинаковые параметры).
Объем газа зависит от температуры и давления, поэтому при расчетах следует брать объем газа при нормальных условиях. Нормальными условиями считается температура 0 градусов и давление 101,325 кПа. Молярный объем 1 моля газа при нормальных условиях всегда одинаков и равен 22,41 дм3 /моль. Этот объем называется молярным объемом идеального газа. То есть, в 1 моле любого газа (кислород, водород, воздух) объем равен 22,41 дм3 /м.
Таблица «молярный объем газов»
В следующей таблице представлен объем некоторых газов:
| Газ | Молярный объем, л |
| H2 | 22,432 |
| O2 | 22,391 |
| Cl2 | 22,022 |
| CO2 | 22,263 |
| NH3 | 22,065 |
| SO2 | 21,888 |
| Идеальный | 22,41383 |
Что мы узнали?
Молярный объем газа, изучаемый по химии (8 класс) наряду с молярной массой и плотностью являются необходимыми величинами для определения состава того или иного химического вещества. Особенностью молярного газа является то, что в одном моле газа всегда содержится одинаковый объем. Этот объем называется молярным объемом газа.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Аэлита Коробка
5/5
-
Александр Котков
5/5
-
Настя Бабич
5/5
-
Александр Котков
5/5
Оценка доклада
4.3
Средняя оценка: 4.3
Всего получено оценок: 502.
А какая ваша оценка?
Данный онлайн калькулятор рассчитывает молярный объем идеального газа в зависимости от условий (разных значений температуры и давления). Формулы и перечисление некоторых часто используемых значений для описания физических условий можно найти под калькулятором.
Молярный объем газа
Точность вычисления
Знаков после запятой: 3
Калькулятор использует уравнение молярного объема идеального газа:
Уравнение идеального газа является достаточно близкой аппроксимацией для многих реальных газов. Для заданных температуры и давления, молярный объем для всех идеальных газов один и тот же, и известен с точностью совпадающей с точностью универсальной газовой постоянной: R = 0.082 057 338(47) Л атм K−1 моль−1, то есть относительная стандартная неопределенность молярного объема равна 5.7×10−7, в соответствии с рекомендацией CODATA от 20141
Так как молярный объем одинаков для всех газов, он может быть вычислен независимо от газа по температуре и давлению (физическим условиям). Например, для стандартных условий по версии НИСТ (стандартной температуре 273.15 K и стандартному давлению 101.325 kPa), молярный объем идеального газа равен 22.413962×10-3 м3 моль-1 со стандартной неопределенностью 0.000013 x 10-3 м3 моль-12
Собственно, слова стандартные условия или нормальные условия (что не одно и тоже) для давления и температуры — это отсылка к «справочным», известным значениям температуры и давления, применяющимся для вычисления значений других физических величин, зависящих от давления и температуры.
Для удобства значения молярного объема для некоторых общеупотребимых физических условий приведены в таблице ниже.
| Физические условия | Температура | Давление | Молярный объем, литры |
|---|---|---|---|
| Стандартные условия (НИСТ) | 0C (273.15K) | 101.325кПа (1атм) | 22.414 |
| Стандартные условия (ИЮПАК) | 0C (273.15K) | 100.000кПа (1бар) | 22.711 |
| Нормальные условия (некоторые ГОСТы, НИСТ) | 20C (293.15K) | 101.325кПа (1атм) | 24.055 |
Разные отрасли и организации, могут использовать свои значения температуры и давления для расчетов. Используя калькулятор, мы можете ввести нужные вам значения температуры и давления и получить молярный объем газа.
Обратите внимание, что для больших значений (сотни атмосфер и тысячи градусов) поведение реальных газов отличается от поведения идеальных газов (собственно, поэтому они и не «идеальные») и использовать уравнение, приведенное выше, нельзя.
From Wikipedia, the free encyclopedia
In chemistry and related fields, the molar volume, symbol Vm,[1] or 
The molar volume has the SI unit of cubic metres per mole (m3/mol),[1] although it is more typical to use the units cubic decimetres per mole (dm3/mol) for gases, and cubic centimetres per mole (cm3/mol) for liquids and solids.
Definition[edit]
Change in volume with increasing ethanol fraction.
The molar volume of a substance i is defined as its molar mass divided by its density ρi0:
For an ideal mixture containing N components, the molar volume of the mixture is the weighted sum of the molar volumes of its individual components. For a real mixture the molar volume cannot be calculated without knowing the density:
There are many liquid–liquid mixtures, for instance mixing pure ethanol and pure water, which may experience contraction or expansion upon mixing. This effect is represented by the quantity excess volume of the mixture, an example of excess property.
Relation to specific volume[edit]
Molar volume is related to specific volume by the product with molar mass. This follows from above where the specific volume is the reciprocal of the density of a substance:
Ideal gases[edit]
For ideal gases, the molar volume is given by the ideal gas equation; this is a good approximation for many common gases at standard temperature and pressure.
The ideal gas equation can be rearranged to give an expression for the molar volume of an ideal gas:
Hence, for a given temperature and pressure, the molar volume is the same for all ideal gases and is based on the gas constant: R = 8.31446261815324 m3⋅Pa⋅K−1⋅mol−1, or about 8.20573660809596×10−5 m3⋅atm⋅K−1⋅mol−1.
The molar volume of an ideal gas at 100 kPa (1 bar) is
- 0.022710954641485… m3/mol at 0 °C,
- 0.024789570296023… m3/mol at 25 °C.
The molar volume of an ideal gas at 1 atmosphere of pressure is
- 0.022413969545014… m3/mol at 0 °C,
- 0.024465403697038… m3/mol at 25 °C.
Crystalline solids[edit]
For crystalline solids, the molar volume can be measured by X-ray crystallography.
The unit cell volume (Vcell) may be calculated from the unit cell parameters, whose determination is the first step in an X-ray crystallography experiment (the calculation is performed automatically by the structure determination software). This is related to the molar volume by
where NA is the Avogadro constant and Z is the number of formula units in the unit cell. The result is normally reported as the «crystallographic density».
Molar volume of silicon[edit]
Ultra-pure silicon is routinely made for the electronics industry, and the measurement of the molar volume of silicon, both by X-ray crystallography and by the ratio of molar mass to mass density, has attracted much attention since the pioneering work at NIST in 1974.[2] The interest stems from that accurate measurements of the unit cell volume, atomic weight and mass density of a pure crystalline solid provide a direct determination of the Avogadro constant.[3]
The CODATA recommended value for the molar volume of silicon is 1.205883199(60)×10−5 m3⋅mol−1, with a relative standard uncertainty of 4.9×10−8.[4]
See also[edit]
- Specific volume
References[edit]
- ^ a b International Union of Pure and Applied Chemistry (1993). Quantities, Units and Symbols in Physical Chemistry, 2nd edition, Oxford: Blackwell Science. ISBN 0-632-03583-8. p. 41. Electronic version.
- ^ Deslattes, R. D.; Henins, A.; Bowman, H. A.; Schoonover, R. M.; Carroll, C. L.; Barnes, I. L.; Machlan, L. A.; Moore, L. J.; Shields, W. R. (1974). «Determination of the Avogadro Constant». Phys. Rev. Lett. 33 (8): 463–66. Bibcode:1974PhRvL..33..463D. doi:10.1103/PhysRevLett.33.463.
- ^ Mohr, Peter J.; Taylor, Barry N. (1999). «CODATA recommended values of the fundamental physical constants: 1998» (PDF). Journal of Physical and Chemical Reference Data. 28 (6): 1713–1852. Bibcode:1999JPCRD..28.1713M. doi:10.1063/1.556049. Archived from the original (PDF) on 2017-10-01.
- ^ «2018 CODATA Value: molar volume of silicon». The NIST Reference on Constants, Units, and Uncertainty. NIST. 20 May 2019. Retrieved 2019-06-23.
External links[edit]
- Interactive table of molar volumes
Концепция идеального газа. Закон Авогадро и молярный объем газа
Идеальный газ представляет собой удобную физическую модель, с использованием которой можно успешно решать многие практические проблемы реальных газов. В данной статье рассмотрим вопросы, что понимают под молярным объемом газа и как его вычислять.
Идеальный газ и его отличие от реального
Следует сразу сказать, что все газы, которые известны человеку, являются реальными. Тем не менее в большинстве случаев их можно считать идеальными. В последних полагают, что взаимодействия между атомами и молекулами не существует, и их размеры пренебрежимо малы, по сравнению со средними межмолекулярными расстояниями. Эти условия с высокой точностью соблюдаются в следующих случаях:
- давление в газах низкое (порядка 1 атмосферы);
- абсолютная температура высокая (300 К и выше);
- составляющие газ молекулы и атомы являются химически инертными, то есть они не способны образовывать друг с другом никакие типы химических связей.

Примером идеальной смеси газов является воздух, который в основном состоит из инертных молекул N2 и O2. Наоборот, водяной пар практически ни при каких давлениях не может считаться идеальным газом из-за существования между его полярными молекулами водородных связей.
Закон Клапейрона-Менделеева
Этот закон позволяет определить любой термодинамический параметр газовой идеальной системы, если известны два других параметра. Речь идет о таких термодинамических характеристиках, как температура T, объем V и давление P. Закон Клапейрона-Менделеева полезно рассмотреть в рамках данной темы статьи, поскольку с его помощью легко определить молярный объем газа идеального.
Закон Клапейрона-Менделеева записывается в виде следующего уравнения:
P*V = n*R*T.
Часть величин уже была описана выше. Величина n — это количество вещества в молях, буквой R обозначена универсальная постоянная для всех газов (8,314 Дж/(моль*К)).
Принцип Авогадро

Изучая в начале XIX века различные газы, итальянский ученый Амедео Авогадро пришел к важному экспериментальному открытию. Он установил, что объем, который занимают газы при постоянных условиях, оказывается прямо пропорциональным количеству вещества и не зависит от химического состава. Под постоянными условиями имеется в виду одинаковая температура и давление для всех газов в эксперименте.
Если положить T, P = const в уравнении Клапейрона-Менделеева, то мы получим математическую формулировку принципа или закона Авогадро:
n/V = const.
То есть при увеличении числа частиц в газовой системе ее объем растет пропорциональным образом.
В некоторых учебниках по физике формулируют следующим образом закон Авогадро: молярный объем газов при одинаковых температурах и давлениях является величиной постоянной, не зависящей от химической природы газовых частиц.
Из описанного принципа Авогадро можно вывести закон Джона Дальтона о парциальных давлениях газовых смесей, согласно которому парциальное давление компонента прямо пропорционально его атомной доле в газовой смеси.

Вычисление молярного объема газа при нормальных условиях
Речь идет об объеме, который в пространстве занимает 1 моль идеального газа при заданных условиях (температура, давление). Для вычисления этой величины воспользуемся уравнением Клапейрона-Менделеева. Из него получаем формулу для объема газовой системы:
V = n*R*T/P.
Поскольку мы вычисляем молярный объем, то n = 1 моль, тогда:
V = 8,314*T/P.
Подставляя в эту формулу интересующие нас значения температуры и давления, мы может рассчитать молярный объем идеального газа. Например, при нормальных условиях (0 oC и 1 атм.), получаем:
V = 8,314*273,15/101325 = 0,0224 м3.
Переводя в более удобные на практике единицы измерения объема, получаем V = 22,4 литра. Заметим, что в формулу мы подставили давление в паскалях и температуру в кельвинах. Обе единицы используются в качестве основных в системе СИ.
Автор:
19-01-2019 12:26
Жду ваши вопросы и мнения в комментариях
- Идеальный газ:
- — теоретическая модель, широко применяемая для описания свойств и поведения реальных газов при умеренных давлениях и температурах;
- — газ, взаимодействие между молекулами которого пренебрежимо мало;
- — математическая модель газа, в которой предполагается, что потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией.
Общие сведения
В модели идеального газа:
-
- предполагается, что составляющие газ частицы не взаимодействуют друг с другом, то есть их размеры пренебрежимо малы, поэтому в объёме, занятом идеальным газом, нет взаимных столкновений частиц. Частицы идеального газа претерпевают столкновения только со стенками сосуда;
- между частицами газа нет дальнодействующего взаимодействия, например, электростатического или гравитационного;
- упругих столкновений между молекулами и стенками сосуда в рамках молекулярно-кинетической теории приводит к термодинамике идеального газа.
Модель идеального газа имеет широкое применения в ряде задач, например в инженерных расчетах (аэродинамический, гидравлический, теплотехнический и т.д.), связанные с воздухом и другими газами, при давлении и температуре близких к нормальным (стандартным) условиям.
При условиях сильно отличных от нормальных (стандартных) условий модель идеального газа дает результаты с погрешностью так, как модель не учитывает:
-
- притяжение между молекулами;
- конечные размеры молекул.
При высоких давления газа следует использовать различные варианты уравнений реальных газов, разработанных на базе модели идеального газа. Наиболее из известных уравнений реального газа — полуэмпирическое уравнение Ван-дер-Ваальса.
Основные уравнения состояние идеального газа
Уравнения состояния идеального газа служат для получения неизвестных параметров идеального газа или газов схожих по свойствам с моделью идеального газа.
В данном разделе будут рассмотрены варианты уравнение состояния идеального газа на основе уравнения Менделеева — Клапейрона (или уравнение Клапейрона).
P⋅VM=R⋅T или P⋅V=(m/M)⋅R⋅T
Эти уравнение имеет наибольшее практическое значение при инженерных расчетах. Но так же существуют другие варианты записи уравнения состояния идеального газа.
Основными параметрами идеального газа служат:
-
- давление идеального газа (Р), Па;
- температура идеального газа (T), °К;
- объем идеального газа (V), м3;
- молярная масса идеального газа (M), кг/моль;
- количества идеального газа (n), моль;
- масса идеального газа (m), кг;
- молярный объем (VM), м3/моль;
Другие физические величины используемые в уравнении состояния идеального газа:
-
- плотность идеального газа (ρ), кг/м3.
Калькуляторы параметров идеального газа
Калькулятор молярного объема идеального газа
Согласно закону Авогадро, одинаковые количества газов при одинаковых условиях занимают одинаковый объём. Молярный объём идеального газа рассчитается по формуле:
VM=(R⋅T)/P
Введите универсальную газовую постоянную (Run0)
Введите температуру газа (T0)
Введите давление газа (абсолютного) (PA0)
Результат расчета молярного объема газа (Vm0)
Формула расчета молярного объема газа:
Скачать результат расчета молярного объема газа:

Поделится ссылкой на расчет молярного объема:
Если по калькулятору, приведенному выше, посчитать молярный объем газа при нормальных условиях:
-
- давление Р=101325 Па;
- температура Т=273,15 ºК.
В результате получится молярный объем идеального газа при нормальных условиях равный 22,413971 литр/моль (частный случай закона Авогадро).
Молярные объёмы реальных газов и идеального газа для практических вычислений имеют не значительные отклонения и принимаются равными .
Калькулятор давления идеального газа
При решении инженерных задач часто необходимо определять давление газа в технических устройствах, для решения задачи по организации технологии, для выполнения расчета на прочность технических устройств или просто для выполнения гидравлических (аэродинамических расчетов).
Расчет давления газа, если известны:
-
- масса газа;
- объем занимаемый газом (внутри сосуда, трубопровода или другого устройства);
- молярная масса газа;
- температура газа,
выполняется по формуле:
P=(m⋅R⋅T)/(M⋅V)
Введите универсальную газовую постоянную (Run2)
Введите температуру газа (T2)
Введите молярную массу газа (Mg2)
Результат расчета давления газа (абсолютного) (PA2)
Формула расчета давления газа (абсолютного):
Скачать результат расчета давления газа (абсолютного):

Поделится ссылкой на расчет давления:
Калькулятор температуры идеального газа
Температуру газа необходимо обычно рассчитывать для:
-
- возможности принятия технологических решения;
- возможности проведения расчета на прочность технологического оборудования;
- расчета теплоизоляции оборудования и защиты персонала от повышенной или пониженной температуры.
Расчет температуры газа, если известны:
-
- масса газа;
- объем занимаемый газом (внутри сосуда, трубопровода или другого устройства);
- молярная масса газа;
- абсолютное давление газа.
выполняется по формуле:
T=(P⋅M⋅V)/(m⋅R)
Введите давление газа (абсолютное) (PA3)
Введите молярную массу газа (Mg3)
Введите универсальную газовую постоянную (Run3)
Результат расчета температуры газа (T3)
Формула расчета температуры газа:
Скачать результат расчета температуры газа:

Поделится ссылкой на расчет температуры:
Калькулятор объема идеального газа
Расчет объем занимаемый газом (внутри сосуда, трубопровода или другого устройства), если известны:
-
- масса газа;
- давление газа;
- молярная масса газа;
- температура газа,
выполняется по формуле:
V=(m⋅R⋅T)/(M⋅P)
На основе этого уравнения, так же находят объемный расход газа при различных условиях.
Введите универсальную газовую постоянную (Run4)
Введите температуру газа (T4)
Введите молярную массу газа (Mg4)
Введите давление газа (абсолютного) (PA4)
Результат расчета объема газа (V4)
Формула расчета объема газа:
Скачать результат расчета объема газа:

Поделится ссылкой на расчет объема:
Калькулятор массы идеального газа
Масса газа рассчитывают для:
-
- решения технологических задач;
- возможности проведения расчета на прочность технологического оборудования и трубопроводов (сбор нагрузок);
- на опасных производственных объектах с опасными веществами для расчета массы опасных веществ для возможности идентификации производственного объекта, как ОПО.
Расчет массы газа, если известны:
-
- абсолютное давление газа;
- молярная масса газа;
- объем занимаемый газом (внутри сосуда, трубопровода или другого устройства);
- температура газа,
выполняется по формуле:
m=(P⋅M⋅V)/(T⋅R)
Введите давление газа (абсолютное) (PA5)
Введите молярную массу газа (Mg5)
Введите температуру газа (T5)
Введите универсальную газовую постоянную (Run5)
Результат расчета массы газа (m5)
Формула расчета массы газа:
Скачать результат расчета массы газа:

Поделится ссылкой на расчет массы:
Калькулятор плотности идеального газа
Расчет плотности газа, если известны:
-
- абсолютное давление газа;
- молярная масса газа;
- температура газа,
выполняется по формуле:
ρ=(P⋅M)/(T⋅R)
Введите давление газа (абсолютное) (PA6)
Введите молярную массу газа (Mg6)
Введите температуру газа (T6)
Введите универсальную газовую постоянную (Run6)
Результат расчета плотности газа (pl6)
Формула расчета плотности газа:
Скачать результат расчета плотности газа:

Поделится ссылкой на расчет плотности :
Калькулятор параметров идеального газа системы исходя из разных состояний системы
Выполняется по формуле:
P1⋅V1/T1=P2⋅V2/T2=P3⋅V3/T3=…=const
Рассмотрим изменение параметров системы по двумя состояниям:
P1⋅V1/T1=P2⋅V2/T2
Калькулятор давления идеального газа
P1=(P2⋅V2⋅T1)/(T2⋅V1)
Введите давление газа (абсолютное) (Pg2)
Введите температуру газа (Tg1)
Введите температуру газа (Tg2)
Результат расчета давления газа (абсолютного) (Pg1)
Формула расчета давления газа (абсолютного):
Скачать результат расчета давления газа (абсолютного):

Поделится ссылкой на расчет давления:
Калькулятор температуры идеального газа
T3=(P3⋅V3⋅T4)/(P4⋅V4)
Введите давление газа (абсолютное) (Pg3)
Введите температуру газа (Tg4)
Введите температуру газа (абсолютное) (Pg4)
Результат расчета температуры газа (Tg3)
Формула расчета температуры газа:
Скачать результат расчета температуры газа:

Поделится ссылкой на расчет температуры:
Калькулятор объема идеального газа
V5=(P6⋅V6⋅T5)/(P5⋅T6)
Введите давление газа (абсолютное) (Pg6)
Введите температуру газа (Tg5)
Введите давление газа (абсолютное) (Pg5)
Введите температуру газа (Tg6)
Результат расчета объема газа (Vg5)
Формула расчета объема газа:
Скачать результат расчета объема газа:

Поделится ссылкой на расчет объема: