Генетические нарушения у человека и методы их выявления
Генами называются участки ДНК, в которых закодирована структура всех белков в теле человека или любого другого живого организма. В биологии действует правило: «один ген – один белок», то есть в каждом гене содержится информация только об одном определенном белке.
В 1990 году большая группа ученых из разных стран начала проект под названием «Геном человека». Он завершился в 2003 году и помог установить, что человеческий геном содержит 20–25 тысяч генов. Каждый ген представлен двумя копиями, которые кодируют один и тот же белок, но могут немного различаться. Большинство генов одинаковые у всех людей – различается всего 1%.
ДНК находится в клетке внутри ядра. Она особым образом организована в виде хромосом – эти нитеподобные структуры можно рассмотреть в микроскоп с достаточно большим увеличением. Внутри хромосомы ДНК намотана на белки – гистоны. Когда гены неактивны, они расположены очень компактно, а во время считывания генетического материала молекула ДНК расплетается.
В клетках человека есть структуры, которые называются митохондриями. Они выполняют роль «электростанций» и отвечают за дыхание. Это единственные клеточные органеллы, у которых есть собственная ДНК. И в ней тоже могут возникать нарушения.
Весь набор хромосом в клетке называется кариотипом. В норме у человека он представлен 23 парами хромосом, всего их 46. Выделяют два вида хромосом:
- 22 пары аутосом одинаковы у мужчин и женщин. В каждой паре хромосомы имеют одинаковую длину и содержат одинаковые наборы генов.
- Одна пара половых хромосом. У женщин это две X-хромосомы. Одна из них неактивна и плотно свернута – ее называют тельцем Барра. У мужчин одна половая хромосома представлена X-хромосомой, а вторая – Y-хромосомой, она меньше по размерам.
Методы исследования хромосом
Для исследования кариотипа применяют специальный метод – световую микроскопию дифференциально окрашенных метафазных хромосом культивированных лимфоцитов периферической крови.
Этот анализ применяется для диагностики различных хромосомных заболеваний. Он позволяет выявлять такие нарушения, как:
- Грубые изменения в кариотипе – изменение количества хромосом. Например, при синдроме Дауна в клетках ребенка присутствует лишняя хромосома №21.
- Присутствие в организме клеток с разными кариотипами. Это явление называется мозаицизмом.
- Хромосомные аберрации – нарушение структуры хромосом, внутрихромосомные и межхромосомные перестройки. Сюда относятся делеции (утрата участка хромосомы), дупликации (удвоение участка хромосомы), инверсии (поворот участка хромосомы на 180 градусов), транслокации (перенос участка одной хромосомы в другую).
Однако с помощью исследования кариотипа можно выявить не все генетические нарушения. Оно не способно обнаружить такие изменения, как:
- микроделеции и микродупликации, когда утрачивается или дублируется очень маленький участок хромосомы;
- болезни обмена, вызванные нарушением последовательности «букв» генетического кода в отдельных генах;
- митохондриальные заболевания, связанные с нарушениями в генетическом материале митохондрий;
- низкопроцентный мозаицизм, когда клеток с неправильным кариотипом очень мало;
- мутации в отдельных генах, которые не приводят к изменению внешнего вида хромосом;
- эпигенетические расстройства, при которых структура хромосом и генов не меняется, но изменяется их функция.
Для получения дополнительной информации, не видимой в световой микроскоп, используют хромосомный микроматричный анализ (ХМА). С его помощью можно изучить все клинически значимые участки генома и выявить изменения в количестве и структуре хромосом, а именно микрополомки (микроделеции и микродупликации).
Во время хромосомного микроматричного анализа применяют технологию полногеномной амплификации и гибридизации фрагментов опытной ДНК с олигонуклеотидами, нанесенными на микроматрицу. Если объяснять простыми словами, то сначала ДНК, которую необходимо изучить, копируют, чтобы увеличить ее количество, а затем смешивают ее со специальными ДНК-микрочипами, которые помогают выявлять различные нарушения.
Эта методика позволяет в одном исследовании выявлять делеции и дупликации участков ДНК по всему геному. Разрешающая способность стандартного ХМА от 100 000 пар нуклеотидов – «букв» генетического кода (в отдельных регионах от 10 000 п. н.).
С помощью ХМА можно выявлять:
- изменения числа хромосом;
- дупликации и делеции, в том числе микродупликации и микроделеции;
- отсутствие гетерозиготности – утрату одной из двух копий гена. Это явление имеет важное значение в онкологии, при болезнях импринтинга (когда активность гена зависит от того, от какого из родителей он получен), аутосомно-рецессивных заболеваниях (связанных с рецессивными генами – о них мы поговорим ниже), близкородственных браках;
- однородительские дисомии, когда в геноме ребенка присутствуют две хромосомы от одного родителя.
Однако, как и предыдущий метод, хромосомный микроматричный анализ имеет некоторые ограничения. Он не позволяет выявлять или ограничен в выявлении таких аномалий, как:
- сбалансированные хромосомные аномалии, когда в хромосомах происходят изменения, которые не приводят к добавлению или утрате генетического материала. К ним относятся инверсии (разворот участка хромосомы на 180 градусов), реципрокные транслокации (обмен участками между хромосомами), небольшие инсерции (вставки в хромосомах);
- мозаицизм, если клеток с нарушениями в кариотипе менее 15%;
- CNV (copy number variation) – повторы небольших участков генома;
- точечные мутации – замены отдельных «букв» генетического кода;
- экспансия (увеличение) повторов коротких участков в ДНК;
- аномалии метилирования – присоединения особых метильных групп к определенным участкам ДНК, которые меняют активность генов.
Мутации в генах и заболевания, к которым они способны приводить
Мутации – это изменения, которые происходят в ДНК как случайным образом, так и под действием разных факторов, например химических веществ, ионизирующих излучений. Они могут затрагивать как отдельные «буквы» генетического кода, так и большие участки генома. Мутации происходят постоянно, и это основной двигатель эволюции. Чаще всего они бывают нейтральными, то есть ни на что не влияют, не приносят ни вреда, ни пользы. В редких случаях встречаются полезные мутации – они дают организму некоторые преимущества. Также встречаются вредные мутации – из-за них нарушается работа важных белков, наоборот, происходят достаточно часто. Генетические изменения, которые происходят более чем у 1% людей, называются полиморфизмами – это нормальная, естественная изменчивость ДНК Полиморфизмы ответственны за множество нормальных отличий между людьми, таких как цвет глаз, волос и группа крови.
Все внешние признаки и особенности работы организма, которые человек получает от родителей, передаются с помощью генов. Это важнейшее свойство всех живых организмов называется наследственностью. В зависимости от того, как проявляются гены в тех или иных признаках, их делят на две большие группы.
- Доминантные гены. Выражаясь простым языком, эти гены более «сильные». Если в клетках присутствует хотя бы одна копия такого гена, его признаки проявятся.
- Рецессивные гены «слабее» доминантных. Если у человека одна копия гена доминантная и одна рецессивная, – проявится признак доминантной. А для проявления рецессивного признака нужно две соответствующих копий.
Например, карий цвет глаз у человека является доминантным. Поэтому у кареглазых родителей с высокой вероятностью родится кареглазый ребенок. Если у одного из родителей глаза карие, а у другого голубые, то вероятность рождения кареглазых детей в такой семье тоже высока. У двух голубоглазых родителей, скорее всего, все дети тоже будут голубоглазыми. А вот у кареглазых родителей может родиться ребенок с голубыми глазами, если у обоих есть рецессивные «гены голубоглазости», и они достанутся ребенку. Конечно, это упрощенная схема, потому что за цвет глаз отвечает не один, а несколько генов, но на практике эти законы наследования зачастую работают. Аналогичным образом потомству могут передаваться и наследственные заболевания.
Как выявляют рецессивные мутации?
Для выявления мутаций, которые передаются рецессивно, используют целый ряд исследований.
Секвенирование по Сэнгеру – метод секвенирования (определения последовательности нуклеотидов, буквально – «прочтение» генетического кода) ДНК, также известен как метод обрыва цепи. Анализ используется для подтверждения выявленных мутаций. Это лучший метод для идентификации коротких тандемных повторов и секвенирования отдельных генов. Метод может обрабатывать только относительно короткие последовательности ДНК (до 300–1000 пар оснований) одновременно. Однако самым большим недостатком этого метода является большое количество времени, которое требуется для его проведения.
Если неизвестно, какую нужно выявить мутацию, то используют специальные панели.
Панель исследования — тестирование на наличие определенных мутаций, входящих в перечень конкретной панели исследования. Анализ позволяет выявить одномоментно разные мутации, которые могут приводить к генетическим заболеваниям. Анализ позволяет компоновать мутации в панели по частоте встречаемости (скрининговые панели, направленные на выявление носительства патологической мутации, часто встречаемой в данном регионе или в определенной замкнутой популяции) и по поражаемому органу или системе органов (панель «Патология соединительной ткани»). Но и у этого анализа есть ограничения. Анализ не позволяет выявить хромосомные аберрации, мозаицизм и мутации, не включенные в панель, митохондриальные заболевания, а также эпигенетические нарушения.
Не в каждой семье можно отследить все возможные рецессивные заболевания. Тогда на помощь приходит секвенирование экзома – тест для определения генетических повреждений (мутаций) в ДНК путем исследования в одном тесте практически всех областей генома, кодирующих белки, изменения которых являются причиной наследственных болезней.
Секвенирование следующего поколения-NGS – определение последовательности нуклеотидов в геномной ДНК или в совокупности информационных РНК (транскриптоме) путем амплификации (копирования) множества коротких участков генов. Это разнообразие генных фрагментов в итоге покрывает всю совокупность целевых генов или, при необходимости, весь геном.
Анализ позволяет выявить точечные мутации, вставки, делеции, инверсии и перестановки в экзоме. Анализ не позволяет выявить большие перестройки; мутации с изменением числа копий (CNV); мутации, вовлеченные в трехаллельное наследование; мутации митохондриального генома; эпигенетические эффекты; большие тринуклеотидные повторы; рецессивные мутации, связанные с Х-хромосомой, у женщин при заболеваниях, связанных с неравномерной Х-деактивацией, фенокопии и однородительские дисомии, и гены, имеющие близкие по структуре псевдогены, могут не распознаваться.
Что делать, если в семье есть наследственное заболевание?
Существуют два способа выявить наследственные генетические мутации у эмбриона:
Предимплантационное генетическое тестирование (ПГТ) в цикле ЭКО. Это диагностика генетических заболеваний у эмбриона человека перед имплантацией в слизистую оболочку матки, то есть до начала беременности. Обычно для анализа проводится биопсия одного бластомера (клетки зародыша) у эмбриона на стадии дробления (4–10 бластомеров). Существует несколько видов ПГТ: на хромосомные отклонения, на моногенные заболевания и на структурные хромосомные перестройки. Данные Simon с соавторами (2018) говорят о том, что в случае проведения ЭКО с ПГТ у пациентки 38–40 лет результативность ЭКО составляет 60%. Но при исследовании эмбриона есть ряд ограничений. Так, из-за ограниченного числа клеток можно не определить мозаицизм.
Если нет возможности провести ЭКО с ПГТ, то используют второй вариант – исследование плодного материала во время беременности.
Для забора плодного материала используют инвазивные методы:
- биопсия хориона – когда берут клетки из плаценты;
- амниоцентез – когда берут клетки амниотической жидкости.
Далее эти клетки исследуют при помощи одного или нескольких генетических тестов (которые имеют свои ограничения). Проведение инвазивных методов может быть связано с риском для беременности порядка 1%.
Таким образом, проведя дополнительные исследования, можно значительно снизить риск рождения ребенка с генетическим заболеванием в конкретной семье. Но привести этот риск к нулю на сегодняшний день, к сожалению, невозможно, так как любой генетический тест имеет ряд ограничений, что делает невозможным исключить абсолютно все генетические болезни.
Автор статьи
Пелина Ангелина Георгиевна
Врач-генетик
Ведёт генетическое обследование доноров Репробанка, осуществляет подбор доноров для пар, имеющих ранее рождённых детей с установленной генетической патологией.
+7 (499) 653-66-09
info@reprobank.ru
Записаться на консультацию
Так что же такое гены? И как выявить мутацию?
Ребенок болен. Врач-генетик что-то объясняет про гены и мутации. Дома, уложив спать своего малыша, мама и папа сидят, склонив головы над монитором. Так что же такое гены? И как выявить мутацию?
А что такое мутация?
Мутация (лат. mutatio — изменение) — стойкое (то есть такое, которое может быть унаследовано потомками данной клетки или организма) преобразование генотипа, происходящее под влиянием внешней или внутренней среды. Это определение было дано Хуго де Фризом.
Мутации бывают геномные (в результате которых образуются клетки с двойным или более набором хромосом),
хромосомные (при которых происходит изменение числа или структуры хромосом) и генные.
В результате генных мутаций происходят замены, делеции или вставки одного или нескольких нуклеотидов, транслокации, дупликации в гене, кодирующем синтез определенного белка в клетке. В том случае, когда под действием мутации изменяется лишь один нуклеотид, говорят о точковых мутациях
Как выявить мутации в генах, отвечающих за развитие того или иного заболевания?
Сначала у пациента берется биологический материал (кровь, моча, биоптат мышц и др), из них с помощью специальных методик выделяется ДНК.
Затем путем специфический методов полученный нами образец ДНК подготавливается к секвенированию гена.
Что такое секвенирование гена? Это название методов, которые позволяют выявить последовательность нуклеотидов в ДНК (рис 2).

В Научном Центре здоровья детей в 2011 году создана лаборатория Молекулярно-генетической диагностики, которая успешно осуществляет молекулярно-генетическую диагностику и энзимодиагностику редких наследственных заболеваний.
При необходимости вы всегда можете обратиться в эту лабораторию по вопросам молекулярно-генетической диагностики наследственных заболеваний.
Заведующий лабораторией молекулярно-генетической диагностики НЦЗД РАМН Савостьянов Кирилл Викторович.
Телефон лаборатории: +7 (499) 134-09-19
При заболеваниях с аллельной гетерогенностью найти мутацию, вызывающую заболевание, непросто. При этих расстройствах необходимо сканировать гены на наличие мутаций, прежде чем можно будет идентифицировать конкретную мутацию, вызывающую заболевание. После обнаружения и характеристики нового варианта последовательности необходимо установить его патогенность. Это обычно достигается путем скрининга большого количества нормальных контрольных особей, которые, как ожидается, не будут нести один и тот же аллельный вариант. Кроме того, следует сравнить последовательность ДНК больных и здоровых людей в одной семье.
В настоящее время доступно множество методов скрининга мутаций, но наиболее широко применяются методы, описанные ниже. Однако даже самые распространенные методы скрининга имеют ограниченное применение в клинико-диагностических лабораториях, поскольку поиск отдельных болезнетворных мутаций – трудоемкий и дорогостоящий процесс.
Гетеродуплексный анализ
Гетеродуплексный анализ используется для обнаружения точечных мутаций на одной нити спирали ДНК. Методика использует денатурацию и повторный отжиг двухцепочечной ДНК-мишени. Если комплементарные одиночные нити повторно отжигаются, они образуют идеально выровненный гомодуплекс. С другой стороны, отдельные цепи, не являющиеся полностью комплементарными из-за наличия точечной мутации в одной цепи, образуют гетеродуплекс. Отсутствие отжига во всех положениях основания приводит к образованию «пузыря» во вновь образованной двойной нити. По сравнению с обычной ДНК, ДНК с пузырьком мигрирует медленнее во время электрофореза.
Этот метод относительно прост в исполнении и требует небольшой оптимизации. Некоторые из доступных гелевых матриц менее токсичны, чем полиакриламидные гели. Недостатком считается то, что этот метод сканирования не позволяет определить местонахождение мутации в анализируемом фрагменте.
Анализ конформации одноцепочечной ДНК
Анализ конформации одноцепочечной ДНК (SSCA) основан на наблюдении, что одноцепочечные фрагменты ДНК принимают уникальные конформации, зависящие от состава их последовательностей, при прогоне в неденатурирующем полиакриламидном геле. Таким образом, миграция через гель зависит от длины цепи, а также от конформации нити. Прежде чем можно будет сделать интерпретацию, необходимо знать специфический характер миграции в контрольных образцах дикого типа. Это может быть достигнуто путем добавления обычных элементов управления в прогоне.
После оптимизации этот метод пригоден для скрининга довольно большого количества образцов за один раз. Однако этот метод сканирования не определяет локализацию мутации в анализируемом фрагменте. Анализ конформации одноцепочечной ДНК также требует оптимизации, и воспроизводимость условий во всех анализах одной и той же последовательности ДНК имеет решающее значение.
Автоматическое секвенирование
Наиболее прямой подход к обнаружению мутаций – автоматическое секвенирование. Представляющая интерес последовательность ДНК амплифицируется в присутствии праймера и терминаторов дидеоксинуклеотидной цепи. Либо праймер, либо терминаторы цепи имеют флуоресцентную маркировку. Когда последовательность подвергается электрофорезу в автоматическом секвенаторе, лазерный луч возбуждает флуоресцентные нуклеотиды, производя сигнал, который может быть скомпилирован в последовательность ДНК.
Преимущества этого метода включают точную идентификацию всех вариаций ДНК в последовательности-мишени. Метод может быть применен как для обнаружения известных и неизвестных мутаций. Для большого числа наследственных состояний продолжают обнаруживаться новые мутации, дополняющие понимание спектров мутаций и корреляций генотип-фенотип. Клиническое тестирование улучшается благодаря более комплексному, инклюзивному подходу к диагностике.
Недостатки метода включают финансовые затраты, время и возможность получения данных низкого качества из-за некачественного исходного материала.
Саузерн и нозерн-блоттинг
Саузерн-блоттинг можно использовать для выявления небольших мутаций, а также крупных делеций, дупликаций и перестроек генов, изменяющих сайты расщепления ферментом рестрикции или размеры полученных фрагментов ДНК. В этом методе геномная ДНК расщепляется одной или несколькими эндонуклеазами рестрикции и переносится на мембрану. Эта мембрана гибридизуется с одноцепочечным радиоактивно меченым зондом в условиях, способствующих образованию двухцепочечных соединений между зондом и фрагментами геля, содержащими комплементарную последовательность. Когда авторадиографическая пленка подвергается воздействию мембраны и проявляется, гибридизированные последовательности становятся видимыми в виде полос. Расположение каждой из этих полос соответствует размеру фрагмента, с которым связан зонд.
Аналогичный метод может быть применен, когда РНК – основной материал. С помощью этого метода, получившего название “Нозерн-блоттинг”, можно анализировать размер, количество и характер экспрессии транскриптов генов в разных тканях.
Преимущества этих методов заключаются в возможности обнаружения широкого спектра мутаций и крупных структурных перестроек. Саузерн-блоттинг также может быть использован для выявления изменений в статусе метилирования генов (влияющих на чувствительность к расщеплению рестрикционных нуклеотидов).
Недостатки включают в себя требование большего количества ДНК, чем другие методы, упомянутые здесь, а также требования к трудозатратам и времени. Как правило, выполнение этого анализа может занять неделю. Использование радиоактивных материалов может быть дорогостоящим и опасным. Однако возможно применение нерадиоактивных методов, таких как хемилюминесценция.
Продолжение статьи
- Современные методы диагностики: молекулярная генетика и цитогенетика. Обнаружение известных мутаций.
- Обнаружение цитогенетических аномалий.
- Генотипирование новых мутаций.
Данная брошюра содержит информацию о том, каким образом проводится исследование образцов в генетической лаборатории. Особенно важными для обсуждения являются следующие вопросы:
- какие лабораторные методики используются для проведения генетических исследований;
- почему одни анализы можно сделать быстро, а другие – нет;
- почему в некоторых случаях лаборатория не может дать определенный ответ.
Более подробная информация о том, почему Вам может понадобиться генетическое исследование, содержится в брошюре «Что такое генетическое исследование?»
Что такое генетическое исследование?
Большинство генетических исследований представляет собой изучение ДНК – химического соединения, которое содержится в наших клетках и содержит «инструкции» для роста, развития и функционирования организма. ДНК можно представить в виде нити кодированной информации, разделенной на отдельные «инструкции», называемые генами. У человека известно более 20,000 различных генов, которые входят в состав хромосом. Мы наследуем хромосомы от наших родителей – 23 от мамы и 23 от папы, всего – 23 пары (или два набора по 23 хромосомы). Если представить генетический набор человека как «книгу жизни», то основания (мономеры) ДНК можно сравнить с буквами, гены – со словами, а хромосомы – с главами.
Рисунок 1: Гены, хромосомы и ДНК
Изменения в генах или хромосомах называются мутациями. Продолжая аналогию с книгой, мутации можно представить в виде неправильно написанных букв или замены слов в предложении. Мутации встречаются очень часто, и у каждого человека есть некоторое количество мутаций. Мутации приводят к заболеваниям, если они нарушают передачу необходимых «инструкций» для нормального функционирования данного гена в организме. Следовательно, целью генетического исследования является поиск мутаций на уровне гена или хромосомы. Как правило, для генетического исследования используются образцы крови. Иногда используются образцы других тканей (например, слюны), однако образцы крови предпочтительнее, так как они позволяют получить достаточное количество качественной ДНК, необходимой для проведения исследования. Образец крови или ткани пациента отправляется в лабораторию для анализа генов или хромосом.
Как правило, медико-генетические центры или клиники имеют свои генетические лаборатории. Однако генетических заболеваний и соответствующих анализов очень много, и выполнить все возможные исследования в одной лаборатории очень трудно. Кроме того, среди генетических заболеваний много очень редких состояний, диагностика которых может осуществляться всего в одной-двух лабораториях во всем мире. Если такую лабораторию найти не удалось, или связь с ней затруднительна, может быть разработан поиск мутаций именно в интересующем Вас гене.
Также важно помнить, что, как правило, результаты генетического исследования содержат информацию только о том заболевании, для которого проводился данный анализ. Пока не существует какого-либо «универсального» генетического теста, который мог бы выявить все возможные генетические заболевания. Целью медицинского генетического исследования является предоставление информации о здоровье данного человека или членов его семьив отношении определенного заболевания. Как правило, в задачи исследования не входит дополнительная генетическая информация (например, установление отцовства), которая иногда может быть выявлена в ходе исследования.
Генетические лаборатории
Существует два основных вида генетических лабораторий. В одном случае исследуются гены, в другом – хромосомы.
1) Цитогенетическое исследование
Если доктор подозревает у пациента генетическое заболевание, связанное с изменениями одной из хромосом, то он назначит исследование в цитогенетической лаборатории. Исследуемым материалом может быть кровь, кожа, амниотическая жидкость или ворсины хориона. Вначале клетки биологического материала необходимо нарастить, затем их помещают на специальные стекла и анализируют с помощью микроскопа. При этом хромосомы окрашивают специальным красителем, чтобы их было лучше видно.
Рисунок 2: Как выглядят хромосомы под микроскопом
В первую очередь цитогенетик определяет число хромосом в клетках. Некоторые заболевания связаны с наличием дополнительных хромосом или, наоборот, отсутствием определенных хромосом. Примером такого заболевания является синдром Дауна, при котором у пациентов присутствует дополнительная хромосома 21. Цитогенетик также оценивает структуру хромосом. Изменения структуры хромосом могут быть связаны с разрывом, изменением формы или размера хромосомы. Это может происходить вследствие утраты части хромосомы или появления в ней дополнительных фрагментов. Иногда эти изменения очень небольшие по размерам, и их трудно выявить. В таких случаях используется специальная методика – флуоресцентная гибридизация in situ (FISH). Она позволяет выявлять изменения, которые слишком малы по размерам для обычного микроскопического исследования, а также используется для проверки и подтверждения данных микроскопического анализа при небольших размерах изменений хромосом.
Рисунок 3: Хромосомы, расположенные в порядке нумерации: кариотип
Цитогенетическое исследование может быть относительно длительным. Необходимое наращивание клеток занимает не менее недели, затем еще около недели может понадобиться для подготовки образцов и микроскопического анализа.
2) Молекулярно-генетическое исследование
Если доктор подозревает у пациента генетическое заболевание, связанное с изменением (мутацией) в гене, то он назначит исследование в молекулярно-генетической лаборатории для анализа ДНК определенного гена. Последовательность ДНК, в которой зашифрованы «инструкции» для организма, состоит из четырех «букв», обозначающих азотистые основания в составе ДНК: А (аденин), Ц (цитозин), Г (гуанин) и Т (тимин). При молекулярно-генетическом исследовании определяется точная последовательность «букв» в анализируемом гене, что позволяет выявить какие-либо отклонения от нормальной последовательности (назовем их «ошибки написания»). Один ген может кодироваться 10000 и более «буквами», и специалисты лаборатории обладают необходимыми знаниями и владеют методиками, позволяющими расшифровать и проанализировать всю протяженность гена. Выявленные изменения (мутации) гена могут являться причиной заболевания.
Молекулярные генетики выделяют ДНК из клеток и с помощью специальных химических реакций и приборов расшифровывают анализируемый ген. Для выявления мутаций используется много разных методов. Одним из наиболее часто используемых и универсальных является секвенирование.
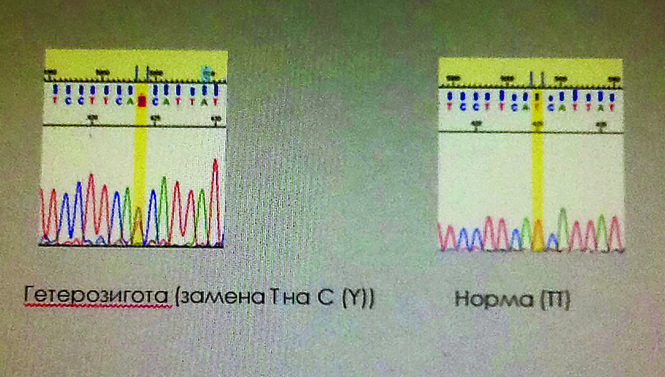
Рисунок 4: секвенирование ДНК: обратите внимание на разницу!
Нормальная последовательность ДНК Последовательность ДНК пациента
На рисунке показан фрагмент последовательности гена. Каждая «буква» кода ДНК обозначена своим цветом. На одном изображении представлена нормальная последовательность ДНК данного фрагмента, а на другом – последовательность ДНК пациента. В нормальной последовательности каждой «букве» соответствует один пик, в то время как у пациента в месте, обозначенном стрелкой, присутствуют два пика в одном и том же положении – Г (черный цвет) и Ц (синий цвет). Это означает, что в данном месте на одной из хромосом соответствующей пары присутствует мутация.
Откуда в лаборатории знают, является ли эта мутация причиной заболевания?
Это очень важный вопрос. Мутации могут иметь разную степень значимости, и ответ на вопрос о последствиях выявленных изменений требует специальных знаний о заболевании и его связи с данным геном или хромосомой, а также очень внимательного анализа всех клинических и генетических данных.
Так как направление поиска лабораторного генетического исследования определяется направляющим диагнозом, то крайне важны данные клинического обследования, проведенные врачом-генетиком (или врачом другого профиля, направившим пациента на генетический анализ). Врач должен осмотреть пациента, его родственников, собрать семейный анамнез, а также учесть результаты других обследований, проведенных ранее. На основании этой информации врач решает, какое лабораторное генетическое исследование необходимо провести в данном случае — цитогенетическое или молекулярно-генетическое, и какую хромосому или какой ген необходимо исследовать. Например, если врач на основании симптомов заболевания и семейного анамнеза предполагает, что у пациента – муковисцидоз, то у пациента возьмут кровь и отправят образец в лабораторию. В сопроводительных документах будет указана соответствующая информация о заболевании и предположительный диагноз, а также ген, который необходимо проанализировать. Если в данном гене у пациента выявляется мутация, которая уже была ранее описана у других больных как причина муковисцидоза, то диагноз считается подтвержденным.
В некоторых случаях у ребенка присутствует заболевание, однако ни у одного из родителей мутаций не обнаружено. В этих случаях вероятнее всего мутация произошла при оплодотворении, и такую мутацию называют «новой», или «вновь возникшей» (от латинского «de novo»).
В некоторых случаях лабораторное исследование не может дать однозначный ответ – является ли найденная мутация причиной заболевания или нет. Такие изменения ДНК относят к «неклассифицированным вариантам». Подобное заключение может разочаровать и врача, и пациента. Однако очень важно отметить, что если бы в сомнительном случае заключение было в пользу мутации как причины заболевания (а на самом деле эта мутация не имела бы отношения к развитию болезни), это привело бы к постановке неправильного диагноза со всеми вытекающими последствиями.
Всегда ли лабораторное исследование выявляет мутации?
В некоторых случаях при проведении поиска причины заболевания мутации не выявляются.
Существует несколько причин для подобной ситуации:
- Иногда при генетическом исследовании проводится поиск только некоторых, наиболее частых, мутаций, известных для данного заболевания. Поэтому редкая мутация, не входящая в число анализируемых в данной лаборатории, может быть не выявлена.
- На сегодняшний день ученым известны далеко не все гены, мутации в которых приводят к тому или иному генетическому заболеванию.
- У пациента может быть не то генетическое заболевание, которое предполагает врач, и, соответственно, поиск ведется не в тех генах или хромосомах, которые ответственны за развитие заболевания.
Важно отметить, что методы генетических исследований постоянно совершенствуются, и наши знания о причинах наследственных заболеваний очень быстро расширяются. Поэтому, если мутация не была выявлена в настоящее время, возможно, в ближайшем будущем это будет возможно.
Почему некоторые генетические анализы проводятся быстро, а другие – медленно?
Если в семье есть другие ранее обследованные больные, в лаборатории знают, какую именно мутацию необходимо искать, и это намного ускоряет сроки выполнения анализа. Анализ проводится быстрее также в ситуации, когда поиск сужен до определенного участка гена. В этих случаях анализ занимает в среднем 1-2 недели.
Однако если в семье раньше не было выявлено мутаций, или известно несколько генов, связанных с заболеванием, то для выполнения анализа может понадобиться больше работы и времени. В этом случае поиск не ограничен определенным участком гена, и может понадобиться анализ полной последовательности одного или нескольких генов. Это длительный процесс, который может занять до двух месяцев. На продолжительность анализа влияют такие факторы как размер гена и спектр мутаций в нем.
Например, в случае мышечной дистрофии Дюшенна, заболевание обусловлено мутациями в гене дистрофина, одном из самых длинных из известных генов. Известны тысячи различных мутаций в данном гене, и поэтому поиск одной из них в конкретной семье может быть длительным и сложным. С другой стороны, при болезни Гентингтона мутации всегда возникают в одном и том же небольшом участке гена гентингтина, и для специалистов в лаборатории проведение такого анализа намного быстрее и проще.
Еще одним важным фактором является качество ДНК. Иногда при проведении анализа необходимо исследование ДНК умерших родственников, и если качество такой ДНК плохое, то время, необходимое для окончательного результата, может увеличиваться в два-три раза. В некоторых случаях проведение или завершение анализа невозможно из-за недостаточного количества ДНК.
Могут ли результаты быть ошибочными?
Так как результаты генетических исследований имеют крайне важные последствия для пациента и его родственников, они должны быть очень тщательно продуманы и правильно сформулированы. Для достоверности полученных данных в ходе исследования на разных этапах предусмотрены «контроли качества». Если обнаруживается мутация, для подтверждения результата ее обязательно проверяют повторно (в процессе исследования есть много автоматических этапов, однако специалист все равно должен все проверить лично). Нередко специалисты проводят дополнительное независимое исследование, чтобы проверить первоначальные результаты. Существуют специальные методы контроля для исключения возможности перепутывания образцов. Кроме этого, существует система внешнего контроля и обмен данными между лабораториями для выработки оптимальных схем и методик лабораторной диагностики генетических заболеваний.
Что произойдет с моим образцом крови (ткани) после выполнения анализа?
Как правило, в лаборатории хранится не кровь, а ДНК и препараты хромосом, если пациент не выразил желание, чтобы их уничтожили после проведения анализа. Лаборатория может выдать образцы ДНК или уничтожить их в любое время по просьбе пациента. ДНК может храниться в лаборатории в течение десятилетий.
Если появляются новые диагностические возможности, лаборатории могут проводить исследования на сохраненных образцах (например, если предыдущий анализ был безрезультатным) при наличии согласия пациента. В этом случае и врачи, и пациенты будут уверены, что на данном этапе сделано все возможное для диагностики данного заболевания. Лаборатории могут использовать анонимные образцы ДНК для разработки новых методов, или использовать их в программах обмена образцами между лабораториями при внешнем контроле качества работы лаборатории и выработки оптимальных схем диагностики. Если пациент не хочет, чтобы его образцы ДНК использовались в этих целях, он должен сообщить об этом.
Некоторых людей беспокоит вероятность доступа к их образцам ДНК лиц из правоохранительных органов. Такая ситуация может возникнуть крайне редко. Однако если в генетическую лабораторию поступает соответствующий запрос о выдаче образцов ДНК (или любого другого медицинского документа или биологического образца), то это возможно только в случае судебного распоряжения.
Гены — это участки молекулы дезоксирибонуклеиновой кислоты (ДНК), составляющей основу хромосом. Собственно ДНК состоит из простых «кирпичиков» — нуклеотидов. Гены у разных людей почти одинаковы, но имеются небольшие нюансы, которые и отличают людей друг от друга. Обычно, причиной различий в генах выступают точечные мутации — замены одних нуклеотидов в молекуле ДНК на другие. Такие замены приводят к изменению свойств гена: редко в лучшую стороны и, как правило, в худшую. Некоторые из мутаций неизбежно становятся причиной генных болезней, которые клинически часто проявляются уже с рождения: муковисцидоз, мышечная дистрофия, фенилкетонурия и др. Это так называемые моногенные болезни. Они всегда связаны с мутацией в одном гене.
Однако в других случаях такие замены одного нуклеотида на другой не приводят к болезням, и встречаются в геномах людей значительно чаще в отличие от мутаций. Их называют генными полиморфизмами (частота встречаемости полиморфизмов в популяции – более 1%). Для ряда таких замен показана связь с предрасположенностью к определённым заболеваниям: злокачественные опухоли, сердечно-сосудистые болезни, аллергические и др. заболевания. Эти предрасположенности в отличие от моногенных болезней носят вероятностный характер и не обязательно приведут к развитию патологии. Сейчас, уже известно, что таких замены в структуре генов, обозначенные выше, как генные полиморфизмы, можно рассматривать в качестве предикторов (от английского predict – предсказывать) болезней только с учётом факторов внешней среды. Другими словами, для развития болезни недостаточно только наличия генных полиморфизмов (изменённых генов), а абсолютно необходимо влияние разнообразных и определённых внешних условий. Такими условиями являются: нарушения питания, поступление в организм токсинов и онкогенов (табачный дым), потребление алкоголя, нехватка витаминов и др. Соответственно, вероятность возникновения таких болезней определяется, как присутствием полиморфных генов, так и обязательным наличием «пусковых» факторов внешней среды. Именно факторы внешней среды определяют степень вероятности развития болезни. Такие болезни принято относить к формам патологии с мультифакторной этиологией.
Задача генетического тестирования – своевременно выявлять мутации и полиморфизмы. Выявление мутаций, связанных с моногенными болезнями, используют в целях диагностики этих заболеваний при наличии соответствующих клинических признаков. Кроме того, эти тесты можно применять для оценки риска этих заболеваний у потомства в случае отягощённой наследственности родителей или большой частоты заболевания в популяции.
Исследование генных полиморфизмов проводят с целью выявления наследственных факторов предрасположенности к мультифакторным заболеваниям и своевременного устранения вредоносных факторов внешней среды. Таким образом, своевременное выявление генных полиморфизмов — основа предиктивной (предсказательной) медицины. Эти знания позволяют врачу дать индивидуальные рекомендации пациенту для предотвращения у него развития одного из мультифакторных заболеваний.
Как проводится генетическое тестирование и какую информацию получает пациент? Материалом для проведения молекулярно-генетического тестирования служит цельная кровь (5 мл), взятая в пробирку с ЭДТА. Кроме того, необходимо заполнить анкету, которая будет необходима для интерпретации полученных результатов. В лаборатории из крови выделяют ДНК, которую используют для обнаружения мутаций, приводящих к развитию моногенных заболеваний и выявления генных полиморфизмов. Так как клетки человека содержат двойной набор всех генов, результат заключения содержит информацию о наличии исследуемой мутации в каждом из парных генов. Таким образом, по каждой точке возможно получения трёх вариантов заключения: -/- мутация отсутствует (нормальный вариант полиморфизма); -/+ мутация в гетерозиготной форме (в одном из парных генов); +/+ мутация в гомозиготной форме (в обоих парных генах). Если данная мутация наследуется по аутосомно-доминантному типу, то она проявляется как в гомозиготном, так и в гетерозиготном виде; мутации, наследуемые по аутосомно-рецессивному типу, проявляются только в гомозиготной форме.
Врач-генетик анализирует полученную информацию о наличии тех или иных мутаций/ полиморфизмов и составляет генетическое заключение. При этом используют данные анкеты, а также обширный научный и клинический материал, в том числе содержащийся в специализированных медицинских базах данных (OMIM, Medline). Врач-генетик оценивает величину риска заболеваний, ассоциированных с теми или иными мутациями/полиморфизмами, и разрабатывает рекомендации для пациента и лечащего врача, содержащие программу профилактических, лечебно-диагностических мероприятий, направленных на минимизацию выявленных рисков.
Выполнение лабораторного исследования и составление заключения занимает 2-3 недели. Генетическое тестирование по заданному перечню мутаций/полиморфизмов проводится всего один раз в жизни пациента. Результат исследования со временем не меняется. Генетическое заключение рекомендуется иметь при себе при любом обращении за медицинской помощью.
Как следует трактовать результаты генетического тестирования? Если выявлены мутации, связанные с моногенными болезнями, таких пациентов направляют на консультацию к врачу-генетику.
Если не выявлено неблагоприятных мутаций или вариантов полиморфизмов, то это не означает, что пациент может не обращать никакого внимания на свое здоровье. Скажем так: обладателю протективных (защищающих) вариантов генов легче сохранить здоровье, но если человек будет подвергать свой организм постоянным экстремальным нагрузкам, то даже самые лучшие ферментативные системы, кодируемые самыми лучшими генами, могут не справиться с постоянными испытаниями и могут дать сбой. Но в то же время, если человек будет разумно относиться к преимуществам, которые обеспечивают «хорошие» гены, он, несомненно, будет располагать большим потенциалом для самореализации, будет иметь больше возможностей для достижения поставленных целей.
Если обнаружены варианты полиморфизмов, связанные с мультифакторными болезнями, — это не является неизбежностью развития заболевания. Как правило, речь идет только об увеличении риска тех или иных болезней относительно среднего популяционного уровня. Если будут предприняты, соответствующие меры, направленные на снижение воздействия внешних неблагоприятных факторов, то величина этого риска будет минимальной. Важным является то, что человек должен знать не только о рисках для своего здоровья, но и о способах снижения этого риска.











