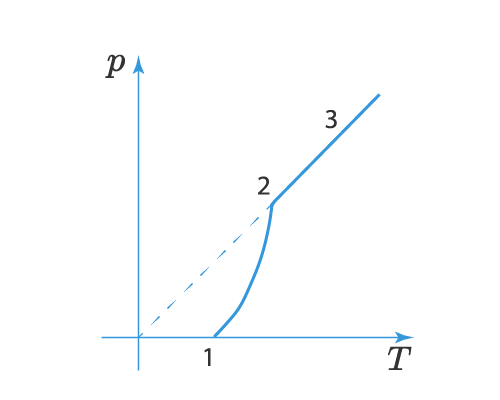Насыщенный пар используется во многих областях промышленности, поэтому для работы различных устройств важно поддерживать состояние насыщения пара.
Рассмотрим, как определить насыщенный пар или нет. Также в статье даны способы определения насыщенности пара, формула и примеры расчета.
Содержание
- Данные для определения насыщенности
- Методы
- Как найти?
- Как рассчитать?
- Несколько примеров
- Где эти расчеты могут пригодиться на практике?
- Заключение
Данные для определения насыщенности
Насыщенный пар или нет, можно определить, зная условия его возникновения и зависимость от различных факторов:
- Этот тип пара образуется только в закрытых сосудах.
- Образуется только над поверхностью исходной жидкости или льдом.
- Имеет свойство конденсации.
- Насыщен влагой.
- Температура пара всегда равна температуре его жидкости.
- Плотность и давления такого пара не зависят от объема.
- Насыщенный пар имеет прямую зависимость от температуры и давления.
Насыщенный пар находится в термодинамическом равновесии с жидкостью из которой он образован. На это указывает равенство массы испарения и последующей конденсации.
Методы
Математический способ определения насыщенного пара используется при вычислении на основе имеющихся данных о его давлении, температуре, влажности и по иным параметрам.
Также есть метод определения на основе отдельных данных:
- Замер температуры пара. Указывает на состояние насыщенного пара при условии равенства температур газа и жидкости. Любое отклонение от равенства укажет на потерю динамического равновесия и уровня влажности.
- По давлению. Измеряется давление пара и сравнивается с табличной величиной при актуальной температуре.
- По степени конденсации. Рассчитывается температура конденсата и скорость его образования.
- По уровню влажности. Влажность насыщенного пара всегда равна 100%.
Также существует метод определения по точке кипения. Он основан на расчете скорости парообразования при актуальном давлении. Например, при давлении 101 кПа, точкой парообразования является температура 100 градусов.
Существуют также некоторые лабораторные методы определения:
- статический,
- динамический,
- кинетический.
Они также основаны на замерах температуры, давления, плотности, влажности и конденсации при определенных условиях и сравнении полученных данных с таблицей насыщенного пара по температуре и давлению.
Как найти?
Свойства насыщенного пара не позволяют приравнивать его к идеальному газу, поэтому для его расчета используется формула Менделеева-Клапейрона.
Как рассчитать?
Расчет выполнятся по формуле: pV=vRT.

- «p» — давление насыщенного пара (Па);
- «V» — его объем (м3);
- «v» — общее количество вещества (моль);
- «R» — газовая постоянная (8,31 м2);
- «T» — температура среды (К).
Данная формула помогает рассчитать не только параметры насыщенного пара, но и их изменения при изменении плотности, объема или давления.
Несколько примеров
Задача:
- В цилиндре находится насыщенный пар и вода при постоянной температуре.
- Поршень сдвигается, уменьшая свободный объем пространства.
- Выяснить, как повлияет уменьшение объема на общую массу жидкости.
Ответ: масса жидкости увеличится, по причине обратного фазового перехода пара в жидкость.
Согласно уравнению pV=m/u*Rt, при снижении общего объема пара не последует снижения его давления, а значит пар конденсируется обратно в воду, увеличив ее общую массу.
Задача:
- Температура насыщенного пара 100 градусов.
- Давление 101 кПа.
- Плотность неизвестна.
Решение: P=pu/Rt=105*18*10-3/8,31*373=0,5 кг/м3.
Ответ: насыщенный пар при температуре 100 градусов по Цельсию и при давлении 101 кПа имеет плотность 0,5 кг/м3. При решении данной задачи использовались табличные величины молярной массы, газовой постоянной и давлении при данной температуре.
Где эти расчеты могут пригодиться на практике?

- при проектировании бытовых систем вентиляции и кондиционирования;
- для эффективной работы отопительных систем;
- при проектировании и поддержании работы паровых турбинных установок.
На основе этих расчетов строятся «умные» датчики влажности, которые реагируют на количество молекул воды или иных веществ в воздухе. Свойства насыщенного пара также применяются при выпаривании летучих веществ с их очисткой за счет последующей конденсации их насыщенных паров.
Заключение
Свойства насыщенного пара не делают его идеальным газом, но позволяют использовать в быту и в промышленности. Этот пар является идеальным источником тепла, влажности и помогает разделять химические элементы за счет способности к конденсации.
Формула расчета по уравнению Менделеева-Клапейрона позволяет рассчитать основные параметры пара и определить степень его схожести с насыщенным.
Насыщенный пар
-
Темы кодификатора ЕГЭ: насыщенные и ненасыщенные пары, влажность воздуха.
-
Испарение и конденсация
-
Динамическое равновесие
-
Свойства насыщенного пара
-
Влажность воздуха
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: насыщенные и ненасыщенные пары, влажность воздуха.
Если открытый стакан с водой оставить на долгое время, то в конце концов вода полностью улетучится. Точнее — испарится. Что такое испарение и почему оно происходит?
Испарение и конденсация
При данной температуре молекулы жидкости обладают разными скоростями. Скорости большинства молекул находятся вблизи некоторого среднего значения (характерного для этой температуры). Но попадаются молекулы, скорости которых значительно отличаются от средней как в меньшую, так и большую сторону.
На рис. 1 изображён примерный график распределения молекул жидкости по скоростям. Голубым фоном показано то самое большинство молекул, скорости которых группируются около среднего значения. Красный «хвост» графика — это небольшое число «быстрых» молекул, скорости которых существенно превышают среднюю скорость основной массы молекул жидкости.
Рис. 1. Распределение молекул по скоростям
Когда такая весьма быстрая молекула окажется на свободной поверхности жидкости (т.е. на границе раздела жидкости и воздуха), кинетической энергии этой молекулы может хватить на то, чтобы преодолеть силы притяжения остальных молекул и вылететь из жидкости. Данный процесс и есть испарение, а молекулы, покинувшие жидкость, образуют пар.
Итак, испарение — это процесс превращения жидкости в пар, происходящий на свободной поверхности жидкости (при особых условиях превращение жидкости в пар может происходить по всему объёму жидкости. Данный процесс вам хорошо известен — это кипение).
Может случиться, что через некоторое время молекула пара вернётся обратно в жидкость.
Процесс перехода молекул пара в жидкость называется конденсацией. Конденсация пара — процесс, обратный испарению жидкости.
к оглавлению ▴
Динамическое равновесие
А что будет, если сосуд с жидкостью герметично закрыть? Плотность пара над поверхностью жидкости начнёт увеличиваться; частицы пара будут всё сильнее мешать другим молекулам жидкости вылетать наружу, и скорость испарения станет уменьшаться. Одновременно начнёт увеличиваться скорость конденсации, так как с возрастанием концентрации пара число молекул, возвращающихся в жидкость, будет становиться всё больше.
Наконец, в какой-то момент скорость конденсации окажется равна скорости испарения. Наступит динамическое равновесие между жидкостью и паром: за единицу времени из жидкости будет вылетать столько же молекул, сколько возвращается в неё из пара. Начиная с этого момента количество жидкости перестанет убывать, а количество пара — увеличиваться; пар достигнет «насыщения».
Насыщенный пар — это пар, который находится в состоянии динамического равновесия со своей жидкостью. Пар, не достигший состояния динамического равновесия с жидкостью, называется ненасыщенным.
Давление и плотность насыщенного пара обозначаются и
. Очевидно,
и
— это максимальные давление и плотность, которые может иметь пар при данной температуре. Иными словами, давление и плотность насыщенного пара всегда превышают давление и плотность ненасыщенного пара.
к оглавлению ▴
Свойства насыщенного пара
Оказывается, что состояние насыщенного пара (а ненасыщенного — тем более) можно приближённо описывать уравнением состояния идеального газа (уравнением Менделеева — Клапейрона). В частности, имеем приближённое соотношение между давлением насыщенного пара и его плотностью:
(1)
Это весьма удивительный факт, подтверждаемый экспериментом. Ведь по своим свойствам насыщенный пар существенно отличается от идеального газа. Перечислим важнейшие из этих отличий.
1. При неизменной температуре плотность насыщенного пара не зависит от его объёма.
Если, например, насыщенный пар изотермически сжимать, то его плотность в первый момент возрастёт, скорость конденсации превысит скорость испарения, и часть пара конденсируется в жидкость — до тех пор, пока вновь не наступит динамическое равновесие, в котором плотность пара вернётся к своему прежнему значению.
Аналогично, при изотермическом расширении насыщенного пара его плотность в первый момент уменьшится (пар станет ненасыщенным), скорость испарения превысит скорость конденсации, и жидкость будет дополнительно испаряться до тех пор, пока опять не установится динамическое равновесие — т.е. пока пар снова не станет насыщенным с прежним значением плотности.
2. Давление насыщенного пара не зависит от его объёма.
Это следует из того, что плотность насыщенного пара не зависит от объёма, а давление однозначно связано с плотностью уравнением (1).
Как видим, закон Бойля — Мариотта, справедливый для идеальных газов, для насыщенного пара не выполняется. Это и не удивительно — ведь он получен из уравнения Менделеева — Клапейрона в предположении, что масса газа остаётся постоянной.
3. При неизменном объёме плотность насыщенного пара растёт с повышением температуры и уменьшается с понижением температуры.
Действительно, при увеличении температуры возрастает скорость испарения жидкости.
Динамическое равновесие в первый момент нарушается, и происходит дополнительное испарение некоторой части жидкости. Пара будет прибавляться до тех пор, пока динамическое равновесие вновь не восстановится.
Точно так же при понижении температуры скорость испарения жидкости становится меньше, и часть пара конденсируется до тех пор, пока не восстановится динамическое равновесие — но уже с меньшим количеством пара.
Таким образом, при изохорном нагревании или охлаждении насыщенного пара его масса меняется, поэтому закон Шарля в данном случае не работает. Зависимость давления насыщенного пара от температуры уже не будет линейной функцией.
4. Давление насыщенного пара растёт с температурой быстрее, чем по линейному закону.
В самом деле, с увеличением температуры возрастает плотность насыщенного пара, а согласно уравнению (1) давление пропорционально произведению плотности на температуру.
Зависимость давления насыщенного пара от температуры является экспоненциальной (рис. 2). Она представлена участком 1–2 графика. Эту зависимость нельзя вывести из законов идеального газа.
Рис. 2. Зависимость давления пара от температуры
В точке 2 вся жидкость испаряется; при дальнейшем повышении температуры пар становится ненасыщенным, и его давление растёт линейно по закону Шарля (участок 2–3).
Вспомним, что линейный рост давления идеального газа вызван увеличением интенсивности ударов молекул о стенки сосуда. В случае нагревания насыщенного пара молекулы начинают бить не только сильнее, но и чаще — ведь пара становится больше. Одновременным действием этих двух факторов и вызван экспоненциальный рост давления насыщенного пара.
к оглавлению ▴
Влажность воздуха
Воздух, содержащий водяной пар, называется влажным.Чем больше пара находится в воздухе, тем выше влажность воздуха.
Абсолютная влажность — это парциальное давление водяного пара, находящегося в воздухе (т. е. давление, которое водяной пар оказывал бы сам по себе, в отсутствие других газов). Иногда абсолютной влажностью называют также плотность водяного пара в воздухе.
Относительная влажность воздуха — это отношение парциального давления водяного пара в нём к давлению насыщенного водяного пара при той же температуре. Как правило, это отношение выражают в процентах:
Из уравнения Менделеева-Клапейрона (1) следует, что отношение давлений пара равно отношению плотностей. Так как само уравнение (1), напомним, описывает насыщенный пар лишь приближённо, мы имеем приближённое соотношение:
Одним из приборов, измеряющих влажность воздуха, является психрометр. Он включает в себя два термометра, резервуар одного из которых завёрнут в мокрую ткань. Чем ниже влажность, тем интенсивнее идёт испарение воды из ткани, тем сильнее охлаждается резервуар «мокрого» термометра, и тем больше разность его показаний и показаний сухого термометра. По этой разности с помощью специальной психрометрической таблицы определяют влажность воздуха.
Спасибо за то, что пользуйтесь нашими публикациями.
Информация на странице «Насыщенный пар» подготовлена нашими авторами специально, чтобы помочь вам в освоении предмета и подготовке к экзаменам.
Чтобы успешно сдать необходимые и поступить в ВУЗ или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из данного раздела.
Публикация обновлена:
08.05.2023
Это пар, находящийся в термодинамическом равновесии с жидкой (или твёрдой) фазой одного и того же вещества.
Одним из параметров, характеризующим насыщенный пар, является его давление.
Давление насыщенного пара зависит от температуры и не зависит от объема.
Разберемся подробнее, почему так происходит.
Почему давление насыщенного пара не зависит от объема?
Рассмотрим этот вопрос на примере дистиллированной воды.
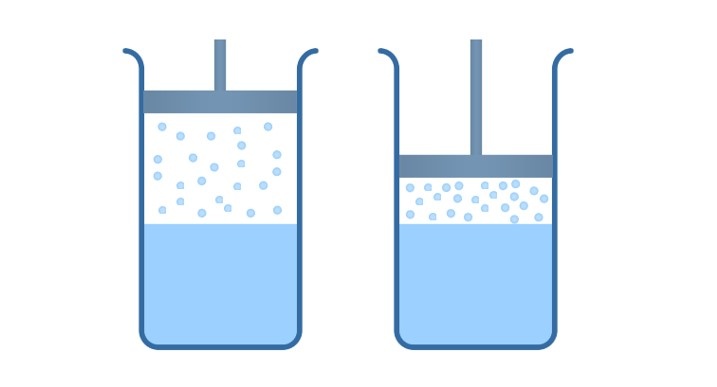
Возьмем цилиндр с поршнем, в полости которого находится дистиллят в термодинамическом равновесии с паром. Начинаем двигать поршень вниз, объем цилиндра начинает уменьшаться, происходит сжатие насыщенного пара, при этом мы поддерживаем постоянную температуру.
Система начнёт выходить из равновесия, плотность пара будет увеличиваться, и из газообразной фазы в жидкую будет переходить молекул больше, чем из жидкой в газообразную.
Другими словами, мы будем наблюдать процесс превращения насыщенного пара обратно в жидкость, этот процесс называется конденсация.
Если мы начнем поднимать поршень, объем полости увеличится, концентрация водяных паров над жидкостью начнет уменьшаться, вследствие чего, вода в сосуде начнет испаряться до тех пор, пока давление и концентрация насыщенного пара над жидкостью не придет в исходное состояние, то есть пока не наступит термодинамическое равновесие.
Из выше сказанного мы делаем вывод, что концентрация молекул насыщенного пара над жидкостью при постоянной температуре не зависит от его объема.
P=nkT,P=nkT,
где PP – давление пара (Па), nn – концентрация молекул пара (м-3), kk – постоянная Больцмана (равна 1,380649 Дж/К), ТТ – температура (К).
Из приведенной формулы мы видим, что давление насыщенного пара прямо пропорционально концентрации молекул и температуре паров над жидкостью (или твердым веществом) и, следовательно, не зависит от занимаемого им объема.
Как давление насыщенного пара зависит от температуры?
Из формулы, приведенной выше, мы наблюдаем, что давление насыщенного пара прямо пропорционально температуре термодинамической системы.
Несмотря на это, экспериментальная зависимость отличается от описанной уравнением, и давление пара увеличивается с большей скоростью с повышением температуры, нежели по линейному закону. Почему так происходит?
Всё дело в том, что во время увеличения подведенной температуры растёт и скорость испарения жидкости (или сублимации твёрдого вещества), вследствие этих факторов, увеличивается и концентрация испарённых (или сублимированных) молекул в газообразном состоянии над жидкой (или твёрдой) фазой. Поэтому и давление насыщенных паров изменяется быстрее. Плотность пара будет возрастать до тех пор, пока термодинамическое равновесие для данной температуры вновь не восстановится.
На участке 1-2 мы как раз видим влияние двух факторов – увеличение температуры и концентрации паров. В точке 2 вся жидкость испаряется (или твердое вещество сублимируется) и пар становится ненасыщенным, тогда давление начинает расти по линейному закону, что видно на участке 2-3.
Значения давления насыщенного пара для воды и других веществ при различных температурах получены эмпирическим методом. Эти данные можно найти в справочных материалах.
Тест по теме «Давление насыщенного пара»
§10. Насыщенный пар. Кипение. Влажность
называется пар, находящийся в динамическом равновесии со своей жидкостью: скорость испарения равна скорости конденсации.
Давление и плотность насыщенного пара для данного вещества зависят от его температуры и увеличиваются при увеличении температуры.
Условие кипения жидкости – это условие роста пузырьков насыщенного пара в жидкости. Пузырёк может расти, если давление насыщенного пара внутри него будет не меньше внешнего давления. Итак,
жидкость кипит при той температуре, при которой давление её насыщенных паров равно внешнему давлению.
Приведём полезный пример.
Известно, что при нормальном атмосферном давлении `p_0~~10^5 «Па»` вода кипит при `100^@»C»`. Это означает, что давление насыщенных паров воды при `100^@»C»` равно `p_0~~10^5 «Па»`.
Пары воды в атмосферном воздухе обычно ненасыщенные. Абсолютной влажностью воздуха называется плотность водяных паров `rho`. Относительной влажностью воздуха называется величина
`varphi=p/p_»нас»`. (24)
Здесь `p` – парциальное давление паров воды при данной температуре в смеси воздух – пары воды, `p_»нас»` – парциальное давление насыщенных водяных паров при той же температуре. Опыт показывает, что `p_»нас»` зависит только от температуры и не зависит от плотности и состава воздуха.
Если пар считать идеальным газом, то `p=rho/muRT`, `p_»нас»=(rho_»нас»)/muRT`,
где `rho` и `rho_»нас»` – плотности ненасыщенного и насыщенного водяного пара, `mu=18 «г»//»моль»`. Деление одного уравнения на другое даёт `p/p_»нас»=rho/rho_»нас»`. Итак,
`varphi=p/p_»нас»~~rho/rho_»нас»`. (25)
Воздух имеет температуру `60^@»C»` и абсолютную влажность `50 «г»//»м»^3`. Какой будет абсолютная влажность этого воздуха, если температура понизится до `10^@»C»`? Известно, что при `10^@»C»` давление насыщенного пара воды `p=1230 «Па»`.
При `10^@»C»` `(T=283 «К»)` плотность насыщенных паров воды
`rho=(mup)/(RT)=9,4*10^(-3) «кг»//»м»^3=9,4 «г»//»м»^3`.
Эта величина меньше, чем `50 «г»//»м»^3`. Поэтому часть пара сконденсируется, и абсолютная влажность будет `9,4 «г»//»м»^3`.
Содержание
-
1 Насыщенные и ненасыщенные пары
- 1.1 Свойства насыщенных паров
-
2 Влажность воздуха
- 2.1 Психрометр. Гигрометр
- 2.2 См. также
- 3 Литература
Насыщенные и ненасыщенные пары
Над свободной поверхностью жидкости всегда имеются пары этой жидкости. Если сосуд с жидкостью не закрыт, то всегда найдутся молекулы пара, которые удаляются от поверхности жидкости и не могут вернуться назад в жидкость. В закрытом сосуде одновременно с испарением жидкости происходит конденсация пара. Сначала число молекул, вылетающих из жидкости за 1 с, больше числа молекул, возвращающихся обратно, и плотность, а значит, и давление пара растет. Число молекул пара возрастает до тех пор, пока число молекул, покинувших жидкость (испарившихся), не станет равно числу молекул, возвратившихся у жидкость (сконденсировавшихся) за один и тот же промежуток времени. Такое состояние называют динамическим равновесием.
Пар, находящийся в состоянии динамического равновесия со своей жидкостью, называется насыщенным паром. Для описания насыщенного пара применяют следующие величины: давление насыщенного пара pн и плотность насыщенного пара ρн. При данной температуры насыщенный пар обладает максимально возможным значением давления и плотности пара.
Пар, давление которого меньше давления насыщенного пара при данной температуре, называется ненассыщенным. Аналогично можно было дать определение и через плотность пара.
Опыт показывает, что ненасыщенные пары подчиняются всем газовым законам, и тем точнее, чем дальше они от насыщения.
Свойства насыщенных паров
Для насыщенных паров характерны следующие свойства:
- плотность и давление насыщенного пара зависят от рода вещества. Чем меньше удельная теплота парообразования жидкости, тем быстрее она испаряется и тем больше давление и плотность ее паров;
- давление и плотность насыщенного пара однозначно определяются его температурой (не зависят от того, каким образом пар достиг этой температуры: при нагревании или при охлаждении);
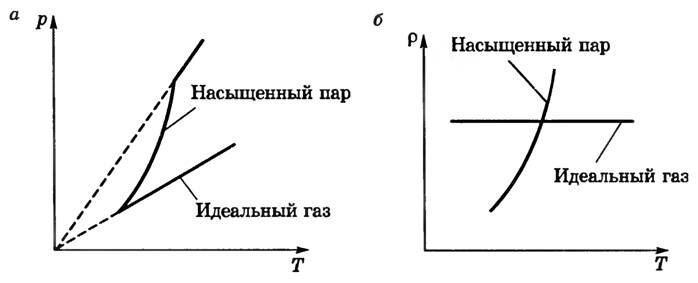
- в замкнутом сосуде (V = const) давление и плотность пара быстро возрастают с увеличением температуры (рис. 1, а, б). Более сильное увеличение давления насыщенного пара по сравнению с идеальным газом объясняется тем, что здесь происходит рост давления не только за счет роста средней кинетической энергии молекул (как у идеального газа), но и за счет увеличения концентрации молекул (было замечено, что при нагревании уровень жидкости в закрытом сосуде понижается, следовательно, масса и плотность пара возрастают). Таким образом, газовый закон для изохорного процесса не применим к насыщенному пару.
Рис. 1
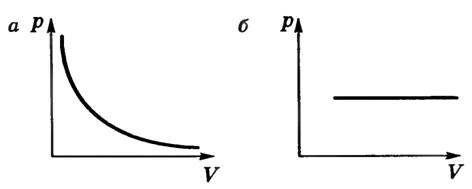
- при постоянной температуре давление и плотность насыщенного пара не зависят от объема. На рисунке 2 для сравнения приведены изотермы идеального газа (а) и насыщенного пара (б). Опыт показывает, что при изотермическом расширении уровень жидкости в сосуде понижается, при сжатии — повышается, т.е. изменяется число молекул пара так, что плотность пара остается постоянной. Таким образом, газовый закон для изотермического процесса также не применим к насыщенному пару;
Рис. 2
- уравнение p = n⋅k⋅T описывает состояние насыщенного пара только приближенно.
Следовательно, насыщенный пар не подчиняется газовым законам идеального газа. Значения давления и плотности насыщенного пара при заданной температуре определяются из таблиц (см. таблицу).
Таблица. Давление (р) и плотность (ρ) насыщенных паров воды при различных температурах (t).
| t, °С | р, кПа | ρ, г/м3 |
|---|---|---|
| 0 | 0,611 | 4,84 |
| 20 | 2,34 | 17,3 |
| 40 | 7,37 | 51,2 |
| 60 | 19,9 | 130 |
| 80 | 47,3 | 293 |
| 100 | 101,3 | 598 |
| 120 | 196 | 1122 |
Влажность воздуха
В результате испарения воды с многочисленных водоемов (морей, озер, рек и др.), а также с растительных покровов в атмосферном воздухе всегда содержится водяной пар. От количества водяного пара, содержащегося в воздухе, зависит погода, самочувствие человека, функционирование многих его органов, жизнь растений, а также сохранность технических объектов, архитектурных сооружений, произведений искусств. Поэтому очень важно следить за влажностью воздуха, уметь измерять ее.
Водяной пар в воздухе обычно является ненасыщенным. Перемещение воздушных масс, обусловленное в конечном счете излучением Солнца, приводит к тому, что в одних местах нашей планеты в данный момент испарение воды преобладает над конденсацией, а в других, наоборот, преобладает конденсация.
Воздух, содержащий водяные пары, называют влажным. Для характеристики содержания водяного пара в воздухе вводят ряд величин: абсолютную влажность и относительную влажность.
Абсолютной влажностью ρ воздуха называют величину, численно равную массе водяного пара, содержащегося в 1 м3 воздуха (т.е. плотность водяного пара в воздухе при данных условиях).
В СИ единицей абсолютной влажности является килограмм на кубический метр (кг/м3). Иногда используются внесистемные единицы грамм на кубический метр (г/м3).
Абсолютная влажность ρ и давление p водяного пара связаны между собой уравнением состояния
(~p cdot V = dfrac {m cdot M}{R cdot T} Rightarrow p = dfrac{rho}{M} cdot R cdot T)
Если известна только абсолютная влажность, еще нельзя судить, насколько сух или влажен воздух. Для определения степени влажности воздуха необходимо знать, близок или далек водяной пар от насыщения.
Относительной влажностью воздуха φ называют выраженное в процентах отношение абсолютной влажности к плотности ρ0 насыщенного пара при данной температуре (или отношение давления p водяного пара к давлению p0 насыщенного пара при данной температуре):
(~varphi = dfrac{rho}{rho_0} cdot 100;%, ;; ~varphi = dfrac{p}{p_0} cdot 100;%.)
Чем меньше относительная влажность, тем дальше пар от насыщения, тем интенсивнее происходит испарение. Давление насыщенного пара p0 при заданной температуре — величина табличная. Давление p водяного пара (а значит, и абсолютную влажность) определяют по точке росы.
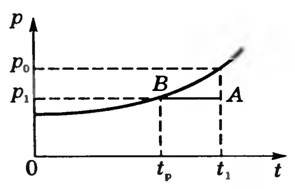
Пусть при температуре t1 давление водяного пара p1. Состояние пара на диаграмме р, t изобразится точкой А (рис. 5).
Рис. 5
При изобарном охлаждении до температуры tp пар становится насыщенным и его состояние изобразится точкой В. Температуру tp, при которой водяной пар становится насыщенным, называют точкой росы. При охлаждении ниже точки росы начинается конденсация паров: появляется туман, выпадает роса, запотевают окна. Точка росы позволяет определить давление водяного пара p1, находящегося в воздухе при температуре t1.
Действительно, из рисунка 5 видим, что давление p1 равно давлению насыщенного пара при точке росы p1 = p0tp . Следовательно, (~varphi = dfrac{p_{0tp}}{p_0} cdot 100 ;%)
Психрометр. Гигрометр
При понижении температуры, относительная влажность воздуха увеличивается. При некоторой температуре (точке росы) водяной пар становится насыщенным. Дальнейшее понижение температуры приводит к тому, что образующийся излишек водяных паров начинает конденсироваться в виде капелек росы или тумана.
Для определения относительной влажности воздуха, можно искусственно понизить температуру воздуха в какой-то ограниченной области до точки росы. Абсолютная влажность и, соответственно, давление водяных паров при этом останутся неизменными. Сравнивая давление водяного пара при точке росы с давлением насыщенного пара, которое могло бы быть при интересующей нас температуре, мы тем самым, найдем относительную влажность воздуха. Быстрого охлаждения можно добиться при интенсивном испарении какой-нибудь летучей жидкости. Такой метод применяют для измерении влажности при помощи конденсационного гигрометра.
Конденсационный гигрометр состоит из металлической коробочки с двумя отверстиями (рис. 6).
Рис. 6
В коробочку заливается эфир. С помощью резиновой груши через коробочку прокачивается воздух. Эфир очень быстро испаряется, температура коробочки и воздуха, находящегося вблизи нее, понижается, а относительная влажность растет. При некоторой температуре, которая измеряется термометром, вставленным в отверстие прибора, поверхность коробочки покрывается мельчайшими капельками росы. Чтобы точнее зафиксировать момент появления на поверхности коробочки росы, эта поверхность полируется до зеркального блеска, а рядом с коробочкой для контроля располагается отполированное металлическое кольцо.
В современных конденсационных гигрометрах для охлаждения зеркальца пользуются полупроводниковым элементом, принцип действия которого основан на Пельтье эффекте, а температура зеркальца измеряется вмонтированным в него проволочным сопротивлением или полупроводниковым микротермометром.
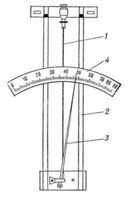
Действие волосного гигрометра основано на свойстве обезжиренного человеческого волоса изменять свою длину при изменении влажности воздуха, что позволяет измерять относительную влажность от 30 до 100%. Волос 1 (рис. 7) натянут на металлическую рамку 2. Изменение длины волоса передаётся стрелке 3, перемещающейся вдоль шкалы.
-
а
-
б
Рис. 7
Действие керамического гигрометра основано на зависимости электрического сопротивления твердой и пористой керамической массы (смесь глины, кремния, каолина и некоторых окислов металла) от влажности воздуха.
Относительную влажность определяют также с помощью психрометра.
Психрометр состоит из двух термометров, шарик одного из них обмотан тканью, нижние концы которой опущены в сосуд с дистиллированной водой (рис. 8). Сухой термометр регистрирует температуру воздуха, а влажный — температуру испаряющейся воды. Но при испарении жидкости ее температура понижается. Чем суше воздух (меньше его относительная влажность), тем интенсивнее испаряется вода из влажной ткани и тем ниже ее температура. Следовательно, разность показаний сухого и влажного термометров (так называемая психрометрическая разность) зависит от относительной влажности воздуха. Зная эту разность температур, определяют относительную влажность воздуха по специальным психрометрическим таблицам.
Рис. 8
- Гигрометр — от греч.Hygros — влажный.
- Психрометр — от греч.Psychros — холодный + Metreo — измеряю
См. также
- Гигрометр Wikipedia.org
- Измерители влажности воздуха и газов (гигрометр ВИТ, гигрометр электронный, гигрометр психометрический …)
- Относительная влажность Wikipedia.org
- Психрометр Wikipedia.org
Литература
- Аксенович Л. А. Физика в средней школе: Теория. Задания. Тесты: Учеб. пособие для учреждений, обеспечивающих получение общ. сред, образования / Л. А. Аксенович, Н.Н.Ракина, К. С. Фарино; Под ред. К. С. Фарино. — Мн.: Адукацыя i выхаванне, 2004. — C. 197-203.
- Жилко В.В. Физика: Учеб. пособие для 11-го кл. общеобразоват. шк. с рус. яз. обучения / В.В. Жилко, А.В.Лавриненко, Л.Г. Маркович. — Мн.: Нар. асвета, 2002. — С. 194-203.
- Открытая Физика