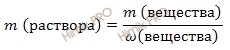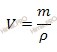Объем раствора азотной кислоты
Какой объем раствора азотной кислоты (HNO3) концентрированного с массовой долей равной 60 % и плотностью раствора 1,37 г/см3 необходимо взять для приготовления 800 см3 раствора с молярной концентрацией вещества, равной 2 моль/л?
Решение задачи
Найдем сколько концентрированной азотной кислоты (HNO3) (в граммах) потребуется для приготовления 800 см3 (или 0,8 л объем раствора азотной кислоты) раствора с молярной концентрацией 2 моль/л. Для расчета будем использовать формулу нахождения молярной концентрации раствора:
где:
CM – молярная концентрация раствора;
n – химическое количество растворенного вещества;
M – молярная масса растворенного вещества;
m – масса растворенного вещества;
V – объем раствора азотной кислоты.
Напомню, что под молярной концентрацией понимают количество (число моль) данного вещества, содержащегося в единице объема раствора. Молярную концентрацию выражают в моль/л или используют сокращение «M».
Из вышеуказанной формулы выразим и рассчитаем массу растворенного вещества:
Учитывая, что молярная масса азотной кислоты (HNO3) равна 63 г/моль (смотри таблицу Менделеева), получаем:
m (HNO3 (конц.)) = 2 моль/л ∙ 63 г/моль ∙ 0,8 л = 100,8 (г).
Используя формулу нахождения массовой доли растворенного вещества:
выразим массу раствора азотной кислоты (HNO3):
Получаем:
m (раствора HNO3 (конц.)) = 100,8 г/ 0,6 = 168 (г).
Если раствор 60-процентный, то массовая доля азотной кислоты (HNO3) в нем 0,6.
Вычислим объем раствора азотной кислоты (HNO3) концентрированного, который потребуется для приготовления 0,8 л раствора с молярной концентрацией 2 моль/л. Будем использовать формулу, устанавливающую связь между объемом раствора азотной кислоты и массой раствора:
Получаем, объем раствора азотной кислоты:
V (раствора HNO3 (конц.)) = 168 г /1,37 г/мл = 122,63 (мл).
Ответ:
объем раствора азотной кислоты концентрированного 122,63 миллилитра.
Похожие задачи
Какой объём раствора азотной кислоты с массовой долей HNO3 60% (r=1,37) нужно взять, чтобы приготовить 200 мл раствора с молярной концентрацией HNO3 равной 3 моль/л?
Решение:
Определяем массу азотной кислоты необходимую для приготовления 200 мл раствора с молярной концентрацией 3 моль/л
с(HNO3) =
m(HNO3) = с(HNO3)×M(HNO3)×V(p-pa) = 3 моль/л× 63 г/моль×0,2 л = 37,8 г
Определяем массу раствора с массовой долей HNO3, в котором содержится HNO3 массой 37,8 г.
В 100 г р-ра содержится 60 гHNO3
х г р-ра 37,8 г
m(р-ра) = х = = 63 гV(p-pa) =
=
= 46,2 мл.
Эту задачу можно решить, используя формулу перехода от массовой доли к молярной концентрации.
Вася Иванов
Мореплаватель — имя существительное, употребляется в мужском роде. К нему может быть несколько синонимов.
1. Моряк. Старый моряк смотрел вдаль, думая о предстоящем опасном путешествии;
2. Аргонавт. На аргонавте были старые потертые штаны, а его рубашка пропиталась запахом моря и соли;
3. Мореход. Опытный мореход знал, что на этом месте погибло уже много кораблей, ведь под водой скрывались острые скалы;
4. Морской волк. Старый морской волк был рад, ведь ему предстояло отчалить в долгое плавание.
Светило науки — 553134 ответа — 388270 раз оказано помощи
Ответ:
Объяснение:
определить объём раствора азотной кислоты с массовой долей кислоты 60% и с плотностью 1,07 г/см3 при реакции с медью массой 32г
Плотность 60% азотной кислоты равна, 1,367 г/см3. Приводимая в задании плотность 1,07 г/см3 соответствует концентрации 12,6%.
Это кислота считается разбавленной и реакция с медью протекает по уравнению:
3Сu + 8HNO₃ = 3Cu(NO₃)₂ + 2NO + 4H₂O
Масса меди 32 г соответствует 0,5 моль, а кислоты расходуется 1,333 моль или 84 г Масса 12,6% раствора 84 г: 0,126 = 667 г или
это соответствует 667 г : 1,07 = 623 см3.
Если опечатка сделана в плотности азотной кислоты и азотная кислота 60% то взаимодействие меди с концентрированной азотной кислотой протекает по уравнению:
Сu + 4HNO₃ = Cu(NO₃)₂ + NO₂ + 2H₂O
Тогда на реакцию с 0,5 моль меди затрачивается 2 моль азотной кислоты или 126 г. Тогда масса 60% раствора 210 г, а объем 60% раствора с плотностью 1,37 г/см³ будет равен 153,3 см³
С точки зрения расхода реактивов, такое условие задачи ближе к реальному.
ответы
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
похожие вопросы 5