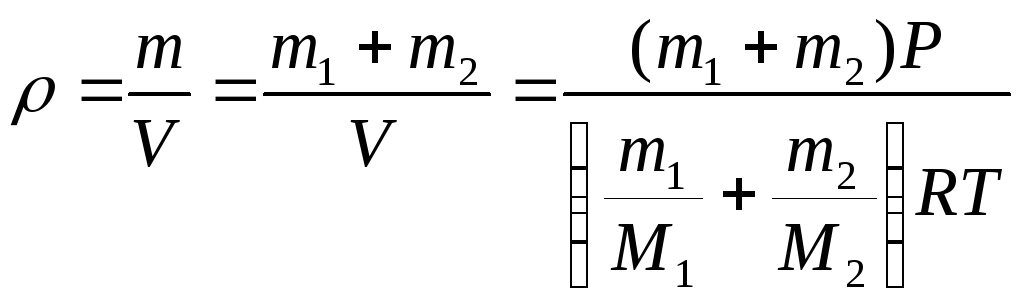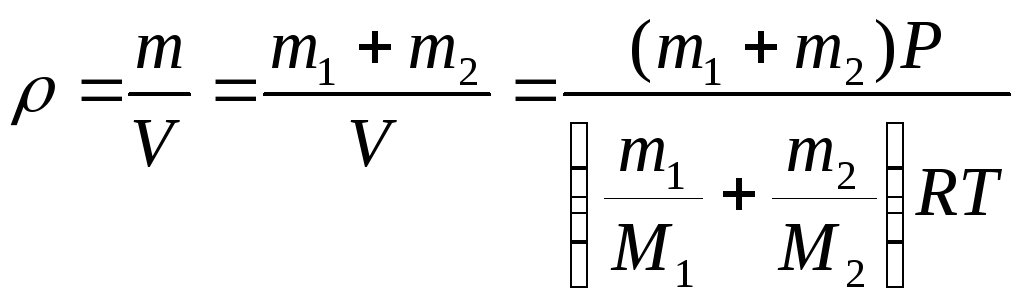План решения задач на газовые законы
-
Если
в задаче рассматривается одно состояние
газа и требуется найти какой-либо
параметр этого состояния, нужно
воспользоваться уравнением Менделеева
– Клапейрона. -
Если
значения давления и объема явно не
заданы, их нужно выразить через заданные
величины, подставить в записанное
уравнение и, решив его, найти неизвестный
параметр. -
В
том случае, когда в задаче рассматриваются
два различных состояния газа, нужно
установить, изменяется ли масса газа
при переходе из одного состояния в
другое. Если масса остается постоянной,
можно применить уравнение Клапейрона.
Если же при постоянной массе в данном
процессе не изменяется какой-либо из
параметров ( р,V или Т), применяются
уравнение соответствующего закона
(Гей-Люссака, Шарля или Бойля-Мариотта). -
Если
в двух состояниях масса газа разная,
то для каждого состояния записывают
уравнение Менделеева-Клапейрона. Затем
систему уравнений решают относительно
искомой величины.
Примеры решения задач
Пример 3.1. Определите
число молекул воды в бутылке вместимостью
0,33л. Молярная масса воды М=18∙10-3
кг/моль, плотность воды ρ=1г/см3.
Дано:
V=0,33л=0,33∙10-3
м3;
М=18∙10-3
кг/моль; ρ=1г/см3=
1∙103
кг/м3;
Найти:
N.
Решение:
Масса
воды, занимающей объём V,
m=ρV,
(1)
где
ρ – плотность воды.
Масса
молекулы
,
(2)
где
М – молярная масса; NA=6,02∙
1023моль-1
–
постоянная Авогадро.
Число
молекул в бутылке
(3)
Подставляя
в выражение (3) формулы (1) и (2), получим
искомое число молекул:
.
Ответ:
N=1,1∙1025.
Пример 3.1. Узкая
цилиндрическая трубка, закрытая с одного
конца, содержит воздух, отделённый от
наружного воздуха столбиком ртути.
Когда трубка обращена закрытым концом
кверху, воздух внутри неё занимает длину
ℓ, когда же трубка обращена кверху
открытым концом, то воздух внутри неё
занимает длину ℓ’ < ℓ. Длина ртутного
столбика h мм. Определить атмосферное
давление.
Дано:
ℓ; ℓ’ < ℓ; h.
Найти:
Р.
Решение:
В данном процессе
изменяются давление и объём воздуха, а
температура остаётся постоянной.
Следовательно, если начальные параметры
воздуха обозначить Р1
и V1,
а конечные как Р2
и V2 получаем
следующее соотношение:
Р1V1
= Р2V2
Когда
трубка обращена закрытым концом кверху,
воздух в ней находится под давлением
Р1=
Ратм
– h ( здесь и далее измеряем в мм.рт. ст.).
Если же трубку перевернуть, давление
воздуха в ней будет равно Р2
= Ратм
+ h .
Учитывая,
что V1 =
Sℓ1,
V2 =
Sℓ2,
где S — площадь сечения трубки, получаем:
(Ратм
– h) Sℓ =
(Ратм
+ h) Sℓ’,
Отсюда
находим атмосферное давление
Ответ.
Пример
3.2. В сосуде находится
смесь m = 7 г азота и m = 11г углекислого
газа при температуре Т = 290 К и давлении
Р = 1 атм. Найти плотность этой смеси,
считая газа идеальными.
Дано:
m1=7
г=7∙10-3кг;
m2=11
г=11∙10-3кг;
Т=290К; Р=1атм=105Па.
Найти:
ρ.
Решение:
Давление газов в сосуде
известно. Если через Р1
обозначить давление
азота, если бы углекислого газа не было,
а через Р2 давление
углекислого газа, если бы не было азота
(так называемые парциальными давления),
то давление смеси газов Р будет согласно
закону Дальтона Р =
Р1 +
Р2.
Учитывая, что температура каждого газа
Т запишем для азота и кислорода уравнение
Менделеева-Клапейрона:
Складывая
эти выражения, получаем:
Отсюда
находим объём, занимаемый смесью газов
Плотность
смеси газов вычисляется по формуле
Ответ:
Пример
3.3. Кислород массой
m=10г
находится под давлением 200кПа при
температуре 280К. В результате изобарного
расширения газ занял объём 9л. Определите:
1) объём газа V1
до расширения; 2) температуру газа T2
после расширения; 3) плотность газа ρ2
после расширения.
Дано:
M=32∙10-3кг/моль;
m=10г=10∙10-3кг;
р=200кПа=2∙105Па=const;
Т1=280К;
V2=9г=9∙10-3м3.
Найти:
1) V1;
2) Т2;
3) ρ2.
Решение:
Объём газа до расширения найдём, согласно
уравнению Клапейрона-Менделеева,
,
откуда
Записав уравнение Клапейрона-Менделеева
для конечного состояния газа:
,
найдём искомую температуру
Плотность газа после расширения газа
.
Ответ:
1) V1=3,64
л; 2) Т2=693
К; 3) ρ2=1,11
кг/м3.
Пример 3.3. В
цилиндре с площадью основания 100 см2
находится воздух. Поршень расположен
на высоте 50 см от дна цилиндра. На поршень
кладут груз массой 50 кг, при этом он
опускается на 10 см. Найти температуру
воздуха после опускания поршня, если
до его опускания давление было равно
101 кПа, а температура 12С.
Дано: S=100см2=1∙10-2м2;h1=50см=0,5
м;m=50кг; Δh=10см=0,1
мt;P1=101∙103Па; Т1=12С=285
К.
Найти:
Т2.
Решение:
Рассмотрим два состояния воздуха под
поршнем: до опускания поршня и после
его опускания. До опускания поршня
состояние воздуха характеризуется
параметрами Р1,
V1,
T1,
после опускания поршня – параметрами
Р2,
V2,
T2,
где V1=Sh1,
Р2=Р0+Р,
,
V2=Sh2,
или, поскольку h2=h1—
Δh,
V2=S(h1—
Δh).
Применим
к этим двум состояниям формулу Клапейрона:
,
откуда
(1)
Подставим
в формулу (1) выражения для Р1,
V1,
Р2
и V2:
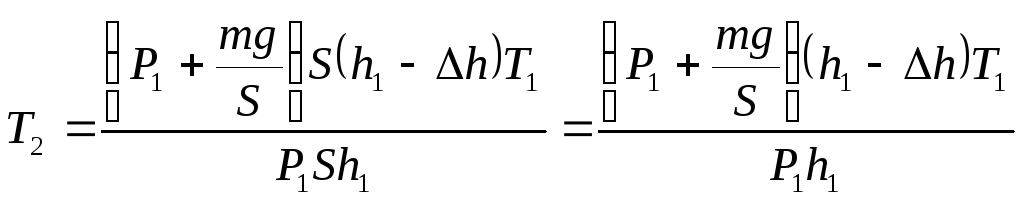
Ответ:
Т2=338К
Пример 3.3. Имеются
два сосуда с газом: один вместимостью
3 л, другой 4 л. В первом сосуде газ
находится под давлением 202 кПа, а во
втором 101 кПа. Под каким давлением будет
находиться газ, если эти cосуды соединить
между собой? Считать, что температура
в сосудах одинакова и постоянна.
Дано: V1=3л=3∙10—3м3;V2=4л=4∙10—3м3;Р1=202кПа=202∙103Па; Р2=101кПа=101∙103Па.
Найти:
Р.
Решение:
По закону Дальтона,
Р
= Р3
+ Р4 (1)
Так
как процесс изотермический, то парциальное
давление газа в каждом сосуде можно
найти по закону Бойля-Мариотта:
Р1V1
=
Р3V,
Р2V2
=
Р4V,
где
V=V1+V2.
Тогда парциальное давление газа в каждом
из сосудов после их соединения
,
, (2)
Подставляем
выражения (2) в (1):
Ответ:
Р=141 Па
Пример 3.3. В
баллоне содержатся сжатый газ при
температуре t1
= 27С
и давлении p1
= 4 МПа. Каково будет давление, если из
баллона выпустить
Δm
= 0,4m
массы газа, а температуру понизить до
t2
= 17С?
Дано: Т1=27С
=300 К;Р1=4МПа=4∙106
Па;Δm
= 0,4m;
Т2=17С
=290 К Найти:
Р.
Решение: Рассмотрим
два состояния газа: до разрежения и
после, когда осталось1-n массы m газа.
Параметры каждого из этих состояний
связаны уравнением Менделеева-Клапейрона:
,
где
Р1,
Т1,
Р2,
Т2
– соответственно давление и температура
газа до и после выпуска; m — масса газа;
М – молярная масса; V — объем.
Разделив
почленно первое равенство на второе,
получим:
,
oткуда
(1)
Ответ:
Р2
= 2,3106
Па = 2,3 МПа.
Пример
3.3. Найти максимально
возможную температуру идеального газа
в процессе P = P0
– αV2,
где P0,
α — положительные постоянные.
Дано:
P = P0
– αV2;
P0, α
— const
Найти:
Tmax.
Решение:
Для нахождения максимальной температуры
необходимо получить явную зависимость
последней от параметров и исследовать
эту зависимость на экстремум. Так как
газ является идеальным, выразим давление
из уравнения Менделеева-Клапейрона и
подставим его в уравнение процесса
Отсюда
выражаем температуру
Условие экстремума
,
которое сводится к выражению.
Решая
данное уравнение, получаем значение
объёма, при котором температура принимает
экстремальное значение
.
Исследуя знак второй производной, приходим к выводу, что при данном
значении объёма температура газа будет
идеальной. Подставляя выражение для
объёма в выражение для температуры при
данном процессе, получаем:
Ответ:
Пример
3.3. В сосуде
вместимостью V=5л
находится кислород массой m=15г.
определите: 1) концентрацию молекул
кислорода в сосуде; 2) число N
молекул газа в сосуде.
Дано:
V=5л=5∙10-3м3;
M=32∙10-3кг/моль;
m=15г=1,5∙10-2кг.
Найти:
1) n; 2) N.
Решение:
Записав
уравнение Клапейрона-Менделеева
(1)
И
уравнение состояния идеального газа
Р=nkT
(2)
И
поделив (1) на (2), найдём искомую концентрацию
молекул кислорода в сосуде
.
Концентрация
молекул
,
Откуда
искомое число молекул газа в сосуде
N=nV.
Ответ:
1)
n=5,64∙1025
м-3;
2) N=2,82∙1023.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Изменение объема при нагревании, первый закон Гей-Люссака
Если
| Vt | объем газа при произвольной температуре t, | метр3 |
|---|---|---|
| V0 | объем газа при температуре 0°С, | метр3 |
| t | температура, | 0°С |
| β | коэффициент объемного расширения газа, | 1/K |
то
[ V_t = V_0 ( 1 + βt ) ]
Из формулы (1) следует, что при температуре t1
[ V_1 = V_0 ( 1 + βt_1 ) ]
[ V_1 = V_0 bigg( 1 + frac{t_1}{273.15} bigg) ]
[ V_1 = V_0 bigg( 1 + frac{t_1}{T_0} bigg) ]
[ V_1 = V_0 bigg( frac{T_0 + t_1}{T_0} bigg) ]
а при другой температуре t2 соответственно
[ V_2 = V_0 ( 1 + βt_2 ) ]
[ V_2 = V_0 bigg( 1 + frac{t_2}{273.15} bigg) ]
[ V_2 = V_0 bigg( 1 + frac{t_2}{T_0} bigg) ]
[ V_2 = V_0 bigg( frac{T_0 + t_2}{T_0} bigg) ]
Разделив первое равенство на второе, получим
[ frac{V_1}{V_2} = frac{T_0 + t_1}{T_0 + t_2} ]
или
[ frac{V_1}{V_2} = frac{T_1}{T_2} ]
или
[ frac{V}{T} = const ]
Первый закон Гей-Люссака
Первый закон Гей-Люссака гласит: При постоянном давлении объем газа V пропорционален абсолютной температуре газа T
[ V sim T qquad (enspace p = const enspace) ]
Изменение объема при нагревании, первый закон Гей-Люссака |
стр. 523 |
|---|
Формулы закона Бойля Мариотта
P1/P2=V2/V1
или
P1V1=P2V2
При пользовании этими формулами безразлично, в каких единицах вы будете измерять объем и давление, лишь бы оба объема и оба давления были измерены в одинаковых единицах. Например, если одно давление измерено в килограммах на квадратный сантиметр, то в тех же единицах должно быть измерено и другое давление. Если один объем измерен в кубических сантиметрах, то так же должен быть измерен и другой.
Применение закона Бойля Мариотта в быту
Пылесос состоит главным образом из вентилятора, приводимого в движение электромотором. Вентилятор выталкивает воздух своими лопастями и создает за ними разреженное пространство. Так как воздух, который из-за разности давлений внутри и снаружи устремляется по трубке в камеру вентилятора, проходит через ковер, то пыль уносится с ковра. В некоторых пылесосах применяется, кроме того, вращающаяся щетка, подметающая и выбивающая ковер. Воздух, прошедший вентилятор, поступает в мешок или другой отстойник для пыли и грязи, которые потом могут быть опорожнены различными способами в зависимости от типа пылесоса.
Водолазные колокола и водолазные костюмы. Когда водолазный колокол погружается в воду, воздух тоже сжимается, но при помощи компрессора, находящегося снаружи. Воздух нагнетается под колокол, поэтому вода совсем не входит в колокол. При этом необходимо все время накачивать в колокол свежий воздух в количестве, необходимом для работающих там людей. Излишек воздуха будет пузырями вырываться наружу. Важной частью водолазного костюма является шлем, который привинчивается к верхней части водонепроницаемого костюма. Обычно шлем снабжают воздухом таким же образом, как водолазный колокол. В некоторых типах костюмов водолаз имеет при себе собственный запас сжатого воздуха.
Одно из своеобразных проявлений закона Бойля — наше дыхание. Когда мускулы, сокращаясь, тянут диафрагму вниз, объем пространства, где помещаются легкие, увеличивается, отчего давление внутри становится меньше наружного. В результате воздух из пространства с большим давлением поступает в легкие, где давление меньше. Обратное движение диафрагмы уменьшает объем легочного пространства и делает давление внутри легких большим наружного. Поэтому воздух и ненужные газы выходят из легких.
30
Масса m = 10 г кислорода находится при давлении p = 304 кПа и температуре t1 = 10 °С. После расширения вследствие нагревания при постоянном давлении кислород занял объем V2 = 10 л. Найти объем V1 газа до расширения, температуру t2 газа после расширения, плотности ρ1 и ρ2 газа до и после расширения.
Раздел:
- Молекулярная физика
Уравнение Клапейрона-Менделеева (уравнение состояния идеального газа).
Уравнение Клапейрона-Менделеева (1834 г) устанавливает связь между объемом V, давлением P и абсолютной температурой Т для газа:
n – число молей газа 
P – давление газа, Па;
V – объем газа, м 3 ;
T – абсолютная температура газа, К;
R – универсальная газовая постоянная 8,314 Дж/моль×K.
Если объём газа выражен в литрах, то уравнение Клапейрона-Менделеева записывается в виде:
Из уравнения Клапейрона-Менделеева следует три закона:
Уравнение Клапейрона-Менделеева. Связь между числом молей газа, его температурой, объемом и давлением.
Уравнение Клапейрона-Менделеева. Связь между числом молей газа, его температурой, объемом и давлением.
Калькулятор ниже предназначен для решения задач на использование уравнения Клапейрона-Менделеева, или уравнение состояния идеального газа. Некоторая теория изложена под калькулятором, ну а чтобы было понятно, о чем идет речь — пара примеров задач:
Примеры задач на уравнение Менделеева-Клапейрона
В колбе объемом 2,6 литра находится кислород при давлении 2,3 атмосфер и температуре 26 градусов Цельсия .
Вопрос: сколько молей кислорода содержится в колбе?
Вопрос: Каков объем этого газа при нормальных условиях? (Напомню, что нормальными условиями для газов считается давление в 1 атмосферу и температура 0 градусов Цельсия)
В калькулятор вводим начальные условия, выбираем, что считать (число моль, новые объем, температуру или давление), заполняем при необходимости оставшиеся условия, и получаем результат.
Уравнение Клапейрона-Менделеева. Связь между числом молей газа, его температурой, объемом и давлением.
Теперь немного формул.
где
P — давление газа (например, в атмосферах)
V — объем газа (в литрах);
T — температура газа (в кельвинах);
R — газовая постоянная (0,0821 л·атм/моль·K).
Если используется СИ, то газовая постоянная равна 8,314 Дж/K·моль
Так как m-масса газа в (кг) и M-молярная масса газа кг/моль, то m/M — число молей газа, и уравнение можно записать также
где n — число молей газа
И как нетрудно заметить, соотношение
есть величина постоянная для одного и того же количества моль газа.
И эту закономерность опытным путем установили еще до вывода уравнения. Это так называемые газовые законы — законы Бойля-Мариотта, Гей-Люссака, Шарля.
Так, закон Бойля-Мариотта гласит (это два человека):
Для данной массы газа m при неизменной температуре Т произведение давления на объем есть величина постоянная.
Закон Гей-Люссака (а вот это один человек):
Для данной массы m при постоянном давлении P объем газа линейно зависит от температуры
Закон Шарля:
Для данной массы m при постоянном объеме V давление газа линейно зависит от температуры
Посмотрев на уравнение, нетрудно убедиться в справедливости этих законов.
Уравнение Менделеева-Клапейрона, также как и опытные законы Бойля-Мариотта, Гей-Люссака и Шарля справедливы для широкого интервала давлений, объемов и температур. То есть во многих случаях эти законы удобны для практического применения. Однако не стоит забывать, что когда давления превышают атмосферное в 300-400 раз, или температуры очень высоки, наблюдаются отклонения от этих законов.
Собственно, идеальный газ потому и называют идеальным, что по определению это и есть газ, для которого не существует отклонений от этих законов.
Уравнение Клапейрона-Менделеева
Что такое уравнение Клапейрона-Менделеева
Идеальный газ — это газ, в котором пренебрегают взаимодействием молекул газа между собой.
Идеальными считают разреженные газы. Особенно близкими к идеальным считают гелий и водород.
Идеальный газ — это упрощенная математическая модель, которая широко применяется для описания свойств и поведения реальных газов при атмосферном давлении и комнатной температуре.
Давление, объем и температура — это основные параметры состояния системы, и они связаны друг с другом. Соотношение, при котором определяется данная связь, называется уравнением состояния данного газа.
Существует эквивалентная макроскопическая формулировка идеального газа — это такой газ, который одновременно будет подчиняться закону Бойля-Мариотта и Гей-Люссака, то есть:
p V = c o n s t * T
В представленном выше уравнении состоянии газа под const подразумевается количество молей.
Свойства классического и квазиклассического идеального газа описываются уравнением состояния идеального газа, которое называется уравнением Менделеева-Клапейрона, ниже представлена формула Менделеева-Клапейрона.
p V = m M R T = n R T , где m — масса газа, M — молярная масса газа, R = 8 , 314 Д ж / ( м о л ь * К ) — универсальная газовая постоянная, T — температура (К), n — количество молей газа.
Таким образом давление и объем прямо пропорциональны количеству молей и температуре.
Также уравнение Клапейрона-Менделеева можно записать в ином виде:
p V = N k T , где N — это количество молекул газа массой m , k = 1 , 38 * 10 — 23 Д ж / К — постоянная Больцмана, которая определяет «долю» газовой постоянной, приходящуюся на одну молекулу и определяется по формуле:
N = m N A M , где
N A = 6 . 02 * 10 23 м о л ь — 1 ; — это постоянная Авогадро.
Какое значение имеет универсальная газовая постоянная
Универсальная газовая постоянная (R) — это величина, которая является константой, численно равная работе расширения одного моля идеального газа в изобарном процессе при увеличении температуры на 1 K.
Значение данной константы находится как произведение постоянной Больцмана ( k = 1 , 38 * 10 — 23 Д ж / К ) на число Авогадро ( N A = 6 . 02 * 10 23 м о л ь — 1 ) . Таким образом универсальная газовая постоянная принимает следующее значение: R = 8 , 314 Д ж / ( м о л ь * К ) .
Постоянную Больцмана используют в формулах, описывающих изучаемое явление или поведение рассматриваемого объекта с микроскопической точки зрения, тогда как универсальная газовая постоянная более удобна при расчетах, касающихся макроскопических систем, когда число частиц задано в молях.
Связь с другими законами состояния идеального газа
С помощью уравнения состояния идеального газа можно исследовать процессы, в которых масса и один трех макропараметров (давление, температура или объем) — остаются неизменными.
Количественные зависимости между двумя параметрами газа при фиксированном третьем параметре называют газовыми законами, которые связывают эти параметры.
Изопроцессы — это термодинамические процессы, во время протекания которых количество вещества и один из макропараметров состояния: давление, объем, температура или энтропия — остается неизменным.
В зависимости от того, какой параметр остается неизменным различают разные процессы, которые выражаются законами, являющимися следствием уравнения состояния газа:
- изотермический процесс (T=const);
- изохорный процесс (V=const);
- изобарный процесс (p=const).
Изотермический процесс (T=const)
Процесс изменения состояния термодинамической системы при постоянной температуре называют изотермическим.
Для поддержания температуры газа постоянной необходимо, чтобы он мог обмениваться теплотой с большой системой — термостатом. Им может служить атмосферный воздух, если температура его заметно не меняется на протяжении всего процесса.
Согласно уравнению Клапейрона-Менделеева, в любом состоянии с неизменной температурой произведение давления газа на объем одно и то же, то есть постоянно:
Этот закон был открыт экспериментально английским ученым Бойлем и несколько позднее французским ученым Мариоттом. Именно поэтому он называется закон Бойля-Мариотта.
Закон Бойля-Мариотта справедлив для любых газов, а также для смеси газов (например, для воздуха).
Зависимость давления газа от объема при постоянной температуре изображается графической кривой — изотермой. Изотерма для различных температур представлена в координатах pV на рис.1. и представляет собой гиперболу.
Рис.1. Изотерма в pV — координатах.
Изохорный процесс (V=const)
Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.
Из уравнения состояния следует, что отношение давлений газа данной массы при постоянно объеме равно отношению его абсолютных температур:
p 1 p 2 = T 1 T 2
Газовый закон был установлен экспериментально в 1787 г. французским физиком Ж. Шарлем и носит название закона Шарля: давление данной массы газа при постоянном объеме прямо пропорционально абсолютной температуре.
Так, если в качестве одного из состояний газа выбрать состояние газа при нормальных условиях, тогда
p = p 0 T T 0 = p 0 γ T
Коэффициент γ называют температурным коэффициентом давления газа. Он одинаков для всех газов.
Зависимость давления газа от температуры при постоянном объеме изображается графически прямой, которая называется изохорой (Рис.2).
Рис.2 Изображение изохоры в pT-координатах.
Изобарный процесс (p=const)
Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным.
Из уравнения Клапейрона-Менделеева вытекает, что отношение объемов газа данной массы при постоянном давлении равно отношению его абсолютных температур.
V 1 V 2 = T 1 T 2
Если в качестве второго состояния газа выбрать состояние при нормальных условиях (нормальном атмосферном давлении, температуре таяния льда) следует:
V = V 0 T T 0 = V 0 α T
Этот газовый закон был установлен экспериментально в 1802 г французским ученым Гей-Люссаком.
Закон Гей-Люссака: объем данной массы газа при постоянном давлении прямо пропорционален абсолютной температуре.
Коэффициент α называют температурным коэффициентом объемного расширения газов.
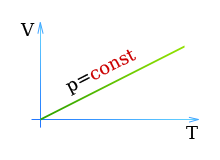
Зависимость объема газа от температуры при постоянном давлении изображается графической прямой, которая называется изобарой (Рис.3).
Рис. 3. Изобара в VT-координатах.
Использование универсального уравнения для решения задачи
В реальности проводятся различные физико-химические процессы. Рассмотрим каким образом уравнение состояния идеального газа и законы, связанные с ним находят применение для решения физических и химических задач.
Определить давление кислорода в баллоне объемом 1 м 3 при температуре t = 27 C o . Масса кислорода 1 кг.
Так как в уравнении даны объем и температура — два из трех макроскопических параметров, а третий (давление) нужно определить, то мы можем использовать уравнение Клапейрона-Менделеева:
p V = n R T = m M R T
Не забываем перевести температуру в Кельвины:
T = t + 273 = 27 + 273 = 300 K
Молярная масса кислорода известна из таблицы Менделеева:
M ( O 2 ) = 2 * 16 = 32 г / м о л ь = 32 * 10 — 3 к г / м о л ь
Выразим из уравнения состояния давления и поставим все имеющиеся данные:
p = n R T V = m R T M V = 1 * 8 . 31 * 300 32 * 10 — 3 * 1 = 77 . 906 П а = 78 к П а
Ответ: p = 78 кПа.
Каким может быть наименьший объем баллона, содержащего кислород массой 6,4 кг, если его стенки при t = 20 C o выдерживают p = 1568 Н / с м 2 ?
Используем уравнение Менделеева-Клапейрона, из которого выражаем объем кислорода, который нужно найти:
p = n R T V = m R T M V
Молярная масса кислорода предполагается равной:
M ( O 2 ) = 2 * 16 = 32 г / м 3
Не забываем перевести температуру в Кельвины:
T = t + 273 = 20 + 273 = 293 K
Переводим давление: p = 15680000 Па
Выражаем из уравнения Клапейрона-Менделеева объем и подставляем значения, данные в условиях задачи:
V = n R T p = m R T M p = 6 . 4 * 8 . 31 * 293 15680000 * 32 * 10 — 3 = 3 . 1 * 10 — 2 м 3 = 31 л .
Используя уравнение состояния идеального газа, доказать, что плотность любого газа равна половине плотности водорода ( ρ Н 2 ) , взятого при тех же условиях, умноженной на относительную молекулярную массу этого газа M_r, то есть ρ = ρ Н 2 * M r 2 .
Согласно уравнению Менделеева-Клапейрона:
p = n R T V = m R T M V
Плотность — это величина, характеризующая массу некоторого объема и находится по формуле:
ρ = m V и л и V = m ρ
Тогда p m ρ = n R T = m R T M
Откуда выражаем плотность газа:
Для водорода эта формула запишется следующим образом:
ρ H 2 = p M H 2 R T
По условию задачи водород и любой другой газ находятся при одинаковых условиях, откуда следует, что:
ρ H 2 M H 2 = p R T
Поставим последнее выражение в выражение для плотности любого газа:
ρ = M * ρ H 2 M H 2
Молярная масса водорода, исходя из таблицы Менделеева равна 2 г/моль и тогда. Молекулярная масса численно равная молярной и представляет собой массу молекулы в атомных единицах, поэтому в дальнейшем мы совершили переход к молекулярной массе.
ρ = M r * ρ H 2 2
Вывод: плотность любого газа равна половине плотности водорода ( ρ Н 2 ) , взятого при тех же условиях, умноженной на относительную молекулярную массу этого газа M_r, то есть ρ = ρ Н 2 * M r 2 .
Рассмотрим несколько задач на законы, связанные с уравнение Клапейрона-Менделеева, то есть на изотермические, изохорные, изобарные процессы.
При уменьшении давления газа в 2,5 раза его объем увеличился на 12 л. Какой объем занимал газ в начальном состоянии, если температура на протяжении всего процесса оставалась постоянной?
По условию задачи температура в ходе всего процесса оставалась постоянной, откуда следует, что у нас изотермический процесс, и мы можем воспользоваться для решения законом Бойля-Мариотта.
p 1 V 1 = p 2 V 2 , г д е p 1 – давление газа в начальном состоянии (до расширения), V 1 — объем газа в начальном состоянии, p 2 = p 1 2 . 5 — давление газа в конечном состоянии (после расширения), V 2 = V 1 + ∆ V — объем газа в конечном состоянии.
Откуда можем найти начальный объем:
p 1 V 1 = p 1 2 . 5 ( V 1 + ∆ V ) = p 1 2 . 5 V 1 + p 1 2 . 5 ∆ V
V 1 ( p 1 — p 1 2 . 5 ) = p 1 2 . 5 ∆ V
p 1 2 . 5 V 1 ( 2 . 5 — 1 ) = p 1 2 . 5 ∆ V
V 1 = ∆ V 1 , 5 = 8 л
Ответ: первоначальный объем газа был равен 8 л.
Газ находится в баллоне при температуре 400 К. До какой температуры нужно нагреть газ, чтобы его давление увеличилось в 1,5 раза?
Так как нагревание газа по условиям данной задачи происходит при постоянном объеме, значит перед нами изохорный процесс.
При изохорном процессе:
p 1 T 1 = p 2 T 2
T 2 = p 2 T 1 p 1
p 2 p 1 = 1 . 5 T 2 = 1 . 5 * T 1 = 1 . 5 * 400 = 600 K
При 27°C объем газа равен 600 мл. Какой объем займет газ при 57°C, если давление будет оставаться постоянным?
Так как давление по условию остается постоянным, то можем использовать закон Гей-Люссака.
V 1 V 2 = T 1 T 2
V_2 – искомый объем
Для правильного расчета необходимо перевести температуры из Цельсий в Кельвины:
T 1 = 273 + 27 = 300 K
T 2 = 273 + 57 = 330 K
T 2 V 1 T 1 = V 2
V 2 = ( 600 * 330 ) / 300 = 660 м л
Газ в трубе плавильной печи охлаждается от температуры t 1 = 1150 ° С д о t 2 = 200 ° С . Во сколько раз увеличивается плотность газа при этом? Давление газа не меняется.
Так как по условию задания давления газа не изменяется, значит перед нами изобарный процесс. Для решения воспользуемся законом Гей-Люссака:
V 1 V 2 = T 1 T 2
Перейдем к абсолютной температуре:
T 1 = 1150 + 273 = 1423 K
T 2 = 200 + 273 = 473 K
Масса газа: m = ρ 1 V 1 = ρ 2 V 2
Использование этих формул приводит к следующему:
http://planetcalc.ru/4265/
http://wika.tutoronline.ru/fizika/class/10/uravnenie-klapejronamendeleeva