Определите, какие элементы имеют в основном состоянии одинаковое количество неспаренных электронов. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Спрятать решение
Решение.
Выпишем валентные электроны в атоме каждого из элементов:
1. — 3d54s1.
2. — 3s23p2.
3. — 3d14s2.
4. — 2s22p4.
5. — 2s22p3.
Чтобы определить, сколько неспаренных электронов в основном состоянии имеет элемент, нужно знать как заполняются электронные слои. Если одну орбиталь занимает один электрон, то он называется неспаренным, а если на одной орбитали два электрона, то их называют спаренными.
Рассмотрим элементы, находящиеся в главных подруппах — кремний, кислород, азот. На p-подуровне — 3 орбитали, на одной орбитали располагается два электрона, всего 6 электронов на подуровне: электроны вначале заполняют каждую из орбиталей по одному. Соответственно, у азота — 3 неспаренных электрона, у кремния и кислорода — 2 неспаренных электрона.
Ответ: 24.
Мы знаем,что у элементов в главной подгруппе число электронов на внешнем уровне равно номеру группы в которой они расположены.
Например Li стоит в первой группе главной подгруппы. Число электронов на внешнем уровне у него равно одному.
Чтобы понять сколько именно неспаренных, нужно знать как именно заполняются электронные слои
На первом всегда два
На втором уже восемь
А на следующем уже 18
У Li всего один электрон на внешнем, мы сразу понимаем что он не спарен.
Также можно изобразить графическую или электронную формулы на которых мы сможем просто посчитать кол. эл.
Например из формул для Al, мы видим, что на внешнем уровне у него три электрона и один из них не спарен.(если рассматривать графическую то намного проше, если электронную, надо смотреть на последнее значение)
Таким образом можно узнать к каждому элементу число его не спаренных эл.
Также в задании у Вас есть такой ионн как Br+7 .
Если у него + значит мы должны убрать эл.(именно столько, сколько стоит после знака+)
Если у него — то добавляем.
(Не стоит путать с балансом в окислительно — восстановительных задачах)
Так у
Br+7 не 45 электронов, а всего 28
и его электронная формула
1s2 2s2 2p6 3s2 sp6 sd10 4s0 4p0 и из нее мы понимаем, что у него нет не спаренных эл.
Теперь N и С
N
1s 22s 22p 3 — 3 не спаренных
(обращаем внимание на последние значения)
С
1s 22s 22p 2 -2 не спаренных
Таким образом
Ответ: Li и Al ( по одному не спаренному эл. у каждого)
Если помог нажми кнопку Спасибо))
Для начала запишем электронные формулы для каждого элемента.
1. Cs — 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^10 4p^6 5s^2 4d^10 5p^6 6s^1. В данном случае получается всего 1 неспаренный электрон.
-
C — 1s^2 2s^2 2p^2. В С 2 неспаренных электрона, что удовлетворяет условию задания.
-
O — 1s^2 2s^2 2p^4 В кислороде два неспаренных электрона. Подходит.
4. Cr — 1s^2 2s^2 2p^6 3s^2 3p^6 4s^1 3d^5. В данном варианты получается 6 неспаренных электронов — не подходит.
- N — 1s^2 2s^2 2p^3. Получается три неспаренных электрона. Не устраивает.
В ответе необходимо указать: 23.
Из представленного ряда р-элементами являются кислород, азот и углерод.
Атомный радиус уменьшается вверх по группе и вправо по периоду.
В ответе необходимо указать следующую последовательность: С, N, O или 253.
Рассмотрим степени окисления для каждого из элементов.
Cs. Наивысшая степень окисления равна +1, наименьшая — 0. Разность равна: 1.
C. Наивысшая +4, наименьшая — 4. Разность: +4 — (-4) = 8.
O. Наивысшая +2, а наименьшая равна -2. Разность: 2 — (-2) = 4.
Cr. Наивысшая степень равна +6, наименьшая 0. Разность: 6.
N. Наивысшая +5, а наименьшая степень равняется -3. Разность: +5 — (-3) = 8.
В ответе необходимо указать комбинацию цифр: 25.
Как найти одинаковое число неспаренных электронов на внешнем уровне в основном состоянии?
1)Li 2)Br + 7 3)N 4)C 5)Al.
Вопрос Как найти одинаковое число неспаренных электронов на внешнем уровне в основном состоянии?, расположенный на этой странице сайта, относится к
категории Химия и соответствует программе для 10 — 11 классов. Если
ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска
похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему.
Для этого ключевые фразы введите в строку поиска, нажав на кнопку,
расположенную вверху страницы. Воспользуйтесь также подсказками посетителей,
оставившими комментарии под вопросом.
Атомно-молекулярное учение
Мы приступаем к изучению химии — мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными
формулами элементов.
Атом (греч. а — отриц. частица + tomos — отдел, греч. atomos — неделимый) — электронейтральная частица вещества микроскопических
размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом

Протон (греч. protos — первый) — положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов
элементов. Нейтрон (лат. neuter — ни тот, ни другой) — нейтральная (0) элементарная частица, присутствующая в ядрах всех
химических элементов, кроме водорода.
Электрон (греч. elektron — янтарь) — стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома —
порядковый номер в таблице Менделеева — равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20)
в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило:
порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим
электроны занимают различные энергетические уровни.
Энергетические уровни подразделяются на несколько подуровней:
- Первый уровень
- Второй уровень
- Третий уровень
- Четвертый уровень
Состоит из s-подуровня: одной «1s» ячейки, в которой помещаются 2 электрона (заполненный электронами — 1s2)
Состоит из s-подуровня: одной «s» ячейки (2s2) и p-подуровня: трех «p» ячеек (2p6), на которых
помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s2), p-подуровня: трех «p» ячеек (3p6) и d-подуровня:
пяти «d» ячеек (3d10), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s2), p-подуровня: трех «p» ячеек (4p6), d-подуровня:
пяти «d» ячеек (4d10) и f-подуровня: семи «f» ячеек (4f14), на которых помещается 14
электронов

Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число
электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а
также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или
атомным орбиталям, движутся электроны, создавая определенный «рисунок».
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь — клеверный лист.

Правила заполнения электронных орбиталей и примеры
Существует ряд правил, которые применяют при составлении электронных конфигураций атомов:
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной «ячейке») не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются
еще одним электроном с противоположным направлением - Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было
бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и
серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода — 6, у серы — 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.

Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил.
А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся
одним электроном дополнили первую ячейку.
Таким образом, электронные конфигурации наших элементов:
- Углерод — 1s22s22p2
- Серы — 1s22s22p63s23p4
Внешний уровень и валентные электроны
Количество электронов на внешнем (валентном) уровне — это число электронов на наивысшем энергетическом уровне, которого достигает элемент. Такие электроны называются валентными: они могут быть спаренными или неспаренными. Иногда
для наглядного представления конфигурацию внешнего уровня записывают отдельно:
- Углерод — 2s22p2 (4 валентных электрона)
- Сера -3s23p4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью — способностью атомов образовывать определенное число химических связей.

- Углерод — 2s22p2 (2 неспаренных валентных электрона)
- Сера -3s23p4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных
электронов. Ниже будет дано наглядное объяснение этой задаче.

Запишем получившиеся электронные конфигурации магния и скандия:
- Магний — 1s22s22p63s2
- Скандий — 1s22s22p63s23p64s23d1
В целом несложная и интересная тема электронных конфигураций отягощена небольшим исключением — провалом электрона, которое только подтверждает общее
правило: любая система стремится занять наименее энергозатратное состояние.
Провал электрона
Провалом электрона называют переход электрона с внешнего, более высокого энергетического уровня, на предвнешний, энергетически более
низкий. Это связано с большей энергетической устойчивостью получающихся при этом электронных конфигураций.
Подобное явление характерно лишь для некоторых элементов: медь, хром, серебро, золото, молибден. Для примера выберем хром, и рассмотрим
две электронных конфигурации: первую «неправильную» (сделаем вид, будто мы не знаем про провал электрона) и вторую правильную, написанную
с учетом провала электрона.
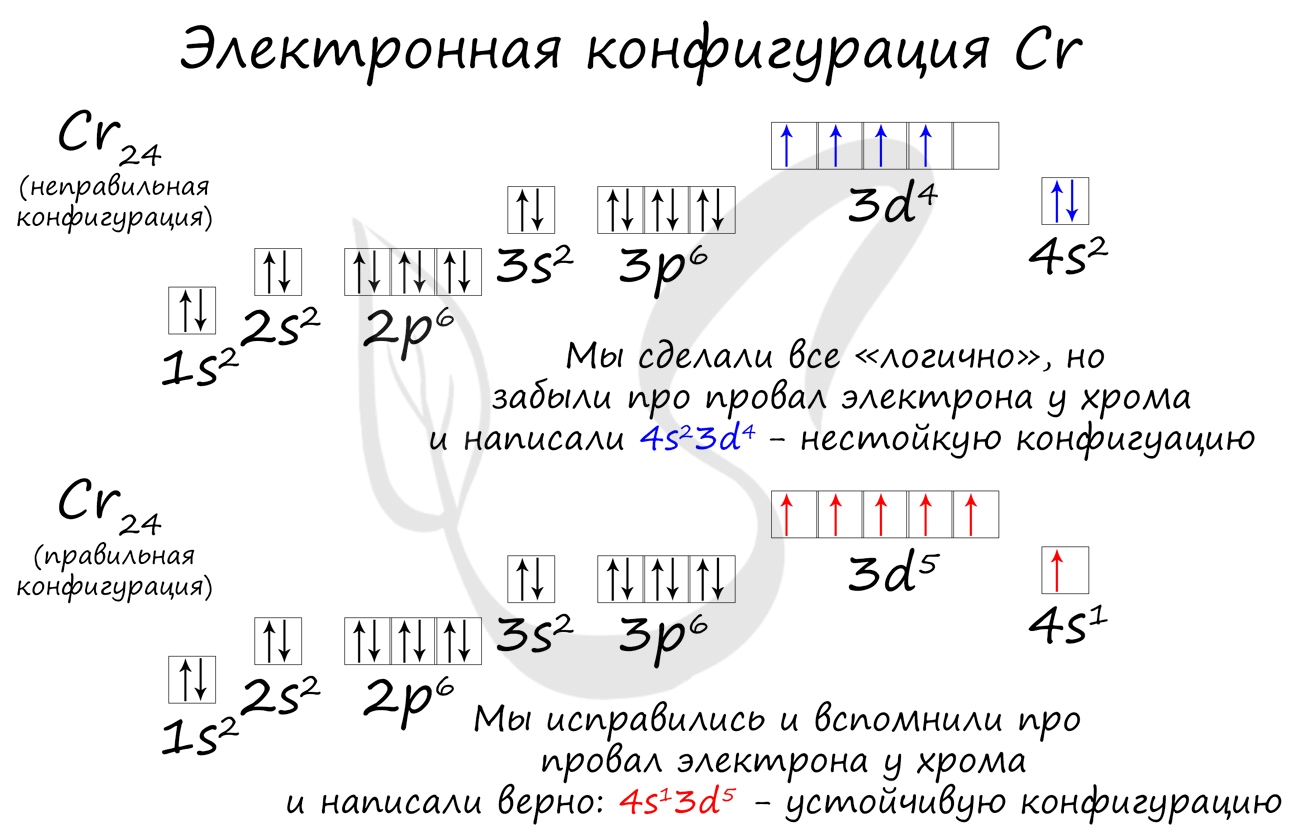
Теперь вы понимаете, что кроется под явлением провала электрона. Запишите электронные конфигурации хрома и меди самостоятельно еще раз и
сверьте с представленными ниже.

Основное и возбужденное состояние атома
Основное и возбужденное состояние атома отражаются на электронных конфигурациях. Возбужденное состояние связано с движением электронов
относительно атомных ядер. Говоря проще: при возбуждении пары электронов распариваются и занимают новые ячейки.
Возбужденное состояние является для атома нестабильным, поэтому долгое время в нем он пребывать не может. У некоторых атомов: азота,
кислорода , фтора — возбужденное состояние невозможно, так как отсутствуют свободные орбитали («ячейки») — электронам некуда перескакивать, к тому
же d-орбиталь у них отсутствует (они во втором периоде).
У серы возможно возбужденное состояние, так как она имеет свободную d-орбиталь, куда могут перескочить электроны. Четвертый энергетический
уровень отсутствует, поэтому, минуя 4s-подуровень, заполняем распаренными электронами 3d-подуровень.
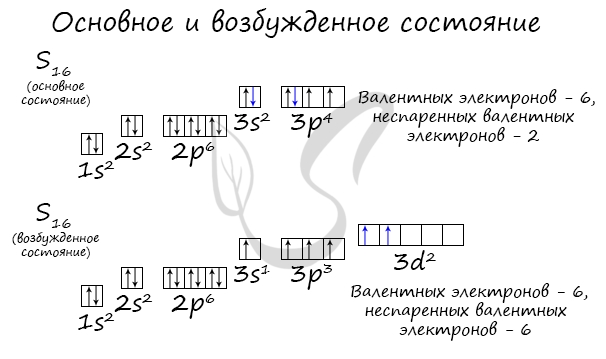
По мере изучения основ общей химии мы еще не раз вернемся к этой теме, однако хорошо, если вы уже сейчас запомните, что возбужденное состояние
связано с распаривание электронных пар.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.




