Рассчитать относительную плотность водорода по воздуха
Получи верный ответ на вопрос 🏆 «Рассчитать относительную плотность водорода по воздуха …» по предмету 📕 Химия, используя встроенную систему поиска. Наша обширная база готовых ответов поможет тебе получить необходимые сведения!
Найти готовые ответы
Главная » Химия » Рассчитать относительную плотность водорода по воздуха
Относительная плотность по… задачи
24-Фев-2013 | комментариев 26 | Лолита Окольнова
В ЕГЭ иногда встречаются задачи (часть С последнее задание), где в условии дана относительная плотность вещества по… водороду, кислороду, воздуху, азоту и т.д.
Например:
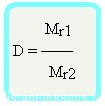
Относительная плотность вещества – отношение плотности вещества Б к плотности вещества А
Относительная плотность — величина безразмерная
Формула достаточно простая, и из нее вытекает другая формула —
Формула молярной массы вещества
Mr1 = D•Mr2
- Если дана относительная плотность паров по водороду, то Mr (вещества)=Mr(H2)•D=2 гмоль • D;
- если дана относительная плотность по воздуху, то Mr (вещества)=Mr(воздуха)•D=29 гмоль • D (обратите внимание, Mr(воздуха) принята равной 29 гмоль);
и т.д.
В условии задачи может быть полная формулировка — «относительная плотность (паров)…», а может быть просто «плотность вещества по…»
Давайте решим нашу задачу:
Дана плотность паров вещества по воздуху, значит, нам подходит формула молярной массы вещества —
Mr (вещества)=Mr(воздуха)•D=29 гмоль • D
Mr(вещества)=29 гмоль • 1.448 = 42 гмоль
Нам дан углеводород — СхHy, значит, мы можем найти Mr(Cx и Mr(Hy). Обратите внимание, именно молярные массы, т.к.у нас несколько атомов углерода и водорода.
Для этого надо молярную массу вещества умножить на процентное содержание элемента:
Mr(Cx)=Mr(вещества)•ω
Mr(Cx)= 42 гмоль · 0.8571=36 гмоль
x=Mr(Cx)Ar(C)=36 гмоль ÷ 12 гмоль =3.
Точно так же находим все данные для водорода:
Mr(Hy)=Mr(вещества)•ω
Mr(Hy)= 42 гмоль · 0.1429=6 гмоль
x=Mr(Hy)Ar(H)=6 гмоль ÷ 1 гмоль =6.
Искомое вещество — C3H6 — пропен.
Еще раз повторим определение —
Относительная плотность газа – это сравнение молярной или относительной молекулярной массы одного газа с аналогичным показателем другого газа.
Дана относительная плотность по аргону.
Mr (вещества)=Ar(Ar)•D
Mr (CxHy)=40 гмоль ·1.05=42 гмоль
Запишем уравнение горения:
СхHy + O2 = xCO2 + y2H2O
Найдем количество углекислого газа и воды:
n(CO2)=V22,4 лмоль = 33.622.4=1.5
n(H2O)=mMr=2718=1.5
Соотношение х : y2 как 1.5 : 1.5, т.е. y=2x, что соответствует общей формуле алкенов: CnH2n
Выражаем в общем виде молярную массу: Mr=Mr(C) + Mr(H)
12n +2n=42
n=3
Наше вещество — C3H6 — пропен
- pадание ЕГЭ по этой теме — задачи С5
Обсуждение: «Относительная плотность по… задачи»
(Правила комментирования)
Перейти к содержанию
Таблица: относительные плотности газов по воздуху по водороду
На чтение 3 мин Просмотров 1.2к. Опубликовано
Относительная плотность или удельный вес – это отношение плотности (масса единицы объема) вещества к плотности данного справочный материал. Удельный вес жидкостей почти всегда измеряется по отношению к воде в ее самой плотной точке (при 4 ° C или 39,2 ° F); для газов эталоном является воздух при комнатной температуре (20 ° C или 68 ° F). Термин «относительная плотность» часто используется в научных целях.

| Газ | Химическая формула | Относительная плотность газа по воздуху | Молекулярный вес | Плотность кг/м³ | Плотность футов/фут³(lb/ft³) |
| Водород / Hydrogen | H2 | 0,07 | 2.016 | 0.08992) | 0.00562) |
| Гелий / Helium | He | 0,14 | 04.фев | 0.16641) | 0.010391) |
| 0.17852) | 0.0111432) | ||||
| Светильный газ угольный газ (горючий газ, состоящий из 20-30% метана и 50% водорода получаемый из каменного угля в процессе его полукоксования и частичного термического крекинга / Coal gas | 0,45 | 0.5802) | |||
| Пригодный газ = натуральный газ / Natural gas | 0,55-0,70 | 19.май | 0.7 – 0.92) | 0.044 – 0.0562) | |
| Метан / Methane | CH4 | 0,56 | 16.043 | 0.6681) | 0.04171) |
| 0.7172) | 0.04472) | ||||
| Аммиак / Ammonia | NH3 | 0,6 | 17.031 | 0.7171) | 0.04481) |
| 0.7692) | 0.04802) | ||||
| Водяной пар / Water Vapor, steam | H2O | 0,67 | 18.016 | 0.804 | 0.048 |
| Неон / Neon | Ne | 0,7 | 20.179 | 0.89992) | 0.0561792) |
| Продукты сгорания = смесь продуктов полного сгорания в виде CO2, Н2О, SO2 и золы + неполного сгорания в виде СО, Н2, и др., а также азота и кислорода / Combustion products | 0,86 | 1.112) | 0.0692) | ||
| Ацетилен = этин / Acetylene (ethyne) | C2H2 | 0,91 | 26 | 1.0921) | 0.06821) |
| 1.1702) | 0.07292) | ||||
| Азот / Nitrogen | N2 | 0,97 | 28.фев | 1.1651) | 0.07271) |
| 1.25062) | 0.0780722) | ||||
| Угарный газ, моноксид углерода / Carbon monoxide | CO | 0,97 | 28.янв | 1.1651) | 0.07271) |
| 1.2502) | 0.07802) | ||||
| Этилен / Ethylene | C2H4 | 0,98 | 28.мар | 1.2602) | 0.07862) |
| Воздух / Air | 1 | 29 | 1.2051) | 0.07521) | |
| 1.2932) | 0.08062) | ||||
| Двукосиь азота / Nitric oxide | NO | 1,04 | 30.0 | 1.2491) | 0.07801) |
| Этан / Ethane | C2H6 | 1,05 | 30.июл | 1.2641) | 0.07891) |
| Кислород / Oxygen | O2 | 1,11 | 32 | 1.3311) | 0.08311) |
| 1.42902) | 0.0892102) | ||||
| Сероводород = сернистый водород / Hydrogen Sulfide | H2S | 1,19 | 34.076 | 1.4341) | 0.08951) |
| Соляная кислота = хлористый водород / Hydrochloric Acid = Hydrogen Chloride | HCl | 1,27 | 36.5 | 1.5281) | 0.09541) |
| Аргон / Argon | Ar | 1,38 | 39.948 | 1.6611) | 0.10371) |
| 1.78372) | 0.1113532) | ||||
| Пропен = пропилен / Propene (propylene) | C3H6 | 1,45 | 42.1 | 1.7481) | 0.10911) |
| Углекислый газ = двуокись углерода, диоксид углерода / Carbon dioxide | CO2 | 1,53 | 44.01 | 1.8421) | 0.11501) |
| 1.9772) | 0.12342) | ||||
| Пропан / Propane | C3H8 | 1,57 | 44.09 | 1.8821) | 0.11751) |
| Веселящий газ, закись азота / Nitrous Oxide | N2O | 1,65 | 44.013 | 1.9801) | 0.114 |
| Озон / Ozone | O3 | 1,78 | 48.0 | 2.142) | 0.125 |
| Оксид серы (II)= диоксид серы = двуокись серы = сернистый ангидрид = сернистый газ / Sulfur Dioxide | SO2 | 1,9 | 64.06 | 2.2791) | 0.17031) |
| 2.9262) | 0.18282) | ||||
| Бутилен = Бутен / Butylene (Butene) | C4H8 | 2,03 | 56.11 | 2.504 | 0.1482) |
| Бутан / Butane | C4H10 | 2,07 | 58.1 | 2.4891) | 0.15541) |
| 2.52) | 0.1562) | ||||
| Хлор / Chlorine | Cl2 | 2,49 | 70.906 | 2.9941) | 0.18691) |
| Бензол / Benzene | C6H6 | 2,9 | 78.11 | 3.486 | 0.20643 |
| Криптон / Krypton | Kr | 2,9 | 83,8 | 3.742) | |
| Метилбензол = толуол / Toluene | C7H8 | 3,42 | 92.141 | 4.111 | 0.2435 |
| Ксенон / Xenon | Xe | 4,54 | 131,293 | 5.862) |
1) NTP – Нормальная температура и давление (Normal Temperature and Pressure) – 20oC (293.15 K, 68oF) при 1 атм ( 101.325 кН/м2, 101.325 кПа, 14.7 psia, 0 psig, 30 in Hg, 760 мм.рт.ст)
2) STP – Стандартная температура и давление (Standard Temperature and Pressure) – 0oC (273.15 K, 32oF) при 1 атм (101.325 кН/м2, 101.325 кПа, 14.7 psia, 0 psig, 30 in Hg, 760 torr=мм.рт.ст)
Как вычислять относительную плотность вещества
Такая характеристика, как относительная плотность вещества, показывает, во сколько раз оно тяжелее или легче другого соединения. Этот параметр можно определять по отношению к любому газообразному веществу. В большинстве случаев проводятся расчеты относительно воздуха или водорода. Однако могут попадаться задания, в которых необходимо вычислить относительную плотность и по другим газам, таким как кислород, аммиак или сероводород. В любом случае принцип решения задания един.

Вам понадобится
- — периодическая система химических элементов Д.И. Менделеева;
- — калькулятор.
Инструкция
Для того чтобы справиться с задачей, необходимо использовать формулы на определение относительной плотности:
D (воздух) = Mr (газа)/ Mr (воздуха), где:
D (воздух) – относительная плотность;
Mr (газа) – относительная молекулярная масса газообразного вещества;
Mr (воздуха) — относительная молекулярная масса воздуха.
Все три параметра единиц измерения не имеют.
Mr (воздуха) = 29 (величина постоянная), следовательно формула будет иметь вид:
D (воздух) = Mr (газа)/ 29.
По аналогии выглядит формула на определение относительной плотности по водороду, с тем исключением, что вместо воздуха стоит водород. А значит, и в расчет берется относительная молекулярная масса водорода.
D (водород) = Mr (газа)/ Mr (водорода);
D (водород) – относительная плотность;
Mr (газа) – относительная молекулярная масса газообразного вещества;
Mr (водорода) — относительная молекулярная масса водорода.
Mr (водорода) = 2, следовательно и формула будет иметь вид:
D (воздух) = Mr (газа)/ 2.
Пример № 1. Вычислите относительную плотность аммиака по воздуху. Аммиак имеет формулу NH3.
Сначала найдите относительную молекулярную массу аммиака, которую можно рассчитать по таблице Д.И. Менделеева.
Ar (N) = 14, Ar (H) = 3 х 1 = 3, отсюда
Mr (NH3) = 14 + 3 = 17
Подставьте полученные данные в формулу на определение относительной плотности по воздуху:
D (воздух) = Mr (аммиака)/ Mr (воздуха);
D (воздух) = Mr (аммиака)/ 29;
D (воздух) = 17/ 29 = 0, 59.
Пример № 2. Вычислите относительную плотность аммиака по водороду.
Подставьте данные в формулу на определение относительной плотности по водороду:
D (водород) = Mr (аммиака)/ Mr (водорода);
D (водород) = Mr (аммиака)/ 2;
D (водород) = 17/ 2 = 8, 5.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,662 -
гуманитарные
33,654 -
юридические
17,917 -
школьный раздел
611,978 -
разное
16,905
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.