Относительная плотность по… задачи
24-Фев-2013 | комментариев 26 | Лолита Окольнова
В ЕГЭ иногда встречаются задачи (часть С последнее задание), где в условии дана относительная плотность вещества по… водороду, кислороду, воздуху, азоту и т.д.
Например:
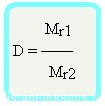
Относительная плотность вещества – отношение плотности вещества Б к плотности вещества А
Относительная плотность — величина безразмерная
Формула достаточно простая, и из нее вытекает другая формула —
Формула молярной массы вещества
Mr1 = D•Mr2
- Если дана относительная плотность паров по водороду, то Mr (вещества)=Mr(H2)•D=2 гмоль • D;
- если дана относительная плотность по воздуху, то Mr (вещества)=Mr(воздуха)•D=29 гмоль • D (обратите внимание, Mr(воздуха) принята равной 29 гмоль);
и т.д.
В условии задачи может быть полная формулировка — «относительная плотность (паров)…», а может быть просто «плотность вещества по…»
Давайте решим нашу задачу:
Дана плотность паров вещества по воздуху, значит, нам подходит формула молярной массы вещества —
Mr (вещества)=Mr(воздуха)•D=29 гмоль • D
Mr(вещества)=29 гмоль • 1.448 = 42 гмоль
Нам дан углеводород — СхHy, значит, мы можем найти Mr(Cx и Mr(Hy). Обратите внимание, именно молярные массы, т.к.у нас несколько атомов углерода и водорода.
Для этого надо молярную массу вещества умножить на процентное содержание элемента:
Mr(Cx)=Mr(вещества)•ω
Mr(Cx)= 42 гмоль · 0.8571=36 гмоль
x=Mr(Cx)Ar(C)=36 гмоль ÷ 12 гмоль =3.
Точно так же находим все данные для водорода:
Mr(Hy)=Mr(вещества)•ω
Mr(Hy)= 42 гмоль · 0.1429=6 гмоль
x=Mr(Hy)Ar(H)=6 гмоль ÷ 1 гмоль =6.
Искомое вещество — C3H6 — пропен.
Еще раз повторим определение —
Относительная плотность газа – это сравнение молярной или относительной молекулярной массы одного газа с аналогичным показателем другого газа.
Дана относительная плотность по аргону.
Mr (вещества)=Ar(Ar)•D
Mr (CxHy)=40 гмоль ·1.05=42 гмоль
Запишем уравнение горения:
СхHy + O2 = xCO2 + y2H2O
Найдем количество углекислого газа и воды:
n(CO2)=V22,4 лмоль = 33.622.4=1.5
n(H2O)=mMr=2718=1.5
Соотношение х : y2 как 1.5 : 1.5, т.е. y=2x, что соответствует общей формуле алкенов: CnH2n
Выражаем в общем виде молярную массу: Mr=Mr(C) + Mr(H)
12n +2n=42
n=3
Наше вещество — C3H6 — пропен
- pадание ЕГЭ по этой теме — задачи С5
Обсуждение: «Относительная плотность по… задачи»
(Правила комментирования)
Азот – химический элемент периодической системы, обозначающийся буквой N и имеющий порядковый номер 7. Существует в виде молекулы N2, состоящей из двух атомов. Это химическое вещество представляет собой бесцветный, без запаха и без вкуса газ, он является инертным при стандартных условиях. Плотность азота при нормальных условиях (при 0 °C и давлении 101,3 кПа) равна 1,251 г/дм3. Элемент входит в состав атмосферы Земли в количестве 78,09 % от ее объема. Впервые был обнаружен как компонент воздуха шотландским врачом Даниэлем Резерфордом в 1772 году.
Жидкий азот является криогенной жидкостью. При атмосферном давлении он кипит при температуре – 195,8 °C. Поэтому его можно хранить только в изолированных сосудах, которыми являются стальные баллоны для сжиженных газов или сосуды Дюара. Только в этом случае его можно хранить или транспортировать без особых потерь из-за испарения. Как и сухой лед (сжиженный углекислый газ, иначе называемый углекислота), жидкий азот используется в качестве хладагента. Кроме того, его применяют для криоконсервации крови, половых клеток (сперматозоидов и яйцеклеток), а также других биологических образцов и материалов. Он востребован и в клинической практике, например, в криотерапии при удалении кисты и бородавок на коже. Плотность жидкого азота равняется 0,808 г/см3.
Многие промышленно важные соединения, такие, как азотная кислота, аммиак, органические нитраты (взрывчатые вещества, топливо) и цианиды, содержат N2. Чрезвычайно сильные связи элементарного азота в молекуле вызывают трудности для участия его в химических реакциях, этим объясняется его инертность при стандартных условиях (температуре и давлении). В том числе и по этим причинам N2 имеет большое значение во многих научных и производственных сферах. Например, он необходим для поддержания внутрипластового давления при добыче нефти или газа. Любое его практическое или научное применений требует знать, какова будет плотность азота при конкретном давлении и температуре. Из законов физики и термодинамики известно, что при постоянном объеме с ростом температуры будет расти давление и плотность газа, и наоборот.
Когда и зачем нужно знать плотность азота? Расчет этого показателя применяется при проектировании технологических процессов, протекающих с применением N2, в лабораторной практике и на производстве. Используя известное значение плотности газа, можно рассчитать его массу в определенном объеме. Например, известно, что газ занимает при нормальных условиях объем 20 дм3. В этом случае можно рассчитать его массу: m = 20 • 1,251 = 25,02 г. Если условия отличные от стандартных, и известен объем N2 при этих условиях, то потребуется сначала найти (по справочникам) плотность азота при определенном давлении и температуре, а затем эту величину умножить на объем, занимаемый газом.
Подобные расчеты проводят на производстве при составлении материальных балансов технологических установок. Они необходимы для ведения технологических процессов, выбора контрольно-измерительных приборов, расчета технико-экономических показателей и прочее. Например, после остановки химического производства все аппараты и трубопроводы должны перед их вскрытием и выводом в ремонт продуваться инертным газом – азотом (он самый дешевый и наиболее доступный по сравнению, например, с гелием или аргоном). Как правило, они продуваются таким количеством N2, который в несколько раз превышает объем аппаратов или трубопроводов, только так можно удалить из системы горючие газы и пары и исключить взрыв или пожар. Планируя операции перед остановочным ремонтом, технолог, зная объем опорожняемой системы и плотность азота, рассчитывает массу N2, которая потребуется для продувки.
Для упрощенных расчетов, не требующих точности, реальные газы приравнивают к идеальным газам и применяют закон Авогадро. Так как масса 1 моль N2 численно равняется 28 граммам, а 1 моль любого идеального газа занимает объем 22,4 литра, то плотность азота будет равняться: 28/22,4 = 1,25 г/л = 1,25 г/дм3. Этот способ быстрого нахождения плотности применим для любого газа, а не только N2. Его часто используют в аналитических лабораториях.
Физические свойства азота
Азот — инертный двухатомный газ без цвета и запаха, химическая формула двухатомной молекулы N2, молярная масса 28,01 кг/кмоль, самый распространённый элемент на Земле. Содержание азота в атмосферном воздухе составляет около 78,09% по объёму.
Применяется в технологических процессах в качестве инертной затворной среды, например, для сухих газовых торцовых уплотнений и уплотнительных комплексов, в химической промышленности для синтеза аммиака.
Жидкий азот используется как хладагент, в машиностроении для сборки неразъемных соединений с натягом [охлаждение охватываемой детали].
Азот находит применение в специальных технологических процессах для нанесения на поверхности стальных деталей тонкого слоя износостойкого покрытия — нитрида титана; в соединении с кремнием образует износостойкий перспективный керамический материал нитрид кремния Si3N4.
Плотность азота при нормальном атмосферном давлении 101,325 кПа (1 атм) и различной температуре
| Температура азота | Плотность азота, ρ |
| оС | кг/м3 |
| -23 | 1,3488 |
| 27 | 1,1233 |
| 77 | 0,9625 |
| 127 | 0,8425 |
| 177 | 0,7485 |
| 227 | 0,6739 |
| 277 | 0,6124 |
Динамическая и кинематическая вязкость азота при нормальном атмосферном давлении и различной температуре
| Температура | Динамическая вязкость азота, μ | Кинематическая вязкость азота, ν |
| оС | (Н • c / м2) x 10-7 | (м2 / с) x 10-6 |
| -73 | 129,2 | 7,65 |
| -23 | 154,9 | 11,48 |
| 27 | 178,2 | 15,86 |
| 77 | 200,0 | 20,78 |
| 127 | 220,4 | 26,16 |
| 177 | 239,6 | 32,01 |
| 227 | 257,7 | 38,24 |
Основные физические свойства азота при различной температуре
| Температура | Плотность, ρ | Удельная теплоёмкость, Cp | Теплопроводность, λ | Кинематическая вязкость, ν | Число Прандтля, Pr |
| K | кг/м3 | Дж / (кг • К) | Вт / (м • К) | (м2 / с) x 10-6 | — |
| 200 | 1,6883 | 1043 | 0,0183 | 7,65 | 0,736 |
| 300 | 1,1233 | 1041 | 0,0259 | 15,86 | 0,716 |
| 400 | 0,8425 | 1045 | 0,0327 | 26,16 | 0,704 |
| 500 | 0,6739 | 1056 | 0,0389 | 38,24 | 0,700 |
| 600 | 0,5615 | 1075 | 0,0446 | 51,79 | 0,701 |
| 700 | 0,4812 | 1098 | 0,0499 | 66,71 | 0,706 |
* Табличные данные подготовлены по материалам зарубежных справочников
Формулы физических свойств азота
При выполнении инженерных расчетов удобнее использовать приближённые формулы для оценки физических свойств азота N2⋆:
Плотность азота N2
⋆ [ кг/м3 ]

Теплоёмкость азота N2
⋆ [ Дж/(кг • К) ]

Теплопроводность азота N2
⋆ [ Вт/(м • K) ]

Динамическая вязкость азота N2
⋆ [ Па • c ]

Кинематическая вязкость азота N2
⋆ [ м2/с ]

Температуропроводность азота N2
[ м2/с ]

Число Прандтля азота N2
[ — ]

⋆ Приближённые формулы физических свойств азота получены авторами настоящего сайта.
Размерность величин: температура — градусы Цельсия. Формула плотности азота приведена для атмосферного давления.
Приближённые формулы действительны в диапазоне температур азота от -23 до 277 oC.
Получи верный ответ на вопрос 🏆 «Вычислить следующие данные для азота а.) относительную плотность во водороду; б.) относительную плотность по воздуху; в.) массу 1 л. (при …» по предмету 📕 Химия, используя встроенную систему поиска. Наша обширная база готовых ответов поможет тебе получить необходимые сведения!
Найти готовые ответы
Главная » Химия » Вычислить следующие данные для азота а.) относительную плотность во водороду; б.) относительную плотность по воздуху; в.) массу 1 л. (при н. у.); г.) массу атома азота (в г.); д.) Обьем 1 г. (при н. у.) (в л.)
Найдите правильный ответ на вопрос ✅ «Расчитайтк плотность азота N2 при н. у. …» по предмету 📘 Химия, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Смотреть другие ответы
Главная » Химия » Расчитайтк плотность азота N2 при н. у.