Плотность – физическая характеристика, присущая твердым, жидким и газообразным веществам.
В статье рассказывается о том, что такое плотность насыщенного пара, ее зависимость от различных условий среды. Дополнительно приведена таблица плотности по температуре, формула и примеры расчета этого параметра.
Содержание
- Что это за параметр, в чем измеряется, как обозначается?
- От чего зависит?
- Как изменяется при изменении температуры?
- Таблица зависимости
- Как определить?
- Формула и правила расчета
- Несколько примеров
- Где используют знания в жизни?
- Заключение
Что это за параметр, в чем измеряется, как обозначается?
Плотностью вещества называют физическую величину, которая указывает на отношение массы к занимаемому объему. Для насыщенного пара, простыми словами, это общее количество газа на единицу занимаемого им объема.
Единицей измерения плотности является кг/м3- килограмм на кубический метр (по системе СИ) или г/см3-грамм на кубический сантиметр (по системе СГС). Обозначается данная величина буквой «p».
Плотность насыщенного пара всегда приравнивается к уровню абсолютной влажности. Связано это с тем, что для данного вида пара свойственно насыщение молекулами воды, которые и повышают плотность.
От чего зависит?
Значение плотности насыщенных паров зависит от нескольких факторов:
Температура. С ее повышением увеличивается плотность пара, так как прослеживается рост числа молекул насыщения.
-
Атмосферное давление. Чем оно выше, тем плотность меньше. Связано это с уменьшением числа свободных молекул, покидающих поверхность воды.
Также стоит учесть, что при снижении давления, плотность растет, так как снижается температура кипения, увеличивается парообразование и уровень насыщения.
- Температура внешней стенки (сосуда). Увеличивает конденсацию, снижает общую температуру жидкости, приводит к дисбалансу динамического равновесия. В следствии этих факторов, снижается плотность пара.
Также стоит учесть, что плотность насыщенного пара зависит от примесей других газов и твердых частиц в нем. Примеси снижают плотность самого пара, так как увеличивают конденсацию при сниженном уровне насыщения.
Как изменяется при изменении температуры?
Плотность насыщенного пара прямо зависит от температуры:
- При понижении температуры прослеживается уменьшение плотности. Связано это с тем, что замедляется процесс парообразования и насыщения пара. Молекулы воды теряют энергию и скорость выхода с поверхности воды, а значит перестают насыщать пар.
- При увеличении температуры плотность растет прямо пропорционально. Связано это с увеличением скорости насыщения среды до уровня 100%. При достижении этого уровня, наступает фазовый переход из газообразного состояния в жидкое (конденсация). Фазовый переход обусловлен термодинамическим равновесием между паром и водой. При таком условии, плотность стабилизируется без дальнейшего роста.
Рост и стабилизация плотности с увеличением температуры возможна только до температуры кипения воды. Дальнейший нагрев снижает плотность, так как выпаривает молекулы воды из пара, делая его перегретым.
Таблица зависимости
Зависимость плотности от температуры легко проследить по приведенной таблице:
| Температура °С | Плотность г/м3 |
| -30 | 0,3 |
| -20 | 0,8 |
| -10 | 2,1 |
| -5 | 3,6 |
| 0 | 4,8 |
| 3 | 6 |
| 4 | 6,4 |
| 5 | 6,8 |
| 10 | 9,4 |
| 11 | 10 |
| 12 | 10,6 |
| 13 | 11,3 |
| 14 | 12 |
| 15 | 12,8 |
| 16 | 13,6 |
| 17 | 14,4 |
| 18 | 15,3 |
| 19 | 16,3 |
| 20 | 17,3 |
| 21 | 18,3 |
| 22 | 19,4 |
| 23 | 20 |
| 24 | 21,7 |
| 25 | 23 |
| 30 | 30,4 |
| 35 | 39,6 |
| 40 | 51,2 |
| 45 | 65,4 |
| 50 | 82,8 |
| 55 | 104 |
| 60 | 129 |
| 65 | 160 |
| 70 | 196,4 |
| 75 | 239,3 |
| 80 | 289,7 |
| 85 | 348,7 |
| 90 | 417,3 |
| 95 | 496,4 |
| при 100 градусах Цельсия | 588,5 |
По таблице можно проследить рост плотности от отрицательной к положительной температуре.
Увеличение связано с ростом количества свободных молекул воды, насыщающих пар. При отрицательной температуре низкая плотность связана с кристаллизацией молекул воды и отсутствием конденсации.
Как определить?
Рассмотрим, как рассчитать параметр.
Формула и правила расчета
Для вычисления плотности вещества используется формула:
Выражение состоит из следующих значений:
- «p» — плотность вещества;
- «F» — абсолютная влажность воздуха (г/м3);
- «m» — его масса (грамм-килограмм);
- «V» — занимаемый объем (см3-м3).
Так как у насыщенного пара плотность связана с уровнем влажности, то данный параметр может быть рассчитан с использованием выражения:
Уравнение состоит из:
- «ф» — абсолютная влажность;
- «p» — плотность пара;
- «pо» — плотность насыщения;
- «100%» — относительная влажность.
При использовании формулы стоит учитывать зависимость плотности от температуры и использовать табличные значения этого параметра.
Несколько примеров
Формулу расчета плотности очень просто использовать для решения задач.
Задача:
- Масса водяного пара 250 г.
- Объем пара 300 м3.
- Плотность неизвестна.
Решение:
- P=m/v=грамм/м3.
- P=250/300=0,83 г/м3.
Ответ: плотность насыщенного пара, массой 250 г и объемом 300 м3 составляет 0,83 г/м3.
Задача:
- Масса водяного пара 700 г.
- Объем пара 150 м3.
- Плотность пара в кг/м3 неизвестна.
Решение:
- P=m/v=грамм/м3.
- P=700/150=4,66 г/м3 или 0,0046 кг/м3.
Ответ: плотность насыщенного пара массой 700 г и объемом 150 м3 составляет 0,0046 кг/м3
Где используют знания в жизни?

Метеорологи применяют расчет плотности для установления уровня насыщения атмосферы влагой.
Также расчет помогает контролировать испарения естественных источников в разные периоды года и устанавливать скорость испарения при различных температурах.
Инженеры применяют данные знания при проектировании:
- отопительных и охладительных систем,
- вентиляции,
- очистительного оборудования.
Плотность помогает рассчитать оптимальный уровень насыщения системы влагой.
Заключение
Плотность насыщенного пара имеет прямую зависимость от температуры, давления и наличия термодинамического равновесия с исходной водой.
Такая зависимость позволяет рассчитать климатические изменения в разный период, а также решить множество задач при проектировании климатических систем.
Как определить плотность насыщенного пара
Для насыщенного пара над жидкостью справедливо уравнение Менделеева-Клапейрона. Поэтому, зная температуру, можно рассчитать плотность насыщенного пара. Она увеличивается с повышением температуры и не зависит от объема жидкости.

Вам понадобится
- — бумага;
- — калькулятор;
- — ручка;
- — давление газа (из условия задачи или в таблице);
- — температура, при которой нужно определить плотность
- — периодическая таблица Менделеева.
Инструкция
Запишите на бумаге уравнение Менделеева-Клапейрона для идеальных газов: PV=(m/M)RT . Его можно использовать и для насыщенного пара, но как только плотность газа становится сравнимой с плотностью насыщенного пара, данное уравнение нельзя использовать в расчете – оно покажет неверный результат. Другим газовым законам насыщенный пар не подчиняется.
Из записанного уравнения выведите плотность насыщенного пара. Она равна массе, деленной на объем. Поэтому уравнение преобразуется: P= (p нас. пара/M)RT. Отсюда можно записать формулу для нахождения плотности насыщенного пара: p= PM/RT . Здесь P – это давление газа. Его табличное значение обычно дается в условии задачи и зависит от температуры. Если не дано, то найдите в таблице для вашей температуры. R – это универсальная газовая постоянная, равна 8,31 Дж/(К*моль).
Если вам известна температура в градусах Цельсия, то переведите ее в градусы Кельвина (обозначается К). Для этого прибавьте 273 к известной температуре, так как -273 – это абсолютный ноль по шкале Кельвина.
Найдите молярную массу жидкости M. Ее можно рассчитать с помощью периодической таблицы Менделеева. Молярная масса вещества численно равна молекулярной. Найдите в таблице значения атомных масс всех элементов, содержащихся в веществе, и умножьте на количество соответствующих атомов в молекуле. Сумма полученных значений даст молекулярную массу вещества.
Подставьте в последнее выражение все известные значения. Давление P нужно подставлять в Па. Если по условию дано в кПа, то умножьте его на 1000. Молярную массу при подстановке переведите в кг/моль (разделите на 1000), так как в периодической таблице она дана в г/моль. С помощью калькулятора рассчитайте значение плотности насыщенного пара. Результат получается в кг/м3.
Источники:
- плотность пара
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Обновлено: 29.05.2023
Плотность насыщенного пара и другие его физические свойства
Пар – это газообразное состояние вещества. Особенность такого состояния заключается в том, что здесь газовая фаза вещества находится в равновесии с жидкой или твердой фазами того же вещества.
Процесс образования пара из жидкой или твердой фазы называют парообразованием. В случае, если пар образует противоположным путем, то процесс носит название конденсация.
Различают два вида состояний пара химических соединений, не содержащих примесные компоненты:
— пар ненасыщенный, т.е. пар, который пока не находится в состоянии динамического равновесия с жидкостью. Если на поверхности жидкости находится ненасыщенный пар, то процесс парообразования преобладает над процессом конденсации. Именно поэтомув данном случае объем жидкости в сосуде будет постепенно уменьшаться.
— пар насыщенный, т.е. пар, который находится в динамическом равновесии с жидкостью, что по-простому означает следующее: ни один из процессов – парообразование или конденсация не преобладает один над другим. Если объем фиксирован, а температура одинакова в двух случаях, тов данном сосуде не будет находиться больше пара, чем изначально. Данное равновесие можно нарушить, если сжимать пар, находящийся над жидкостью при помощи поршня: конденсация станет преобладать над парообразованием. Стоит помнить, что данный процесс – явление временное и он будет продолжаться до тех пор, пока динамическое равновесие снова не установится.
Время установления динамического равновесия между паром и жидкостью значительно зависит от плотности пара, что связано с различием сил межмолекулярного взаимодействия.
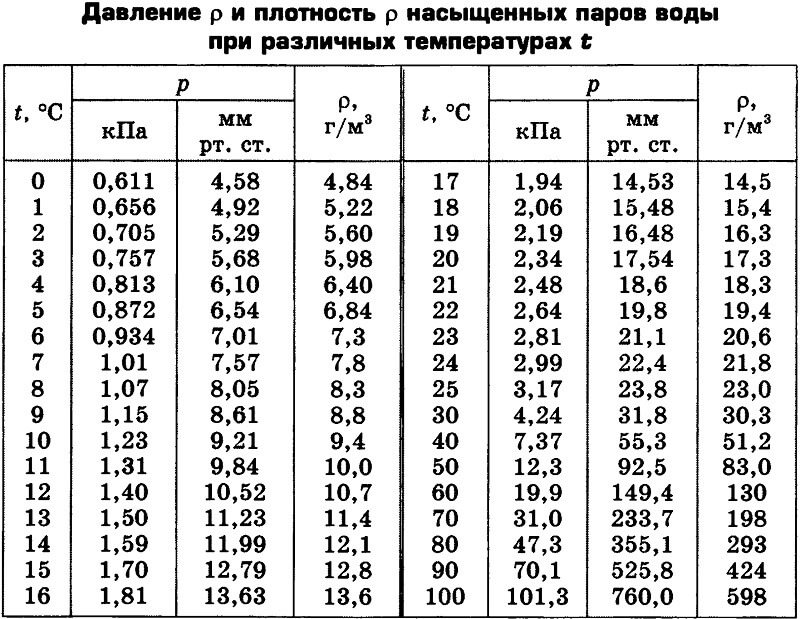
Зависимость изменения плотности, а также других физических характеристик водяного пара (насыщенный) от температуры приведены в таблице:
Для насыщенного пара над жидкостью справедливо уравнение Менделеева-Клапейрона. Поэтому, зная температуру, можно рассчитать плотность насыщенного пара. Она увеличивается с повышением температуры и не зависит от объема жидкости.
- Как определить плотность насыщенного пара
- Как найти абсолютную влажность воздуха
- Как найти давление водяного пара
- — бумага;
- — калькулятор;
- — ручка;
- — давление газа (из условия задачи или в таблице);
- — температура, при которой нужно определить плотность
- — периодическая таблица Менделеева.
Запишите на бумаге уравнение Менделеева-Клапейрона для идеальных газов: PV=(m/M)RT . Его можно использовать и для насыщенного пара, но как только плотность газа становится сравнимой с плотностью насыщенного пара, данное уравнение нельзя использовать в расчете – оно покажет неверный результат. Другим газовым законам насыщенный пар не подчиняется.
Из записанного уравнения выведите плотность насыщенного пара. Она равна массе, деленной на объем. Поэтому уравнение преобразуется: P= (p нас. пара/M)RT. Отсюда можно записать формулу для нахождения плотности насыщенного пара: p= PM/RT . Здесь P – это давление газа. Его табличное значение обычно дается в условии задачи и зависит от температуры. Если не дано, то найдите в таблице для вашей температуры. R – это универсальная газовая постоянная, равна 8,31 Дж/(К*моль).
Если вам известна температура в градусах Цельсия, то переведите ее в градусы Кельвина (обозначается К). Для этого прибавьте 273 к известной температуре, так как -273 – это абсолютный ноль по шкале Кельвина.
Найдите молярную массу жидкости M. Ее можно рассчитать с помощью периодической таблицы Менделеева. Молярная масса вещества численно равна молекулярной. Найдите в таблице значения атомных масс всех элементов, содержащихся в веществе, и умножьте на количество соответствующих атомов в молекуле. Сумма полученных значений даст молекулярную массу вещества.
Подставьте в последнее выражение все известные значения. Давление P нужно подставлять в Па. Если по условию дано в кПа, то умножьте его на 1000. Молярную массу при подстановке переведите в кг/моль (разделите на 1000), так как в периодической таблице она дана в г/моль. С помощью калькулятора рассчитайте значение плотности насыщенного пара. Результат получается в кг/м3.
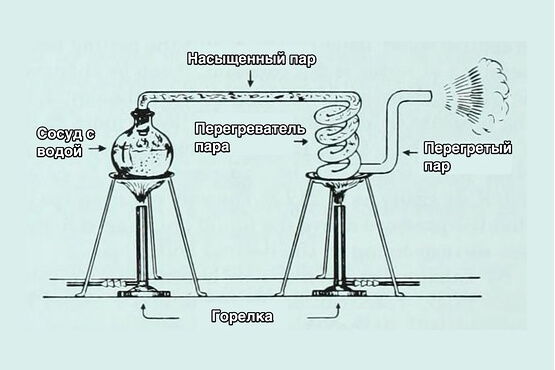
Термины насыщенный пар и перегретый пар относятся к термодинамическому состоянию воды. Вода и пар являются средами, используемыми для теплообмена в котловых установках благодаря своей доступности и высокой теплоемкости. Особенно эффективно передавать тепло посредством испарения и конденсации воды, которая обладает большой скрытой теплоты испарения.
Насыщенный пар (НП) и перегретый пар (ПП) относятся к определенному давлению среды. Первый НП может существовать во влажном и сухом состоянии, а перегретый ПП – только в сухом, поскольку не может содержать в своем составе частиц воды.
Чаще всего эти понятия применяются в теплоэнергетике, для расчета термодинамических циклов в контуре парового котла и в паровых турбинах, генерирующих электрическую энергию на ТЭЦ, ТЭС, ГРЭС и АЭС.
Что такое насыщенный пар
Водяной пар, пребывающий в термодинамическом равновесии с котловой водой, является насыщенным. Это формулировка дает понимание того, что давление насыщенного пара при температуре может иметь только одно значение
В котлоагрегатах парообразование протекает при постоянном давлении и подводе тепла к котловой воде от уходящих газов. Этот процесс базируется на следующих последовательных стадиях: подпитка котла водой, подогрев ее до температуры точки насыщения, и образование сухого насыщенного пара, когда вся жидкость испаряется из него.
В паровых котлах питательная вода, пройдя через экономайзер, попадает в барабан. Из него более холодные потоки под воздействием силы тяжести опускаются по необогреваемым трубам, а поднимаются по подъёмным топочным экранам обогреваемые более горячими дымовыми газами.
Здесь начинается процесс парообразования, поскольку температура воды достигает значения точки насыщения при рабочем давлении в котлоагрегате.
Плотность пароводяной смеси в экранных пакетах уменьшается и становится ниже плотности воды в опускных трубах, что создает напор для движения пароводяной смеси по экранам в барабан, где смесь сепарируется на воду и пар.
В закрытой поверхности нагрева при не меняющейся температуре в точке насыщения устанавливается термодинамическое равновесие между котловой водой и водяным паром. Число молекул пара, выделяющихся из поверхности воды за определенное время, будет равняться числу молекул сконденсированного пара, которые перейдут обратно в воду в барабане котла.
Давление насыщенного пара
Давление насыщения в котле зависит от температуры котловой воды в равновесном термодинамическом состоянии. При росте давления, пар сжимается и баланс нарушается. Плотность пара первоначально несколько возрастает, и из паровой среды в котловую воду будет переходить больше молекул конденсата, чем наоборот.
Поскольку количество молекул, переходящих из воды в единицу времени связано исключительно с температурой, то сжатие паровой среды не будет влиять на изменение этого числа.
Процесс будет протекать пока не возникнет термодинамическое равновесие, а следовательно, и концентрация возвращающихся молекул не достигнет первоначального уровня. Таким образом, Тнп напрямую зависит от давления насыщения в котле.
Таблица насыщенного пара
Характеристики сухого НП, приводятся в Таблице водяного пара. В ней указывают Т (С), при точке кипения котловой воды и давление (кПа и мм. рт.ст.) при которой этот процесс протекает.
Дополнительно в таблице могут указываться и другие параметры пара:
- eдельный объем, м3/кг;
- плотность, кг/м3;
- удельная энтальпия, кДж/кг
- удельная теплота парообразования, кДж/кг.
Плотность насыщенного пара
Плотность НП определяют по формуле.
D st = 216,49 * P / (Z st * (t + 273))
- D st — плотность насыщенного пара в кг / м3;
- P- абсолютное давление пара в барах;
- t — температура в градусах Цельсия;
- Z st — коэффициент сжимаемости насыщенного пара при Р и t.
Влажность насыщенного пара
Когда котлоагрегат нагревает воду, пузырьки, прорывающиеся через слой воды, захватываются паром. Влажный пар определяется как пар, в котором вода присутствует в виде микрокапель паров воды. В этом случае соотношение может составлять от 0 до 1. Если пар имеет 20 % воды по объему — он считается сухим на 80% или имеет долю сухости 0,8.
Таблицы НП содержит значения, такие как температура, энтальпия и удельный объем для сухого НП, но не для влажного. Для того чтобы их определить потребуется воспользоваться формулами, учитывая соотношение двух сред:
Удельный объем (v) мокрого пара
v = X * v g + (1 — X) * v f
- X = сухость (% / 100);
- v f = удельный объем жидкости;
- v g = удельный объем НП.
Удельная энтальпия пара сухостью Х:
h = h f + X * h fg
- X = сухость (%);
- h f = удельная энтальпия жидкости;
- h fg = удельная энтальпия НП.
Чем влажнее пар, тем ниже значения удельного объема, теплосодержание, энтальпия и энтропия. Таким образом сухость пара оказывает существенное влияние на все эти значения.
Задачей теплоэнергетиков является организация процессов парообразования в котле с сухостью 100%. Для этого в барабанах котлов устанавливают специальные сепарационные устройства, отделяющие пар от воды.
Перегретый пар
Перегретый пар — это пар с температурой, превышающей его температуру кипения при абсолютном давлении, при котором проводились измерение температуры. Давление и температура перегретого пара не зависят друг от друга, поскольку температура может увеличиваться, в то время как давление остается постоянным.
Процесс перегрева водяного пара на диаграмме Ts представлен на рисунке между состоянием E и кривой насыщенного пара. Чтобы оценить тепловую эффективность цикла, энтальпия должна быть получена из таблиц перегретого пара.
Процесс перегрева — единственный способ увеличить пиковую температуру цикла Ренкина и повысить эффективность без увеличения давления в котле. Это требует добавления в конструкцию котла особого теплообменника, называемого пароперегревателем.
В пароперегревателе дальнейший нагрев при фиксированном давлении приводит к увеличению, как температуры, так и удельного объема. Наибольшее значение перегретого пара заключается в его огромной внутренней энергии, которая может быть использована для кинетической реакции для движения лопастей турбины, создающих вращательное движение вала.
Температура перегретого пара
Характеристики перегретого пара (ПП) аналогичны идеальному газу, но не равны насыщенному пару. Поскольку ПП не обладает зависимостью между температурой и давлением, при конкретном давлении он может вырабатываться в широком температурном диапазоне, что будет зависеть от площади нагрева пароперегревателя.
Перегретый пар отличается от насыщенного такими преимуществами:
- gри равном давлении насыщения он обладает намного большей температурой;
- обладает большим удельным объемом, что дает экономию энергоресурсов при использовании;
- при снижении он не конденсируется, пока температура не упадет ниже точки насыщения при давлении среды.
Методы регулирования температуры перегретого пара
Довольно часто для технологических процессов, требуется получение перегретого пара строго определенной температуры. Для того чтобы снять ее излишки, обычно используют три метода воздействия на температуру ПП:
- cмешивание разных температурных потоков, когда в ПП впрыскивают котловую воду или паровой теплоноситель меньшего теплосодержания;
- поверхностное охлаждение, заключается в перенаправление ПП через систему специальных теплообменных аппаратов, выполняющих роль охладителей;
- изменение тепловосприятия потока, реализуется через изменение температуры или расхода уходящих котловых газов.
В теплоэнергетике в котлах высокого давления наиболее часто применяют первый метод, путем впрыскивания в поток ПП питательной воды или конденсата от турбогенератора. Впрыском насыщенного пара, как правило, регулируют температуру вторичного перегрева пара.
Получение перегретого пара
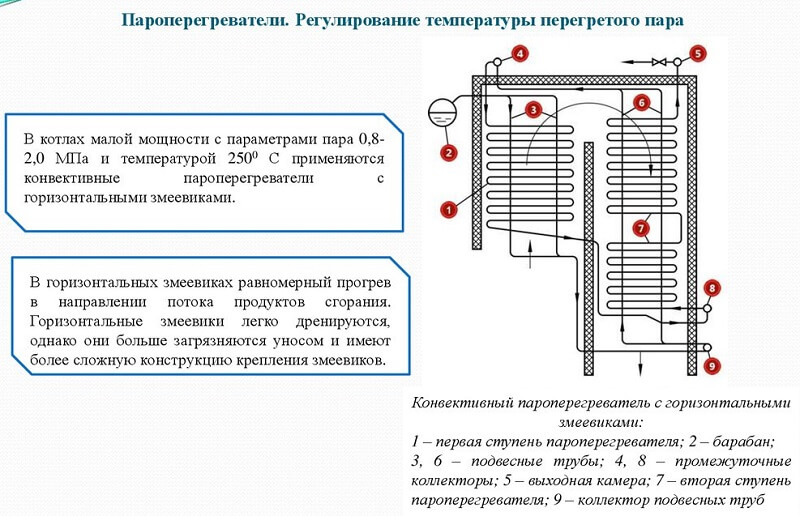
Пароперегреватель устройство, устанавливаемый в котлоагрегате, вырабатывает перегретый пар с параметрами, превышающими температуру насыщения в барабане котла. Он относится к особо критичным котловым элементам, поскольку из-за высоких температур ПП металл конструкции функционирует в предельно-допустимых условиях.
Пароперегреватели бывают основного типа, работающие в зоне сверхкритического давления и промежуточного типа, которые направляют пар отработанный в турбине для промперегрева.
Кроме того пароперегреватели классифицируются по тепловосприятию на конвективные, установленные в конвективной части котла, радиационные — расположены около топочных экранов и ширмовые — установленные в верхней части топки. По направлению движения потоков ПП и уходящих котловых газов выпускают ПП : прямоточные, противоточные и смешанные.
Использование перегретого пара в технике
В современных паровых турбинах применяют ПП с температурой перегретого пара существенно выше критической (374C).
Перегретый пар используется в турбинах для повышения теплового КПД. Другое использование перегретого пара:
- Пищевые технологии.
- Технологии очистки.
- Катализ / химическая обработка.
- Технологии поверхностной сушки.
- Технологии отверждения.
- Энергетика.
- Нанотехнологии.
Котлы перегретого пара
В России применяется ГОСТ 3619-76 на паровые котлоагрегаты, в котором установлены параметры насыщенного и перегретого пара, а также паровая производительность и температура воды для питания котла.
Современная российская энергетика использует котлоагрегаты производительностью вырабатывающих 1000/1650/2650/3950 т/ч пара для турбогенераторов соответствующей мощностью 300/500/800/1200 МВт, работающих на сверхкритических параметрах по давлению 25,5 МПа и Тпп=545С.
Энергетические котлы классифицируются по давлению пара — высокого от 10 до 14 МПа и сверхкритического свыше 25,5 МПа. Котлоагрегаты сверхвысокого давления, обычно, выполняют с вторичным перегревом пара.
Паровые котлоагрегаты малой и средней паропроизводительности используются для производства насыщенного и перегретого пара с характеристиками до 3,9 МПа и Т=450 С. Они эксплуатируются на промпредприятиях и в жилищно-коммунальном хозяйстве для производственно-технологических нужд и в системах центрального теплоснабжения.
Типичными представителями агрегатов данной категории являются котел Е (ДЕ) производительностью пара от 1 до 25 т/ч, Е (КЕ) производительностью пара до 25 т/ч с газомазутной горелкой и ДКВР производительностью до 20 т/ч. Их применение – источники тепловой энергии для центрального теплоснабжения с параметрами насыщенного и перегретого пара.
Здравствуйте. Я автор этого сайта. Продолжительное время я занимаюсь монтажом и пусконаладкой котельного оборудования. Если вы наладчик «старой гвардии» прошу подписаться на обновления. Будем вместе обсуждать интересные моменты монтажа и ПНР котельных.
Если открытый стакан с водой оставить на долгое время, то в конце концов вода полностью улетучится. Точнее — испарится. Что такое испарение и почему оно происходит?
Испарение и конденсация
При данной температуре молекулы жидкости обладают разными скоростями. Скорости большинства молекул находятся вблизи некоторого среднего значения (характерного для этой температуры). Но попадаются молекулы, скорости которых значительно отличаются от средней как в меньшую, так и большую сторону.
Рис. 1. Распределение молекул по скоростям
Когда такая весьма быстрая молекула окажется на свободной поверхности жидкости (т.е. на границе раздела жидкости и воздуха), кинетической энергии этой молекулы может хватить на то, чтобы преодолеть силы притяжения остальных молекул и вылететь из жидкости. Данный процесс и есть испарение, а молекулы, покинувшие жидкость, образуют пар.
Итак, испарение — это процесс превращения жидкости в пар, происходящий на свободной поверхности жидкости (при особых условиях превращение жидкости в пар может происходить по всему объёму жидкости. Данный процесс вам хорошо известен — это кипение).
Может случиться, что через некоторое время молекула пара вернётся обратно в жидкость.
Процесс перехода молекул пара в жидкость называется конденсацией. Конденсация пара — процесс, обратный испарению жидкости.
Динамическое равновесие
А что будет, если сосуд с жидкостью герметично закрыть? Плотность пара над поверхностью жидкости начнёт увеличиваться; частицы пара будут всё сильнее мешать другим молекулам жидкости вылетать наружу, и скорость испарения станет уменьшаться. Одновременно начнёт увеличиваться скорость конденсации, так как с возрастанием концентрации пара число молекул, возвращающихся в жидкость, будет становиться всё больше.
Насыщенный пар — это пар, который находится в состоянии динамического равновесия со своей жидкостью. Пар, не достигший состояния динамического равновесия с жидкостью, называется ненасыщенным.
Давление и плотность насыщенного пара обозначаются и . Очевидно, и — это максимальные давление и плотность, которые может иметь пар при данной температуре. Иными словами, давление и плотность насыщенного пара всегда превышают давление и плотность ненасыщенного пара.
Свойства насыщенного пара
Оказывается, что состояние насыщенного пара (а ненасыщенного — тем более) можно приближённо описывать уравнением состояния идеального газа (уравнением Менделеева — Клапейрона). В частности, имеем приближённое соотношение между давлением насыщенного пара и его плотностью:
Это весьма удивительный факт, подтверждаемый экспериментом. Ведь по своим свойствам насыщенный пар существенно отличается от идеального газа. Перечислим важнейшие из этих отличий.
1. При неизменной температуре плотность насыщенного пара не зависит от его объёма.
Если, например, насыщенный пар изотермически сжимать, то его плотность в первый момент возрастёт, скорость конденсации превысит скорость испарения, и часть пара конденсируется в жидкость — до тех пор, пока вновь не наступит динамическое равновесие, в котором плотность пара вернётся к своему прежнему значению.
Аналогично, при изотермическом расширении насыщенного пара его плотность в первый момент уменьшится (пар станет ненасыщенным), скорость испарения превысит скорость конденсации, и жидкость будет дополнительно испаряться до тех пор, пока опять не установится динамическое равновесие — т.е. пока пар снова не станет насыщенным с прежним значением плотности.
2. Давление насыщенного пара не зависит от его объёма.
Это следует из того, что плотность насыщенного пара не зависит от объёма, а давление однозначно связано с плотностью уравнением (1) .
Как видим, закон Бойля — Мариотта, справедливый для идеальных газов, для насыщенного пара не выполняется. Это и не удивительно — ведь он получен из уравнения Менделеева — Клапейрона в предположении, что масса газа остаётся постоянной.
3. При неизменном объёме плотность насыщенного пара растёт с повышением температуры и уменьшается с понижением температуры.
Действительно, при увеличении температуры возрастает скорость испарения жидкости.
Динамическое равновесие в первый момент нарушается, и происходит дополнительное испарение некоторой части жидкости. Пара будет прибавляться до тех пор, пока динамическое равновесие вновь не восстановится.
Точно так же при понижении температуры скорость испарения жидкости становится меньше, и часть пара конденсируется до тех пор, пока не восстановится динамическое равновесие — но уже с меньшим количеством пара.
Таким образом, при изохорном нагревании или охлаждении насыщенного пара его масса меняется, поэтому закон Шарля в данном случае не работает. Зависимость давления насыщенного пара от температуры уже не будет линейной функцией.
4. Давление насыщенного пара растёт с температурой быстрее, чем по линейному закону.
В самом деле, с увеличением температуры возрастает плотность насыщенного пара, а согласно уравнению (1) давление пропорционально произведению плотности на температуру.
Зависимость давления насыщенного пара от температуры является экспоненциальной (рис. 2 ). Она представлена участком 1–2 графика. Эту зависимость нельзя вывести из законов идеального газа.
Рис. 2. Зависимость давления пара от температуры
В точке 2 вся жидкость испаряется; при дальнейшем повышении температуры пар становится ненасыщенным, и его давление растёт линейно по закону Шарля (участок 2–3).
Вспомним, что линейный рост давления идеального газа вызван увеличением интенсивности ударов молекул о стенки сосуда. В случае нагревания насыщенного пара молекулы начинают бить не только сильнее, но и чаще — ведь пара становится больше. Одновременным действием этих двух факторов и вызван экспоненциальный рост давления насыщенного пара.
Влажность воздуха
Воздух, содержащий водяной пар, называется влажным.Чем больше пара находится в воздухе, тем выше влажность воздуха.
Абсолютная влажность — это парциальное давление водяного пара, находящегося в воздухе (т. е. давление, которое водяной пар оказывал бы сам по себе, в отсутствие других газов). Иногда абсолютной влажностью называют также плотность водяного пара в воздухе.
Относительная влажность воздуха — это отношение парциального давления водяного пара в нём к давлению насыщенного водяного пара при той же температуре. Как правило, это отношение выражают в процентах:
Из уравнения Менделеева-Клапейрона (1) следует, что отношение давлений пара равно отношению плотностей. Так как само уравнение (1) , напомним, описывает насыщенный пар лишь приближённо, мы имеем приближённое соотношение:
Оказывается, у насыщенного пара и бизнес-центра много общего, а чтобы вскипятить чайник при температуре меньше 100°C, нужно забраться на Эльбрус.
О чем эта статья:
Фазовые переходы: изменение агрегатных состояний вещества
Прежде чем говорить о насыщенном паре, нужно освежить знания об агрегатных состояниях и фазовых переходах между ними. Если вы забыли, какие бывают агрегатные состояния, то можете сбегать в нашу статью про них.
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Вот какие бывают фазовые переходы:
Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
На схеме — названия всех фазовых переходов:
Фазовые переходы — важная штука. Все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы в металлургии и микроэлектронике.
Парообразование
Итак, парообразование — это переход из жидкого состояния в газообразное.
При парообразовании всегда происходит поглощение энергии: к веществу необходимо подводить теплоту, чтобы оно испарялось. Из-за этого внутренняя энергия вещества увеличивается.
У процесса парообразования есть две разновидности: испарение и кипение.
Испарение — это превращение или переход жидкости в газ (пар) со свободной поверхности жидкости. Если поверхность жидкости открыта и с нее начинается переход вещества из жидкого состояния в газообразное, это будет называться испарением.
Кипение — процесс интенсивного парообразования, который происходит в жидкости при определенной температуре.
Например, мы заварили себе горячий чай. Над чашкой мы увидим пар, так как вода только что поучаствовала в процессе кипения.
Подождите-ка, мы ведь только что сказали, что кипение и испарение — разные вещи. 🤔 Это действительно так, но при этом оба процесса могут происходить параллельно.
Испарение может происходить и без кипения, просто тогда оно не будет для нас заметно. Например, вода в озере испаряется, хотя мы этого и не замечаем. Кипение по сути своей — это интенсивное испарение, которое вызвали внешними условиями — доведя вещество до температуры кипения.
Физика объясняет испарение тем, что жидкость обычно несколько холоднее окружающего воздуха, и из-за разницы температур происходит испарение.
Если нет каких-то внешних воздействий, испарение жидкостей происходит крайне медленно. Молекулы покидают жидкость из-за явления диффузии.
Направление тепловых потоков при испарении может идти в разной последовательности и комбинациях:
из глубины жидкости к поверхности, а затем в воздух;
только из жидкости к поверхности;
к поверхности из воды и газовой среды одновременно;
к площади поверхности только от воздуха.
Подытожим, чтобы не запутаться, в чем главная разница между испарением и кипением:
при любой температуре
с поверхности жидкости
при определенной температуре
с поверхности жидкости
Температура кипения
При температуре кипения давление насыщенного пара становится равным внешнему давлению на жидкость — чаще всего это атмосферное давление. Значит, чем больше внешнее давление, тем при более высокой температуре начнется кипение.
При нормальном атмосферном давлении, которое приблизительно равно 100 кПа, температура кипения воды равна 100°C. Поэтому можно сразу сказать, что давление насыщенного водяного пара при температуре 100 градусов по Цельсию равно 100 кПа. Это значение пригодится при решении задач.
Чем выше мы поднимаемся, тем меньше становится атмосферное давление, потому что масса атмосферы над нами уменьшается. Так, например, на вершине Эльбруса атмосферное давление составляет 5 × 104 Па — в два раза меньше, чем нормальное атмосферное давление. Поэтому и температура кипения на вершине Эльбруса будет ниже, чем на уровне моря. Вода там закипит при температуре 82°C.
Температура кипения при нормальном атмосферном давлении — это строго определенная величина для каждой жидкости.
Испарение и конденсация
Молекулы в жидкости непрерывно и хаотично движутся. Это значит, что направление движения отдельно взятых молекул — это случайные направления. При этом жидкость сохраняет свой объем. Также молекулы силами притяжения притягиваются друг к другу, из-за чего не могут покинуть Омск жидкость.
Значения скоростей молекул случайны. Из-за этого среди всех молекул обязательно есть те, что движутся очень быстро. Если такая молекула окажется вблизи поверхности раздела жидкости и окружающей среды, то ее кинетическая энергия может достигнуть большого значения, и молекула покинет жидкость.
Собственно, именно так происходит процесс испарения (мы говорили о нем выше, когда речь шла о фазовых переходах). Когда испарившихся молекул становится много, образуется пар.
Обратный процесс тоже возможен: вырвавшиеся за пределы жидкости молекулы вернутся в жидкость. Это конденсация, о ней мы тоже говорили.
Если открыть сосуд с жидкостью, то испарившиеся молекулы будут покидать пространство над жидкостью и не возвращаться обратно. Количество жидкости таким образом будет уменьшаться. То есть жидкость испаряется, а пар обратно не конденсируется (потому что молекулы этого пара удаляются от жидкости) — так происходит высыхание.
Испарение может происходить с разной скоростью. Чем больше силы притяжения молекул друг к другу, тем меньшее число молекул в единицу времени окажется в состоянии преодолеть эти силы притяжения и вылететь наружу, и тем меньше скорость испарения.
Быстро испаряются такие жидкости, как эфир, ацетон, спирт. Из-за этого свойства их иногда называют летучими жидкостями. Медленнее — вода. Намного медленнее воды испаряются масло и ртуть.
Курсы подготовки к ОГЭ по физике помогут снять стресс перед экзаменом и получить высокий балл.
Определение насыщенного пара
Оставим стакан воды на столе и будем замерять уровень воды в нем каждый день. Если записать эти измерения и сравнить их, станет очевидно: уровень воды стал меньше, то есть вода испарилась.
Теперь давайте накроем стакан сверху. Молекулы пара уже не смогут покидать пространство над жидкостью, по мере испарения их количество начнет расти, а значит, будет расти и количество молекул, которые конденсируются в единицу времени.
Сначала количество конденсирующихся молекул за единицу времени будет меньше количества испаряющихся молекул. Но по мере роста концентрации пара (то есть увеличении количества молекул в единице объема пара) поток конденсирующихся молекул вырастет. Это приведет к состоянию, которое называется динамическим равновесием.
Пар, находящейся в динамическом равновесии, называют насыщенным.
Представьте себе огромный бизнес-центр с не менее огромными дверями. У сотрудников бизнес-центра разный график работы, поэтому люди одновременно заходят в здание и выходят из него в произвольном количестве. Допустим, в 6 часов вечера 100 человек заходят в здание, чтобы попасть на деловую встречу, а другие 100 человек уже закончили работать и идут домой. Количество заходящих в бизнес-центр и выходящих из него будет одинаковым — это и есть состояние насыщения.
Значение давления насыщенного пара и его плотности являются максимальными при заданном значении температуры. Если это не так, то пар ненасыщенный.
Свойства насыщенного пара
При постоянной температуре плотность насыщенного пара не зависит от его объема.
Представьте, что объем сосуда с насыщенным паром уменьшили, не изменив температуры.
Количество молекул, переходящих от пара к жидкости, превысит количество испаряющихся молекул, но при этом часть пара сконденсируется, а оставшийся пар снова придет в динамическое равновесие. В итоге плотность этого пара будет равна начальной плотности.
Давление насыщенного пара не зависит от его объема.
Это связано с тем, что давление и плотность связаны через уравнение Менделеева-Клапейрона, и следует из первого свойства насыщенного пара.
Кстати, уравнение Менделеева-Клапейрона справедливо для насыщенного пара. При этом нужно быть внимательным с частными случаями. Так, например, закон Бойля-Мариотта для насыщенного пара не выполняется.
pV = νRT
p — давление газа [Па]
V — объем [м3]
ν — количество вещества [моль]
T — температура [К]
R — универсальная газовая постоянная
R = 8,31 м 2 × кг × с -2 × К -1 × моль -1
При неизменном объеме плотность насыщенного пара растет с повышением температуры и уменьшается с понижением температуры.
В начальный момент испарения динамическое равновесие будет нарушено (некоторая часть жидкости испарится дополнительно). Плотность пара будет расти, пока динамическое равновесие не восстановится.
Давление и температура насыщенного пара растут быстрее, чем по линейному закону, который справедлив для идеального газа.
В случае идеального газа рост давления обусловлен только ростом температуры, а в случае с насыщенном паром имеют значение два фактора: температура и масса пара.
В случае нагревания насыщенного пара молекулы начинают ударяться чаще, так как их в целом стало больше, потому что пара стало больше.
Главное отличие насыщенного пара от идеального газа: пар сам по себе не является замкнутой системой, а находится в постоянном контакте с жидкостью.
Применим свойства насыщенного пара при решении задач.
Задачка раз
В цилиндрическом сосуде под поршнем длительное время находятся вода и ее пар. Поршень начинают вдвигать в сосуд. При этом температура воды и пара остается неизменной. Как будет меняться при этом масса жидкости в сосуде? Ответ поясните.
Решение
Так как пар и вода находятся в контакте длительное время, пар является насыщенным. При уменьшении объема сосуда давление насыщенного пара не меняется. Из уравнения Менделеева-Клапейрона следует, что для того, чтобы давление пара не менялось, его количество вещества (а значит и масса) должно уменьшаться.
В этом процессе происходит конденсация, часть молекул пара переходят в жидкость, поэтому масса жидкости увеличивается.
Ответ
Масса жидкости увеличивается.
Задачка два
Какова плотность насыщенного пара при температуре 100°С?
Решение
При нормальном давлении (p = 105 Па) 100°С — это температура кипения воды. Значит, давление насыщенного пара при этой температуре равно атмосферному давлению.
Найдем связь между давлением и плотностью через уравнение Менделеева-Клапейрона.
Подставим значение давления в уравнение состояния идеального газа, предварительно переведя температуру в Кельвины: T = 100 + 273 = 373 K
Читайте также:
- Какие полезные инициативы выдвигала общественная палата рф кратко
- 14 школа сызрань педагогический состав
- Что запрещено в конфликте кратко
- Какие виды искусства получили развитие на кубани в первой половине 19 века ответ кратко
- С помощью каких органов осуществляется связь организма с внешней средой кратко
Насыщенный пар
-
Темы кодификатора ЕГЭ: насыщенные и ненасыщенные пары, влажность воздуха.
-
Испарение и конденсация
-
Динамическое равновесие
-
Свойства насыщенного пара
-
Влажность воздуха
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: насыщенные и ненасыщенные пары, влажность воздуха.
Если открытый стакан с водой оставить на долгое время, то в конце концов вода полностью улетучится. Точнее — испарится. Что такое испарение и почему оно происходит?
Испарение и конденсация
При данной температуре молекулы жидкости обладают разными скоростями. Скорости большинства молекул находятся вблизи некоторого среднего значения (характерного для этой температуры). Но попадаются молекулы, скорости которых значительно отличаются от средней как в меньшую, так и большую сторону.
На рис. 1 изображён примерный график распределения молекул жидкости по скоростям. Голубым фоном показано то самое большинство молекул, скорости которых группируются около среднего значения. Красный «хвост» графика — это небольшое число «быстрых» молекул, скорости которых существенно превышают среднюю скорость основной массы молекул жидкости.
Рис. 1. Распределение молекул по скоростям
Когда такая весьма быстрая молекула окажется на свободной поверхности жидкости (т.е. на границе раздела жидкости и воздуха), кинетической энергии этой молекулы может хватить на то, чтобы преодолеть силы притяжения остальных молекул и вылететь из жидкости. Данный процесс и есть испарение, а молекулы, покинувшие жидкость, образуют пар.
Итак, испарение — это процесс превращения жидкости в пар, происходящий на свободной поверхности жидкости (при особых условиях превращение жидкости в пар может происходить по всему объёму жидкости. Данный процесс вам хорошо известен — это кипение).
Может случиться, что через некоторое время молекула пара вернётся обратно в жидкость.
Процесс перехода молекул пара в жидкость называется конденсацией. Конденсация пара — процесс, обратный испарению жидкости.
к оглавлению ▴
Динамическое равновесие
А что будет, если сосуд с жидкостью герметично закрыть? Плотность пара над поверхностью жидкости начнёт увеличиваться; частицы пара будут всё сильнее мешать другим молекулам жидкости вылетать наружу, и скорость испарения станет уменьшаться. Одновременно начнёт увеличиваться скорость конденсации, так как с возрастанием концентрации пара число молекул, возвращающихся в жидкость, будет становиться всё больше.
Наконец, в какой-то момент скорость конденсации окажется равна скорости испарения. Наступит динамическое равновесие между жидкостью и паром: за единицу времени из жидкости будет вылетать столько же молекул, сколько возвращается в неё из пара. Начиная с этого момента количество жидкости перестанет убывать, а количество пара — увеличиваться; пар достигнет «насыщения».
Насыщенный пар — это пар, который находится в состоянии динамического равновесия со своей жидкостью. Пар, не достигший состояния динамического равновесия с жидкостью, называется ненасыщенным.
Давление и плотность насыщенного пара обозначаются и
. Очевидно,
и
— это максимальные давление и плотность, которые может иметь пар при данной температуре. Иными словами, давление и плотность насыщенного пара всегда превышают давление и плотность ненасыщенного пара.
к оглавлению ▴
Свойства насыщенного пара
Оказывается, что состояние насыщенного пара (а ненасыщенного — тем более) можно приближённо описывать уравнением состояния идеального газа (уравнением Менделеева — Клапейрона). В частности, имеем приближённое соотношение между давлением насыщенного пара и его плотностью:
(1)
Это весьма удивительный факт, подтверждаемый экспериментом. Ведь по своим свойствам насыщенный пар существенно отличается от идеального газа. Перечислим важнейшие из этих отличий.
1. При неизменной температуре плотность насыщенного пара не зависит от его объёма.
Если, например, насыщенный пар изотермически сжимать, то его плотность в первый момент возрастёт, скорость конденсации превысит скорость испарения, и часть пара конденсируется в жидкость — до тех пор, пока вновь не наступит динамическое равновесие, в котором плотность пара вернётся к своему прежнему значению.
Аналогично, при изотермическом расширении насыщенного пара его плотность в первый момент уменьшится (пар станет ненасыщенным), скорость испарения превысит скорость конденсации, и жидкость будет дополнительно испаряться до тех пор, пока опять не установится динамическое равновесие — т.е. пока пар снова не станет насыщенным с прежним значением плотности.
2. Давление насыщенного пара не зависит от его объёма.
Это следует из того, что плотность насыщенного пара не зависит от объёма, а давление однозначно связано с плотностью уравнением (1).
Как видим, закон Бойля — Мариотта, справедливый для идеальных газов, для насыщенного пара не выполняется. Это и не удивительно — ведь он получен из уравнения Менделеева — Клапейрона в предположении, что масса газа остаётся постоянной.
3. При неизменном объёме плотность насыщенного пара растёт с повышением температуры и уменьшается с понижением температуры.
Действительно, при увеличении температуры возрастает скорость испарения жидкости.
Динамическое равновесие в первый момент нарушается, и происходит дополнительное испарение некоторой части жидкости. Пара будет прибавляться до тех пор, пока динамическое равновесие вновь не восстановится.
Точно так же при понижении температуры скорость испарения жидкости становится меньше, и часть пара конденсируется до тех пор, пока не восстановится динамическое равновесие — но уже с меньшим количеством пара.
Таким образом, при изохорном нагревании или охлаждении насыщенного пара его масса меняется, поэтому закон Шарля в данном случае не работает. Зависимость давления насыщенного пара от температуры уже не будет линейной функцией.
4. Давление насыщенного пара растёт с температурой быстрее, чем по линейному закону.
В самом деле, с увеличением температуры возрастает плотность насыщенного пара, а согласно уравнению (1) давление пропорционально произведению плотности на температуру.
Зависимость давления насыщенного пара от температуры является экспоненциальной (рис. 2). Она представлена участком 1–2 графика. Эту зависимость нельзя вывести из законов идеального газа.
Рис. 2. Зависимость давления пара от температуры
В точке 2 вся жидкость испаряется; при дальнейшем повышении температуры пар становится ненасыщенным, и его давление растёт линейно по закону Шарля (участок 2–3).
Вспомним, что линейный рост давления идеального газа вызван увеличением интенсивности ударов молекул о стенки сосуда. В случае нагревания насыщенного пара молекулы начинают бить не только сильнее, но и чаще — ведь пара становится больше. Одновременным действием этих двух факторов и вызван экспоненциальный рост давления насыщенного пара.
к оглавлению ▴
Влажность воздуха
Воздух, содержащий водяной пар, называется влажным.Чем больше пара находится в воздухе, тем выше влажность воздуха.
Абсолютная влажность — это парциальное давление водяного пара, находящегося в воздухе (т. е. давление, которое водяной пар оказывал бы сам по себе, в отсутствие других газов). Иногда абсолютной влажностью называют также плотность водяного пара в воздухе.
Относительная влажность воздуха — это отношение парциального давления водяного пара в нём к давлению насыщенного водяного пара при той же температуре. Как правило, это отношение выражают в процентах:
Из уравнения Менделеева-Клапейрона (1) следует, что отношение давлений пара равно отношению плотностей. Так как само уравнение (1), напомним, описывает насыщенный пар лишь приближённо, мы имеем приближённое соотношение:
Одним из приборов, измеряющих влажность воздуха, является психрометр. Он включает в себя два термометра, резервуар одного из которых завёрнут в мокрую ткань. Чем ниже влажность, тем интенсивнее идёт испарение воды из ткани, тем сильнее охлаждается резервуар «мокрого» термометра, и тем больше разность его показаний и показаний сухого термометра. По этой разности с помощью специальной психрометрической таблицы определяют влажность воздуха.
Спасибо за то, что пользуйтесь нашими публикациями.
Информация на странице «Насыщенный пар» подготовлена нашими авторами специально, чтобы помочь вам в освоении предмета и подготовке к экзаменам.
Чтобы успешно сдать необходимые и поступить в ВУЗ или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из данного раздела.
Публикация обновлена:
08.05.2023
Как определить плотность насыщенного пара
Для насыщенного пара над жидкостью справедливо уравнение Менделеева-Клапейрона. Поэтому, зная температуру, можно рассчитать плотность насыщенного пара. Она увеличивается с повышением температуры и не зависит от объема жидкости.
Запишите на бумаге уравнение Менделеева-Клапейрона для идеальных газов: PV=(m/M)RT. Его можно использовать и для насыщенного пара, но как только плотность газа становится сравнимой с плотностью насыщенного пара, данное уравнение нельзя использовать в расчете – оно покажет неверный результат. Другим газовым законам насыщенный пар не подчиняется.
Из записанного уравнения выведите плотность насыщенного пара. Она равна массе, деленной на объем. Поэтому уравнение преобразуется:P= (p нас. пара/M)RT. Отсюда можно записать формулу для нахождения плотности насыщенного пара: p= PM/RT . Здесь P – это давление газа. Его табличное значение обычно дается в условии задачи и зависит от температуры. Если не дано, то найдите в таблице для вашей температуры. R – это универсальная газовая постоянная, равна 8,31 Дж/(К*моль).
Если вам известна температура в градусах Цельсия, то переведите ее в градусы Кельвина (обозначается К). Для этого прибавьте 273 к известной температуре, так как -273 – это абсолютный ноль по шкале Кельвина.
Найдите молярную массу жидкости M. Ее можно рассчитать с помощью периодической таблицы Менделеева. Молярная масса вещества численно равна молекулярной. Найдите в таблице значения атомных масс всех элементов, содержащихся в веществе, и умножьте на количество соответствующих атомов в молекуле. Сумма полученных значений даст молекулярную массу вещества.
Подставьте в последнее выражение все известные значения. Давление P нужно подставлять в Па. Если по условию дано в кПа, то умножьте его на 1000. Молярную массу при подстановке переведите в кг/моль (разделите на 1000), так как в периодической таблице она дана в г/моль. С помощью калькулятора рассчитайте значение плотности насыщенного пара. Результат получается в кг/м3.

 Температура. С ее повышением увеличивается плотность пара, так как прослеживается рост числа молекул насыщения.
Температура. С ее повышением увеличивается плотность пара, так как прослеживается рост числа молекул насыщения.