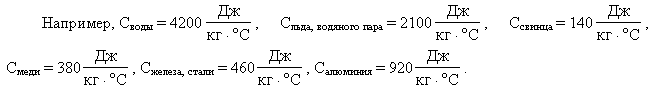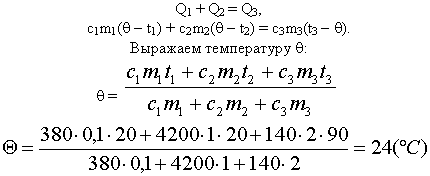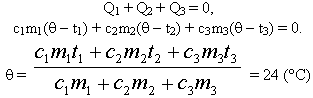В физике и некоторых других науках греческой буквой D («дельта») принято обозначать разницу между определенными параметрами. Это могут быть, например, температура, время, давление, длины отрезков, расстояния между координатами по одной и той же оси и т.д. Латинской буквой t чаше всего обозначают время и температуру.

Вам понадобится
- — данные измерений;
- — калькулятор.
Инструкция
Если буквой t в данном разделе физики обозначается температура, проведите измерения температуры. Термометр может быть любым. Нужно, чтобы его шкала соответствовала нужной вам степени точности. Разумеется, измерять оба показателя необходимо по одному и тому же термометру.
Второй показатель зависит от условий задачи. Например, если вам нужно отследить изменение состояния объекта, снимите второй показатель через некоторое время. Самый доступный эксперимент — измерить температуру своего тела утром и вечером. Вычтите из большего числа меньшее. Это и будет дельта t. Поскольку температура с течением времени может как увеличиваться, так и уменьшаться, вам нужен модуль разности.
В задаче может быть предложено и сравнение изменений разных объектов. Дельта t в этом случае приобретает несколько иной смысл, но все равно она остается разностью температур. Например, вам нужно определить, насколько нужно разогреть горелку, чтобы расплавить два разных металла. Сравните температуры плавления одного и другого вещества. Точно так же, как и в первом случае, вычтите из большего показателя меньший. Если вы проводите эксперимент, то сначала вам нужно разогреть горелку до меньшей температуры, затем прибавить к ней Dt, что и даст вам температуру плавления другого металла.
Во многих отраслях знаний буквой t обозначают время. Выражение «дельта t» в этих случаях также означает разность, но уже в показаниях часов. Засеките время и запишите результат. Подождите немного и снова посмотрите на часы. Допустим, в первый раз вы посмотрели на циферблат ровно в 14 часов, а второй — по прошествии 13 минут. Разность в этом случае составляет 13 минут. Это и есть Dt по условиям данной задачи.
На практике довольно часто приходится определять Dt без всяких вычислений. Например, во время соревнований по легкой атлетике арбитру важно знать, за какое время бегуны пробежали ту или иную дистанцию. При этом не особенно важно, во сколько начались состязания, объявлен старт раньше или позже указанного в афишах времени. В этом случае судья определяет только Dt. В начале забега он ставит секундомер на 0, а в конце — отмечает результат.
Обратите внимание
Определить Dt бывает необходимо и при сравнении движения разных объектов при прочих равных условиях. Этот способ тоже наиболее понятен, если представить себе спортсменов. Допустим, участников соревнований очень много, они все бегут одну и ту же дистанцию, но в разных забегах. Судьям нужно понять, кто окажется на каком месте в итоговой таблице. Для этого определяется лучший результат — в данном случае минимальный. С ним сравниваются все остальные. То есть каждый раз судьи находят Dt между временем первого и второго, второго и третьего спортсменов и т.д.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
План урока:
Изменение внутренней энергии в расчетах
Что означает удельная теплоемкость?
Какое количество тепла выделяется или поглощается?
Термос. Сосуд Дьюара. Калориметр
Где взять тепло?
Изменение внутренней энергии в расчетах
Работа и теплообмен (теплопередача) – два пути, изменяющих внутреннюю энергию. В преодолении этих путей внутренняя энергия изменяется или на величину совершенной работы А или на величину Q – количество переданной (может быть и отданной) теплоты.
(В седьмом классе было введена буква Δ для обозначения изменения какой-нибудь физической величины. Это использование прописной греческой буквы общепринято).
Пусть через ΔU обозначается изменение внутренней энергии. Тогда ΔU = U2 – U1. Здесь U2 – конечная, а U1 – начальная внутренняя энергия.
В зависимости от пути изменения ΔU можно определить следующими способами:
ΔU = А (если совершается работа) или ΔU = Q (если произошел теплообмен). Изменение ΔU может одновременно пройти двумя способами. И тогда для общего случая:
Источник
Согласно уравнению ΔU = Q + A,
Источник
Величина ΔU находится математическими расчетами. Результат вычислений бывает как отрицательной, так и положительной:
- U2 ˃ U1, то есть энергия растет, тогда ΔU ˃ 0;
- U2 ˂ U1, то есть энергия убывает, тогда ΔU˂ 0.
Слагаемые работа и количество теплоты в равенстве ΔU = Q + A так же могут обладать разными знаками:
- работает внешняя сила, значит, А˃ 0;
- работает само тело — А˂ 0;
- тело получает тепло – Q ˃ 0;
- тело отдает тепло – Q ˂ 0.
На примере это выглядит так.
Внимательно изучив уравнение ΔU = Q + A, можно заметить следующее: если систему рассматриваемых тел изолировать, то есть не выполнять работу, и не дать возможности обмена теплом с внешней средой, то внутренняя энергия тела не сможет изменяться. Это утверждение определяет закон сохранения внутренней энергии и означает, что тепловое движение постоянно.
Еще один важный вывод следует для двух тел, находящихся в изолированном состоянии. При плотном контакте этих тел, начинается процесс теплообмена, что будет продолжаться до той поры, пока температура не выровняется у обоих тел.
Источник
Тела изолированы, а значит, изменяется только их внутренняя энергия, причем на величину тепла (ΔU = Q). Тело холодное получило тепло, а теплое — это тепло отдало.
Почему в нем присутствует знак модуля? Дело в том, что получение тепла имеет положительное значение, а отдача тепла – отрицательное. Но модули этих чисел равны (модуль – это абсолютное числовое значение величины).
Что означает удельная теплоемкость?
Удельное княжество, удельные земли, удел, как судьба или участь, конечно же, не имеют никакого отношения к физике. Но все же они обозначают что-то отдельное, часть, долю. Вот и в случае с теплотой используется понятие удельной теплоемкости вещества, как величины, связанной с частью, а вернее, с единицей объема этого вещества.
Такой простой опыт можно провести в домашних условиях. В равные емкости налить молока и воды одной массы. Нагревать на одинаковых горелках. Термометром для жидкостей следить за температурой обоих веществ. Не пройдет и минуты, станет заметно, что молоко нагревается быстрее.

Это значит, что для нагрева воды до той же температуры, что и молоко, нужно тепла больше.
Следует вывод:
Величина, которая характеризует степень поглощения (или выделения) тепла веществом в физике называется удельной теплоемкостью. Чтобы выяснить, что она означает, надо взять единицу массы вещества (1 кг) нагреть его на 1о С. То количество джоулей тепла, которое поглотится телом при этом и является удельной теплоемкостью данного вещества. Или наоборот, то количество тепла, которое выделится при охлаждении 1 кг вещества на 1о С — это та же самая удельная теплоемкость. Обозначают эту величину буквой c.
Источник
Теперь объяснима разница в нагревании молока и воды. Удельные теплоемкости этих веществ различны: вода – 4200 Дж/кг∙оС, молоко – 4020 (нежирное) и 3875 Дж/кг∙оС (жирное). Это значит, что нагреть молоко легче, чем воду. Из веществ, приведенных в таблице, вода – самое теплоемкое вещество.
Стоит обратить внимание, что в разных агрегатных состояниях, удельная теплоемкость одного и того же вещества различна. Это зависит от того, что структура вещества в разных состояниях различна.
Источник
Какое количество тепла выделяется или поглощается?
Чтобы ответить на этот вопрос, надо выяснить от чего зависит количество теплоты. Зависимость от рода вещества показана на примере нагревания молока и воды. Но этого недостаточно.
Источник
Нетрудно догадаться, что тепла понадобится больше, если нужно нагреть воду до горячего состояния, а не сделать ее только теплой. В процессе охлаждения тепла выделится больше от горячей воды, чем от теплой. А характеризует степень нагретости тела температура. Значит, чем больше разница в начальной и конечной температуре, тем большее количество тепла выделяется или поглощается телом.
Разность температур – это Δt = tкон — tнач .
Теперь еще одна зависимость. Даже младший школьник мог наблюдать у себя на кухне, что целая кастрюля воды нагреваться будет намного дольше, чем половина кастрюли, если ее греть.
Источник
Это значит, количество тепла, потребляемого телом или выделяемого им, зависит от массы тела.
Получается прямая зависимость тепла от трех величин:
- характеристики вещества (удельной теплоемкости);
- величины, на которую изменится температура;
- количественной характеристики тела (массы).
Итак,
Следует обратить внимание на Δt. Если tкон ˃ tнач, разность температур положительна, значит тело нагревается, идет процесс потребления тепла. Если tкон ˂ tнач, разность температур отрицательна, тело охлаждается, происходит выделение тепла.
Термос. Сосуд Дьюара. Калориметр
Достаточно часто требуется остановить или задержать процесс остывания. В бытовых целях для этого используются термосы. Устройство их несложно. Главную роль здесь играет прослойка с низкой теплопроводностью между стенками двойного стеклянного (бывает и из другого вещества) сосуда.
Источник
Для сохранения повышенных или пониженных температур веществ в промышленности, медицине, ветеринарии, косметологии, лабораториях используют теплонепроницаемый сосуд, который носит название своего изобретателя – сосуд Дьюара.
Источник
Состоит сосуд из двух основных резервуаров, изготовленных из термостойкого алюминия. Меньший резервуар находится внутри большего и скреплен с ним небольшими прочными перемычками. Внешний резервуар покрыт защитным веществом, а внутренний очень хорошо отполирован. Сосуд закрыт непроводящей тепло пенопластиковой крышкой. Устройство сосуда Дьюара аналогично строению обычного бытового термоса, но термос – это упрощенный вариант дьюаровского изобретения.
Изначально сосуды Дьюара применялись для легко испаряющихся жидкостей. Теперь же эти сосуды используют для поддержания и сохранения свойств веществ при необходимых температурах. Чаще других в таких сосудах хранят жидкий азот, применение которого очень разнообразно:
- удаление недоброкачественных и доброкачественных опухолей в медицине;
- удаление бородавок и папиллом в косметологии;
- транспортировка биоматериалов для искусственного оплодотворения животных в ветеринарии;
- научные исследования в лабораториях;
- достижение прочности металлов в машиностроении;
- шоу, развлечения.
приготовление мороженого, заморозка сметаны или фруктов в кулинарии

При исследованиях в школе и проведении опытов вместо сосудов Дьюара и термосов используют более простой прибор, который называют калориметром
Источник
Такое приспособление не может исключить полную связь содержимого внутреннего сосуда с внешней средой. Чтобы потеря тепла во внешнюю среду была минимальной, нужно опыты проводить достаточно быстро.
Используя калориметр, в условиях учебного класса можно проверить справедливость уравнения теплового баланса. Для этого понадобится одинаковое количество (например, 50 г) холодной и горячей воды, калориметр и термометр.
Пусть в первом калориметре температура горячей воды 80оС, а во втором — комнатная температура, равная 20оС.
Нужно аккуратно холодную воду перелить в калориметр с горячей водой. Полученную смесь осторожно перемешать термометром (трубочку или ложку для смешивания брать не стоит, чтобы лишний раз не нарушать выбранную изолированную систему тел).
Начальные температуры воды и температуру смеси записать и использовать в дальнейших расчетах. Учитывая табличное значение удельной теплоемкости воды (4200 Дэ/кг о С), взятую массу (50 г = 0, 05 кг), вычисления будут следующими:
Конечно, такой результат может получиться лишь теоретически. В опыте с калориметром есть недостаток в том, что существует недостаточная изоляция системы рассматриваемых тел. Тепло горячей воды попадает во внешнюю среду, так как калориметр с горячей водой не закрыт. Нельзя забывать, что измерения проводятся с определенной долей погрешности.
Но суть проделанных набольших исследований понятна и подтверждает уравнение теплового баланса.
Где взять тепло?
Ответ прост. При сгорании топлива, виды которого разнообразны.
Источник
Отопительная ценность, например, каменного угля определяется количеством тепла, выделяющегося в процессе сгорания одного его килограмма.
Откуда в угле берется тепло? По одной из теорий топливные материалы, такие как уголь и торф, образовались из растений.
Некогда почти вся земля была покрыта растительностью, главным образом гигантскими лесными чащами. На месте сваленных бурей деревьев вырастали новые. С течением времени образовался толстый слой гниющего дерева. Некоторые пространства земного шара были опустошены буйными ураганами или сползающими ледниками. Пространства эти со временем покрыл ил, нанесенный волнами рек и морей. Или же землю засыпал песок пустынь. В таких условиях бревна, находящиеся под большим давлением и без доступа воздуха, образовали слой вещества, которое теперь называют каменным углем.
Долгое время тепло от сгорания топлива измерялось в калориях (1 кал) – это количество тепла, необходимое для нагревания 1 г воды на 1оС. Большая калория – килокалория (1 ккал) – количество тепла, необходимое для повышения температуры 1 килограмма воды на 1оС.
Сейчас вместо калорий и килокалорий используются Джоули и единицы, производные от 1 Джоуля.
Эта величина тепла называется удельной теплотой сгорания топлива и обозначается буквой q.
Источник
Например, табличное значение для природного газа, который сейчас очень широко применяется, q = 4,4 ∙ 107 Дж/кг означает: при сгорании 1 кг природного газа выделяется 4,4 ∙ 107 Джоулей тепла.
Если сгорает не один килограмм топлива, то полученное количество выделившегося тепла определяется формулой Q = qm.
Само тепло получается, как результат изменения опять же внутренней энергии сгорающего топлива. Горение происходит всегда с участием кислорода. При этом атомы кислорода, соединившись с атомами углерода (содержится и в древесном угле, и в каменном, и в нефти, и бензине), образуют продукт горения – это углекислый газ. Его молекулы обладают кинетической энергией большей, чем молекулы кислорода и углерода, отдельно взятые. Следовательно, внутренняя энергия становится больше и проявляется в виде выделения тепла.
Процесс увеличения энергии во время горения называют выделением энергии, то есть выделением тепла.
Чтобы можно было использовать тепло от сгоревшего топлива, человеком с давних пор применяются и простые, и сложные приспособления. Это костер, свеча, печь, газовая горелка, спиртовка, тепловые машины, двигатели.
На службе человека находятся и такие мощные преобразователи тепла, как тепловые электростанции.
Пособие рекомендовано учащимся, желающим
получить практические навыки в решении задач на
теплообмен, и может быть полезным для учителей и
абитуриентов.
При соприкосновении тел, имеющих разные
температуры, между этими телами происходит
теплообмен. С точки зрения
молекулярно-кинетической теории, это
объясняется так: молекулы более нагретого тела
имеют большую кинетическую энергию, чем молекулы
тела, менее нагретого. При “столкновениях”
молекул соприкасающихся тел происходит процесс
выравнивания их средних кинетических энергий.
Молекулы более нагретого тела теряют часть своей
кинетической энергии, при этом нагретое тело
будет остывать. Кинетическая энергия молекул
холодного тела возрастает, поэтому температура
этого тела будет увеличиваться. В конечном итоге
кинетические энергии молекул обоих тел
сравняются, и температуры тел станут
одинаковыми. На этом теплообмен прекращается.
Энергию, которую тело получает или отдаёт в
процессе теплообмена, называют количеством
теплоты (Q).
Количество теплоты, как и все другие виды
энергии, измеряется в системе СИ в Джоулях: [Q] = Дж.
(Здесь и в дальнейшем единицы измеряются в
системе СИ.)
Нагревание или охлаждение
При нагревании или охлаждении тела количество
теплоты, поглощаемое или выделяемое им,
рассчитывается по формуле:
Q = сm(t2 – t1), (1)
где m – масса тела, кг;
(t2 – t1) – разность температур
тела,° С (или К);
с – удельная теплоёмкость вещества, из
которого состоит тело,
Удельная теплоёмкость вещества – это
количество теплоты, которое нужно сообщить
одному килограмму данного вещества, чтобы
увеличить его температуру на 1° С (или это
количество теплоты, которое выделяет один
килограмм данного вещества, остывая на 1° С).
Значения удельных теплоемкостей других
веществ можно найти в справочниках, а также в
школьном учебнике или задачнике.
При нагревании тела его внутренняя энергия
увеличивается. Это требует притока энергии к
телу от других тел. Значит, оно поглощает
некоторое количество теплоты, принимая его от
других тел, участвующих в теплообмене.
При охлаждении тела его внутренняя энергия
уменьшается. Поэтому остывающее тело отдаёт
кому-либо некоторое количество теплоты.
Обычно конечную температуру, установившуюся в
результате теплообмена, обозначают греческой
буквой (тэта).
В формуле (1) произведение cm для каждого
конкретного тела есть величина постоянная. Её
называют теплоёмкостью тела и обозначают С:
C = c m.(2)
Размерность теплоемкости: Теплоемкость тела показывает,
сколько энергии нужно подвести к данному телу,
чтобы нагреть его на 1° С (или сколько энергии
выделяет это тело, остывая на 1° С).
Теплообмен между телами, имеющими одинаковые
температуры, не происходит, даже если
контактируют вещества, находящиеся в разных
агрегатных состояниях. Например, при температуре
плавления (0° С) лёд и вода могут находиться
бесконечно долго, при этом количество льда и
количество воды останутся неизменными.
Аналогично ведут себя пар и жидкость,
находящиеся при температуре кипения. Теплообмен
между ними не происходит.
Плавление или кристаллизация
Если при нагревании тела его температура
достигнет температуры плавления, то начинает
происходить процесс перехода этого вещества из
твердого состояния в жидкое. При этом идут
изменения в расположении и характере
взаимодействия молекул. Температура при
плавлении не изменяется. Это означает, что
средние кинетические энергии молекул жидкости и
твердого тела при температуре плавления
одинаковы. Однако внутренняя энергия тела при
плавлении возрастает за счет увеличения энергии
взаимодействия молекул. Количество теплоты,
поглощаемое телом при плавлении, рассчитывается
по формуле
(3)
где m – масса тела, кг;
–
удельная теплота плавления,
При кристаллизации, наоборот, внутренняя
энергия тела уменьшается на величину и эта теплота данным
телом выделяется. Она поглощается другими
телами, участвующими в теплообмене.
Удельная теплота плавления показывает,
сколько энергии нужно сообщить одному
килограмму данного вещества, взятого при
температуре плавления, чтобы полностью
превратить его при этой температуре в жидкость
(или сколько энергии выделяет 1 кг жидкости,
взятой при температуре кристаллизации, если вся
она при этой температуре полностью превратится в
твёрдое тело).
Удельную теплоту плавления любого вещества
можно найти в справочниках. Для льда же
Температура плавления у каждого вещества своя.
Её также можно найти в справочниках. Важно
подчеркнуть, что температура плавления вещества
равна температуре кристаллизации этого же
вещества. У льда tпл = 0° С.
Кипение или конденсация
При достижении жидкостью температуры кипения
начинает происходить другой фазовый переход –
кипение, при котором расстояния между молекулами
значительно увеличиваются, а силы
взаимодействия молекул уменьшаются. Вся
подводимая к жидкости теплота идет на разрыв
связей между молекулами. При конденсации пара в
жидкость, наоборот, расстояния между молекулами
значительно сокращаются, а силы взаимодействия
молекул увеличиваются. Для кипения жидкости
энергию к жидкости нужно подводить, при
конденсации пара энергия выделяется. Количество
теплоты, поглощаемое при кипении или выделяемое
при конденсации, рассчитывается по формуле:
где m – масса тела, кг; L – удельная
теплота парообразования,
Удельная теплота парообразования
показывает, сколько энергии нужно сообщить
одному килограмму жидкости, взятой при
температуре кипения, чтобы при этой температуре
полностью превратить её в пар (для конденсации:
сколько энергии выделяет один килограмм пара,
взятого при температуре конденсации, полностью
превращаясь в жидкость).
При одинаковом давлении температура кипения и
температура конденсации одного и того же
вещества одинаковы.
Температуры кипения и удельные теплоты
парообразования также можно найти в
справочниках. Для воды же они соответственно
равны: рис. 9 (при нормальном атмосферном
давлении).
Уравнение теплового баланса
Тела, участвующие в теплообмене, представляют
собой термодинамическую систему.
Термодинамическая система называется теплоизолированной,
если она не получает энергию извне и не отдаёт её;
теплообмен происходит только между телами,
входящими в эту систему. Для любой
теплоизолированной системы тел справедливо
следующее утверждение: количество теплоты,
отданное одними телами, равно количеству
теплоты, принимаемому другими телами.
Qотд. = Qполуч. (5)
Это утверждение описывает частный случай
закона сохранения и превращения энергии в
применении к процессу теплообмена. А формула (5)
является одним из видов уравнения теплового
баланса.
При решении задач с помощью данного вида
уравнения теплового баланса в формуле (1) в
качестве t2 следует брать большую
температуру, а в качестве t1 – меньшую.
Тогда разность (t2 – t1) будет
положительна и всё произведение cm(t2–t1)
также будет положительным. Все теплоты, отданные
и полученные, будут положительными.
Уравнение теплового баланса можно записать и в
таком виде:
Q1+ Q2+…+ Qn= 0, (6)
где n – количество тел системы.
Алгебраическая сумма всех количеств теплоты
(поглощенных и выделенных) в теплоизолированной
системе равна нулю.
Q1, Q2, …, Qn – это теплоты,
поглощаемые или выделяемые участниками
теплообмена. Очевидно, что в этом случае какие-то
теплоты должны быть положительны, а какие-то –
отрицательны. При записи уравнения теплового
баланса в виде (6) всегда t2 – конечная
температура, а t1 – начальная.
Если тело нагревается, то разность (t2 – t1)
положительна и все произведение cm(t2 – t1)
положительно. То есть Q > 0 тогда, когда теплота к
данному телу подводится.
А если t2 < t1 (тело остывает), то
разность (t2 – t1) отрицательна, то есть
Q < 0. В этом случае тело энергию выделяет.
Если при фазовом переходе энергия к телу
подводится (плавление, кипение), то Q > 0; если
тело выделяет энергию (кристаллизация,
конденсация), то Q < 0.
В принципе уравнения (5) и (6) равносильны.
Результат решения задачи не зависит от того,
каким видом уравнения пользуемся. Выбор способа
решения – за читателем.
Применим уравнение теплового баланса для
решения ряда задач (здесь приводим лишь одну
задачу, остальные материалы можно найти по
адресу http:// kirov-festival.nm.ru).
Задача 1
В медном калориметре массой 100 г находится 1 кг
воды при температуре 20° С. В воду опускают
свинцовую деталь массой 2 кг, имеющую температуру
90° С. До какой температуры нагреется вода? (В этой
и последующих задачах потерями теплоты в
калориметре пренебречь.)
Решение
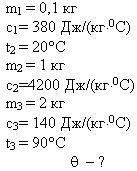 |
Проведём анализ:
Вода и калориметр При опускании в воду с температурой 20° С |
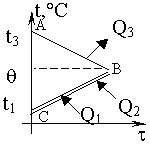 |
Изменение температур тел с течением времени удобно изображать на графике зависимости t(t ). Отрезок АВ соответствует |
| Два параллельных отрезка СВ соответствуют графикам изменения температур калориметра и воды. Стрелки, идущие к ним, показывают, что для нагревания калориметра и воды требуется энергия Q1 и Q2, которую они поглощают. |
|
| Решим задачу с использованием уравнения теплового баланса в виде (5): |
Решим задачу с использованием уравнения
теплового баланса в виде (6):
Ответ: Вода нагреется до 24° С.
Предлагаю читателю самостоятельно сделать
проверку размерности.
Напомним, остальной материал (полноценную
версию пособия) можно найти по адресу http:// kirov-festival.nm.ru.
Привет! Найти это всё очень просто, зная просто-напросто формулы.
Чтоб найти конечную температуру или t2 в физике, надо следовать вот этой формуле: t1+дельта t. Как видишь, всё просто.
t1 — это начальная температура, а дельта t — это изменение температуры.
Чтоб найти t1, надо сделать так: из t2 вычесть дельта t.
А чтобы найти дельту t, надо Q разделить на cm.
Чтобы найти массу, зная лишь объем, надо этот самый известный объем просто умножить на плотность вещества. Плотность можно найти в таблице плотностей, она есть в учебниках, на физике она часто встречается и её разрешают пользоваться.
—
Самое главное, — записывай всё, что диктует тебе учитель. Это важно! Зная формулы, легко решишь то, что тебе надо. Физику понимать надо, её не заучишь как тот же русский язык.
Тела, температура которых отличается, могут обмениваться тепловой энергией. То есть, между телами будет происходить теплообмен. Самостоятельно тепловая энергия переходит от более нагретых тел к менее нагретым.
Что такое теплообмен и при каких условиях он происходит
Тела, имеющие различные температуры, будут обмениваться тепловой энергией. Этот процесс называется теплообменом.
Теплообмен – процесс обмена тепловой энергией между телами, имеющими различные температуры.
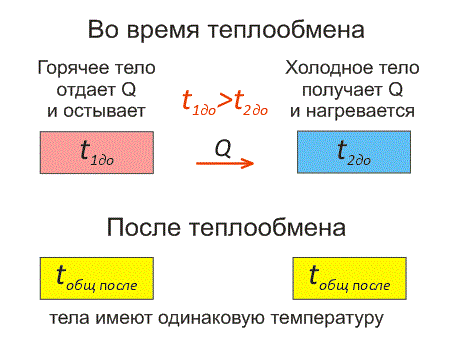
Рассмотрим два тела, имеющие различные температуры (рис. 1).
Тело, имеющее более высокую температуру, будет остывать и отдавать тепловую энергию телу, имеющему низкую температуру. А тело с низкой температурой будет получать количество теплоты и нагреваться.
Рис.1. Два тела во время теплообмена и после
На рисунке, горячее тело имеет розовый оттенок, а холодное изображено голубым цветом.
Когда температуры тел выравниваются, теплообмен прекращается.
Чтобы теплообмен происходил, нужно, чтобы тела имели различные температуры.
Когда температура тел выравняется, теплообмен прекратится.
Тепловое равновесие — это состояние, при котором тела имеют одинаковую температуру.
Уравнение теплового баланса и сохранение тепловой энергии
Когда тело остывает, оно отдает тепловую энергию (теплоту). Утерянное количество теплоты Q имеет знак «минус».
А когда тело нагревается – оно получает тепловую энергию. Приобретенное количество теплоты Q имеет знак «плюс».
Эти факты отражены на рисунке 2.
Рис. 2. Полученное количество теплоты имеет знак «+», а отданное Q – знак «-»
Закон сохранения тепловой энергии: Количество теплоты, отданное горячим телом равно количеству теплоты, полученному холодным телом.
Примечание: Существует и другая формулировка закона сохранения энергии: Энергия не появляется сама собой и не исчезает бесследно. Она переходит из одного вида в другой.
Уравнение теплового баланса
Тот факт, что тепловая энергия сохраняется, можно записать с помощью математики в виде уравнения. Такую запись называют уравнением теплового баланса.
Запишем уравнение теплового баланса для двух тел, обменивающихся тепловой энергией:
[large boxed{ Q_{text{остывания горяч}} + Q_{text{нагревания холод}} = 0 }]
(large Q_{text{остывания горяч}} left( text{Дж} right) ) – это количество теплоты горячее тело теряет.
(large Q_{text{нагревания холод}} left( text{Дж} right) ) – это количество теплоты холодное тело получает.
В левой части уравнения складываем количество теплоты каждого из тел, участвующих в теплообмене.
Записываем ноль в правой части уравнения, когда теплообмен с окружающей средой отсутствует. То есть, теплообмен происходит только между рассматриваемыми телами.
В некоторых учебниках применяют сокращения:
[large Q_{1} + Q_{2} = 0 ]
Примечание: Складывая два числа мы получим ноль, когда эти числа будут:
- равными по модулю и
- имеют различные знаки (одно число — знак «плюс», а второе – знак «минус»).
Если несколько тел участвуют в процессе теплообмена
Иногда в процессе теплообмена участвуют несколько тел. Тогда, для каждого тела нужно записать формулу количества теплоты Q. А потом все количества теплоты подставить в уравнение для теплового баланса:
[large boxed{ Q_{1} + Q_{2} + Q_{3} + ldots + Q_{n} = 0 } ]
При этом:
- Q для каждого нагреваемого тела будет обладать знаком «+»,
- Q для каждого охлаждаемого тела — знаком «-».
Пример расчетов для теплообмена между холодным и горячим телом
К горячей воде, массой 200 грамм, имеющей температуру +80 градусов Цельсия, добавили холодную воду, в количестве 100 грамм при температуре +15 градусов Цельсия. Какую температуру будет иметь смесь после установления теплового равновесия? Считать, что окружающая среда в теплообмене не участвует.
Примечание: Здесь мы рассматриваем упрощенную задачу, для того, чтобы облегчить понимание закона сохранения энергии. Мы не учитываем в этой задаче, что вода содержится в емкости. И часть тепловой энергии будет затрачиваться на то, чтобы изменить температуру емкости.
При решении других задач обязательно учитывайте, что емкость, в которой будет содержаться вещество, имеет массу. И часть тепловой энергии будет затрачиваться на то, чтобы изменить температуру емкости.
Решение:
В условии сказано, что окружающая среда в теплообмене не участвует. Поэтому, будем считать рассматриваемую систему замкнутой. А в замкнутых системах выполняются законы сохранения. Например, закон сохранения энергии.
Иными словами, с сосудом и окружающим воздухом теплообмен не происходит и, все тепловая энергия, отданная горячей водой, будет получена холодной водой.
1). Запишем уравнение теплового баланса, в правой части которого можно записать ноль:
[large Q_{text{остывания горяч}} + Q_{text{нагревания холод}} = 0 ]
2). Теперь запишем формулу для каждого количества теплоты:
[large Q_{text{остывания горяч}} = c_{text{воды}} cdot m_{text{горяч}} cdot (t_{text{общ}} — t_{text{горяч}} ) ]
[large Q_{text{нагревания холодн}} = c_{text{воды}} cdot m_{text{холодн}} cdot (t_{text{общ}} — t_{text{холодн}} ) ]
Примечания:
- (large c_{text{воды}} ) – удельную теплоемкость воды находим в справочнике;
- Массу воды переводим в килограммы;
- Горячая вода остывает и отдает тепловую энергию. Поэтому, разность (large (t_{text{общ}} — t_{text{горяч}} ) ) будет иметь знак «минус», потому, что конечная температура горячей воды меньше ее начальной температуры;
- Холодная вода получает тепловую энергию и нагревается. Из-за этого, разность (large (t_{text{общ}} — t_{text{холодн}} ) ) будет иметь знак «плюс», потому, что конечная температура холодной воды больше ее начальной температуры;
3). Подставим выражения для каждого Q в уравнение баланса:
[large c_{text{воды}} cdot m_{text{горяч}} cdot (t_{text{общ}} — t_{text{горяч}} ) + c_{text{воды}} cdot m_{text{холодн}} cdot (t_{text{общ}} — t_{text{холодн}} ) = 0 ]
4). Для удобства, заменим символы числами:
[large 4200 cdot 0,2 cdot (t_{text{общ}} — 80 ) + 4200 cdot 0,1 cdot (t_{text{общ}} — 15 ) = 0 ]
Проведем упрощение:
[large 840 cdot (t_{text{общ}} — 80 ) + 420 cdot (t_{text{общ}} — 15 ) = 0 ]
Раскрыв скобки и решив это уравнение, получим ответ:
[large t_{text{общ}} = 58,33 ]
Ответ: Температура смеси после прекращения теплообмена будет равна 58,33 градуса Цельсия.
Задача для самостоятельного решения:
В алюминиевом калориметре массой 100 грамм находится керосин массой 250 грамм при температуре +80 градусов Цельсия. В керосин поместили свинцовый шарик, массой 300 грамм. Начальная температура шарика +20 градусов Цельсия. Найдите температуру тел после установления теплового равновесия. Внешняя среда в теплообмене не участвует.
Примечание к решению: В левой части уравнения теплового баланса теперь будут находиться три слагаемых. Потому, что мы учитываем три количества теплоты:
- (large Q_{1} ) – охлаждение алюминия от температуры +80 градусов до конечной температуры;
- (large Q_{2} ) – охлаждение керосина от температуры +80 градусов до конечной температуры;
- (large Q_{3} ) – нагревание свинца от температуры +20 градусов до конечной температуры;
А справа в уравнение теплового баланса запишем ноль. Так как внешняя среда в теплообмене не участвует.
Выводы
- Если тела имеют различную температуру, то между ними возможен обмен тепловой энергией, т. е. теплообмен;
- Когда тела будут иметь равную температуру, теплообмен прекратится;
- Тело с высокой температурой, отдает тепловую энергию (теплоту) и остывает. Отданное количество теплоты Q имеет знак «минус»;
- А тело с низкой температурой получает тепловую энергию и нагревается. Полученное количество теплоты Q имеет знак «плюс»;
- Количество теплоты, отданное горячим телом равно количеству теплоты, полученному холодным телом. Это – закон сохранения тепловой энергии;
- Сохранение тепловой энергии можно записать в виде уравнения теплового баланса;
- В левой части уравнения складываем количества теплоты (всех тел, участвующих в теплообмене);
- В правой части уравнения записываем ноль, когда теплообмен с окружающей средой отсутствует.