Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
Содержание
- 1 Положение в таблице Менделеева
- 2 Алюминий
- 3 Положение активных металлов в таблице Менделеева
- 4 Свойства
- 5 Тест по теме
-
- 5.0.1 Оценка доклада
-
Положение в таблице Менделеева
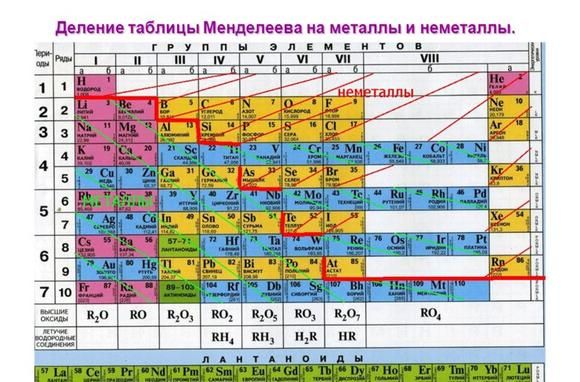
Металлические свойства элементов ослабевают слева направо в периодической таблице Менделеева. Поэтому наиболее активными считаются элементы I и II групп.
Рис. 1. Активные металлы в таблице Менделеева.
Все металлы являются восстановителями и легко расстаются с электронами на внешнем энергетическом уровне. У активных металлов всего один-два валентных электрона. При этом металлические свойства усиливаются сверху вниз с возрастанием количества энергетических уровней, т.к. чем дальше электрон находится от ядра атома, тем легче ему отделиться.
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
К щелочноземельным металлам относятся:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.
Узнать степень активности металла можно по электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен. Металлы, стоящие справа от водорода, малоактивны и могут взаимодействовать только с концентрированными кислотами.
Рис. 2. Электрохимический ряд напряжений металлов.
К списку активных металлов в химии также относят алюминий, расположенный в III группе и стоящий левее водорода. Однако алюминий находится на границе активных и среднеактивных металлов и не реагирует с некоторыми веществами при обычных условиях.
Алюминий
Алюминий представляет собой серебристо-белого цвета. Основные физические свойства алюминия – легкость, высокая тепло- и электропроводность. В свободном состоянии при пребывании на воздухе алюминий покрывается прочной пленкой оксида Al2O3, которая делает его устойчивым к действию концентрированных кислот.
Алюминий относится к металлам p-семейства. Электронная конфигурация внешнего энергетического уровня – 3s
2
3p
1
. В своих соединениях алюминий проявляет степень окисления равную «+3».
Алюминий получают электролизом расплава оксида этого элемента:
2Al2O3 = 4Al + 3O2↑
Однако из-за небольшого выхода продукта, чаще используют способ получения алюминия электролизом смеси Na3 и Al2O3. Реакция протекает при нагревании до 960С и в присутствии катализаторов – фторидов (AlF3, CaF2 и др.), при этом на выделение алюминия происходит на катоде, а на аноде выделяется кислород.
Алюминий способен взаимодействовать с водой после удаления с его поверхности оксидной пленки (1), взаимодействовать с простыми веществами (кислородом, галогенами, азотом, серой, углеродом) (2-6), кислотами (7) и основаниями (8):
2Al + 6H2O = 2Al(OH)3 +3H2↑ (1)
2Al +3/2O2 = Al2O3 (2)
2Al + 3Cl2 = 2AlCl3 (3)
2Al + N2 = 2AlN (4)
2Al +3S = Al2S3 (5)
4Al + 3C = Al4C3 (6)
2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑ (7)
2Al +2NaOH +3H2O = 2Na + 3H2↑ (8)
Положение активных металлов в таблице Менделеева
К активным металлам относятся три группы элементов:
- щелочные металлы;
- щелочноземельные металлы;
- алюминий.
Щелочные металлы находятся в первой группе таблицы Менделеева, то есть занимают в ней крайнее левое положение. В частности щелочными металлами являются:
- литий (Li);
- натрий (Na);
- калий (K);
- рубидий (Rb);
- цезий (Cs);
- франций (Fr).
Щелочноземельные металлы находятся во второй группе, то есть правее щелочных металлов. К ним относятся:
- бериллий (Be);
- магний (Mg);
- кальций (Ca);
- стронций (Sr);
- барий (Ba);
- радий (Ra).

В целом активные металлы отличаются тем, что имеют один или два валентных электрона, поэтому они легко отдают эти электроны в ходе химических реакций, выступая в качестве восстановителей. Степень активности металла можно оценить по его расположению в электрохимическом ряде активности металлов. Чем левее там находится металл, тем сильнее выражены его восстановительные свойства. Крайнее левое положение в ряде занимает литий. В вот крайне правое положение в ряду занимает золото, именно поэтому оно почти не окисляется кислотами.

Алюминий – это так называемый постпереходный металл, по своим свойствам он находится где-то между активными и среднеактивными металлами. Разные ученые придерживаются различного мнения о том, стоит ли считать алюминий активным металлом.
Активные металлы не встречаются в природе в чистом виде, так как они быстро вступают в химические реакции с другими элементами. Чаще всего в природе они присутствуют в виде оксидов. Например, даже если алюминий получен в чистом виде, то на воздухе он быстро покрывается оксидной пленкой.
Свойства
Активные металлы отличаются мягкостью (можно разрезать ножом), лёгкостью, невысокой температурой плавления.
Основные химические свойства металлов представлены в таблице.
|
Реакция |
Уравнение |
Исключение |
|
Щелочные металлы самовозгораются на воздухе, взаимодействуя с кислородом |
K + O2 → KO2 |
Литий реагирует с кислородом только при высокой температуре |
|
Щелочноземельные металлы и алюминий на воздухе образуют оксидные плёнки, а при нагревании самовозгораются |
2Ca + O2 → 2CaO |
|
|
Реагируют с простыми веществами, образуя соли |
– Ca + Br2 → CaBr2; |
Алюминий не вступает в реакцию с водородом |
|
Бурно реагируют с водой, образуя щёлочи и водород |
– 2Na + 2H2O → 2NaOH + H2; |
Реакция с литием протекает медленно. Алюминий реагирует с водой только после удаления оксидной плёнки |
|
Реагируют с кислотами, образуя соли |
– Ca + 2HCl → CaCl2 + H2; – 2K + 2HMnO4 → 2KMnO4 + H2 |
|
|
Взаимодействуют с растворами солей, сначала реагируя с водой, а затем с солью |
2Na + CuCl2 + 2H2O: – 2Na + 2H2O → 2NaOH + H2; |
Активные металлы легко вступают в реакции, поэтому в природе находятся только в составе смесей – минералов, горных пород.
Рис. 3. Минералы и чистые металлы.
Тест по теме
Доска почёта
Чтобы попасть сюда — пройдите тест.
-
Александр Котков
5/5
-
Илья Ударцев
5/5
-
Инесса Медведева
4/5
-
Александр Котков
5/5
-
Лидия Маслова
5/5
-
Александр Котков
5/5
-
Сергей Ефремов
2/5
-
Дима Мухтаров
5/5
-
Сергей Макаров
5/5
-
Александр Просто
5/5
Оценка доклада
Средняя оценка: 4.4. Всего получено оценок: 705.
|
Поделитесь в соц.сетях: |
Оцените статью:
|
Содержание
- — Какой металл считается активным?
- — Какой металл активнее рубидий или цезий?
- — Какой из металлов самый активный элемент?
- — Какие металлы не активные?
- — Какой самый твердый металл в мире?
- — Какие металлы самые лёгкие?
- — Какие свойства проявляют щелочные металлы?
- — Как определить щелочные металлы?
- — Какой металл является Щелочноземельным?
- — Как найти самый активный металл?
- — Какой самый пластичный металл?
- — Почему франций самый активный металл?
- — Какие металлы не реагируют с кислотой?
- — Какие неметаллы не реагируют с водой?
- — Почему водород не является металлом?
Какой металл считается активным?
Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
…
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
Какой металл активнее рубидий или цезий?
Цезий и рубидий очень похожи по своим свойствам, а в химическом отношении они похожи на калий и являются самыми активными из всех стабильных элементов, встречающихся в природе в виде тех или иных соединений.
Какой из металлов самый активный элемент?
Элементы: Цезий – самый активный металл
Какие металлы не активные?
Активность металлов убывает слева направо:
- Металлы, стоящие в ЭХ ряду после водорода, называют неактивными металлами. …
- Все металлы, стоящие в ряду левее водорода, вытесняют его из разбавленных кислот, а металлы, расположенные справа от водорода, с растворами кислот не реагируют (азотная кислота – исключение).
Какой самый твердый металл в мире?
В наше время продолжаются эксперименты, благодаря которым можно выявить самые прочные металлы в мире.
- 1 Иридий Самый прочный металл – иридий – серебристо-белый, твердый и тугоплавкий, который относится к платиновой группе.
- 2 Рутений …
- 3 Тантал …
- 4 Хром …
- 5 Бериллий …
- 6 Осмий …
- 7 Рений …
- 8 Вольфрам …
11 дек. 2020 г.
Какие металлы самые лёгкие?
Классификация металлов по плотности
По плотности металлы делят на: легкие — (плотность < 5 г/см3). К ним относят: литий, натрий, калий, магний, алюминий и др. Самый легкий — литий (Li, r=0,53г/см3).
Какие свойства проявляют щелочные металлы?
Щелочные металлы – это серебристо-белые вещества с характерным металлическим блеском. Они быстро тускнеют на воздухе из-за окисления. Это мягкие металлы, по мягкости Na, K, Rb, Cs подобны воску. Они легко режутся ножом.
Как определить щелочные металлы?
Щелочны́е мета́ллы — элементы 1-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы главной подгруппы I группы): литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr.
Какой металл является Щелочноземельным?
Щёлочноземе́льные мета́ллы — химические элементы 2-й группы периодической таблицы элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba), радий (Ra).
Как найти самый активный металл?
Активность металлов в системе Менделеева возрастает сверху вниз и справа налево, таким образом, самый активный — франций, на последнем слое у которого 1 электрон, расположенный достаточно далеко от ядра.
Какой самый пластичный металл?
золото: самый пластичный (из 1 г этого металла можно вытянуть проволоку длиной 2,4 км);
Почему франций самый активный металл?
Самый активный металл — франций (Fr). Франций легче всего отдает электрон внешнего слоя. Он обладает самым большим атомным радиусом, поэтому энергия взаимодействия ядра атома с внешней электронной оболочкой мала.
Какие металлы не реагируют с кислотой?
С концентрированной азотной кислотой не взаимодействуют благородные металлы (Au, Ru, Os, Rh, Ir, Pt), а ряд металлов (Al, Ti, Cr, Fe, Co, Ni) при низкой температуре пассивируются концентрированной азотной кислотой.
Какие неметаллы не реагируют с водой?
Из неметаллов с водой реагируют только наиболее активные – фтор, хлор, бром и йод. Фтор, хлор, бром и йод реагируют со щелочами по той же схеме, что и с водой, только образуются не кислоты, а их соли, и реакции не обратимы, а протекают до конца.
Почему водород не является металлом?
Водород – неметалл, имеет молекулярное строение. Молекула водорода состоит из двух атомов, связанных между собой ковалентной неполярной связью. Энергия связи в молекуле водорода составляет 436 кДж/моль, что объясняет низкую химическую активность молекулярного водорода. … В своих соединениях водород всегда одновалентен.
Интересные материалы:
Как на самсунге сохранить контакты на сим карту?
Как начисляются проценты на остаток денежных средств на банковской карте?
Как найти карту клада в майнкрафте?
Как найти особняк по карте в Майнкрафт?
Как найти Сбербанк Онлайн реквизиты карты?
Как найти Сириус на карте?
Как найти старые карты гугл?
Как найти свою карту Летуаль?
Как настроить голос в Яндекс картах?
Как настроить карту халва?
Содержание
- 1 2.2. Устройство и работа гальванического элемента
- 1.1 3. 1. Качественное определение различной электрохимической активности металлов
- 2 Ряд активности металлов в химии
- 2.1 Алюминий
- 2.2 Кальций
- 2.3 Железо и его соединения
- 2.4 Производство чугуна и стали
- 2.5 Примеры решения задач
- 3 Как определить активность металла
- 3.1 Свойства металлов
- 3.2 Благородные металлы
- 3.3 Щелочные металлы
- 3.4 Щелочноземельные металлы
- 3.5 Металлы 3-й и 4-й групп
- 3.6 Переходные металлы
- 3.7 Ряд активности
- 3.8 Металлы и пламя
- 3.9 Коррозия
2.2. Устройство и работа гальванического элемента
Возникновениеэлектродного потенциала на металлическихэлектродах делает возможной работугальванического элемента.
Гальваническийэлемент – это система, состоящая издвух электродов, на поверхности которыххимическая энергия окислительно-восстановительныхпроцессов превращается в электрическуюэнергию.
Гальваническийэлемент состоит из двух различныхметаллических электродов, каждый изкоторых погружен в раствор своей соли.Растворы солей должны быть разделеныпористой перегородкой, котораяпрепятствует смешению растворов, нодает возможность анионам электролитапереходить из одного раствора вдругой. Иногда растворы солей помещаютв разные сосуды, тогда их соединяютэлектролитическим мостиком, предназначеннымтакже для осуществления ионнойпроводимости в элементе.
Электрод,помещенный в раствор своей соли, образуетполуэлемент. Таким образом, гальваническийэлемент состоит из двух полуэлементов.В каждом полуэлементе возникаетэлектродный потенциал. Посколькуметаллы, из которых сделаны электроды,различны, то и электродные потенциалыбудут иметь разное значение.
Если этидва полуэлемента соединить между собойпроводником первого рода, то электроныначнут переходить от электрода, где ихбольше (электродный потенциал меньшепо своей величине), к электроду, накотором электронов меньше (электродныйпотенциал больше по величине). Этотпереход электронов вызовет нарушениеравновесия в двойном электрическомслое на обоих электродах.
При этом наэлектроде с меньшим электроднымпотенциалом новое количество катионовметалла перейдут в раствор, а навтором электроде с большим электроднымпотенциалом катионы из раствора перейдутна электрод. Таким образом, на первомэлектроде будет проходить реакцияокисления:
Ме1-nе= Me1+n,
гдеMe1– первый металл;
n– число электронов;
ана втором электроде будет идти реакциявосстановления:
.
Me2+n+ ne= Me2,
гдеМе2– второй металл.
Электрод,на котором протекает реакция окисления(электрод с меньшим электроднымпотенциалом), называется анодом. Электрод,на котором протекает реакция восстановления(электрод с большим потенциалом),называется катодом. Разность потенциаловэлектродов служит мерой способностигальванического элемента совершатьэлектрическую работу и называетсяэлектродвижущей силой (ЭДС) и обозначаетсяЕт.э.ЭДС гальванического элемента равнаразности потенциалов катода и анода:Ет.е.= Екатода- Еанода.Схематически можно записать формулугальванического элемента следующимобразом:
Ме1 | Me1+nx || Me2+nx | Me2
раствор раствор
Вформуле одна вертикальная чертаобозначает границу раздела твердойфазы и раствора; двойная вертикальнаячерта — граница раздела растворов,стрелки указывают направление переходаэлектронов.
3. 1. Качественное определение различной электрохимической активности металлов
Установитеопытным путем относительную активностьшести металлов: меди, железа, олова,свинца, алюминия и цинка. Для этоговозьмите шесть пробирок, внесите вкаждую из них по 12-15 капель одного изследующих растворов: соли меди (II),соли железа (II),соли свинца (II),соли алюминия и соли цинка.
Во всерастворы, кроме раствора соли меди,опустите на 1-2 минуты по кусочку медиили медной проволоки.
В какой пробиркекрасная медь покрылась налетом другогометалла? Что это за металл, оказавшийсяменее активным, чем медь? Напишите вионном виде уравнение реакциивзаимодействия меди с ионами этогометалла.
Выньтеиз пробирок медные полоски и опуститево все пробирки, кроме раствора солижелеза (II),железную проволоку или кусочки железа.Какие металлы вытесняются из растворасолей железом? Напишите уравненияреакций взаимодействия железа с ионамиэтих металлов. Какова восстановительнаяактивность железа по сравнению свытесненными металлами?
Проведитеаналогичные опыты с кусочками свинца,алюминия, олова и пинка. Наблюдайтекаждый раз, в каких пробирках происходитвытеснение металла из его соли. Напишитеуравнения протекающих реакций суказанием направления переходаэлектронов. Результаты опытов запишитев следующей таблице.
| Опускаемыйметалл | Ионы металлов в растворе | ||||
| Cu2+ | Fe2+ | Pb2+ | Al3+ | Sn2+ | Zn2+ |
| Cu | |||||
| Fe | |||||
| Pb | |||||
| Al | |||||
| Sn | |||||
| Zn |
Знаком(+) под соответствующими ионами металловобозначайте вытеснение металлов израствора своей соли при действии тогоили другого чистого металла и знаком(-), если вытеснения не происходит.
Какойиз исследованных металлов самый активныйи вытеснил все остальные из их солей?Какой металл наименее активный?Расположите все остальные исследованныеметаллы между ними в порядке убывающейвосстановительной активности.
Напишитев ряду активности под каждым металломего нормальный электродный потенциал.Соответствует ли составленный вами рядпоследовательности расположенияметаллов в ряду нормальных электродныхпотенциалов? Принимая электродныйпотенциал водорода равным 0, поместитеводород в полученный ряд активности.
Какие из исследованных металлов могутвытеснить водород из разбавленныхкислот?
Источник: https://studfile.net/preview/3549070/page:41/
Ряд активности металлов в химии
Все металлы, в зависимости от их окислительно-восстановительной активности объединяют в ряд, который называется электрохимическим рядом напряжения металлов (так как металлы в нем расположены в порядке увеличения стандартных электрохимических потенциалов) или рядом активности металлов:
Li, K, Ва, Ca, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, H2, Cu, Hg, Ag, Рt, Au
Наиболее химически активные металлы стоят в ряду активности до водорода, причем, чем левее расположен металл, тем он активнее. Металлы, занимающие в ряду активности, место после водорода считаются неактивными.
Алюминий
Алюминий представляет собой серебристо-белого цвета. Основные физические свойства алюминия – легкость, высокая тепло- и электропроводность. В свободном состоянии при пребывании на воздухе алюминий покрывается прочной пленкой оксида Al2O3, которая делает его устойчивым к действию концентрированных кислот.
Алюминий относится к металлам p-семейства. Электронная конфигурация внешнего энергетического уровня – 3s23p1. В своих соединениях алюминий проявляет степень окисления равную «+3».
Алюминий получают электролизом расплава оксида этого элемента:
2Al2O3 = 4Al + 3O2↑
Однако из-за небольшого выхода продукта, чаще используют способ получения алюминия электролизом смеси Na3[AlF6] и Al2O3. Реакция протекает при нагревании до 960С и в присутствии катализаторов – фторидов (AlF3, CaF2 и др.), при этом на выделение алюминия происходит на катоде, а на аноде выделяется кислород.
Алюминий способен взаимодействовать с водой после удаления с его поверхности оксидной пленки (1), взаимодействовать с простыми веществами (кислородом, галогенами, азотом, серой, углеродом) (2-6), кислотами (7) и основаниями (8):
2Al + 6H2O = 2Al(OH)3 +3H2↑ (1)
2Al +3/2O2 = Al2O3 (2)
2Al + 3Cl2 = 2AlCl3 (3)
2Al + N2 = 2AlN (4)
2Al +3S = Al2S3 (5)
4Al + 3C = Al4C3 (6)
2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑ (7)
2Al +2NaOH +3H2O = 2Na[Al(OH)4] + 3H2↑ (8)
Кальций
В свободном виде Ca – серебристо-белый металл. При нахождении на воздухе мгновенно покрывается желтоватой пленкой, которая представляет собой продукты его взаимодействия с составными частями воздуха. Кальций – достаточно твердый металл, имеет кубическую гранецентрированную кристаллическую решетку.
Электронная конфигурация внешнего энергетического уровня – 4s2. В своих соединениях кальций проявляет степень окисления равную «+2».
Кальций получают электролизом расплавов солей, чаще всего – хлоридов:
CaCl2 = Ca + Cl2↑
Кальций способен растворяются в воде с образованием гидроксидов, проявляющих сильные основные свойства (1), реагировать с кислородом (2), образуя оксиды, взаимодействовать с неметаллами (3 -8), растворяться в кислотах (9):
Ca + H2O = Ca(OH)2 + H2↑ (1)
2Ca + O2 = 2CaO (2)
Ca + Br2 =CaBr2 (3)
3Ca + N2 = Ca3N2 (4)
2Ca + 2C = Ca2C2 (5)
Ca +S = CaS (6)
2Ca + 2P = Ca3P2 (7)
Ca + H2 = CaH2 (8)
Ca + 2HCl = CaCl2 + H2↑ (9)
Железо и его соединения
Железо – металл серого цвета. В чистом виде оно довольно мягкое, ковкое и тягучее. Электронная конфигурация внешнего энергетического уровня – [Ar]3d 64s2. В своих соединениях железо проявляет степени окисления «+2» и «+3».
Металлическое железо реагирует с водяным паром, образуя смешанный оксид (II, III) Fe3O4:
3Fe + 4H2O(v) ↔ Fe3O4 + 4H2↑
На воздухе железо легко окисляется, особенно в присутствии влаги (ржавеет):
3Fe + 3O2 + 6H2O = 4Fe(OH)3
Как и другие металлы железо вступает в реакции с простыми веществами, например, галогенами (1), растворяется в кислотах (2):
2Fe + Br2 = 2FeBr3 (при нагревании) (1)
Fe + 2HCl = FeCl2 + H2↑ (2)
Железо образует целый спектр соединений, поскольку проявляет несколько степеней окисления: гидроксид железа (II), гидроксид железа (III), соли, оксиды и т.д. Так, гидроксид железа (II) можно получить при действии растворов щелочей на соли железа (II) без доступа воздуха:
FeSO4 + 2NaOH = Fe(OH)2↓ + Na2SO4
Гидроксид железа (II) растворим в кислотах и окисляется до гидроксида железа (III) в присутствии кислорода.
Соли железа (II) проявляют свойства восстановителей и превращаются в соединения железа (III).
Оксид железа (III) нельзя получить по реакции горения железа в кислороде, для его получения необходимо сжигать сульфиды железа или прокаливать другие соли железа:
4FeS2 + 11O2 = 2Fe2O3 +8SO2↑
2FeSO4 = Fe2O3 + SO2↑ + 3H2O
Соединения железа (III) проявляют слабые окислительные свойства и способны вступать в ОВР с сильными восстановителями:
2FeCl3 + H2S = Fe(OH)3↓ + 3NaCl
Производство чугуна и стали
Стали и чугуны – сплавы железа с углеродом, причем содержание углерода в стали до 2%, а в чугуне 2-4%. Стали и чугуны содержат легирующие добавки: стали– Cr, V, Ni, а чугун – Si.
Выделяют различные типы сталей, так, по назначению выделяют конструкционные, нержавеющие, инструментальные, жаропрочные и криогенные стали. По химическому составу выделяют углеродистые (низко-, средне- и высокоуглеродистые) и легированные (низко-, средне- и высоколегированные). В зависимости от структуры выделяют аустенитные, ферритные, мартенситные, перлитные и бейнитные стали.
Стали нашли применение во многих отраслях народного хозяйства, таких как строительная, химическая, нефтехимическая, охрана окружающей среды, транспортная энергетическая и другие отрасли промышленности.
В зависимости от формы содержания углерода в чугуне — цементит или графит, а также их количества различают несколько типов чугуна: белый (светлый цвет излома из-за присутствия углерода в форме цементита), серый (серый цвет излома из-за присутствия углерода в форме графита), ковкий и жаропрочный. Чугуны очень хрупкие сплавы.
Области применения чугунов обширны – из чугуна изготавливают художественные украшения (ограды, ворота), корпусные детали, сантехническое оборудование, предметы быта (сковороды), его используют в автомобильной промышленности.
Примеры решения задач
Источник: http://ru.solverbook.com/spravochnik/ximiya/9-klass/ryad-aktivnosti-metallov/
Как определить активность металла
У всех металлов есть общие физические свойства, например блеск и электропроводность, однако в зависимости от химических свойств они делятся на несколько групп. Такие металлы, как калий и натрий, очень активны и мгновенно вступают в реакции с водой и воздухом, в то время как золото вообще не вступает в реакции. На рисунке изображена золотая маска царя Микен (см. статью «Загадочные жители Греции»)
Свойства металлов
При комнатной температуре (20 °С) все металлы, кроме ртути, пребывают в твердом состоянии и хорошо проводят тепло и электричество. На срезе металлы блестят и некоторые, как железо и никель, обладают магнитными свойствами. Многие металлы пластичны — из них можно делать проволоку — и ковки — им несложно придать другую форму.
Благородные металлы
Благородные металлы в земной коре встречаются в чистом виде, а не в составе соединений. К ним относятся медь, серебро, золото и платина. Они химически пассивны и с трудом вступают в химические реакции с другими элементами.
Медь — благородный металл. Золото — один из самых инертных элементов. Из-за своей инертности благородные металлы не подвержены коррозии, поэтому из них делают украшения и монеты.
Золото настолько инертно, что древние золотые изделия до сих пор ярко сияют.
Щелочные металлы
Группу 1 в периодической таблице составляют 6 очень активных металлов, в т.ч. натрий и калий. Они плавятся при сравнительно низкой температуре (температура плавления калия 64 °С) и настолько мягкие, что их можно резать ножом. Вступая в реакцию с водой, эти металлы образуют щелочной раствор и поэтому называются щелочными. Калий бурно реагирует с водой. При этом выделяется водород, который сгорает сиреневым пламенем.
Щелочноземельные металлы
Шесть металлов, составляющих 2-ю группу периодической таблицы (в т.ч. магний и кальций), называются щелочноземельными. Эти металлы входят в состав множества минералов.
Так, кальций имеется в кальците, прожилки которого можно обнаружить в известняке и меле. Щелочноземельные металлы менее активны, чем щелочные, они тверже и плавятся при более высокой температуре. Кальций содержится в ракушках, костях и губках.
Магний входит в состав хлорофилла, зеленого пигмента, необходимого для фотосинтеза.
Металлы 3-й и 4-й групп
Семь металлов этих групп расположены в периодической таблице справа от переходных металлов. Алюминий — один из наименее плотных металлов, поэтому он легкий. А вот свинец очень плотный; из него делают экраны, защищающие от рентгеновских лучей. Все эти металлы довольно мягкие и плавятся при относительно низкой температуре. Многие из них используются в сплавах — создаваемых с определенными целями смесях металлов. Велосипеды и самолеты делают из алюминиевых сплавов.
Переходные металлы
Переходные металлы обладают типично металлическими свойствами. Они прочные, твердые, блестящие и плавятся при высоких температурах. Они менее активны, чем щелочные и щелочноземельные металлы. К ним относятся железо, золото, серебро, хром, никель, медь.
Они все ковкие и широко применяются в промышленности — как в чистом виде, так и в виде сплавов. Около 77% от массы автомобиля составляют металлы, в основном сталь, т.е. сплав железа и углерода (см. статью «Железо, сталь и прочие металлы«). Ступицы колес делают из хромированной стали — для блеска и предохранения от коррозии.
Корпус машины сделан из листовой стали. Стальные бамперы предохраняют автомобиль в случае столкновения.
Ряд активности
Положение металла в ряду активности показывает, насколько охотно металл вступает в реакции. Чем более активен металл, тем легче он отнимает кислород у менее активных металлов.
Активные металлы трудно выделить из соединений, тогда как малоактивные металлы встречаются в чистом виде. Калий и натрий хранят в керосине, так как они моментально вступают в реакции с водой и воздухом. Медь – наименее активный металл из числа недорогих.
Она используется в производстве труб, резервуаров для горячей воды и электрических проводов.
Металлы и пламя
Некоторые металлы, если поднести их к огню, придают пламени определенный оттенок. По цвету пламени можно определить присутствие в соединении того или иного металла. Для этого крупинку вещества помешают в пламя на конце проволоки из инертной платины.
Соединении натрия окрашивают пламя в желтый цвет, соединения меди — в сине-зеленый, соединении кальции — в красный, и калия — в сиреневый. В состав фейерверков входят разные металлы, сообщающие пламени разные оттенки.
Барий дает зеленый цвет, стронций — красный, натрий — желтый, а медь — сине-зеленый.
Коррозия
Коррозия — это химическая реакция, происходящая при контакте металла с воздухом или водой. Металл взаимодействует с кислородом воздуха, и на его поверхности образуется оксид. Металл теряет блеск и покрывается налетом. Высокоактивные металлы подвергаются коррозии быстрее, чем менее активные.
Рыцари смазывали стальные доспехи маслом или воском, чтобы они не ржавели (сталь содержит много железа). Для предохранения от ржавчины стальной корпус автомобиля покрывают несколькими слоями краски. Некоторые металлы (например, алюминий) покрываются защищающей их плотной оксидной пленкой.
Железо при коррозии образует неплотную пленку оксида, которая при реакции с водой дает ржавчину. Слой ржавчины легко осыпается, и процесс коррозии распространяется вглубь. Для предохранения от коррозии стальные консервные банки покрывают слоем олова — менее активного металла. Крупные сооружения, например мосты, спасает от коррозии краска.
Источник: https://masakarton.com/kak-opredelit-aktivnost-metalla/
Активные металлы

4.4
Средняя оценка: 4.4
Всего получено оценок: 1349.
4.4
Средняя оценка: 4.4
Всего получено оценок: 1349.
Металлы, легко вступающие в реакции, называются активными металлами. К ним относятся щелочные, щелочноземельные металлы и алюминий.
Положение в таблице Менделеева
Металлические свойства элементов ослабевают слева направо в периодической таблице Менделеева. Поэтому наиболее активными считаются элементы I и II групп.
Все металлы являются восстановителями и легко расстаются с электронами на внешнем энергетическом уровне. У активных металлов всего один-два валентных электрона. При этом металлические свойства усиливаются сверху вниз с возрастанием количества энергетических уровней, т.к. чем дальше электрон находится от ядра атома, тем легче ему отделиться.
Наиболее активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
К щелочноземельным металлам относятся:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.
Узнать степень активности металла можно по электрохимическому ряду напряжений металлов. Чем левее от водорода расположен элемент, тем более он активен. Металлы, стоящие справа от водорода, малоактивны и могут взаимодействовать только с концентрированными кислотами.
К списку активных металлов в химии также относят алюминий, расположенный в III группе и стоящий левее водорода. Однако алюминий находится на границе активных и среднеактивных металлов и не реагирует с некоторыми веществами при обычных условиях.
Свойства
Активные металлы отличаются мягкостью (можно разрезать ножом), лёгкостью, невысокой температурой плавления.
Основные химические свойства металлов представлены в таблице.
|
Реакция |
Уравнение |
Исключение |
|
Щелочные металлы самовозгораются на воздухе, взаимодействуя с кислородом |
K + O2 → KO2 |
Литий реагирует с кислородом только при высокой температуре |
|
Щелочноземельные металлы и алюминий на воздухе образуют оксидные плёнки, а при нагревании самовозгораются |
2Ca + O2 → 2CaO |
|
|
Реагируют с простыми веществами, образуя соли |
– Ca + Br2 → CaBr2; |
Алюминий не вступает в реакцию с водородом |
|
Бурно реагируют с водой, образуя щёлочи и водород |
– 2Na + 2H2O → 2NaOH + H2; |
Реакция с литием протекает медленно. Алюминий реагирует с водой только после удаления оксидной плёнки |
|
Реагируют с кислотами, образуя соли |
– Ca + 2HCl → CaCl2 + H2; – 2K + 2HMnO4 → 2KMnO4 + H2 |
|
|
Взаимодействуют с растворами солей, сначала реагируя с водой, а затем с солью |
2Na + CuCl2 + 2H2O: – 2Na + 2H2O → 2NaOH + H2; |
Активные металлы легко вступают в реакции, поэтому в природе находятся только в составе смесей – минералов, горных пород.
Что мы узнали?
К активным металлам относятся элементы I и II групп – щелочные и щелочноземельные металлы, а также алюминий. Их активность обусловлена строением атома – немногочисленные электроны легко отделяются от внешнего энергетического уровня. Это мягкие лёгкие металлы, быстро вступающие в реакцию с простыми и сложными веществами, образуя оксиды, гидроксиды, соли. Алюминий находится ближе к водороду и для его реакции с веществами требуются дополнительные условия – высокие температуры, разрушение оксидной плёнки.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Руслан Катылов
5/5
-
Александр Котков
5/5
-
Илья Ударцев
5/5
-
Инесса Медведева
4/5
-
Александр Котков
5/5
-
Лидия Маслова
5/5
-
Александр Котков
5/5
-
Сергей Ефремов
2/5
-
Дима Мухтаров
5/5
-
Сергей Макаров
5/5
Оценка доклада
4.4
Средняя оценка: 4.4
Всего получено оценок: 1349.
А какая ваша оценка?
Содержание:
- Химическая активность металлов
- Реакции металлов с кислородом и водой
- Взаимодействие металлов с кислотами. ряд активности металлов
- Взаимодействие металлов с растворами солей
Электрохимический ряд активности металлов (ряд напряжений, ряд стандартных электродных потенциалов) — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0, отвечающих полуреакции восстановления катиона металла Men+: Men+ + nē → Me
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Химическая активность металлов
Электрохимический ряд активности металлов показывает, какие из металлов более активные, какие менее. Расположение элементов в горизонтальном ряду слева направо показывает направление снижения восстановительной способности и возрастание окислительной.
Реакции металлов с кислородом и водой
Что вы знаете о ржавлении железа? Расскажите о разрушении металлов?
Как вы думаете, как можно защитить металлы от разрушения? Где применяются металлы? Приведите примеры из жизни.
Металлы мы часто применяем в повседневной жизни. Это алюминий, медь, железо, золото, серебро и т. д. Алюминий и медь применяются для изготовления проводов. Алюминиевой фольгой упаковывают лекарства. В домашнем обиходе вы часто встречаете алюминиевую посуду и упаковки для напитков. Но больше всего применяется железо для изготовления различных металлоконструкций, трубопроводов, деталей машин и т. д. Этот металл от
воды и кислорода воздуха приходит в негодность, изменяет цвет и тускнеет.
Железо покрывается ржавчиной красно-бурого цвета. Железо + вода + воздух → ржавчина. Такой химический процесс называется коррозией (от лат. corrodere – разъедать).
Самопроизвольное разрушение металлов в результате их взаимодействия с веществами окружающей среды называется коррозией.
Поверхность алюминия покрывается оксидной пленкой, которая препятствует коррозии:
Химические активные металлы легко окисляются кислородом воздуха (Na, Mg, Ca). Железо и медь окисляются только при нагревании:
А золото и некоторые благородные металлы вообще не окисляются кислородом.
Рассмотрите рисунок 15 и сами сделайте выводы.
Ежегодно четвертая часть всего производимого металла из-за коррозии приходит в негодность (рис. 16).
Знаменитую Эйфелеву башню в Париже красили уже 18 раз, в результате чего ее масса увеличилась на 70 т.
Коррозия вызывает серьезные экологические катастрофы. Из разрушенных трубопроводов может быть утечка газа, нефти, опасных химических продуктов.
Это приводит к загрязнению окружающей среды, что отрицательно влияет на здоровье и жизнь людей.
Металлы защищают от коррозии нанесением покрытий на поверхность изделия: окраска металла лаками, красками, эмалями. Но это покрытие недолговечно. Предохраняют металл покрытием другого металла, менее подверженного коррозии. Это – золото, серебро, хром, никель, олово, цинк и др. В повседневной жизни часто применяют оцинкованные ведра, никелированные кровати. Для консервных банок применяют железо, покрытое оловом. Такое железо называют белой жестью. Белую жесть получают в г. Темиртау Карагандинской области на металлургическом заводе. Можно уменьшить коррозию железа, добавляя другие металлы: никель, хром, молибден. Таким образом, получают сплав, который называется нержавеющей сталью. Из этой стали изготавливают столовые приборы, трубы и другие изделия.
Олово — достаточно редкий, но очень полезный металл. Известно, что его начали добывать раньше, чем железо.
Олово — это мягкий белый металл, который можно сплавлять с медью, чтобы получить бронзу. Олово — один из первых освоенных человеком металлов. Оно не подвержено коррозии, поэтому из него делают тару для упаковки. Слой олова, нанесенный на другие металлы, делает их поверхность гладкой и блестящей. Банки для хранения консервов и напитков также делают из тонкого стального листа, покрытого оловом.
Взаимодействие воды с некоторыми металлами (рис. 17).
1. Взаимодействие воды с активными металлами в обычных условиях идет очень интенсивно.
При этом протекают реакции замещения
При проведении таких опытов необходимо соблюдать меры предосторожности.
2. При взаимодействии металлов средней активности с водой вместо щелочи выделяется оксид металла:
3. Малоактивные металлы (Cu) с водой не реагируют.
Коррозия, ржавчина, защита от коррозии, белая жесть, алюминиевая фольга, сплав
Свинец — тяжелый голубовато-серый металл, который не ржавеет. Он используется в автомобильных аккумуляторах. Свинцовые экраны защищают людей от опасной радиации. Но свинец токсичен и ядовит для человека.
Демонстрация №2
Взаимодействие активных металлов с холодной и горячей водой
Демонстрацию выполняет учитель, учащиеся наблюдают, делают выводы.
Цель: узнать, как реагируют активные металлы с холодной и горячей водой.
Обрежьте кусочек натрия скальпелем, высушите фильтровальной бумагой. Высушенный кусочек натрия следует бросить в кристаллизатор с холодной, а затем горячей водой. Наблюдать за ходом реакции через стекло вытяжного шкафа. Такую же реакцию проделать и с металлическим кальцием. Испытать полученные растворы двумя индикаторами.
Взаимодействие металлов с кислотами. ряд активности металлов
Что такое кислоты? Какие кислые вещества вы встречали в природе?
В соответствии с определением кислоты должны вступать в реакции с металлами. Все ли металлы взаимодействуют с кислотами? Это можно проверить на опыте.
В четыре пронумерованные пробирки нальем одинаковое количество раствора соляной кислоты и добавим: в первую пробирку – Mg; во вторую – Zn; в третью – Sn; в четвертую – Cu.
Как видим, не все металлы могут взаимодействовать с кислотами и скорости их взаимодействия различны (рис. 18).
На основании интенсивности взаимодействия металлов с кислотами русским ученым Н.Н. Бекетовым был составлен ряд активности металлов:
Li K Ca Na Mg Al Zn Fe Ni Sn Pb (H2) Cu Hg Ag Au
При использовании ряда химической активности нужно помнить
следующие правила:
1) металлы, стоящие в начале этого ряда, химически активны, они могут вытеснить водород из воды.
2) активность металлов в этом ряду снижается слева направо
3) только металлы, стоящие в ряду активности до водорода, вытесняют водород из растворов кислот 
активный металл + кислота —> соль + водород
Протекает реакция замещения.
Металлы, стоящие в ряду активности после водорода, не реагируют с разбавленными растворами кислот (табл. 6).
Лабораторный опыт №3
Взаимодействие металлов с растворами кислот
Цель: исследовать реакции различных металлов с растворами кислот и
сделать вывод о существовании химически инертных металлов.
Налейте в четыре пробирки раствор соляной кислоты. В одну из пробирок насыпьте порошка магния, в другую – поместите гранулы цинка, в третью – опилки железа, в четвертую – стружки меди.
Может ли железо не подвергаться коррозии? Да, если оно очень чистое. Например, в Дели (Индия) находится Кутубская колонна высотой 7 м, массой 6,5 т. Она установлена в IX в. до н. э., в ее составе 99,72% Fe. До сих пор эта колонна не подверглась коррозии.
Взаимодействие металлов с растворами солей
Какие соли вы встречали в повседневной жизни?
Химически активные металлы вытесняют менее активные металлы из растворов солей, при этом протекает реакция замещения. Например, из раствора сульфата меди (ІІ) железо вытесняет медь (рис. 19):
Выделение красного налета меди является признаком реакции. Обратная реакция не протекает 
Схема реакций замещения выглядит следующим образом:
соль 4- активный металл = новая соль + новый металл (менее активный)
Реакции такого типа протекают при следующих условиях:
1) взаимодействующие соли должны быть растворимыми в воде;
2) более активный металл вытесняет из соли менее активный металл.
Демонстрация №3
Вытеснение металлов из растворов солей
Цель: понимать, что более активный металл вытесняет менее активный
металл из растворов его солей.
В пробирку поместите гранулы цинка и налейте раствор сульфата меди.
В другую пробирку поместите небольшие кусочки железа и налейте раствор сульфата меди. Что наблюдаете? Напишите уравнение реакции. Сделайте вывод.
Практическая работа № 1
Сравнение активности металлов
Цель: Разработать ряд активности металлов. Обобщить результаты и сделать выводы.
Ход работы
В пять пробирок налейте растворы солей по 5 мл, опустите в каждую пробирку стружки меди. Затем такие опыты повторите с другими металлами. Наблюдайте за интенсивностью хода реакций. Заполните таблицу: где идет реакция следует поставить знак “+”, если не идет реакция – знак “–”. По сравнительной интенсивности, т. е. по числу протекающих реакций, составьте ряд активности металлов.
ДЕЛАЕМ ВЫВОДЫ:
- 1. Атомы металлов в реакциях только отдают электроны, образуя положительно заряженные ионы.
- 2. Самопроизвольное разрушение металлов в результате их взаимодействия с веществами окружающей среды называется коррозией.
- 3. Сравнительную активность металлов можно определить с помощью ряда активности, составленного Н. Н. Бекетовым.
- 4. Металлы IA, НА группы очень легко вступают во взаимодействие с кислородом и водой. Многие металлы образуют оксидную пленку, которая препятствует дальнейшему окислению. Благородные металлы вообще не реагируют с кислородом и водой.
Услуги по химии:
- Заказать химию
- Заказать контрольную работу по химии
- Помощь по химии
Лекции по химии:
- Основные понятия и законы химии
- Атомно-молекулярное учение
- Периодический закон Д. И. Менделеева
- Химическая связь
- Скорость химических реакций
- Растворы
- Окислительно-восстановительные реакции
- Дисперсные системы
- Атомно-молекулярная теория
- Строение атома в химии
- Простые вещества
- Химические соединения
- Электролитическая диссоциация
- Химия и электрический ток
- Чистые вещества и смеси
- Изменения состояния вещества
- Атомы. Молекулы. Вещества
- Воздух
- Химические реакции
- Закономерности химических реакций
- Периодическая таблица химических элементов
- Относительная атомная масса химических элементов
- Химические формулы
- Движение электронов в атомах
- Формулы веществ и уравнения химических реакций
- Количество вещества
- Стехиометрические расчёты
- Энергия в химических реакциях
- Вода
- Необратимые реакции
- Кинетика
- Химическое равновесие
- Разработка новых веществ и материалов
- Зеленая химия
- Термохимия
- Правило фаз Гиббса
- Диаграммы растворимости
- Законы Рауля
- Растворы электролитов
- Гидролиз солей и нейтрализация
- Растворимость электролитов
- Электрохимические процессы
- Электрохимия
- Кинетика химических реакций
- Катализ
- Строение вещества в химии
- Строение твердого тела и жидкости
- Протекание химических реакций
- Комплексные соединения
Лекции по неорганической химии:
- Важнейшие классы неорганических соединений
- Водород и галогены
- Подгруппа кислорода
- Подгруппа азота
- Подгруппа углерода
- Общие свойства металлов
- Металлы главных подгрупп
- Металлы побочных подгрупп
- Свойства элементов первых трёх периодов периодической системы
- Классификация неорганических веществ
- Углерод
- Качественный анализ неорганических соединений
- Металлы и сплавы
- Металлы и неметаллы
- Производство металлов
- Переходные металлы
- Элементы 1 (1А), 2 IIA и 13 IIIA групп и соединения
- Элементы 17(VIIA), 16(VIA) 15(VA), 14(IVA) групп и их соединения
- Важнейшие S -элементы и их соединения
- Важнейшие d элементы и их соединения
- Важнейшие р-элементы и их соединения
- Производство неорганических соединений и сплавов
- Главная подгруппа шестой группы
- Главная подгруппа пятой группы
- Главная подгруппа четвертой группы
- Первая группа периодической системы
- Вторая группа периодической системы
- Третья группа периодической системы
- Побочные подгруппы четвертой, пятой, шестой и седьмой групп
- Восьмая группа периодической системы
- Водород
- Кислород
- Озон
- Водород
- Галогены
- Естественные семейства химических элементов и их свойства
- Химические элементы и соединения в организме человека
- Геологические химические соединения
Лекции по органической химии:
- Органическая химия
- Углеводороды
- Кислородсодержащие органические соединения
- Азотсодержащие органические соединения
- Теория А. М. Бутлерова
- Соединения ароматического ряда
- Циклические соединения
- Карбонильные соединения
- Амины и аминокислоты
- Химия живого вещества
- Синтетические полимеры
- Органический синтез
- Элементы 14(IVA) группы
- Азот и сера
- Растворы кислот и оснований