Формулы для расчета процентного содержания металлов в сплаве приведены под калькулятором.
Процентное содержание металлов в сплаве
Плотность первого металла
Плотность второго металла
Точность вычисления
Знаков после запятой: 2
Процентное содержание первого металла
Процентное содержание второго металла
Расчет процентного содержания металлов в сплаве двух металлов
Пусть нам известны физические характеристики сплава, масса и плотность, их можно просто померять, и плотности металлов, составляющих сплав (например, их можно узнать из справочника).
Имеем следующие очевидные соотношения:
,
где
m — масса сплава,
V — объем сплава,
m₁ — масса первого металла,
V₁ — объем первого металла,
ρ₁ — плотность первого металла,
m₂ — масса второго металла,
V₂ — объем второго металла,
ρ₂ — плотность второго металла.
m₁, V₁, m₂, V₂ — четыре неизвестных на четыре уравнения — существует единственное решение.
Выполнив подстановки, можно получить довольно громоздкие формулы для m₁ и m₂
Процентные соотношения получим, поделив массы металлов на массу сплава.
Наибольшие трудности при изучении физики
учащиеся испытывают при решении задач, т.е. когда
требуется применить знания. Эти трудности
представляются ребятам настолько большими, что
многие из них отказываются даже от попыток
решать задачи. Отказ от решения задач еще как-то
«проходил» во времена устных экзаменов по
физике. Но теперь – как при прохождении
Государственной итоговой аттестации, выполнении
заданий Единого государственного экзамена или
тестирования при поступлении – проверяют именно
умение применять полученные знания, а не
декларировать их.
Понимание смысла физических законов – главная
цель школьного курса физики, но понимание этих
законов может родиться только в осознанной
деятельности по применению этих законов.
Школьникам же часто предлагают алгоритмы
решения задач, которые провоцируют бездумное,
автоматическое применение физических формул.
Преодолеть эту принципиальную трудность можно,
только неоднократно применяя законы физики в
тщательно отобранных простейших ситуациях,
когда смысл этих законов кристально ясен.
В школьном курсе физики тысячи задач. Однако,
если посмотреть на все множество этих задач «с
высоты птичьего полета», то нетрудно заметить,
что подавляющее их большинство группируются
вокруг нескольких десятков типичных учебных
ситуаций. Эти ситуации можно назвать ключевыми.
А овладение ключевыми ситуациями «даст ключи» к
решению задач.
Ключевые ситуации – важнейшая связь между
«теорией» и «задачами». Без этой связи теория
мертва для школьника, а задачи представляются
ему случайной россыпью неинтересных загадок.
Однако пока еще некоторые учителя «дают» своим
ученикам «теорию» отдельно, а «задачи» отдельно.
После такого разрезания по живому от живой
физики остаются только мертвые формулы-шаблоны
для примитивных задач на подстановку.
Изучение ключевых ситуаций – это живой мост
между «теорией» и «задачами», причем мост с
двухсторонним движением. С одной стороны, задачи
рождаются при изучении ключевых ситуаций, в
которых наглядно проявляется действие
физических законов, с другой стороны, благодаря
решению задач на основе ключевой ситуации теория
осознается, т.е. становится действенной силой, а
не пассивным набором фактов и формул.
И еще одна очень важная роль ключевых ситуаций.
Дело в том, что результатом изучения школьного
курса физики должен быть не набор решенных задач
(это быстро забывается), а понимание физических
законов и физическая интуиция, которая может
развиваться именно при рассмотрении ключевых
ситуаций.
Приложение 1.
Фрагмент урока с выделением ключевой ситуации по
теме «Плотность».
Приложение 2. Фрагмент
урока с выделением ключевой ситуации по теме
«Полые тела».
Приложение 3.
Дополнительный материал по теме «Сплавы».
Приведем фрагмент урока с выделение ключевой
ситуации по теме «Сплавы».
Фрагмент урока по теме «СПЛАВЫ»
Учитель. Тема урока зашифрована
ребусом. Кто первый раскроет секрет?
Ученики. …
Учитель. Тема урока «Сплавы».
Сплав — макроскопически однородная смесь двух
или большего числа химических элементов с
преобладанием металлических компонентов.
Основной или единственной фазой сплава, как
правило, является твёрдый раствор легирующих
элементов в металле, являющемся основой сплава.
Сплавы имеют металлические свойства, например:
металлический блеск, высокие электропроводность
и теплопроводность. Иногда компонентами сплава
могут быть не только химические элементы, но и
химические соединения, обладающие
металлическими свойствами. Например, основными
компонентами твёрдых сплавов являются карбиды
вольфрама или титана. Макроскопические свойства
сплавов всегда отличаются от свойств их
компонентов, а макроскопическая однородность
многофазных (гетерогенных) сплавов достигается
за счёт равномерного распределения примесных
фаз в металлической матрице.
Сплавы обычно получают с помощью смешивания
компонентов в расплавленном состоянии с
последующим охлаждением. При высоких
температурах плавления компонентов, сплавы
производятся смешиванием порошков металлов с
последующим спеканием (так получаются, например,
многие вольфрамовые сплавы).
Сплавы являются одним из основных
конструкционных материалов. Среди них
наибольшее значение имеют сплавы на основе
железа и алюминия. В состав многих сплавов могут
вводиться и неметаллы, такие как углерод,
кремний, бор и др. В технике применяется более 5
тыс. сплавов.
Цель нашего урока –
научиться решать задачи для определения
плотности, массы или объема сплавов или веществ
входящих в их состав.
Рассматривая сплавы, обычно предполагают, что
объем сплава равен сумме объемов
составляющих его веществ. В таком случае
плотность сплава ,
где индексы 1 и 2 относятся к двум компонентам
сплава.
Если заданы или требуется найти массы
компонентов известной плотности ρ1 и ρ2, то объемы
компонентов надо выразить через их массы и
плотности, в результате чего формула для
плотности сплава примет вид 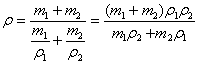
Часто в задаче дано или требуется найти
соотношение масс компонентов сплава. Обозначим . Тогда
. Эта формула связывает
плотность сплава ρ и массовое отношение
компонент . Из
нее при следует:
. Приведенные
формулы позволяют по заданному значению одной из
величин ( или ρ)
найти значение другой.
Запишите в тетрадях:
Примечание.
1. Задача первого уровня предназначена для
применения основной формулы: .
2. Задачи второго уровня похожи, поэтому
целесообразно применить разные способы решения.
3. Задачи третьего уровня предусмотрены для
закрепления способов решения задач предложенных
ранее с добавлением дополнительных вычислений
(объема и процентного отношения).
РЕШЕНИЕ ЗАДАЧ
Задачи по теме «СПЛАВЫ»:
УРОВЕНЬ 1
Найдите плотность бронзы, для изготовления
которой взяли 100 г меди и 30 г олова, считая, что
объем сплава равен сумме объемов входящих в него
металлов.
УРОВЕНЬ 2
1. Кусок сплава из свинца и олова массой 664 г
имеет плотность 8,3 г/см3. Определите массу
свинца в сплаве. Принять объем сплава равным
сумме объемов его составных частей.
2. В куске кварца содержится небольшой
самородок золота. Масса куска 100 г, а его
плотность 8 г/см3. Определите массу
золота, содержащегося в кварце. Принять, что
плотность кварца и золота соответственно равны
2,65 и 19,36 г/см3.
УРОВЕНЬ 3
1. Сплав золота и серебра массой 400 г имеет
плотность 14·103 кг/м3. Полагая объем сплава
равным сумме объемов его составных частей,
определите массу, объем золота и процентное
содержание его в сплаве.
2. В чистой воде растворена кислота. Масса
раствора 240 г, а его плотность 1,2 г/см3.
Определите объем кислоты в растворе и его
процентное содержание, если плотность кислоты 1,8
г/см3. Принять объем раствора равным сумме
объемов его составных частей.
Выходной контроль:
Установите соответствие:
Ответы: 1-Д, 2-Ж, 3-А, 4-Б, 5-В. 6-Г, 7-Е.
Домашнее задание:
Дополнительный материал.
Сплавы различаются по своему предназначению.
Конструкционные сплавы: стали, чугуны,
дюралюминий.
Конструкционные со специальными свойствами
(например, искробезопасность, антифрикционные
свойства): бронзы, латуни.
Для заливки подшипников: баббит.
Для измерительной и электронагревательной
аппаратуры: манганин, нихром.
Для изготовления режущих инструментов:
победит.
Подготовьте сообщение о каком-нибудь сплаве.
Расскажите о веществах, которые в него входят, о
их процентном вхождении в сплав и т.д.
Задачи:
1. Найдите плотность стали (сталь —
деформируемый (ковкий) сплав железа с углеродом),
для изготовления которой взяли 100 г железа и 2 г
углерода (углекислого газа), считая, что объем
сплава равен сумме объемов входящих в него
веществ.
2. Чтобы получить латунь, сплавили куски меди
массой 178 кг и цинка массой 355 кг. Какой плотности
была получена латунь? Объем сплава равен сумме
объемов его составных частей.
3. Сплав золота и серебра массой 500 г имеет
плотность 11 г/см3. Полагая объем сплава равным
сумме объемов его составных частей, определите
массу, объем золота и процентное содержание его в
сплаве.
Ответы: 1. 0,098 г/см3, 2. 8540 кг/м3, 3. 50 г, 2,59
см3, 10%.
Подведение итогов урока. Рефлексия
На полях рабочей тетради изобрази схематически
один из рисунков, который соответствует степени
усвоения материала на уроке. Солнце – мне все
понятно, туча – материал интересный, но надо еще
поработать, луна – я все проспал.
Литература
- Материалы курса «Как научить решать задачи по
физике (основная школа). Подготовка к ГИА: лекции
1-4. – М.: Педагогический университет «Первое
сентября», 2010. -80с. - Сборник задач по физике: Учеб. Пособие для
учащихся 7-8 классов средней школы. – 6-е изд.,
перераб. – М.: Просвещение, 1994. – 191 с.: ил. - Физическая олимпиада в 6-7 классах средней школы:
Пособие для учащихся. – 2-е изд, перераб. И доп. –
М.: Просвещение, 1987. – 192 с: ил.
Расчет состава нового сплава
Начну с легенды. «Старые мастера делали серебряный припой так: брали серебряный полтинник и медный пятак…» А вот интересно, что за сплав получится, если сплавить полтинник и пятак?
Другой случай. Ты по ошибке сплавил в один кусок два изделия разной пробы. Что делать? Опять это страшное слово «аффинаж»? Конечно, нет. Нужно просто вычислить состав полученного «неправильного» сплава и использовать его дальше: или для его исправления, или в качестве добавки к другим сплавам.
В общем, бывают случаи, когда нужно узнать состав сплава, полученного при смешивании нескольких других. Для этого, конечно, необходимо знать состав и количество (массу) исходных сплавов.
Для простоты рассмотрим случай, когда исходных сплавов только два (как чаще всего и бывает).
Дано:




Найти:

Решение:
Алгоритм простой: вычисляем массу каждого компонента и делим на общую массу.
Суммарная масса компонента: 
Суммарная масса сплава: 
Состав результирующего сплава: 
Пример расчета
Теперь проверим, что получится, если сплавить полтинник и пятак. Возьмем 10 г серебра 900 пробы (полтинник) и 16 г меди (пятак), подставим в формулу (1) и получим:
доля серебра — (0,9*10 + 0*16) / (10 + 16) = 0,346;
доля меди — (0,1*10 + 1*16) / (10 + 16) = 0,654.
То есть, это серебро 346 пробы, которое никак ювелирным сплавом считаться не может. Не всем легендам стоит доверять.
Кстати
Программа Alloy теперь умеет решать и эту задачу. Число исходных сплавов — до четырех.
Здесь находится описание программы, а здесь можно ее заказать.
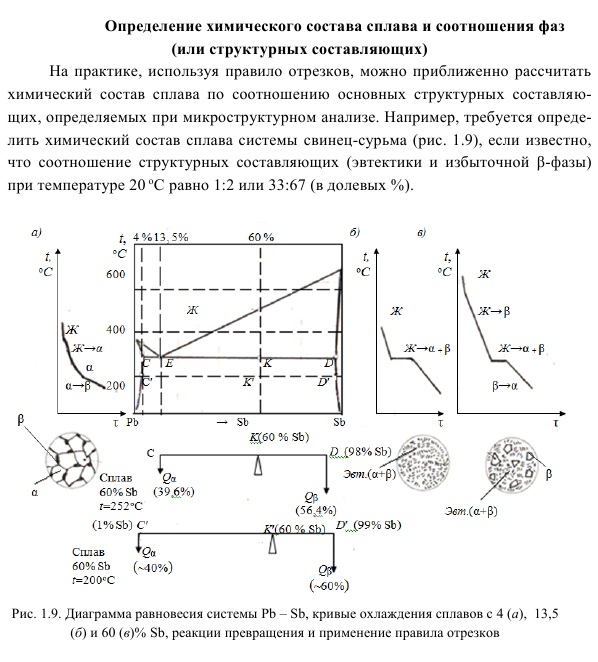
Определение химического состава сплава и соотношения фаз
Фактически, химический состав сплава можно аппроксимировать из пропорций ключевых структурных компонентов, определенных микроструктурным анализом с использованием правил сегментов.
Например, если известно, что отношение структурных компонентов (эвтектика к избыточной β-фазе) при температуре 20 ° C составляет 1: 2 или 33:67 (долевой процент), химический состав сплавов свинец-сурьма Необходимо определить состав (рисунок 1.9)) 28 Рисунок 1.9.
Диаграмма равновесия системы Pb-Sb, кривые охлаждения сплавов, содержащих 4 (a), 13,5 (b) и 60 (c)% Sb, реакция превращения и применение закона сегментации в присутствии основного сплава Cx
Определить диапазон концентраций структурных компонентов эвтектики и бета-фазы. Область с таким структурным компонентом находится между точками E и D. То есть 17,3 <Cx <98%. Далее нарисуйте конус при 20 ° С.
- Конец конуса ограничен этими концентрациями. Постройте схему рычага и используйте правила сегмента для описания отношения QE ∙ EK = Qβ ∙ KD или QE / Qβ = KD ∙ EK.
- Найти длину сегмента по концентрации сплава: KD = 98% -Cx EK = Cx –17,5%, откуда QE / Qβ = 98% -Cx / Cx –17,5% = Это связано с 1/2 Cx из условия задачи Решение уравнения дает состав сплава: ~ 71% Sb, остальное — Pb. Для найденного состава сплава определите соотношение α- и β-фаз при 150 ° C.
Для этого конус от точки k´ до пересечения ближайших линий на рисунке (точки c´ и d´) ничья. Определите химический состав фаз α (4% Sb, включая оставшийся Pb) и β (99% Sb, оставшийся Pb). Постройте схему рычага и опишите соотношение Qα / Qβ = k´d´ / c´k´. Длина сегмента выражается концентрацией 29 сплавов, Qα / Qβ = 99–71 (%) / 71–4 (%) = 28/67.
В пропорции Qα и Qβ составляют 29,5 и 70,5% соответственно. Вы можете использовать правила сегмента, чтобы построить зависимость фазовой массовой доли от состава сплава при определенной температуре или температуры рассматриваемого сплава.
На рисунке 1.10 показана зависимость массовой доли фазы Al2Li от состава сплава Al-Li при 300 ° C. Рисунок 1. 10. Зависимость весовой доли фазы Al2Li от состава сплава Al-Li при 300 ° C. Графическое представление этой зависимости указывает на то, что конкретная фаза бинарной системы имеет определенную температуру.
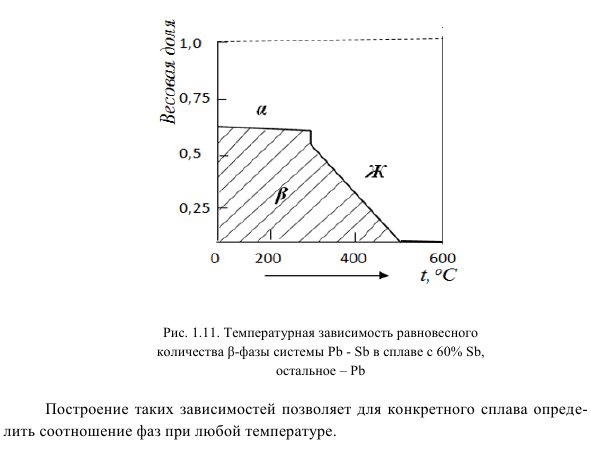
- Вы можете определить процент. Рисунок 1.11. Построена температурная зависимость равновесного количества β-фазы системы Pb-Sb сплава, содержащего 60% Sb, а остальное — Pb.
Смотрите также:
Примеры решения задач по материаловедению
Задачи на смеси и сплавы — подробнее
Концентрация какого-то вещества в растворе – это отношение массы или объема этого вещества к массе или объему всего раствора.
То же самое относится и к сплавам: содержание одного из металлов в сплаве – это отношение массы этого металла к массе всего сплава.
Обычно концентрация измеряется в процентах.
Что такое процент?
Напомню, что это сотая доля числа. То есть, если массу или объем разделить на ( displaystyle 100), получим ( displaystyle 1%) этой массы или объема.
Чтобы вычислить концентрацию в процентах, достаточно полученное число умножить на ( displaystyle 100%).
Почему?
Сейчас покажу: пусть масса всего раствора равна ( displaystyle M), а масса растворенного вещества (например, соли или кислоты) – ( displaystyle m). Тогда один процент от массы раствора равен ( displaystyle frac{M}{100}).
Как узнать, сколько таких процентов содержится в числе ( displaystyle m)?
Просто: поделить число ( displaystyle m) на этот один процент: ( displaystyle frac{m}{frac{M}{100}}=frac{m}{M}cdot 100), но ведь ( displaystyle frac{m}{M}) – это концентрация.
Вот и получается, что ее надо умножить на ( displaystyle 100), чтобы узнать, сколько процентов вещества содержится в растворе.
Более подробно о процентах – в темах «Дроби, и действия с дробями»и «Проценты».
Поехали дальше.
Масса раствора, смеси или сплава равна сумма масс всех составляющих.
Логично, правда?
Например, если в растворе массой ( displaystyle 10) кг содержится ( displaystyle 3) кг соли, то сколько в нем воды? Правильно, ( displaystyle 7)кг.
И еще одна очевидность:
При смешивании нескольких растворов (или смесей, или сплавов), масса нового раствора становится равной сумме масс всех смешанных растворов.
А масса растворенного вещества в итоге равна сумме масс этого же вещества в каждом растворе отдельно.
Например: в первом растворе массой ( displaystyle 10) кг содержится ( displaystyle 3) кг кислоты, а во втором растворе массой ( displaystyle 14) кг – ( displaystyle 5) кг кислоты.
Когда мы их смешаем, чему будет равна масса нового раствора?
( displaystyle 10+14=24) кг.
А сколько в новом растворе будет кислоты? ( displaystyle 3+5=8) кг.
Перейдем к задачам.
Бонус: Вебинары из нашего курса подготовки к ЕГЭ по математике
ЕГЭ №11. Задачи на растворы, смеси и сплавы (и на проценты)
В этом видео мы научимся решать текстовые задачи на проценты, а так же на растворы, смеси и сплавы — на все, что содержит разные вещества в каком-то соотношении.
Задачи на смеси и сплавы очень часто попадаются на ОГЭ (№23) и профильном ЕГЭ (под номером 12).
Мы научимся очень простому способу сводить эти задачи к обычному линейному уравнению или к системе из двух таких уравнений.
Также мы научимся решать сложные задачи на проценты — в основном они на банковские вклады и кредиты и прочие финансовые штуки.
Это, в том числе, даст нам очень большой задел для “ экономической» задачи №17 (которая стоит аж 3 первичных балла).
ЕГЭ №17 Экономическая задача. Вклады
Экономические задачи в основном довольно простые, но дают аж 3 первичных балла!
Но это не совсем 3 балла нахаляву. Эти задачи требуют очень подробного и чёткого описания решения.
По сути, мы составляем математическую модель какой-то жизненной ситуации (например, связанной с банковскими вкладами или кредитами), и важно научиться ничего не пропускать при описании этой модели: описывать словами все введённые обозначения, обосновывать уравнения, которые мы записываем, и всё в таком духе.
Если не написать эти объяснения, вы гарантированно получите 0 баллов даже за правильно найденный ответ!
На этом уроке мы узнаем, как работают вклады, научимся решать и, главное, правильно оформлять решение таких задач.