Средняя
кинетическая энергия поступательного
движения молекулы идеального газа
(воспользуемся формулой 2.10)
Екин.
пост. =
=
=
kТ
Екин.
пост.
=
kТ
(2.11)
Поступательное
движение молекул может происходить по
осям «Х», «Y»,
«Z»
— есть три поступательных степени
свободы. На одну степень свободы
приходится средняя кинетическая энергия.
Екин.
=
kТ
(2.12)
Если
у молекулы i
степеней свободы, средняя кинетическая
энергия молекулы
Екин.
=
kТ (2.13)
i
— число степеней свободы, число независимых
координат, определяющих положение тела
в пространстве.
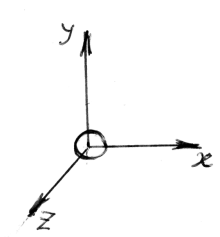
Молекулу
одноатомного идеального газа (например,
инертного газа) можно считать материальной
точкой с тремя степенями свободы (x,
y, z) поступательного движения.
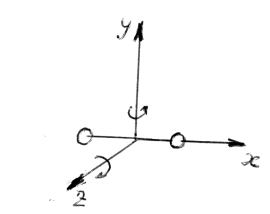
Для
молекулы двухатомного газа можно принять
с некоторыми допущениями модель жесткой
«гантели» с тремя поступательными
степенями свободы (x,
y, z) и двумя вращательными (вокруг оси Y
и оси Z).
Вращение вокруг оси X
(см. рисунок в таблице 2.3) не учитывается,
поскольку поперечные размеры «гантели»
принимаются пренебрежимо малыми. Итого
число степеней свободы молекулы
двухатомного газа i
= 5 (3 поступательных + 2 вращательных).
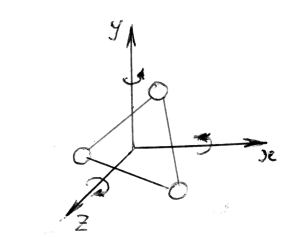
У
молекулы трехатомного и многоатомного
газа, если принять модель жёсткого
трехмерного тела (атомы и молекулы не
расположены на одной прямой), число
степеней свободы i
= 3 поступательных + 3 вращательных = 6
В
этом случае учитывается три вращательных
степени свободы: вокруг оси x,
y и z.
Соответственно
средние кинетические энергии молекул
будут равны:
Для
молекулы одноатомного газа –
kТ,
Двухатомного
—
kТ,
Трех-
и многоатомного – 3kТ
(см. таблицу 2.3).
Таблица
2.3. Средние кинетические энергии молекул
идеального газа
|
Газ |
рисунок |
Число |
Средняя |
|
Одноатомный |
|
3 |
|
|
Двухатомный |
|
3 |
|
|
Трехатомный |
|
3 |
|
Внутренняя
энергия идеального тела U
(см 1.2) складывается из суммарной
кинетической энергии движения молекул
относительно друг друга Екин
i
, суммарной потенциальной энергии
взаимодействия молекул друг с другом
и энергии U0
внутримолекулярных, внутриатомных,
внутриядерных движений и взаимодействий
и т. д. и т. д.
Будем
считать, что в изучаемых нами в этой
главе молекулярных явлениях эта часть
внутренней энергии U0
не меняется.
Итак,
внутренняя энергия идеального газа:
(2.14)
Но
так как в модели идеального газа
пренебрегаем взаимодействиями молекул
на расстоянии
0 и остается
U
=
Екин
i
+
U0
(2.15)
а
Екин
i
=
kT,
где
N
– число молекул,
kT
– средняя кинетическая энергия одной
молекулы (согласно 2.13).
Поэтому
U
=
kT
+ U0
А
так как
N
= NАm/М,
U
=
NА
kT
+ U0
Учтя,
что
NАk
= R,
получим для внутренней энергии идеального
газа
U
=
R
T
+ U0
(2.16)
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
12.02.201514.57 Mб29Уход за хирургическими больными. Буянов В.М.pdf
- #
- #
- #
- #
- #
- #
- #
- #
- #
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,666 -
гуманитарные
33,654 -
юридические
17,917 -
школьный раздел
611,992 -
разное
16,906
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Физика, 10 класс
Урок 18. Основное уравнение МКТ
Перечень вопросов, рассматриваемых на уроке:
1) средняя кинетическая энергия молекулы;
2) давление газа;
3) основное уравнение МКТ;
Глоссарий по теме:
Давление идеального газа пропорционально произведению концентрации молекул и средней кинетической энергии поступательного движения молекул.
Средняя кинетическая энергия молекул – усреднённая величина, равная половине произведения массы молекулы на среднюю величину квадрата её скорости.
Концентрация – число молекул в единице объёма.
Масса молекулы (или атома) – чрезвычайно маленькая величина в макроскопических масштабах (граммах и килограммах), вычисляется через отношение массы вещества к количеству содержащихся в ней молекул (или атомов).
Изменение импульса тела – произведение силы на время действия силы. Импульс силы всегда показывает, как изменяется импульс тела за данное время.
Основная и дополнительная литература по теме урока:
- Мякишев Г.Я., Буховцев Б.Б., Сотский Н.Н. Физика.10 класс. Учебник для общеобразовательных организаций М.: Просвещение, 2017. С. 188 – 192.
- Кирик Л.А., Генденштейн Л.Э., Гельфгат И.М.. Задачи по физике. 10-11 классы для профильной школы. – М.: Илекса, 2010. С. 111.
- Рымкевич А.П. Физика. Задачник. 10-11 классы. – М.: Дрофа, 2013. С. 65 – 67.
Открытые электронные ресурсы по теме урока:
- http://kvant.mccme.ru/1991/09/idealnyj_gaz_-_universalnaya_f.htm
- http://kvant.mccme.ru/1983/10/davlenie_idealnogo_gaza.htm
- http://kvant.mccme.ru/1987/09/davlenie_gaza_v_sosude.htm
Теоретический материал для самостоятельного изучения
Основная задача молекулярно-кинетической теории газа заключается в том, чтобы установить соотношение между давлением газа и его микроскопическими параметрами — массой молекул, их средней скоростью и концентрацией. Это соотношение называется основным уравнением молекулярно-кинетической теории газа.
Давление газа на стенку сосуда обусловлено ударами молекул, давление газа пропорционально концентрации молекул: чем больше молекул в единице объема, тем больше ударов молекул о стенку за единицу времени. Каждая молекула при ударе о стенку передает ей импульс, пропорциональный импульсу молекулы m0v.
Давление пропорционально второй степени скорости, так как, чем больше скорость молекулы, тем чаще она бьется о стенку сосуда. Расчеты показывают, что основное уравнение молекулярно-кинетической теории идеального газа имеет вид:

n— концентрация молекул,

Коэффициент 
Средняя кинетическая энергия поступательного движения
тогда уравнение примет вид:

Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
Примеры и разбор решения заданий.
1. К каждой позиции первого столбца подберите соответствующую позицию второго:
|
ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ |
ФОРМУЛЫ |
|
1) импульс тела |
А) |
|
2) средняя кинетическая энергия молекул |
Б) |
|
3) давление газа на стенку сосуда |
В) |
|
4) концентрация молекул |
Г) |
Правильный ответ: вспомнив формулы величин, устанавливаем соответствие:
|
ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ |
ФОРМУЛЫ |
|
1) импульс тела |
В) |
|
2) средняя кинетическая энергия молекул |
А) |
|
3) давление газа на стенку сосуда |
Г) |
|
4) концентрация молекул |
Б) |
2. Кислород находится при нормальных условиях. Средняя квадратичная скорость молекул кислорода в этом случае равна ___ м/с.
Решение:

Ответ: 460 м/с.
Дано:
t = 150 градусов.
Найти: Е кинетическая.
Решение:
Для решения задачи будем использовать формулу для поступательного движения. Она выглядит так: Uп = 3/2VRT.
Дальше запишем формулу для полного числа молекул: N = VNa.
Далее нам надо поделить кинетическую энергию на эту формулу и мы получим способ найти потенциальную энергию. Еп = Ек /Na.
Подставим в нее другие выражения и получим: Еп = 3/2VRT: (VNa) = 3/2RT : Na = 3/2 R/Na *T = 3/2kT.
Важно не забыть, что Т в кельвинах будет выражаться через Т в Цельсиях, то есть Т = t + 273K.
Тогда получим Еп = 3/2k (T+ 273K).
Подставим значения и посчитаем: Еп = 3/2 * 1,38 * 10^-23 (-50 +273) = (3/2 * 1,38 * 10^-23 * 223) = 4, 62 * 10^-21 Дж.
Ответ: 4, 62 * 10^-21