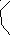Материалы из методички: Сборник задач по теоретическим основам химии для студентов заочно-дистанционного отделения / Барботина Н.Н., К.К. Власенко, Щербаков В.В. – М.: РХТУ им. Д.И. Менделеева, 2007. -155 с.
Степень диссоциации
Классификация электролитов
Диссоциация электролитов
Константа диссоциации
Примеры решения задач
Задачи для самостоятельного решения
Степень диссоциации
Вещества, которые в растворах или расплавах полностью или частично распадаются на ионы, называются электролитами.
Степень диссоциации α — это отношение числа молекул, распавшихся на ионы N′ к общему числу растворенных молекул N:
α = N′/N
Степень диссоциации выражают в процентах или в долях единицы. Если α =0, то диссоциация отсутствует и вещество не является электролитом. В случае если α =1, то электролит полностью распадается на ионы.
Классификация электролитов
Согласно современным представлениям теории растворов все электролиты делятся на два класса: ассоциированные (слабые) и неассоциированные (сильные). Неассоциированные электролиты в разбавленных растворах практически полностью диссоциированы на ионы. Для этого класса электролитов a близко к единице (к 100 %). Неассоциированными электролитами являются, например, HCl, NaOH, K2SO4 в разбавленных водных растворах.
Ассоциированные электролиты подразделяются на три типа:
-
-
- Слабые электролиты существуют в растворах как в виде ионов, так и в виде недиссоциированных молекул. Примерами ассоциированных электролитов этой группы являются, в частности, Н2S, Н2SO3, СН3СOОН в водных растворах.
- Ионные ассоциатыобразуются в растворах путем ассоциации простых ионов за счет электростатического взаимодействия. Ионные ассоциаты возникают в концентрированных растворах хорошо растворимых электролитов. В результате в растворе находятся как простые ионы, так и ионные ассоциаты. Например, в концентрированном водном растворе КCl образуются простые ионы К+, Cl— , а также возможно образование ионных пар (К+Cl— ), ионных тройников (K2Cl+, KCl2— ) и ионных квадруполей (K2Cl2, KCl32- , K3Cl2+).
- Комплексные соединения(как ионные, так и молекулярные), внутренняя сфера которых ступенчато диссоциирует на ионные и (или) молекулярные частицы.
Примеры комплексных ионов: [Cu(NH3)4]2+, [Fe(CN)6]3+, [Cr(H2O)3Cl2]+.
-
При таком подходе один и тот же электролит может относиться к различным типам в зависимости от концентрации раствора, вида растворителя и температуры. Подтверждением этому являются данные, приведенные в таблице.
Таблица. Характеристика растворов KI в различных растворителях
| Концентрация электролита, С, моль/л | Температура
t,оС |
Растворитель | Тип электролита |
| 0,01 | 25 | Н2О | Неассоциированный (сильный) |
| 5 | 25 | Н2О | Ионный ассоциат |
| 0,001 | 25 | С6Н6 | Ассоциированный (слабый) |
Приближенно, для качественных рассуждений можно пользоваться устаревшим делением электролитов на сильные и слабые. Выделение группы электролитов “средней силы” не имеет смысла. Эти электролиты являются ассоциированными. К слабым электролитам обычно относят электролиты, степень диссоцииации которых мала α<<1.
Таким образом, к сильным электролитам относятся разбавленные водные растворы почти всех хорошо растворимых в воде солей, многие разбавленные водные растворы минеральных кислот (НСl, HBr, НNО3, НСlO4 и др.), разбавленные водные растворы гидроксидов щелочных металлов. К слабым электролитам принадлежат все органические кислоты в водных растворах, некоторые водные растворы неорганических кислот, например, H2S, HCN, H2CO3, HNO2, HСlO и др. К слабым электролитам относится и вода.
Диссоциация электролитов
Уравнение реакции диссоциации сильного электролита можно представить следующим образом. Между правой и левой частями уравнения реакции диссоциации сильного электролита ставится стрелка или знак равенства:
HCl → H+ + Cl—
Na2SO3 = 2Na+ + SO32-
Допускается также ставить знак обратимости, однако в этом случае указывается направление, в котором смещается равновесие диссоциации, или указывается, что α≈1. Например:
NaOH → Na+ + OH—
Диссоциация кислых и основных солей в разбавленных водных растворах протекает следующим образом:
NaHSO3 → Na+ + HSO3—
Анион кислой соли будет диссоциировать в незначительной степени, поскольку является ассоциированным электролитом:
HSO3— → H+ + SO32-
Аналогичным образом происходит диссоциация основных солей:
Mg(OH)Cl → MgOH+ + Cl—
Катион основной соли подвергается дальнейшей диссоциации как слабый электролит:
MgOH+ → Mg2+ + OH—
Двойные соли в разбавленных водных растворах рассматриваются как неассоциированные электролиты:
KAl(SO4)2 → K+ + Al3+ + 2SO42-
Комплексные соединения в разбавленных водных растворах практически полностью диссоциируют на внешнюю и внутреннюю сферы:
K3[Fe(CN)6] → 3K+ + [Fe(CN)6]3-
В свою очередь, комплексный ион в незначительной степени подвергается дальнейшей диссоциации:
[Fe(CN)6]3- → Fe3+ + 6CN—
Константа диссоциации
При растворении слабого электролита КА в растворе установится равновесие:
КА ↔ К+ + А—
которое количественно описывается величиной константы равновесия Кд, называемой константой диссоциации:
Kд = [К+] · [А—] /[КА] (2)
Константа диссоциации характеризует способность электролита диссоциировать на ионы. Чем больше константа диссоциации, тем больше ионов в растворе слабого электролита. Например, в растворе азотистой кислоты HNO2 ионов Н+ больше, чем в растворе синильной кислоты HCN, поскольку К(HNO2) = 4,6·10— 4, а К(HCN) = 4,9·10— 10.
Для слабых I-I электролитов (HCN, HNO2, CH3COOH) величина константы диссоциации Кд связана со степенью диссоциации α и концентрацией электролита c уравнением Оствальда:
Кд = (α2·с)/(1-α) (3)
Для практических расчетов при условии, что α<<1 используется приближенное уравнение:
Кд = α2·с (4)
Поскольку процесс диссоциации слабого электролита обратим, то к нему применим принцип Ле Шателье. В частности, добавление CH3COONa к водному раствору CH3COOH вызовет подавление собственной диссоциации уксусной кислоты и уменьшение концентрации протонов. Таким образом, добавление в раствор ассоциированного электролита веществ, содержащих одноименные ионы, уменьшает его степень диссоциации.
Следует отметить, что константа диссоциации слабого электролита связана с изменением энергии Гиббса в процессе диссоциации этого электролита соотношением:
ΔGT0 = — RTlnKд (5)
Уравнение (5) используется для расчета констант диссоциации слабых электролитов по термодинамическим данным.
Примеры решения задач
Задача 1. Определите концентрацию ионов калия и фосфат-ионов в 0,025 М растворе K3PO4.
Решение. K3PO4 – сильный электролит и в водном растворе диссоциирует полностью:
K3PO4 → 3К+ + РО43-
Следовательно, концентрации ионов К+ и РО43- равны соответственно 0,075М и 0,025М.
Задача 2. Определите степень диссоциации αд и концентрацию ионов ОН— (моль/л) в 0,03 М растворе NH3·H2О при 298 К, если при указанной температуре Кд(NH3·H2О) = 1,76× 10— 5.
Решение. Уравнение диссоциации электролита:
NH3·H2О → NH4+ + OH—
Концентрации ионов: [NH4+] = αС ; [OH—] = αС , где С – исходная концентрация NH3·H2О моль/л. Следовательно:
Kд = αС · αС /(1 — αС)
Поскольку α << 1, то:
Кд ≈ α 2С
Константа диссоциации зависит от температуры и от природы растворителя, но не зависит от концентрации растворов NH3·H2О. Закон разбавления Оствальда выражает зависимость α слабого электролита от концентрации.
α = √(Кд / С) = √(1,76× 10— 5 / 0,03) = 0,024 или 2,4 %
[OH—] = αС, откуда [OH— ] = 2,4·10— 2·0,03 = 7,2·10-4 моль/л.
Задача 3. Определите константу диссоциации уксусной кислоты, если степень диссоциации CH3CОOH в 0,002 М растворе равна 9,4 %.
Решение. Уравнение диссоциации кислоты:
CH3CОOH → СН3СОО— + Н+.
α = [Н+] / Сисх(CH3CОOH)
откуда [Н+] = 9,4·10—2·0,002 = 1,88·10-4 М.
Так как [CH3CОO—] = [Н+] и [CH3CОOH] ≈ Сисх(CH3CОOH), то:
Kд = [Н+]2 / Сисх(CH3CОOH)
Константу диссоциации можно также найти по формуле: Кд ≈ α 2С.
Задача 4. Константа диссоциации HNO2 при 298К равна 4,6× 10— 4. Найдите концентрацию азотистой кислоты, при которой степень диссоциации HNO2 равна 5 %.
Решение.
Кд =α 2С , откуда получаем Сисх(HNO2) = 4,6·10— 4/(5·10— 2)2 = 0,184 М.
Задача 5. На основе справочных данных рассчитайте константу диссоциации муравьиной кислоты при 298 К.
Решение. Уравнение диссоциации муравьиной кислоты
НСООН →Н+ + СООН—
В “Кратком справочнике физико–химических величин” под редакцией А.А. Равделя и А.М. Пономаревой приведены значения энергий Гиббса образований ионов в растворе, а также гипотетически недиссоциированных молекул. Значения энергий Гиббса для муравьиной кислоты и ионов Н+ и СООН— в водном растворе приведены ниже:
| Вещество, ион | НСООН | Н+ | СООН— |
| ΔGT0, кДж/моль | — 373,0 | 0 | — 351,5 |
Изменение энергии Гиббса процесса диссоциации равно:
ΔGT0 = — 351,5- (- 373,0) = 21,5 кДж/моль.
Для расчета константы диссоциации используем уравнение (5). Из этого уравнения получаем:
lnKд = — Δ GT0/RT= — 21500/(8,31 298) = — 8,68
Откуда находим: Kд = 1,7× 10— 4.
Задачи для самостоятельного решения
1. К сильным электролитам в разбавленных водных растворах относятся:
- СН3СOOH
- Na3PO4
- NaCN
- NH3
- C2H5OH
- HNO2
- HNO3
13.2. К слабым электролитам в водных растворах относятся:
- KAl(SO4)2
- NaNO3
- HCN
- NH4Cl
- C2H5OH
- H2SO3
- H2SO4
3. Определите концентрацию ионов NH4+ в 0,03 М растворе (NH4)2Fe(SO4)2;
4. Определите концентрацию ионов водорода в 6 мас.% растворе H2SO4, плотность которого составляет 1,038 г/мл. Принять степень диссоциации кислоты по первой и второй ступеням равной 100 %.
5. Определите концентрацию гидроксид-ионов в 0,15 М растворе Ba(OH)2.
6. Степень диссоциации муравьиной кислоты в 0,1 М растворе равна 4 %. Рассчитайте Концентрацию ионов водорода в этом растворе и константу диссоциации НСООН.
7. Степень диссоциации муравьиной кислоты в водном растворе увеличится при:
а) уменьшении концентрации HCOOH;
б) увеличении концентрации HCOOH;
в) добавлении в раствор муравьиной кислоты HCOONa;
г) добавлении в раствор муравьиной кислоты НCl.
8. Константа диссоциации хлорноватистой кислоты равна 5× 10— 8. Определите концентрацию HClO, при которой степень диссоциации HClO равна 0,5 %, и концентрацию ионов Н+ в этом растворе.
9. Вычислите объем воды, который необходимо добавить к 50 мл 0,02 М раствора NH3·H2О, чтобы степень диссоциации NH3·H2О увеличилась в 10 раз, если Кд(NH4OH) = 1,76·10— 5.
10. Определите степень диссоциации азотистой кислоты в 0,25 М растворе при 298 К, если при указанной температуре Кд(HNO2) = 4,6× 10— 4.
Степень диссоциации и ее связь с константой равновесия
Под диссоциацией
понимают процесс разложения сложного
вещества на более простые, обычно
диссоциация происходит при высоких
температурах.
Доля исходного вещества
, которая
разложилась к моменту достижения
равновесия, называется степенью
диссоциации. Состав смеси при равновесии
зависит от степени диссоциации и,
следовательно, константа равновесия,
зависящая от полноты реакции, может
быть выражена через степень диссоциации
K=f().
Рассмотрим реакцию
аА
bВ + cС,
(a)
выражение для константы
равновесия которой имеет вид

(b)
Формуле (а) отвечает,
например, химическая реакция
.
(c)
К моменту наступления
равновесия число киломолей каждого из
веществ составит:
Таким образом, число
киломолей смеси
(d)
В разделе «Газовые
смеси» было показано, что объемная
доля i-го компонента
равна мольной доле
,
тогда
.
Выразим парциальные давления газов
через мольные доли и давление смеси:
Подставляя парциальные
давления в (b), найдем
искомую зависимость константы равновесия
от степени диссоциации
.
(13.29)
Зная константу
равновесия, можно определить степень
диссоциации. Каждая химическая реакция
имеет свою функциональную зависимость
K=f().
В рассматриваемом случае число киломолей
образовавшихся продуктов реакции п2=3,
число киломолей исходных веществ п1=2,
тогда п=п2
– п1 = 1. На основании формулы
(13.28) можно написать
.
(13.30)
Термодинамические
условия равновесия химических реакций
В разделе 7
«Термодинамические потенциалы и
дифференциальные уравнения термодинамики»
были введены в рассмотрение функции
свободная энергия F
= U – TS
и свободная энтальпия Ф = I
– TS. Было
показано, что при T=const
сумма работы изменения объема L
и работ, не связанных с изменением объема
равна убыли свободной энергии
.
В случае
изохорно-изотермической реакции при
dL = pdV
= 0 работа химической реакции также
равна убыли свободной энергии
.
(13.31)
В
процессе перехода системы в равновесное
состояние из уравнения
(см. раздел 
свободная энергия должна уменьшаться,
а в состоянии равновесия
. Из условия
также следует, что при протекании
обратимых химических реакций свободная
энергия остается неизменной, а при
необратимых – уменьшается.
Аналогичным образом
для изобарно-изотермической реакции
можно написать
.
Так как
,
то при переходе в равновесное состояние
изобарно-изотермический потенциал
уменьшается (dФ0),
а в состоянии равновесия
.
При протекании обратимых реакций dФ=0,
при необратимых равновесие наступает
при
.
В общем случае свободная
энтальпия для химически реагирующей
ТС может быть записана в виде
,
откуда
.
Для изобарно-изотермической
системы будем иметь
,
(13.32)
но
(см. химический потенциал) , таким образом
.
(13.33)
Если в системе
происходят химические превращения, то
dФ<0. При наступлении
химического равновесия выделение или
поглощение теплоты прекращается и dФ=0.
Химическое
сродство
Под химическим
сродством понимают степень способности
различных веществ соединяться друг с
другом.
Было показано, что
переход изохорно-изотермической системы
в равновесное состояние сопровождается
уменьшением свободной энергии (dF<0),
и в состоянии равновесия dF=0,
d2F>0,
F=Fmin.
Для изобарно-изотермической системы,
соответственно, dФ<0,
dФ=0, d2Ф>0,
Ф=Фmin.
Таким образом,
возможными являются лишь те реакции,
которые приводят к уменьшению свободной
энергии или свободной энтальпии, что
иллюстрируется рис.13.2. Из рисунка видно,
что протекание прямой и обратной реакций
возможно лишь при выполнении условий
или
,
где F0 и Ф0
– значения потенциалов после реакции.
В точке С имеет место химическое
равновесие. Отметим, что в этом состоянии
ни одна из концентраций веществ не равна
нулю. Чем больше
,
тем больше работа реакции, а следовательно,
и химическое сродство. Впервые это
положение было высказано русским ученым
Н.Н.Бекетовым, а затем Гельмгольцем и
Вант-Гоффом.
С
FB,ФB
FA,ФA
CA,%
100
0
F0,Ф0
F,Ф
Р
F,Ф
F0,Ф0
ис. 13.2
Уравнение
изотермы химической реакции
Получим уравнение,
связывающее максимальную работу
химической реакции с константой
равновесия и начальными давлениями
веществ, участвующих в реакции. Это
уравнение называется уравнением изотермы
химической реакции. Рассмотрим обратимые
процессы, протекающие в установке,
предложенной Вант-Гоффом (рис.13.3).
РА
,
СА
РB
,
СB
РC
,
СC
РD
,
СD
pA,
pB
, pC
, pD
cA,
cB
, cC
, cD
Емкости A,B,C,D
Ящик Вант-Гоффа
Турбины
Рис.13.3
Установка Вант-Гоффа состоит из
турбин, емкостей A,B,C,D,
в которых находятся компоненты реакции
с давлениями РA,
РB , РC
, РD
и концентрациями СA,
СB , СC
, СD, и
ящика Вант-Гоффа, содержащего равновесную
смесь компонентов и имеющего полупроницаемые
перегородки, каждая из которых пропускает
только один из компонентов. При этом
РA> pA,
РB> pB,
pC
>РC, pD
>РD . Работа химической
реакции L* может
быть представлена алгебраической
суммой работ идеальных турбин, работающих
при Т=const. Так как
работа изотермического расширения
равна
,
то в нашем случае, складывая работы всех
турбин, получаем уравнение изотермы
химической реакции
(13.34)
Выразив парциальные
давления через концентрации компонетов,
получим

(13.35)
Если

то ТС находится в неравновесном состоянии,
работа положительна и возможна лишь
прямая реакция. При L*<0
возможна только обратная реакция. Если
L*=0, то ТС находится
в равновесии и химическая реакция не
протекает.
Для сравнительной
оценки химического сродства полагают

тогда
и
.
Эти значения максимальной работы
химической реакции при разных температурах,
характеризующие химическое сродство,
приводятся в таблицах.
Вычислить степень диссоциации
Вычислить степень диссоциации (α) и равновесную концентрацию ионов водорода ([H+]) в 0,1 М растворе хлорноватистой кислоты (HClO). Константа диссоциации составляет 5 ∙ 10-8. Как изменится равновесная концентрация ионов водорода ([H+]), если к 1 литру 0,1 М раствора хлорноватистой кислоты (HClO) добавить 0,2 моля гипохлорита натрия (NaClO)?
Решение задачи
Перед тем как решить предложенную задачу и вычислить степень диссоциации, думаю, следует напомнить, что степень диссоциации слабого электролита резко снижается при добавлении к нему сильного электролита с одноименным ионом. Если в растворе слабого электролита , диссоциирующего по схеме:
увеличить концентрацию H+-ионов за счет прибавления сильной кислоты или концентрацию ионов A— за счет прибавления соли этой кислоты, это приведет к сдвигу равновесия влево, то есть к уменьшению относительного количества диссоциированных молекул электролита.
Запишем уравнение диссоциации хлорноватистой кислоты (HClO):
Найдем равновесную концентрацию ионов водорода ([H+]) по формуле:
Вычислим степень диссоциации хлорноватистой кислоты (HClO), используя формулу вычисления степени диссоциации:
Если к 1 л раствора хлорноватистой кислоты (HClO) добавить 0,2 моля гипохлорита натрия (NaClO), то концентрация ионов водорода (H+) уменьшится за счет увеличения концентрации ионов ClO—.
Запишем уравнение диссоциации гипохлорита натрия (NaClO):
Обозначим концентрацию ионов водорода (H+) через х, тогда концентрация ионов ClO— будет равна:
х + αClO— (αClO— – активность ионов ClO—, образовавшихся при диссоциации гипохлорита натрия (NaClO)).
Из таблицы 1 находим, что для 0,2 раствора гипохлорита натрия (NaClO) (µ = 0,2) коэффициент активности ионов ƒ = 0,7, а αClO— составит 0,14 моля (0,2 ∙ 0,7).
Таблица 1. Приближенные значения средних коэффициентов активности (ƒ) в зависимости от ионной силы (µ) раствора и заряда иона
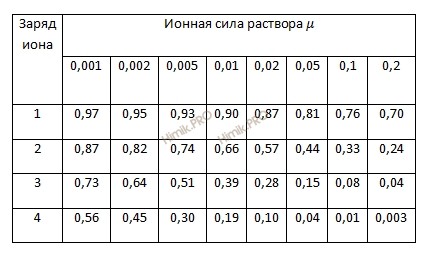
Подставим эти величины в выражение для константы диссоциации:
откуда:
х2 + 0,14х = 5 ⋅ 10-9.
Так как х2 величина очень маленькая, для упрощения вычислений пренебрегаем ею, тогда:
0,14х = 5 ⋅ 10-9
х = 3,6 ⋅ 10-8 (моль/л).
Найдем во сколько раз уменьшилась равновесную концентрацию ионов водорода ([H+]), а следовательно и степень диссоциации:
Ответ:
степень диссоциации равна 0,07 % или 7 ⋅ 10-4 моль/л;
равновесная концентрация ионов водорода равна 7 ⋅ 10-5 моль/л;
равновесная концентрация ионов водорода уменьшится в 1950 раз.